MG_9.ppt
- Количество слайдов: 31

Плазміди бактерій 1

q Це позахромосомні кільцеві, або лінійні молекули ДНК, що здатні до автономної реплікації q Плазміди є у складі геномів Bacteria, Archea, Eukaria q Плазміди, здатні до інтеграції в хромосому бактерій називають епісомами q Розміри плазмід – від декількох тисяч п. н. до декількох сотень тисяч п. н. q Плазмідна ДНК зазвичай складає декілька відсотків сумарної ДНК клітини бактерій q Кожній плазміді властиве певна кількість її копій, що припадають на одну хромосому бактерії. Розрізняють плазміди: малокопійні (плазміда F E. coli -1 -2 копії на хромосому), олігокопійні (Col. E 1 – 10 -15 копій) і мультикопійні (p. UC 18, 200 -500 копій) q Бактерії різних видів здатні обмінюватися своїми плазмідами. Обмін плазмідами – важливий процес “горизонтального” перенесення генів і чинник мінливості бактерій, що дає їм змогу швидко адаптуватися до мінливих умов середовища існування q Плазміди бактерій – вихідний матеріал для створення векторних молекул ДНК для генетичної інженерії 2
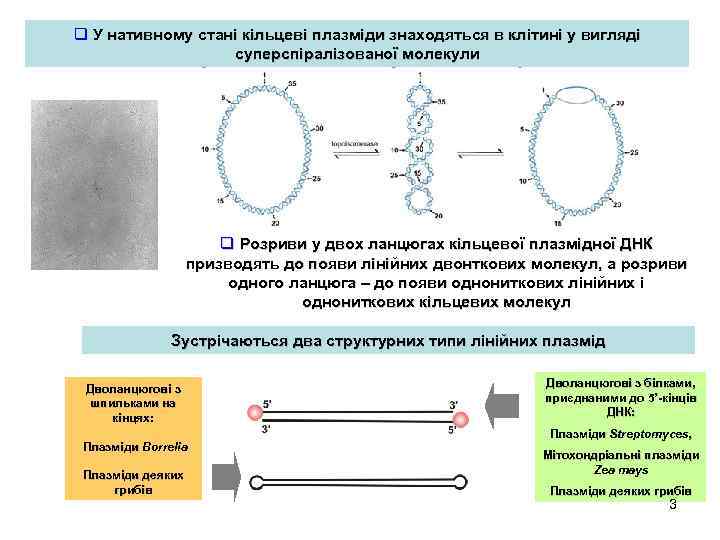
q У нативному стані кільцеві плазміди знаходяться в клітині у вигляді суперспіралізованої молекули q Розриви у двох ланцюгах кільцевої плазмідної ДНК призводять до появи лінійних двонткових молекул, а розриви одного ланцюга – до появи однониткових лінійних і однониткових кільцевих молекул Зустрічаються два структурних типи лінійних плазмід Дволанцюгові з шпильками на кінцях: Плазміди Borrelia Плазміди деяких грибів Дволанцюгові з білками, приєднаними до 5’-кінців 5’ ДНК: Плазміди Streptomyces, Мітохондріальні плазміди Zea mays Плазміди деяких грибів 3
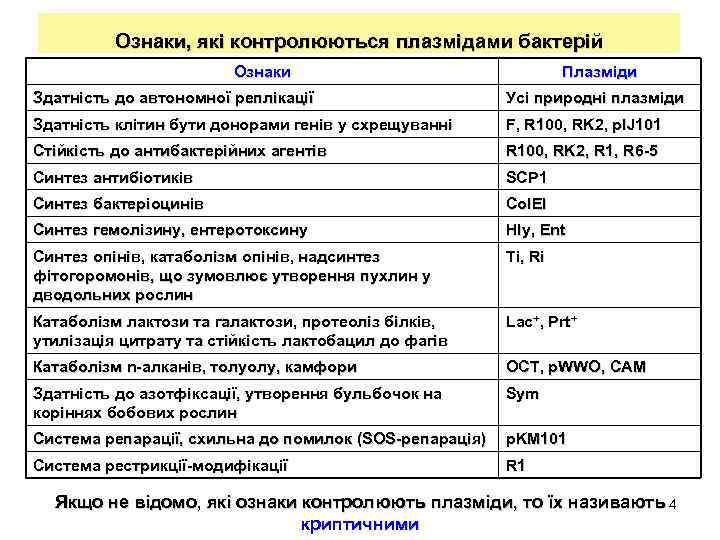
Ознаки, які контролюються плазмідами бактерій Ознаки Плазміди Здатність до автономної реплікації Усі природні плазміди Здатність клітин бути донорами генів у схрещуванні F, R 100, RK 2, p. IJ 101 Стійкість до антибактерійних агентів R 100, RK 2, R 1, R 6 -5 Cинтез антибіотиків SCP 1 Cинтез бактеріоцинів Col. EI Синтез гемолізину, ентеротоксину Hly, Ent Синтез опінів, катаболізм опінів, надсинтез фітогоромонів, що зумовлює утворення пухлин у дводольних рослин Ti, Ri Катаболізм лактози та галактози, протеоліз білків, утилізація цитрату та стійкість лактобацил до фагів Lac+, Prt+ Катаболізм n-алканів, толуолу, камфори OCT, p. WWO, CAM Здатність до азотфіксації, утворення бульбочок на коріннях бобових рослин Sym Система репарації, схильна до помилок (SOS-репарація) p. KM 101 Система рестрикції-модифікації R 1 Якщо не відомо, які ознаки контролюють плазміди, то їх називають 4 криптичними

Виявлення плазмід у клітинах бактерій q Генетичні підходи – аналіз успадкування ознак, які ймовірно визначаються плазмідами § генетичний детермінант ознаки не зчеплений з хромосомними генами (статевий фактор F, що визначає здатність клітин E. coli бути донором генів у схрещуваннях) § висока частота успадкування генетичного детермінанта у схрещування перенесення (всі нащадки від схрещування F+×Fуспадковують F – фактор) § висока частота спонтанної незворотної втрати ознаки (штами F+ перетворюються у F- з частотою ~ 10 -2 -10 -3). Ця частота сильно зростає під впливом чинників, що селективно інгібують реплікацію плазмід (акридинові барвники, бромід етидію, УФ – опромінення) q Фізичне виділення плазмідної ДНК. § ультрацентрифугування в градієнті густини Cs. Cl з бромідом етидію 5 § гель-електрофорез
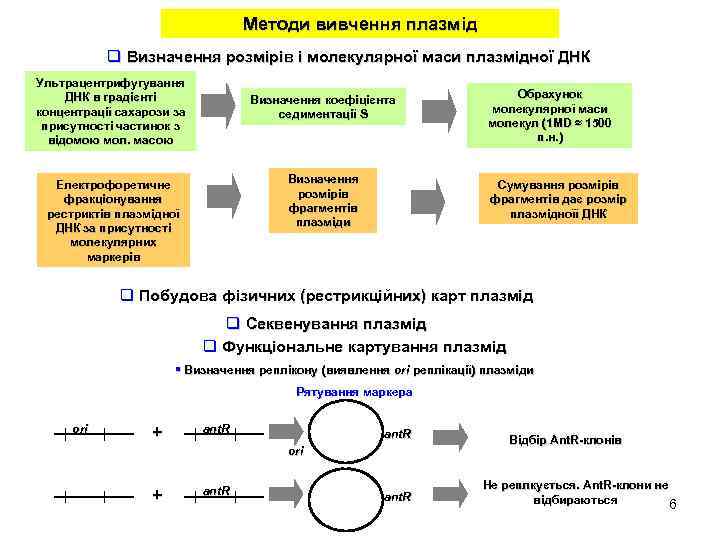
Методи вивчення плазмід q Визначення розмірів і молекулярної маси плазмідної ДНК Ультрацентрифугування ДНК в градієнті концентрації сахарози за присутності частинок з відомою мол. масою Визначення коефіцієнта седиментації S Визначення розмірів фрагментів плазміди Електрофоретичне фракціонування рестриктів плазмідної ДНК за присутності молекулярних маркерів Обрахунок молекулярної маси молекул (1 MD ≈ 1500 (1 MD п. н. ) Сумування розмірів фрагментів дає розмір плазмідноїї ДНК q Побудова фізичних (рестрикційних) карт плазмід q Секвенування плазмід q Функціональне картування плазмід § Визначення реплікону (виявлення ori реплікації) плазміди Рятування маркера ori + ant. R Відбір Ant. R-клонів Ant. R- Не реплкується. Аnt. R-клони не реплкується. Аnt. Rвідбираються 6
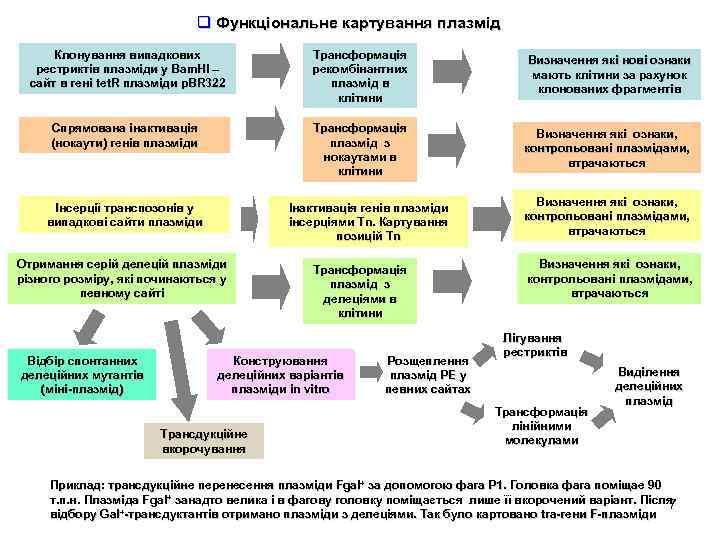
q Функціональне картування плазмід Клонування випадкових рестриктів плазміди у Bam. HI – сайт в гені tet. R плазміди p. BR 322 Трансформація рекомбінантних плазмід в клітини Визначення які нові ознаки мають клітини за рахунок клонованих фрагментів Спрямована інактивація (нокаути) генів плазміди Трансформація плазмід з нокаутами в клітини Визначення які ознаки, контрольовані плазмідами, втрачаються Інсерції транспозонів у випадкові сайти плазміди Інактивація генів плазміди інсерціями Tn. Картування Tn. позицій Tn Отримання серій делецій плазміди різного розміру, які починаються у певному сайті Відбір спонтанних делеційних мутантів (міні-плазмід) Трансформація плазмід з делеціями в клітини Конструювання делеційних варіантів плазміди in vitro Трансдукційне вкорочування Розщеплення плазмід РЕ у певних сайтах Визначення які ознаки, контрольовані плазмідами, втрачаються Лігування рестриктів Трансформація лінійними молекулами Виділення делеційних плазмід Приклад: трансдукційне перенесення плазміди Fgal+ за допомогою фага Р 1. Головка фага поміщае 90 т. п. н. Плазміда Fgal+ занадто велика і в фагову головку поміщається лише її вкорочений варіант. Після т. п. н. 7 відбору Gal+-трансдуктантів отримано плазміди з делеціями. Так було картовано tra-гени F-плазміди делеціями. tra. F-плазмі

Реплікація плазмід q Найголовніша особливість плазмід – це їхня здатність до реплікації, яка не залежить від реплікації хромосом клітин-господaрів. Тому плазміди часто називають автономними репліконами. q Реплікон – це молекула ДНК (РНК), подвоєння якої починається з фіксованого сайту молекули, який називають вегетативним сайтом початку реплікації ori. V (від англ. the vegetative origin of replication). q Однак, окремими репліконами можуть бути й частини молекули, кожна з яких несе свій сайт ori. Зазвичай плазміда – єдиний реплікон, що подвоюється за один неперервний акт реплікації. q Існує й інше широко вживане значення терміну «реплікон» . q Репліконом називають мінімальну (зазвичай не більше, ніж 4 т. п. н. ) ділянку плазміди, яка підтримує її автономну реплікацію, а також забезпечує властиву для неї кількість копій у клітині. q У цій ділянці містяться: § а) сайт ori. V; § б) гени, що кодують білки і РНК, необхідні для ініціювання реплікації плазміди і контролювання цього процесу; § в) послідовності ДНК, з якими взаємодіють вказані білки клітинигосподаря, задіяні у реплікацію плазміди. q У плазміді може бути один, або декілька таких репліконів. 8
Особливості реплікації плазмід, регулювання цього процесу, розподілу (сегрегації) плазмід між дочірніми клітинами під час клітинного поділу визначають такі їхні характеристики Коло клітингосподарів, в яких господарів, плазміди здатні підтримуватися Кількість копій однієї плазміди, що одночасно присутні в клітині Стабільність підтримання плазміди в певній клітинній лінії Несумісність плазмід – нездатність двох різних, але близьких за будовою плазмід, підтримуватися в певній плазмід, клітинній лінії q Для ініціювання реплікації багатьох плазмід потрібен білок (Rep) який кодується самою плазмідою і здатний специфічно зв’язуватися з ori. V. Він функціонує замість клітинного білка ініціації реплікації хромосомної ДНК Dna. A, або у комбінації з ним q Однак є й такі плазміди, як наприклад Col. E 1, які для ініціювання реплікації не потребують білка Rep q Існує два основних механізми реплікації кільцевих плазмід: § «тета» -реплікація, у ході якої утворюються проміжні продукти, які за виглядом нагадують грецьку букву «тета» – Θ; § реплікація за механізмом кільця, що котиться (RC-реплікація, від англ. rolling-circle replication) q Одні плазміди (наприклад Col. E 1, R 1) реплікуються однонаправлено, інші – двонаправлено (F). Деяким плазмідам, наприклад, R 6 K, властиві обидва способи реплікації. q Завершується повний цикл однонаправленої реплікації плазмід у сайті ori. Натомість при двонаправленій реплікації вона закінчується у певній фіксованій точці, або там, де зустрічаються реплікативні вилки, залежно від швидкості руху кожної з них. Кількість копій плазміди визначається частотою, з якої буде ініціюватися синтез її ДНК 9
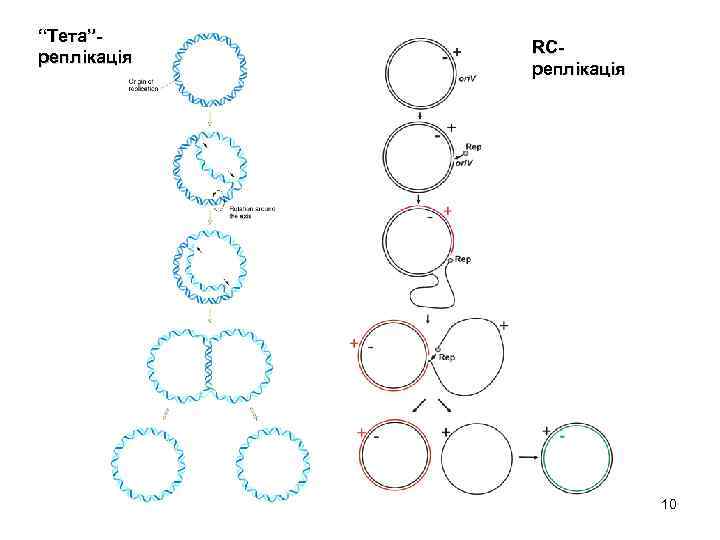
“Тета”реплікація RCреплікація 10
11
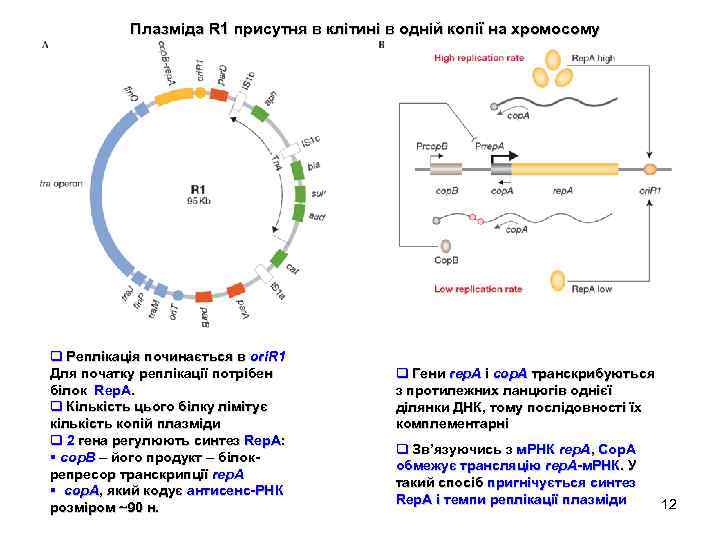
Плазміда R 1 присутня в клітині в одній копії на хромосому q Реплікація починається в ori. R 1 Для початку реплікації потрібен білок Rep. A. q Кількість цього білку лімітує кількість копій плазміди q 2 гена регулюють синтез Rep. A: § cop. B – його продукт – білокрепресор транскрипції rep. A § сop. A, який кодує антисенс-РНК розміром ~90 н. q Гени rep. A і cop. A транскрибуються з протилежних ланцюгів однієї ділянки ДНК, тому послідовності їх комплементарні q Зв’язуючись з м. РНК rep. A, Coр. A обмежує трансляцію rep. A-м. РНК. У такий спосіб пригнічується синтез Rep. A і темпи реплікації плазміди 12
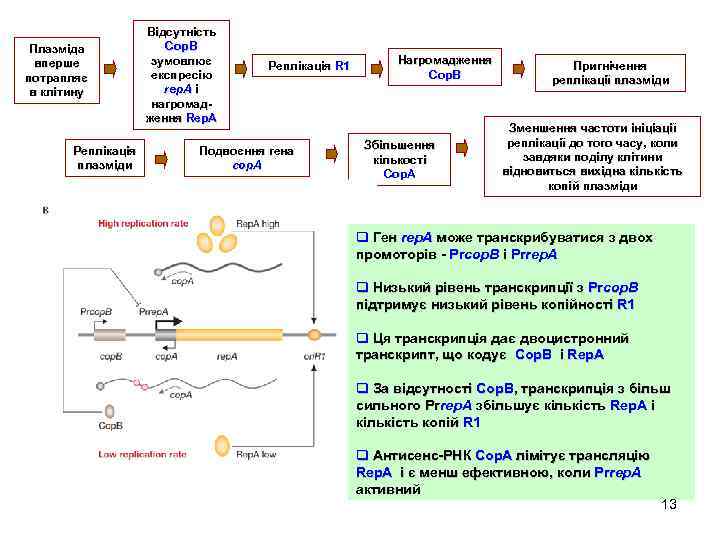
Плазміда вперше потрапляє в клітину Реплікація плазміди Відсутність Cop. B зумовлює експресію rep. A і нагромадження Rep. A Реплікація R 1 Подвоєння гена cop. A Нагромадження Cop. B Збільшення кількості Cop. A Пригнічення реплікації плазміди Зменшення частоти ініціації реплікації до того часу, коли завдяки поділу клітини відновиться вихідна кількість копій плазміди q Ген rep. A може транскрибуватися з двох промоторів - Prcop. B і Prrep. A q Низький рівень транскрипції з Prcop. B підтримує низький рівень копійності R 1 q Ця транскрипція дає двоцистронний транскрипт, що кодує Cop. B і Rep. A q За відсутності Cop. B, транскрипція з більш сильного Prrep. A збільшує кількість Rep. A і кількість копій R 1 q Антисенс-РНК Сop. A лімітує трансляцію Rep. A і є менш ефективною, коли Prrep. A активний 13
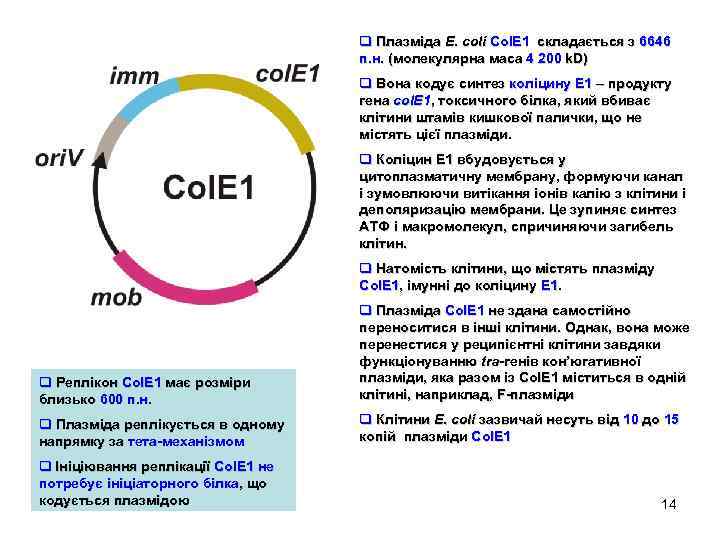
q Плазміда E. coli Col. E 1 складається з 6646 п. н. (молекулярна маса 4 200 k. D) q Вона кодує синтез коліцину Е 1 – продукту гена col. E 1, токсичного білка, який вбиває клітини штамів кишкової палички, що не містять цієї плазміди. q Коліцин Е 1 вбудовується у цитоплазматичну мембрану, формуючи канал і зумовлюючи витікання іонів калію з клітини і деполяризацію мембрани. Це зупиняє синтез АТФ і макромолекул, спричиняючи загибель клітин. q Натомість клітини, що містять плазміду Col. E 1, імунні до коліцину E 1. q Реплікон Col. E 1 має розміри близько 600 п. н. q Плазміда Col. E 1 не здана самостійно переноситися в інші клітини. Однак, вона може перенестися у реципієнтні клітини завдяки функціонуванню tra-генів кон’югативної плазміди, яка разом із Col. E 1 міститься в одній клітині, наприклад, F-плазміди q Плазміда реплікується в одному напрямку за тета-механізмом q Клітини E. coli зазвичай несуть від 10 дo 15 копій плазміди Col. E 1 q Ініціювання реплікації Col. E 1 не потребує ініціаторного білка, що кодується плазмідою 14
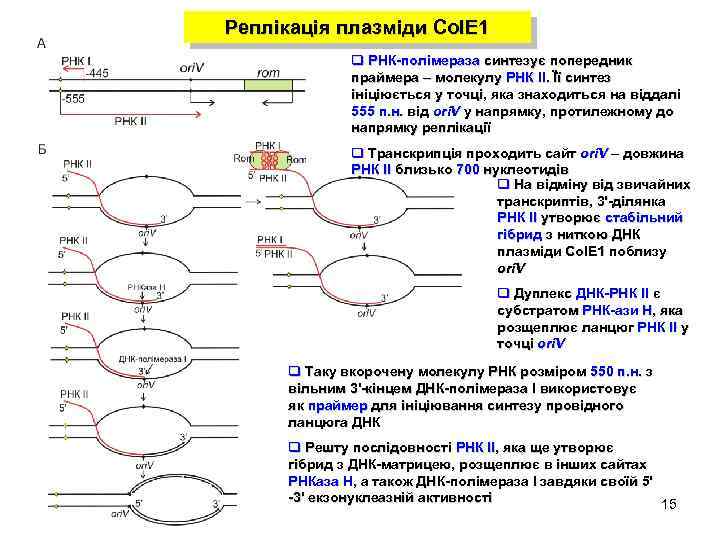
Реплікація плазміди Col. E 1 q РНК-полімераза синтезує попередник праймера – молекулу РНК ІІ. Її синтез ініціюється у точці, яка знаходиться на віддалі 555 п. н. від ori. V у напрямку, протилежному до напрямку реплікації q Транскрипція проходить сайт ori. V – довжина РНК ІІ близько 700 нуклеотидів q На відміну від звичайних транскриптів, 3'-ділянка РНК II утворює стабільний гібрид з ниткою ДНК плазміди Col. E 1 поблизу ori. V q Дуплекс ДНК-РНК ІІ є субстратом РНК-ази Н, яка розщеплює ланцюг РНК ІІ у точці ori. V q Таку вкорочену молекулу РНК розміром 550 п. н. з вільним 3'-кінцем ДНК-полімераза І використовує як праймер для ініціювання синтезу провідного ланцюга ДНК q Решту послідовності РНК ІІ, яка ще утворює гібрид з ДНК-матрицею, розщеплює в інших сайтах РНКаза Н, а також ДНК-полімераза І завдяки своїй 5' -3' екзонуклеазній активності 15
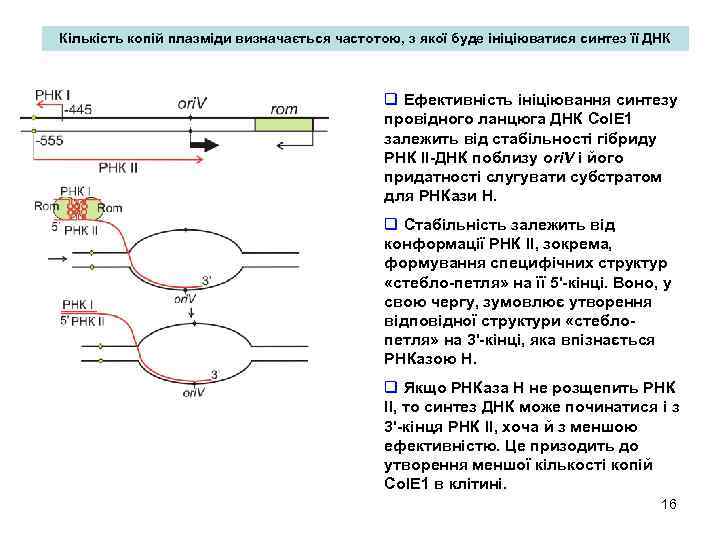
Кількість копій плазміди визначається частотою, з якої буде ініціюватися синтез її ДНК q Ефективність ініціювання синтезу провідного ланцюга ДНК Col. E 1 залежить від стабільності гібриду РНК ІІ-ДНК поблизу ori. V і його придатності слугувати субстратом для РНКази Н. q Стабільність залежить від конформації РНК ІІ, зокрема, формування специфічних структур «стебло-петля» на її 5'-кінці. Воно, у свою чергу, зумовлює утворення відповідної структури «стеблопетля» на 3'-кінці, яка впізнається РНКазою Н. q Якщо РНКаза H не розщепить РНК ІІ, то синтез ДНК може починатися і з 3'-кінця РНК II, хоча й з меншою ефективністю. Це призодить до утворення меншої кількості копій Col. E 1 в клітині. 16
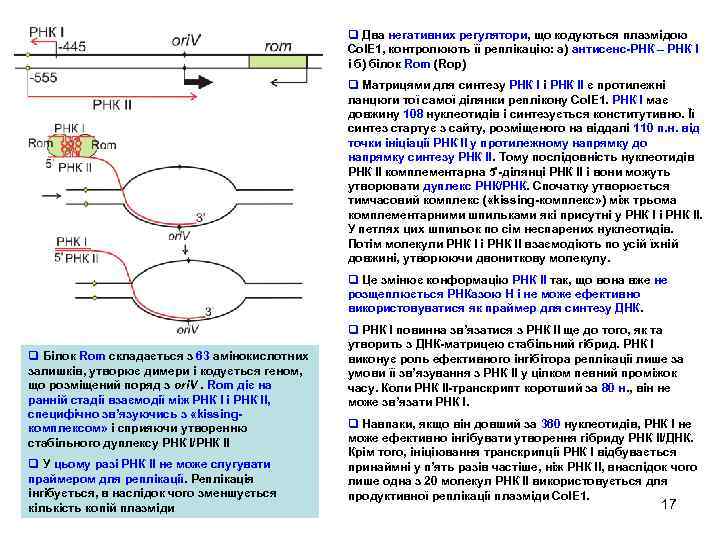
q Два негативних регулятори, що кодуються плазмідою Col. E 1, контролюють її реплікацію: а) антисенс-РНК – РНК І і б) білок Rom (Rop) q Матрицями для синтезу РНК І і РНК ІІ є протилежні ланцюги тої самої ділянки реплікону Col. E 1. РНК І має довжину 108 нуклеотидів і синтезується конститутивно. Її синтез стартує з сайту, розміщеного на віддалі 110 п. н. від точки ініціації РНК ІІ у протилежному напрямку до напрямку синтезу РНК ІІ. Тому послідовність нуклеотидів РНК ІІ комплементарна 5'-ділянці РНК ІІ і вони можуть утворювати дуплекс РНК/РНК. Спочатку утворюється тимчасовий комплекс ( «kissing-комплекс» ) між трьома комплементарними шпильками які присутні у РНК І і РНК ІІ. У петлях цих шпильок по сім неспарених нуклеотидів. Потім молекули РНК І і РНК ІІ взаємодіють по усій їхній довжині, утворюючи двониткову молекулу. q Це змінює конформацію РНК ІІ так, що вона вже не розщеплюється РНКазою Н і не може ефективно використовуватися як праймер для синтезу ДНК. q Білок Rom складається з 63 амінокислотних залишків, утворює димери і кодується геном, що розміщений поряд з ori. V. Rom діє на ранній стадії взаємодії між РНК І і РНК ІІ, специфічно зв’язуючись з «kissingкомплексом» і сприяючи утворенню стабільного дуплексу РНК І/РНК ІІ q У цьому разі РНК ІІ не може слугувати праймером для реплікації. Реплікація інгібується, в наслідок чого зменшується кількість копій плазміди q РНК І повинна зв’язатися з РНК ІІ ще до того, як та утворить з ДНК-матрицею стабільний гібрид. РНК І виконує роль ефективного інгібітора реплікації лише за умови її зв’язування з РНК ІІ у цілком певний проміжок часу. Коли РНК ІІ-транскрипт коротший за 80 н. , він не може зв’язати РНК І. q Навпаки, якщо він довший за 360 нуклеотидів, РНК І не може ефективно інгібувати утворення гібриду РНК ІІ/ДНК. Крім того, ініціювання транскрипції РНК І відбувається принаймні у п’ять разів частіше, ніж РНК ІІ, внаслідок чого лише одна з 20 молекул РНК ІІ використовується для продуктивної реплікації плазміди Col. E 1. 17
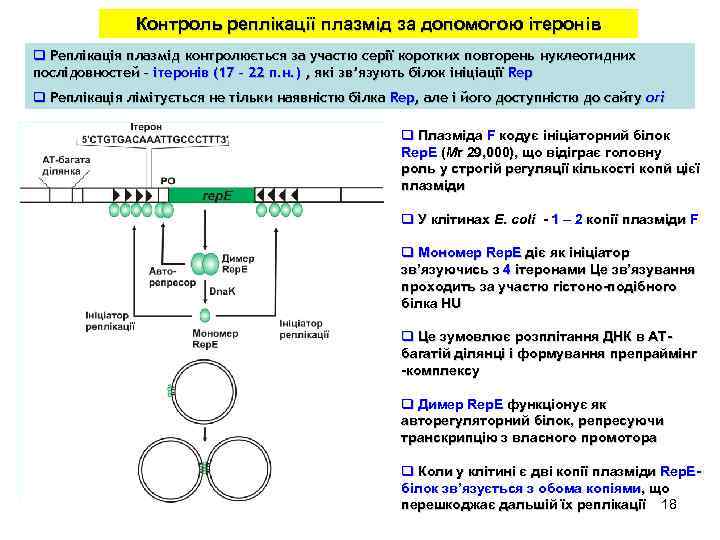
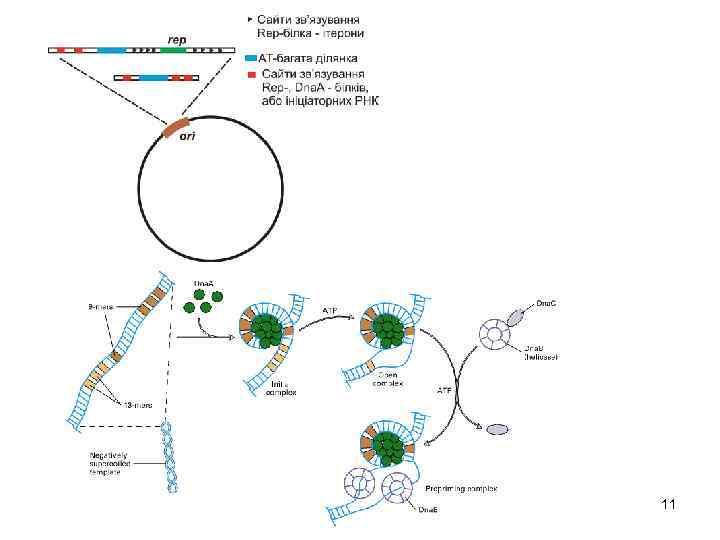
Контроль реплікації плазмід за допомогою ітеронів q Реплікація плазмід контролюється за участю серії коротких повторень нуклеотидних послідовностей – ітеронів (17 – 22 п. н. ) , які зв’язують білок ініціації Rep q Реплікація лімітується не тільки наявністю білка Rep, але і його доступністю до cайту ori q Плазміда F кодує ініціаторний білок Rep. E (Mr 29, 000), що відіграє головну роль у строгій регуляції кількості копй цієї плазміди q У клітинах E. coli - 1 – 2 копії плазміди F q Мономер Rep. E діє як ініціатор зв’язуючись з 4 ітеронами Це зв’язування проходить за участю гістоно-подібного білка HU q Це зумовлює розплітання ДНК в ATбагатій ділянці і формування препраймінг -комплексу q Димер Rep. E функціонує як авторегуляторний білок, репресуючи транскрипцію з власного промотора q Коли у клітині є дві копії плазміди Rep. Eбілок зв’язується з обома копіями, що перешкоджає дальшій їх реплікації 18
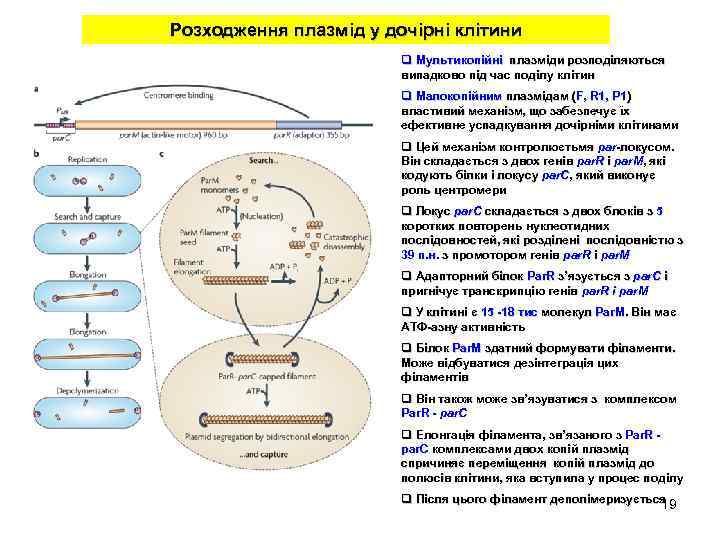
Розходження плазмід у дочірні клітини q Мультикопійні плазміди розподіляються випадково під час поділу клітин q Малокопійним плазмідам (F, R 1, P 1) (F, P 1) властивий механізм, що забезпечує їх ефективне успадкування дочірніми клітинами q Цей механізм контролюєтьмя par-локусом. par. Він складається з двох генів par. R і par. M, які par. M, кодують білки і локусу par. C, який виконує par. C, роль центромери q Локус par. C складається з двох блоків з 5 коротких повторень нуклеотидних послідовностей, які розділені послідовністю з 39 п. н. з промотором генів par. R і par. M п. н. q Адапторний білок Par. R з’язується з par. C і пригнічує транскрипцію генів par. R і par. M q У клітині є 15 -18 тис молекул Par. M. Він має Par. M. АТФ-азну активність q Білок Par. M здатний формувати філаменти. Може відбуватися дезінтеграція цих філаментів q Він також може зв’язуватися з комплексом зв’ Par. R - par. C q Елонгація філамента, зв’язаного з Par. R філамента, зв’ par. C комплексами двох копій плазмід спричиняє переміщення копій плазмід до полюсів клітини, яка вступила у процес поділу q Після цього філамент деполімеризується 19
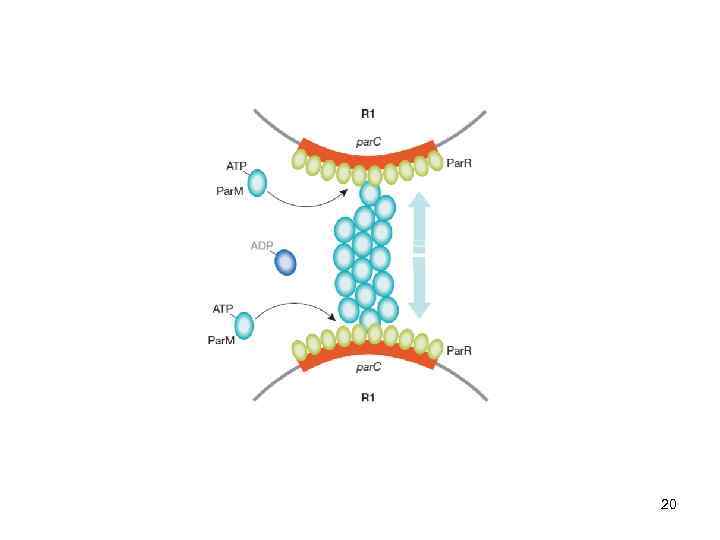
20
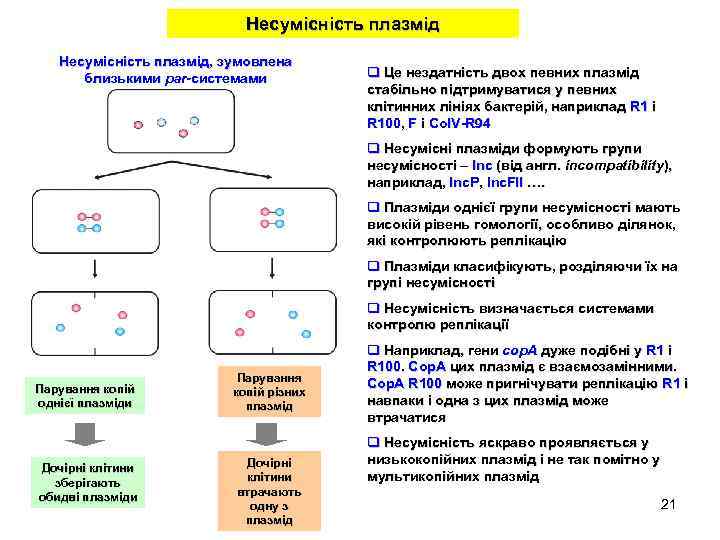
Несумісність плазмід, зумовлена близькими par-системами q Це нездатність двох певних плазмід стабільно підтримуватися у певних клітинних лініях бактерій, наприклад R 1 і R 100, F і Col. V-R 94 q Несумісні плазміди формують групи несумісності – Inc (від англ. incompatibility), наприклад, Inc. P, Inc. FII …. q Плазміди однієї групи несумісності мають високій рівень гомології, особливо ділянок, які контролюють реплікацію q Плазміди класифікують, розділяючи їх на групі несумісності q Несумісність визначається системами контролю реплікації Парування копій однієї плазміди Дочірні клітини зберігають обидві плазміди Парування копій різних плазмід Дочірні клітини втрачають одну з плазмід q Наприклад, гени cop. A дуже подібні у R 1 і R 100. Cop. A цих плазмід є взаємозамінними. Cop. A R 100 може пригнічувати реплікацію R 1 і навпаки і одна з цих плазмід може втрачатися q Несумісність яскраво проявляється у низькокопійних плазмід і не так помітно у мультикопійних плазмід 21
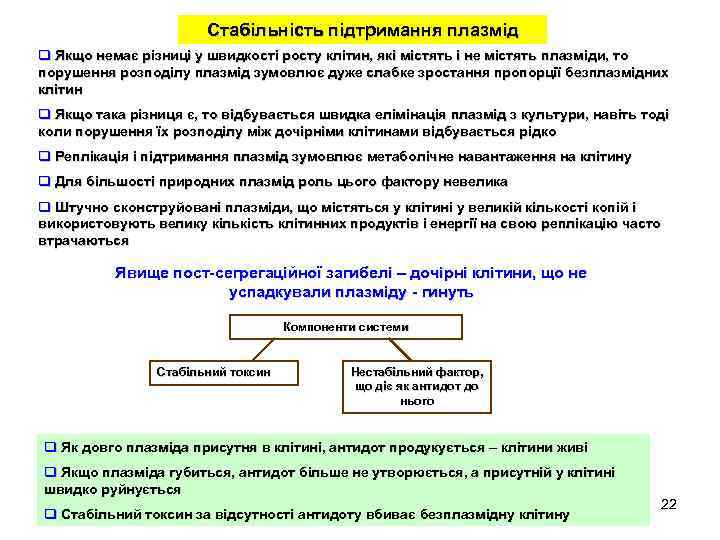
Стабільність підтримання плазмід q Якщо немає різниці у швидкості росту клітин, які містять і не містять плазміди, то порушення розподілу плазмід зумовлює дуже слабке зростання пропорції безплазмідних клітин q Якщо така різниця є, то відбувається швидка елімінація плазмід з культури, навіть тоді коли порушення їх розподілу між дочірніми клітинами відбувається рідко q Реплікація і підтримання плазмід зумовлює метаболічне навантаження на клітину q Для більшості природних плазмід роль цього фактору невелика q Штучно сконструйовані плазміди, що містяться у клітині у великій кількості копій і використовують велику кількість клітинних продуктів і енергії на свою реплікацію часто втрачаються Явище пост-сегрегаційної загибелі – дочірні клітини, що не успадкували плазміду - гинуть Компоненти системи Стабільний токсин Нестабільний фактор, що діє як антидот до нього q Як довго плазміда присутня в клітині, антидот продукується – клітини живі q Якщо плазміда губиться, антидот більше не утворюється, а присутній у клітині швидко руйнується q Стабільний токсин за відсутності антидоту вбиває безплазмідну клітину 22
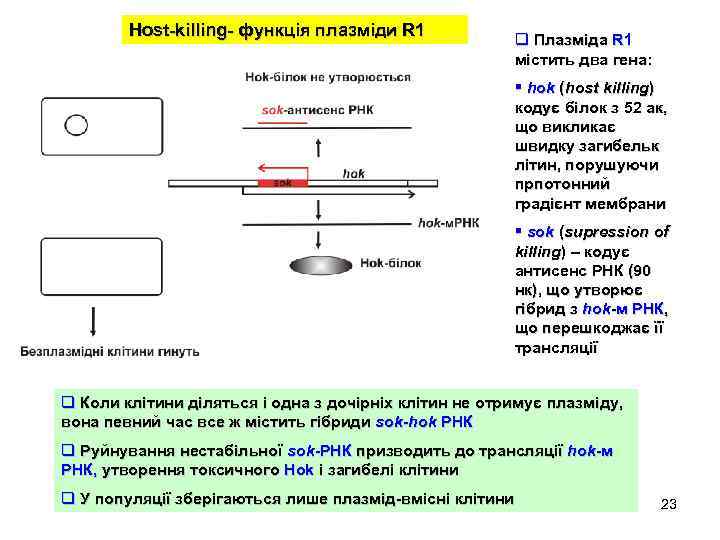
Host-killing- функція плазміди R 1 q Плазміда R 1 містить два гена: § hok (host killing) кодує білок з 52 ак, що викликає швидку загибельк літин, порушуючи прпотонний градієнт мембрани § sok (supression of killing) – кодує антисенс РНК (90 нк), що утворює гібрид з hok-м РНК, що перешкоджає її трансляції q Коли клітини діляться і одна з дочірніх клітин не отримує плазміду, вона певний час все ж містить гібриди sok-hok РНК q Руйнування нестабільної sok-РНК призводить до трансляції hok-м РНК, утворення токсичного Hok і загибелі клітини q У популяції зберігаються лише плазмід-вмісні клітини 23
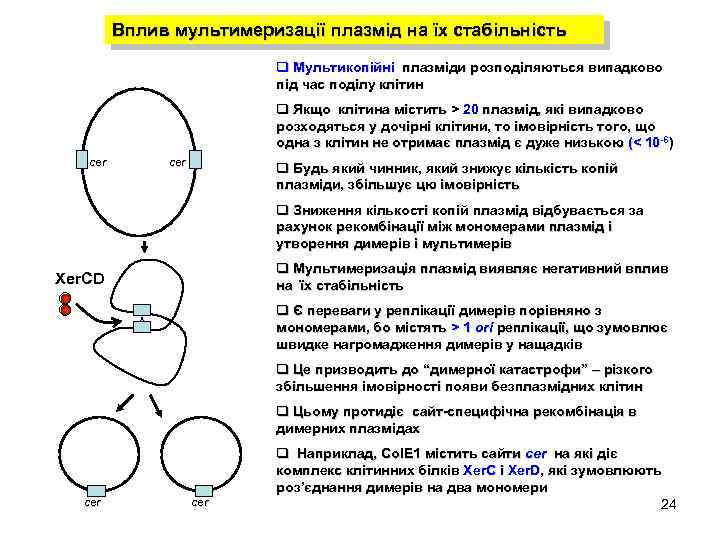
Вплив мультимеризації плазмід на їх стабільність q Мультикопійні плазміди розподіляються випадково під час поділу клітин q Якщо клітина містить > 20 плазмід, які випадково розходяться у дочірні клітини, то імовірність того, що одна з клітин не отримає плазмід є дуже низькою (< 10 -6) сer q Будь який чинник, який знижує кількість копій плазміди, збільшує цю імовірність q Зниження кількості копій плазмід відбувається за рахунок рекомбінації між мономерами плазмід і утворення димерів і мультимерів q Мультимеризація плазмід виявляє негативний вплив на їх стабільність Xer. CD q Є переваги у реплікації димерів порівняно з мономерами, бо містять > 1 ori реплікації, що зумовлює швидке нагромадження димерів у нащадків х q Це призводить до “димерної катастрофи” – різкого збільшення імовірності появи безплазмідних клітин q Цьому протидіє сайт-специфічна рекомбінація в димерних плазмідах сer q Наприклад, Col. E 1 містить сайти cer на які діє комплекс клітинних білків Xer. C і Xer. D, які зумовлюють роз’єднання димерів на два мономери 24

Статевий фактор Е. coli – плазміда F q Кільцева двохниткова молекула ДНК розміром у 100 т. п. н. IS 3 a q У клітині E. coli – 1 копія F – плазміди на 1 хромосому q Містить чотири мобільних генетичних елементи – 1 IS 2, 2 - IS 3 (IS 3 а та IS 3 b), 1 -Tn 1000. Інтеграція F-фактора IS 2 в хромосому може відбуватися за рахунок рекомбінації між гомологічними мобільними генетичними елементами в плазміді та хромосомі. IS 3 b q У хромосомі E. coli є більше 20 сайтів інтеграції плазміди F. Інтеграція в різні сайти хромосоми відбувається з різною частотою і зазвичай не супроводжується мутаціями. Виявлено, що для інтеграції в більшість сайтів необхідний білок Rec. A, тобто інтеграція найчастіше проходить за рахунок гомологічної рекомбінації. q IS-елемент хромосоми, що бере участь в рекомбінації, може мати одну з двох протилежних орієнтацій. Залежно від цього можливі й дві протилежні орієнтації інтегрованого F-фактора q Реплікацію та підтримання плазміди F у клітинах контролює головно ділянка Rep. FIA, де містяться два сайти початку реплікації – ori. V та ori. S, гени inc, cop. A, B, sop. A, B, C, які контролюють, відповідно, несумісність F-подібних плазмід, кількість копій плазмід у клітині, стабільність їхнього підтримання та сегрегацію. Крім того, є ще дві ділянки Rep. FIВ та Rep. FIС, де містяться гени, що контролюють реплікацію плазміди. У ділянці 25 Rep. FIС є інсерція транспозону Tn 1000
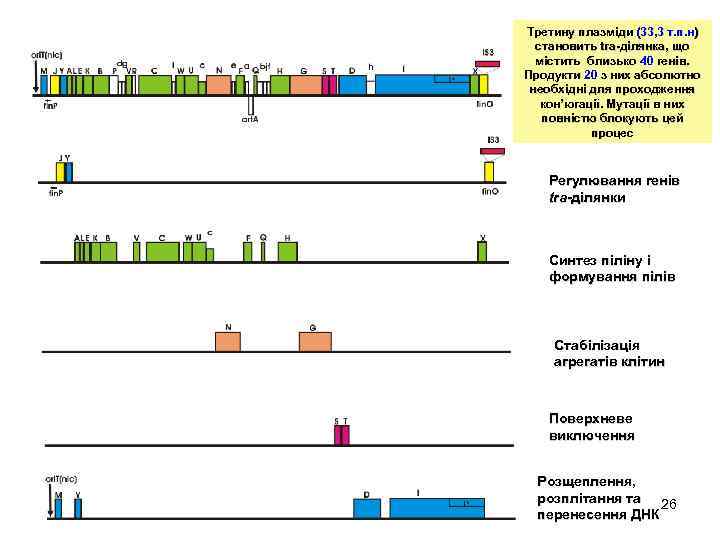
Третину плазміди (33, 3 т. п. н) становить tra-ділянка, що tra-ділянка, містить близько 40 генів. Продукти 20 з них абсолютно необхідні для проходження кон’югації. Мутації в них повністю блокують цей процес Регулювання генів tra-ділянки Синтез піліну і формування пілів Стабілізація агрегатів клітин Поверхневе виключення Розщеплення, розплітання та 26 перенесення ДНК
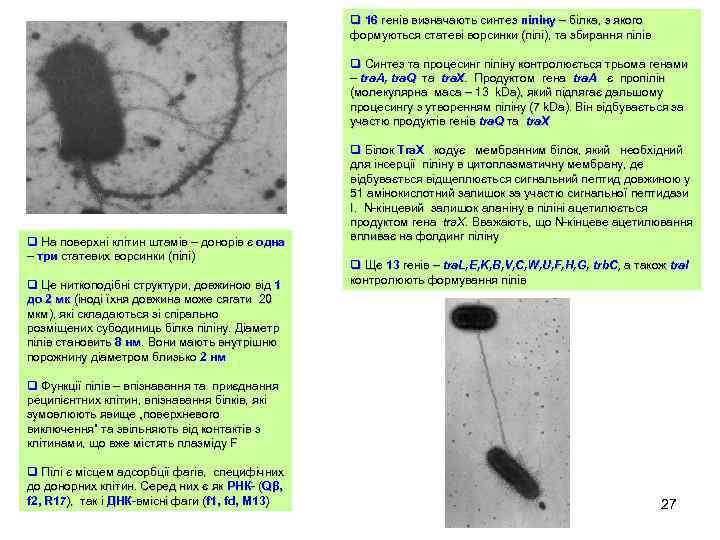
q 16 генів визначають синтез піліну – білка, з якого формуються статеві ворсинки (пілі), та збирання пілів (пілі), q Синтез та процесинг піліну контролюється трьома генами – tra. A, tra. Q та tra. X. Продуктом гена tra. A є пропілін tra. A, tra. X. (молекулярна маса – 13 k. Da), який підлягає дальшому k. Da), процесингу з утворенням піліну (7 k. Da). Він відбувається за k. Da). участю продуктів генів tra. Q та tra. X q На поверхні клітин штамів – донорів є одна – три статевих ворсинки (пілі) q Це ниткоподібні структури, довжиною від 1 до 2 мк (іноді їхня довжина може сягати 20 мкм), які складаються зі спірально розміщених субодиниць білка піліну. Діаметр піліну. пілів становить 8 нм. Вони мають внутрішню нм. порожнину діаметром близько 2 нм q Білок Tra. X кодує мембранним білок, який необхідний для інсерції піліну в цитоплазматичну мембрану, де відбувається відщеплюється сигнальний пептид довжиною у 51 амінокислотний залишок за участю сигнальної пептидази І. N-кінцевий залишок аланіну в піліні ацетилюється продуктом гена tra. X. Вважають, що N-кінцеве ацетилювання tra. X. впливає на фолдинг піліну q Ще 13 генів – tra. L, E, K, B, V, C, W, U, F, H, G, trb. C, а також traІ tra. L, trb. C, traІ контролюють формування пілів q Функції пілів – впізнавання та приєднання реципієнтних клітин, впізнавання білків, які зумовлюють явище „поверхневого виключення” та звільняють від контактів з клітинами, що вже містять плазміду F q Пілі є місцем адсорбції фагів, специфічних фагів, до донорних клітин. Серед них є як РНК- (Qβ, f 2, R 17), так і ДНК-вмісні фаги (f 1, fd, M 13) 17), ДНК-вмісні (f fd, 13) 27
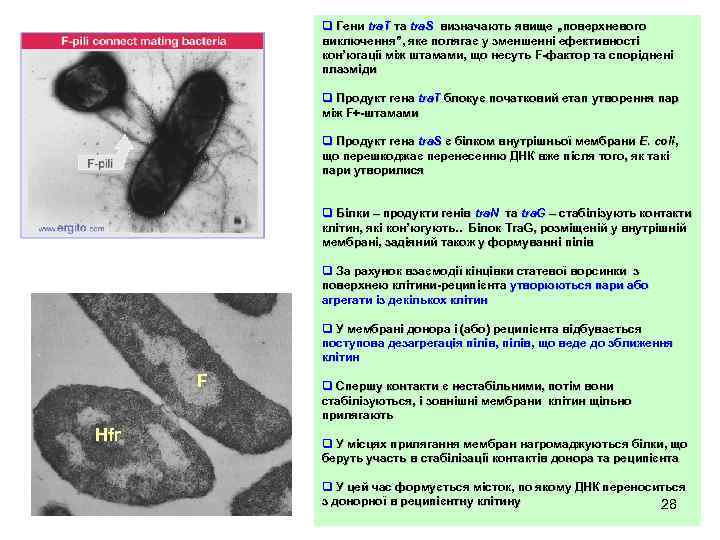
q Гени tra. T та tra. S визначають явище „поверхневого виключення”, яке полягає у зменшенні ефективності виключення”, кон’югації між штамами, що несуть F-фактор та споріднені плазміди q Продукт гена tra. T блокує початковий етап утворення пар між F+-штамами q Продукт гена tra. S є білком внутрішньої мембрани E. coli, що перешкоджає перенесенню ДНК вже після того, як такі пари утворилися q Білки – продукти генів tra. N та tra. G – стабілізують контакти клітин, які кон’югують. . Білок Tra. G, розміщеній у внутрішній кон’югують. . Tra. G, мембрані, задіяний також у формуванні пілів q За рахунок взаємодії кінцівки статевої ворсинки з поверхнею клітини-реципієнта утворюються пари або агрегати із декількох клітин q У мембрані донора і (або) реципієнта відбувається поступова дезагрегація пілів, що веде до зближення пілів, клітин F Hfr q Спершу контакти є нестабільними, потім вони стабілізуються, і зовнішні мембрани клітин щільно прилягають q У місцях прилягання мембран нагромаджуються білки, що беруть участь в стабілізації контактів донора та реципієнта q У цей час формується місток, по якому ДНК переноситься з донорної в реципієнтну клітину 28
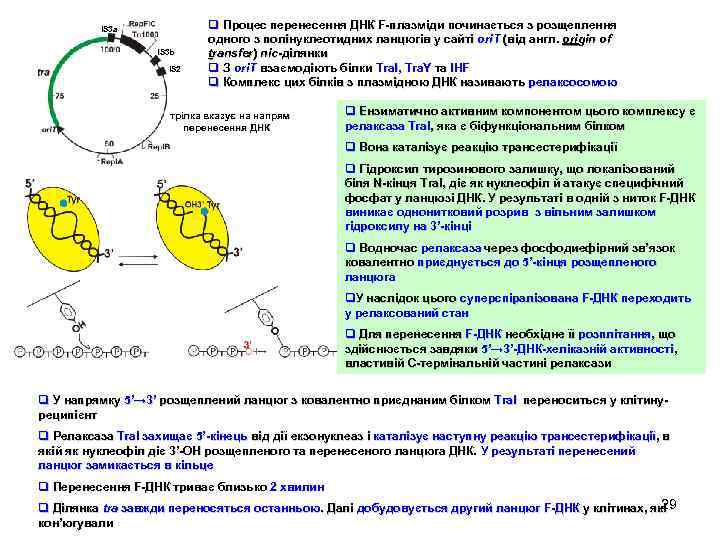
IS 3 a IS 3 b IS 2 q Процес перенесення ДНК F-плазміди починається з розщеплення F-плазміди одного з полінуклеотидних ланцюгів у сайті ori. T (від англ. origin of origin transfer) nic-ділянки q З ori. T взаємодіють білки Tra. I, Tra. Y та IHF Tra. I, q Комплекс цих білків з плазмідною ДНК називають релаксосомою стрілка вказує на напрям перенесення ДНК q Ензиматично активним компонентом цього комплексу є релаксаза Tra. I, яка є біфункціональним білком Tra. I, q Вона каталізує реакцію трансестерифікації q Гідроксил тирозинового залишку, що локалізований біля N-кінця Tra. I, діє як нуклеофіл й атакує специфічний Tra. I, фосфат у ланцюзі ДНК. У результаті в одній з ниток F-ДНК виникає однонитковий розрив з вільним залишком гідроксилу на 3’-кінці q Водночас релаксаза через фосфодиефірний зв’язок ковалентно приєднується до 5’-кінця розщепленого ланцюга q. У наслідок цього суперспіралізована F-ДНК переходить у релаксований стан q Для перенесення F-ДНК необхідне її розплітання, що розплітання, здійснюється завдяки 5’→ 3’-ДНК-хеліказній активності, властивій С-термінальній частині релаксази q У напрямку 5’→ 3’ розщеплений ланцюг з ковалентно приєднаним білком Tra. I переноситься у клітинуреципієнт q Релаксаза Tra. I захищає 5’-кінець від дії екзонуклеаз і каталізує наступну реакцію трансестерифікації, в трансестерифікації, якій як нуклеофіл діє 3’-OH розщепленого та перенесеного ланцюга ДНК. У результаті перенесений ланцюг замикається в кільце q Перенесення F-ДНК триває близько 2 хвилин 29 q Ділянка tra завжди переносяться останньою. Далі добудовується другий ланцюг F-ДНК у клітинах, які останньою. кон’югували
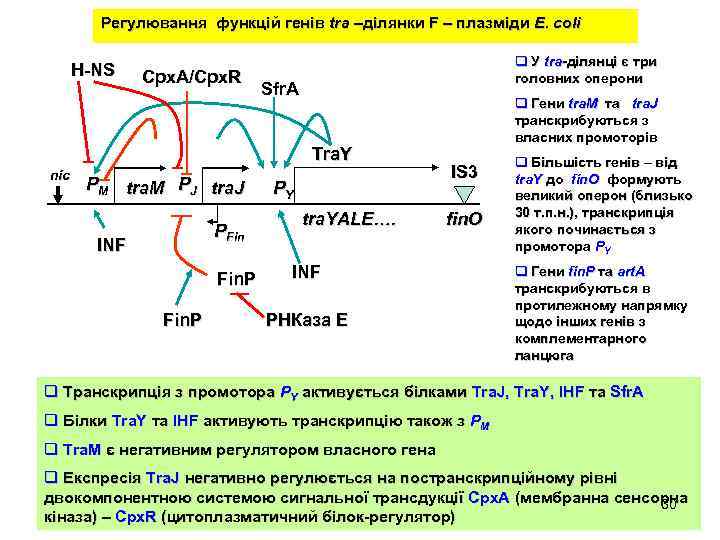
Регулювання функцій генів tra –ділянки F – плазміди E. coli H-NS Cpx. A/Cpx. R q У tra-ділянці є три головних оперони Sfr. A Tra. Y nic PM tra. M PJ tra. J PFin INF Fin. P PY tra. YALE…. q Гени tra. M та tra. J транскрибуються з власних промоторів IS 3 fin. O INF РНКаза Е q Більшість генів – від tra. Y до fin. O формують великий оперон (близько 30 т. п. н. ), транскрипція якого починається з промотора PY q Гени fin. P та art. A транскрибуються в протилежному напрямку щодо інших генів з комплементарного ланцюга q Транскрипція з промотора PY активується білками Tra. J, Tra. Y, IHF та Sfr. A q Білки Tra. Y та IHF активують транскрипцію також з PM q Tra. M є негативним регулятором власного гена q Експресія Tra. J негативно регулюється на постранскрипційному рівні двокомпонентною системою сигнальної трансдукції Cpx. A (мембранна сенсорна 30 кіназа) – Срх. R (цитоплазматичний білок-регулятор)
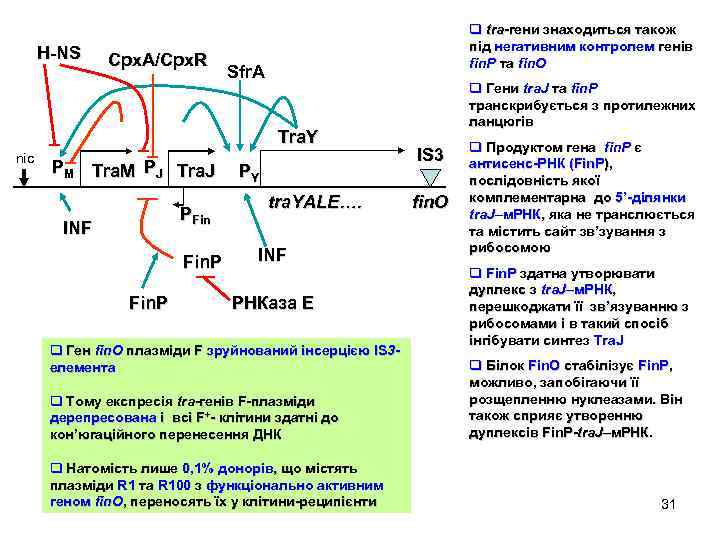
H-NS Cpx. A/Cpx. R q tra-гени знаходиться також під негативним контролем генів fin. P та fin. О Sfr. A Tra. Y nic PM Tra. M PJ Tra. J PFin INF Fin. P PY tra. YALE…. INF РНКаза Е q Ген fin. О плазміди F зруйнований інсерцією IS 3 елемента q Тому експресія tra-генів F-плазміди дерепресована і всі F+- клітини здатні до кон’югаційного перенесення ДНК q Натомість лише 0, 1% донорів, що містять плазміди R 1 та R 100 з функціонально активним геном fin. О, переносять їх у клітини-реципієнти q Гени tra. J та fin. P транскрибується з протилежних ланцюгів IS 3 fin. O q Продуктом гена fin. P є антисенс-РНК (Fin. P), послідовність якої комплементарна до 5’-ділянки tra. J–м. РНК, яка не транслюється та містить сайт зв’зування з рибосомою q Fin. P здатна утворювати дуплекс з tra. J–м. РНК, перешкоджати її зв’язуванню з рибосомами і в такий спосіб інгібувати синтез Tra. J q Білок Fin. О стабілізує Fin. P, можливо, запобігаючи її розщепленню нуклеазами. Він також сприяє утворенню дуплексів Fin. P-tra. J–м. РНК. 31
MG_9.ppt