 Плавление и кристаллизация
Плавление и кристаллизация
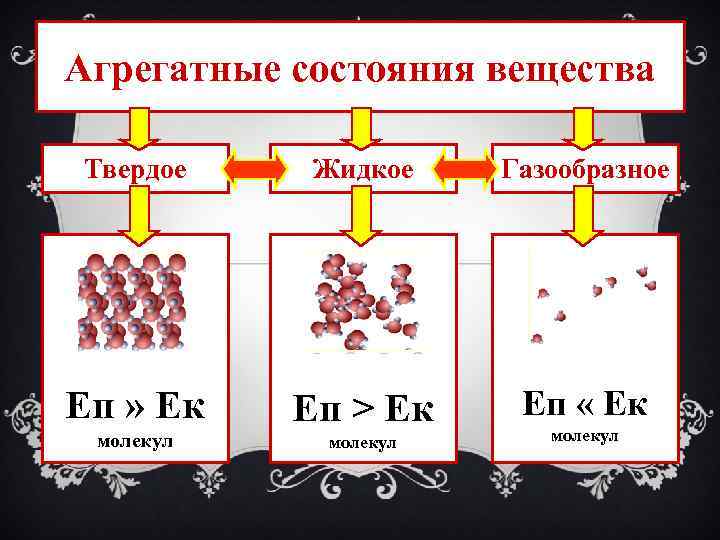 Агрегатные состояния вещества Твердое Жидкое Газообразное Еп » Ек Еп > Ек Еп « Ек молекул
Агрегатные состояния вещества Твердое Жидкое Газообразное Еп » Ек Еп > Ек Еп « Ек молекул
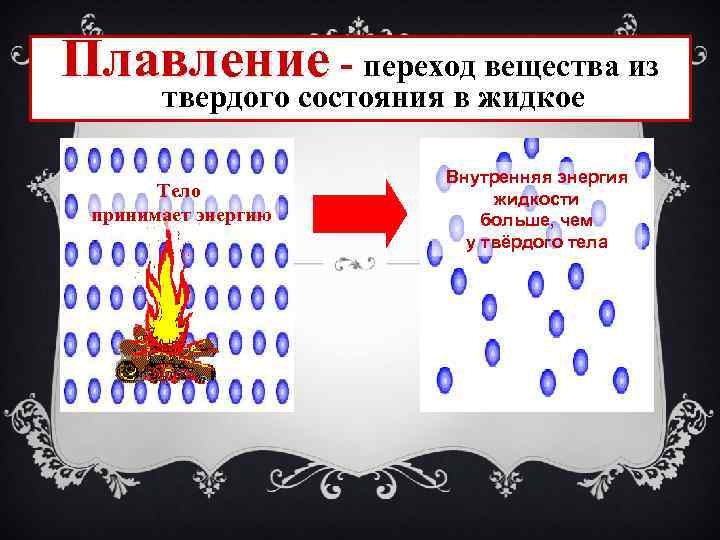 Плавление - переход вещества из твердого состояния в жидкое Тело принимает энергию Внутренняя энергия жидкости больше, чем у твёрдого тела
Плавление - переход вещества из твердого состояния в жидкое Тело принимает энергию Внутренняя энергия жидкости больше, чем у твёрдого тела
 на гре ва ни е плавление ни е ва на гре Поглощение Q 1. При нагревании увеличивается температура тела. 2. Скорость колебания частиц возрастает. 3. Увеличивается внутренняя энергия тела. 4. Когда тело нагревается до температуры плавления, кристаллическая решетка начинает разрушаться. 5. Энергия нагревателя идет на разрушение решетки кристалла. Температуру, при которой вещество плавится, называют температурой плавления вещества. Каждое вещество имеет собственную температуру плавления.
на гре ва ни е плавление ни е ва на гре Поглощение Q 1. При нагревании увеличивается температура тела. 2. Скорость колебания частиц возрастает. 3. Увеличивается внутренняя энергия тела. 4. Когда тело нагревается до температуры плавления, кристаллическая решетка начинает разрушаться. 5. Энергия нагревателя идет на разрушение решетки кристалла. Температуру, при которой вещество плавится, называют температурой плавления вещества. Каждое вещество имеет собственную температуру плавления.
 При нормальном давлении, наибольшей температурой плавления среди металлов облада ет вольфрам (3422 °C), простых веществ вообще - углерод (по разным данным 3500 — 4500 °C[2]) а среди произвольных веществ — карбид гафния Hf. C (3890 °C). Можно считать, что самой низкой температурой плавления обладает гелий: при нормальном давлении он остаётся жидким при сколь угодно низких температурах.
При нормальном давлении, наибольшей температурой плавления среди металлов облада ет вольфрам (3422 °C), простых веществ вообще - углерод (по разным данным 3500 — 4500 °C[2]) а среди произвольных веществ — карбид гафния Hf. C (3890 °C). Можно считать, что самой низкой температурой плавления обладает гелий: при нормальном давлении он остаётся жидким при сколь угодно низких температурах.
 Кристаллизация — процесс фазового перехода вещества из жидкого состояния в твёрдое кристаллическое с образованием кристаллов.
Кристаллизация — процесс фазового перехода вещества из жидкого состояния в твёрдое кристаллическое с образованием кристаллов.
 и ен жд ла ох е Выделение Q отвердевание ие ен жд ла ох 1. При охлаждении уменьшается температура жидкости. 2. Скорость движения частиц уменьшается. 3. Уменьшается внутренняя энергия жидкости. 4. Когда тело охлаждается до температуры плавления, кристаллическая решетка начинает восстанавливаться. t плавления = t отвердевания Температуру, при которой вещество отвердевает, называют температурой отвердевания. Количество теплоты, выделяющееся при отвердевании (кристаллизации), равно количеству теплоты, поглощённому при плавлении.
и ен жд ла ох е Выделение Q отвердевание ие ен жд ла ох 1. При охлаждении уменьшается температура жидкости. 2. Скорость движения частиц уменьшается. 3. Уменьшается внутренняя энергия жидкости. 4. Когда тело охлаждается до температуры плавления, кристаллическая решетка начинает восстанавливаться. t плавления = t отвердевания Температуру, при которой вещество отвердевает, называют температурой отвердевания. Количество теплоты, выделяющееся при отвердевании (кристаллизации), равно количеству теплоты, поглощённому при плавлении.
 В начале 2010 года группа физиков из Ливерморской национальной лаборатории им. Лоуренса, Калифорнийского университета в Беркли и Рочестерского университета провела уникальные измерения температуры плавления алмаза. «Особенность эксперимента заключается в том, что простым повышением температуры перехода в жидкое состояние добиться невозможно, — объясняет ведущий автор исследования Джон Эггерт. — Приходится создавать высочайшее давление, что резко усложняет процесс измерения» . Увеличивать давление необходимо для того, чтобы алмаз в процессе нагревания не превращался в графит. По данным БСЭ, на которые ссылается Википедия (http: //ru. wikipedia. org), на воздухе алмаз сгорает при температуре 850 -1000 °С, а при нагреве до температур примерно 1800 -2000 °C без доступа воздуха алмаз переходит в графит.
В начале 2010 года группа физиков из Ливерморской национальной лаборатории им. Лоуренса, Калифорнийского университета в Беркли и Рочестерского университета провела уникальные измерения температуры плавления алмаза. «Особенность эксперимента заключается в том, что простым повышением температуры перехода в жидкое состояние добиться невозможно, — объясняет ведущий автор исследования Джон Эггерт. — Приходится создавать высочайшее давление, что резко усложняет процесс измерения» . Увеличивать давление необходимо для того, чтобы алмаз в процессе нагревания не превращался в графит. По данным БСЭ, на которые ссылается Википедия (http: //ru. wikipedia. org), на воздухе алмаз сгорает при температуре 850 -1000 °С, а при нагреве до температур примерно 1800 -2000 °C без доступа воздуха алмаз переходит в графит.
 В настоящее время можно считать твердо установленным, что жидкость может затвердевать после ее охлаждения до температуры плавления только при наличии в ней «центров кристаллизации» . В случае их отсутствия жидкость «переохлаждается» , т. е. температура понижается ниже точки плавления данного вещества, но вещество остается в жидком состоянии. Возможность такого переохлаждения для воды была замечена уже более двухсот лет назад, в 1724 г. , Фаренгейтом.
В настоящее время можно считать твердо установленным, что жидкость может затвердевать после ее охлаждения до температуры плавления только при наличии в ней «центров кристаллизации» . В случае их отсутствия жидкость «переохлаждается» , т. е. температура понижается ниже точки плавления данного вещества, но вещество остается в жидком состоянии. Возможность такого переохлаждения для воды была замечена уже более двухсот лет назад, в 1724 г. , Фаренгейтом.
 СПАСИБО ЗА ВНИМАНИЕ!
СПАСИБО ЗА ВНИМАНИЕ!