Пример2_2011.ppt
- Количество слайдов: 14
![Планирование синтеза координационного соединения Бис(2, 4 -пентандионато)цинк(II) [Zn(C 5 H 7 O 2)2] [Zn(AA)2] Планирование синтеза координационного соединения Бис(2, 4 -пентандионато)цинк(II) [Zn(C 5 H 7 O 2)2] [Zn(AA)2]](https://present5.com/presentation/83958387_147578116/image-1.jpg)
Планирование синтеза координационного соединения Бис(2, 4 -пентандионато)цинк(II) [Zn(C 5 H 7 O 2)2] [Zn(AA)2]
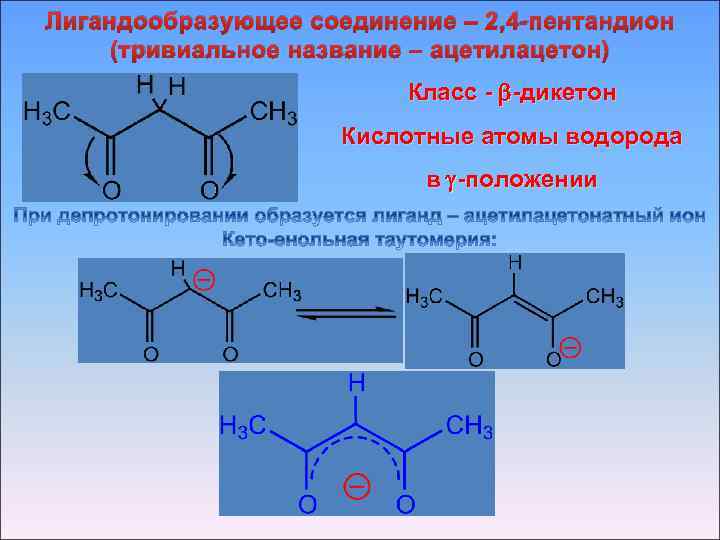
Лигандообразующее соединение – 2, 4 -пентандион (тривиальное название – ацетилацетон) Класс - -дикетон Кислотные атомы водорода в -положении
![[Zn(C 5 H 7 O 2)2] Из Кембриджского банка структурных данных! [Zn(C 5 H 7 O 2)2] Из Кембриджского банка структурных данных!](https://present5.com/presentation/83958387_147578116/image-3.jpg)
[Zn(C 5 H 7 O 2)2] Из Кембриджского банка структурных данных!

Расчет начинается с:
![Zn(NO 3)2 6 H 2 O + 2 HAA = [Zn(AA)2] + 2 HNO Zn(NO 3)2 6 H 2 O + 2 HAA = [Zn(AA)2] + 2 HNO](https://present5.com/presentation/83958387_147578116/image-5.jpg)
Zn(NO 3)2 6 H 2 O + 2 HAA = [Zn(AA)2] + 2 HNO 3 + + 6 H 2 O HNO 3 + NH 3 H 2 O(5% р-р) = NH 4 NO 3 + H 2 O Zn(NO 3)2 6 H 2 O + 2 HAA + 2 NH 3 H 2 O(5%р-р) = =[Zn(AA)2] + 2 NH 4 NO 3 + 8 H 2 O

Стехиометрические расчеты Zn(NO 3)2 6 H 2 O + 2 HAA + 297, 46 100, 12 22, 57 2 NH 3 H 2 O(5% =[Zn(AA)2] + 2 NH 4 NO 3 + 8 H 2 O 35 263, 59 Мr, г/моль 15, 19 5, 31 20/ 21, 37! m, г 7, 59*10 -2 1, 52*10 -1 7, 59*10 -2 n, моль 1843 200 При =25% р25%=0. 908 г/мл При =5% р5%=0. 977 г/мл 4 Растворимость в воде, г/л, 20 С р-р) m(Zn(NO 3)2 6 H 2 O) = m([Zn(AA)2])*M(Zn(NO 3)2 6 H 2 O)/M([Zn(AA)2]) = 20*297, 46/263, 59 = 22, 57 г m(HAA) = 2*m([Zn(AA)2])*M(HAA)/M([Zn(AA)2]) = 20*100, 12/263, 59 = 15, 19 г V(HAA) = 1. 05*m(HAA)/ (HAA) = 1. 05*15, 19/0. 97 = 16, 4 мл m(NH 3 H 2 O) = m([Zn(AA)2])*M(NH 3 H 2 O)/M([Zn(AA)2]) = 20*35/263, 59 = 5. 31 г Vр(NH 3 H 2 O)25% = m(NH 3 H 2 O) /(0, 25* р (NH 3 H 2 O)25%) = 5, 31/(0, 25*0, 908) = 23, 4 мл Vр(NH 3 H 2 O)5% = m(NH 3 H 2 O) /(0, 05* р (NH 3 H 2 O)5%) = 5, 31/(0, 05*0, 977) = 108, 7 мл

V(H 2 O для Zn(NO 3)2 6 H 2 O) = m(Zn(NO 3)2 6 H 2 O)*1000/k = 22, 57*1000/1843 = = 12, 25 мл V(H 2 O для НАА) = m(НАА)*1000/k = 15, 19*1000/200 = 75, 95 мл m(Zn(NO 3)2 6 H 2 O), г V(HAA), мл Vр(NH 3 H 2 O)25%, мл V(H 2 O для р-ра NH 3 H 2 O 5%), мл 22, 54 16, 4 23, 4 85, 3 V(H 2 O для растворения реагентов), мл 80

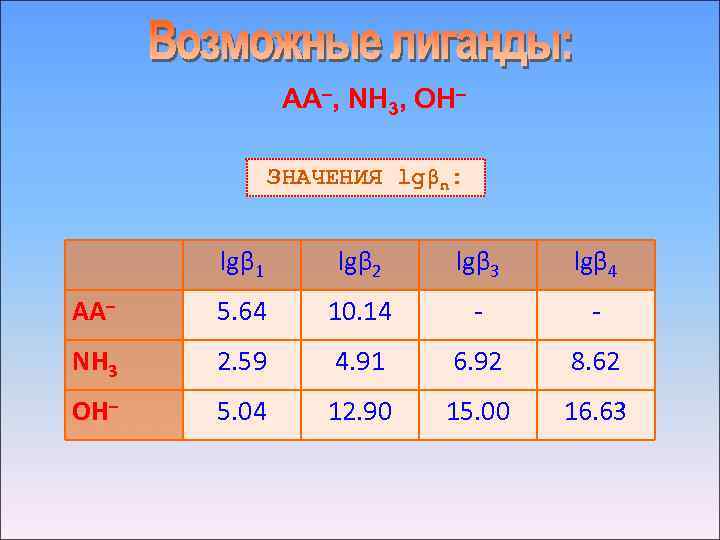
AA–, NH 3, OH– ЗНАЧЕНИЯ lgβn: lgβ 1 lgβ 2 lgβ 3 lgβ 4 AA– 5. 64 10. 14 - - NH 3 2. 59 4. 91 6. 92 8. 62 OH– 5. 04 12. 90 15. 00 16. 63
![[Zn(AA)2] + 4 NH 3 [Zn(NH 3)4]2+ + 2 AA– Kc = [Zn(NH 3)42+][AA–]2 [Zn(AA)2] + 4 NH 3 [Zn(NH 3)4]2+ + 2 AA– Kc = [Zn(NH 3)42+][AA–]2](https://present5.com/presentation/83958387_147578116/image-10.jpg)
[Zn(AA)2] + 4 NH 3 [Zn(NH 3)4]2+ + 2 AA– Kc = [Zn(NH 3)42+][AA–]2 [Zn(AA)2][NH 3]4 = β 4([Zn(NH 3)4]2+) β 2([Zn(AA)2]) = 108. 62 1010. 14 = 10– 1. 52 < 1 [Zn(AA)2] + 4 OH– [Zn(OH)4]2– + 2 AA– Kc = [Zn(OH)42–][AA–]2 [Zn(AA)2][OH–]4 = β 4([Zn(OH)4]2–) β 2([Zn(AA)2]) = 1016. 63 1010. 14 = 106. 49 > 1 Образование гидроксо-комплексов возможно, поэтому следует обратить особое внимание на добавление гидрата аммиака!

р. Н, при котором в растворе соли без присутствия лиганда может образоваться гидроксид: Zn(OH)2(т) Zn 2+ + 2 OH– ПР(Zn(OH)2)25 C = 3, 0 10 -16 ПР = [Zn 2+][OH–]2 = 0. 5*[OH–]3 => p. H = 8, 8
![[Zn(AA)2] + 2 OH– Zn(OH)2(т)+ 2 AA– Kc = Примем! =1 = β 2([Zn(AA)2])*ПР(Zn(OH)2) [Zn(AA)2] + 2 OH– Zn(OH)2(т)+ 2 AA– Kc = Примем! =1 = β 2([Zn(AA)2])*ПР(Zn(OH)2)](https://present5.com/presentation/83958387_147578116/image-12.jpg)
[Zn(AA)2] + 2 OH– Zn(OH)2(т)+ 2 AA– Kc = Примем! =1 = β 2([Zn(AA)2])*ПР(Zn(OH)2) 1 [AA–]2 [Zn(AA)2][OH–]4 Zn(OH)2(т) Zn 2+ + 2 OH– ПР = [Zn 2+][OH–]2 = 0. 5*[OH–]3 => Kc = [OH–] = ( 1 β 2([Zn(AA)2])* 0. 5*[OH–]3 1 )1/3 = 5. 25*10 -4 моль/л β 2([Zn(AA)2])* 0. 5*Kc р. Н < 14+lg[OH–] < 10. 7, а лучше < 8, 8

Методика синтеза: • Описание 1. Взвешивание соли. 2. Растворение навески в 80 мл воды. 3. Фильтрация раствора через бумажный фильтр. 4. Измерение объема НАА, смешение с раствором соли. 5. Приготовление 5 %-ного раствора NH 3 H 2 O. 6. Медленное прикапывание 5%-ного раствора NH 3 H 2 O к раствору соли и НАА при интенсивн. перемешивании. 7. Периодически проверять р. Н, рекомендуемое значение < 7. • Необходимое оборудование и материалы: 1. Весы техн. , точность 0, 01 г 2. Стакан хим. , объем 150 – 200 мл, цилиндр мерн. на 100 мл. 3. Стекл. воронка, фильтр. бумага, стакан на 400 мл. 4. Мерн. цилиндр на 25 мл, механич. мешалка. 5. Емкость для хранения этого р -ра, мерн. цилиндры на 25 и 100 мл. 6. Капельная воронка объемом не менее 150 мл с пробкой, штатив. 7. Индикаторная бумага.

• РИСУНКИ УСТАНОВОК ДЛЯ СИНТЕЗА И ВЫДЕЛЕНИЯ • После массового осаждения соединения отделить осадок от маточного раствора вакуумным фильтрованием. На фильтре промыть охлажденной дист. водой. • Сушить вещество при температуре 60 -75 С до постоянной массы. • Взвесить, рассчитать выход. • Далее соединение следует перекристаллизовать из пропанола. • Выделить соединение, высушить до постоянной массы (70 С), расфасовать. • Идентифицировать методами элементного анализа – анализ на металл, ИК-спектроскопия, РФА. • Написание и сдача отчета.
Пример2_2011.ppt