
 План 1. Хімічна кінетика - як розділ хімії. 2. Класифікація хімічних реакцій. 3. Швидкість гомогенних хімічних реакцій. 3. 1. Закон діючих мас. Порядок реакцій. 3. 2. Вплив температури швидкість. Енергія активації. Правило Вант-Гоффа. Рівняння Арреніуса. 3. 3. Каталізатори. Каталіз. 4. Швидкість гетерогенних хімічних реакцій.
План 1. Хімічна кінетика - як розділ хімії. 2. Класифікація хімічних реакцій. 3. Швидкість гомогенних хімічних реакцій. 3. 1. Закон діючих мас. Порядок реакцій. 3. 2. Вплив температури швидкість. Енергія активації. Правило Вант-Гоффа. Рівняння Арреніуса. 3. 3. Каталізатори. Каталіз. 4. Швидкість гетерогенних хімічних реакцій.
 Хімічна кінетика – розділ хімії що вивчає механізми хімічних процесів та закономірності перебігу хімічних реакцій у часі.
Хімічна кінетика – розділ хімії що вивчає механізми хімічних процесів та закономірності перебігу хімічних реакцій у часі.
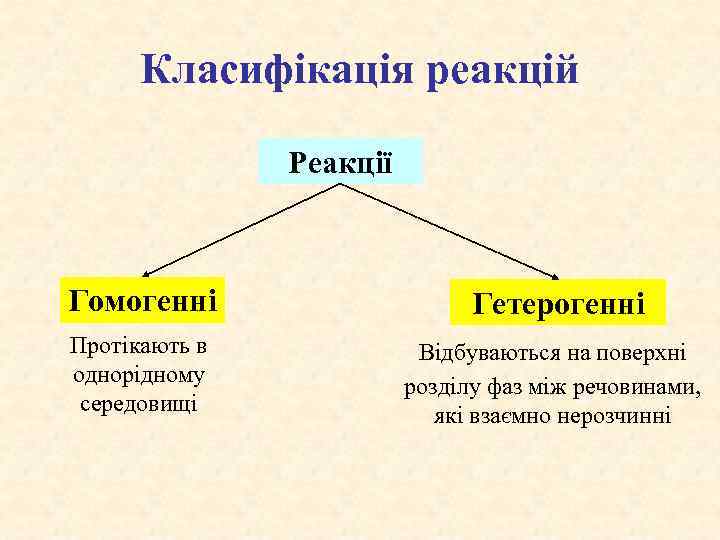 Класифікація реакцій Реакції Гомогенні Гетерогенні Протікають в однорідному середовищі Відбуваються на поверхні розділу фаз між речовинами, які взаємно нерозчинні
Класифікація реакцій Реакції Гомогенні Гетерогенні Протікають в однорідному середовищі Відбуваються на поверхні розділу фаз між речовинами, які взаємно нерозчинні
 Класифікація реакцій Реакції Оборотні Необоротні
Класифікація реакцій Реакції Оборотні Необоротні
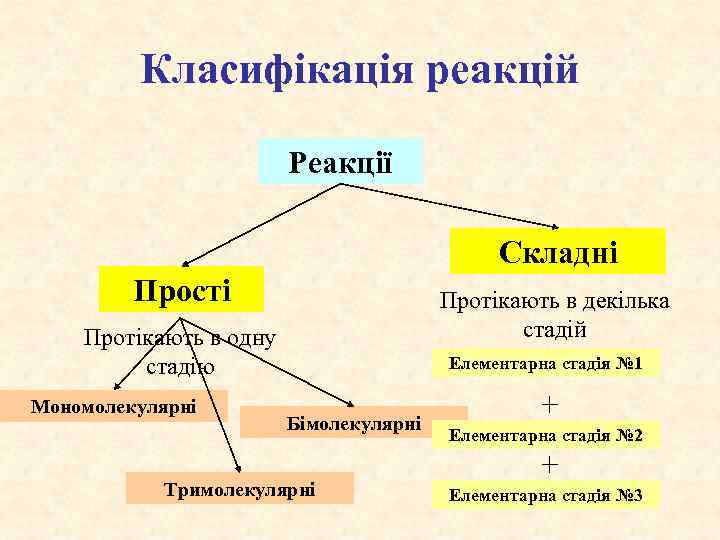 Класифікація реакцій Реакції Складні Прості Протікають в декілька стадій Протікають в одну стадію Мономолекулярні Елементарна стадія № 1 Бімолекулярні Тримолекулярні + Елементарна стадія № 2 + Елементарна стадія № 3
Класифікація реакцій Реакції Складні Прості Протікають в декілька стадій Протікають в одну стадію Мономолекулярні Елементарна стадія № 1 Бімолекулярні Тримолекулярні + Елементарна стадія № 2 + Елементарна стадія № 3
 Класифікація реакцій 2 NO + Br 2 = 2 NOBr 1) NO + Br 2 = NOBr 2 2) NOBr 2 + NO = 2 NOBr
Класифікація реакцій 2 NO + Br 2 = 2 NOBr 1) NO + Br 2 = NOBr 2 2) NOBr 2 + NO = 2 NOBr
 Швидкість хімічної реакції це кількість актів взаємодії за одиницю часу в одиниці об’єму (для гомогенних реакцій) або на одиниці поверхні розділу фаз (для гетерогенних реакцій).
Швидкість хімічної реакції це кількість актів взаємодії за одиницю часу в одиниці об’єму (для гомогенних реакцій) або на одиниці поверхні розділу фаз (для гетерогенних реакцій).
 Швидкість гомогенної хімічної реакції при сталому об’ємі системи вимірюється зміною концентрацій реагентів за одиницю часу: ; де с – концентрація реагенту, моль/л; t– час, с. Яку швидкість називають істинною, а яку середньою?
Швидкість гомогенної хімічної реакції при сталому об’ємі системи вимірюється зміною концентрацій реагентів за одиницю часу: ; де с – концентрація реагенту, моль/л; t– час, с. Яку швидкість називають істинною, а яку середньою?
 Вплив концентрацій реагуючих речовин на швидкість. Закон діючих мас швидкість хімічної реакції прямопропорційна добутку концентрацій реагуючих речовин у ступенях, які дорівнюють стехіометричним коефіцієнтам, що стоять перед формулами відповідних речовин у рівнянні реакції. x. A+y. B=z. AB Для прямої реакції Для зворотної реакції v = k C Ax C B y v = k CABz v = k [A]x [B]y v = k [AB]z
Вплив концентрацій реагуючих речовин на швидкість. Закон діючих мас швидкість хімічної реакції прямопропорційна добутку концентрацій реагуючих речовин у ступенях, які дорівнюють стехіометричним коефіцієнтам, що стоять перед формулами відповідних речовин у рівнянні реакції. x. A+y. B=z. AB Для прямої реакції Для зворотної реакції v = k C Ax C B y v = k CABz v = k [A]x [B]y v = k [AB]z
 Закон діючих мас Гульдберг і Вааге (1867 р. ) швидкість гомогенної реакції при сталій температурі прямопропорційна добутку концентрацій речовин, що реагують H 2(г) + І2(г) = 2 HІ(г) v 1 = k 1[H 2] [І2] Константа швидкості хімічної реакції 2 NO(г) + О 2(г) = 2 NO 2(г), v 2 = k 2[NO]2 [O 2]. Константа швидкості хімічної реакції рівна швидкості хімічної реакції за умови, що концентрації реагуючих речовин рівні 1.
Закон діючих мас Гульдберг і Вааге (1867 р. ) швидкість гомогенної реакції при сталій температурі прямопропорційна добутку концентрацій речовин, що реагують H 2(г) + І2(г) = 2 HІ(г) v 1 = k 1[H 2] [І2] Константа швидкості хімічної реакції 2 NO(г) + О 2(г) = 2 NO 2(г), v 2 = k 2[NO]2 [O 2]. Константа швидкості хімічної реакції рівна швидкості хімічної реакції за умови, що концентрації реагуючих речовин рівні 1.
 Закон діючих мас. Задачі. В скільки разів збільшиться швидкість хімічної реакції 2 NO + Cl 2 = 2 NOCl якщо концентрацію нітроґен II оксиду збільшити в 3 рази, а хлору в два рази Дано: [NO]1 = a моль/л, [Cl 2]1 = b моль/л. [NO]1 = 3 a моль/л, [Cl 2]1 = 2 b моль/л. 2 NO + Cl 2 = 2 NOCl, v = k [NO]2 [Cl 2] v 1 = ka 2 b v 2 = k(3 a)2 (2 b) = 18 ka 2 b v 2 18 ka 2 b =18 = 2 b v 1 ka Відповідь: якщо концентрацію нітроґен II оксиду збільшити в 3 рази, а хлору в два рази то швидкість реакції 2 NO + Cl 2 = 2 NOCl зросте у 18 раз
Закон діючих мас. Задачі. В скільки разів збільшиться швидкість хімічної реакції 2 NO + Cl 2 = 2 NOCl якщо концентрацію нітроґен II оксиду збільшити в 3 рази, а хлору в два рази Дано: [NO]1 = a моль/л, [Cl 2]1 = b моль/л. [NO]1 = 3 a моль/л, [Cl 2]1 = 2 b моль/л. 2 NO + Cl 2 = 2 NOCl, v = k [NO]2 [Cl 2] v 1 = ka 2 b v 2 = k(3 a)2 (2 b) = 18 ka 2 b v 2 18 ka 2 b =18 = 2 b v 1 ka Відповідь: якщо концентрацію нітроґен II оксиду збільшити в 3 рази, а хлору в два рази то швидкість реакції 2 NO + Cl 2 = 2 NOCl зросте у 18 раз
 Лімітуюча стадія хімічної реакції. Порядок хімічної реакції Найповільніша стадія, яка визначає швидкість реакції в цілому, називається лімітуючою. Na 2 S 2 O 3 + H 2 SO 4 H 2 S 2 O 3 + Na 2 SO 4 H 2 S 2 O 3 S + H 2 SO 3 - лімітуюча стадія v = k [H 2 S 2 O 3] Показники в реальному кінетичному рівнянні отримали назву порядків реакції – по кожній з реагуючих речовин, а суму цих показників називають сумарним порядком реакції. Порядки реакції a b v = k [A] [B] (a + b) - сумарний порядок реакції.
Лімітуюча стадія хімічної реакції. Порядок хімічної реакції Найповільніша стадія, яка визначає швидкість реакції в цілому, називається лімітуючою. Na 2 S 2 O 3 + H 2 SO 4 H 2 S 2 O 3 + Na 2 SO 4 H 2 S 2 O 3 S + H 2 SO 3 - лімітуюча стадія v = k [H 2 S 2 O 3] Показники в реальному кінетичному рівнянні отримали назву порядків реакції – по кожній з реагуючих речовин, а суму цих показників називають сумарним порядком реакції. Порядки реакції a b v = k [A] [B] (a + b) - сумарний порядок реакції.
 Порядок хімічної реакції Порядки реакції співпадають зі стехіометричними коефіцієнтами хімічного рівняння лише у випадку простих реакцій, що протікають через одну елементарну стадію. Якщо ж реакції складні і протікають через ряд паралельних і послідовних стадій (а таких реакцій переважна більшість), то в цих випадках порядок реакції носить формальний характер і може набувати будь-яке значення (в тому числі дробове чи, навіть, нульове, при великому надлишку реагенту). Порядок реакції показує лише ступінь залежності швидкості реакції від концентрації того чи іншого реагенту.
Порядок хімічної реакції Порядки реакції співпадають зі стехіометричними коефіцієнтами хімічного рівняння лише у випадку простих реакцій, що протікають через одну елементарну стадію. Якщо ж реакції складні і протікають через ряд паралельних і послідовних стадій (а таких реакцій переважна більшість), то в цих випадках порядок реакції носить формальний характер і може набувати будь-яке значення (в тому числі дробове чи, навіть, нульове, при великому надлишку реагенту). Порядок реакції показує лише ступінь залежності швидкості реакції від концентрації того чи іншого реагенту.
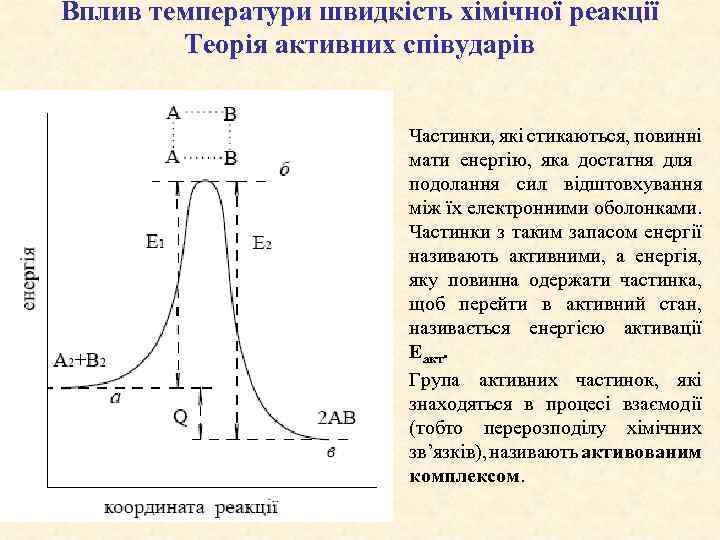 Вплив температури швидкість хімічної реакції Теорія активних співударів Частинки, які стикаються, повинні мати енергію, яка достатня для подолання сил відштовхування між їх електронними оболонками. Частинки з таким запасом енергії називають активними, а енергія, яку повинна одержати частинка, щоб перейти в активний стан, називається енергією активації Еакт. Група активних частинок, які знаходяться в процесі взаємодії (тобто перерозподілу хімічних зв’язків), називають активованим комплексом.
Вплив температури швидкість хімічної реакції Теорія активних співударів Частинки, які стикаються, повинні мати енергію, яка достатня для подолання сил відштовхування між їх електронними оболонками. Частинки з таким запасом енергії називають активними, а енергія, яку повинна одержати частинка, щоб перейти в активний стан, називається енергією активації Еакт. Група активних частинок, які знаходяться в процесі взаємодії (тобто перерозподілу хімічних зв’язків), називають активованим комплексом.
 Енергія активації Енергія, яка необхідна для переведення реагуючих речовин у стан активованого комплексу , називається енергією активації. Енергія активації Еакт – це різниця між середніми значеннями енергії активованого комплексу та середніми значеннями енергій початкових реагентів за даної температури реакції.
Енергія активації Енергія, яка необхідна для переведення реагуючих речовин у стан активованого комплексу , називається енергією активації. Енергія активації Еакт – це різниця між середніми значеннями енергії активованого комплексу та середніми значеннями енергій початкових реагентів за даної температури реакції.
 Теорія активних співударів H 2+I 2 2 HI
Теорія активних співударів H 2+I 2 2 HI
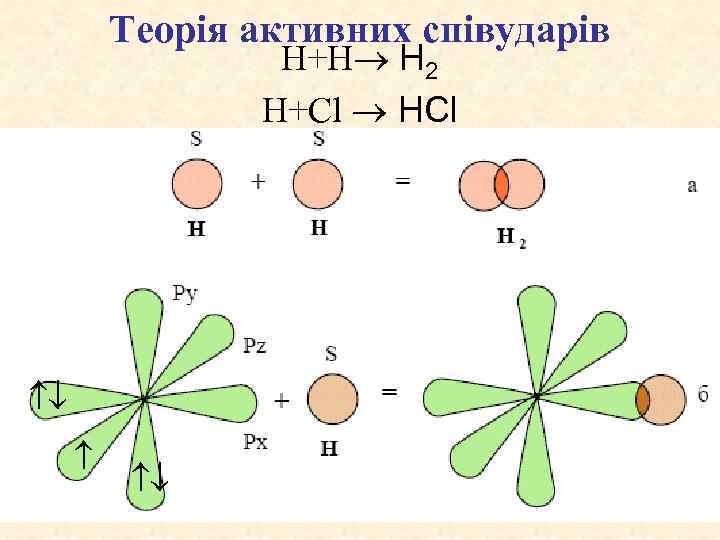 Теорія активних співударів H+Н H 2 H+Cl HCl
Теорія активних співударів H+Н H 2 H+Cl HCl
 Вплив температури на швидкість реакції Правило Вант-Гоффа підвищення температури на кожні 10 градусів збільшує швидкість реакції приблизно у 2 -4 рази Т 2 – Т 1 = Т – збільшення температури, V 1 i V 2 – початкова і кінцева швидкість реакції, g - температурний коефіцієнт швидкості
Вплив температури на швидкість реакції Правило Вант-Гоффа підвищення температури на кожні 10 градусів збільшує швидкість реакції приблизно у 2 -4 рази Т 2 – Т 1 = Т – збільшення температури, V 1 i V 2 – початкова і кінцева швидкість реакції, g - температурний коефіцієнт швидкості
 Рівняння Арреніуса (1889 р. ): k – константа швидкості реакції, Еакт. – енергія активації (для хімічних реакцій Еакт. = 40 -400 к. Дж/моль), А – передекспоненційний множник Арреніуса. Частотний фактор. Пов'язаний із частотою стикання молекул та їх взаємною орієнтацією. Вимірюється в тих же одиницях що і константа швидкості реакції. е=2. 718
Рівняння Арреніуса (1889 р. ): k – константа швидкості реакції, Еакт. – енергія активації (для хімічних реакцій Еакт. = 40 -400 к. Дж/моль), А – передекспоненційний множник Арреніуса. Частотний фактор. Пов'язаний із частотою стикання молекул та їх взаємною орієнтацією. Вимірюється в тих же одиницях що і константа швидкості реакції. е=2. 718
 Каталізатори (позитивні каталізатори) Каталізатори – це речовини, які збільшують швидкість реакції без змін загальної стехіометрії реакції. Каталізатор бере участь у проміжній хімічній взаємодії з компонентами реакційної системи, але не входить до складу продуктів реакції. Як правило, збільшення швидкості каталітичної реакції пов’язане із зменшенням енергії активації
Каталізатори (позитивні каталізатори) Каталізатори – це речовини, які збільшують швидкість реакції без змін загальної стехіометрії реакції. Каталізатор бере участь у проміжній хімічній взаємодії з компонентами реакційної системи, але не входить до складу продуктів реакції. Як правило, збільшення швидкості каталітичної реакції пов’язане із зменшенням енергії активації
 Ферменти ФЕРМЕНТИ (від лат. “fermentum” — шумування, закваска), ензими, специфічні білки, що збільшують швидкість протікання хімічних реакцій у клітках усіх живих організмів. Основні властивості ферментів 1. Специфічність. 2. Термолабільність. 3. Чутливість до р. Н та наявності іонів Na+, K+, Ca 2+ Mn 2+, Zn 2+, Co 2+, Cu 2+, Mg 2+ та ін. 4. Висока активність.
Ферменти ФЕРМЕНТИ (від лат. “fermentum” — шумування, закваска), ензими, специфічні білки, що збільшують швидкість протікання хімічних реакцій у клітках усіх живих організмів. Основні властивості ферментів 1. Специфічність. 2. Термолабільність. 3. Чутливість до р. Н та наявності іонів Na+, K+, Ca 2+ Mn 2+, Zn 2+, Co 2+, Cu 2+, Mg 2+ та ін. 4. Висока активність.
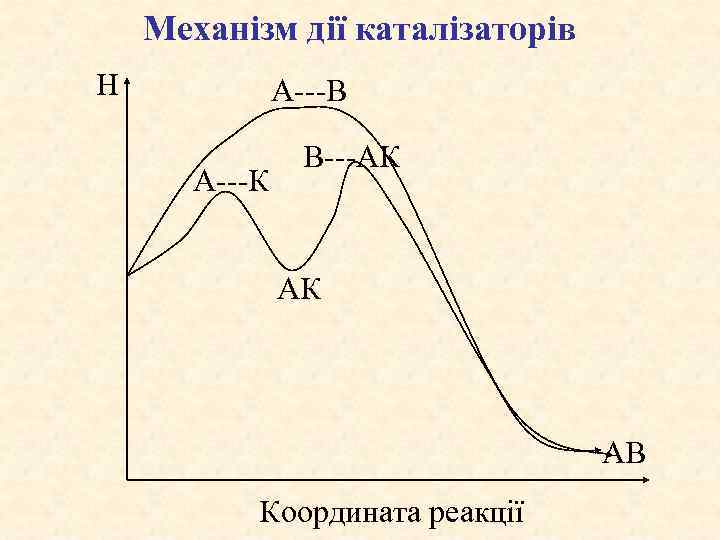 Механізм дії каталізаторів Н А---В А---К B---АК АК АВ Координата реакції
Механізм дії каталізаторів Н А---В А---К B---АК АК АВ Координата реакції
 Інгібітори. (негативні каталізатори) Зменшують швидкість хімічних реакцій, але самі при цьому не витрачаються під час їх перебігу.
Інгібітори. (негативні каталізатори) Зменшують швидкість хімічних реакцій, але самі при цьому не витрачаються під час їх перебігу.
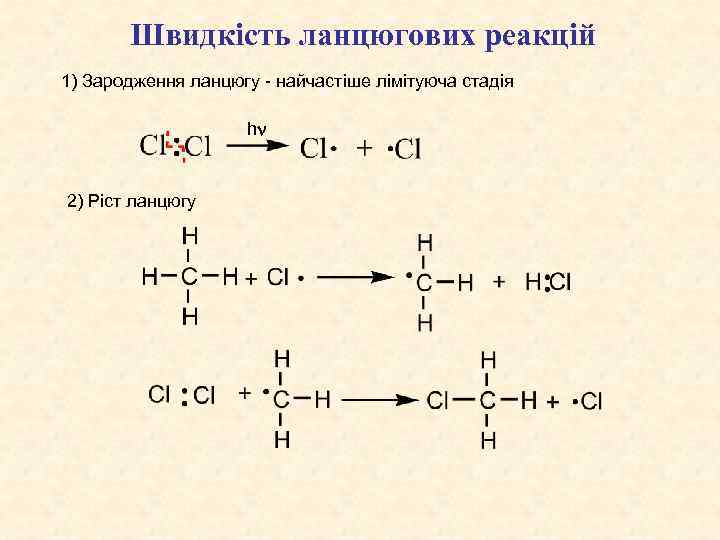 Швидкість ланцюгових реакцій 1) Зародження ланцюгу - найчастіше лімітуюча стадія h 2) Ріст ланцюгу
Швидкість ланцюгових реакцій 1) Зародження ланцюгу - найчастіше лімітуюча стадія h 2) Ріст ланцюгу
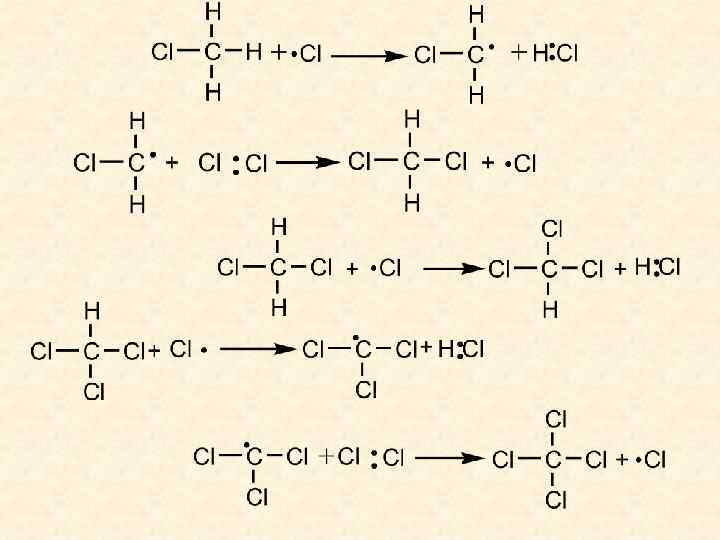
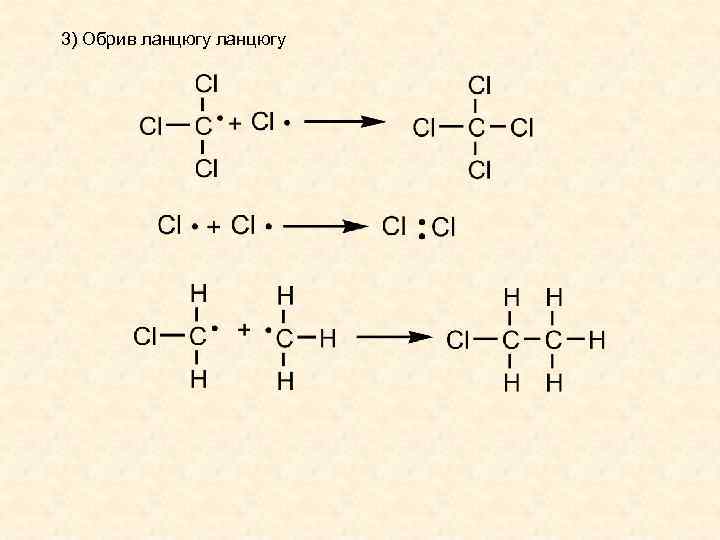 3) Обрив ланцюгу
3) Обрив ланцюгу
 Швидкість гетерогенних хімічних реакцій dn - різниця між кількістю речовини в кінцевий t 2 і початковий t 1 моменти часу (dn = n 2 - n 1). S – площина поверхні.
Швидкість гетерогенних хімічних реакцій dn - різниця між кількістю речовини в кінцевий t 2 і початковий t 1 моменти часу (dn = n 2 - n 1). S – площина поверхні.
 Основні стадії гетерогенних реакцій • підведення однієї реагуючої речовин; • хімічна взаємодія на поверхні; • відведення продукту від поверхні.
Основні стадії гетерогенних реакцій • підведення однієї реагуючої речовин; • хімічна взаємодія на поверхні; • відведення продукту від поверхні.

 План 1. Поняття про хімічну рівновагу. 2. Константа рівноваги. 3. Принцип Ле Шательє
План 1. Поняття про хімічну рівновагу. 2. Константа рівноваги. 3. Принцип Ле Шательє
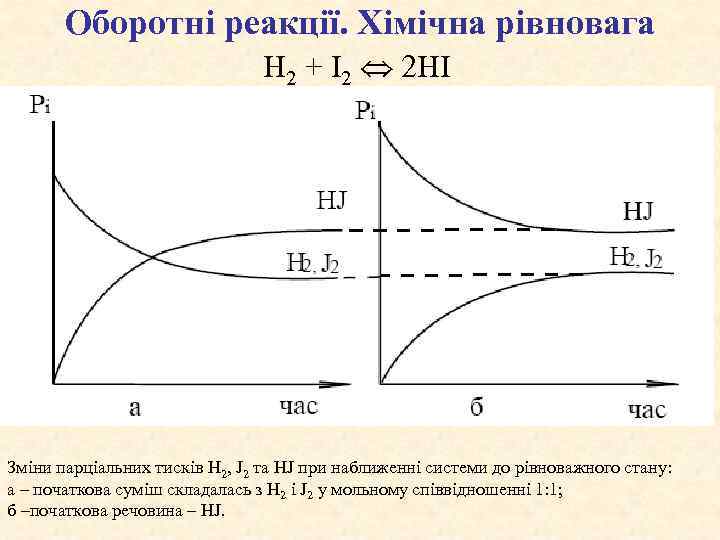 Оборотні реакції. Хімічна рівновага H 2 + I 2 2 HI Зміни парціальних тисків H 2, J 2 та HJ при наближенні системи до рівноважного стану: а – початкова суміш складалась з H 2 i J 2 у мольному співвідношенні 1: 1; б –початкова речовина – HJ.
Оборотні реакції. Хімічна рівновага H 2 + I 2 2 HI Зміни парціальних тисків H 2, J 2 та HJ при наближенні системи до рівноважного стану: а – початкова суміш складалась з H 2 i J 2 у мольному співвідношенні 1: 1; б –початкова речовина – HJ.
 Хімічна рівновага – це стан реакційної системи, у якій пряма та зворотна реакції відбуваються з однаковими швидкостями, внаслідок чого склад системи залишається сталим доти, доки зберігаються незмінними умови її існування (температура, тиск для газофазних систем і т. ін. ).
Хімічна рівновага – це стан реакційної системи, у якій пряма та зворотна реакції відбуваються з однаковими швидкостями, внаслідок чого склад системи залишається сталим доти, доки зберігаються незмінними умови її існування (температура, тиск для газофазних систем і т. ін. ).
 Константа рівноваги а. А + b. B d. D + e. E K – константа хімічної рівноваги це відношення констант швидкостей прямої та зворотної реакцій. В рівноважному стані добуток концентрацій продуктів реакції, поділений на добуток концентрацій вихідних речовин (з врахуванням стехіометричних коефіцієнтів) при постійній температурі-величина стала - константа хімічної рівноваги. Вона не залежить від початкових концентрацій реагентів і продуктів. Значення константи рівноваги залежить тільки від температури.
Константа рівноваги а. А + b. B d. D + e. E K – константа хімічної рівноваги це відношення констант швидкостей прямої та зворотної реакцій. В рівноважному стані добуток концентрацій продуктів реакції, поділений на добуток концентрацій вихідних речовин (з врахуванням стехіометричних коефіцієнтів) при постійній температурі-величина стала - константа хімічної рівноваги. Вона не залежить від початкових концентрацій реагентів і продуктів. Значення константи рівноваги залежить тільки від температури.
 Принцип Ле Шательє Якщо на систему, що перебуває в стані рівноваги, подіяти зовнішнім фактором, то положення рівноваги зміститься у напрямі процесу, який зменшить цю дію. 1. Збільшення концентрації речовини зміщує положення рівноваги в напрямку реакції, в якій ця речовина витрачається. 2. Підвищення температури зміщує положення рівноваги в напрямку ендотермічного процесу: 3. Підвищення тиску (в газофазних системах) зміщує положення рівноваги в напрямку процесу, який супроводжується зменшенням об’єму (а зниження тиску діє протилежним чином). 4. Оскільки каталізатор змінює енергію активації прямої і зворотної реакції на одну і ту ж величину, він прискорює ці реакції однаковою мірою і не впливає на значення константи рівноваги. Тому каталізатор не може змістити положення рівноваги, тобто змінити вихід продукту реакції. Він може лише прискорити досягнення стану рівноваги.
Принцип Ле Шательє Якщо на систему, що перебуває в стані рівноваги, подіяти зовнішнім фактором, то положення рівноваги зміститься у напрямі процесу, який зменшить цю дію. 1. Збільшення концентрації речовини зміщує положення рівноваги в напрямку реакції, в якій ця речовина витрачається. 2. Підвищення температури зміщує положення рівноваги в напрямку ендотермічного процесу: 3. Підвищення тиску (в газофазних системах) зміщує положення рівноваги в напрямку процесу, який супроводжується зменшенням об’єму (а зниження тиску діє протилежним чином). 4. Оскільки каталізатор змінює енергію активації прямої і зворотної реакції на одну і ту ж величину, він прискорює ці реакції однаковою мірою і не впливає на значення константи рівноваги. Тому каталізатор не може змістити положення рівноваги, тобто змінити вихід продукту реакції. Він може лише прискорити досягнення стану рівноваги.
 Типові задачі. Принцип Ле Шательє 3 Н 2(г) + N 2(г) 2 NH 3(г) - Н I 2(г) + H 2(г) 2 HI(г) - Н Fe. O (т) + CO (г) CO 2 (г)
Типові задачі. Принцип Ле Шательє 3 Н 2(г) + N 2(г) 2 NH 3(г) - Н I 2(г) + H 2(г) 2 HI(г) - Н Fe. O (т) + CO (г) CO 2 (г)
 Типові задачі. Константа рівноваги Швидкість утворення HI з йоду та водню при 443°С у момент коли [H 2]=[I 2] =1 дорівнює 1, 5· 10 -2 моль/(хв·л). Швидкість розкладу йодоводню при тій самій температурі та при [HI]=1 дорівнює 3· 104 моль/(хв·л). Визначте константу рівноваги при наведеній температурі. Дано: [H 2]=[I 2] =1 моль/л I 2(г) + H 2(г) 2 HI(г) [HI]=1 моль/л V(утворення HI) = =1, 5· 10 -2 моль/(хв·л) V(розкладу) = =3· 10 -4 моль/(хв·л) Відповідь: I 2(г) + H 2(г) 2 HI(г) Kр=50 K-?
Типові задачі. Константа рівноваги Швидкість утворення HI з йоду та водню при 443°С у момент коли [H 2]=[I 2] =1 дорівнює 1, 5· 10 -2 моль/(хв·л). Швидкість розкладу йодоводню при тій самій температурі та при [HI]=1 дорівнює 3· 104 моль/(хв·л). Визначте константу рівноваги при наведеній температурі. Дано: [H 2]=[I 2] =1 моль/л I 2(г) + H 2(г) 2 HI(г) [HI]=1 моль/л V(утворення HI) = =1, 5· 10 -2 моль/(хв·л) V(розкладу) = =3· 10 -4 моль/(хв·л) Відповідь: I 2(г) + H 2(г) 2 HI(г) Kр=50 K-?
 Типові задачі. Константа рівноваги Рівновага реакції H 2+I 2=2 HI утворилася при таких концентрації речовин, моль/л: [H 2]=0, 3; [I 2]=0, 08; [HI]=0, 35. Визначте вихідні концентрації йоду та водню. Дано: [H 2]=0, 3 [I 2]=0, 08 [HI]=0, 35 Xмоль Yмоль 0, 35 моль I 2(г) + H 2(г) 2 HI(г) 1 моль 2 моль X=(1· 0, 35)/2= 0, 175 Y=(1· 0, 35)/2= 0, 175 Відповідь: початкові концентрації:
Типові задачі. Константа рівноваги Рівновага реакції H 2+I 2=2 HI утворилася при таких концентрації речовин, моль/л: [H 2]=0, 3; [I 2]=0, 08; [HI]=0, 35. Визначте вихідні концентрації йоду та водню. Дано: [H 2]=0, 3 [I 2]=0, 08 [HI]=0, 35 Xмоль Yмоль 0, 35 моль I 2(г) + H 2(г) 2 HI(г) 1 моль 2 моль X=(1· 0, 35)/2= 0, 175 Y=(1· 0, 35)/2= 0, 175 Відповідь: початкові концентрації:
 Типові задачі. Константа рівноваги В системі 2 NO + Cl 2 = 2 NOCl вихідні концентрації становлять моль/л: С(NO)=0, 5, C(Cl 2)=0, 2. Розрахуйте константу рівноваги, знаючи, що в момент рівноваги оксид азоту прореагував на 20%. Дано: C(NO)=0, 5 моль/л C(Cl 2)=0, 2 моль/л (NO)=20% K-? [NO]=0. 5 -0. 5*0. 2=0. 4 0. 1 X Y 2 NO + Cl 2 = 2 NOCl 2 1 2 X=(0. 1*1)/2=0. 05 [Cl 2]=0. 2 -0. 05=0. 15 Y=(0. 1*2)/2=0. 1 [NOCl]=0. 1 Відповідь: 2 NO + Cl 2 = 2 NOCl K=0. 417
Типові задачі. Константа рівноваги В системі 2 NO + Cl 2 = 2 NOCl вихідні концентрації становлять моль/л: С(NO)=0, 5, C(Cl 2)=0, 2. Розрахуйте константу рівноваги, знаючи, що в момент рівноваги оксид азоту прореагував на 20%. Дано: C(NO)=0, 5 моль/л C(Cl 2)=0, 2 моль/л (NO)=20% K-? [NO]=0. 5 -0. 5*0. 2=0. 4 0. 1 X Y 2 NO + Cl 2 = 2 NOCl 2 1 2 X=(0. 1*1)/2=0. 05 [Cl 2]=0. 2 -0. 05=0. 15 Y=(0. 1*2)/2=0. 1 [NOCl]=0. 1 Відповідь: 2 NO + Cl 2 = 2 NOCl K=0. 417
 Типові задачі. Константа рівноваги При 400°С для реакції I 2(г) + H 2(г) 2 HI(г) Кр=6, 3. Встановіть рівноважні концентрації речовин якщо початкові концентрації реагуючих речовин були 2 моль/л Дано: I 2(г) + H 2(г) 2 HI(г) Нехай: [I 2]=? [H 2]=? [HI]=x
Типові задачі. Константа рівноваги При 400°С для реакції I 2(г) + H 2(г) 2 HI(г) Кр=6, 3. Встановіть рівноважні концентрації речовин якщо початкові концентрації реагуючих речовин були 2 моль/л Дано: I 2(г) + H 2(г) 2 HI(г) Нехай: [I 2]=? [H 2]=? [HI]=x
 Типові задачі. Константа рівноваги 25, 2 -12, 6 x+1, 575 x 2=x 2 25, 2 -12, 6 x+1, 575 x 2 - x 2 =0 0, 575 x 2 -12, 6 x +25, 2=0 25, 2 -12, 6 x+0, 575 x 2=0
Типові задачі. Константа рівноваги 25, 2 -12, 6 x+1, 575 x 2=x 2 25, 2 -12, 6 x+1, 575 x 2 - x 2 =0 0, 575 x 2 -12, 6 x +25, 2=0 25, 2 -12, 6 x+0, 575 x 2=0
 Типові задачі. Константа рівноваги 0, 575 x 2 -12, 6 x +25, 2=0 Відповідь:
Типові задачі. Константа рівноваги 0, 575 x 2 -12, 6 x +25, 2=0 Відповідь:


