Лекция 2011 люм.pptx
- Количество слайдов: 30

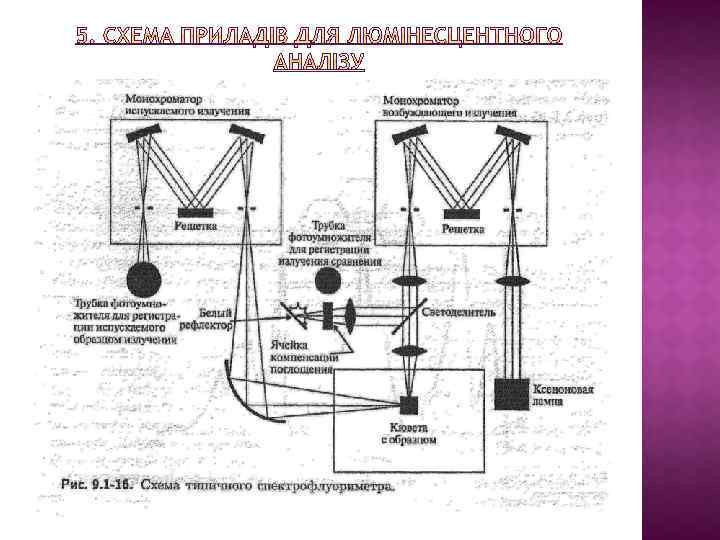
 План 1. СУТЬ ЛЮМІНЕСЦЕНЦІЇ. КЛАСИФІКАЦІЯ ВИДІВ ЛЮМІНЕСЦЕНЦІЇ 2. ХАРАКТЕРИСТИКИ ЛЮМІНЕСЦЕНЦІЇ 3. ОСНОВНІ ЗАКОНИ МОЛЕКУЛЯРНОЇ ЛЮМІНЕСЦЕНЦІЇ 4. ГАСІННЯ ЛЮМІНЕСЦЕНЦІЇ 5. СХЕМА ПРИЛАДІВ ДЛЯ ЛЮМІНЕСЦЕНТНОГО АНАЛІЗУ 6. ЯКІСНИЙ АНАЛІЗ 7. КІЛЬКІСНИЙ АНАЛІЗ 8. ПРАКТИЧНЕ ЗНАЧЕННЯ 9. ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТОДУ
План 1. СУТЬ ЛЮМІНЕСЦЕНЦІЇ. КЛАСИФІКАЦІЯ ВИДІВ ЛЮМІНЕСЦЕНЦІЇ 2. ХАРАКТЕРИСТИКИ ЛЮМІНЕСЦЕНЦІЇ 3. ОСНОВНІ ЗАКОНИ МОЛЕКУЛЯРНОЇ ЛЮМІНЕСЦЕНЦІЇ 4. ГАСІННЯ ЛЮМІНЕСЦЕНЦІЇ 5. СХЕМА ПРИЛАДІВ ДЛЯ ЛЮМІНЕСЦЕНТНОГО АНАЛІЗУ 6. ЯКІСНИЙ АНАЛІЗ 7. КІЛЬКІСНИЙ АНАЛІЗ 8. ПРАКТИЧНЕ ЗНАЧЕННЯ 9. ЗАГАЛЬНА ХАРАКТЕРИСТИКА МЕТОДУ
 Люмінесценція — це світіння атомів, молекул, іонів та інших більш складних комплексів, яке виникає в результаті електронного переходу в цих частинках, при їх повертанні зі збудженого стану в нормальний. В. Л. Левшин Речовини, які здатні люмінесціювати, називають люмінофорами. - Неорганічні люмінофори називають просто люмінофорами. - Органічні люмінофори називають органолюмінофорами. - Складні неорганічні кристалічні люмінофори з дефектною структурою, яка визвана втіленням в їх кристалічну гратку іонів важких металів (активаторів) називають кристалофосфорами.
Люмінесценція — це світіння атомів, молекул, іонів та інших більш складних комплексів, яке виникає в результаті електронного переходу в цих частинках, при їх повертанні зі збудженого стану в нормальний. В. Л. Левшин Речовини, які здатні люмінесціювати, називають люмінофорами. - Неорганічні люмінофори називають просто люмінофорами. - Органічні люмінофори називають органолюмінофорами. - Складні неорганічні кристалічні люмінофори з дефектною структурою, яка визвана втіленням в їх кристалічну гратку іонів важких металів (активаторів) називають кристалофосфорами.
 Дата народження методу 4 березня 1864 року доповідь англійського фізика Стокса у Королівському товаристві. Вказав на можливість використання люмінесценції для аналізу органічних сполук. В розробку теорії люмінесценції великий внесок зробив радянський вчений С. І. Вавілов.
Дата народження методу 4 березня 1864 року доповідь англійського фізика Стокса у Королівському товаристві. Вказав на можливість використання люмінесценції для аналізу органічних сполук. В розробку теорії люмінесценції великий внесок зробив радянський вчений С. І. Вавілов.
 Сергій Іванович Вавілов (1891 -1951) Бібліографічна довідка: – радянський фізик, засновник наукової школи фізичної оптики в Радянському Союзі, академік та Президент АН в СРСР, лауреат Сталінської премії. Молодший брат В. І. Вавілова, російського вченого -генетика. Основним напрямком в науці було дослідження оптики, зокрема явища люмінесценції.
Сергій Іванович Вавілов (1891 -1951) Бібліографічна довідка: – радянський фізик, засновник наукової школи фізичної оптики в Радянському Союзі, академік та Президент АН в СРСР, лауреат Сталінської премії. Молодший брат В. І. Вавілова, російського вченого -генетика. Основним напрямком в науці було дослідження оптики, зокрема явища люмінесценції.

 ВИДИ КЛАСИФІКАЦІЇ ЛЮМІНЕСЦЕНЦІЇ За зовнішнім джерелом збудження За тривалістю світіння За механізмом світіння
ВИДИ КЛАСИФІКАЦІЇ ЛЮМІНЕСЦЕНЦІЇ За зовнішнім джерелом збудження За тривалістю світіння За механізмом світіння
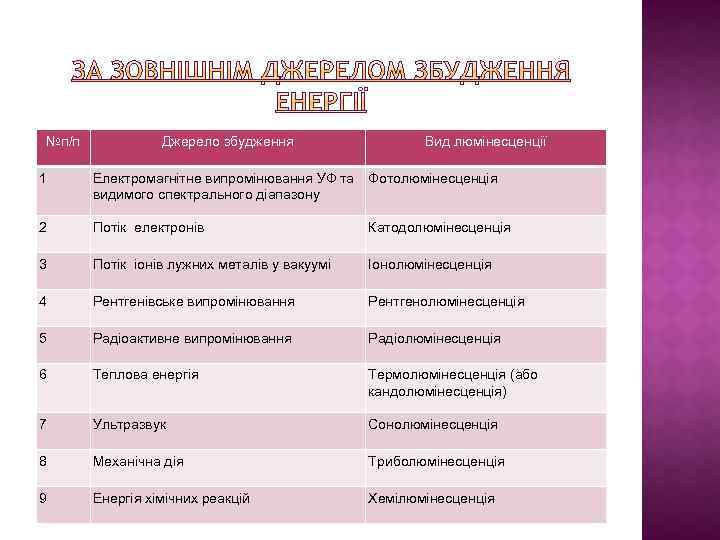 №п/п Джерело збудження Вид люмінесценції 1 Електромагнітне випромінювання УФ та видимого спектрального діапазону Фотолюмінесценція 2 Потік електронів Катодолюмінесценція 3 Потік іонів лужних металів у вакуумі Іонолюмінесценція 4 Рентгенівське випромінювання Рентгенолюмінесценція 5 Радіоактивне випромінювання Радіолюмінесценція 6 Теплова енергія Термолюмінесценція (або кандолюмінесценція) 7 Ультразвук Сонолюмінесценція 8 Механічна дія Триболюмінесценція 9 Енергія хімічних реакцій Хемілюмінесценція
№п/п Джерело збудження Вид люмінесценції 1 Електромагнітне випромінювання УФ та видимого спектрального діапазону Фотолюмінесценція 2 Потік електронів Катодолюмінесценція 3 Потік іонів лужних металів у вакуумі Іонолюмінесценція 4 Рентгенівське випромінювання Рентгенолюмінесценція 5 Радіоактивне випромінювання Радіолюмінесценція 6 Теплова енергія Термолюмінесценція (або кандолюмінесценція) 7 Ультразвук Сонолюмінесценція 8 Механічна дія Триболюмінесценція 9 Енергія хімічних реакцій Хемілюмінесценція
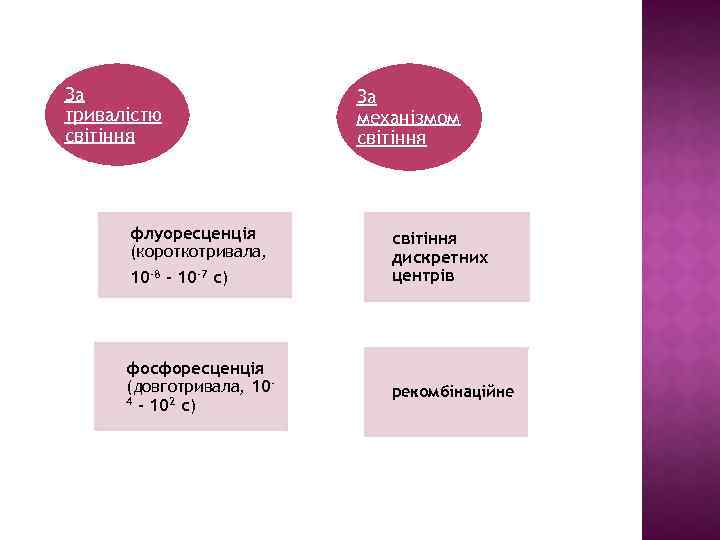 За тривалістю світіння За механізмом світіння флуоресценція (короткотривала, 10 -8 – 10 -7 с) світіння дискретних центрів фосфоресценція (довготривала, 104 – 102 с) рекомбінаційне
За тривалістю світіння За механізмом світіння флуоресценція (короткотривала, 10 -8 – 10 -7 с) світіння дискретних центрів фосфоресценція (довготривала, 104 – 102 с) рекомбінаційне
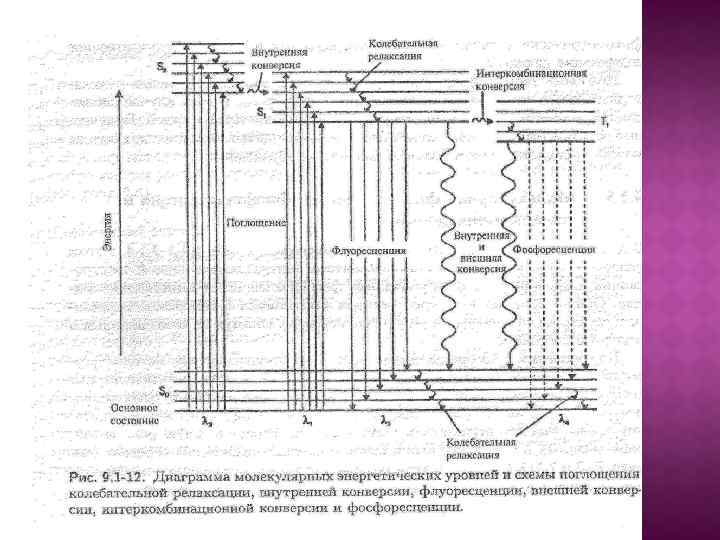
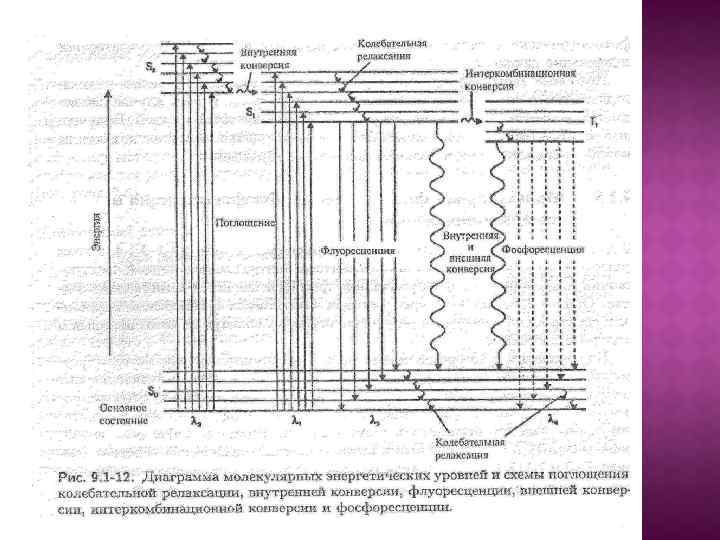
 2. Основні характеристики люмінесценції 1) Спектри поглинання та люмінесценції Спектри поглинання молекул обумовлені переходами з основного стану на збуджений. Спектри поглинання виражають у вигляді залежності поглинання від частоти (довжини хвилі). Спектри люмінесценції молекул обумовлені електронними переходами зі збудженого стану на основний. Спектри люмінесценції представляють у вигляді залежності інтенсивності люмінесценції (І) (або І/ν) від частоти (або λ) випромінювання. Рисунок. Спектр поглинання ε=f(ν) (крива 2) та спектр флуоресценції І/ν = f(ν) (крива 1) родаміну 6 Ж в ацетоні
2. Основні характеристики люмінесценції 1) Спектри поглинання та люмінесценції Спектри поглинання молекул обумовлені переходами з основного стану на збуджений. Спектри поглинання виражають у вигляді залежності поглинання від частоти (довжини хвилі). Спектри люмінесценції молекул обумовлені електронними переходами зі збудженого стану на основний. Спектри люмінесценції представляють у вигляді залежності інтенсивності люмінесценції (І) (або І/ν) від частоти (або λ) випромінювання. Рисунок. Спектр поглинання ε=f(ν) (крива 2) та спектр флуоресценції І/ν = f(ν) (крива 1) родаміну 6 Ж в ацетоні
 2) Тривалість світіння , τ – середній проміжок часу, на протязі якого молекули люмінофора знаходяться в збудженому стані. Флуоресценція (короткотривала)– випромінювальний перехід між двома електронними станами однакової мультиплетності: S 1 → S 0. Тривалість флуоресценції – τ 10 -8 – 10 -7 с. Фосфоресценція (довготривала)- випромінювальний перехід між двома електронними станами різної мультиплетності: Т 1 → S 0. Тривалість фосфоресценції -4 – 102 с. – τ - 10 Спектр фосфоресценції здвигнутий в низькочастотну (довгохвильову) область відносно спектру флуоресценції на величину, рівну різниці енергій станів S 1 і Т 1. Фосфоресценцію не спостерігають у сполук, які мають сильну флуоресценцію. Фосфоресценція характерна для пестицидів, аніонних кислот, ферментів, вуглеводнів нафти.
2) Тривалість світіння , τ – середній проміжок часу, на протязі якого молекули люмінофора знаходяться в збудженому стані. Флуоресценція (короткотривала)– випромінювальний перехід між двома електронними станами однакової мультиплетності: S 1 → S 0. Тривалість флуоресценції – τ 10 -8 – 10 -7 с. Фосфоресценція (довготривала)- випромінювальний перехід між двома електронними станами різної мультиплетності: Т 1 → S 0. Тривалість фосфоресценції -4 – 102 с. – τ - 10 Спектр фосфоресценції здвигнутий в низькочастотну (довгохвильову) область відносно спектру флуоресценції на величину, рівну різниці енергій станів S 1 і Т 1. Фосфоресценцію не спостерігають у сполук, які мають сильну флуоресценцію. Фосфоресценція характерна для пестицидів, аніонних кислот, ферментів, вуглеводнів нафти.
 3) ВИХІД ЛЮМІНЕСЦЕНЦІЇ Величина виходу люмінесценції В характеризує ефективність трансформації світла збудження в світло люмінесценції. Енергетичним виходом люмінесценції Вен називають відношення енергії, яка випромінюється речовиною, Евипр до енергії збудження Епогл, за рахунок якої виникає люмінесценція. Вен=Евипр / Епогл Квантовий вихід люмінесценції Вкв — це відношення кількості квантів люмінесценції (Nвипр), які випущені речовиною, до числа поглинених квантів світла, що збуджує (Nпогл) Вкв= Nвипр / Nпогл
3) ВИХІД ЛЮМІНЕСЦЕНЦІЇ Величина виходу люмінесценції В характеризує ефективність трансформації світла збудження в світло люмінесценції. Енергетичним виходом люмінесценції Вен називають відношення енергії, яка випромінюється речовиною, Евипр до енергії збудження Епогл, за рахунок якої виникає люмінесценція. Вен=Евипр / Епогл Квантовий вихід люмінесценції Вкв — це відношення кількості квантів люмінесценції (Nвипр), які випущені речовиною, до числа поглинених квантів світла, що збуджує (Nпогл) Вкв= Nвипр / Nпогл
 3. ОСНОВНІ ЗАКОНИ ЛЮМІНЕСЦЕНЦІЇ 1. Правило Каші 2. Закон Стокса-Ломеля 3. Правило Левшина ( дзеркальна симетрія) 4. Закон Вавілова 5. Закон затухання люмінесценції 6. Залежність інтенсивності люмінесценції від концентрації люмінофора
3. ОСНОВНІ ЗАКОНИ ЛЮМІНЕСЦЕНЦІЇ 1. Правило Каші 2. Закон Стокса-Ломеля 3. Правило Левшина ( дзеркальна симетрія) 4. Закон Вавілова 5. Закон затухання люмінесценції 6. Залежність інтенсивності люмінесценції від концентрації люмінофора
 Спектр люмінесценції не залежить від довжини хвилі світла збудження.
Спектр люмінесценції не залежить від довжини хвилі світла збудження.
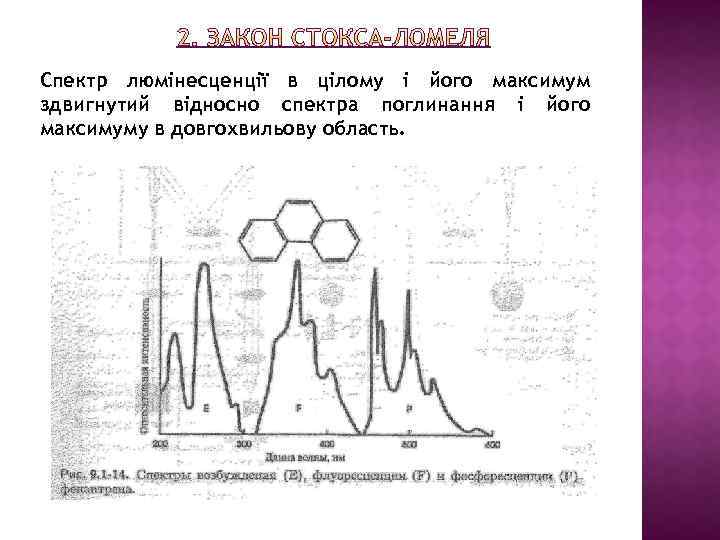 Спектр люмінесценції в цілому і його максимум здвигнутий відносно спектра поглинання і його максимуму в довгохвильову область.
Спектр люмінесценції в цілому і його максимум здвигнутий відносно спектра поглинання і його максимуму в довгохвильову область.
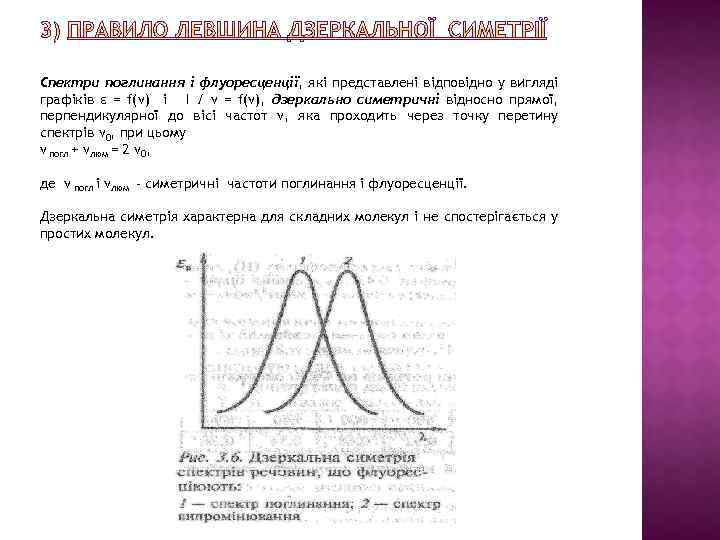 Спектри поглинання і флуоресценції, які представлені відповідно у вигляді графіків ε = f(ν) і I / ν = f(ν), дзеркально симетричні відносно прямої, перпендикулярної до вісі частот ν, яка проходить через точку перетину спектрів ν 0, при цьому ν погл + νлюм = 2 ν 0, де ν погл і νлюм - симетричні частоти поглинання і флуоресценції. Дзеркальна симетрія характерна для складних молекул і не спостерігається у простих молекул.
Спектри поглинання і флуоресценції, які представлені відповідно у вигляді графіків ε = f(ν) і I / ν = f(ν), дзеркально симетричні відносно прямої, перпендикулярної до вісі частот ν, яка проходить через точку перетину спектрів ν 0, при цьому ν погл + νлюм = 2 ν 0, де ν погл і νлюм - симетричні частоти поглинання і флуоресценції. Дзеркальна симетрія характерна для складних молекул і не спостерігається у простих молекул.
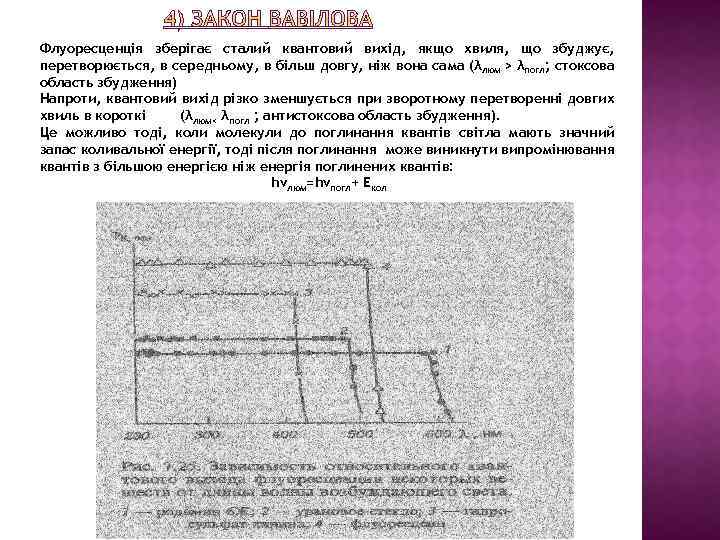 Флуоресценція зберігає сталий квантовий вихід, якщо хвиля, що збуджує, перетворюється, в середньому, в більш довгу, ніж вона сама (λлюм > λпогл; стоксова область збудження) Напроти, квантовий вихід різко зменшується при зворотному перетворенні довгих хвиль в короткі (λлюм< λпогл ; антистоксова область збудження). Це можливо тоді, коли молекули до поглинання квантів світла мають значний запас коливальної енергії, тоді після поглинання може виникнути випромінювання квантів з більшою енергією ніж енергія поглинених квантів: hνлюм=hνпогл+ Екол
Флуоресценція зберігає сталий квантовий вихід, якщо хвиля, що збуджує, перетворюється, в середньому, в більш довгу, ніж вона сама (λлюм > λпогл; стоксова область збудження) Напроти, квантовий вихід різко зменшується при зворотному перетворенні довгих хвиль в короткі (λлюм< λпогл ; антистоксова область збудження). Це можливо тоді, коли молекули до поглинання квантів світла мають значний запас коливальної енергії, тоді після поглинання може виникнути випромінювання квантів з більшою енергією ніж енергія поглинених квантів: hνлюм=hνпогл+ Екол
 Після припинення збудження інтенсивність флуоресценції спадає з часом за експоненціальним законом: It = I 0 e-t/τ, де І0 – інтенсивність світіння в момент припинення збудження люмінесценції; It – інтенсивність світіння в момент часу t; Τ– тривалість люмінесценції, або середній час життя, або середня тривалість збудженого стану.
Після припинення збудження інтенсивність флуоресценції спадає з часом за експоненціальним законом: It = I 0 e-t/τ, де І0 – інтенсивність світіння в момент припинення збудження люмінесценції; It – інтенсивність світіння в момент часу t; Τ– тривалість люмінесценції, або середній час життя, або середня тривалість збудженого стану.
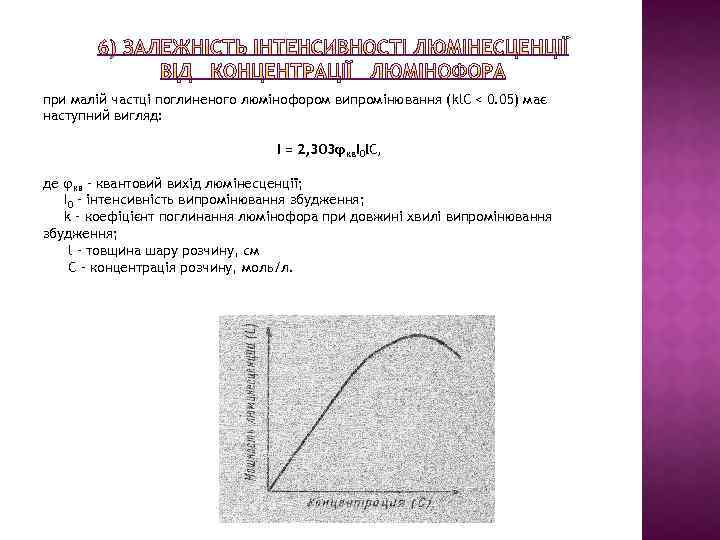 при малій частці поглиненого люмінофором випромінювання (kl. C < 0. 05) має наступний вигляд: І = 2, 303φквІ0 l. С, де φкв – квантовий вихід люмінесценції; І0 – інтенсивність випромінювання збудження; k – коефіцієнт поглинання люмінофора при довжині хвилі випромінювання збудження; l – товщина шару розчину, см C – концентрація розчину, моль/л.
при малій частці поглиненого люмінофором випромінювання (kl. C < 0. 05) має наступний вигляд: І = 2, 303φквІ0 l. С, де φкв – квантовий вихід люмінесценції; І0 – інтенсивність випромінювання збудження; k – коефіцієнт поглинання люмінофора при довжині хвилі випромінювання збудження; l – товщина шару розчину, см C – концентрація розчину, моль/л.
 концентраційне гасіння температурне гасіння домішками
концентраційне гасіння температурне гасіння домішками

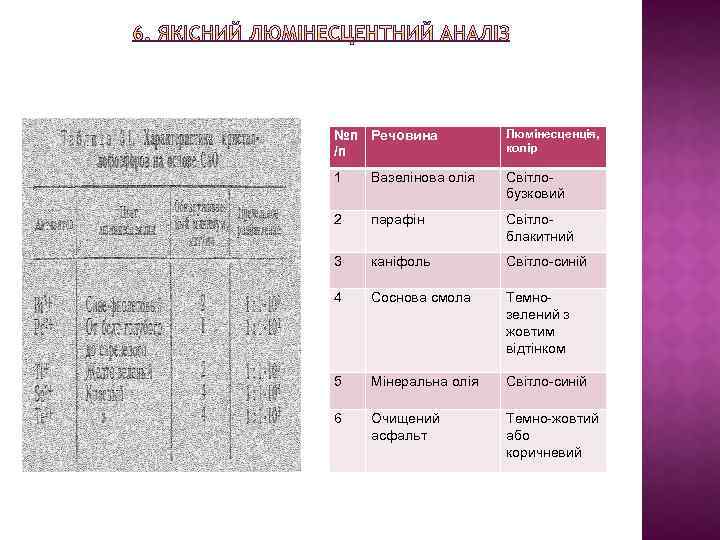 №п Речовина /п Люмінесценція, колір 1 Вазелінова олія Світлобузковий 2 парафін Світлоблакитний 3 каніфоль Світло-синій 4 Соснова смола Темнозелений з жовтим відтінком 5 Мінеральна олія Світло-синій 6 Очищений асфальт Темно-жовтий або коричневий
№п Речовина /п Люмінесценція, колір 1 Вазелінова олія Світлобузковий 2 парафін Світлоблакитний 3 каніфоль Світло-синій 4 Соснова смола Темнозелений з жовтим відтінком 5 Мінеральна олія Світло-синій 6 Очищений асфальт Темно-жовтий або коричневий

 Біологіїя та медицина, охорона навколишнього середовища Оптико-механічна промисловість Паперова промисловість Алмазо добувна промисловість Археологія Криміналістика, судмедекспертиза Географія
Біологіїя та медицина, охорона навколишнього середовища Оптико-механічна промисловість Паперова промисловість Алмазо добувна промисловість Археологія Криміналістика, судмедекспертиза Географія
 Метод високочутливий Потребує використання реагентів та посуду дуже високої чистоти, бідистильовану воду для приготування розчинів. Нижня межа визначення 10 -8 М або 0, 001 мкг/мл Верхня межа визначення 10 -3– 10 -4 М Широкий спектр використання Похибка методу 5 -7% Титрування мутних та забарвлених розчинів з люмінесцентними індикаторами. Визначення суміші флуоресцентних речовин.
Метод високочутливий Потребує використання реагентів та посуду дуже високої чистоти, бідистильовану воду для приготування розчинів. Нижня межа визначення 10 -8 М або 0, 001 мкг/мл Верхня межа визначення 10 -3– 10 -4 М Широкий спектр використання Похибка методу 5 -7% Титрування мутних та забарвлених розчинів з люмінесцентними індикаторами. Визначення суміші флуоресцентних речовин.


