Галогены.ppt
- Количество слайдов: 47


План. 1. Общая характеристика. А) Положение в Периодической системе химических элементов Д. И. Менделеева Б) Строение атома В) Валентности и степени окисления Г) Изменение свойств элементов с ростом порядкового номера 2. Нахождение в природе. 3. Физические свойства. 4. Химические свойства. 5. Получение в промышленности и в лаборатории. 6. Галогеноводороды. 7. Галогениды металлов. 8. Кислородные соединения галогенов.

Положение в системе. Галогены (солероды) – фтор F, хлор Cl, бром Br, йод I и астат At расположены в главной подгруппе VII группы периодической системы элементов Д. И. Менделеева. Все галогены, кроме астата, встречаются в природе. Молекулы простых веществ-галогенов при обычных условиях имеют состав Наl 2, т. е. F 2, Cl 2, Br 2, I 2. Все галогены имеют характерный запах и ядовиты.

Строение атома. Галогены относятся к p – элементам, так как в их атомах электронами заполняется р – подуровень внешнего электронного слоя. Строение внешнего электронного слоя атомов галогенов: F 1 s 22 p 5 Cl 1 s 22 p 63 s 23 p 5 Br 1 s 22 s 23 p 63 d 104 s 24 p 5 I 1 s 22 s 23 p 63 d 104 s 24 p 64 d 105 s 25 p 5

Валентности и степени окисления. Так как у атомов галогенов на внешнем электронном слое имеется один неспаренный электрон, для них характерна валентность I. Степени окисления: F: -1 Сl, Br, I : -1, +3, +5, +7.

Валентные состояния атомов галогенов

Ионы галогенов восстановители(кроме F-1) Cl-1 Br-1 I-1 Восстановительная способность галогенидионов увеличивается

Изменение свойств элементов с ростом порядкового номера F Cl Br I Увеличивается: Уменьшается: • число электронных оболочек в атоме, • радиус атома. • прочность связи электронов внешнего слоя с ядром, • сродство к электрону, • энергия ионизации , • электроотрицательность, • неметаллические свойства, • окислительные свойства.

Галогены – типичные неметаллы При протекании химических реакций они легко присоединяют один недостающий до октета электрон и проявляют окислительные свойства. Ионы галогенов (кроме F-) способны отдавать электроны, поэтому они являются восстановителями. Восстановительная способность увеличивается от хлорид-иона к йодид-иону:
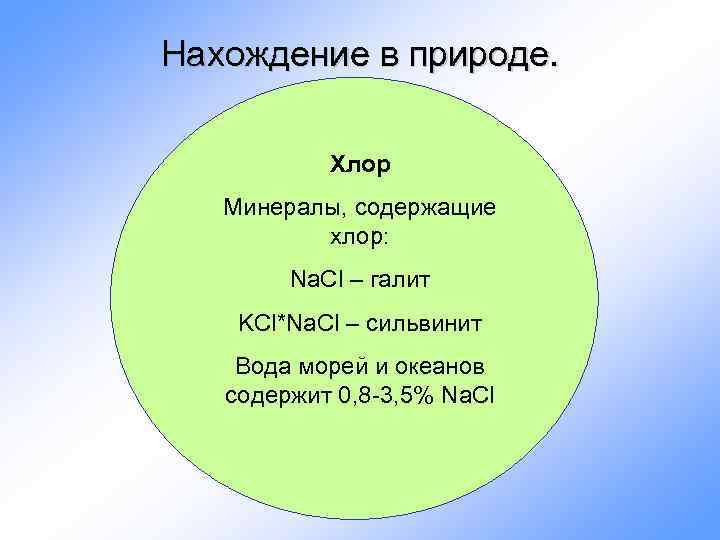
Нахождение в природе. Хлор Минералы, содержащие хлор: Na. Cl – галит KCl*Na. Cl – сильвинит Вода морей и океанов содержит 0, 8 -3, 5% Na. Cl
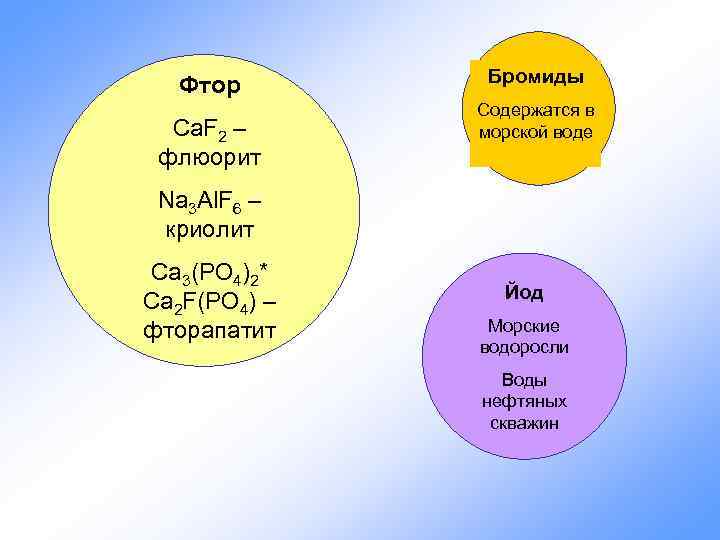
Фтор Ca. F 2 – флюорит Бромиды Содержатся в морской воде Na 3 Al. F 6 – криолит Ca 3(PO 4)2* Ca 2 F(PO 4) – фторапатит Йод Морские водоросли Воды нефтяных скважин
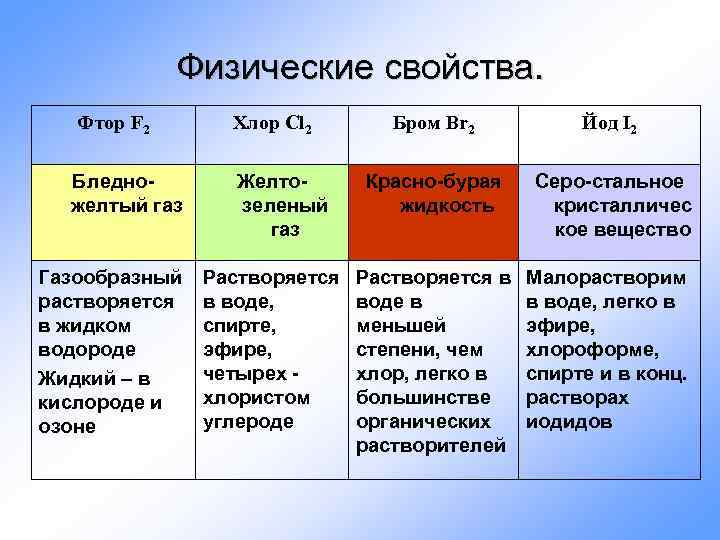
Физические свойства. Фтор F 2 Бледножелтый газ Газообразный растворяется в жидком водороде Жидкий – в кислороде и озоне Хлор Cl 2 Желтозеленый газ Растворяется в воде, спирте, эфире, четырех хлористом углероде Бром Br 2 Йод I 2 Красно-бурая жидкость Серо-стальное кристалличес кое вещество Растворяется в воде в меньшей степени, чем хлор, легко в большинстве органических растворителей Малорастворим в воде, легко в эфире, хлороформе, спирте и в конц. растворах иодидов

Галогены типичные неметаллы При протекании химических реакции они легко присоединяют один недостающий до октета электрон и проявляют окислительные свойства: Г 0+1ē = Г-1 Г 20+2ē=2 Г-1

Химические свойства. При взаимодействии с металлами образуют соли: 2 e 0 0 +1 -1 2 Na + Cl 2 = 2 Na. Cl 2 Fe + 3 Cl 2 = 2 Fe. Cl 3 2 Cu + Cl 2 = Cu. Cl 2

Взаимодействие с водородом: H 2 + F 2 = 2 HF в темноте, со взрывом H 2 + Cl 2 = 2 HCl на ярком солнечном свете, а также при нагревании H 2 + Br 2 = 2 HBr только при нагревании H 2 + I 2 2 HI не проходит до конца даже при сильном нагревании

Взаимодействие с некоторыми неметалами 3 Cl 20+2 P 0 = 2 P+3 Cl-13 Cl 20 +S 0 = S+2 Cl-12 С кислородом и азотом галогены непосредственно не взаимодействует.

• Взаимодействие галогенов со сложными веществами Cl 20+H 2 O HCl + HCl. O Затем происходит разложение хлорноватистой кислоты на свету: HCl. O = HCl +[O] атомарный кислород На холоду: Cl 20+2 Na. OH = Na. Cl + Na. Cl. O + H 2 O При нагревании: 3 Cl 20+6 KOH=5 KCl+KCl. O 3+3 H 2 O

Галогены проявляют окислительные свойства, которые понижаются от фтора к йоду. Фтор может быть только окислителем! 2 H 2 O + 2 F 2 = 4 HF + O 2 + Q Si. O 2 + 2 F 2 = Si. F 4 + O 2 + Q

Более активные галогены могут вытеснять менее активные из их соединений. 2 KCl + F 2 = 2 KF + Cl 2 2 KBr +Cl 2 = 2 KCl + Br 2 2 KI + Br 2 = 2 KBr + I 2

Качественная реакция на Cl- ион Na. Cl + Ag. NO 3 = Ag. Cl + Na. NO 3 Ag+ + Cl- = Ag. Cl + 2 NH 3*H 2 O = [Ag(NH 3)2]Cl + 2 H 2 O [Ag(NH 3)2]Cl + 2 HNO 3 = Ag. Cl + 2 NH 4 NO 3

- Качественная реакция на Br ион. Na. Br + Ag. NO 3 = Ag. Br + Na. NO 3 Ag+ + Br- = Ag. Br Качественная реакция на I- ион. Na. I + Ag. NO 3 = Ag. I + Na. NO 3 Ag+ - + I = Ag. I Качественная реакция на свободный йод. I 2 + крахмал темно-синее окрашивание

Получение. Фтор. Единственный возможный способ получения – электролиз фтористых соединений, где фторид-ион окисляется на аноде и выделяется в виде F 2: 2 F 2 e F 2 В настоящее время основным источником получения фтора является кислая соль KHF 2. Электролиз проводят в стальных электролизерах.

Хлор. В промышленности получают электролизом водного раствора или расплава хлорида натрия:

В лаборатории хлор можно получить действием концентрированной соляной кислоты (при нагревании) на различные окислители, такие как оксид марганца (IV) Mn. O 2, перманганат калия KMn. O 4, бертолетова соль KCl. O 3 и др.

Бром и Йод. В лабораторных условиях получают действием оксида марганца (IV) на бромиды и йодиды в кислой среде. Mn. O 2 + 2 KBr + 2 H 2 SO 4 = Mn. SO 4 + Br 2 + K 2 SO 4 + 2 H 2 O Mn. O 2 + 2 KI + 2 H 2 SO 4 = Mn. SO 4 + I 2 + K 2 SO 4 + 2 H 2 O

Сущность получения свободных галогенов из их природных соединений заключается в окислении соединений галогенов (отрицательно заряженных ионов галогенов) подходящими окислителями: 2 Э 2 е Э 2, где Э = F , Cl , Br , I

Галогеноводороды H+Hal- – соединения галогенов с водородом, где Hal – любой галоген. HF HCl HBr HI Ослабление связи между водородом и галогеном

Все галогеноводороды – бесцветные газы с резким запахом, легко растворяются в воде. При 0 С в 1 объеме воды растворяется 500 объемов HCl, 600 объемов HBr и 450 объемов HI. Фтороводород смешивается с водой в любых соотношениях.

Галогеноводородные кислоты. Формула Название кислоты Соли HF Плавиковая Фтороводородная Фториды HCl Соляная Хлороводородная Хлориды HBr Бромоводородная Бромиды HI Йодоводородная Йодиды


Галогеноводороды – газы. Фтороводород HF Как в лаборатории, так и в промышленности получают действием концентрированной серной кислоты на плавиковый шпат: Ca. F 2 + H 2 SO 4 = Ca. SO 4 + 2 HF

Хлороводород HCl – бесцветный газ с резким запахом, на воздухе при соприкосновении с парами воды образует капельки тумана ( «дымит» ). Получают: 1. Непосредственным взаимодействием водорода с хлором: H 2 + Cl 2 = 2 HCl Этот процесс осуществляется путем сжигания водорода в струе хлора.

2. Сульфатным способом. Реакция взаимодействия концентрированной серной кислоты с кристаллической поваренной солью. На холоду: Na. Cl + H 2 SO 4 = Na. HSO 4 + HCl При нагревании протекает вторая стадия реакции: Na. Cl + Na. HSO 4 = Na 2 SO 4 + HCl В медицинской практике находит применение разведенная соляная кислота, которая является составной частью желудочного сока (0, 5%).

Бромоводород HBr – бесцветный газ с резким запахом, «дымит» на воздухе. При соприкосновении с кислородом воздуха окисляется до свободного брома: 4 HBr + O 2 = 2 Br 2 + 2 H 2 O Йодоводород HI – бесцветный газ, «дымит» на воздухе. При соприкосновении с кислородом воздуха окисляется до свободного йода: 4 HI + O 2 = 2 I 2 + 2 H 2 O

Галогениды металлов. Натрия хлорид Natrii chloridum Основная функция натрия хлорида обеспечивать постоянство осмотического давления крови. При дефиците натрия хлорида в организме он вводится внутривенно или подкожно в виде 0, 9% водного раствора. Na. Cl применяют также для ванн, обтираний, полосканий при заболеваниях верхних дыхательных путей.

Калия хлорид Kalii chloridum Применяется при нарушениях сердечного ритма, особенно в связи с интоксикацией сердечными гликозидами, когда происходит обеднение клеток миокарда ионами калия. Калия хлорид применяется также в случае гипогликемии ( снижение концентрации ионов калия в организме). Калия хлорид назначают обычно внутрь в виде 10% водородного раствора или в составе препарата «Панангин» .

Кальция хлорид Calcii chloridum Применяется в медицине: 1. как кровоостанавливающее средство при легочных, желудочно – кишечных, носовых и маточных кровотечениях; 2. в хирургической практике для повышения свертываемости крови; 3. при аллергических заболеваниях ( бронхиальная астма, крапивница) для снятия зуда; 4. в качестве противоядия при отравлении солями магния.

Препарат назначается внутрь в виде 5 -10% раствора, внутривенно по 5 -10 мл 10% раствора. Выпускается в ампулах по 5 - 10 мл 10% раствора, а также в небольших хорошо закупоренных стеклянных банках с пробкой, залитой парафином, в сухом месте. Растворы кальция хлорида нельзя вводить подкожно и внутримышечно, так как в этом случае могут возникнуть некрозы.

Калия бромид. Kali bromidum Натрия бромид. Natrii bromidum Применение. Успокаивающее действие препаратов брома основано на их способности усиливать процессы торможения в коре большого мозга. Поэтому бромиды применяются при неврастении, повышенной раздражительности. Бромиды принимают внутрь в растворах(микстурах) и таблетках.

Натрия йодид Natrii iodidum Калия йодид Kali iodidum Представляют собой кристаллический порошок белого цвета. Применяют иодиды как носители йода при гипертиреозе, эндемическом зобе. Если пища или вода не содержит достаточного количества йода, как это бывает в некоторых горных местностях, то у местного населения возникает заболевание – кретинизм, или зобная болезнь. Назначают иодиды в виде растворов (микстур).

Кислородные соединения галогенов. Фторид кислорода OF 2. Это газ, который при температуре – 145 С превращается в жидкость желтого цвета, сильный окислитель. 2 F 2 + 2 Na. OH = 2 Na. F + H 2 O + OF 2

Кислородсодержащие кислоты хлора.

Кислоты являются более сильными окислителями, чем соответствующие им соли. Увеличение силы и устойчивости кислот HCl. O 2 HCl. O 3 HCl. O 4 Увеличение окислительной активности кислот

Большое практическое применение находит раствор хлора в водном растворе Ca(OH)2. Эта смесь называется хлорной известью. 2 Cl 2 + 2 Ca(OH)2 = Ca. Cl 2 + Ca(OCl)2 + 2 H 2 O Cl 2 + Ca(OH)2 = Ca. OCl 2 + H 2 O Ca(OCl)2 + CO 2 + H 2 O = Ca. CO 3 + 2 HCl. O Хлорная известь представляет собой порошок белого или сероватого цвета с запахом хлора. Ее широко применяют для дезинфекции помещений и различных источников распространения болезнетворных бактерий.

Большое практическое значение имеет также хлорат калия KCl. O 3, называемый бертолетовой солью, в честь французского химика К. Л. Бертолле. Бертолетова соль проявляет сильные окислительные свойства. 2 KCl. O 3 = 2 KCl + 3 O 2 4 KCl. O 3 = KCl + 3 KCl. O 4 (в присутствии Mn. O 2)

Бромноватистая кислота HBr. O. Слабая кислота, обладает окислительными свойствами. Соли этой кислоты – гипобромиты – существуют только в растворах, нестойки. Br 2 + 2 Na. OH = Na. Br. O + Na. Br + H 2 O (при обычной температуре) t 3 Br 2 + 6 KOH = KBr. O 3 + 5 KBr + 3 H 2 O (при кипячении)

Йодноватая кислота HIO 3 и Йодная кислота HIO 4 Соли – гипойодиты – образуются на холоду при действии щелочи на йод: I 2 + 2 KOH = KIO + KI + H 2 O I 2 + 2 Na. OH = Na. IO + Na. I + H 2 O Уже на холоду гипойодиты подвергаются диспропорционированию с образованием йодата и йодида: 3 KIO = KIO 3 + 2 KI
Галогены.ppt