Питтинговая коррозия Диагностические признаки:































Питтинговая коррозия.ppt
- Количество слайдов: 35
 Питтинговая коррозия Диагностические признаки: 1. Разрушение металла (сплава) сосредоточено в отдельных точках запассивированной поверхности 2. Материальный эффект коррозии (потери массы) практически полностью обусловлен растворением металла (сплава) в локальных участках поверхности (питтингах) 3. При слиянии нескольких точек (питтингов) и относительно небольшой их глубине наблюдается язвенная коррозия 4. При внешне незначительном поражении поверхности возможно возникновение сквозного питтинга (перфорация)
Питтинговая коррозия Диагностические признаки: 1. Разрушение металла (сплава) сосредоточено в отдельных точках запассивированной поверхности 2. Материальный эффект коррозии (потери массы) практически полностью обусловлен растворением металла (сплава) в локальных участках поверхности (питтингах) 3. При слиянии нескольких точек (питтингов) и относительно небольшой их глубине наблюдается язвенная коррозия 4. При внешне незначительном поражении поверхности возможно возникновение сквозного питтинга (перфорация)
 Основные термины и понятия Ø Потенциал питтингообразования Епит (потенциал пробоя, критический потенциал питтинговой коррозии, потенциал активирования) – минимальное значение потенциала, при котором возникает ПК. Признак достижения Епит: устойчивый рост плотности тока при Е > Епит Ø Потенциал репассивации Ереп (защитный потенциал Езащ) – потенциал прекращения работы питтингов, возникших при Е > Епит Потенциалы и области ПК на потенциодинамической кривой Ø Потенциал ингибирования Еинг – коррозионностойких сталей; потенциал (положительнее Епит), при котором подавляется ПК, возникшая при Екор1 и Екор2 – потенциалы Е > Епит (плотность тока возвращается к коррозии в кислых и плотности тока пассивного состояния). нейтральных средах ; Наблюдается в средах, содержащих эффективные ингибиторы ПК (нитрат- Епит – потенциал ионы) питтингообразования; Ереп – потенциал репассивации
Основные термины и понятия Ø Потенциал питтингообразования Епит (потенциал пробоя, критический потенциал питтинговой коррозии, потенциал активирования) – минимальное значение потенциала, при котором возникает ПК. Признак достижения Епит: устойчивый рост плотности тока при Е > Епит Ø Потенциал репассивации Ереп (защитный потенциал Езащ) – потенциал прекращения работы питтингов, возникших при Е > Епит Потенциалы и области ПК на потенциодинамической кривой Ø Потенциал ингибирования Еинг – коррозионностойких сталей; потенциал (положительнее Епит), при котором подавляется ПК, возникшая при Екор1 и Екор2 – потенциалы Е > Епит (плотность тока возвращается к коррозии в кислых и плотности тока пассивного состояния). нейтральных средах ; Наблюдается в средах, содержащих эффективные ингибиторы ПК (нитрат- Епит – потенциал ионы) питтингообразования; Ереп – потенциал репассивации
 Характерные виды питтингов а – открытый питтинг с защитным слоем на окружающей поверхности; б – закрытый , без окружающего защитного слоя; в – закрытый с окружающим защитным слоем. 1 – металл; 2 – раствор; 3 – защитный слой; 4 – пористые продукты коррозии и Поверхность образца стали отложения; 5 – крышка над питтингом; 12 Х 18 Н 10 Т, подвергнутая 6 – отверстия в крышке питтинговой коррозии в 10%- ном растворе Fe. Cl 3
Характерные виды питтингов а – открытый питтинг с защитным слоем на окружающей поверхности; б – закрытый , без окружающего защитного слоя; в – закрытый с окружающим защитным слоем. 1 – металл; 2 – раствор; 3 – защитный слой; 4 – пористые продукты коррозии и Поверхность образца стали отложения; 5 – крышка над питтингом; 12 Х 18 Н 10 Т, подвергнутая 6 – отверстия в крышке питтинговой коррозии в 10%- ном растворе Fe. Cl 3
 Основные термины и понятия Ø Критическая плотность тока в гальваностатическом режиме iкр – минимальная плотность тока заряжения, вызывающая ПК; Ø Активирующие анионы – анионы, вызывающие при определенных условиях ПК (анионы Cl, Br, I, CNS, Cl. O 4); Ø Критическая (минимальная) концентрация аниона- активатора Скр в конкретных условиях, ниже которой ПК не возникает; Ø Ингибиторы ПК – анионы, присутствие которых в среде вызывает подавление и предотвращение ПК: ØЗащитная концентрация ингибитора– минимальная концентрация, обеспечивающая предотвращение ПК;
Основные термины и понятия Ø Критическая плотность тока в гальваностатическом режиме iкр – минимальная плотность тока заряжения, вызывающая ПК; Ø Активирующие анионы – анионы, вызывающие при определенных условиях ПК (анионы Cl, Br, I, CNS, Cl. O 4); Ø Критическая (минимальная) концентрация аниона- активатора Скр в конкретных условиях, ниже которой ПК не возникает; Ø Ингибиторы ПК – анионы, присутствие которых в среде вызывает подавление и предотвращение ПК: ØЗащитная концентрация ингибитора– минимальная концентрация, обеспечивающая предотвращение ПК;
 Основные термины и понятия Ø Критическая температура питтингообразования (КТП) – температура, ниже которой ПК не проявляется; Ø Индукционный период (время) питтингообразования, tинд – временной интервал с момента обеспечения необходимых условий ПК до появления первого питтинга; Ø Коэффициент питтингообразования Кпит – отношение средней глубины всех питтингов к условной глубине коррозии, рассчитанной из потерь массы, при допущении, что коррозия носит равномерный характер; Ø Эквивалент питтингостойкости ПК (ЭСП) – сумма содержания в стали хрома, молибдена и азота с учетом их вклада в повышение стойкости против ПК; ЭСП= %Cr+3, 3(% Mo)+16(%N)
Основные термины и понятия Ø Критическая температура питтингообразования (КТП) – температура, ниже которой ПК не проявляется; Ø Индукционный период (время) питтингообразования, tинд – временной интервал с момента обеспечения необходимых условий ПК до появления первого питтинга; Ø Коэффициент питтингообразования Кпит – отношение средней глубины всех питтингов к условной глубине коррозии, рассчитанной из потерь массы, при допущении, что коррозия носит равномерный характер; Ø Эквивалент питтингостойкости ПК (ЭСП) – сумма содержания в стали хрома, молибдена и азота с учетом их вклада в повышение стойкости против ПК; ЭСП= %Cr+3, 3(% Mo)+16(%N)
 Условия возникновения и протекания ПК 1. Пассивирующая среда (нахождение металла в пассивном состоянии). 2. Наличие в растворе аниона-активатора в количестве, превышающем (минимальную) критическую концентрацию. 3. Наличие в растворе окислителя, способного сместить потенциал коррозии положительнее потенциала питтингообразования Епит (или за счет внешней анодной поляризации). 4. Электрический контакт с более благородными металлами и наличие зазоров и щелей повышают вероятность возникновения ПК: - контакт с благородным металлом может сместить потенциал коррозии до значений, превышающих Епит; - щель создает возможность накопления продуктов коррозии, повышает кислотность среды, затрудняет доступ пассиватора (кислорода), т. е. создают условия для понижения Епит
Условия возникновения и протекания ПК 1. Пассивирующая среда (нахождение металла в пассивном состоянии). 2. Наличие в растворе аниона-активатора в количестве, превышающем (минимальную) критическую концентрацию. 3. Наличие в растворе окислителя, способного сместить потенциал коррозии положительнее потенциала питтингообразования Епит (или за счет внешней анодной поляризации). 4. Электрический контакт с более благородными металлами и наличие зазоров и щелей повышают вероятность возникновения ПК: - контакт с благородным металлом может сместить потенциал коррозии до значений, превышающих Епит; - щель создает возможность накопления продуктов коррозии, повышает кислотность среды, затрудняет доступ пассиватора (кислорода), т. е. создают условия для понижения Епит
 Механизмы питтинговой коррозии Ø ПК – сложное явление, зависящее от внешних и внутренних факторов (в основном роли легирующих компонентов), а также стадийности возникновения и развития питтингов. Ø Стадии: 1. Процессы, вызывающие нарушение пассивности. Наблюдаются изменения в пассивной пленке, но питтинги еще не обнаруживаются (ни по величине тока, ни металлографически). 2. Начальный этап роста питтингов. Наблюдается непрерывный рост тока, появляются первые питтинги микрометрических размеров. 3. Поздний этап роста питтингов. Обнаруживается осаждение солевых пленок и большое падение потенциала. 4. Репассивация питтингов. Наступает (если она возможна) после стадии 2 и характеризуется возвратом к пассивному состоянию и токам пассивности; бывший питтинг становится подобным остальной части пассивной поверхности. 5. Стабильный рост питтинга
Механизмы питтинговой коррозии Ø ПК – сложное явление, зависящее от внешних и внутренних факторов (в основном роли легирующих компонентов), а также стадийности возникновения и развития питтингов. Ø Стадии: 1. Процессы, вызывающие нарушение пассивности. Наблюдаются изменения в пассивной пленке, но питтинги еще не обнаруживаются (ни по величине тока, ни металлографически). 2. Начальный этап роста питтингов. Наблюдается непрерывный рост тока, появляются первые питтинги микрометрических размеров. 3. Поздний этап роста питтингов. Обнаруживается осаждение солевых пленок и большое падение потенциала. 4. Репассивация питтингов. Наступает (если она возможна) после стадии 2 и характеризуется возвратом к пассивному состоянию и токам пассивности; бывший питтинг становится подобным остальной части пассивной поверхности. 5. Стабильный рост питтинга
 Механизмы питтинговой коррозии Все механизмы ПК предусматривают нарушение пассивности 1. Проникновение аниона Агрессивные анионы мигрируют через оксидную пленку к границе Ме. О/Ме под влиянием электрического поля напряженностью 2. Разрушение пленки происходит под влиянием электрострикции, вызванной адсорбцией хлорид-ионов. Механическое разрушение пассивной пленки приводит к обнажению поверхности, которая подвергается воздействию электролита Электростри кция — эффект изменения линейных размеров вещества приложении к нему электрического поля. 3. Адсорбция аниона на поверхности пассивирующего оксида Анионы образуют поверхностные комплексы с металлическими ионами. Облегчается переход ионов металла в электролит, толщина пассивной пленки уменьшается. Увеличивается напряженность электрического поля внутри оксидного слоя, что способствует увеличению скорости миграции металлических ионов. Растворение металла в общем виде идет по реакции: Далее гидролиз, вызывающий подкисление среды
Механизмы питтинговой коррозии Все механизмы ПК предусматривают нарушение пассивности 1. Проникновение аниона Агрессивные анионы мигрируют через оксидную пленку к границе Ме. О/Ме под влиянием электрического поля напряженностью 2. Разрушение пленки происходит под влиянием электрострикции, вызванной адсорбцией хлорид-ионов. Механическое разрушение пассивной пленки приводит к обнажению поверхности, которая подвергается воздействию электролита Электростри кция — эффект изменения линейных размеров вещества приложении к нему электрического поля. 3. Адсорбция аниона на поверхности пассивирующего оксида Анионы образуют поверхностные комплексы с металлическими ионами. Облегчается переход ионов металла в электролит, толщина пассивной пленки уменьшается. Увеличивается напряженность электрического поля внутри оксидного слоя, что способствует увеличению скорости миграции металлических ионов. Растворение металла в общем виде идет по реакции: Далее гидролиз, вызывающий подкисление среды
 Общая физическая картина развития питтинга Развитие питтинга характеризуется тремя последовательными стадиями Ø Обезвоживание. Смешанные адсорбированные комплексы в растворе диссоциируют, ионы хлора регенерируют и снова принимают участие в процессе. Молекулы воды, участвующие в элементарных актах растворения, вытесняются ионными компонентами, концентрация которых быстро растет. Молекулы воды расходуются также на гидратацию ионов металла и непрерывно отводятся на периферию в составе гидратных оболочек. Возникает дефицит воды. Ø Образование резистивного слоя. Из-за отсутствия воды в составе раствора около поверхности дна питтинга возникает состояние раствора (полная сольватация), характеризующееся присутствием только гидратированных ионов металла и противоионов (хлорид-ионов), практически лишенных гидратных оболочек. Ø Стабилизация роста. После достижения критического размера питтинга рост с внешней стороны прекращается и начинается стабилизационная стадия – продвижение слоя вглубь вслед за растворяющейся поверхностью металла в питтинге, а внешняя граница остается неизменной.
Общая физическая картина развития питтинга Развитие питтинга характеризуется тремя последовательными стадиями Ø Обезвоживание. Смешанные адсорбированные комплексы в растворе диссоциируют, ионы хлора регенерируют и снова принимают участие в процессе. Молекулы воды, участвующие в элементарных актах растворения, вытесняются ионными компонентами, концентрация которых быстро растет. Молекулы воды расходуются также на гидратацию ионов металла и непрерывно отводятся на периферию в составе гидратных оболочек. Возникает дефицит воды. Ø Образование резистивного слоя. Из-за отсутствия воды в составе раствора около поверхности дна питтинга возникает состояние раствора (полная сольватация), характеризующееся присутствием только гидратированных ионов металла и противоионов (хлорид-ионов), практически лишенных гидратных оболочек. Ø Стабилизация роста. После достижения критического размера питтинга рост с внешней стороны прекращается и начинается стабилизационная стадия – продвижение слоя вглубь вслед за растворяющейся поверхностью металла в питтинге, а внешняя граница остается неизменной.
 Питтинговая коррозия – вероятностный процесс Основания: 1. Плохая воспроизводимость результатов при определении Епит и tинд. 2. Появление питтингов происходит случайно во времени и пространстве с определенной частотой. 3. Предпочтительные места зарождения питтингов на поверхности металла – выделения, неметаллические включения, сегрегации примесей, шероховатости поверхности (в пределах этого множества процесс носит случай характер).
Питтинговая коррозия – вероятностный процесс Основания: 1. Плохая воспроизводимость результатов при определении Епит и tинд. 2. Появление питтингов происходит случайно во времени и пространстве с определенной частотой. 3. Предпочтительные места зарождения питтингов на поверхности металла – выделения, неметаллические включения, сегрегации примесей, шероховатости поверхности (в пределах этого множества процесс носит случай характер).
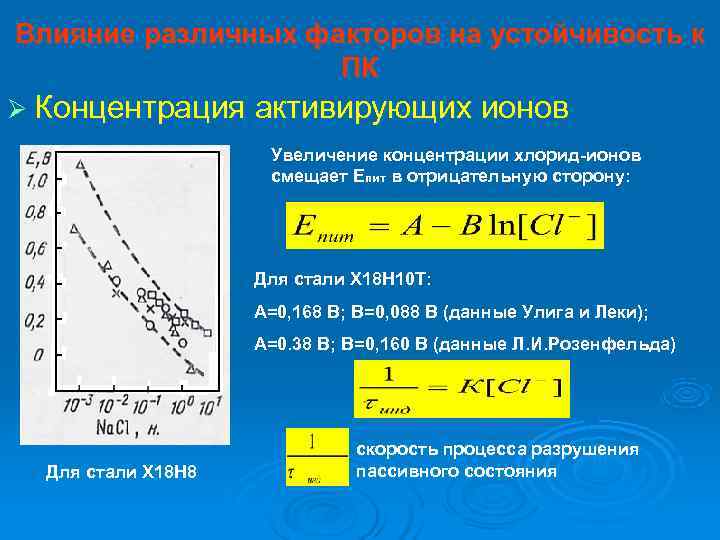
 Влияние различных факторов на устойчивость к ПК Ø Концентрация активирующих ионов Увеличение концентрации хлорид-ионов смещает Епит в отрицательную сторону: Для стали Х 18 Н 10 Т: А=0, 168 В; В=0, 088 В (данные Улига и Леки); А=0. 38 В; В=0, 160 В (данные Л. И. Розенфельда) скорость процесса разрушения Для стали Х 18 Н 8 пассивного состояния
Влияние различных факторов на устойчивость к ПК Ø Концентрация активирующих ионов Увеличение концентрации хлорид-ионов смещает Епит в отрицательную сторону: Для стали Х 18 Н 10 Т: А=0, 168 В; В=0, 088 В (данные Улига и Леки); А=0. 38 В; В=0, 160 В (данные Л. И. Розенфельда) скорость процесса разрушения Для стали Х 18 Н 8 пассивного состояния
 Влияние р. Н Повышение р. Н незначительно влияет на Епит - максимальное смещение Епит в положительную сторону на единицу р. Н составляет 10 м. В (в интервале р. Н 1, 6… 11). Для стали Х 18 Н 10 Т при р. Н 1… 5 Епит=0, 40+0, 030 р. Н. Сильно щелочные растворы оказывают более значительное влияние на Епит
Влияние р. Н Повышение р. Н незначительно влияет на Епит - максимальное смещение Епит в положительную сторону на единицу р. Н составляет 10 м. В (в интервале р. Н 1, 6… 11). Для стали Х 18 Н 10 Т при р. Н 1… 5 Епит=0, 40+0, 030 р. Н. Сильно щелочные растворы оказывают более значительное влияние на Епит
 Присутствие анионов Анионы среды могут оказывать ингибирующее действие на развитие ПК Ингибирующая способность убывает в ряду: Нитрат-ион не только увеличивает Епит, но подавляет ПК при потенциалах, больших, чем Епит Ингибирующим эффектом обладают хроматы, бихроматы, молибдаты Ингибирующее действие анионов вызвано конкурирующей адсорбцией их на поверхности металла, обеспечивающей вытеснение агрессивных галогенид- ионов, или образованием оксида при анодной поляризации
Присутствие анионов Анионы среды могут оказывать ингибирующее действие на развитие ПК Ингибирующая способность убывает в ряду: Нитрат-ион не только увеличивает Епит, но подавляет ПК при потенциалах, больших, чем Епит Ингибирующим эффектом обладают хроматы, бихроматы, молибдаты Ингибирующее действие анионов вызвано конкурирующей адсорбцией их на поверхности металла, обеспечивающей вытеснение агрессивных галогенид- ионов, или образованием оксида при анодной поляризации
 Влияние химического состава стали на устойчивость к ПК Ø Хром Не склонен к ПК в водных растворах, содержащих галогенид-ионы. Склонность к ПК появляется при низком содержании воды в электролите. Сильно выраженное положительное влияние хрома на сопротивляемость против ПК обусловлено его высокой стойкостью против активирования хлорид-ионами. При легировании стали 30 -35 % и более хрома сталь становится устойчивой в растворах хлоридов любой концентрации.
Влияние химического состава стали на устойчивость к ПК Ø Хром Не склонен к ПК в водных растворах, содержащих галогенид-ионы. Склонность к ПК появляется при низком содержании воды в электролите. Сильно выраженное положительное влияние хрома на сопротивляемость против ПК обусловлено его высокой стойкостью против активирования хлорид-ионами. При легировании стали 30 -35 % и более хрома сталь становится устойчивой в растворах хлоридов любой концентрации.
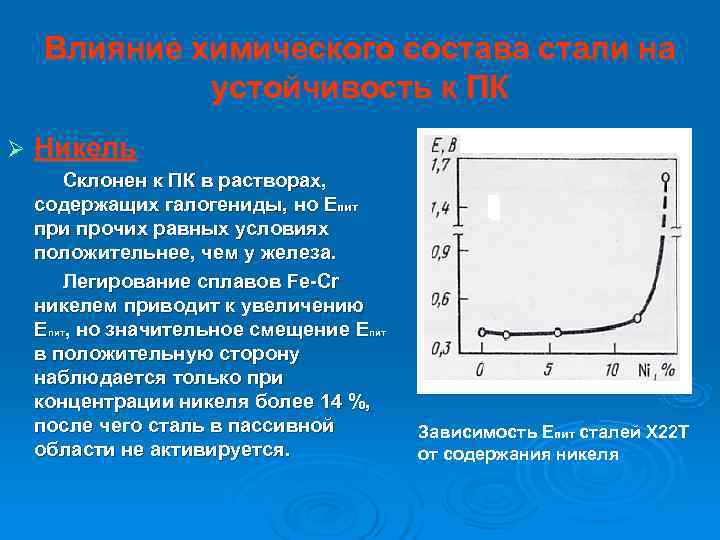
 Влияние химического состава стали на устойчивость к ПК Ø Никель Склонен к ПК в растворах, содержащих галогениды, но Епит при прочих равных условиях положительнее, чем у железа. Легирование сплавов Fe-Cr никелем приводит к увеличению Епит, но значительное смещение Епит в положительную сторону наблюдается только при концентрации никеля более 14 %, после чего сталь в пассивной Зависимость Епит сталей Х 22 Т области не активируется. от содержания никеля
Влияние химического состава стали на устойчивость к ПК Ø Никель Склонен к ПК в растворах, содержащих галогениды, но Епит при прочих равных условиях положительнее, чем у железа. Легирование сплавов Fe-Cr никелем приводит к увеличению Епит, но значительное смещение Епит в положительную сторону наблюдается только при концентрации никеля более 14 %, после чего сталь в пассивной Зависимость Епит сталей Х 22 Т области не активируется. от содержания никеля
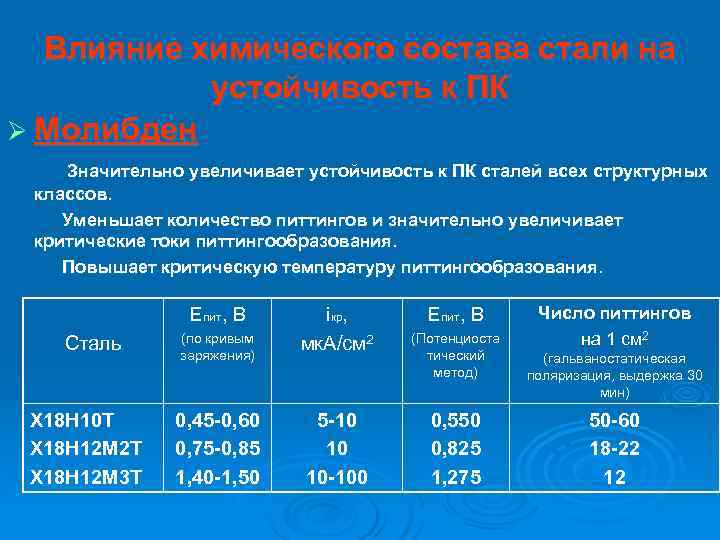
 Влияние химического состава стали на устойчивость к ПК Ø Молибден Значительно увеличивает устойчивость к ПК сталей всех структурных классов. Уменьшает количество питтингов и значительно увеличивает критические токи питтингообразования. Повышает критическую температуру питтингообразования. Епит, В iкр, Епит, В Число питтингов Сталь (по кривым мк. А/см 2 (Потенциоста на 1 см 2 заряжения) тический (гальваностатическая метод) поляризация, выдержка 30 мин) Х 18 Н 10 Т 0, 45 -0, 60 5 -10 0, 550 50 -60 Х 18 Н 12 М 2 Т 0, 75 -0, 85 10 0, 825 18 -22 Х 18 Н 12 М 3 Т 1, 40 -1, 50 10 -100 1, 275 12
Влияние химического состава стали на устойчивость к ПК Ø Молибден Значительно увеличивает устойчивость к ПК сталей всех структурных классов. Уменьшает количество питтингов и значительно увеличивает критические токи питтингообразования. Повышает критическую температуру питтингообразования. Епит, В iкр, Епит, В Число питтингов Сталь (по кривым мк. А/см 2 (Потенциоста на 1 см 2 заряжения) тический (гальваностатическая метод) поляризация, выдержка 30 мин) Х 18 Н 10 Т 0, 45 -0, 60 5 -10 0, 550 50 -60 Х 18 Н 12 М 2 Т 0, 75 -0, 85 10 0, 825 18 -22 Х 18 Н 12 М 3 Т 1, 40 -1, 50 10 -100 1, 275 12
 Влияние химического состава стали на устойчивость к ПК Ø Кремний Повышает стойкость против ПК, особенно при одновременном легировании молибденом. При высоком содержании кремния (4 -6%) возможно проявление двойственной роли кремния – положительной, в результате легирования твердого раствора, и отрицательной – при образовании неметаллических включений (НВ), содержащих Si. O 2, не устойчивых при высоких температурах среды и высоких концентрациях хлоридов. Образование питтингов происходит около включений Si. O 2 Пример: При температурах выше 55 С активация кремнийсодержащей стали 03 Х 17 Н 14 С 4 происходит при значительно более отрицательных значениях (Епит), чем стали 03 Х 17 Н 14 без кремния.
Влияние химического состава стали на устойчивость к ПК Ø Кремний Повышает стойкость против ПК, особенно при одновременном легировании молибденом. При высоком содержании кремния (4 -6%) возможно проявление двойственной роли кремния – положительной, в результате легирования твердого раствора, и отрицательной – при образовании неметаллических включений (НВ), содержащих Si. O 2, не устойчивых при высоких температурах среды и высоких концентрациях хлоридов. Образование питтингов происходит около включений Si. O 2 Пример: При температурах выше 55 С активация кремнийсодержащей стали 03 Х 17 Н 14 С 4 происходит при значительно более отрицательных значениях (Епит), чем стали 03 Х 17 Н 14 без кремния.
 Влияние химического состава стали на устойчивость к ПК Ø Марганец Легирование марганцем на устойчивость к ПК рассматривается совместно с его способностью к изменению структуры стали (аустенитообразованию). В структуре стали могут присутствовать аустенит, феррит, мартенсит. Легирование марганцем (6 %) хромоникелевых сталей с низким содержанием никеля (Х 18 Н 6) обеспечивает переход от мартенситной к аустенитной структуре. При этом Епит резко уменьшается и при дальнейшем увеличении содержания марганца (до 10 -15%) практически не меняется. В аустенитных сталях (типа Х 18 Н 10) резкое ухудшение стойкости против ПК наблюдается уже при содержании марганца 0, 4 -0, 6%, после чего наблюдается не столь резкое снижение стойкости. Резкое ослабление стойкости против ПК обусловлено образованием марганцесодержащих сульфидов. Дальнейший рост содержания марганца влияет на ослабление стойкости к ПК уже за счет роли марганца как легирующего элемента, входящего в состав твердого раствора. Меняются и свойства самих сульфидов, в которых увеличивается содержание марганца. Вредное влияние марганца на устойчивость к ПК преодолевается добавками молибдена и азота.
Влияние химического состава стали на устойчивость к ПК Ø Марганец Легирование марганцем на устойчивость к ПК рассматривается совместно с его способностью к изменению структуры стали (аустенитообразованию). В структуре стали могут присутствовать аустенит, феррит, мартенсит. Легирование марганцем (6 %) хромоникелевых сталей с низким содержанием никеля (Х 18 Н 6) обеспечивает переход от мартенситной к аустенитной структуре. При этом Епит резко уменьшается и при дальнейшем увеличении содержания марганца (до 10 -15%) практически не меняется. В аустенитных сталях (типа Х 18 Н 10) резкое ухудшение стойкости против ПК наблюдается уже при содержании марганца 0, 4 -0, 6%, после чего наблюдается не столь резкое снижение стойкости. Резкое ослабление стойкости против ПК обусловлено образованием марганцесодержащих сульфидов. Дальнейший рост содержания марганца влияет на ослабление стойкости к ПК уже за счет роли марганца как легирующего элемента, входящего в состав твердого раствора. Меняются и свойства самих сульфидов, в которых увеличивается содержание марганца. Вредное влияние марганца на устойчивость к ПК преодолевается добавками молибдена и азота.
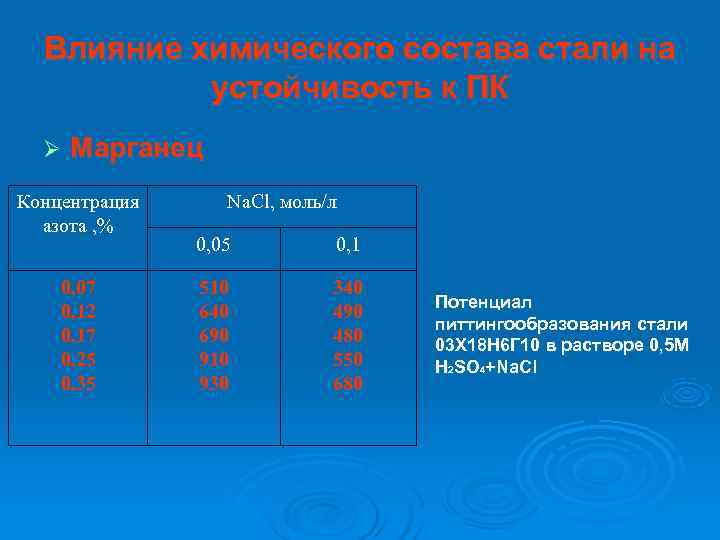
 Влияние химического состава стали на устойчивость к ПК Ø Марганец Концентрация Na. Cl, моль/л азота , % 0, 05 0, 1 0, 07 510 340 Потенциал 0, 12 640 490 питтингообразования стали 0, 17 690 480 03 Х 18 Н 6 Г 10 в растворе 0, 5 М 0, 25 910 550 H 2 SO 4+Na. Cl 0, 35 930 680
Влияние химического состава стали на устойчивость к ПК Ø Марганец Концентрация Na. Cl, моль/л азота , % 0, 05 0, 1 0, 07 510 340 Потенциал 0, 12 640 490 питтингообразования стали 0, 17 690 480 03 Х 18 Н 6 Г 10 в растворе 0, 5 М 0, 25 910 550 H 2 SO 4+Na. Cl 0, 35 930 680
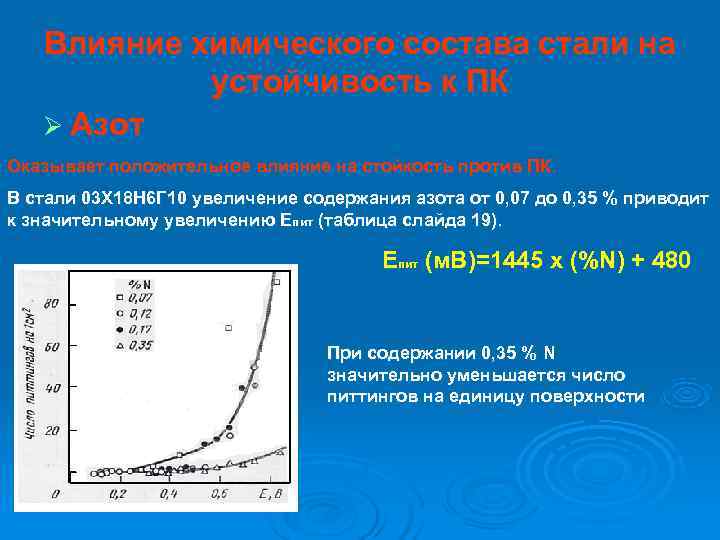
 Влияние химического состава стали на устойчивость к ПК Ø Азот Оказывает положительное влияние на стойкость против ПК. В стали 03 Х 18 Н 6 Г 10 увеличение содержания азота от 0, 07 до 0, 35 % приводит к значительному увеличению Епит (таблица слайда 19). Епит (м. В)=1445 х (%N) + 480 При содержании 0, 35 % N значительно уменьшается число питтингов на единицу поверхности
Влияние химического состава стали на устойчивость к ПК Ø Азот Оказывает положительное влияние на стойкость против ПК. В стали 03 Х 18 Н 6 Г 10 увеличение содержания азота от 0, 07 до 0, 35 % приводит к значительному увеличению Епит (таблица слайда 19). Епит (м. В)=1445 х (%N) + 480 При содержании 0, 35 % N значительно уменьшается число питтингов на единицу поверхности
 Влияние химического состава стали на устойчивость к ПК Ø Азот Механизм действия азота: 1. Азот образует нитрат-ион, который действует как ингибитор ПК 2. Азот увеличивает р. Н среды в приэлектродном пространстве в результате возникновения ионов аммония, как продукта разложения нитридов хрома
Влияние химического состава стали на устойчивость к ПК Ø Азот Механизм действия азота: 1. Азот образует нитрат-ион, который действует как ингибитор ПК 2. Азот увеличивает р. Н среды в приэлектродном пространстве в результате возникновения ионов аммония, как продукта разложения нитридов хрома
 Влияние химического состава стали на устойчивость к ПК Ø Углерод Увеличивает склонность к ПК как при нахождении в состоянии твердого раствора (после закалки стали) , так и в состоянии карбидов или карбонитридов – первичных (Тi. CN, Nb. CN) и вторичных (выделившихся при отпуске). Причина высокого сопротивления к ПК ферритных сталей (суперферритов) – низкое содержание углерода (0, 001 -0, 002 %).
Влияние химического состава стали на устойчивость к ПК Ø Углерод Увеличивает склонность к ПК как при нахождении в состоянии твердого раствора (после закалки стали) , так и в состоянии карбидов или карбонитридов – первичных (Тi. CN, Nb. CN) и вторичных (выделившихся при отпуске). Причина высокого сопротивления к ПК ферритных сталей (суперферритов) – низкое содержание углерода (0, 001 -0, 002 %).
 Влияние химического состава стали на устойчивость к ПК Ø Ниобий, титан, цирконий, тантал – снижают стойкость против ПК. Причина – увеличение степени гетерогенности структуры из-за высокой склонности к образованию карбидов и карбонитридов. Наиболее сильно отрицательная роль титана проявляется в кислых средах с достаточно высоким окислительно- восстановительным потенциалом из-за анодного окисления карбида титана Ø Церий – понижает стойкость против ПК в результате появления в стали неметаллических включений (химически нестойких оксидов) Ø Ванадий – увеличивает стойкость к ПК. Причина: препятствует зарождению питтинга, находясь в составе пассивной пленки, и повышает склонность к репассивации
Влияние химического состава стали на устойчивость к ПК Ø Ниобий, титан, цирконий, тантал – снижают стойкость против ПК. Причина – увеличение степени гетерогенности структуры из-за высокой склонности к образованию карбидов и карбонитридов. Наиболее сильно отрицательная роль титана проявляется в кислых средах с достаточно высоким окислительно- восстановительным потенциалом из-за анодного окисления карбида титана Ø Церий – понижает стойкость против ПК в результате появления в стали неметаллических включений (химически нестойких оксидов) Ø Ванадий – увеличивает стойкость к ПК. Причина: препятствует зарождению питтинга, находясь в составе пассивной пленки, и повышает склонность к репассивации
 Влияние химического состава стали на устойчивость к ПК Ø Сера и фосфор Сера ухудшает стойкость к ПК по причине низкой растворимости и склонности к образованию неметаллических включений (сульфидов Mn. S, Fe. S, окси- и карбосульфидов). Распределение серы между марганцем, железом и хромом в простых и сложных сульфидах зависит от содержания марганца в стали. Отсутствие серы в стали, исключающее образование сульфидов, не устраняет возможности возникновения питтингов, связанных с другими факторами, в частности из-за наличия неметаллических включений на основе оксидов, нитридов и т. д. Фосфор не влияет на стойкость к ПК. Однако склонность фосфора к сегрегации на границах зерен способствует повышению дефектности границ и увеличению вероятности зарождения питтинга.
Влияние химического состава стали на устойчивость к ПК Ø Сера и фосфор Сера ухудшает стойкость к ПК по причине низкой растворимости и склонности к образованию неметаллических включений (сульфидов Mn. S, Fe. S, окси- и карбосульфидов). Распределение серы между марганцем, железом и хромом в простых и сложных сульфидах зависит от содержания марганца в стали. Отсутствие серы в стали, исключающее образование сульфидов, не устраняет возможности возникновения питтингов, связанных с другими факторами, в частности из-за наличия неметаллических включений на основе оксидов, нитридов и т. д. Фосфор не влияет на стойкость к ПК. Однако склонность фосфора к сегрегации на границах зерен способствует повышению дефектности границ и увеличению вероятности зарождения питтинга.
 Влияние структурного состояния стали на устойчивость к ПК Ø Резко выраженного влияния структурного фактора на устойчивость к ПК не установлено Ø Считается, что аустенитная структура несколько более стойка к ПК, чем другие. Наличие в структуре аустенитной стали феррита (после термообработки) и мартенсита (при деформации) снижает Епит на 60 -90 м. В. Но причина снижения к стойкости к ПК связана не с наличием феррита как фазы, а локальным изменением химического состава аустенита. Поэтому питтингообразование проявляется предпочтительно на межфазной границе «аустенит- феррит» Ø Различие в устойчивости к ПК аустенитной и ферритной структуры связано различными свойствами граней ГЦК и ОЦК решеток. ОЦК: грань {100} более устойчива, чем грань {111} ГЦК: грань {111} растворяется с большей скоростью, чем {100} и {110}
Влияние структурного состояния стали на устойчивость к ПК Ø Резко выраженного влияния структурного фактора на устойчивость к ПК не установлено Ø Считается, что аустенитная структура несколько более стойка к ПК, чем другие. Наличие в структуре аустенитной стали феррита (после термообработки) и мартенсита (при деформации) снижает Епит на 60 -90 м. В. Но причина снижения к стойкости к ПК связана не с наличием феррита как фазы, а локальным изменением химического состава аустенита. Поэтому питтингообразование проявляется предпочтительно на межфазной границе «аустенит- феррит» Ø Различие в устойчивости к ПК аустенитной и ферритной структуры связано различными свойствами граней ГЦК и ОЦК решеток. ОЦК: грань {100} более устойчива, чем грань {111} ГЦК: грань {111} растворяется с большей скоростью, чем {100} и {110}
 Влияние структурного состояния стали на устойчивость к ПК Ø Термическая обработка (ТО) влияет на изменение устойчивости к ПК, повышая или уменьшая гетерогенность структруры Ø Полностью гомогенная структура – наиболее стойка к ПК (даже при наличии неметаллических включений) Ø ТО, вызывающая появление в структуре других фаз ухудшает стойкость к ПК, прежде всего по причине возникновения участков, обедненных Cr и Mo. Пониженное содержание Cr и Mo по границам зерен вызывает питтинг даже в отсутствие склонности к МКК. Влияние термической обработки на склонность к ПК стали 12 Х 18 Н 9 Т в хлоридсодержащем электролите: 1 – средняя глубина питтингов; 2 – число питтингов на 1 дм 2 Ø Области склонности МКК и ПК не совпадают: при низких температурах отпуска ПК возникает задолго до наступления склонности к МКК
Влияние структурного состояния стали на устойчивость к ПК Ø Термическая обработка (ТО) влияет на изменение устойчивости к ПК, повышая или уменьшая гетерогенность структруры Ø Полностью гомогенная структура – наиболее стойка к ПК (даже при наличии неметаллических включений) Ø ТО, вызывающая появление в структуре других фаз ухудшает стойкость к ПК, прежде всего по причине возникновения участков, обедненных Cr и Mo. Пониженное содержание Cr и Mo по границам зерен вызывает питтинг даже в отсутствие склонности к МКК. Влияние термической обработки на склонность к ПК стали 12 Х 18 Н 9 Т в хлоридсодержащем электролите: 1 – средняя глубина питтингов; 2 – число питтингов на 1 дм 2 Ø Области склонности МКК и ПК не совпадают: при низких температурах отпуска ПК возникает задолго до наступления склонности к МКК
 Влияние структурного состояния стали на устойчивость к ПК Ø Склонность к ПК возрастает в присутствии в структуре избыточных фаз даже в отсутствие обеднения хромом и молибденом границ зерен. Ø ПРИЧИНЫ: 1. неустойчивость самих фаз, активирующихся при потенциалах более отрицательных, чем Епит твердого раствора; 2. Уменьшение стойкости твердого раствора в зонах, примыкающих к этим фазам, в частности, из-за механических напряжений, возникающих при их выделении. Способ повышения устойчивости к ПК – аустенизация сталей, проводимая при достаточно высоких температурах, при которых происходит растворение избыточных фаз.
Влияние структурного состояния стали на устойчивость к ПК Ø Склонность к ПК возрастает в присутствии в структуре избыточных фаз даже в отсутствие обеднения хромом и молибденом границ зерен. Ø ПРИЧИНЫ: 1. неустойчивость самих фаз, активирующихся при потенциалах более отрицательных, чем Епит твердого раствора; 2. Уменьшение стойкости твердого раствора в зонах, примыкающих к этим фазам, в частности, из-за механических напряжений, возникающих при их выделении. Способ повышения устойчивости к ПК – аустенизация сталей, проводимая при достаточно высоких температурах, при которых происходит растворение избыточных фаз.
 Влияние структурного состояния стали на устойчивость к ПК Ø Влияние размера зерна на склонность к ПК Мелкозернистая сталь имеет меньшую склонность к ПК, чем крупнозернистая. Причина: увеличение межзеренной поверхности, на которой распределяются неметаллические включения. Количество питтингов по границам зерен возрастает, но их размеры и глубина уменьшаются, что вызывает уменьшение скорости ПК. Ø Влияние холодной деформации на склонность к ПК Холодная деформация аустенитных сталей при 25 С и -196 С, сопровождающаяся образованием мартенсита, вызывает уменьшение Епит на 0, 3 -0, 4 В. Но деформация не влияет на Ереп, что указывает на то, что деформация оказывает влияние только на стадию зарождения питтинга.
Влияние структурного состояния стали на устойчивость к ПК Ø Влияние размера зерна на склонность к ПК Мелкозернистая сталь имеет меньшую склонность к ПК, чем крупнозернистая. Причина: увеличение межзеренной поверхности, на которой распределяются неметаллические включения. Количество питтингов по границам зерен возрастает, но их размеры и глубина уменьшаются, что вызывает уменьшение скорости ПК. Ø Влияние холодной деформации на склонность к ПК Холодная деформация аустенитных сталей при 25 С и -196 С, сопровождающаяся образованием мартенсита, вызывает уменьшение Епит на 0, 3 -0, 4 В. Но деформация не влияет на Ереп, что указывает на то, что деформация оказывает влияние только на стадию зарождения питтинга.
 Влияние температуры среды на устойчивость к ПК Ø С повышением температуры скорость ПК возрастает. Епит смещается в отрицательную сторону, характер смещения зависит от состава стали и среды. Стойкость против ПК при повышении температуры оценивается критической температурой питтингообразования (КТП), зависящей от содержания в аустенитных сталях молибдена: Более точно связь между химическим составом стали и КТП устанавливает эквивалент стойкости против ПК (ЭСП): Чем больше ЭСП, тем выше КТП
Влияние температуры среды на устойчивость к ПК Ø С повышением температуры скорость ПК возрастает. Епит смещается в отрицательную сторону, характер смещения зависит от состава стали и среды. Стойкость против ПК при повышении температуры оценивается критической температурой питтингообразования (КТП), зависящей от содержания в аустенитных сталях молибдена: Более точно связь между химическим составом стали и КТП устанавливает эквивалент стойкости против ПК (ЭСП): Чем больше ЭСП, тем выше КТП
 Влияние состояния поверхности на устойчивость к ПК Ø Грубо обработанная поверхность имеет большую склонность к ПК ПРИЧИНА – макродефекты (задиры, закаты окалины, вмятины, неудаленные загрязнения), повышающие гетерогенность поверхности и способствющие возникновению концентрационных неоднородностей и мирощелей. СПОСОБЫ достижения максимальной устойчивости к ПК: 1. Травление поверхности с целью вытравливания «слабых» мест, особенно химически нестойких неметаллических включений 2. Тонкое шлифование, затем полирование с последующим пассивированием
Влияние состояния поверхности на устойчивость к ПК Ø Грубо обработанная поверхность имеет большую склонность к ПК ПРИЧИНА – макродефекты (задиры, закаты окалины, вмятины, неудаленные загрязнения), повышающие гетерогенность поверхности и способствющие возникновению концентрационных неоднородностей и мирощелей. СПОСОБЫ достижения максимальной устойчивости к ПК: 1. Травление поверхности с целью вытравливания «слабых» мест, особенно химически нестойких неметаллических включений 2. Тонкое шлифование, затем полирование с последующим пассивированием
 Влияние неметаллических включений на устойчивость к ПК Питтингообразование в коррозионностойких сталях всех структурных классов происходит только у частиц неметаллических включений (НВ) В основном питтинг возникает около оксисульфидов. Питтинг начинается с зарождения узкой канавки около НВ. По мере расширения и углубления канавки само НВ постепенно разрушется, растворяется и удаляется из питтинга. В закаленном состоянии большая часть питтингов наблюдается около НВ в теле зерна, в отпущенном – у НВ по границам зерен, что указывает на важную роль твердого раствора, состав которого меняется при термообработке. ВАЖНО! Не наличие НВ, а присутствие ионов-активаторов и достаточно высокий потенциал коррозии вызывают склонность сталей к ПК, а НВ только облегчают процесс зарождения питтинга
Влияние неметаллических включений на устойчивость к ПК Питтингообразование в коррозионностойких сталях всех структурных классов происходит только у частиц неметаллических включений (НВ) В основном питтинг возникает около оксисульфидов. Питтинг начинается с зарождения узкой канавки около НВ. По мере расширения и углубления канавки само НВ постепенно разрушется, растворяется и удаляется из питтинга. В закаленном состоянии большая часть питтингов наблюдается около НВ в теле зерна, в отпущенном – у НВ по границам зерен, что указывает на важную роль твердого раствора, состав которого меняется при термообработке. ВАЖНО! Не наличие НВ, а присутствие ионов-активаторов и достаточно высокий потенциал коррозии вызывают склонность сталей к ПК, а НВ только облегчают процесс зарождения питтинга
 Влияние неметаллических включений на устойчивость к ПК Ø Наиболее чувствительные места для зарождения питтинга – сульфидные НВ. Питтинги возникают или на самих сульфидах или на сульфидной оболочке, окружающей оксиды. При содержании Mn менее 0, 3 -0, 4% (ниже предела растворимости, все в твердом растворе), образуются сульфиды хрома, концентрация хрома в которых достигает 50 %, что вызывает их легкую пассивацию. Скорость растворения металла вокруг Инициирование питтинга на НВ в 100 раз выше, чем средняя двойных оксидно- скорость растворения стали. сульфидномарганцевых включениях: 1 – оксид; 2 – Mn. S; 3 – Причины: локальная деформация Cr. S; П – пассивная пленка; А – (различие КТР металла и НВ, анод; К - катод появление структурно-химических дефектов - дислокаций), либо активирующее действие продуктов растворения включений
Влияние неметаллических включений на устойчивость к ПК Ø Наиболее чувствительные места для зарождения питтинга – сульфидные НВ. Питтинги возникают или на самих сульфидах или на сульфидной оболочке, окружающей оксиды. При содержании Mn менее 0, 3 -0, 4% (ниже предела растворимости, все в твердом растворе), образуются сульфиды хрома, концентрация хрома в которых достигает 50 %, что вызывает их легкую пассивацию. Скорость растворения металла вокруг Инициирование питтинга на НВ в 100 раз выше, чем средняя двойных оксидно- скорость растворения стали. сульфидномарганцевых включениях: 1 – оксид; 2 – Mn. S; 3 – Причины: локальная деформация Cr. S; П – пассивная пленка; А – (различие КТР металла и НВ, анод; К - катод появление структурно-химических дефектов - дислокаций), либо активирующее действие продуктов растворения включений
 Электрохимические методы исследования ПК Ø Потенциодинамический метод 1. Вариант «А» : проводят снятие кривой i=f(E) в режиме развертки потенциала с определенной скоростью (d. E/dt). Определяют Епит, Ереп, Езащ, Еинг Т. 1 – Епит при плотности тока выше 10 мк. А/см 2; Т. 2 – обратный ход начинают при плотности тока 500 мк. А/см 2 для определения Ереп (т. 3 или т. 4) и Езащ (т. 5). Еинг (т. 4) – определяют в средах, содержащих т. 4 ингибирующие анионы (нитрат-ионы); соответствует потенциалу, при котором после прохождения участка питтингообразования фиксируется плотность тока пассивного состояния 2. Вариант «Б» : проводят построение кривой i=f(E) в режиме ступенчатого изменения потенциалов с определенной величиной шага за определенное время
Электрохимические методы исследования ПК Ø Потенциодинамический метод 1. Вариант «А» : проводят снятие кривой i=f(E) в режиме развертки потенциала с определенной скоростью (d. E/dt). Определяют Епит, Ереп, Езащ, Еинг Т. 1 – Епит при плотности тока выше 10 мк. А/см 2; Т. 2 – обратный ход начинают при плотности тока 500 мк. А/см 2 для определения Ереп (т. 3 или т. 4) и Езащ (т. 5). Еинг (т. 4) – определяют в средах, содержащих т. 4 ингибирующие анионы (нитрат-ионы); соответствует потенциалу, при котором после прохождения участка питтингообразования фиксируется плотность тока пассивного состояния 2. Вариант «Б» : проводят построение кривой i=f(E) в режиме ступенчатого изменения потенциалов с определенной величиной шага за определенное время
 Электрохимические методы исследования ПК Ø Потенциостатический метод 1. Вариант «А» : проводят постороение кривой i=f(E) в режиме постоянных значений потенциала Е=const c выдержкой при каждом значении плотности тока. Епит определяют как потенциал, положительнее которого начинается устойчивый рост плотности тока. 2. Вариант «Б» : проводят построение кривой i=f(t) при заданных значениях потенциала Значение Епит определяют как величину, находящуюся в интервале потенциалов между величиной, при которой i во времени падает, и величиной, при которой i растет При этом первоначальное состояние образца пассивированное, с тем чтобы при воспроизводилась плотность тока пассивного состояния
Электрохимические методы исследования ПК Ø Потенциостатический метод 1. Вариант «А» : проводят постороение кривой i=f(E) в режиме постоянных значений потенциала Е=const c выдержкой при каждом значении плотности тока. Епит определяют как потенциал, положительнее которого начинается устойчивый рост плотности тока. 2. Вариант «Б» : проводят построение кривой i=f(t) при заданных значениях потенциала Значение Епит определяют как величину, находящуюся в интервале потенциалов между величиной, при которой i во времени падает, и величиной, при которой i растет При этом первоначальное состояние образца пассивированное, с тем чтобы при воспроизводилась плотность тока пассивного состояния
 Электрохимические методы исследования ПК 3. Вариант «В» : построение кривой i=f(E) проводят при заданных значениях потенциала Отличие от варианта «Б» - первоначальное состояние образца – локально-активированное, что обеспечивается заданием высоких анодных потенциалов, соответствующих области ПК. Затем задают потенциал отрицательнее этого значения. При потенциале, при котором i во времени стабильно падает, происходит репассивация первоначально образовавшихся питтингов. Епит находится в интервале Е между величиной, при которой i во времени растет, и величиной Е, при которой i во времени падает. Гальваностатический метод Получают зависимость Е=f(t) при заданной плотности тока. Епит определяют как потенциал, устанавливающийся при iкр через определенное время (25 -30 мин)
Электрохимические методы исследования ПК 3. Вариант «В» : построение кривой i=f(E) проводят при заданных значениях потенциала Отличие от варианта «Б» - первоначальное состояние образца – локально-активированное, что обеспечивается заданием высоких анодных потенциалов, соответствующих области ПК. Затем задают потенциал отрицательнее этого значения. При потенциале, при котором i во времени стабильно падает, происходит репассивация первоначально образовавшихся питтингов. Епит находится в интервале Е между величиной, при которой i во времени растет, и величиной Е, при которой i во времени падает. Гальваностатический метод Получают зависимость Е=f(t) при заданной плотности тока. Епит определяют как потенциал, устанавливающийся при iкр через определенное время (25 -30 мин)

