дождевые черви_2_3курс_2012.ppt
- Количество слайдов: 52
 Питание дождевых червей
Питание дождевых червей
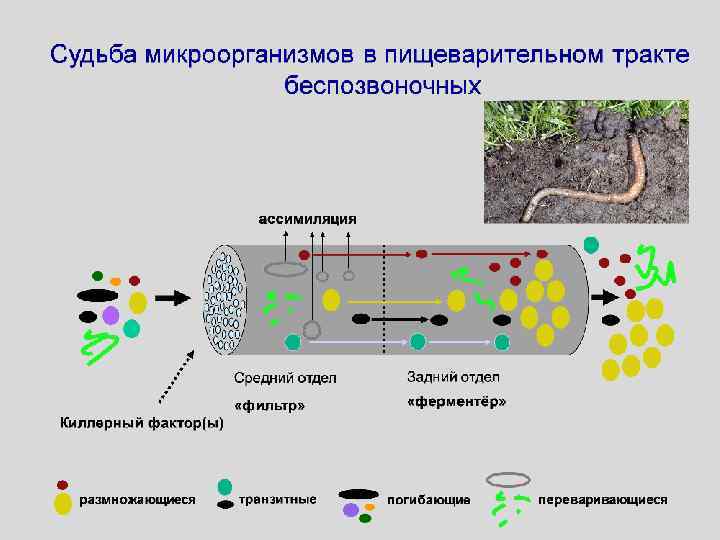
 Микроорганизмы и питание червей (беспозвоночных) Почему микроорганизмы - необходимый компонент диеты почвенных беспозвоночных? Беспозвоночные не могут потреблять свежий растительный опад (репелленты, токсины? ) Mindermann, Daniels , 1963 Беспозвоночные не образуют целлюлазы (исключение - термиты) Siepel, de Ruiter- Dukman, 1993; Lattaud et al. , 1998 Животные используют гидролитические Martin, 1984 ферменты перевариваемых микроорганизмов Begon et al. , 1989 или их образую симбионты
Микроорганизмы и питание червей (беспозвоночных) Почему микроорганизмы - необходимый компонент диеты почвенных беспозвоночных? Беспозвоночные не могут потреблять свежий растительный опад (репелленты, токсины? ) Mindermann, Daniels , 1963 Беспозвоночные не образуют целлюлазы (исключение - термиты) Siepel, de Ruiter- Dukman, 1993; Lattaud et al. , 1998 Животные используют гидролитические Martin, 1984 ферменты перевариваемых микроорганизмов Begon et al. , 1989 или их образую симбионты
 Begon et al. , 1989 Беспозвоночные зависят от Pokarzhevskii et al. , 1984 микробов как источника незаменимых аминокислот (сами не синтезируют) В почве ресурс аминокислот сосредоточен в микроорганизмах Pokarzhevskii et al. , 1984
Begon et al. , 1989 Беспозвоночные зависят от Pokarzhevskii et al. , 1984 микробов как источника незаменимых аминокислот (сами не синтезируют) В почве ресурс аминокислот сосредоточен в микроорганизмах Pokarzhevskii et al. , 1984
 Баланс метионина в кишечнике дождевых червей (Pokarzhevskii et al, 1997) • время полужизни азота в тела дождевых червей составляет около 2 -х недель • для удовлетворения потребностей в метионине черви должны синтезировать в 20 раз больше метионина, чем содержится в пище • животные не синтезируют незаменимые аминокислоты симбионты
Баланс метионина в кишечнике дождевых червей (Pokarzhevskii et al, 1997) • время полужизни азота в тела дождевых червей составляет около 2 -х недель • для удовлетворения потребностей в метионине черви должны синтезировать в 20 раз больше метионина, чем содержится в пище • животные не синтезируют незаменимые аминокислоты симбионты
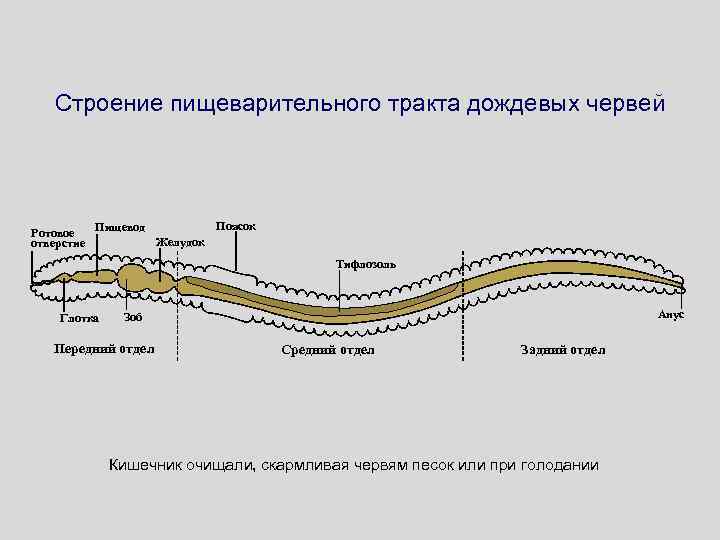 Строение пищеварительного тракта дождевых червей Поясок Пищевод Ротовое Желудок отверстие Тифлозоль Глотка Анус Зоб Передний отдел Средний отдел Задний отдел Кишечник очищали, скармливая червям песок или при голодании
Строение пищеварительного тракта дождевых червей Поясок Пищевод Ротовое Желудок отверстие Тифлозоль Глотка Анус Зоб Передний отдел Средний отдел Задний отдел Кишечник очищали, скармливая червям песок или при голодании
 Чем питаются дождевые черви? гипотеза о симбиотическом пищеварении (Trigo, Lavelle, 1993) • по мере продвижения по кишечнику p. H возрастает более, чем на 1 (по-видимому, за счет увеличения концентрации обменного кальция) • в 2 раза возрастает содержание воды • в передний отдел кишечника червей секретируются водорастворимые органические вещества (мукус), концентрация которых затем резко падает в среднем и заднем отделах • активизируются (растут? ) бактерии, усиливается разложение ОВ (затравочный эффект или «priming effect» ), часть их реабсорбируется в заднем отделе кишечника, чтобы стать снова источником энергии для роста бактерий в следующем цикле
Чем питаются дождевые черви? гипотеза о симбиотическом пищеварении (Trigo, Lavelle, 1993) • по мере продвижения по кишечнику p. H возрастает более, чем на 1 (по-видимому, за счет увеличения концентрации обменного кальция) • в 2 раза возрастает содержание воды • в передний отдел кишечника червей секретируются водорастворимые органические вещества (мукус), концентрация которых затем резко падает в среднем и заднем отделах • активизируются (растут? ) бактерии, усиливается разложение ОВ (затравочный эффект или «priming effect» ), часть их реабсорбируется в заднем отделе кишечника, чтобы стать снова источником энергии для роста бактерий в следующем цикле
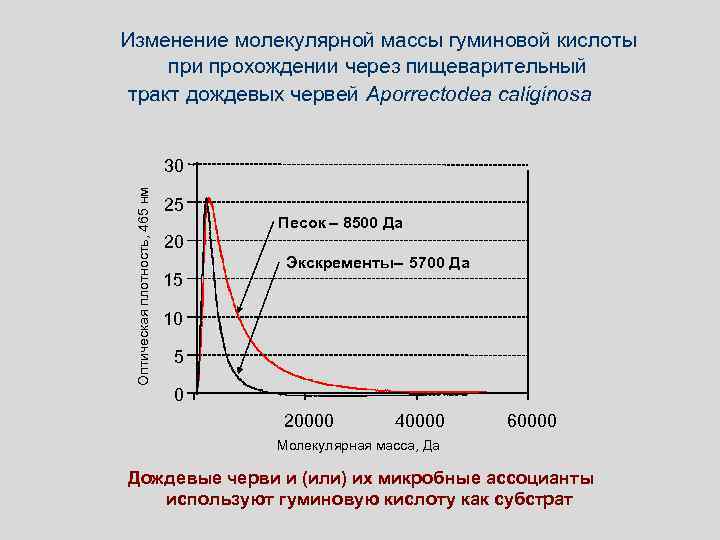 Изменение молекулярной массы гуминовой кислоты при прохождении через пищеварительный тракт дождевых червей Aporrectodea caliginosa Оптическая плотность, 465 нм 30 25 Песок – 8500 Да 20 15 Экскременты – 5700 Да 10 5 0 20000 40000 60000 Молекулярная масса, Да Дождевые черви и (или) их микробные ассоцианты используют гуминовую кислоту как субстрат
Изменение молекулярной массы гуминовой кислоты при прохождении через пищеварительный тракт дождевых червей Aporrectodea caliginosa Оптическая плотность, 465 нм 30 25 Песок – 8500 Да 20 15 Экскременты – 5700 Да 10 5 0 20000 40000 60000 Молекулярная масса, Да Дождевые черви и (или) их микробные ассоцианты используют гуминовую кислоту как субстрат
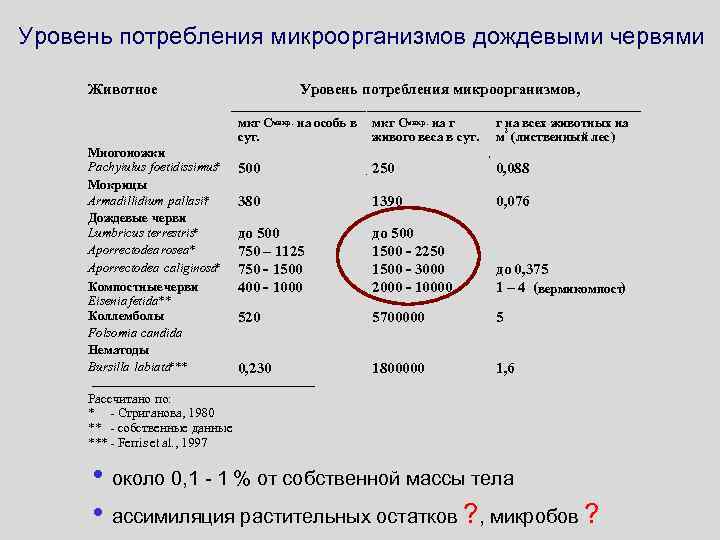 Уровень потребления микроорганизмов дождевыми червями Животное Уровень потребления микроорганизмов, мкг Смикр. на особь в сут. Многоножки Pachyiulus foetidissimus * Мокрицы Armadillidium pallasii * Дождевые черви Lumbricus terrestris * Aporrectodearosea* Aporrectodea caliginosa * Компостные черви Eisenia fetida** Коллемболы Folsomia candida Нематоды Bursilla labiata *** мкг Смикр. на г живого веса в сут. г 2 всех животных на на м (лиственный лес) 500 250 0, 088 380 1390 0, 076 до 500 750 – 1125 750 - 1500 400 - 1000 до 500 1500 - 2250 1500 - 3000 2000 - 10000 до 0, 375 1 – 4 (вермикомпост) 520 5700000 5 0, 230 1800000 1, 6 Рассчитано по: * - Стриганова, 1980 ** - собственные данные *** - Ferris et al. , 1997 • около 0, 1 - 1 % от собственной массы тела • ассимиляция растительных остатков ? , микробов ?
Уровень потребления микроорганизмов дождевыми червями Животное Уровень потребления микроорганизмов, мкг Смикр. на особь в сут. Многоножки Pachyiulus foetidissimus * Мокрицы Armadillidium pallasii * Дождевые черви Lumbricus terrestris * Aporrectodearosea* Aporrectodea caliginosa * Компостные черви Eisenia fetida** Коллемболы Folsomia candida Нематоды Bursilla labiata *** мкг Смикр. на г живого веса в сут. г 2 всех животных на на м (лиственный лес) 500 250 0, 088 380 1390 0, 076 до 500 750 – 1125 750 - 1500 400 - 1000 до 500 1500 - 2250 1500 - 3000 2000 - 10000 до 0, 375 1 – 4 (вермикомпост) 520 5700000 5 0, 230 1800000 1, 6 Рассчитано по: * - Стриганова, 1980 ** - собственные данные *** - Ferris et al. , 1997 • около 0, 1 - 1 % от собственной массы тела • ассимиляция растительных остатков ? , микробов ?
 Дождевые черви и продукция микроорганизмов дерново-подзолистая почва, луг: численность червей - до 500 экз. /м 2, живая биомасса – 250 г/м 2 • сезонная продукция бактерий (100 суток) с учетом скорости их размножения в кишечнике червей A. caliginosa - около 1012 клеток/м 2 • среднее сезонное содержание бактерий - около 1012 клеток/м 2 • в дерново-подзолистой почве за счет роста в кишечнике червей осуществляется одна генерация неспороносных бактерий (Горбенко и др. , 1986) за сезон в почве - 3 -25 генераций микроорганизмов - в ряде экосистем, например, в луговых, роль дождевых червей как регуляторов продукционного процесса бактерий существенна
Дождевые черви и продукция микроорганизмов дерново-подзолистая почва, луг: численность червей - до 500 экз. /м 2, живая биомасса – 250 г/м 2 • сезонная продукция бактерий (100 суток) с учетом скорости их размножения в кишечнике червей A. caliginosa - около 1012 клеток/м 2 • среднее сезонное содержание бактерий - около 1012 клеток/м 2 • в дерново-подзолистой почве за счет роста в кишечнике червей осуществляется одна генерация неспороносных бактерий (Горбенко и др. , 1986) за сезон в почве - 3 -25 генераций микроорганизмов - в ряде экосистем, например, в луговых, роль дождевых червей как регуляторов продукционного процесса бактерий существенна
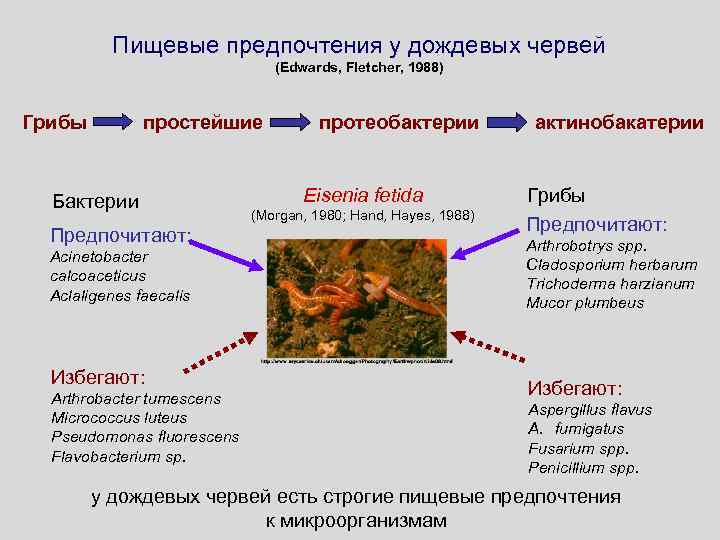 Пищевые предпочтения у дождевых червей (Edwards, Fletcher, 1988) Грибы простейшие Бактерии Предпочитают: Acinetobacter calcoaceticus Aclaligenes faecalis Избегают: Arthrobacter tumescens Micrococcus luteus Pseudomonas fluorescens Flavobacterium sp. протеобактерии Eisenia fetida (Morgan, 1980; Hand, Hayes, 1988) актинобакатерии Грибы Предпочитают: Arthrobotrys spp. Cladosporium herbarum Trichoderma harzianum Mucor plumbeus Избегают: Aspergillus flavus A. fumigatus Fusarium spp. Peniсillium spp. у дождевых червей есть строгие пищевые предпочтения к микроорганизмам
Пищевые предпочтения у дождевых червей (Edwards, Fletcher, 1988) Грибы простейшие Бактерии Предпочитают: Acinetobacter calcoaceticus Aclaligenes faecalis Избегают: Arthrobacter tumescens Micrococcus luteus Pseudomonas fluorescens Flavobacterium sp. протеобактерии Eisenia fetida (Morgan, 1980; Hand, Hayes, 1988) актинобакатерии Грибы Предпочитают: Arthrobotrys spp. Cladosporium herbarum Trichoderma harzianum Mucor plumbeus Избегают: Aspergillus flavus A. fumigatus Fusarium spp. Peniсillium spp. у дождевых червей есть строгие пищевые предпочтения к микроорганизмам
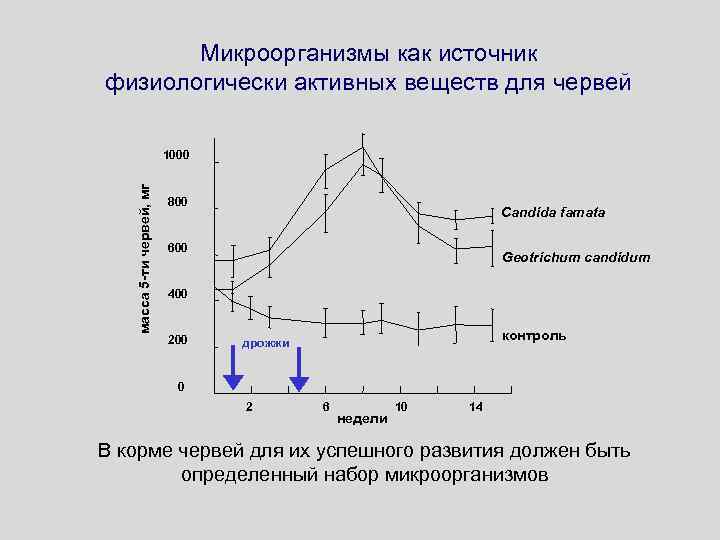 Микроорганизмы как источник физиологически активных веществ для червей масса 5 -ти червей, мг 1000 800 Candida famata 600 Geotrichum candidum 400 200 контроль дрожжи 0 2 6 недели 10 14 В корме червей для их успешного развития должен быть определенный набор микроорганизмов
Микроорганизмы как источник физиологически активных веществ для червей масса 5 -ти червей, мг 1000 800 Candida famata 600 Geotrichum candidum 400 200 контроль дрожжи 0 2 6 недели 10 14 В корме червей для их успешного развития должен быть определенный набор микроорганизмов
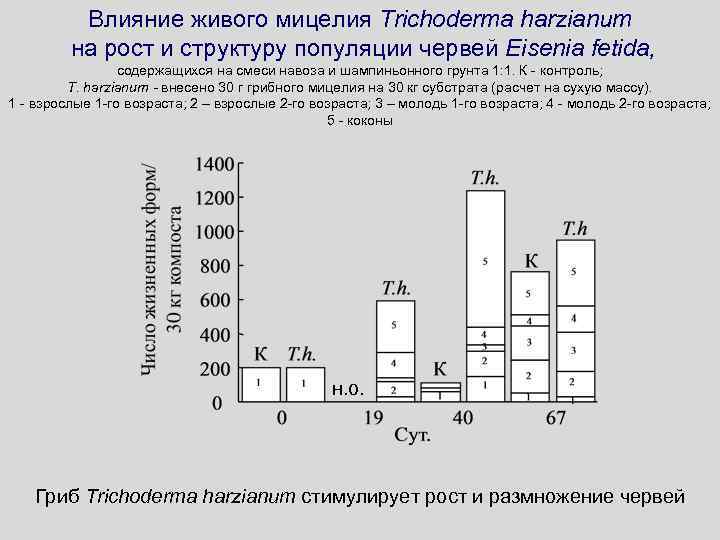 Влияние живого мицелия Trichoderma harzianum на рост и структуру популяции червей Eisenia fetida, содержащихся на смеси навоза и шампиньонного грунта 1: 1. К - контроль; T. harzianum - внесено 30 г грибного мицелия на 30 кг субстрата (расчет на сухую массу). 1 - взрослые 1 -го возраста; 2 – взрослые 2 -го возраста; 3 – молодь 1 -го возраста; 4 - молодь 2 -го возраста; 5 - коконы н. о. Гриб Trichoderma harzianum стимулирует рост и размножение червей
Влияние живого мицелия Trichoderma harzianum на рост и структуру популяции червей Eisenia fetida, содержащихся на смеси навоза и шампиньонного грунта 1: 1. К - контроль; T. harzianum - внесено 30 г грибного мицелия на 30 кг субстрата (расчет на сухую массу). 1 - взрослые 1 -го возраста; 2 – взрослые 2 -го возраста; 3 – молодь 1 -го возраста; 4 - молодь 2 -го возраста; 5 - коконы н. о. Гриб Trichoderma harzianum стимулирует рост и размножение червей
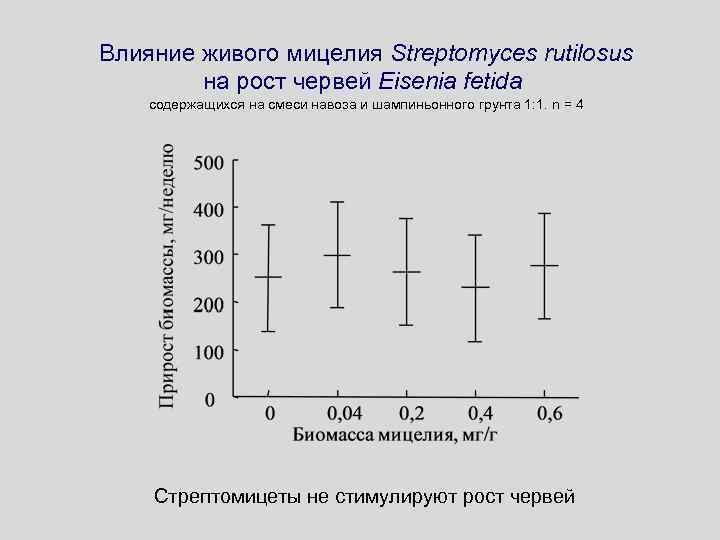 Влияние живого мицелия Streptomyces rutilosus на рост червей Eisenia fetida содержащихся на смеси навоза и шампиньонного грунта 1: 1. n = 4 Стрептомицеты не стимулируют рост червей
Влияние живого мицелия Streptomyces rutilosus на рост червей Eisenia fetida содержащихся на смеси навоза и шампиньонного грунта 1: 1. n = 4 Стрептомицеты не стимулируют рост червей
 Модификация микробного комплекса червями пассаж через пищеварительный тракт
Модификация микробного комплекса червями пассаж через пищеварительный тракт
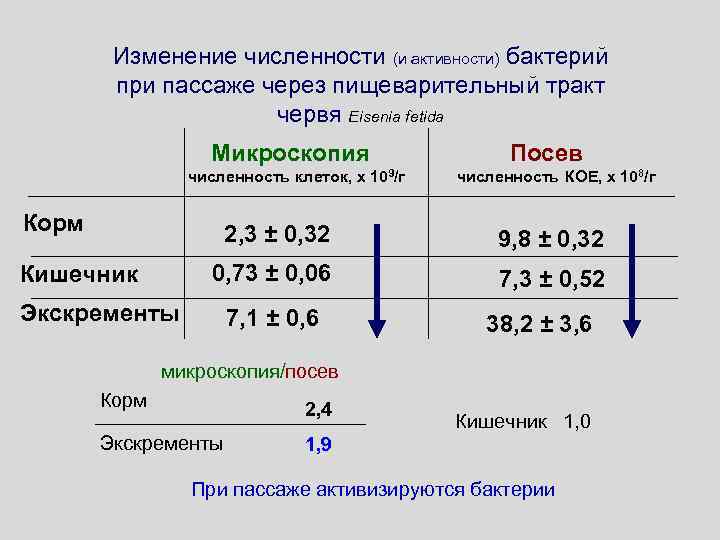 Изменение численности (и активности) бактерий при пассаже через пищеварительный тракт червя Eisenia fetida Микроскопия численность клеток, х 109/г Корм Посев численность КОЕ, х 108/г 2, 3 ± 0, 32 0, 73 ± 0, 06 Кишечник 9, 8 ± 0, 32 7, 3 ± 0, 52 Экскременты 7, 1 ± 0, 6 38, 2 ± 3, 6 микроскопия/посев Корм 2, 4 Экскременты 1, 9 Кишечник 1, 0 При пассаже активизируются бактерии
Изменение численности (и активности) бактерий при пассаже через пищеварительный тракт червя Eisenia fetida Микроскопия численность клеток, х 109/г Корм Посев численность КОЕ, х 108/г 2, 3 ± 0, 32 0, 73 ± 0, 06 Кишечник 9, 8 ± 0, 32 7, 3 ± 0, 52 Экскременты 7, 1 ± 0, 6 38, 2 ± 3, 6 микроскопия/посев Корм 2, 4 Экскременты 1, 9 Кишечник 1, 0 При пассаже активизируются бактерии
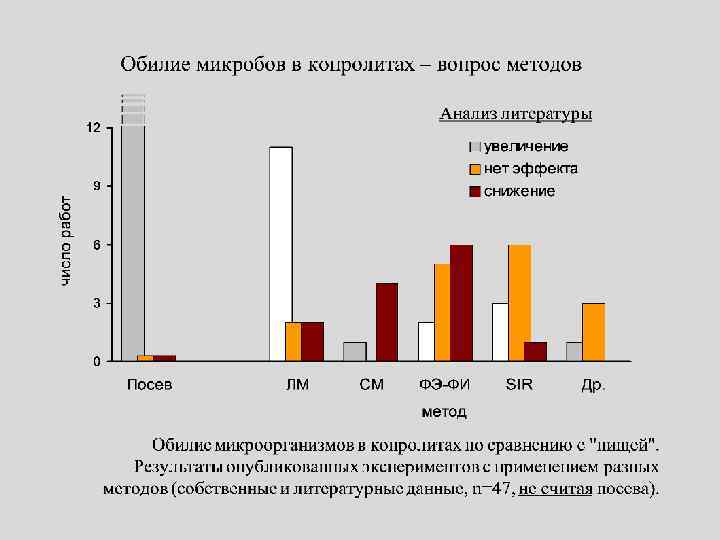
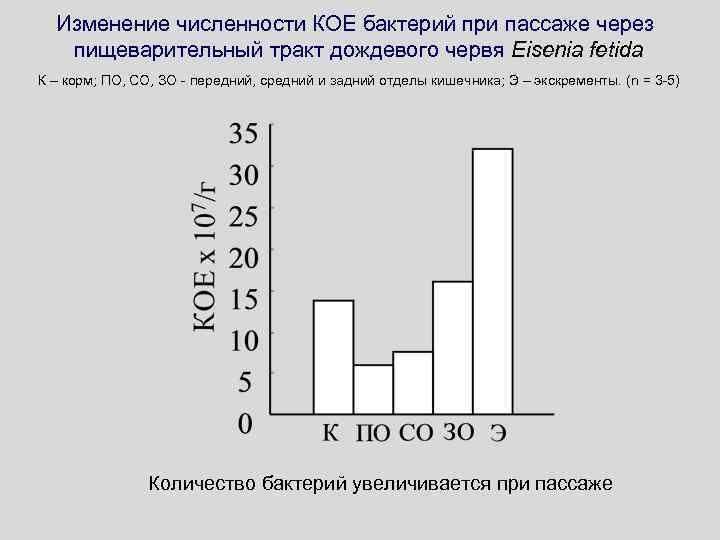 Изменение численности КОЕ бактерий при пассаже через пищеварительный тракт дождевого червя Eisenia fetida К – корм; ПО, СО, ЗО - передний, средний и задний отделы кишечника; Э – экскременты. (n = 3 -5) Количество бактерий увеличивается при пассаже
Изменение численности КОЕ бактерий при пассаже через пищеварительный тракт дождевого червя Eisenia fetida К – корм; ПО, СО, ЗО - передний, средний и задний отделы кишечника; Э – экскременты. (n = 3 -5) Количество бактерий увеличивается при пассаже
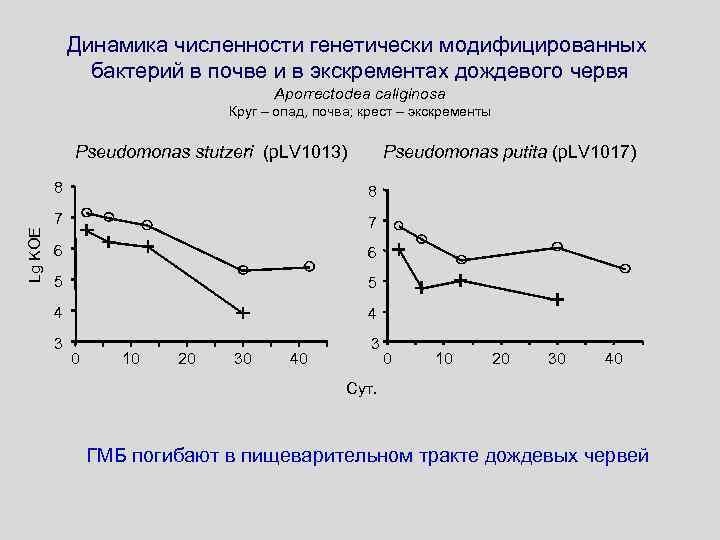 Динамика численности генетически модифицированных бактерий в почве и в экскрементах дождевого червя Aporrectodea caliginosa Круг – опад, почва; крест – экскременты Pseudomonas stutzeri (p. LV 1013) Pseudomonas putita (p. LV 1017) Lg KOE 8 8 7 7 6 6 5 5 4 4 3 3 0 10 20 30 40 Cут. ГМБ погибают в пищеварительном тракте дождевых червей
Динамика численности генетически модифицированных бактерий в почве и в экскрементах дождевого червя Aporrectodea caliginosa Круг – опад, почва; крест – экскременты Pseudomonas stutzeri (p. LV 1013) Pseudomonas putita (p. LV 1017) Lg KOE 8 8 7 7 6 6 5 5 4 4 3 3 0 10 20 30 40 Cут. ГМБ погибают в пищеварительном тракте дождевых червей
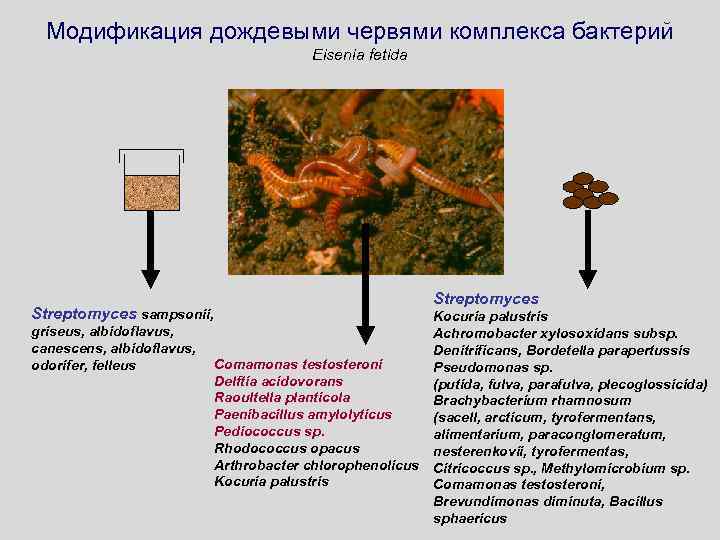 Модификация дождевыми червями комплекса бактерий Eisenia fetida Streptomyces sampsonii, griseus, albidoflavus, canescens, albidoflavus, odorifer, felleus Streptomyces Kocuria palustris Achromobacter xylosoxidans subsp. Denitrificans, Bordetella parapertussis Comamonas testosteroni Pseudomonas sp. Delftia acidovorans (putida, fulva, parafulva, plecoglossicida) Raoultella planticola Brachybacterium rhamnosum Paenibacillus amylolyticus (sacell, arcticum, tyrofermentans, Pediococcus sp. alimentarium, paraconglomeratum, Rhodococcus opacus nesterenkovii, tyrofermentas, Arthrobacter chlorophenolicus Citricoccus sp. , Methylomicrobium sp. Kocuria palustris Comamonas testosteroni, Brevundimonas diminuta, Bacillus sphaericus
Модификация дождевыми червями комплекса бактерий Eisenia fetida Streptomyces sampsonii, griseus, albidoflavus, canescens, albidoflavus, odorifer, felleus Streptomyces Kocuria palustris Achromobacter xylosoxidans subsp. Denitrificans, Bordetella parapertussis Comamonas testosteroni Pseudomonas sp. Delftia acidovorans (putida, fulva, parafulva, plecoglossicida) Raoultella planticola Brachybacterium rhamnosum Paenibacillus amylolyticus (sacell, arcticum, tyrofermentans, Pediococcus sp. alimentarium, paraconglomeratum, Rhodococcus opacus nesterenkovii, tyrofermentas, Arthrobacter chlorophenolicus Citricoccus sp. , Methylomicrobium sp. Kocuria palustris Comamonas testosteroni, Brevundimonas diminuta, Bacillus sphaericus
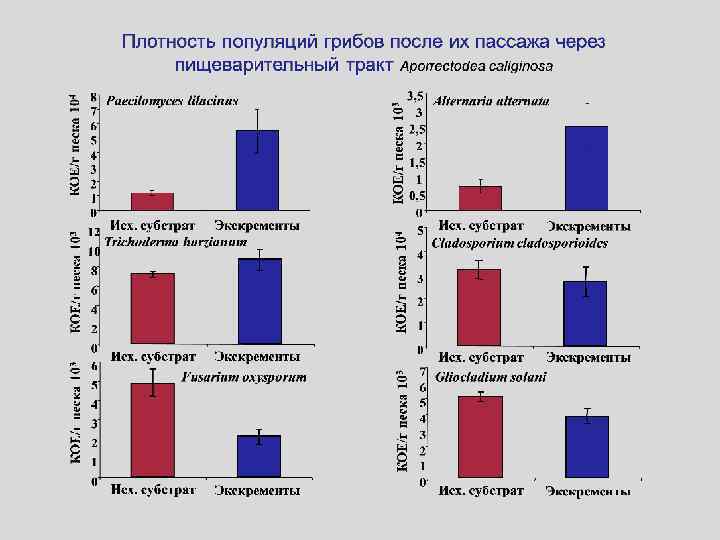
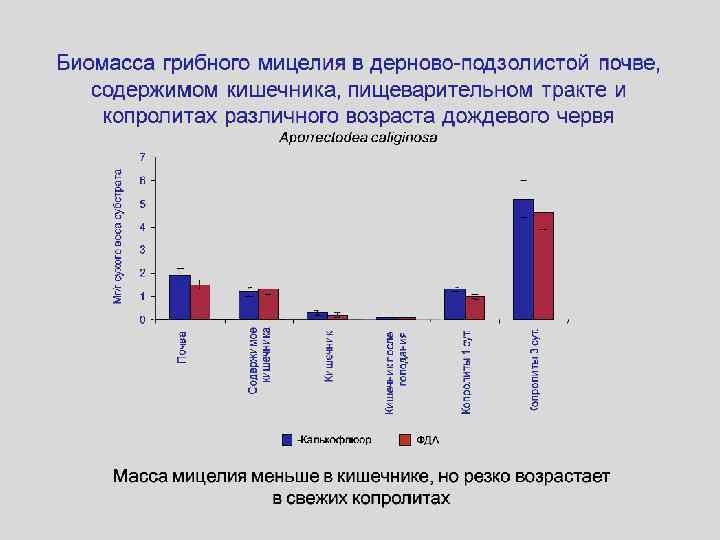
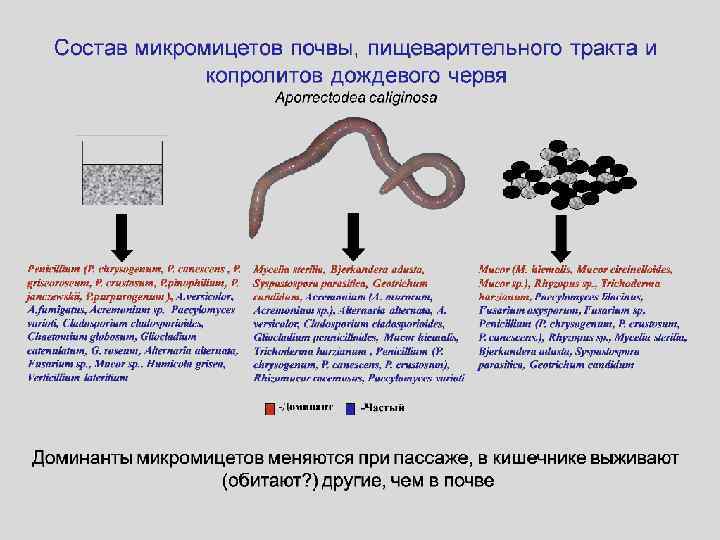
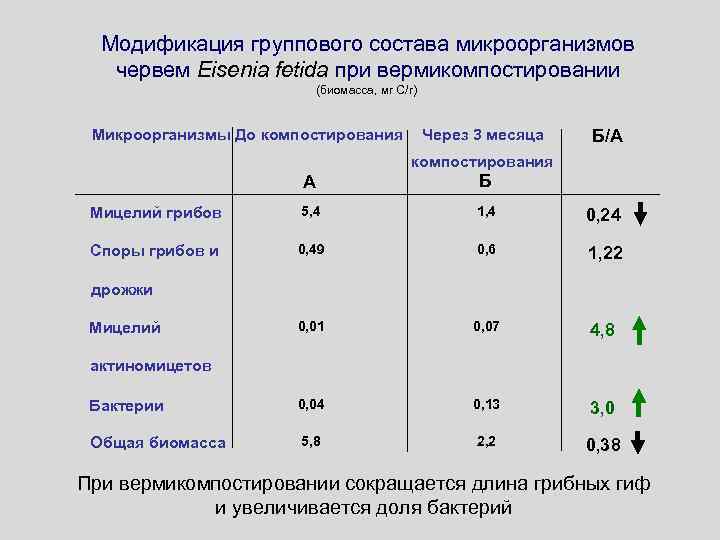 Модификация группового состава микроорганизмов червем Eisenia fetida при вермикомпостировании (биомасса, мг С/г) Микроорганизмы До компостирования Через 3 месяца Б/А компостирования А Б Мицелий грибов 5, 4 1, 4 0, 24 Споры грибов и 0, 49 0, 6 1, 22 0, 01 0, 07 4, 8 Бактерии 0, 04 0, 13 3, 0 Общая биомасса 5, 8 2, 2 0, 38 дрожжи Мицелий актиномицетов При вермикомпостировании сокращается длина грибных гиф и увеличивается доля бактерий
Модификация группового состава микроорганизмов червем Eisenia fetida при вермикомпостировании (биомасса, мг С/г) Микроорганизмы До компостирования Через 3 месяца Б/А компостирования А Б Мицелий грибов 5, 4 1, 4 0, 24 Споры грибов и 0, 49 0, 6 1, 22 0, 01 0, 07 4, 8 Бактерии 0, 04 0, 13 3, 0 Общая биомасса 5, 8 2, 2 0, 38 дрожжи Мицелий актиномицетов При вермикомпостировании сокращается длина грибных гиф и увеличивается доля бактерий
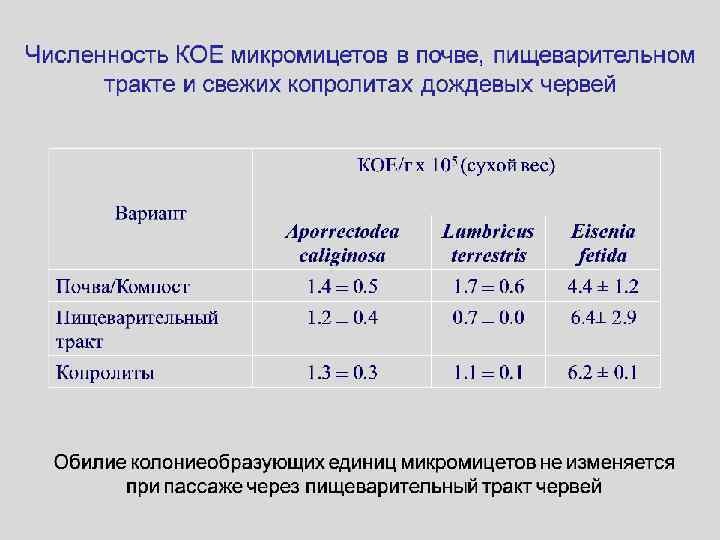
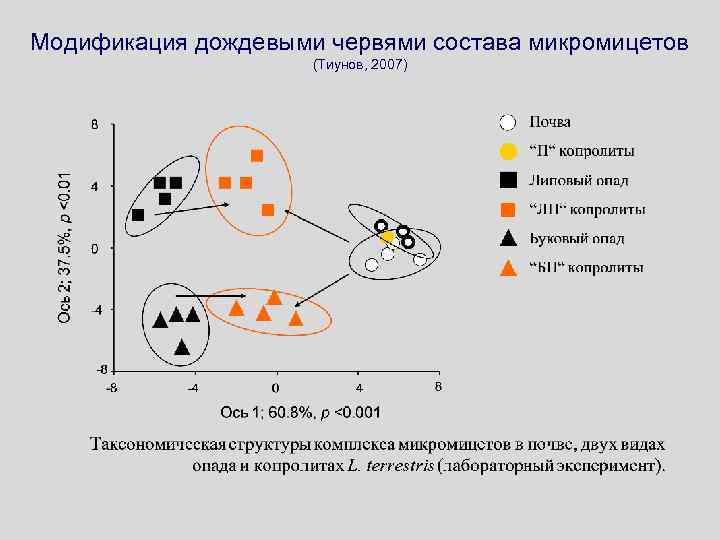 Модификация дождевыми червями состава микромицетов (Тиунов, 2007)
Модификация дождевыми червями состава микромицетов (Тиунов, 2007)
 Микроорганизмы и беспозвоночные в ходах дождевых червей
Микроорганизмы и беспозвоночные в ходах дождевых червей
 Работы д. б. н. А. В. Тиунова «Средообразующая деятельность дождевых червей»
Работы д. б. н. А. В. Тиунова «Средообразующая деятельность дождевых червей»
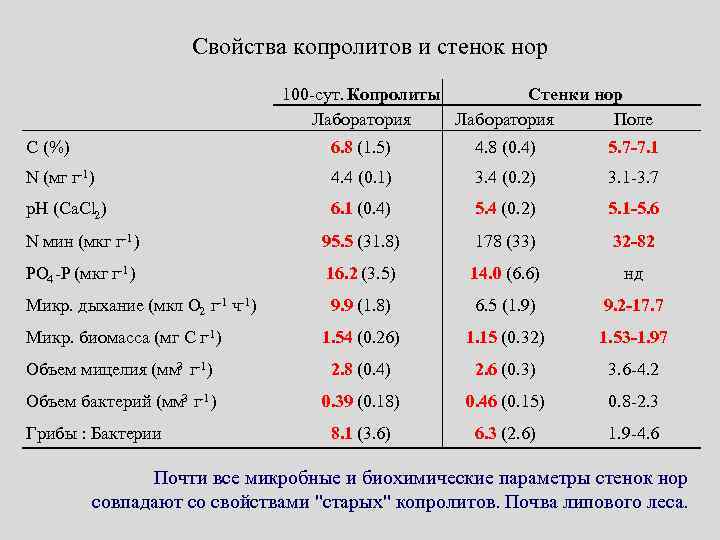 Свойства копролитов и стенок нор 100 -сут. Копролиты Стенки нор Лаборатория Поле C (%) 6. 8 (1. 5) 4. 8 (0. 4) 5. 7 -7. 1 N (мг г-1 ) 4. 4 (0. 1) 3. 4 (0. 2) 3. 1 -3. 7 p. H (Ca. Cl 2 ) 6. 1 (0. 4) 5. 4 (0. 2) 5. 1 -5. 6 N мин (мкг г-1 ) 95. 5 (31. 8) 178 (33) 32 -82 PO 4 -P (мкг г-1 ) 16. 2 (3. 5) 14. 0 (6. 6) нд Микр. дыхание (мкл О 2 г-1 ч-1 ) 9. 9 (1. 8) 6. 5 (1. 9) 9. 2 -17. 7 Микр. биомасса (мг С г-1 ) 1. 54 (0. 26) 1. 15 (0. 32) 1. 53 -1. 97 Объем мицелия (мм 3 г-1 ) 2. 8 (0. 4) 2. 6 (0. 3) 3. 6 -4. 2 Объем бактерий (мм 3 г-1 ) 0. 39 (0. 18) 0. 46 (0. 15) 0. 8 -2. 3 8. 1 (3. 6) 6. 3 (2. 6) 1. 9 -4. 6 Грибы : Бактерии Почти все микробные и биохимические параметры стенок нор совпадают со свойствами "старых" копролитов. Почва липового леса.
Свойства копролитов и стенок нор 100 -сут. Копролиты Стенки нор Лаборатория Поле C (%) 6. 8 (1. 5) 4. 8 (0. 4) 5. 7 -7. 1 N (мг г-1 ) 4. 4 (0. 1) 3. 4 (0. 2) 3. 1 -3. 7 p. H (Ca. Cl 2 ) 6. 1 (0. 4) 5. 4 (0. 2) 5. 1 -5. 6 N мин (мкг г-1 ) 95. 5 (31. 8) 178 (33) 32 -82 PO 4 -P (мкг г-1 ) 16. 2 (3. 5) 14. 0 (6. 6) нд Микр. дыхание (мкл О 2 г-1 ч-1 ) 9. 9 (1. 8) 6. 5 (1. 9) 9. 2 -17. 7 Микр. биомасса (мг С г-1 ) 1. 54 (0. 26) 1. 15 (0. 32) 1. 53 -1. 97 Объем мицелия (мм 3 г-1 ) 2. 8 (0. 4) 2. 6 (0. 3) 3. 6 -4. 2 Объем бактерий (мм 3 г-1 ) 0. 39 (0. 18) 0. 46 (0. 15) 0. 8 -2. 3 8. 1 (3. 6) 6. 3 (2. 6) 1. 9 -4. 6 Грибы : Бактерии Почти все микробные и биохимические параметры стенок нор совпадают со свойствами "старых" копролитов. Почва липового леса.

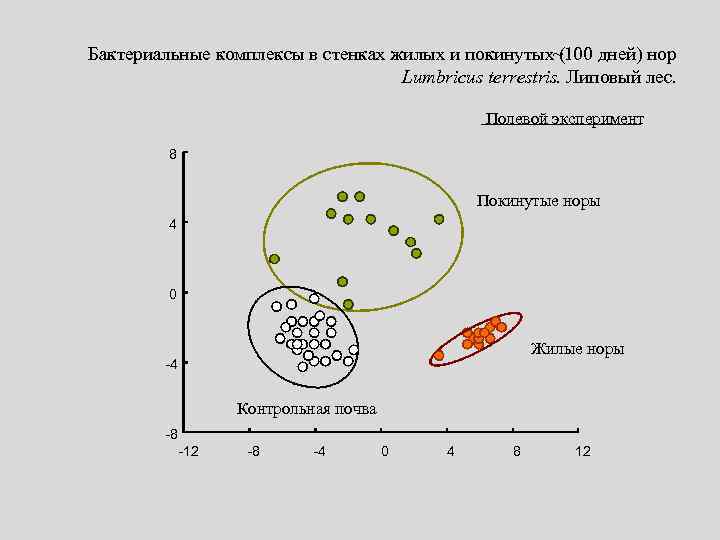 Бактериальные комплексы в стенках жилых и покинутых~100 дней) нор ( Lumbricus terrestris. Липовый лес. Полевой эксперимент 8 Покинутые норы 4 0 Жилые норы -4 Контрольная почва -8 -12 -8 -4 0 4 8 12
Бактериальные комплексы в стенках жилых и покинутых~100 дней) нор ( Lumbricus terrestris. Липовый лес. Полевой эксперимент 8 Покинутые норы 4 0 Жилые норы -4 Контрольная почва -8 -12 -8 -4 0 4 8 12
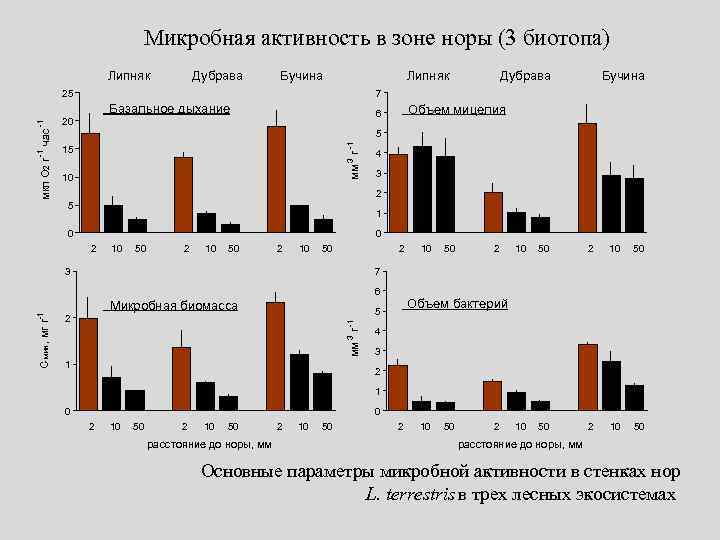 Микробная активность в зоне норы (3 биотопа) Липняк Дубрава Бучина Липняк 25 -1 5 15 3 мм г -1 час -1 мкл O 2 г Объем мицелия 6 20 10 4 3 2 5 1 0 0 2 10 50 2 3 10 50 2 10 50 7 6 Микробная биомасса Объем бактерий 5 -1 2 3 мм г -1 Бучина 7 Базальное дыхание С мик , мг г Дубрава 1 4 3 2 1 0 0 2 10 50 расстояние до норы, мм 2 10 50 2 расстояние до норы, мм Основные параметры микробной активности в стенках нор L. terrestris в трех лесных экосистемах
Микробная активность в зоне норы (3 биотопа) Липняк Дубрава Бучина Липняк 25 -1 5 15 3 мм г -1 час -1 мкл O 2 г Объем мицелия 6 20 10 4 3 2 5 1 0 0 2 10 50 2 3 10 50 2 10 50 7 6 Микробная биомасса Объем бактерий 5 -1 2 3 мм г -1 Бучина 7 Базальное дыхание С мик , мг г Дубрава 1 4 3 2 1 0 0 2 10 50 расстояние до норы, мм 2 10 50 2 расстояние до норы, мм Основные параметры микробной активности в стенках нор L. terrestris в трех лесных экосистемах
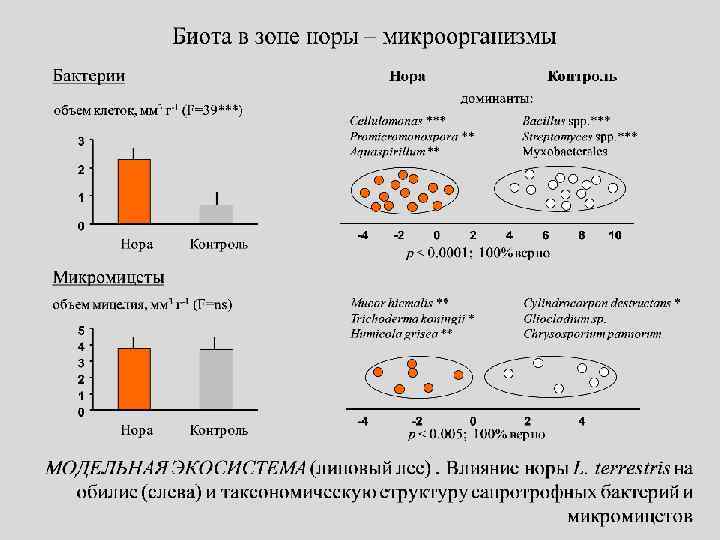
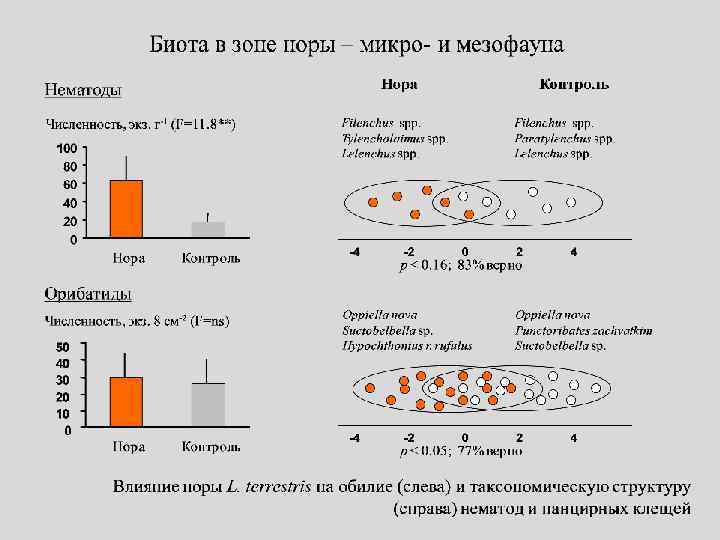
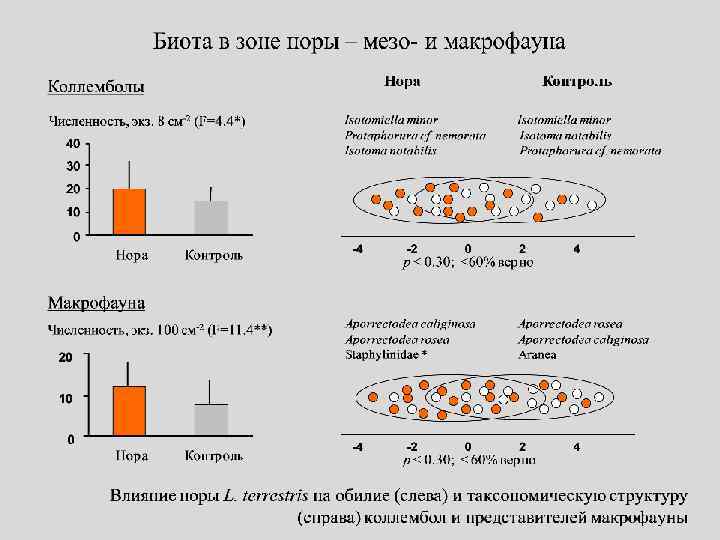
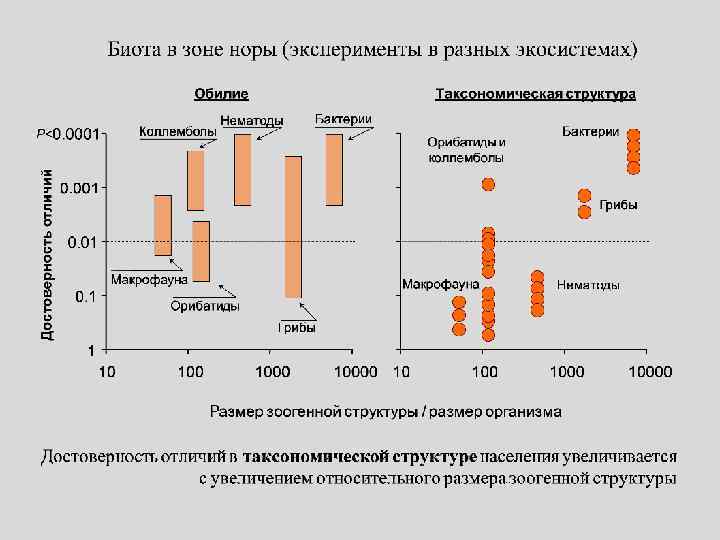
 Биологическая активность пищеварительной среды и экскретов червей
Биологическая активность пищеварительной среды и экскретов червей
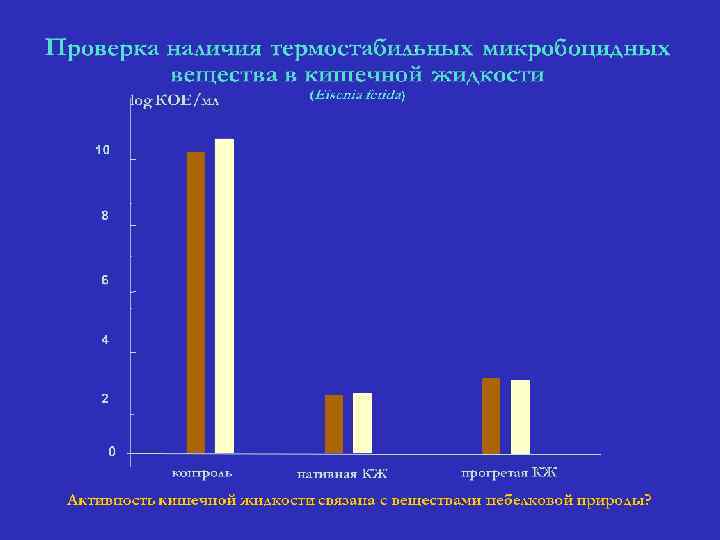
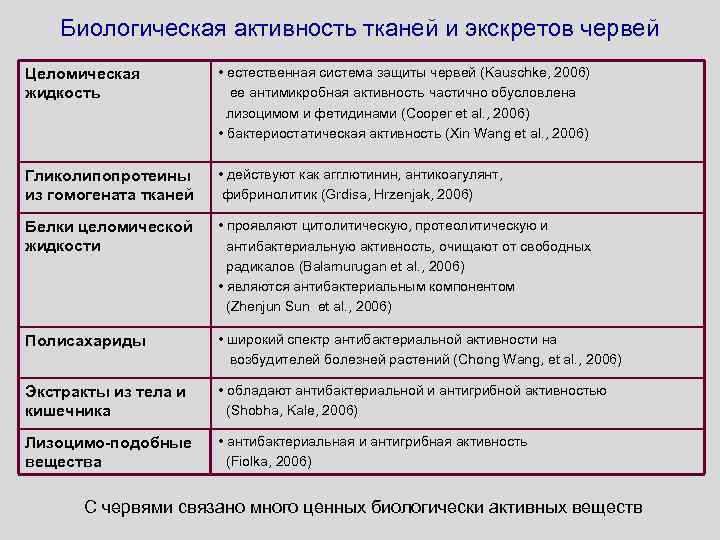 Биологическая активность тканей и экскретов червей Целомическая жидкость • естественная система защиты червей (Kauschke, 2006) ее антимикробная активность частично обусловлена лизоцимом и фетидинами (Cooper et al. , 2006) • бактериостатическая активность (Xin Wang et al. , 2006) Гликолипопротеины из гомогената тканей • действуют как агглютинин, антикоагулянт, фибринолитик (Grdisa, Hrzenjak, 2006) Белки целомической жидкости • проявляют цитолитическую, протеолитическую и антибактериальную активность, очищают от свободных радикалов (Balamurugan et al. , 2006) • являются антибактериальным компонентом (Zhenjun Sun et al. , 2006) Полисахариды • широкий спектр антибактериальной активности на возбудителей болезней растений (Chong Wang, et al. , 2006) Экстракты из тела и кишечника • обладают антибактериальной и антигрибной активностью (Shobha, Kale, 2006) Лизоцимо-подобные вещества • антибактериальная и антигрибная активность (Fiolka, 2006) С червями связано много ценных биологически активных веществ
Биологическая активность тканей и экскретов червей Целомическая жидкость • естественная система защиты червей (Kauschke, 2006) ее антимикробная активность частично обусловлена лизоцимом и фетидинами (Cooper et al. , 2006) • бактериостатическая активность (Xin Wang et al. , 2006) Гликолипопротеины из гомогената тканей • действуют как агглютинин, антикоагулянт, фибринолитик (Grdisa, Hrzenjak, 2006) Белки целомической жидкости • проявляют цитолитическую, протеолитическую и антибактериальную активность, очищают от свободных радикалов (Balamurugan et al. , 2006) • являются антибактериальным компонентом (Zhenjun Sun et al. , 2006) Полисахариды • широкий спектр антибактериальной активности на возбудителей болезней растений (Chong Wang, et al. , 2006) Экстракты из тела и кишечника • обладают антибактериальной и антигрибной активностью (Shobha, Kale, 2006) Лизоцимо-подобные вещества • антибактериальная и антигрибная активность (Fiolka, 2006) С червями связано много ценных биологически активных веществ
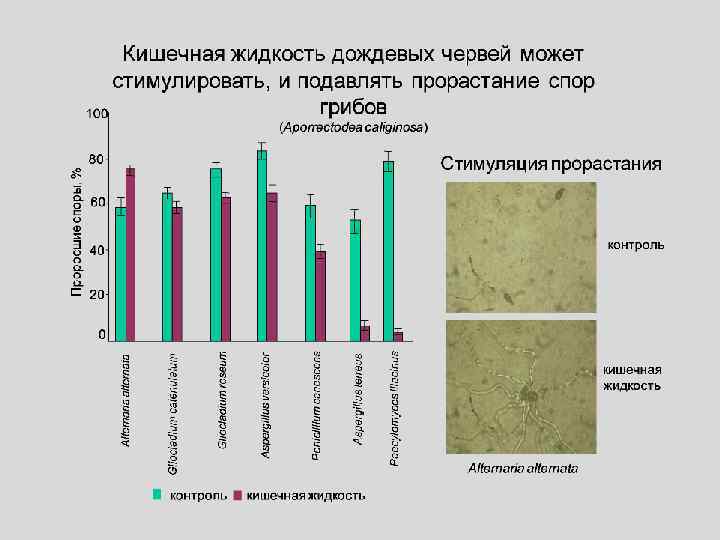
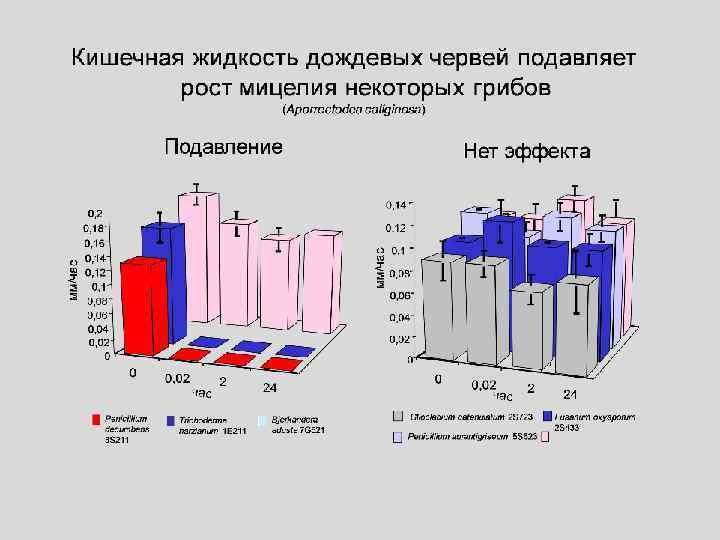
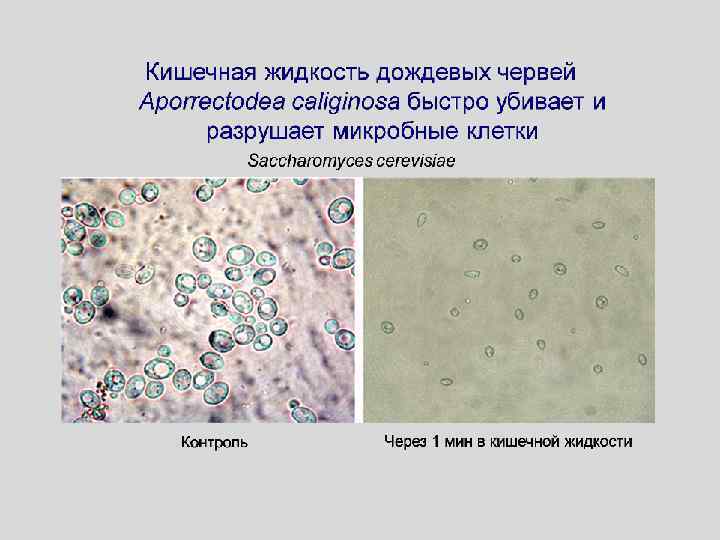
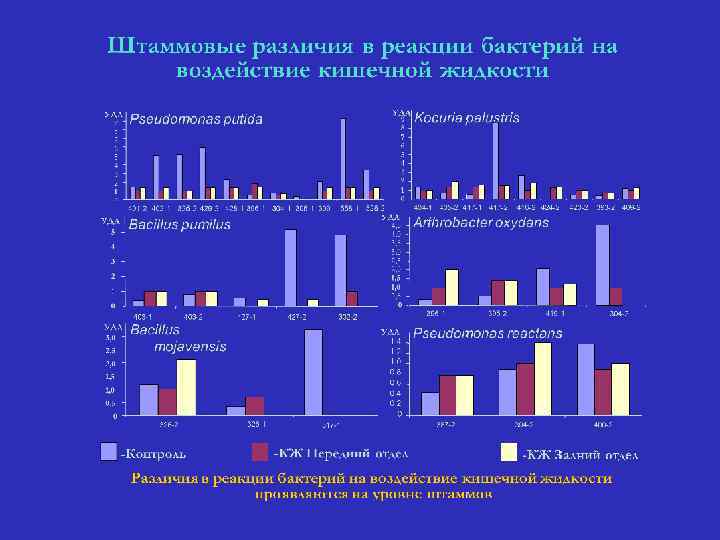
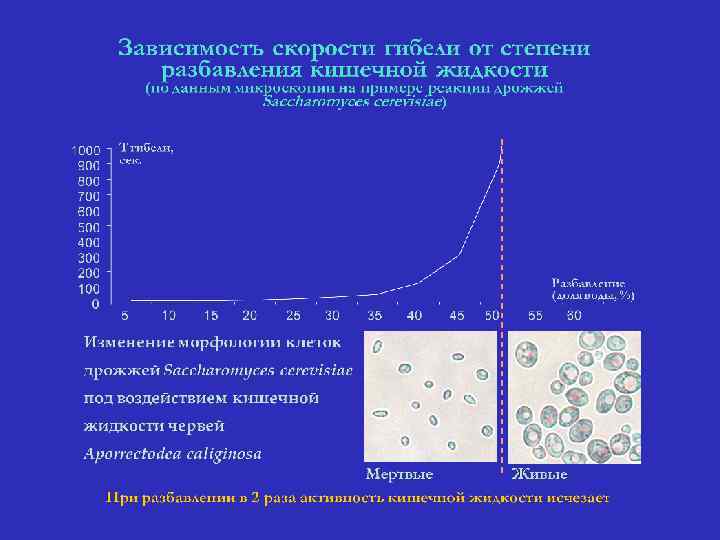


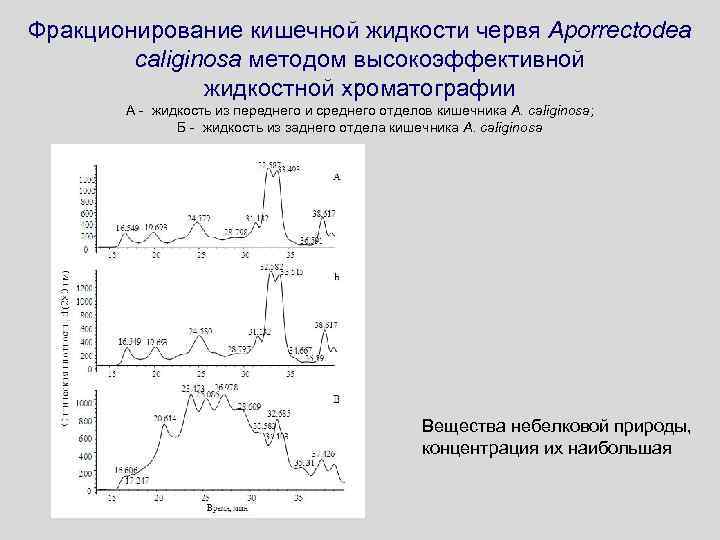 Фракционирование кишечной жидкости червя Aporrectodea caliginosa методом высокоэффективной жидкостной хроматографии А - жидкость из переднего и среднего отделов кишечника A. caliginosa; Б - жидкость из заднего отдела кишечника A. caliginosa Вещества небелковой природы, концентрация их наибольшая
Фракционирование кишечной жидкости червя Aporrectodea caliginosa методом высокоэффективной жидкостной хроматографии А - жидкость из переднего и среднего отделов кишечника A. caliginosa; Б - жидкость из заднего отдела кишечника A. caliginosa Вещества небелковой природы, концентрация их наибольшая
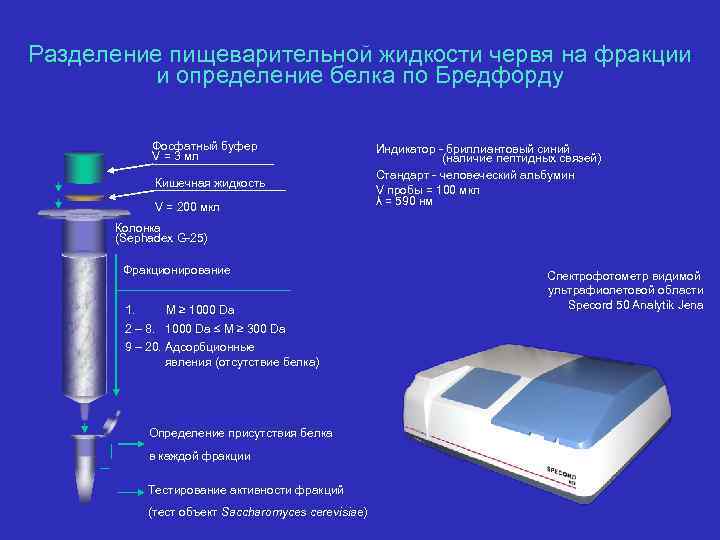 Разделение пищеварительной жидкости червя на фракции и определение белка по Бредфорду Фосфатный буфер V = 3 мл Кишечная жидкость V = 200 мкл Индикатор - бриллиантовый синий (наличие пептидных связей) Стандарт - человеческий альбумин V пробы = 100 мкл λ = 590 нм Колонка (Sephadex G-25) Фракционирование 1. М ≥ 1000 Da 2 – 8. 1000 Da ≤ М ≥ 300 Da 9 – 20. Адсорбционные явления (отсутствие белка) Определение присутствия белка в каждой фракции Тестирование активности фракций (тест объект Saccharomyces cerevisiae) Спектрофотометр видимой ультрафиолетовой области Specord 50 Analytik Jena
Разделение пищеварительной жидкости червя на фракции и определение белка по Бредфорду Фосфатный буфер V = 3 мл Кишечная жидкость V = 200 мкл Индикатор - бриллиантовый синий (наличие пептидных связей) Стандарт - человеческий альбумин V пробы = 100 мкл λ = 590 нм Колонка (Sephadex G-25) Фракционирование 1. М ≥ 1000 Da 2 – 8. 1000 Da ≤ М ≥ 300 Da 9 – 20. Адсорбционные явления (отсутствие белка) Определение присутствия белка в каждой фракции Тестирование активности фракций (тест объект Saccharomyces cerevisiae) Спектрофотометр видимой ультрафиолетовой области Specord 50 Analytik Jena
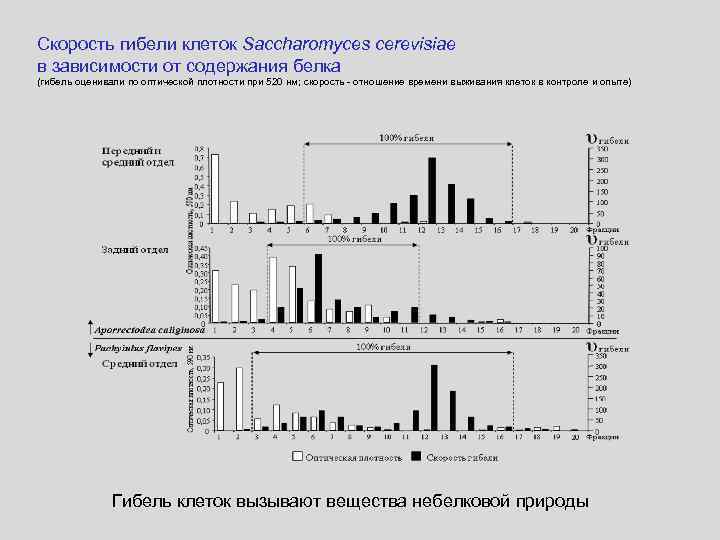 Скорость гибели клеток Saccharomyces cerevisiae в зависимости от содержания белка (гибель оценивали по оптической плотности при 520 нм; скорость - отношение времени выживания клеток в контроле и опыте) Гибель клеток вызывают вещества небелковой природы
Скорость гибели клеток Saccharomyces cerevisiae в зависимости от содержания белка (гибель оценивали по оптической плотности при 520 нм; скорость - отношение времени выживания клеток в контроле и опыте) Гибель клеток вызывают вещества небелковой природы
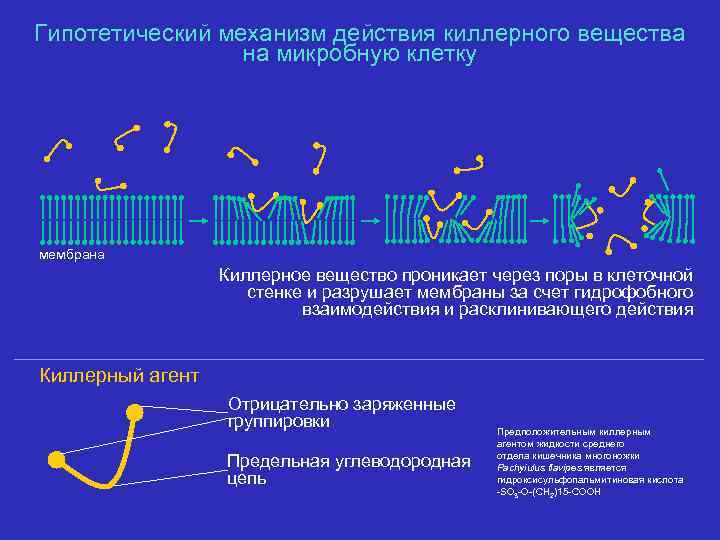 Гипотетический механизм действия киллерного вещества на микробную клетку мембрана Киллерное вещество проникает через поры в клеточной стенке и разрушает мембраны за счет гидрофобного взаимодействия и расклинивающего действия Киллерный агент Отрицательно заряженные группировки Предельная углеводородная цепь Предположительным киллерным агентом жидкости среднего отдела кишечника многоножки Pachyiulus flavipes является гидроксисульфопальмитиновая кислота -SO 3 -O-(CH 2)15 -COOH
Гипотетический механизм действия киллерного вещества на микробную клетку мембрана Киллерное вещество проникает через поры в клеточной стенке и разрушает мембраны за счет гидрофобного взаимодействия и расклинивающего действия Киллерный агент Отрицательно заряженные группировки Предельная углеводородная цепь Предположительным киллерным агентом жидкости среднего отдела кишечника многоножки Pachyiulus flavipes является гидроксисульфопальмитиновая кислота -SO 3 -O-(CH 2)15 -COOH