Л2_Пищевая химия.ppt
- Количество слайдов: 75

ПИЩЕВАЯ ХИМИЯ КУРС ЛЕКЦИЙ

БЕЛКОВЫЕ ВЕЩЕСТВА В ПРОДОВОЛЬСТВЕННОМ СЫРЬЕ

Содержание лекции Белки в питании человека. p Классификация белков. p Аминокислотный состав белков. p Свойства белков. p Превращения белков при производстве продуктов питания. p Денатурация белков. p Гидролиз белков. p Пенообразование белков. p

Содержание лекции p p p Основные виды белкового пищевого сырья. Белки семян растений. Белки злаков. Белки бобовых культур. Белки масличных культур. Белки картофеля, овощей и плодов. Белки мяса. Белки рыбы. Белки молока. Новые формы белковых веществ. Ферменты и ингибиторы белковой природы. Небелковые азотистые вещества.
Структурная Ферментативная Транспортная Резервная Функции белков Гормональная Защитная Сократительная

Биологическая ценность белков определяется сбалансированностью аминокислотного состава по содержанию незаменимых аминокислот, которые не синтезируются в организме человека. p К незаменимым аминокислотам относят: валин, лейцин, изолейцин, фенилаланин, лизин, треонин, метионин, триптофан. Аминокислоты аргинин и гистидин относятся к частично заменимым, так как они медленно синтезируются организмом человека. p

Биологическая ценность белков p p p Аминокислотный скор выражается в процентах, представляющих отношение содержания незаменимой аминокислоты в исследуемом белке продукта к ее количеству в эталонном белке. Аминокислотный состав эталонного белка сбалансирован и идеально соответствует потребностям человека в каждой незаменимой аминокислоте. Аминокислота, скор которой имеет самое низкое значение, называется первой лимитирующей аминокислотой. Например, в белке пшеницы лимитирующей является аминокислота лизин, в кукурузе – метионин, в картофеле и бобовых культурах лимитирующими являются метионин и цистин – это серосодержащие аминокислоты.

Сравнительный анализ белков растительного и животного происхождения Белки растительного происхождения Полноценные. Близки к аминокислотному составу белков человека. Неполноценные. Содержат пониженное содержание лизина, триптофана, треонина, метионина, цистина. Имеют высокую степень усвояемости – 90 -95%. Имеют меньшую степень усвояемости – 60 -80%. Суточная потребность – 60 -100 г Суточная потребность – 40 -60 г Сравнительная биологическая ценность белков характеризуется следующими цифрами: белки молока – 100 единиц (условно), белки мяса и рыбы – 90, картофеля – 80, овса, ржаного хлеба – 75, гороха – 55, пшеницы – 50.

p p Белковый минимум – минимальное количество белков в рационе, которое обеспечивает азотистое равновесие при диете, которая удовлетворяет энергетические потребности организма. Уровень белкового минимума зависит от физиологических особенностей организма, возраста, профессии, количества белков и небелковых компонентов пищи. У взрослого практически здорового человека азотистое равновесие сохраняется при поступлении ежесуточно с едой 55 -60 г белков, биологическая ценность которых составляет 70%. Однако при определенных условиях белковый минимум может привести к негативному азотистому балансу. В связи с этим разработаны рекомендованные нормы суточной потребности в белках, которые составляют в среднем 1 г белков на 1 кг массы тела или 85 -100 г в сутки. Для детей рекомендованы нормы белков 1, 5 – 4 г на 1 кг массы тела.

p p p Таблица 2. Суточная потребность в белке Возрастная группа Количество общего белка, г В т. ч. животный белок, г Дети, возраст: 1– 3 25213– 7 48397– 11 684811– 15 9856 Подростки: 11972 Взрослые: Умственный труд 10967 Физический труд (легкий)12272 Физический труд (тяжелый)16394

КЛАССИФИКАЦИЯ БЕЛКОВ

Белковыми веществами называются высокомолекулярные органические соединения, молекулы которых состоят из остатков различных α-аминокислот, соединенных пептидной связью (- СО – NН -), которая образуется за счет карбоксильной группы первой аминокислоты и αаминогруппы второй аминокислоты. p Большинство белков имеют следующий элементный состав (%): углерод 50 -54, азот 1518, кислород 20 -25, водород 6 -8, сера 0, 3 -2, 5. p

Пептиды, полипептиды и белки Пептиды – соединения, включающие до 10 аминокислот, связанных пептидной связью (молекулярная масса до 1000). p Полипептиды – соединения, включающие до 40 аминокислот, связанных пептидной связью (молекулярная масса до 4000). p Белки – соединения, включающие до 40 аминокислот, связанных пептидной связью (молекулярная масса от 5000 до нескольких миллионов). p 13

Классификация аминокислот p p p p По строению радикалов (алифатические, ароматические и гетероциклические) По числу функциональных групп (моноаминомонокарбоновые и т. п. ) По взаимному положению функциональных групп: α, β, γ, δ По химическим свойствам R-групп (неполярные, отрицательно и положительно заряженные) По химическому составу входящих в радикал групп (гидроксимонокислоты, серосодержащие) По оптической активности (D- и L-формы) По способности синтезироваться в живых организмах (заменимые, незаменимые)

Классификация белков по строению пептидной цепочки p по ориентации белковой молекулы в пространстве p по степени растворимости белка p по форме белковой молекулы p по строению белковой молекулы p по наличию небелковых веществ p

Классификация по ориентации белковой молекулы в пространстве p первичная структура - соединение аминокислот в простейшую линейную цепь за счет только пептидных связей p вторичная структура - пространственное расположение полипептидой цепи в виде ά - спирали или β - складчатой структуры. p третичная структура - специфическое укладывание ά - спирали в виде глобул. p четвертичная структура - соединение нескольких глобул, находящихся в состоянии третичной структуры, в одну укрупненную структуру, обладающую новыми свойствами, не характерными для отдельных глобул.
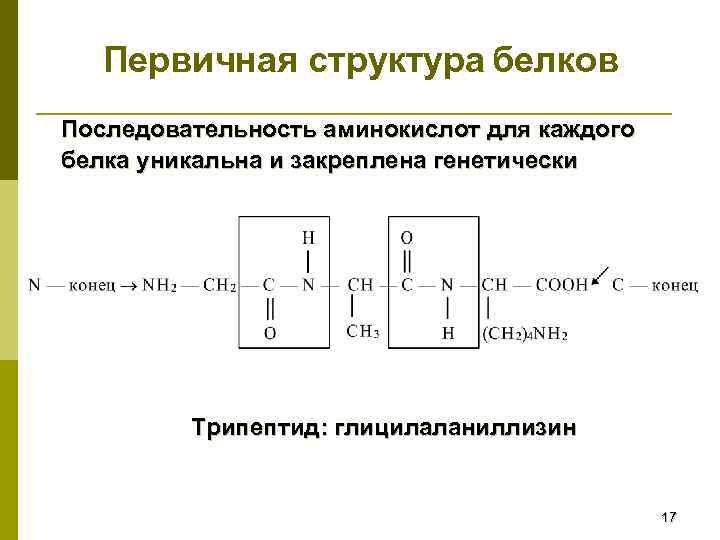
Первичная структура белков Последовательность аминокислот для каждого белка уникальна и закреплена генетически Трипептид: глицилаланиллизин 17
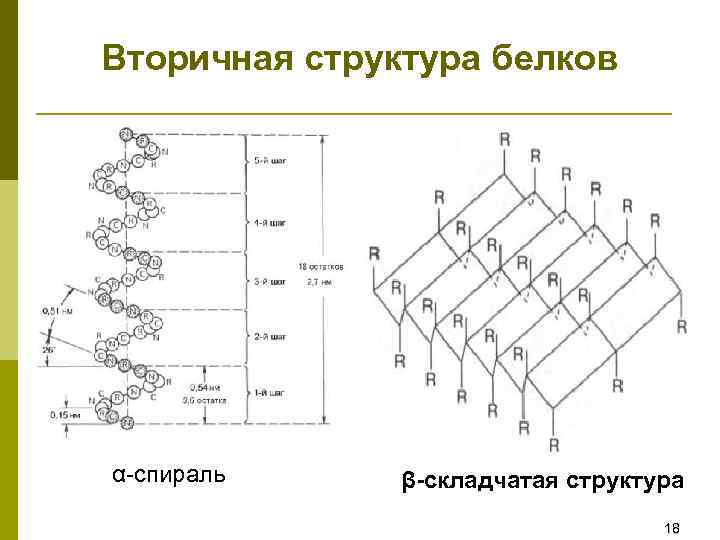
Вторичная структура белков α-спираль β-складчатая структура 18
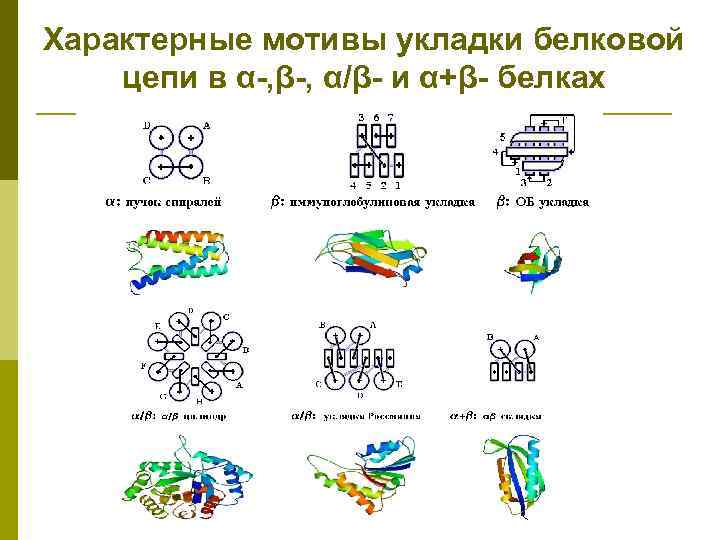
Характерные мотивы укладки белковой цепи в α-, β-, α/β- и α+β- белках
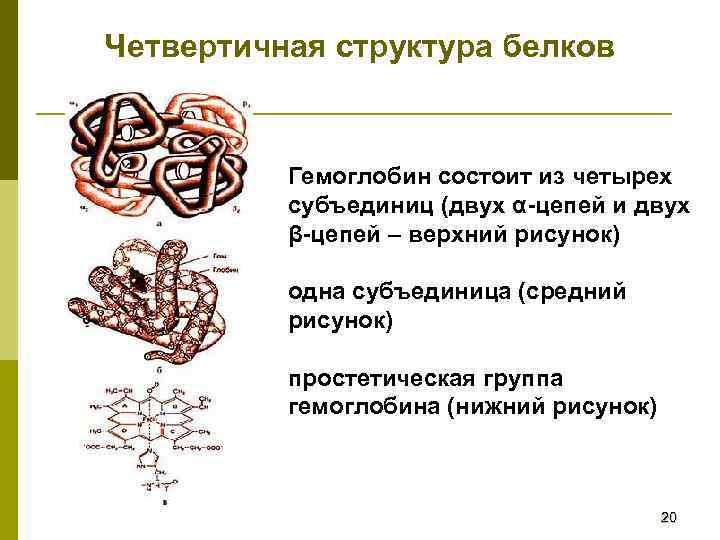
Четвертичная структура белков Гемоглобин состоит из четырех субъединиц (двух α-цепей и двух β-цепей – верхний рисунок) одна субъединица (средний рисунок) простетическая группа гемоглобина (нижний рисунок) 20

Классификация по степени растворимости белка Водорастворимые белки имеют небольшую молекулярную массу, их представляют альбумины яйца. p Солерастворимые белки растворяются в 10 % растворе хлорида натрия, их представляют глобулины: белок молока казеин, белок крови глобулин. p Щелочерастворимые белки растворяются в 0, 2 % растворе гидроксила натрия, их представляют глютелины: белок клейковины пшеницы. p Спирторастворимые белки растворяются в 60 -80 % спирте, их представляют проламины: белки злаковых культур. p

Классификация белков по форме молекул p Фибриллярные белки – расположенные параллельно другу вытянутые полипептидные цепи, образующие длинные нити или слои (фибриллы). p Глобулярные белки – белки, в молекулах которых полипептидные цепи плотно свёрнуты в компактные шарообразные структуры – глобулы (третичные структуры белка).

Сложные белки – соединения, состоящие из белка и небелковой (простетической) части. p В качестве простетической группы выступают: углеводы, липиды, ионы металлов, нуклеиновые кислоты, фосфорная кислота. p Сложные белки биологически активны лишь находясь в комплексе друг с другом. p 23
Липопротеиды Нуклеопротеиды Фосфопротеиды Сложные белки Гликопротеиды Хромопротеиды

ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА БЕЛКОВ
Растворимость Пенообразование Гидратация Свойства белки Гидролиз Денатурация Гелеобразование

Реакции осаждения белков p p p Обратимые реакции осаждения не приводят к глубоким изменениям структуры белка, поэтому получаемые осадки могут быть вновь растворены в первоначальном растворителе. Белки при этом сохраняют свои начальные нативные, включая биологические, свойства. Необратимые реакции вызывают глубокие изменения структуры белка, поэтому получаемые осадки не могут быть растворены в первоначальных растворителях. Наступает денатурация белка. Денатурацией называют такое изменение белка, при котором он утрачивает свои естественные биологические и физико-химические свойства, становится менее гидрофильным и теряет способность растворяться в воде.

Реакции осаждения белков Для осаждения белка нужно лишить его факторов, удерживающих белок в растворе, используя различные агенты, снижающие заряд или разрушающие гидратную оболочку белковой частицы. p Практическое значение реакций осаждения белков состоит в том, что они дают возможность: 1) изучить свойства белков 2) освободить жидкость от присутствия белка 3) установить наличие белка в анализируемом объекте 4) разделить отдельные белковые фракции на альбумины и глобулины p

Изоэлектрическая точка белков p p Изоэлектрической точкой белка называется определенная величина р. Н среды, при которой белок находится в виде нейтральных молекул (в изоэлектрическом состоянии), несущих равные количества положительных и отрицательных зарядов. Растворы белков в изоэлектрической точке наименее устойчивы и легко выпадают в осадок. Для большинства белков изоэлектрическая точка близка к нейтральной среде, но не вполне совпадает с ней; она сдвинута в кислую или щелочную сторону (ИЭТ 5, 5 -7, 2).

Денатурация белков p p Процесс изменения пространственной структуры белка под влиянием внешних факторов: нагревание, механическое воздействие, химическое воздействие, физическое воздействие и т. д. При денатурации распадается четвертичная, третичная, вторичная структура белка, но сохранятся первичная структура и не изменяется химический состав белка. При денатурации меняются физические свойства белка: снижается растворимость и водосвязывающая способность, теряется биологическая активность белка. Одновременно увеличивается активность некоторых химических групп, облегчается ферментативный гидролиз белка. При технологической переработке сырья (очистка, перемешивание, варка, обработка химическими реагентами, использование вакуума или повышенного давления) белки подвергаются денатурации, что повышает степень их усвоения.
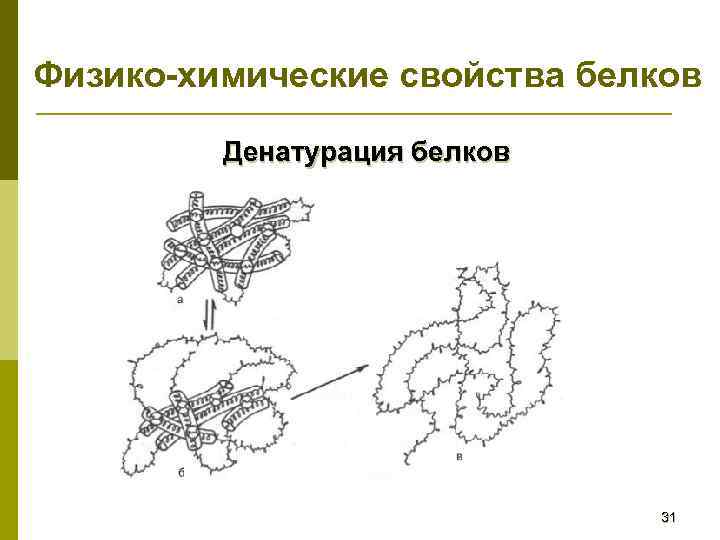
Физико-химические свойства белков Денатурация белков 31

При денатурации белков происходят следующие основные изменения: p p p p резко снижается растворимость белков; теряется биологическая активность, способность к гидратации и видовая специфичность; улучшается атакуемость протеолитическими ферментами; повышается реакционная способность белков; происходит агрегирование белковых молекул; заряд белковой молекулы равен нулю. Потеря белками биологической активности в результате тепловой денатурации приводит к инактивации ферментов и отмиранию микроорганизмов.

p p p Тепловая денатурация белков является одним из основных физико-химических процессов, лежащих в основе выпечки хлеба, печенья, бисквитов, пирожных, сухарей, сушки макаронных изделий, получения экструдатов и сухих завтраков, варки, жарения овощей, рыбы, мяса, консервирования, пастеризации и стерилизации молока. Данный вид превращений относится к полезным, так как он ускоряет переваривание белков в желудочно-кишечном тракте человека (облегчая доступ к ним протеолитических ферментов) и обусловливает потребительские свойства пищевых продуктов (текстуру, внешний вид, органолептические свойства). В связи с тем, что степень денатурации белков может быть различной (от незначительной до полного изменения расположения пептидных цепей с образованием новых ковалентных –S–Sсвязей), то и усвояемость белков может не только улучшаться, но и ухудшаться.

Водосвязывающая способность (гидратация) p p p Белки способны связывать воду, то есть проявляют гидрофильные свойства. При этом белки набухают, увеличивается их масса и объем. В процессе технологической переработки сырья происходит связывание воды, продукты увеличиваются в объеме – набухают. Высокая способность белков удерживать воду в пищевых продуктах (мясных, хлебобулочных и т. д. ) повышает выход последних, удлиняет сроки хранения и улучшает текстуру.
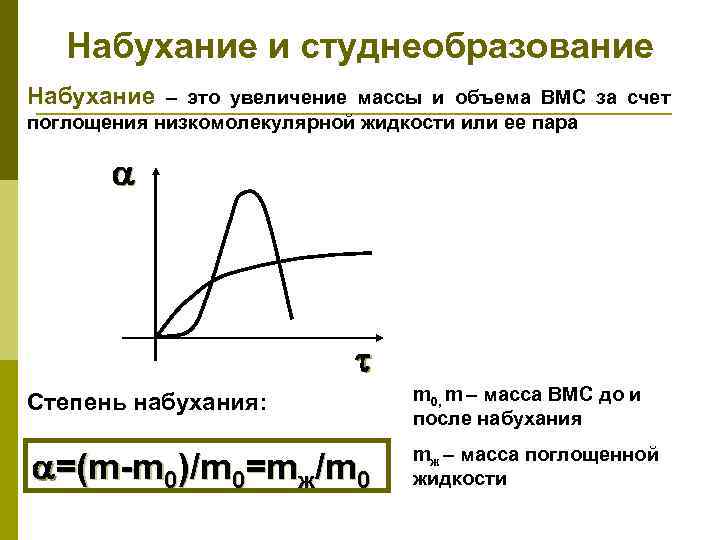
Набухание и студнеобразование Набухание – это увеличение массы и объема ВМС за счет поглощения низкомолекулярной жидкости или ее пара Степень набухания: m 0, m – масса ВМС до и после набухания =(m-m 0)/m 0=mж/m 0 mж – масса поглощенной жидкости

Кинетика набухания Скорость набухания Константа набухания Процесс набухания частиц муки включает две стадии: 1. Адсорбция воды мицеллами белка и крахмальными зернами ( Б = 30%, кр = 10% ) 2. Диффузия воды внутрь мицелл белка и крахмальных зерен ( Б = 200 -220%, кр = 20 -30%)
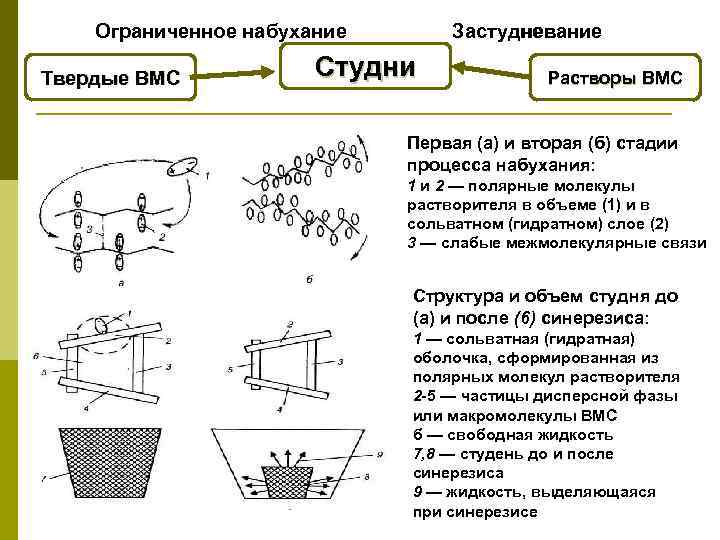
Ограниченное набухание Твердые ВМС Застудневание Студни Растворы ВМС Первая (а) и вторая (б) стадии процесса набухания: 1 и 2 — полярные молекулы растворителя в объеме (1) и в сольватном (гидратном) слое (2) 3 — слабые межмолекулярные связи Структура и объем студня до (а) и после (6) синерезиса: 1 — сольватная (гидратная) оболочка, сформированная из полярных молекул растворителя 2 -5 — частицы дисперсной фазы или макромолекулы ВМС б — свободная жидкость 7, 8 — студень до и после синерезиса 9 — жидкость, выделяющаяся при синерезисе

Гелеобразование p p p Гелеобразующие свойства белков характеризуются способностью перехода из свободнодисперсного состояния в связнодисперсное. Белок как гелеобразователь должен образовывать гели в широком диапазоне р. Н, при минимальной концентрации и с необходимыми физико-химическими свойствами (прочность, твердость, эластичность, температура размягчения и плавления, степень набухания, способность к синерезису и др. ) К подобного рода «универсальным» гелеобразователям относится желатин, позволяющий в широких пределах обеспечить регулирование химического состава и биологическую ценность пищевых продуктов.

Реологические свойства p p Отличительным свойством некоторых пищевых белков является низкий уровень полярности функциональных групп. Молекулы воды, окружая частицы белков, отталкиваются, а молекулы белков, наоборот, агрегируются с образованием комплексов с присущими им реологическими свойствами (вязкость, эластичность, упругость). Наиболее выраженным комплексом таких свойств обладают белки пшеничной клейковины, обуславливающие текстуру хлеба и создающие непрерывную фазу в изделиях с наполнителями (зерно, отруби, изюм). За свойство упругости и эластичности белков ответственность несет глютениновая фракция белков.

Пенообразование p p Белки способны образовывать высококонцентрированные системы жидкость – газ, твердое тело – газ в виде пены. Белки выполняют функцию пенообразователей в кондитерской промышленности (суфле, пастила), в хлебопечении, в производстве пива. Поверхность газовых пузырьков покрывает жидкая или твердая оболочка, состоящая из белков. При истончении этой оболочки газовые пузырьки лопаются, происходит коалесценция или слияние пузырьков, пена становится рыхлой, менее стойкой. Устойчивость структуры пены является важным фактором повышения качества пищевых продуктов, в том числе и пива.
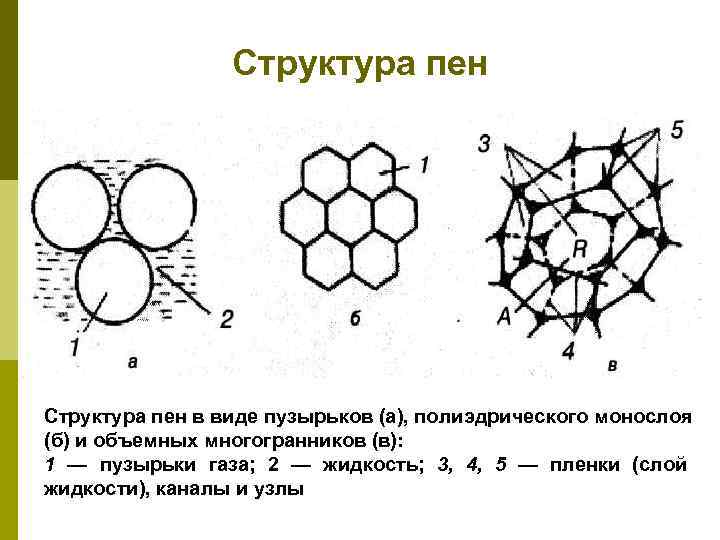
Структура пен в виде пузырьков (а), полиэдрического монослоя (б) и объемных многогранников (в): 1 — пузырьки газа; 2 — жидкость; 3, 4, 5 — пленки (слой жидкости), каналы и узлы

Пенообразование p p p Пены (дисперсные системы с газообразной фазой и жидкой или твердой средой) получают механическим распределением воздуха в растворе белка путем взбивания или за счет вскипания воды, понижения давления, обеспечения химических или микробиологических процессов в белоксодержащих пищевых системах. Пенообразующие свойства белков характеризуются пенообразующей способностью и стабильностью пены. Эти показатели зависят от р. Н среды, концентрации белка, солей, температуры, присутствия липидов, сахарозы, пищевых волокон, фракционного состава и строения белков.

Гидролиз белков p p Гидролиз – распад сложного вещества на более простые составные части, связанный с присоединением воды в месте разрыва связей. В зависимости от применяющегося катализатора, различают кислотный, щелочной и ферментативный гидролиз. При гидролизе простого белка конечными продуктами являются аминокислоты. В организме гидролиз белка постоянно протекает в процессе как пищеварения, так и в ходе жизнедеятельности клеток под действием протеолитических ферментов.

Гидролиз белков p p p При кислотном гидролизе белка разрушаются некоторые аминокислоты (триптофан подвергается полному разрушению, серин, треонин, цистин, тирозин, фенилаланин – частичному). При кислотном гидролизе белки распадаются сначала на высокомолекулярные пептиды, а затем – на низкомолекулярные пептиды, дипептиды и аминокислоты. При щелочном гидролизе отмечается значительно более сильное разрушение аминокислот.

Ферментативный гидролиз белков p p p Пепсин расщепляет связь между фенилаланином и тирозином, глутаминовой кислотой и цистином (метионином, глицином), между валином и лейцином. Трипсин расщепляет связь между аргинином (лизином) и другими аминокислотами. Химотрипсин – между ароматическими аминокислотами (триптофан, тирозин, фенилаланин) и метионином. Аминопептидазы действуют со стороны N – концевой аминокислоты, карбоксипептидазы со стороны С – концевой аминокислоты. Эндопептидазы разрушают белок внутри молекулы, экзопептидазы – действуют с конца молекулы.

Меланоидинообразование (реакция Майяра) p p p При взаимодействии аминогрупп белков и аминокислот с карбонильными группами углеводов происходит реакция меланоидинообразования. Это окислительно-восстановительный процесс с образованием различных промежуточных продуктов, конечные продукты реакции – меланоидины имеют коричневый цвет, влияют на цвет и вкус готовых продуктов. Реакция Майяра происходит при сушке солода, при кипячении сусла с хмелем, выпечке хлеба, варке сахарных сиропов, переработке овощей и фруктов. Скорость и глубина реакции меланоидинообразования зависит от состава продукта, уровня р. Н среды, температура, влажность.

Вопросы 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. Перечислите функции белков в организме. Дайте определение аминокислоты, пептида, белка. По каким основаниям классифицируют аминокислоты? Перечислите незаменимые аминокислоты. Как связаны между собой аминокислоты в молекуле белка? По каким основаниям классифицируют белки? Приведите примеры белков, относящихся к различным группам. Перечислите структурные уровни белков. Какие существуют дополнительные связи, сохраняющие пространственную конфигурацию молекулы белка? Дайте определение глобулярным и фибриллярным белкам.

Вопросы 1. 2. 3. 4. 5. 6. 7. 8. 9. Почему белки заметно отличаются по растворимости? От чего зависит заряд белка в водном растворе? От чего зависит растворимость белка? Какие факторы стабилизируют белок в растворе? Каковы общие механизмы осаждения белка из раствора? Какими способами можно осадить белок, не вызывая его денатурацию? Что такое изоэлектрическая точка, и как ее определить? Что такое высаливание белка? Что такое денатурация белка? Какие агенты, денатурирующие белки, Вам известны? В чем заключается разница между осаждением и денатурацией? Назовите мероприятия при отравлении человека солями тяжелых металлов, основанные на необратимых реакциях осаждения белка.

Вопросы 1. 2. 3. 4. 5. Каким образом проявляются гидрофильные свойства белков? Что такое гидролиз белка, и какие виды гидролиза Вы знаете? С чем связана пенообразующая способность белков? Дайте характеристику реакции меланоидинообразования. Каким образом знание физико-химических свойств белков учитывается в технологиях переработки белоксодержащего сырья?

БЕЛКИ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ

Белки злаковых культур p p Среднее содержание белков в злаках составляет от 7 до 17%. Причем наибольшее количество белка содержится в пшенице, наименьшее количество белка – в рисе и кукурузе (7 – 9%). Белки неравномерно распределяются между морфологическими частями зерна. Основное их количество приходится на эндосперм (65 – 75%); на зародыш до 22%, на алейроновый слой до 15, 5%.
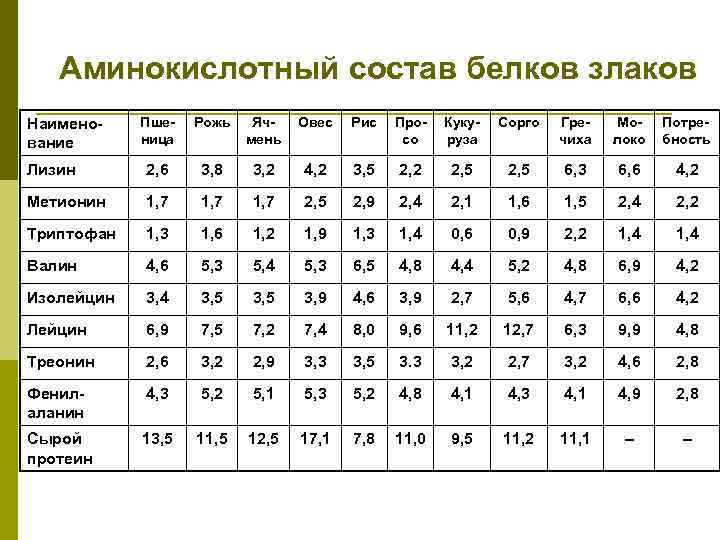
Аминокислотный состав белков злаков Пшеница Рожь Ячмень Овес Рис Просо Кукуруза Сорго Гречиха Молоко Потребность Лизин 2, 6 3, 8 3, 2 4, 2 3, 5 2, 2 2, 5 6, 3 6, 6 4, 2 Метионин 1, 7 2, 5 2, 9 2, 4 2, 1 1, 6 1, 5 2, 4 2, 2 Триптофан 1, 3 1, 6 1, 2 1, 9 1, 3 1, 4 0, 6 0, 9 2, 2 1, 4 Валин 4, 6 5, 3 5, 4 5, 3 6, 5 4, 8 4, 4 5, 2 4, 8 6, 9 4, 2 Изолейцин 3, 4 3, 5 3, 9 4, 6 3, 9 2, 7 5, 6 4, 7 6, 6 4, 2 Лейцин 6, 9 7, 5 7, 2 7, 4 8, 0 9, 6 11, 2 12, 7 6, 3 9, 9 4, 8 Треонин 2, 6 3, 2 2, 9 3, 3 3, 5 3. 3 3, 2 2, 7 3, 2 4, 6 2, 8 Фенилаланин 4, 3 5, 2 5, 1 5, 3 5, 2 4, 8 4, 1 4, 3 4, 1 4, 9 2, 8 Сырой протеин 13, 5 11, 5 12, 5 17, 1 7, 8 11, 0 9, 5 11, 2 11, 1 – – Наименование

Аминокислотный состав белков различных злаковых культур p p Наиболее сбалансированными по аминокислотному составу являются овес и гречиха. Все злаки, за исключением гречихи и овса, бедны лизином (2, 2 – 3, 3%), а за исключением риса, гречихи и сорго – изолейцином. Для белков пшеницы, сорго, ячменя и ржи характерно относительно небольшое количество метионина (1, 6 – 1, 7 мг/100 г белка). Белки пшеницы содержат недостаточное количество треонина (2, 6%), а белки кукурузы – триптофана (0, 6%).
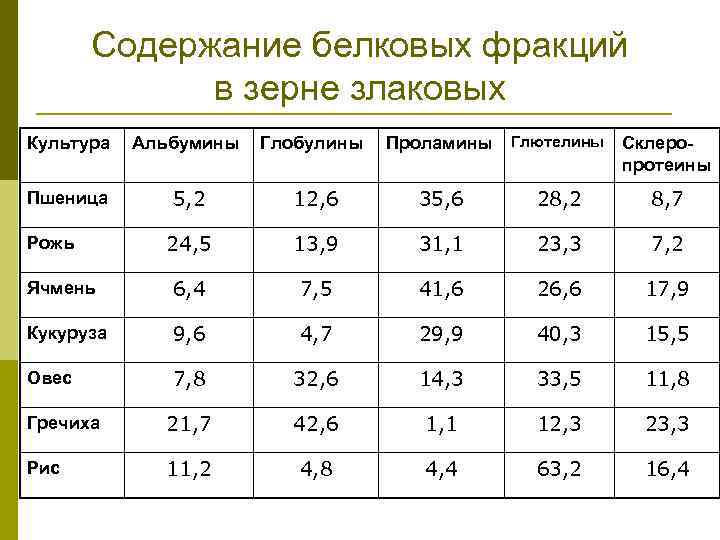
Содержание белковых фракций в зерне злаковых Культура Альбумины Глобулины Проламины Глютелины Склеропротеины Пшеница 5, 2 12, 6 35, 6 28, 2 8, 7 24, 5 13, 9 31, 1 23, 3 7, 2 Ячмень 6, 4 7, 5 41, 6 26, 6 17, 9 Кукуруза 9, 6 4, 7 29, 9 40, 3 15, 5 Овес 7, 8 32, 6 14, 3 33, 5 11, 8 Гречиха 21, 7 42, 6 1, 1 12, 3 23, 3 Рис 11, 2 4, 8 4, 4 63, 2 16, 4 Рожь
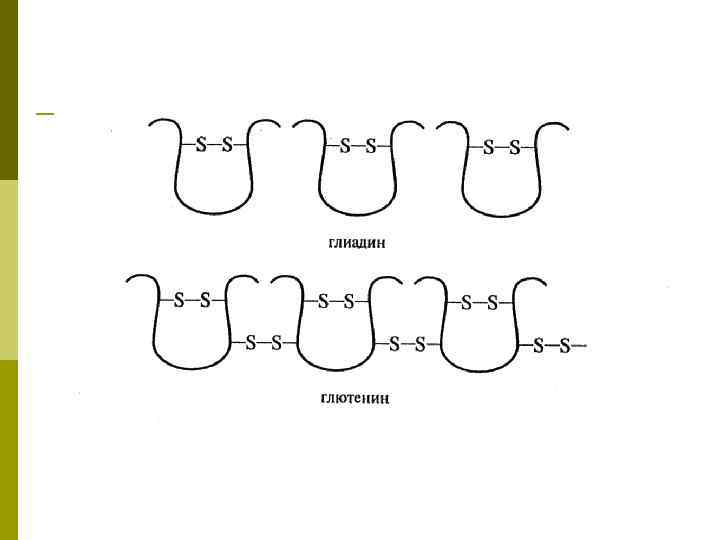

Реологические свойства белков клейковины пшеницы p p p Наиболее выраженное влияние на реологические свойства клейковины оказывают присутствие высокомолекулярных субъединиц глютенина (100 к. Д) или соотношение высоко- и низкомолекулярных субъединиц. Всего обнаружено около 25 субъединиц с высокой молекулярной массой, 3 – 5 из них присутствует в каждом сорте. Реологические свойства клейковины и качество пшеничного хлеба зависят также от полиморфизма глютенина и глиадина, количества белка и активности α-амилазы. Глютенин придает клейковине упругие свойства, а глиадин обуславливает растяжимость и связность, то есть ни глютенин, ни глиадин в отдельности не обладают характерными реологическими свойствами клейковины, только взаимодействие этих фракций в едином комплексе создает клейковинный белок со всеми присущими ему особенностями.

p p p На качество клейковины большое влияние оказывают вещества, содержащие сульфгидрильные группы, – SH (цистеин, глютатион и др. ). Эти вещества при добавлении их в небольшом количестве к муке или к тесту резко ухудшают качество клейковины и теста, вызывают их расплывание и разжижение. Например, глютатион оказывает на клейковину сильное разжижающее действие – клейковина и тесто расплываются и ослабевают. Качество клейковины зависит также от действия протеолитических ферментов. Под их влиянием клейковина теряет свои первоначальные физические свойства, разжижается и иногда становится неотмываемой.

p p p Огромное значение для изменения свойств и агрегативного состояния белков в ходе технологического процесса приготовления теста имеет дисульфидно-сульфгидрильный обмен: P 1 S SP 2 + P 3 SH P 1 S SP 3 + P 2 SH Считают, что лабильность дисульфидных связей обеспечивает образование новых прочных межмолекулярных связей и релаксацию (ослабление) напряжения структур клейковины при замесе теста. Сильная мука, содержащая крепкую клейковину, требует дльше времени замеса, так как она содержит больше дисульфидных связей и меньше SH-групп, чем слабая. В процессе созревания муки при ее отлежке, а также под влиянием окислителей типа броматов, улучшение реологических свойств клейковины объясняется увеличением содержания S–S-связей и уменьшением, соответственно, SH-групп. В присутствии восстанавливающих агентов (сульфит натрия) реологические свойства клейковины ухудшаются, как это имеет место в прорастающем зерне или в процессе приготовления теста из зерна, пораженного клопом-черепакой. Во всех случаях показатели качества и реологические характеристики теста взаимосвязаны с изменением в соотношении S–S-связей и SH-групп в белках. В результате действия протеолетических ферментов в технологическом потоке производства пищевых продуктов белковые вещества так же претерпевают ряд существенных изменений. Так, на стадии солодоращения при производстве пива в эндосперме ячменя наблюдается гидролиз глобулина (эдестин), альбумина (лейкозин), проламина (гордеин) и глютелина с накоплением азотистых соединений с более низкой молекулярной массой (пептиды, аминокислоты). В результате в зерне накапливается растворимая, коагулируемая и аминная формы азота, тогда как в зародышевом листке и ростках зерна, наоборот, увеличивается количество белкового азота за счет процессов синтеза.

p p Глютатион оказывает большое влияние на активность ферментов, особенно тех, действие которых связано с превращениями белков. Окисленный глютатион изображают сокращенно Г–S–S–Г, восстановленный –Г–SH. Свойства белков созревающего и прорастающего зерна связаны с содержанием –S–S– связей и –SH -групп. При хорошем качестве клейковины соотношение Г–S–S–Г/Г–SH высокое. При прорастании зерна дисульфидные связи распадаются с одновременным увеличением сульфгидрильных групп и ослаблением качества клейковины.
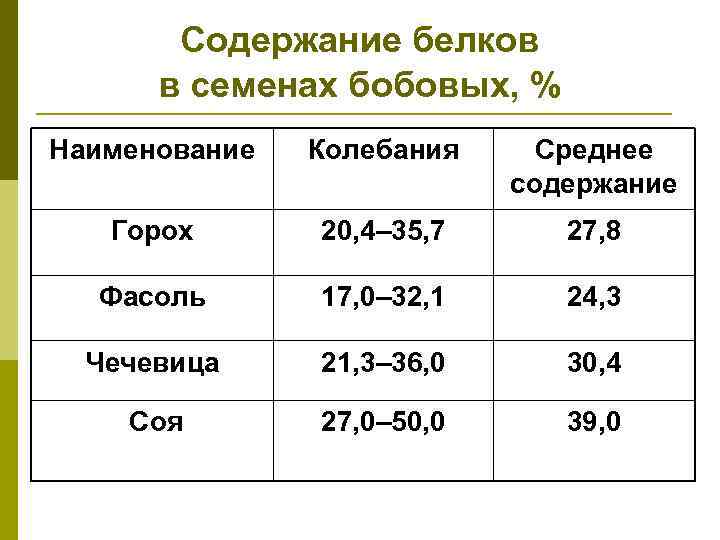
Содержание белков в семенах бобовых, % Наименование Колебания Среднее содержание Горох 20, 4– 35, 7 27, 8 Фасоль 17, 0– 32, 1 24, 3 Чечевица 21, 3– 36, 0 30, 4 Соя 27, 0– 50, 0 39, 0

p p p Проламиновая фракция в белках семян бобовых отсутствует. Основная фракция – глобулины. Наименьшее количество приходится на долю глютелинов. Альбуминов немного больше, чем глютелинов. В семенах бобовых найдены отдельные, характерные для той или другой культуры белки – в семенах гороха глобулин легумин и вицилин, в семенах фасоли – глобулин фазеолин, в семенах сои – глобулин глицинин.

p p p Несмотря на количественные расхождения, аминокислотный состав семян бобовых имеет много общего, аспарагиновая и особенно глютаминовая кислоты содержатся в наибольшем количестве, в наименьшем – цистин, метионин и триптофан. Белки семян бобовых бедны серосодержащими аминокислотами. Многие незаменимые аминокислоты содержатся в значительных количествах.

Белки семян масличных культур p p p Большинство масличных культур (подсолнечник, арахис, рапс, хлопчатник, кунжут) по содержанию белков не уступает бобовым культурам. Большая часть белков масличных семян относится к глобулиновой фракции (80 – 90%). Альбуминовая и глютелиновая фракции находятся примерно на одинаковом уровне (5 – 10%). Проламины практически отсутствуют. Для обогащения пищевых продуктов используют выделенные белковые концентраты и изоляты.

p p При использовании отходов, получаемых при производстве растительного масла, большое значение приобретает изменение белковых веществ в результате промышленной переработки маслосемян. Влажно-тепловая обработка измельченных масличных семян вызывает тепловую денатурацию белковых веществ, что приводит к изменению их растворимости. Одновременно проходят реакции взаимодействия сахаров с белковыми веществами (меланоидинообразование), что приводит к уменьшению количества сахаров и незаменимых аминокислот. Так, содержание лизина при обработке шрота уменьшается на 15 -30%.
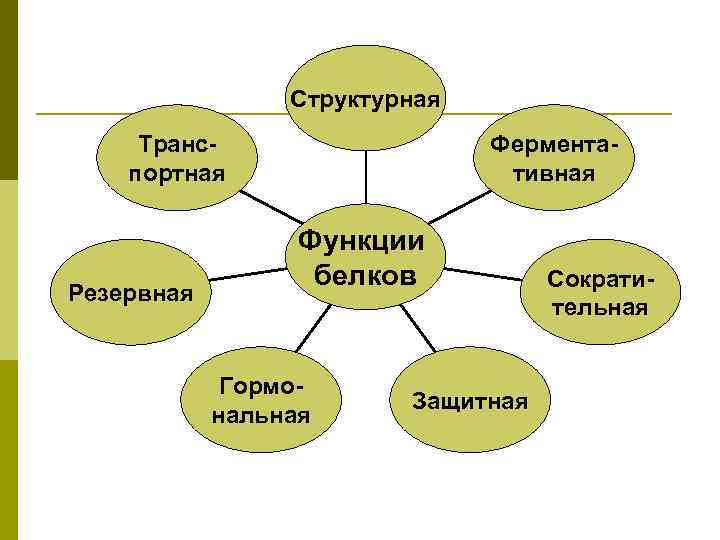
Структурная Ферментативная Транспортная Резервная Функции белков Гормональная Защитная Сократительная

p p В технологических процессах производства белковых продуктов из сои предусматривается инактивация ингибиторов протеиназ обработкой паром, микроволновым нагревом, вымачиванием с последующим кипячением и другими способами. Инактивация ингибиторов трипсина на 80 – 90% по сравнению с их активностью в исходном сырье уже позволяет отнести белковые продукты к пищевым, не обладающим отрицательном воздействием на организм.

p p В целом овощи характеризуются низким содержанием белков. Больше всего их в зеленом горошке – в среднем 5, 0%, в овощной фасоли – 4, 0, шпинате – 2, 9, цветной капусте – 2, 5, картофеле – 2, 0, моркови – 1, 5, томатах – 0, 6%. Еще меньше белков во многих плодах. Но в некоторых плодах белков содержится не меньше, чем в овощах. Так, в малине содержится в среднем 7% белков, ежевике – 2%, бананах – 1, 5%.

.
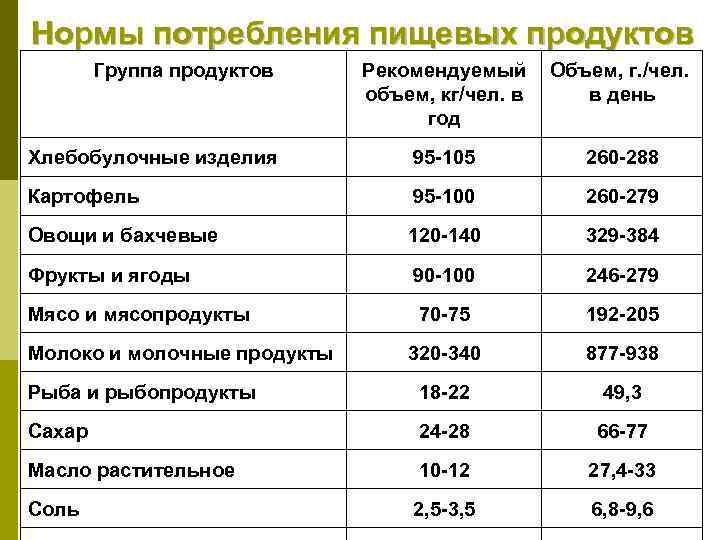
Нормы потребления пищевых продуктов Группа продуктов Рекомендуемый Объем, г. /чел. объем, кг/чел. в в день год Хлебобулочные изделия 95 -105 260 -288 Картофель 95 -100 260 -279 Овощи и бахчевые 120 -140 329 -384 Фрукты и ягоды 90 -100 246 -279 Мясо и мясопродукты 70 -75 192 -205 320 -340 877 -938 Рыба и рыбопродукты 18 -22 49, 3 Сахар 24 -28 66 -77 Масло растительное 10 -12 27, 4 -33 Соль 2, 5 -3, 5 6, 8 -9, 6 Молоко и молочные продукты

? Вопросы


Кафедра «Технологии продовольственных продуктов» г. Тамбов, ул. Ленинградская, 1 тел. : (4752) 63 -94 -42 mail: topt@topt. tstu. ru Разработка кондитерских изделий функционального назначения с улучшенными потребительскими характеристиками Кондитерские изделия ВИТАМИНЫ МАКРОЭЛЕМЕНТЫ МИКРОЭЛЕМЕНТЫ ПИЩЕВЫЕ ВОЛОКНА Местное растительное сырье – перспективный источник БАВ Производство функциональных продуктов питания Порошки Экстракты ФУНКЦИОНАЛЬНЫЕ ДОБАВКИ с использованием местных сырьевых ресурсов представляется одним из наиболее эффективных путей биокоррекции в целях нормализации деятельности определенных систем организма, укрепления здоровья, повышения иммунитета, выведения радионуклидов, токсинов, тяжелых металлов и др. Наиболее подходящими для этой цели сырьевыми компонентами являются овощи, лекарственные и пряноароматические травы в виде порошков или различных экстрактов из местных видов сырья. Стабилизаторы Структурообразователи Вкусовые добавки Ароматические добавки Красители

Стенды кафедры ТПП на второй Международной Покровской ярмарке


С днем Пищевика!
Л2_Пищевая химия.ppt