Первичные иммунодефициты.ppt
- Количество слайдов: 27

Первичные иммунодефициты

Иммунодефицитные состояния (ИДС) включают обширную группу самостоятельных заболеваний (нозологических форм) и сопутствующих синдромов, общими признаками которых являются недостаточность одного или более компонентов иммунной системы, неспособность организма противостоять чужеродной антигенной агрессии. Такие состояния могут иметь наследственную основу (первичные ИДС), а также формироваться во внутриутробном или постнатальном периодах жизни под влиянием иммунотоксинов, вирусов или ионизирующей радиации (вторичные ИДС).

Оппозитные этапы онтогенеза иммунной системы. Физиологический иммунодефицит А. Иммунодефицит новорожденных 1. В-клеток достаточно, но они не способны к синтезу антител. Иммунитет: трансплацентарный (Ig. G) и секреторный (Ig. G, Ig. E, Ig. M). Ig. G = или чуть выше материнского, через 1 мес. исчезают. Собственные Ig. M 6 -8 лет, Ig. G 1 год у мальчиков и 2 года у девочек, Ig. А 9 -12 лет, Ig. Е 10 -15 лет. 2. Неспецифические факторы защиты: лизоцим (грам+), лактоферрин (кишечная палочка). 3. Т-клеток достаточно, но они функционально неполноценны. 4. Недостаточная фагоцитарная активность нейтрофилов и моноцитов Благоприятные условия для развития инфекций Далее – антигенная стимуляция, заселение слизистых БЛТ и ЖКТ микрофлорой (аг пищи и вдыхаемые аг) – формирование местного иммунитета (барьерная функция). Б. Т-лимфоцитарный дефицит пожилого и старческого возраста: атрофия тимуса снижение продукции тимических гормонов, Т-лимфоцитопения со снижением их функциональной активности, слабая ГЗТ, снижение продукции цитокинов, дисбаланс регуляторных клеток. Увеличение содержания аутоантител, повышение частоты вирусных, опухолевых, грибковых заболеваний

Типы наследования при первичных иммунодефицитах 1. 2. 3. Рецессивный, сцепленный с полом (агаммаглобулинемия типа Брутон, ПИД с гиперпродукцией Ig. M, синдром Вискотта-Олдрича) Аутосомно-рецессивный (синдром Луи-Бар, ТКИН) Неустановленный

Молекулярные дефекты, лежащие в основе ПИД • 1. Делеции (выпадение или выключение) генов, кодирующих синтез тяжелых цепей иммуноглобулинов и рецепторов Т-лимфоцитов. Хромосомные мутации (делеции Х-хромосомы и аутосом). • 2. Мутации, ведущие к нарушениям сборки–реаранжировки генов иммуноглобулинов и Т-рецепторов. Известно, что гены легких и тяжелых цепей этих белков локализуются на разных хромосомах, а активация этих генов начинается с их организации. • 3. Дефекты альтернативного сплайсинга РНК (излишняя вырезка некодируемых генных фрагментов при транскрипции). • 4. Мутации генов Х-хромосомы, регулирующих дифференцировку и созревание лимфоцитов. • 5. Мутации, ведущие к потере антигенов тканевой совместимости. • 6. Мутации, нарушающие созревание и дифференцировку • Т-лимфоцитов в вилочковой железе. • 7. Мутации генов, кодирующих синтез цитокинов. • 8. Мутации генов, кодирующих синтез ферментов и компонентов комплемента.
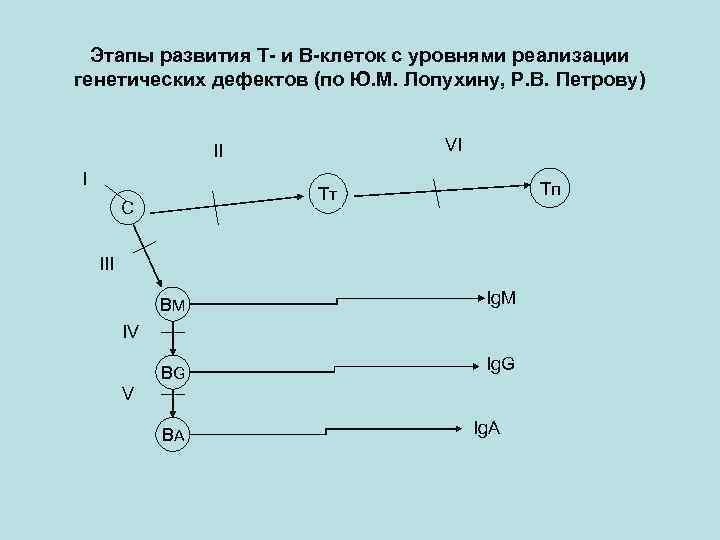
Этапы развития Т- и В-клеток с уровнями реализации генетических дефектов (по Ю. М. Лопухину, Р. В. Петрову) VI II I Тп Тт C III BM Ig. M BG Ig. G IV V BA Ig. A
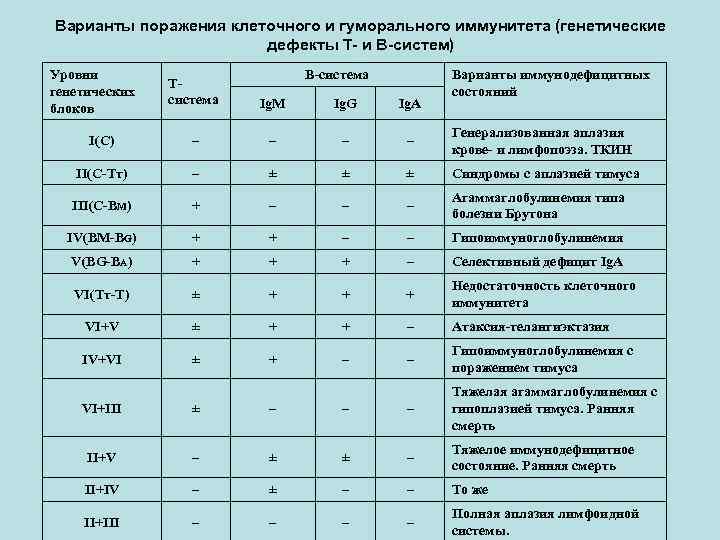
Варианты поражения клеточного и гуморального иммунитета (генетические дефекты Т- и В-систем) Уровни генетических блоков В-система Варианты иммунодефицитных состояний Тсистема Ig. M Ig. G Ig. A I(C) – – Генерализованная аплазия крове- и лимфопоэза. ТКИН II(C-Tт) – ± ± ± Синдромы с аплазией тимуса III(C-BM) + – – – Агаммаглобулинемия типа болезни Брутона IV(BM-BG) + + – – Гипоиммуноглобулинемия V(BG-BA) + + + – Селективный дефицит Ig. A VI(Tт-T) ± + + + Недостаточность клеточного иммунитета VI+V ± + + – Атаксия-телангиэктазия IV+VI ± + – – Гипоиммуноглобулинемия с поражением тимуса VI+III ± – – – Тяжелая агаммаглобулинемия с гипоплазией тимуса. Ранняя смерть II+V – ± ± – Тяжелое иммунодефицитное состояние. Ранняя смерть II+IV – ± – – То же II+III – – Полная аплазия лимфоидной системы.
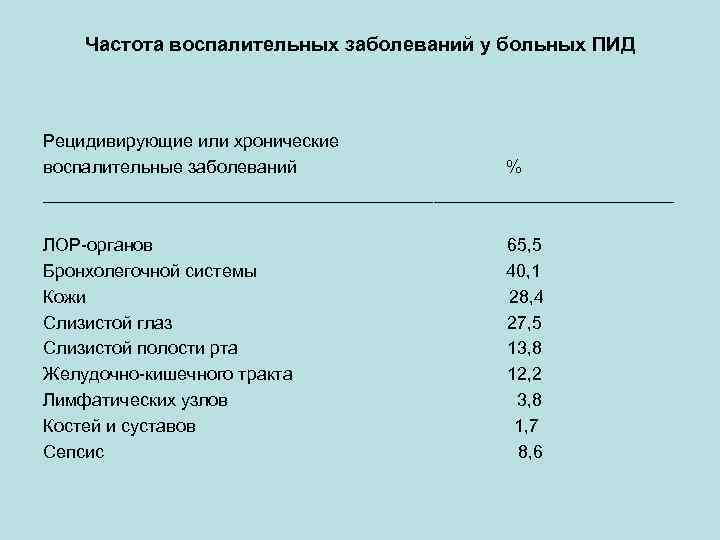
Частота воспалительных заболеваний у больных ПИД Рецидивирующие или хронические воспалительные заболеваний % ________________________________ ЛОР-органов Бронхолегочной системы Кожи Слизистой глаз Слизистой полости рта Желудочно-кишечного тракта Лимфатических узлов Костей и суставов Сепсис 65, 5 40, 1 28, 4 27, 5 13, 8 12, 2 3, 8 1, 7 8, 6

Зависимость клинических проявлений ПИД от преимущественного поражения гуморального или клеточного звеньев иммунной системы • Локальные гнойные микробно-воспалительные процессы в дыхательных путях, коже, суставах и костях – при дефектах гуморального иммунитета и фагоцитоза • Склонность к вирусным и грибковым заболеваниям более типична для недостаточности клеточного иммунитета • При комбинированных формах ПИД – сочетание микробновоспалительных, вирусных и грибковых заболеваний; септические процессы. Активация условно-патогенной флоры.

Клинико-лабораторные синдромы и заболевания, сопровождающие ПИД • • • Гематологический синдром: нейтропения, эозинофилия и тромбоцитопения, лимфопения ниже 1 000/1 мкл крови. Желудочно-кишечные расстройства: малабсорбция, расстройства пищеварения. Эти проявления обусловлены желудочно-кишечными инфекциями, на фоне снижения защитного действия секреторного Ig. A и бактерицидного Ig. M. Часто развивается дисбактериоз, нарушение белкового синтеза способствует снижению продукции иммуноглобулинов. Аутоиммунные заболевания как органоспецифические, так и органонеспецифические, чаще развиваются при ПИД с агаммаглобулинемией, селективным дефицитом Ig. A, с дефектами системы комплемента. Встречаются пернициозная анемия, аутоиммунная гемолитическая анемия, идиопатическая тромбоцитопеническая пурпура, ситемная красная волчанка (СКВ), тиреоидит, синдром Съегрена, хронический активный гепатит и миастения гравис. Опухолевые, чаще лимфопролиферативные заболевания. Например, при синдромах Вискотта-Олдрича и Луи-Бар опухоли выявляются у 20 и соответственно у 30 % больных, при селективном дефиците Ig. A – у 35 % пациентов. Следует отметить, что смертность от рака в соответствующей возрастной группе у больных ПИД в 10– 200 раз превышает смертность в популяции. Аллергические реакции являются следствием многих ПИД, причина их связана с дефектом регуляции иммунитета при воздействии аллергена.

Первичные иммунодефициты – это генетически детерминированные или врожденные синдромы нарушения содержания и функциональной активности иммунокомпетентных клеток, неспецифических факторов защиты. ПИД – это не нозологическая форма заболеваний, а клинико-иммунологический синдром, лежащий в основе развития рецидивирующих инфекций, аллергических, аутоиммунных и опухолевых заболеваний

Упрощенная классификация ПИД Первичные иммунодефициты селективные с дефектами: • • • В-лимфоцитов Т-лимфоцитов моноцитов–макрофагов неспецифических факторов защиты Цитокинов Первичные иммунодефициты комбинированные

Дефекты антителообразования (В-лимфоцитов) • • • Х-Сцепленная первичная агаммаглобулинемия – болезнь Брутона рецидивирующие гнойные инфекции в раннем возрасте (5 6 мес); Ig. G менее 200 mg / d. L, отсутствие (снижение) Ig. M, Ig. A, Ig. D; снижение (отсутствие) циркулирующих В-лимфоцитов; эффективность заместительной терапии (применение иммуноглобулинов). • • • Общий вариабельный иммунодефицит (ОВИД) Общая вариабельная гипогаммаглобулинемия (ОВГ) рецидивирующие гнойные инфекции, возникающие в любом возрасте; высокая частота аутоиммунных заболеваний; тотальный уровень Ig менее 300 mg / d. L, уровень Ig. G ниже 250 mg / d. L; количество В-клеток в норме. • • Селективный дефицит Ig. A уровень Ig. A ниже 50 mg / d. L, при нормальном или повышенном уровне других Ig; нормальные показатели клеточного звена иммунитета; высокая частота аллергических и аутоиммунных заболеваний, рецидивирующих синопульмональных инфекций, болезней ЖКТ. • • • Селективный дефицит субклассов Ig. G субнормальный уровень одного или более субклассов Ig. G; нормальные показатели Т-клеточного звена иммунитета; рецидивирующие бактериальные инфекции; ассоциативность с другими ПИД (селективный дефицит Ig. A или атаксиятелеангиэктазия).

• ИДС с гипер-Ig. M (CD 40 -ligand deficiency) • Пациенты с так называемым Х-сцепленным гипер Ig. M (HIGM) синдромом склонны к инфекциям и имеют пониженную концентрацию Ig. G, Ig. A, Ig. E в сыворотке, но нормальный или повышенный уровень Ig. M. CD 40 (В-клеточный протеин) CD 40 L – на активированных Тх CD 40/CD 40 L взаимодействия: – индукция переключения классов иммуноглобулинов – стимуляция активированными Т-клетками макрофагов к продукции ИЛ-12 (отсюда склонность к инфекциям, вызванным внутриклеточными патогенами) ---------------------------------

Преимущественные дефекты Т-лимфоцитов Иммунодефицитные состояния, характеризующиеся изолированными Т-клеточными нарушениями, встречаются редко. Имеются наблюдения о значительном снижении количества циркулирующих CD 4+ T-клеток и дефектных клеточных реакциях у пациентов, не зараженных ВИЧ. Клинические проявления синдрома включают оппортунистические инфекциии (криптококковый менингит, кандидоз полости рта). • • • Синдром Ди-Джорджа Основной симптомокомплекс: врожденная аплазия или гипоплазия тимуса; лимфопения как следствие снижения числа Т-клеток; снижение функций Т-клеток периферической крови; уровень антител не нарушен; эффективность терапии путем трансплантации тимуса.

Комбинированные иммунодефициты • Тяжелая комбинированная иммунологическая недостаточность (ТКИН). • начало заболевания – до 6 мес, с рецидивирующих вирусных, бактериальных, грибковых, протозойных инфекций; • встречаются Х-сцепленные, аутосомные и спорадические формы; • ТКИН имеет два иммунологических варианта. В одном обнаруживается недостаток лимфоцитов (Т–, В– ТКИН), в другом – нормальное или повышенное число В-клеток и недостаточное – Т-лимфоцитов (Т–, В+ ТКИН). γс- дефицит или Х 1 - сцепленная с Х-хромосомой форма иммунодефицита (нарушение дифференцировки Т- и NK-клеток) В основе – мутация гена, кодирующего γ-цепь рецептора для ИЛ-2. γ-цепь является компонентом рецепторов для ИЛ-4, -7, -9, 15. Т-клеточная лимфопения – нарушения пролиферации протимоцитов, опосредуемой ИЛ-7 Нарушение дифференцировки NK-клеток – нет сигнала от ИЛ-15.

• • • Синдром Вискотт–Олдрича проявляет себя экземой, рецидивирующими гнойными инфекциями (отиты, пиодермии, пневмонии, колиты) и геморрагическим синдромом; диагностируется по тромбоцитопении у детей мужского пола с позитивной семейной историей; дефицит Ig. M при нормальном содержании Ig. G и увеличении Ig. A/Ig. E в крови; тромбоцитопения и уменьшение размеров тромбоцитов, а также их адгезии и аггрегации; часто встречается злокачественный рост лимфоидной ткани. Атаксия-телеангиэктазия (Луи Бар) болезнь выявляется до двух лет; полный синдром – атаксия, телеангиэктазия и рецидивирующие синопульмональные инфекции; у 40 % больных отмечается селективный дефицит продукции Ig. A; высокая предрасположенность к новообразованиям: лимфомам, лейкемиям.

Патология фагоцитоза • • • Хроническая гранулематозная болезнь повышенная чувствительность к слабовирулентным микроорганизмам: Staphylococcus epidermidis, Serratia marcescens, Aspergillus; Х-сцепленное наследование (возможен аутосомный вариант); Начало заболевания до двух лет жизни: лимфаденит, гепатоспленомегалия, пневмония, остеомиелит, абсцессы; Процесс фагоцитоза не сопровождается хемилюминесценцией, восстановление нитросинего тетразолия отсутствует, галогеноксиды не образуются, отсутствует кислородный взрыв фагоцитов. Синдром Чедиака–Хигаси Заболевание характеризуется сочетанием проявлений частичного альбинизма кожи, волос и глаз, лихорадочных состояний, гепатоспленомегалии, панцитопении, склонности к микробновоспалительным заболеваниям, сенсорной и моторной невропатии; высока вероятность лимфоретикулярного рака. Кожа светлая, волосы серебристые, характерна светобоязнь. Воспалительные процессы в слизистых оболочках дыхательных путей и на коже чаще всего вызваны золотистым стафилококком. Нейтрофилы, моноциты и тромбоциты содержат гигантские гранулярные включения. Наблюдается нарушение хемотаксиса нейтрофилов, снижение NКактивности, повышенный титр антител к вирусу Эпштейн-Бар.

Дефекты системы комплемента являются наиболее редкой разновидностью ПИД (1– 3 %). Описаны наследственные дефекты практически всех компонентов комплемента. Наиболее часто встречается дефицит С 2 компонента. Дефекты ранних фракций комплемента (С 1–С 4) сопровождаются высокой частотой аутоиммунных заболеваний, в т. ч. системной красной волчанки. Дефекты терминальных компонентов (С 5–С 9) предрасполагают к развитию тяжёлых инфекций, вызванных представителями рода Neisseria. Дефицит С 3 компонента часто по клиническим проявлениям напоминает гуморальные ПИД и сопровождается тяжёлыми рецидивирующими инфекциями: пневмонией, менингитом, перитонитом. С другой стороны, некоторые больные с дефицитом С 2, С 4, С 9 могут не иметь никаких клинических проявлений. Универсальной терапии этих состояний не существует, она зависит от конкретных клинических проявлений.

Ангионевротический отёк (дефицит С 1 эстеразы) • Бывает Ig. E-зависимый, комплемент-зависимый. Резко ограниченный, локализованный отек кожи с вовлечением глубоких слоев, вкл. клетчатку) В основе заболевания лежит снижение концентрации и/или функции С 1 -ингибитора (С 1 -эстеразы) – практически единственного ингибитора системы комплемента. Частота инфекционных проявлений у этих больных может быть несколько повышена, однако основным симптомом заболевания являются рецидивирующие отеки конечностей, брюшной полости (спазмы кишечника), лица и гортани. Отёки могут возникать самопроизвольно, а также провоцироваться стрессом, минимальной травмой, инфекцией. В патогенезе отёков лежит образование вазоактивных веществ, отличных от гистамина, в связи с чем терапия антигистаминными препаратами и глюкокортикостероидами при этом состоянии не эффективна.

Другие формы ПИД ИДС, обусловленные наследованием метаболического блока в иммунокомпетентных клетках. • При дефиците фермента АДА наблюдается одна из тяжелых форм ТКИН. Лимфоциты не реагируют на митогены, интактны в смешанной культуре лимфоцитов; отсутствуют кожные реакции на туберкулин, наблюдается низкое содержание изогемагглютининов в крови, не синтезируются антитела, отсутствуют реакции отторжения кожного трансплантата. • Недостаточность фермента ПНФ – аутосомно-рецессивный дефект, при котором синтез ДНК снижается в связи с недостаточностью как пуриновых, так и пиримидиновых оснований. Больные с дефектом ПНФ страдают рецидивирующими микробно-воспалительными заболеваниями дыхательных путей и легких. Однако они проявляются в более легкой форме, чем другие формы ТКИН. Т-лимфоциты особенно чувствительны к недостатку ПНФ и поражаются больше, чем В-лимфоциты.

Нарушения в системе цитокинов Наследственный дефицит рецептора для ИФНгамма: Высокая и селективная чувствительность к слабопатогенной микобактерии, БЦЖ, или нетуберкулезной микобактерии. Неблагоприятный прогноз (фатальная инфекция). Неспособность формировать гранулемы в ответ на микобактерии. Отсутствие ощутимых дефектов в иммунной системе при лаб. обследовании. Характерная особенность ПИД – неспособность формировать гранулемы в ответ на микобактерию. Облигатность ИФНгамма как для формирования гранулем, так и для эффективной антимикобактериальной активности.

Периодические аутовоспалительные синдромы (лихорадка, лейкоцитоз, СОЭ, нейтрофилия, амилоидоз, начало – детский возраст) • DIRA- дефицит агониста рецептора к ИЛ-1 • ТРАПС – дефицит взаимодействия рецепторлиганд (ФНО) периодический синдром (2 -3 приступа/год) • CAPS-CIAS 1 – Associated Periodic Syndromes • FCAS (семейный холодовой аутовоспалительный синдром)

Аутоиммунный лимфопролиферативный синдром Fas/CD 95 дефицит (лимфопролиферативный синдром) Мыши lpr/lpr: Т-В-клеточный пролиферативный синдром с манифестацией аутоиммунных проявлений вследствие нарушения апоптоза лимфоцитов (Fas – член семейства TNFR) Fas ligand (Fas. L)-дефицит – схожее заболевание у мышей gld. У мышей и у ряда пациентов – повышенное число циркулирующих CD 4 -CD 8 - Т-клеток. • Диагноз АЛПС можно предположить при наличии у больного поликлональной гипериммуноглобулинемии (повышены один или несколько классов сывороточных иммуноглобулинов), выраженного увеличения лимфоузлов, гепатоспленомегалии (при исключении других, в т. ч. онкологических, причин этих симптомов). Характерным лабораторным признаком АЛПС является наличие двойных негативных CD 3+CD 4 -CD 8 - лимфоцитов, в норме отсутствующих в периферической крови. Однако подтверждением диагноза является выявление дефекта апоптоза in vitro. Основными клиническими проявлениями АЛПС являются лимфаденопатия, гепатоспленомегалия, аутоиммунные гемоцитопении в виде гемолитической анемии и/или агранулоцитоза и/или тромбоцитопении и другие аутоиммунные расстройства (неспецифический язвенный колит, артрит, узловатая эритема, сиалоаденит и др. ). У большинства больных выявляются аутоантитела к различным клеткам и тканям организма.

Диагностика ПИД. 10 настораживающих признаков • • • Частые заболевания отитом(не менее 6 8 раз в течение года) Персистирующая молочница или грибковое поражение кожи в возрасте менее одного года Несколько подтвержденных серьезных синуситов (4 6 раз в год) Отставание грудного ребенка в росте и массе Более двух подтвержденных пневмоний В семье: наличие ПИД, факты ранней смерти от тяжелых инфекций или наличие одного из указанных выше симптомов Повторные глубокие абсцессы кожи или внутренних органов Потребность в терапии антибиотиками для купирования инфекции до 2 мес и более (торпидность терапии) Не менее двух глубоких инфекций (менингит, остеомиелит, целлюлит, сепсис) Потребность во внутривенном введении антибиотиков для купирования инфекции Если у ребенка имеется более одного из перечисленных симптомов, то вероятность иммунодефицита высока.

• • Лечение ПИД Антибактериальная терапия ПИД она должна быть длительной, сроки отмены препарата определяются индивидуально используются максимальные возрастные или максимально допустимые дозы антибактериальных препаратов; при отсутствии выраженного положительного эффекта от применения избранного препарата в течение пяти дней его заменяют препаратом другой группы; рекомендуется парентеральное введение препарата, преимущество отдается внутривенному или ингаляционному методам применения антибиотиков; одновременно с антибиотиками показаны противогрибковые препараты. Трансплантация органов и тканей иммунной системы Трансплантация клеток костного мозга от HLA-идентичных доноров ведет к полному иммунологическому восстановлению у большинства пациентов с ТКИН, при синдроме Вискотта- Олдрича, хронической гранулематозной болезни, дефиците IFN -R 1, Х-сцепленном гипер-Ig. Mсиндроме и синдроме Чедиака-Хигаси. Наибольшую трудность при этом методе составляет подбор подходящего донора. Кроме пересадок костного мозга, осуществляют трансплантацию вилочковой железы плода или взрослого донора, селезенки, лимфоцитов иммунологически зрелых доноров.

Лечение ПИД • • • Применение иммуноглобулинов. Для лечения гипо- и агаммаглобулинемий назначается заместительная терапия препаратами гамма-глобулина. Рекомендуются регулярные внутривенные инфузии иммуноглобулина, обычно из расчета 0, 2– 0, 4 г на 1 кг массы тела больного каждые 3– 4 недели. Минимальный эффективный уровень Ig. G в сыворотке больного перед очередной инфузией должен составлять 500 мг / мл. Альтернативный вариант терапии – инфузии свежезамороженной плазмы (20– 40 мл плазмы эквивалентны примерно 0, 2– 0, 4 г Ig. G при концентрации Ig. G 1 000 мг / мл). В будущем альтернативный подход для лечения ПИД – генная терапия (трансфекция генов в стволовые клетки. Нескольким больным проведена пересадка гена, кодирующего АДА. У пациентов фиксируется экспрессия пересаженного гена, однако сохраняется зависимость от периодического введения полиэтиленгликольдезаминазы. Перспективным методом лечения дефицита IFN R 1 является также трансфекция соответствующего гена.
Первичные иммунодефициты.ppt