простр структуры белка_методы_12.ppt
- Количество слайдов: 81

ПЕРВИЧНАЯ СТРУКТУРА БЕЛКА
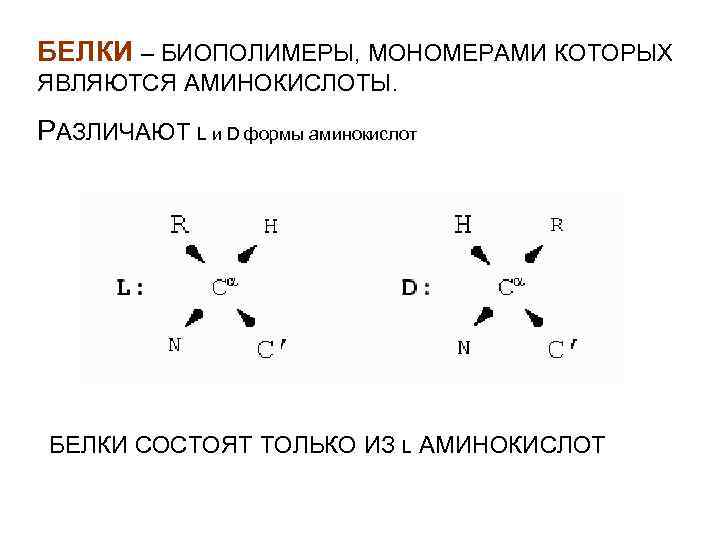
БЕЛКИ – БИОПОЛИМЕРЫ, МОНОМЕРАМИ КОТОРЫХ ЯВЛЯЮТСЯ АМИНОКИСЛОТЫ. РАЗЛИЧАЮТ L и D формы аминокислот БЕЛКИ СОСТОЯТ ТОЛЬКО ИЗ L АМИНОКИСЛОТ
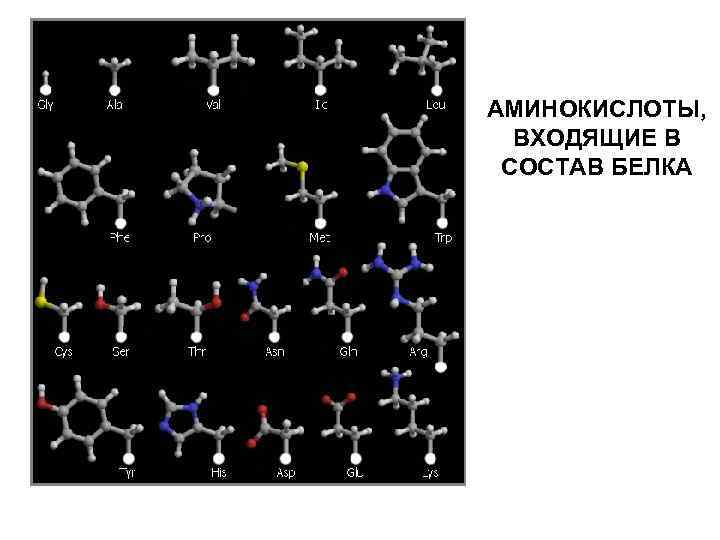
АМИНОКИСЛОТЫ, ВХОДЯЩИЕ В СОСТАВ БЕЛКА
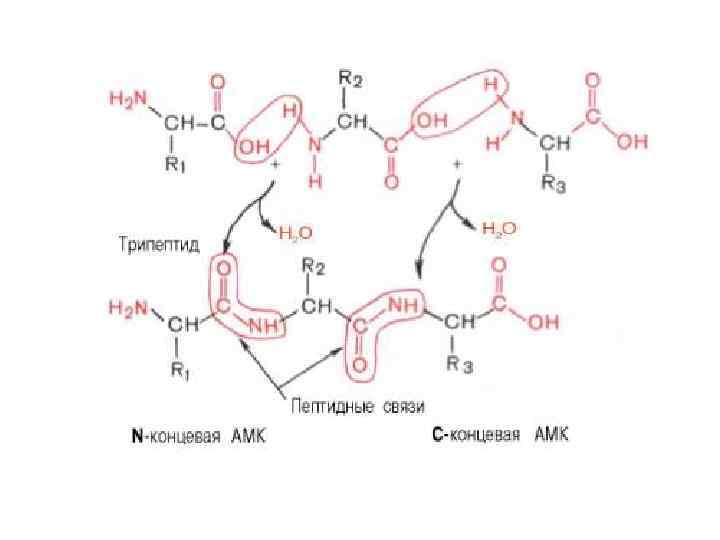
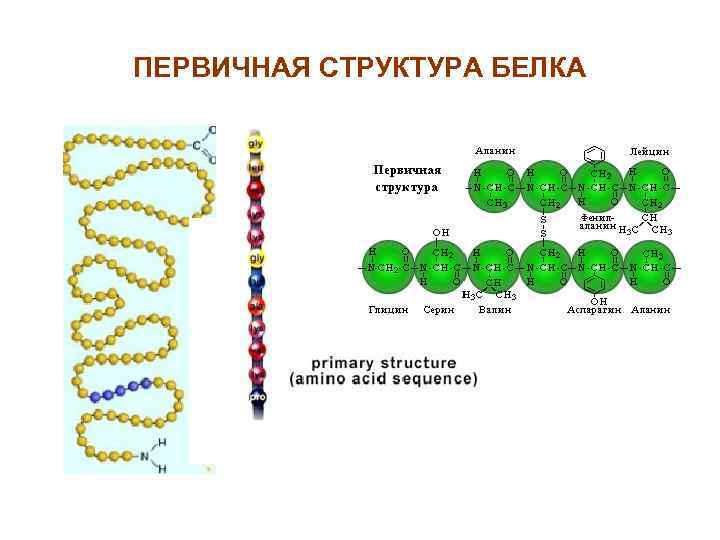
ПЕРВИЧНАЯ СТРУКТУРА БЕЛКА
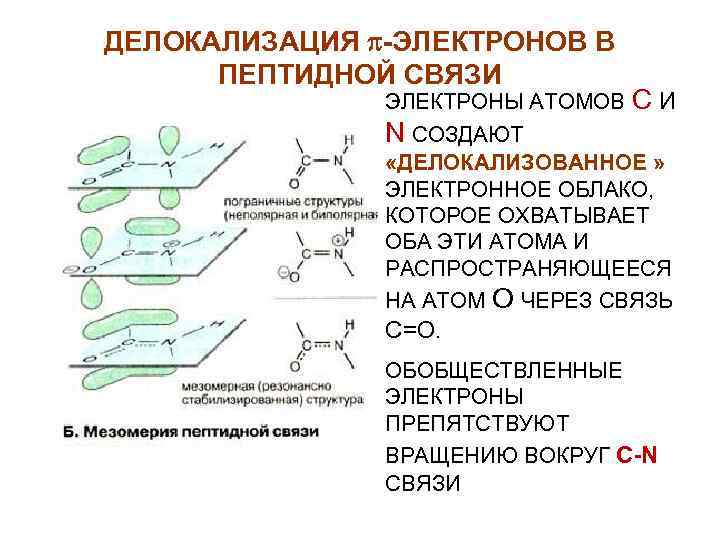
ДЕЛОКАЛИЗАЦИЯ -ЭЛЕКТРОНОВ В ПЕПТИДНОЙ СВЯЗИ ЭЛЕКТРОНЫ АТОМОВ СИ N СОЗДАЮТ «ДЕЛОКАЛИЗОВАННОЕ » ЭЛЕКТРОННОЕ ОБЛАКО, КОТОРОЕ ОХВАТЫВАЕТ ОБА ЭТИ АТОМА И РАСПРОСТРАНЯЮЩЕЕСЯ НА АТОМ О ЧЕРЕЗ СВЯЗЬ С=О. ОБОБЩЕСТВЛЕННЫЕ ЭЛЕКТРОНЫ ПРЕПЯТСТВУЮТ ВРАЩЕНИЮ ВОКРУГ C-N СВЯЗИ
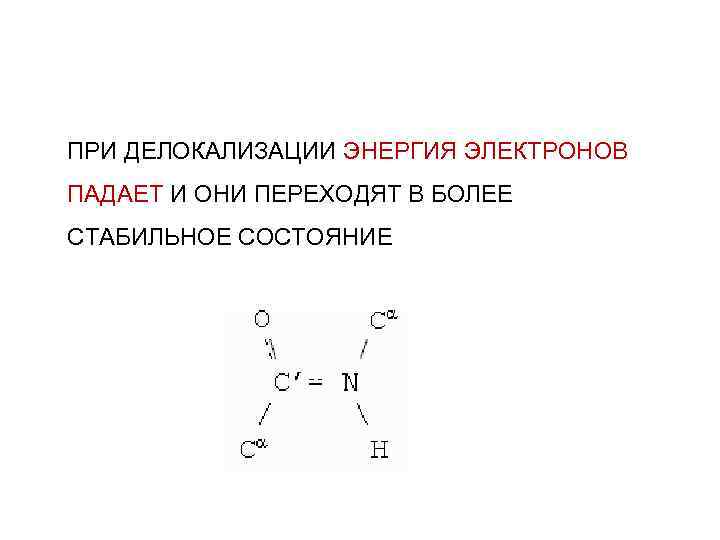
ПРИ ДЕЛОКАЛИЗАЦИИ ЭНЕРГИЯ ЭЛЕКТРОНОВ ПАДАЕТ И ОНИ ПЕРЕХОДЯТ В БОЛЕЕ СТАБИЛЬНОЕ СОСТОЯНИЕ

ДЛИНЫ СВЯЗЕЙ N – C (ПЕПТИДНАЯ СВЯЗЬ) 0, 132 НМ N – C (ОДИНОЧНАЯ) 0, 147 НМ N = C (ДВОЙНАЯ) 0, 125 НМ 0, 147 < 0, 132 < 0, 125 ПЕПТИДНАЯ СВЯЗЬ ЗАНИМАЕТ ПРОМЕЖУТОЧНОЕ ПОЛОЖЕНИЕ
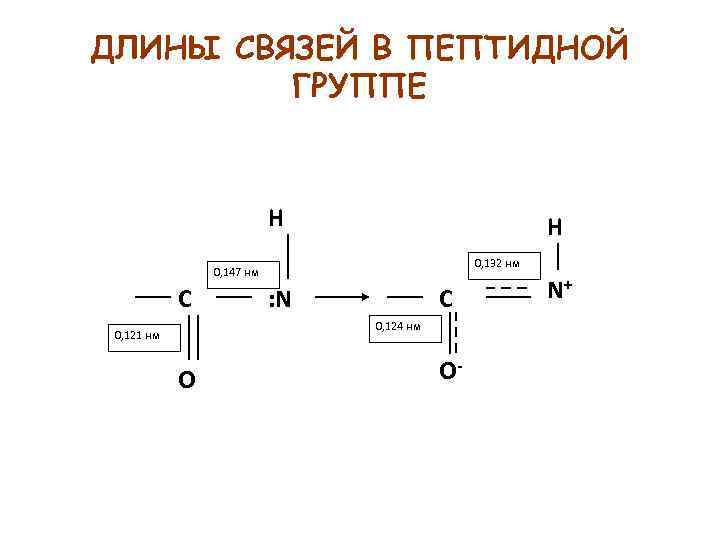
ДЛИНЫ СВЯЗЕЙ В ПЕПТИДНОЙ ГРУППЕ H H 0, 132 нм 0, 147 нм С : N С 0, 124 нм 0, 121 нм O O- N+

ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ ВАЛЕНТНЫЕ СВЯЗИ НЕ ФЛУКТУИРУЮТ: ЧАСТОТА КОЛЕБАНИЙ ЭТИХ СВЯЗЕЙ 2 х1013 сек ЧАСТОТА ТЕПЛОВЫХ КОЛЕБАНИЙ 7 х1012 сек – 1 АМПЛИТУДА ТЕПЛОВЫХ КОЛЕБАНИЙ ВАЛЕНТНЫХ УГЛОВ НЕВЕЛИКА И СОСТАВЛЯЕТ ОКОЛО 5 о. ТАКИМ ОБРАЗОМ, ГИБКОСТЬ ПОЛИПЕПТИДНОЙ ЦЕПИ ОБЕСПЕЧИВАЕТСЯ ДРУГИМИ ФАКТОРАМИ.

ГИБКОСТЬ ПОЛИПЕПТИДНОЙ ЦЕПИ, А, ЗНАЧИТ, И ЕЕ СПОСОБНОСТЬ ОБРАЗОВЫВАТЬ СПИРАЛИ И ГЛОБУЛЫ ОБЕСПЕЧИВАЕТ ВРАЩЕНИЕ ВОКРУГ ВАЛЕНТНЫХ СВЯЗЕЙ.
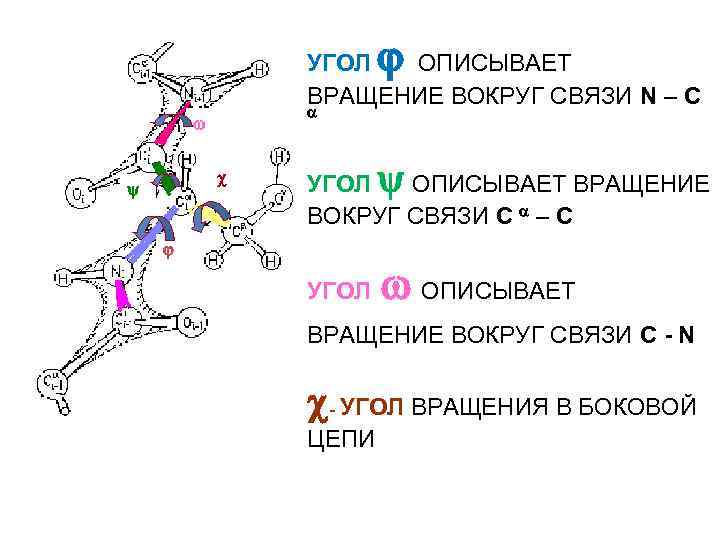
УГОЛ ОПИСЫВАЕТ ВРАЩЕНИЕ ВОКРУГ СВЯЗИ N – C УГОЛ ОПИСЫВАЕТ ВРАЩЕНИЕ ВОКРУГ СВЯЗИ C – C УГОЛ ОПИСЫВАЕТ ВРАЩЕНИЕ ВОКРУГ СВЯЗИ C - N - УГОЛ ВРАЩЕНИЯ В БОКОВОЙ ЦЕПИ
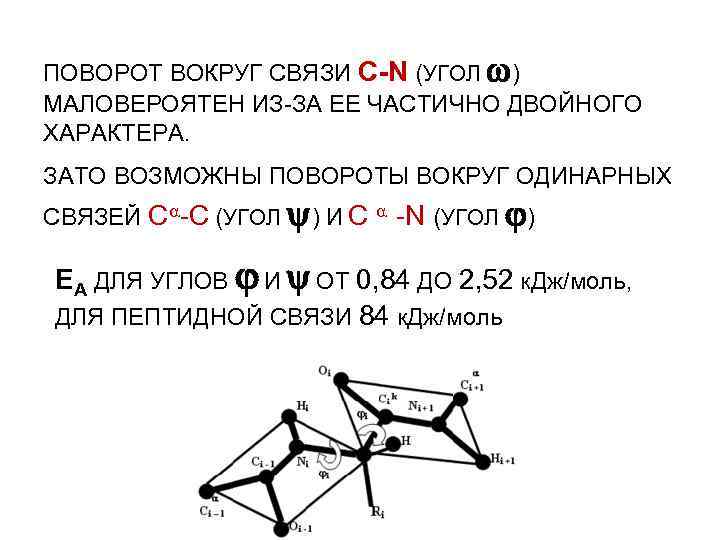
ПОВОРОТ ВОКРУГ СВЯЗИ С-N (УГОЛ ) МАЛОВЕРОЯТЕН ИЗ-ЗА ЕЕ ЧАСТИЧНО ДВОЙНОГО ХАРАКТЕРА. ЗАТО ВОЗМОЖНЫ ПОВОРОТЫ ВОКРУГ ОДИНАРНЫХ СВЯЗЕЙ C -C (УГОЛ ) И C -N (УГОЛ ) ЕА ДЛЯ УГЛОВ И ОТ 0, 84 ДО 2, 52 к. Дж/моль, ДЛЯ ПЕПТИДНОЙ СВЯЗИ 84 к. Дж/моль
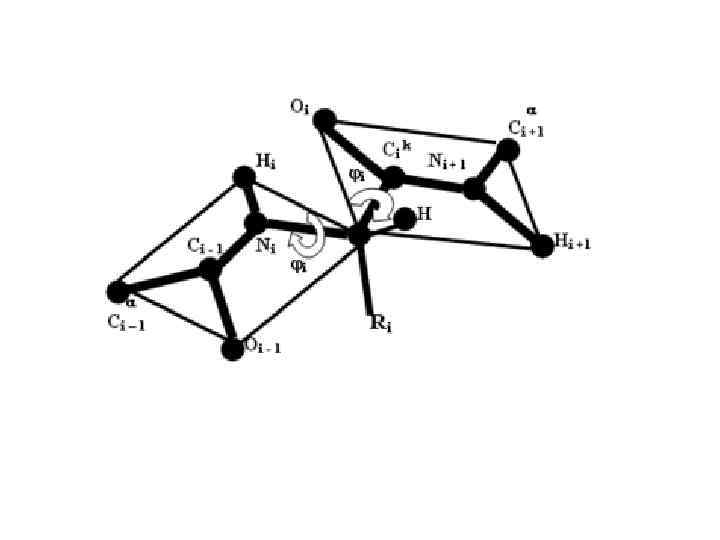

ВТОРИЧНАЯ СТРУКТУРА БЕЛКА
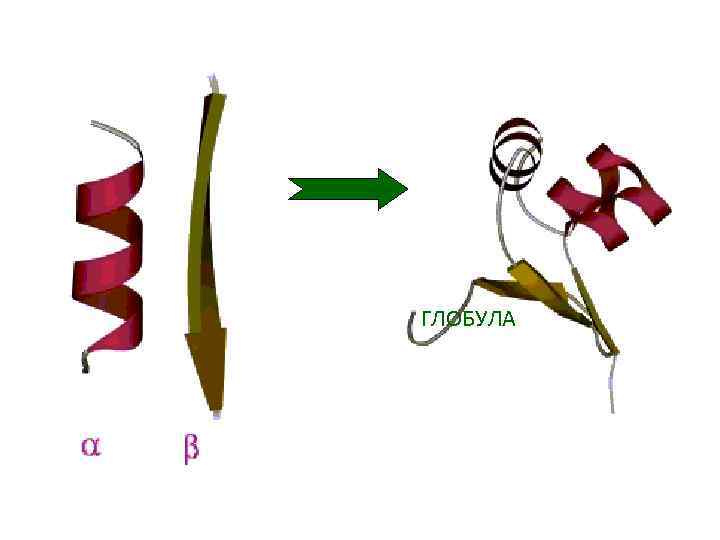
ГЛОБУЛА
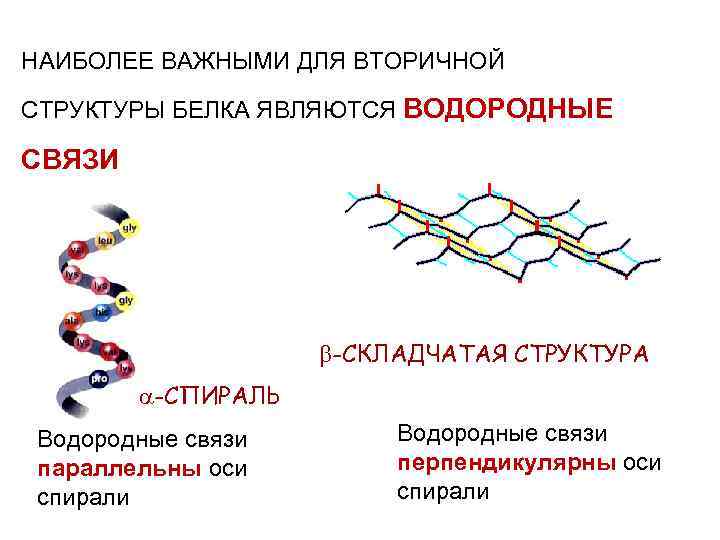
НАИБОЛЕЕ ВАЖНЫМИ ДЛЯ ВТОРИЧНОЙ СТРУКТУРЫ БЕЛКА ЯВЛЯЮТСЯ ВОДОРОДНЫЕ СВЯЗИ -СКЛАДЧАТАЯ СТРУКТУРА -СПИРАЛЬ Водородные связи параллельны оси спирали Водородные связи перпендикулярны оси спирали
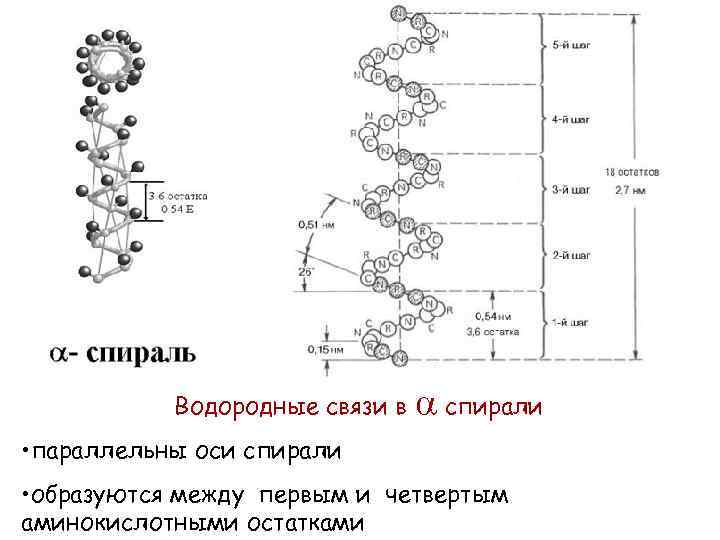
Водородные связи в спирали • параллельны оси спирали • образуются между первым и четвертым аминокислотными остатками

ПАРАМЕТРЫ -СПИРАЛИ НА КАЖДЫЙ ВИТОК (ШАГ) СПИРАЛИ ПРИХОДИТСЯ 3, 6 АМИНОКИСЛОТНЫХ ОСТАТКОВ. ШАГ СПИРАЛИ (РАССТОЯНИЕ ВДОЛЬ ОСИ) – 0, 54 НМ. НА ОДИН АМИНОКИСЛОТНЫЙ ОСТАТОК ПРИХОДИТСЯ 0, 15 НМ. ЧЕРЕЗ 5 ВИТКОВ СПИРАЛИ (18 АМИНОКИСЛОТНЫХ ОСТАТКОВ) СТРУКТУРНАЯ КОНФИГУРАЦИЯ ПОЛИПЕПТИДНОЙ ЦЕПИ ПОВТОРЯЕТСЯ
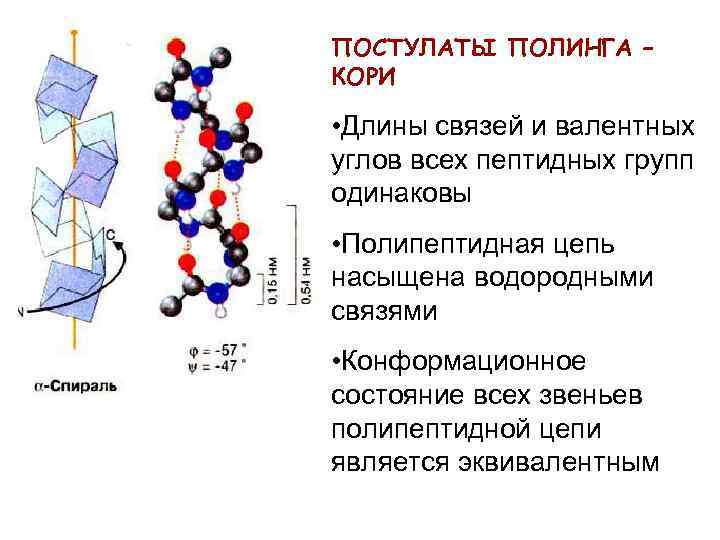
ПОСТУЛАТЫ ПОЛИНГА – КОРИ • Длины связей и валентных углов всех пептидных групп одинаковы • Полипептидная цепь насыщена водородными связями • Конформационное состояние всех звеньев полипептидной цепи является эквивалентным

-складчатые структуры
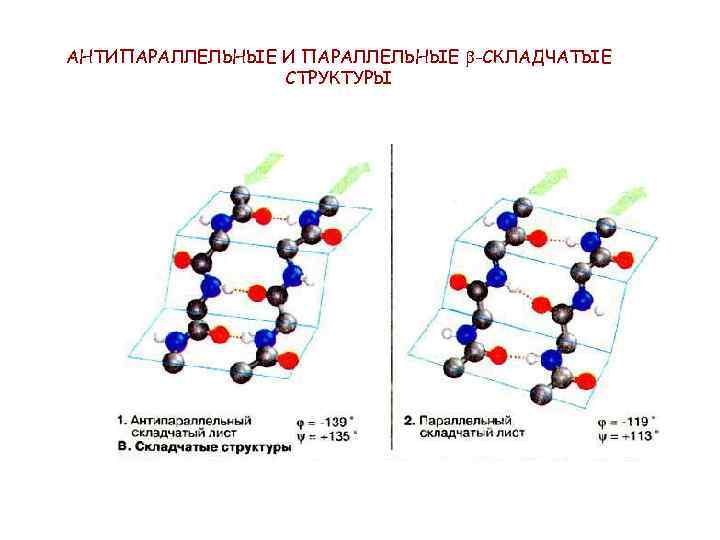
АНТИПАРАЛЛЕЛЬНЫЕ И ПАРАЛЛЕЛЬНЫЕ -СКЛАДЧАТЫЕ СТРУКТУРЫ
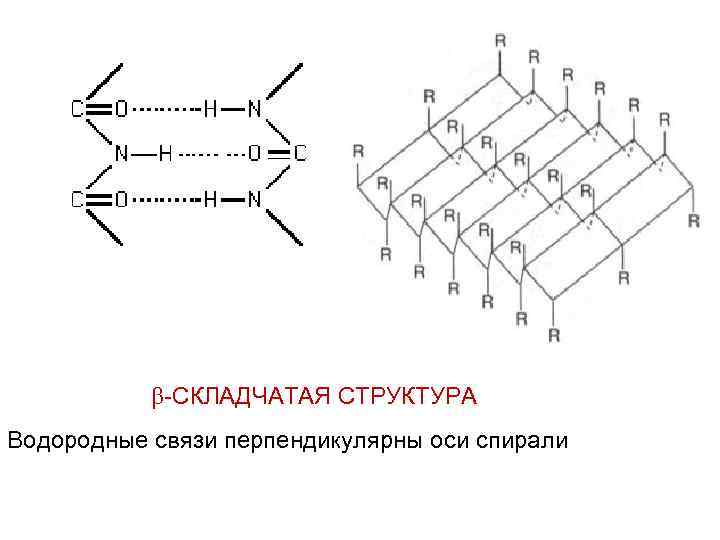
-СКЛАДЧАТАЯ СТРУКТУРА Водородные связи перпендикулярны оси спирали
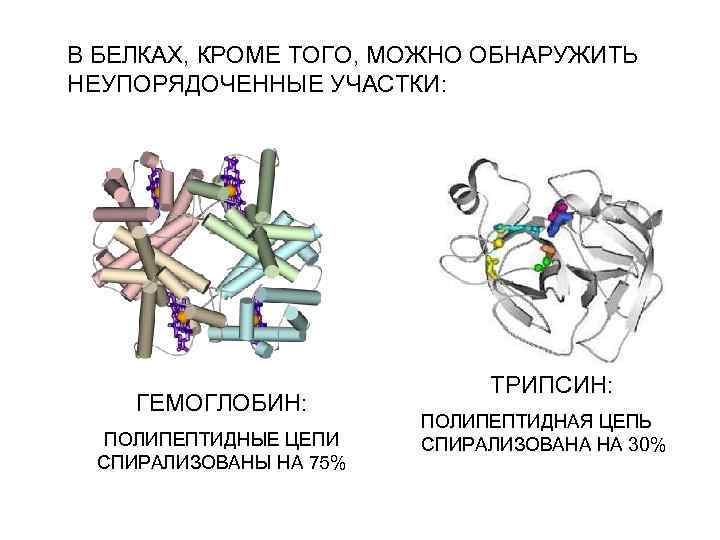
В БЕЛКАХ, КРОМЕ ТОГО, МОЖНО ОБНАРУЖИТЬ НЕУПОРЯДОЧЕННЫЕ УЧАСТКИ: ГЕМОГЛОБИН: ПОЛИПЕПТИДНЫЕ ЦЕПИ СПИРАЛИЗОВАНЫ НА 75% ТРИПСИН: ПОЛИПЕПТИДНАЯ ЦЕПЬ СПИРАЛИЗОВАНА НА 30%

ДРУГИЕ СПИРАЛЬНЫЕ КОНФОРМАЦИИ СПИРАЛЬ 310 • 3 ОСТАТКА АМИНОКИСЛОТ НА ШАГ (ВИТОК) СПИРАЛИ • РАДИУС 0, 19 НМ p. СПИРАЛЬ 4, 4 ОСТАТКА НА ШАГ СПИРАЛИ РАДИУС 0, 28 НМ

СВЕРХВТОРИЧНЫЕ СТРУКТУРЫ

СВЕРХВТОРИЧНЫЕ СТРУКТУРЫ – ЭТО ТЕРМОДИНАМИЧЕСКИ ИЛИ КИНЕТИЧЕСКИ СТАБИЛЬНЫЕ КОМПЛЕКСЫ -СПИРАЛЕЙ И СТРУКТУР, КОТОРЫЕ ФОРМИРУЮТСЯ ЗА СЧЕТ МЕЖРАДИКАЛЬНЫХ ВЗАИМОДЕЙСТВИЙ.
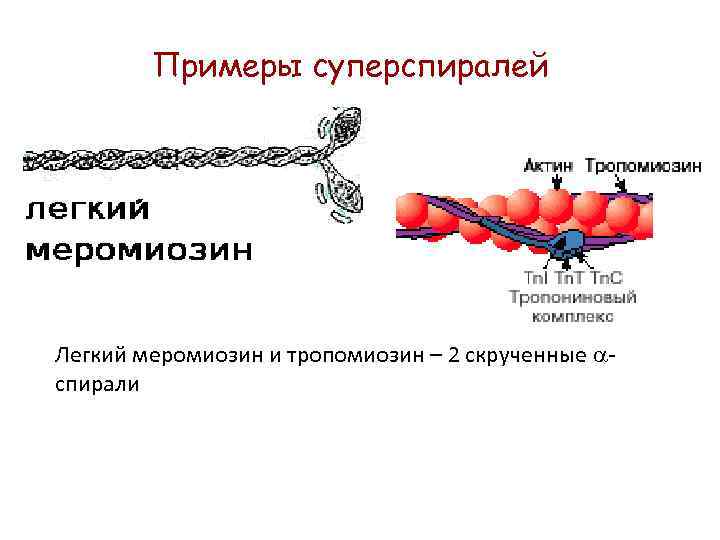
Примеры суперспиралей Легкий меромиозин и тропомиозин – 2 скрученные спирали

СУПЕРСПИРАЛЬ, СОСТОЯЩАЯ ИЗ НЕСКОЛЬКИХ -СПИРАЛЕЙ В ПЕРЕВИТЫХ СПИРАЛЯХ ПЕРИОДИЧНОСТЬ 3, 5 ОСТАТКОВ НА ВИТОК (ВМЕСТО 3, 6 В ОДИНОЧНОЙ -СПИРАЛИ )
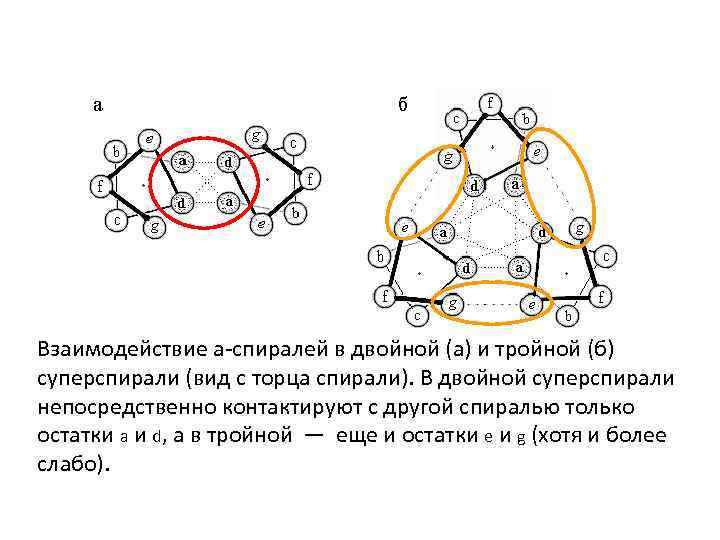
Взаимодействие a-спиралей в двойной (а) и тройной (б) суперспирали (вид с торца спирали). В двойной суперспирали непосредственно контактируют с другой спиралью только остатки а и d, а в тройной — еще и остатки e и g (хотя и более слабо).

МЕТОДЫ ИЗУЧЕНИЯ ВТОРИЧНОЙ СТРУКТУРЫ БЕЛКА

ДИСПЕРСИЯ ОПТИЧЕСКОГО ВРАЩЕНИЯ и КРУГОВОЙ ДИХРОИЗМ – методы, основанные на взаимодействии поляризованного света с оптически активными молекулами

Метод КРУГОВОГО ДИХРОИЗМА основан на различии в поглощении право- и левополяризованного света оптически активным веществом.

Левый и правый поляризованные по кругу лучи поразному поглощаются средой, т. е где коэффициенты экстинкции для лучей с левой и правой круговой поляризацией. Суммирование соответствующих им ВЕКТОРОВ неравной величины El и Еr дает результирующий вектор, конец которого описывает эллипс, т. е. плоскополяризованный свет после прохождения через оптически активную среду становится эллиптически поляризованным. Это явление называют КРУГОВЫМ ДИХРОИЗМОМ.

ПАРАМЕТРЫ, ОПРЕДЕЛЯЕМЫЕ МЕТОДОМ КРУГОВОГО ДИХРОИЗМА
![Молярная эллиптичность [ ] Характерные формы спектров КД для полилизина в форме aспирали (a), Молярная эллиптичность [ ] Характерные формы спектров КД для полилизина в форме aспирали (a),](https://present5.com/presentation/53476435_171788473/image-37.jpg)
Молярная эллиптичность [ ] Характерные формы спектров КД для полилизина в форме aспирали (a), b-структуры (b) и неупорядоченного клубка (r).
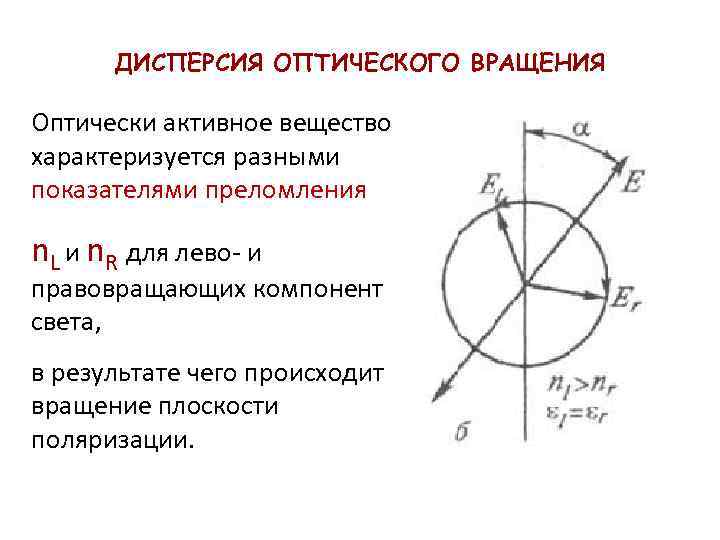
ДИСПЕРСИЯ ОПТИЧЕСКОГО ВРАЩЕНИЯ Оптически активное вещество характеризуется разными показателями преломления n. L и n. R для лево- и правовращающих компонент света, в результате чего происходит вращение плоскости поляризации.

ПАРАМЕТРЫ, ОПРЕДЕЛЯЕМЫЕ МЕТОДОМ ДОВ Оптическое вращение Удельное оптическое вращение Молярное вращение

В белках спектры ДОВ и КД регистрируют в области поглощения пептидных групп (УФ-область). Спектры КД будут отличаться в спиралях различной закрученности.

МЕТОДЫ ИЗУЧЕНИЯ ДИНАМИКИ БЕЛКОВЫХ СТРУКТУР – ЯМР ЭПР И

ЭЛЕКТРОННЫЙ ПАРАМАГНИТНЫЙ РЕЗОНАНС

Метод электронного парамагнитного резонанса был открыт в 1944 г. в Казанском Университете Е. К. ЗАВОЙСКИМ. Пионерами применения ЭПР в биологических исследованиях в России были Л. А. Блюменфельд и А. Э. Калмансон (1958).

УСЛОВИЕ ВОЗНИКНОВЕНИЯ ЭПР – НАЛИЧИЕ У ЧАСТИЦ НЕСКОМПЕНСИРОВАННЫХ МАГНИТНЫХ МОМЕНТОВ, ОБУСЛОВЛЕННЫХ СПИНОМ НЕСПАРЕННЫХ ЭЛЕКТРОНОВ
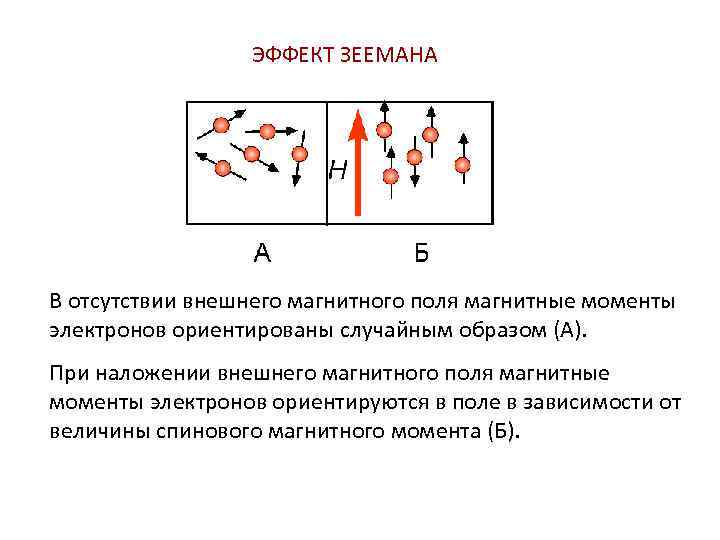
ЭФФЕКТ ЗЕЕМАНА В отсутствии внешнего магнитного поля магнитные моменты электронов ориентированы случайным образом (А). При наложении внешнего магнитного поля магнитные моменты электронов ориентируются в поле в зависимости от величины спинового магнитного момента (Б).
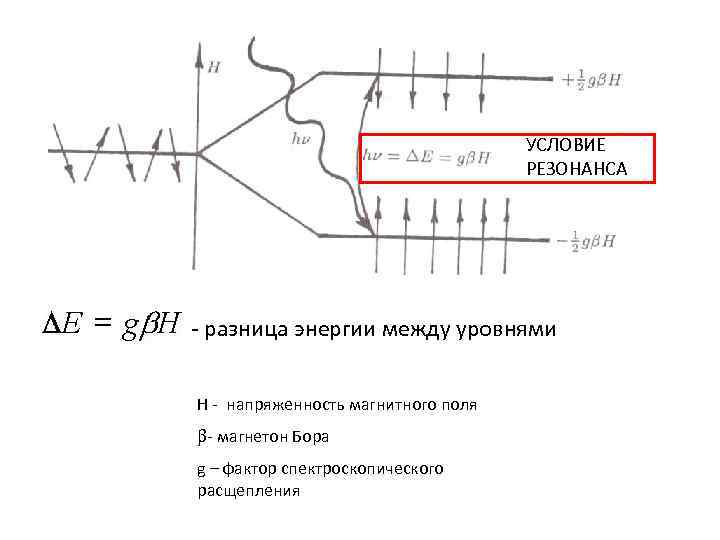
УСЛОВИЕ РЕЗОНАНСА - разница энергии между уровнями H - напряженность магнитного поля - магнетон Бора g – фактор спектроскопического расщепления
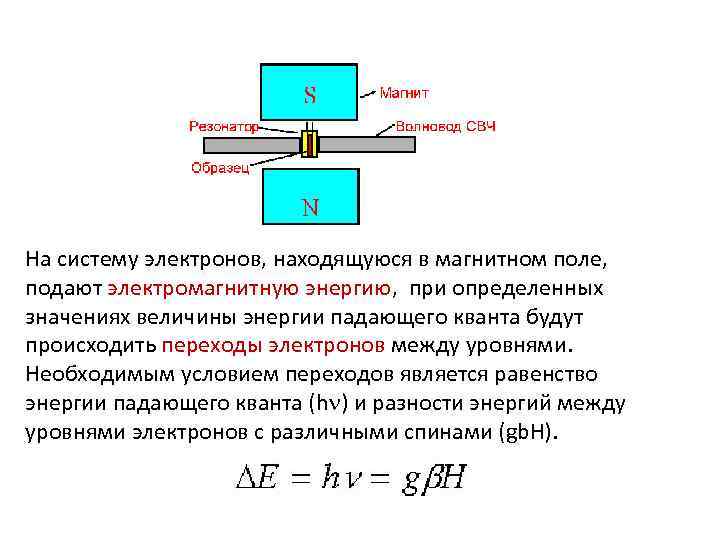
На систему электронов, находящуюся в магнитном поле, подают электромагнитную энергию, при определенных значениях величины энергии падающего кванта будут происходить переходы электронов между уровнями. Необходимым условием переходов является равенство энергии падающего кванта (h ) и разности энергий между уровнями электронов с различными спинами (gb. H).
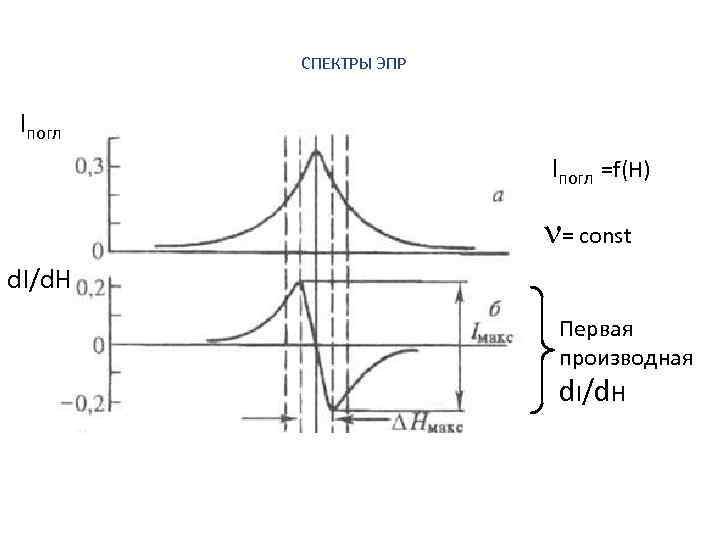
СПЕКТРЫ ЭПР Iпогл =f(H) = const d. I/d. H Первая производная d. I/d. H

ИСПОЛЬЗОВАНИЕ ЭПР ДЛЯ БЕЛКОВ – МЕТОД СПИНОВЫХ МЕТОК. В ИХ РОЛИ – НИТРОКСИЛЬНЫЕ РАДИКАЛЫ Формула спинового зонда ТЕМПО и его спектр ЭПР. В этом радикале неспаренный электрон локализован около ядра азота, магнитное поле которого накладывается на внешнее магнитное поле.

ЯДЕРНЫЙ МАГНИТНЫЙ РЕЗОНАНС

Ядерный магнитный резонанс (ЯМР) – резонансное поглощение электромагнитной энергии веществом, обусловленное переориентацией магнитных моментов атомных ядер.

Наблюдается в сильном постоянном магнитном поле H 0, на которое накладывается слабое радиочастотное магнитное поле H ^ H 0. Резонансный характер явления определяется свойствами ядер, обладающих моментом количества движения и магнитным моментом.

ЯДЕРНЫЙ МАГНИТНЫЙ РЕЗОНАНС Н 0 УСЛОВИЕ РЕЗОНАНСА Н 0 Н 0 – напряженность магнитного поля - магнитное квантовое число
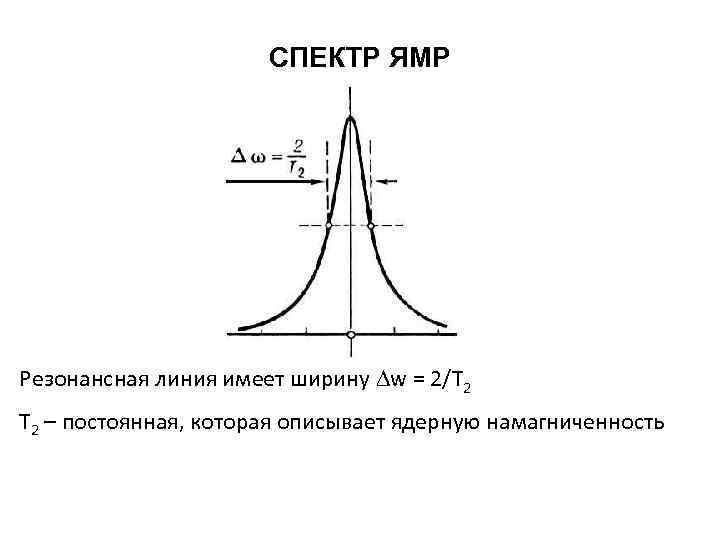
СПЕКТР ЯМР Резонансная линия имеет ширину w = 2/T 2 Т 2 – постоянная, которая описывает ядерную намагниченность
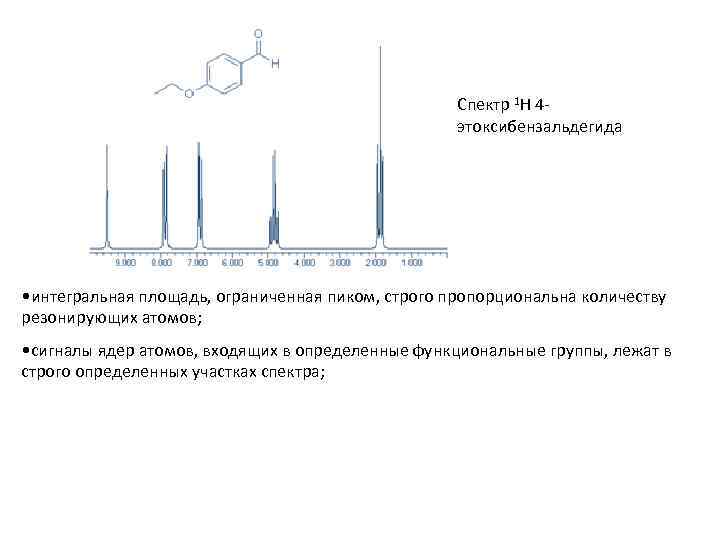
Спектр 1 H 4 этоксибензальдегида • интегральная площадь, ограниченная пиком, строго пропорциональна количеству резонирующих атомов; • сигналы ядер атомов, входящих в определенные функциональные группы, лежат в строго определенных участках спектра;

ХИМИЧЕСКИЙ СДВИГ Положение сигнала в спектрах ЯМР характеризуют ХИМИЧЕСКИМ СДВИГОМ их относительно эталонного сигнала Экспериментальные значения резонансных линий в ЯМР для ядер в атомах и молекулах отличаются от теоретического значения, рассчитанного для свободного ядра. Это связано с эффектом экранирования, который обеспечивается влиянием локального магнитного поля. Оно, в свою очередь, создается внутри атома электронными токами, которые индуцируются внешним магнитным полем. Следствием вышесказанного является смещение резонансной частоты из-за химического окружения. Это явление называют ХИМИЧЕСКИМ СДВИГОМ.
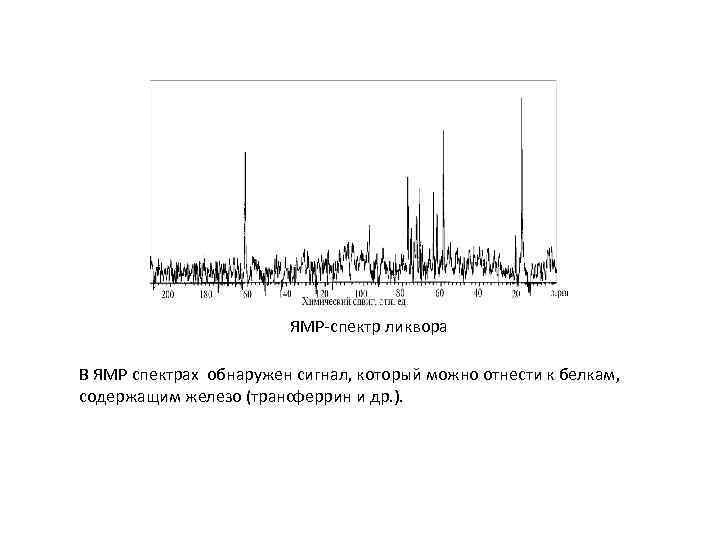
ЯМР-спектр ликвора В ЯМР спектрах обнаружен сигнал, который можно отнести к белкам, содержащим железо (трансферрин и др. ).

ДОМЕННАЯ СТРУКТУРА БЕЛКА ДОМЕНЫ – ОБЛАСТИ В ТРЕТИЧНОЙ СТРУКТУРЕ БЕЛКА С ОПРЕДЕЛЕННОЙ СТРУКТУРНОЙ АВТОНОМИЕЙ, ПОДУРОВЕНЬ СТРУКТУРНОЙ ОРГАНИЗАЦИИ БЕЛКА НА ПУТИ ОТ ВТОРИЧНОЙ К ТРЕТИЧНОЙ СТРУКТУРЕ.

ВПЕРВЫЕ ДОМЕННАЯ СТРУКТУРА ПОКАЗАНА НА ПРИМЕРЕ ЛИЗОЦИМА, ИММУНОГЛОБУЛИНОВ, ХИМОТРИПСИНА, ПАПАИНА И ДР. Домены в структуре протеолитического фермента папайи - папаина. Прерывистыми линиями намечено направление впадины между двумя доменами, в которой связывается субстрат и размещен каталитический центр. Дисульфидные связи заштрихованы

РАЗЛИЧАЮТ ДВА ВИДА ДОМЕНОВ (Д. УЕТЛАУФЕР) • С НЕПРЕРЫВНОЙ ПОЛИПЕПТИДНОЙ ЦЕПЬЮ • С РАЗРЫВНОЙ ПОЛИПЕПТИДНОЙ ЦЕПЬЮ ОБЛАСТЬ, ОБЪЕДИНЯЮЩАЯ ДОМЕНЫ – ЯДРО (НУКЛЕАЦИЯ)

ТРЕТИЧНАЯ СТРУКТУРА БЕЛКА И СИЛЫ, ЕЁ СТАБИЛИЗИРУЮЩИЕ

Третичная структура белка: пространственная ориентация полипептидной спирали или способ укладки полипептидной цепи в определенном объеме.
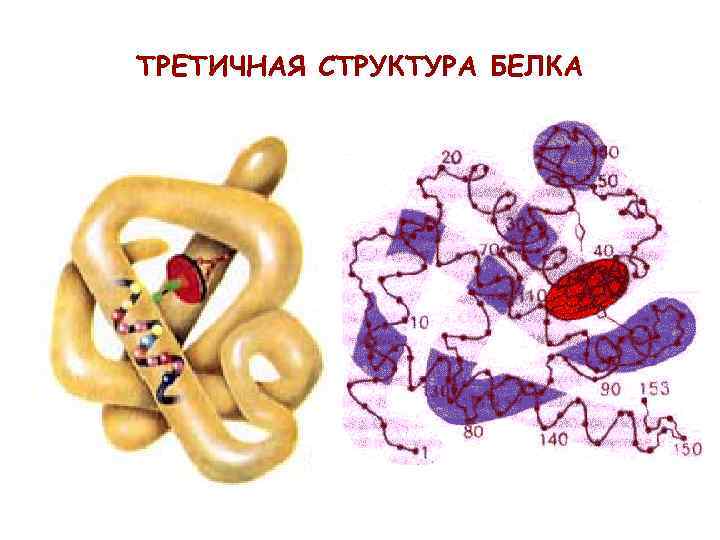
ТРЕТИЧНАЯ СТРУКТУРА БЕЛКА
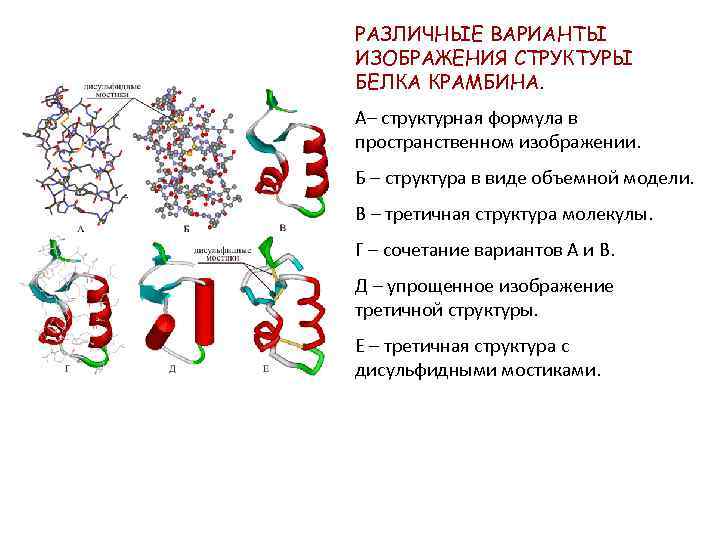
РАЗЛИЧНЫЕ ВАРИАНТЫ ИЗОБРАЖЕНИЯ СТРУКТУРЫ БЕЛКА КРАМБИНА. А– структурная формула в пространственном изображении. Б – структура в виде объемной модели. В – третичная структура молекулы. Г – сочетание вариантов А и В. Д – упрощенное изображение третичной структуры. Е – третичная структура с дисульфидными мостиками.
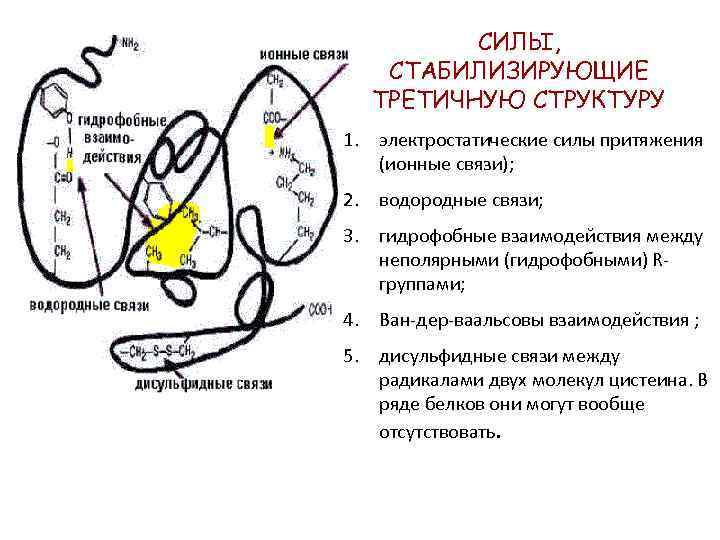
СИЛЫ, СТАБИЛИЗИРУЮЩИЕ ТРЕТИЧНУЮ СТРУКТУРУ 1. электростатические силы притяжения (ионные связи); 2. водородные связи; 3. гидрофобные взаимодействия между неполярными (гидрофобными) Rгруппами; 4. Ван-дер-ваальсовы взаимодействия ; 5. дисульфидные связи между радикалами двух молекул цистеина. В ряде белков они могут вообще отсутствовать.
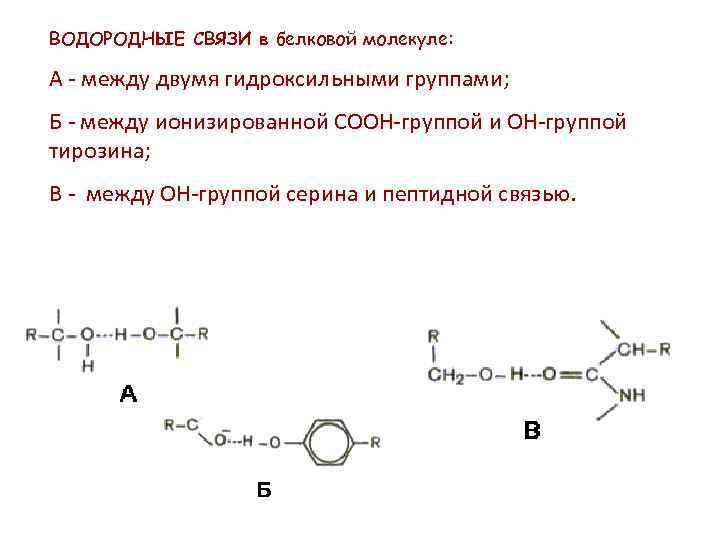
ВОДОРОДНЫЕ СВЯЗИ в белковой молекуле: А - между двумя гидроксильными группами; Б - между ионизированной СООН-группой и ОН-группой тирозина; В - между ОН-группой серина и пептидной связью.
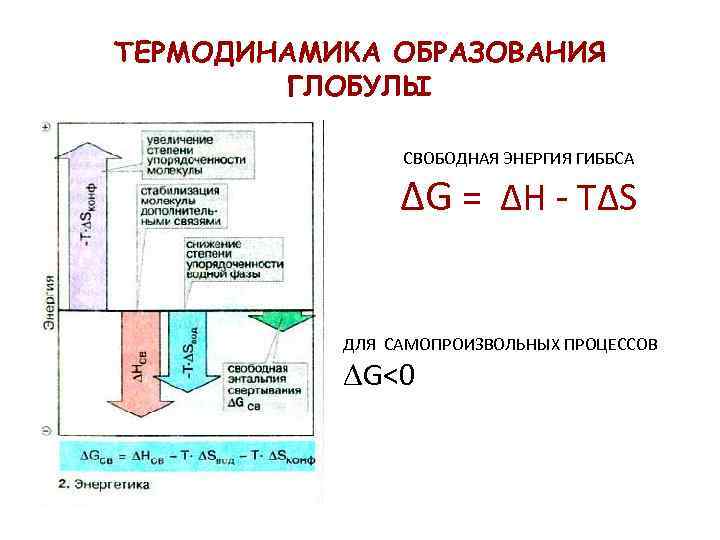
ТЕРМОДИНАМИКА ОБРАЗОВАНИЯ ГЛОБУЛЫ СВОБОДНАЯ ЭНЕРГИЯ ГИББСА ΔG = ΔH - TΔS ДЛЯ САМОПРОИЗВОЛЬНЫХ ПРОЦЕССОВ G<0

ДЛЯ САМОПРОИЗВОЛЬНО ПРОТЕКАЮЩИХ ПРОЦЕССОВ ВЫГОДНО УМЕНЬШЕНИЕ ЭНТАЛЬПИИ или УВЕЛИЧЕНИЕ ЭНТРОПИИ. ОБРАЗОВАНИЕ СВЯЗЕЙ РАЗРЫВ СВЯЗЕЙ ЭНТАЛЬПИЯ СНИЖАЕТСЯ ЭНТАЛЬПИЯ ПОВЫШАЕТСЯ. ΔG<0.

При свертывании белковой глобулы выигрыша в числе водородных связей не происходит, т. к. одновременно утрачиваются водородные связи полипептидная цепь – вода. При свертывании глобулы убывает энтропия пептидной цепи, но одновременно происходит возрастание энтропии растворителя - воды, что играет решающую роль в стабилизации третичной структуры белка.

СТЕПЕНЬ ГИДРОФОБНОСТИ АМИНОКИСЛОТЫ ОПРЕДЕЛЯЮТ ПО РАЗНОСТИ СВОБОДНЫХ ЭНЕРГИЙ ЕЕ РАСТВОРЕНИЯ В СЛАБОПОЛЯРНОМ РАСТВОРИТЕЛЕ И ВОДЕ ГИДРОФОБНЫЕ АМИНОКИСЛОТЫ: ЛЕЙ, ВАЛ, ЛИЗ, ГИС ТРИ, ИЛЕ, ТИР, ФЕН, ПРО, АЛА, АРГ, ЦИС, ГЛУ, АСП, ТРЕ, СЕР, ГЛИ, АСН, ГЛН ГИДРОФИЛЬНЫЕ АМИНОКИСЛОТЫ: ГИПОТЕЗА ОБ ОПРЕДЕЛЯЮЩЕЙ РОЛИ ГИДРОФОБНЫХ ВЗАИМОДЕЙСТВИЙ ДОКАЗАНА В 1944.
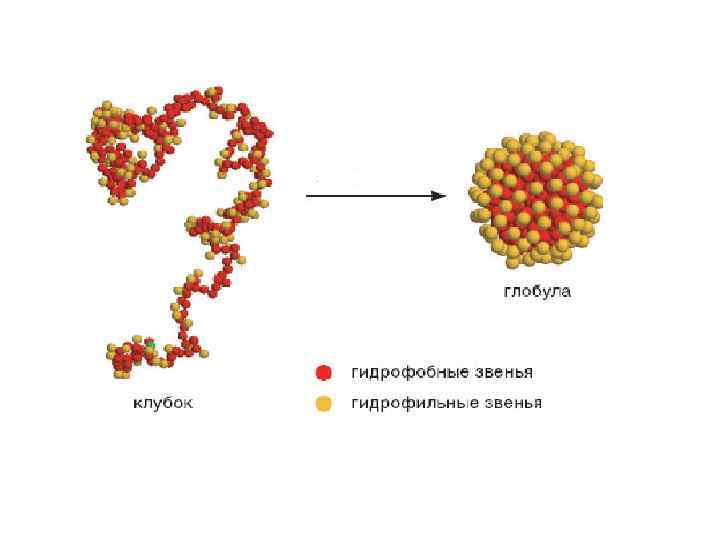

В 1964 году Фишер установил, что, зная общее число аминокислотных остатков в ядре и отношение полярных остатков к неполярным, можно предсказать форму глобулы.

bs - отношение числа полярных остатков к неполярным.
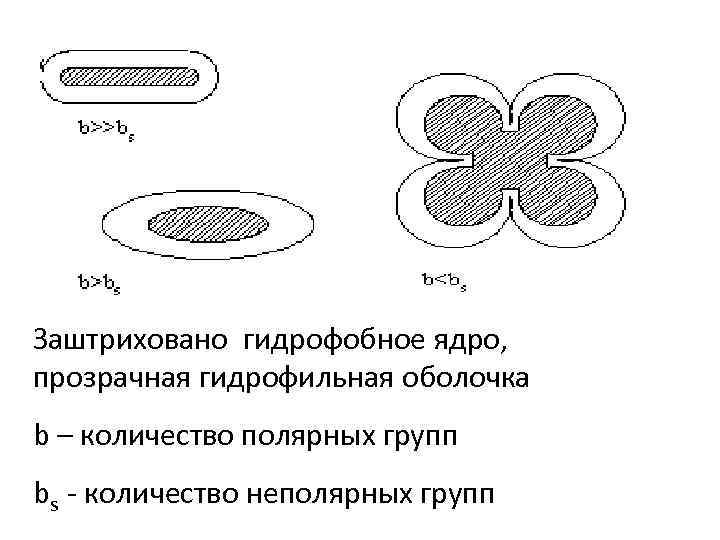
Заштриховано гидрофобное ядро, прозрачная гидрофильная оболочка b – количество полярных групп bs - количество неполярных групп
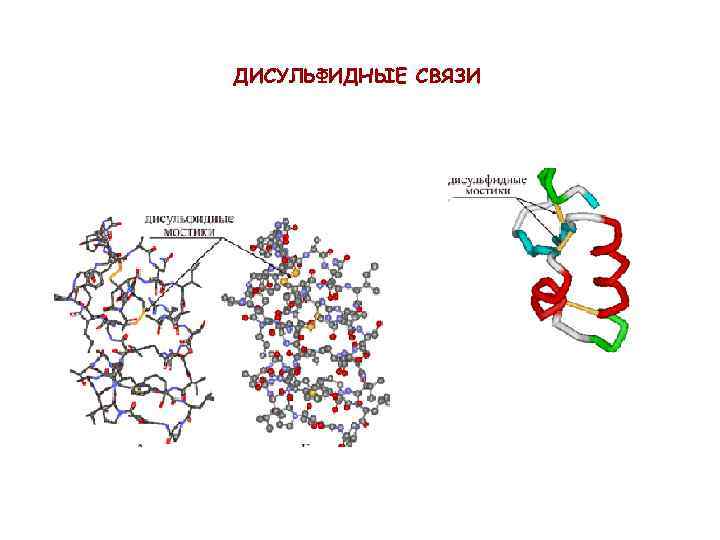
ДИСУЛЬФИДНЫЕ СВЯЗИ

ОСНОВНЫЕ ТИПЫ ДВИЖЕНИЙ В БЕЛКОВОЙ МОЛЕКУЛЕ

ØАтомные флуктуации (несогласованные перемещения отдельных атомов, например, повороты на 20 - 60º вокруг простых связей пептидного скелета и боковых групп) ØКоллективные (согласованные) перемещения групп атомов (от нескольких до сотен) ØИндуцированные внешними факторами изменения конформации

ЧЕТВЕРТИЧНАЯ СТРУКТУРА БЕЛКА Гидрофильные остатки не полностью покрывают гидрофобное ядро, что приводит к образованию надмолекулярных структур.
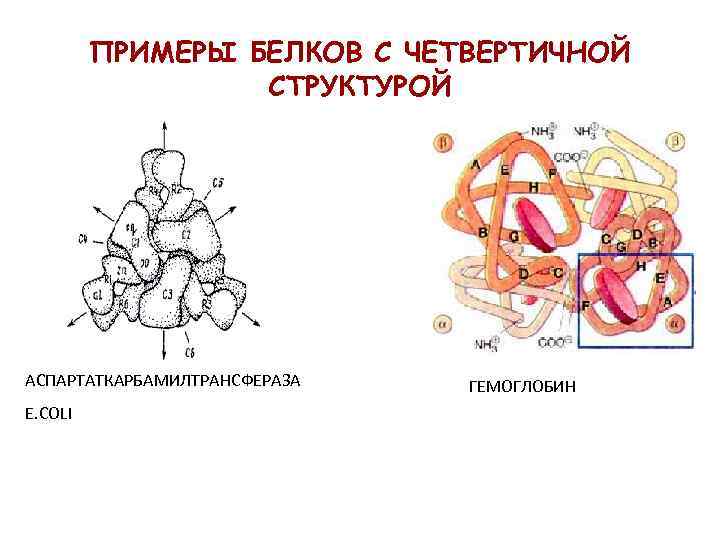
ПРИМЕРЫ БЕЛКОВ С ЧЕТВЕРТИЧНОЙ СТРУКТУРОЙ АСПАРТАТКАРБАМИЛТРАНСФЕРАЗА E. COLI ГЕМОГЛОБИН

РОЛЬ ЧЕТВЕРТИЧНОЙ СТРУКТУРЫ 1. АРХИТЕКТУРНАЯ ФУНКЦИЯ 2. ОБЕСПЕЧЕНИЕ МНОЖЕСТВЕННЫХ ВЗАИМОДЕЙСТВИЙ БЕЛКА С ПРОТЯЖЕННЫМИ СТРУКТУРАМИ 3. РЕГУЛЯТОРНАЯ ФУНКЦИЯ 4. ОБЪЕДИНЕНИЕ НЕСКОЛЬКИХ ВЗАИМОСВЯЗАННЫХ ФУНКЦИЙ В ЕДИНОЙ СТРУКТУРЕ

Удачной сессии!
простр структуры белка_методы_12.ppt