ПИН И ВИН 2.ppt
- Количество слайдов: 32
 ПЕРВИЧНАЯ ИММУННАЯ НЕДОСТАТОЧНОСТЬ
ПЕРВИЧНАЯ ИММУННАЯ НЕДОСТАТОЧНОСТЬ
 Первичная иммунная недостаточность – это врожденные нарушения системы иммунитета, связанные с генетическими дефектами одного или нескольких ее компонентов: клеточного и гуморального иммунитета, фагоцитоза, комплемента К первичным ИДС относят случаи стойкого нарушения конечной эффекторной функции поврежденного звена, характеризующиеся стабильностью и воспроизводимыми лабораторными характеристиками. Частота ПИН в целом составляет 1 случай на 10– 100 тыс. живых новорождённых Селективный дефицит Ig. A встречается гораздо чаще — 1 на 500– 1500 жителей общей популяции
Первичная иммунная недостаточность – это врожденные нарушения системы иммунитета, связанные с генетическими дефектами одного или нескольких ее компонентов: клеточного и гуморального иммунитета, фагоцитоза, комплемента К первичным ИДС относят случаи стойкого нарушения конечной эффекторной функции поврежденного звена, характеризующиеся стабильностью и воспроизводимыми лабораторными характеристиками. Частота ПИН в целом составляет 1 случай на 10– 100 тыс. живых новорождённых Селективный дефицит Ig. A встречается гораздо чаще — 1 на 500– 1500 жителей общей популяции
 На сегодня расшифрованы десятки разнообразных генетических дефектов, приводящих к стойким иммунным дисфункциям. Такие дефекты обнаружены в 13 из 23 соматических и половых хромосом, картированы дефектные гены, установлены связанные с ними аномальные продукты и пораженные клетки различных форм ПИН. Фенотипическая классификация ПИН: • синдромы недостаточности антител (гуморальные иммунодефициты); • преимущественно клеточные (лимфоидные) дефекты иммунитета; • синдромы ТКИН; • дефекты фагоцитоза; • дефицит комплемента; • первичные ИДС, ассоциированные с другими главными дефектами (другие четко очерченные первичные ИДС)
На сегодня расшифрованы десятки разнообразных генетических дефектов, приводящих к стойким иммунным дисфункциям. Такие дефекты обнаружены в 13 из 23 соматических и половых хромосом, картированы дефектные гены, установлены связанные с ними аномальные продукты и пораженные клетки различных форм ПИН. Фенотипическая классификация ПИН: • синдромы недостаточности антител (гуморальные иммунодефициты); • преимущественно клеточные (лимфоидные) дефекты иммунитета; • синдромы ТКИН; • дефекты фагоцитоза; • дефицит комплемента; • первичные ИДС, ассоциированные с другими главными дефектами (другие четко очерченные первичные ИДС)
 КЛИНИЧЕСКИ ПЕРВИЧНАЯ ИММУННАЯ НЕДОСТАТОЧНОСТЬ ПРОЯВЛЯЕТСЯ В ВИДЕ СЛЕДУЮЩИХ ОСНОВНЫХ СИМПТОМОКОМПЛЕКСОВ Инфекционного Его особенности: политопность инфекций, упорное или непрерывно рецидивирующее течение, недостаточность эффекта противомикробной терапии, поствакцинальные инфекции Аллергического аллергические проявления присущи таким формам ПИН, как селективная недостаточность Ig. A, синдром Вискотта-Олдрича Аутоиммунного Возможно формирование различных аутоиммунных синдромов: системной красной волчанки, синдрома Шегрена, хронического активного гепатита, гемолитической анемии, тромбоцитопении и др. Онкологического Частота злокачественных новообразований в несколько раз выше, чем в целом в популяции. Особенно часто опухоли наблюдаются у больных атаксией-телеангиоэктазией и синдромом Вискотта-Олдрича (чаще лимфоретикулярные опухоли)
КЛИНИЧЕСКИ ПЕРВИЧНАЯ ИММУННАЯ НЕДОСТАТОЧНОСТЬ ПРОЯВЛЯЕТСЯ В ВИДЕ СЛЕДУЮЩИХ ОСНОВНЫХ СИМПТОМОКОМПЛЕКСОВ Инфекционного Его особенности: политопность инфекций, упорное или непрерывно рецидивирующее течение, недостаточность эффекта противомикробной терапии, поствакцинальные инфекции Аллергического аллергические проявления присущи таким формам ПИН, как селективная недостаточность Ig. A, синдром Вискотта-Олдрича Аутоиммунного Возможно формирование различных аутоиммунных синдромов: системной красной волчанки, синдрома Шегрена, хронического активного гепатита, гемолитической анемии, тромбоцитопении и др. Онкологического Частота злокачественных новообразований в несколько раз выше, чем в целом в популяции. Особенно часто опухоли наблюдаются у больных атаксией-телеангиоэктазией и синдромом Вискотта-Олдрича (чаще лимфоретикулярные опухоли)
 НАСТОРАЖИВАЮЩИЕ ПРИЗНАКИ ПЕРВИЧНОЙ ИММУННОЙ НЕДОСТАТОЧНОСТИ 1. Частые отиты (не менее 6 -8 раз в течении одного года) 2. Несколько подтвержденных серьезных синуситов (не менее 4 -6 в год) 3. 2 и более пневмонии в течении года 4. Повторные глубокие абсцессы кожи или внутренних органов 5. Потребность в длительной терапии антибиотиками для купирования инфекций (до 2 месяцев или более) 6. Потребность во внутривенном введении больших доз антибиотиков для купирования инфекций 7. Не менее двух глубоких инфекций, таких как менингит, остеомиелит, сепсис 8. Отставание грудного ребенка в росте и весе 9. Персистирующая молочница или грибковое поражение кожи в возрасте старше одного года 10. Наличие у родственников первичных иммунодефицитов, ранние смерти от тяжелых инфекций или один из названных признаков
НАСТОРАЖИВАЮЩИЕ ПРИЗНАКИ ПЕРВИЧНОЙ ИММУННОЙ НЕДОСТАТОЧНОСТИ 1. Частые отиты (не менее 6 -8 раз в течении одного года) 2. Несколько подтвержденных серьезных синуситов (не менее 4 -6 в год) 3. 2 и более пневмонии в течении года 4. Повторные глубокие абсцессы кожи или внутренних органов 5. Потребность в длительной терапии антибиотиками для купирования инфекций (до 2 месяцев или более) 6. Потребность во внутривенном введении больших доз антибиотиков для купирования инфекций 7. Не менее двух глубоких инфекций, таких как менингит, остеомиелит, сепсис 8. Отставание грудного ребенка в росте и весе 9. Персистирующая молочница или грибковое поражение кожи в возрасте старше одного года 10. Наличие у родственников первичных иммунодефицитов, ранние смерти от тяжелых инфекций или один из названных признаков
 I. Первичные иммунодефициты с дефектами иммуноглобулинов Х–СЦЕПЛЕННАЯ АГАММАГЛОБУЛИНЕМИЯ БРУТОНА Болеют мальчики, матери которых — носительницы дефектной хромосомы X. Дефектен один ген в хромосоме X (Xq 22), кодирующий B– лимфоцит–специфичную протеинтирозинкиназу (обозначена в честь Брутона как Btk) Лабораторные данные • стойкое снижение концентрации Ig. G в сыворотке (менее 200 мг/дл), отсутствие Ig. M, Ig. A, Ig. E, Ig. D; • глубокий дефицит В-клеток (CD 19 -22, CD 72<1% от числа циркулирующих лимфоцитов). • число T–лимфоцитов и функциональные тесты на T–лимфоциты в норме
I. Первичные иммунодефициты с дефектами иммуноглобулинов Х–СЦЕПЛЕННАЯ АГАММАГЛОБУЛИНЕМИЯ БРУТОНА Болеют мальчики, матери которых — носительницы дефектной хромосомы X. Дефектен один ген в хромосоме X (Xq 22), кодирующий B– лимфоцит–специфичную протеинтирозинкиназу (обозначена в честь Брутона как Btk) Лабораторные данные • стойкое снижение концентрации Ig. G в сыворотке (менее 200 мг/дл), отсутствие Ig. M, Ig. A, Ig. E, Ig. D; • глубокий дефицит В-клеток (CD 19 -22, CD 72<1% от числа циркулирующих лимфоцитов). • число T–лимфоцитов и функциональные тесты на T–лимфоциты в норме
 Клиническая картина (Болезнь Брутона) Клиническая манифестация со второго полугодия жизни • Для заболевания характерны тяжело протекающие пиогенные инфекции, инфекции органов дыхания (синуситы, отиты, бронхиты, пневмонии), гастроэнтериты, пиодермии, септические артриты (бактериальные или хламидиозные), септицемия, менингиты, Энцефалиты и др. • У больных детей при иммунизации живой полиовакциной, как правило, наблюдают продолжительное выделение через слизистые оболочки вируса полиомиелита, причём с восстановленной и нарастающей вирулентностью. • При осмотре таких детей обращают внимание на отставание в росте, пальцы в виде барабанных палочек, изменение формы грудной клетки, характерные для заболеваний нижних дыхательных путей, гипоплазию лимфатических узлов и миндалин. При гистологическом исследовании лимфоидной ткани — отсутствие герминативных центров и плазматических клеток.
Клиническая картина (Болезнь Брутона) Клиническая манифестация со второго полугодия жизни • Для заболевания характерны тяжело протекающие пиогенные инфекции, инфекции органов дыхания (синуситы, отиты, бронхиты, пневмонии), гастроэнтериты, пиодермии, септические артриты (бактериальные или хламидиозные), септицемия, менингиты, Энцефалиты и др. • У больных детей при иммунизации живой полиовакциной, как правило, наблюдают продолжительное выделение через слизистые оболочки вируса полиомиелита, причём с восстановленной и нарастающей вирулентностью. • При осмотре таких детей обращают внимание на отставание в росте, пальцы в виде барабанных палочек, изменение формы грудной клетки, характерные для заболеваний нижних дыхательных путей, гипоплазию лимфатических узлов и миндалин. При гистологическом исследовании лимфоидной ткани — отсутствие герминативных центров и плазматических клеток.
 Х-СЦЕПЛЕНИЯ АГАММАГЛОБУЛИНЕМИЯ С СИНДРОМОМ ГИПЕРИММУНОГЛОБУЛИНЕМИИ M Болеют мальчики, матери которых — носительницы дефекта. Недостаточность экспрессии CD 40 L в T–лимфоцитах приводит к невозможности переключения синтеза классов иммуноглобулинов в B– лимфоцитах с M на все остальные изотипы. Лабораторные данные. • резкое снижение уровней Ig. G, Ig. A и Ig. E при резко повышенном уровне Ig. M, • количество В-клеток (CD 19 -22) нормальное или субнормальное Клиническая картина. • рекуррентные бактериальные и грибковые инфекции, включая оппортунистические (Pneumocystis carinii). • могут быть лимфаденопатия и спленомегалия. • достаточно часто наблюдаются аутоиммунные цитопении Похожую клиническую картину описывают для предположительно аутосомного типа наследования патологии
Х-СЦЕПЛЕНИЯ АГАММАГЛОБУЛИНЕМИЯ С СИНДРОМОМ ГИПЕРИММУНОГЛОБУЛИНЕМИИ M Болеют мальчики, матери которых — носительницы дефекта. Недостаточность экспрессии CD 40 L в T–лимфоцитах приводит к невозможности переключения синтеза классов иммуноглобулинов в B– лимфоцитах с M на все остальные изотипы. Лабораторные данные. • резкое снижение уровней Ig. G, Ig. A и Ig. E при резко повышенном уровне Ig. M, • количество В-клеток (CD 19 -22) нормальное или субнормальное Клиническая картина. • рекуррентные бактериальные и грибковые инфекции, включая оппортунистические (Pneumocystis carinii). • могут быть лимфаденопатия и спленомегалия. • достаточно часто наблюдаются аутоиммунные цитопении Похожую клиническую картину описывают для предположительно аутосомного типа наследования патологии
 ОБЩИЙ ВАРИАБЕЛЬНЫЙ ИММУНОДЕФИЦИТ Этот синдром может впервые манифестировать как в раннем детстве, так и подростковом возрасте или у молодых людей. Молекулярный дефект точно неизвестен. Лабораторные данные. • Существенно снижены уровни Ig. G и Ig. A, примерно у 50% больных — и Ig. M (вплоть до полностью неопределимых количеств). • Число B–лимфоцитов в крови может быть в норме или снижено. • Число T–лимфоцитов у большинства больных в норме Клиническая картина. Рекуррентные бактериальные инфекции, преобладает синопульмонарная локализация. Возможны гастроинтестинальные инфекции с диареей, стеатореей и мальабсорбцией. От агаммаглобулинемии Брутона вариабельный иммунодефицит отличают следующие признаки: 1. более поздний возраст манифестации; 2. равное распределение по полу; 3. возможны тенденции к дефектному функционированию и T–лимфоцитов; 4. тенденция к развитию аутоиммунной патологии (цитопении); 5. повышенная частота лимфом;
ОБЩИЙ ВАРИАБЕЛЬНЫЙ ИММУНОДЕФИЦИТ Этот синдром может впервые манифестировать как в раннем детстве, так и подростковом возрасте или у молодых людей. Молекулярный дефект точно неизвестен. Лабораторные данные. • Существенно снижены уровни Ig. G и Ig. A, примерно у 50% больных — и Ig. M (вплоть до полностью неопределимых количеств). • Число B–лимфоцитов в крови может быть в норме или снижено. • Число T–лимфоцитов у большинства больных в норме Клиническая картина. Рекуррентные бактериальные инфекции, преобладает синопульмонарная локализация. Возможны гастроинтестинальные инфекции с диареей, стеатореей и мальабсорбцией. От агаммаглобулинемии Брутона вариабельный иммунодефицит отличают следующие признаки: 1. более поздний возраст манифестации; 2. равное распределение по полу; 3. возможны тенденции к дефектному функционированию и T–лимфоцитов; 4. тенденция к развитию аутоиммунной патологии (цитопении); 5. повышенная частота лимфом;
 ДЕФИЦИТ ИММУНОГЛОБУЛИНА A Молекулярный дефект точно не известен Дефицит иммуноглобулина A, при наличии иммуноглобулинов других классов встречается с высокой частотой в общей популяции: 1 случай на 500– 1500 жителей. Недостаточность Ig. A может быть: • частичной (30% случаев) • полной (70% случаев). Дефицит подкласса Ig. A 2 приводит к более выраженной клинической патологии, чем дефицит подкласса Ig. A 1 Клиническая картина. • В 50% случаев никаких специфических клинических проявлений нет, • В 50% — рекуррентные инфекции верхних дыхательных путей. • У пациентов с аллергией дефицит Ig. A встречается чаще, чем у остального населения. Соответственно у таких пациентов имеется клиническая картина аллергического заболевания.
ДЕФИЦИТ ИММУНОГЛОБУЛИНА A Молекулярный дефект точно не известен Дефицит иммуноглобулина A, при наличии иммуноглобулинов других классов встречается с высокой частотой в общей популяции: 1 случай на 500– 1500 жителей. Недостаточность Ig. A может быть: • частичной (30% случаев) • полной (70% случаев). Дефицит подкласса Ig. A 2 приводит к более выраженной клинической патологии, чем дефицит подкласса Ig. A 1 Клиническая картина. • В 50% случаев никаких специфических клинических проявлений нет, • В 50% — рекуррентные инфекции верхних дыхательных путей. • У пациентов с аллергией дефицит Ig. A встречается чаще, чем у остального населения. Соответственно у таких пациентов имеется клиническая картина аллергического заболевания.
 ТРАНЗИТОРНАЯ ГИПОГАММАГЛОБУЛИНЕМИЯ У ДЕТЕЙ У здоровых новорожденных минимальный уровень иммуноглобулинов в крови устанавливается к 3–месячному возрасту: к этому времени значительная часть иммуноглобулинов материнского происхождения, попавших к ребенку внутриутробно через плаценту, распадается, а выработка собственных иммуноглобулинов только начинается. С 3– месячного возраста нарастание в крови уровня иммуноглобулинов происходит уже «собственными силами» ребенка. У некоторых детей, однако, выработка собственных иммуноглобулинов может задерживаться и становится определимой только к 1, 5– 3 годам. Клиническая картина. Является доброкачественным иммунодефицитным состоянием. • Может обнаруживаться у практически здоровых детей как случайная находка. • Однако у детей часто выявляют повышенную частоту респираторных инфекций, инфекций ЛОР-органов, кожи, мочеполовых и кишечных инфекций с благоприятной эволюцией (после 7 лет инфекционная симптоматика неотличима от таковой у здоровых детей)
ТРАНЗИТОРНАЯ ГИПОГАММАГЛОБУЛИНЕМИЯ У ДЕТЕЙ У здоровых новорожденных минимальный уровень иммуноглобулинов в крови устанавливается к 3–месячному возрасту: к этому времени значительная часть иммуноглобулинов материнского происхождения, попавших к ребенку внутриутробно через плаценту, распадается, а выработка собственных иммуноглобулинов только начинается. С 3– месячного возраста нарастание в крови уровня иммуноглобулинов происходит уже «собственными силами» ребенка. У некоторых детей, однако, выработка собственных иммуноглобулинов может задерживаться и становится определимой только к 1, 5– 3 годам. Клиническая картина. Является доброкачественным иммунодефицитным состоянием. • Может обнаруживаться у практически здоровых детей как случайная находка. • Однако у детей часто выявляют повышенную частоту респираторных инфекций, инфекций ЛОР-органов, кожи, мочеполовых и кишечных инфекций с благоприятной эволюцией (после 7 лет инфекционная симптоматика неотличима от таковой у здоровых детей)
 II. Первичные иммунодефициты с дефектами Т-лимфоцитов СИНДРОМ ДИ ДЖОРДЖИ В основе лежит порок развития третьего-четвертого глоточных карманов, приводящий к агенезии или дисгенезии паращитовидных желез и тимуса Клиническая картина характеризуется классической триадой: 1. гипоплазия тимуса - рецидивирующие вирусные и грибковые заболевания кожи и слизистых, диарея 2. гипоплазия паращитовидных желез (в большинстве случаев) - гипокальцемические судороги 3. врожденный пороки сердца и магистральных сосудов (в значительной части случаев) Часто сочетается - с пороками развития лицевого скелета Лабораторные данные: Количесвенные показатели Т-клеток варьируют от нормы до резкого снижения. Сохранность В-звена иммунитета
II. Первичные иммунодефициты с дефектами Т-лимфоцитов СИНДРОМ ДИ ДЖОРДЖИ В основе лежит порок развития третьего-четвертого глоточных карманов, приводящий к агенезии или дисгенезии паращитовидных желез и тимуса Клиническая картина характеризуется классической триадой: 1. гипоплазия тимуса - рецидивирующие вирусные и грибковые заболевания кожи и слизистых, диарея 2. гипоплазия паращитовидных желез (в большинстве случаев) - гипокальцемические судороги 3. врожденный пороки сердца и магистральных сосудов (в значительной части случаев) Часто сочетается - с пороками развития лицевого скелета Лабораторные данные: Количесвенные показатели Т-клеток варьируют от нормы до резкого снижения. Сохранность В-звена иммунитета
 III. Комбинированные иммунодефициты Тяжелый комбинированный иммунодефицит с ретикулярной дисгенезией Нарушена дифференцировка и пролиферация гемопоэтической стволовой клетки в лимфоидную и миелоидную стволовую клетку Клиническая картина типична: после нескольких недель благополучия у ребенка происходит остановка роста и развития, возникают неукротимый понос, рвота, обширная молочница, нарастающая одышка, сухой кашель Дети погибают в первые месяцы жизни от септического процесса. Без радикальной иммунореконструктивной терапии (пересадка HLAсовместимого костного мозга) заболевание инвариантно заканчивается летально на 1 -м году жизни. Лабораторные данные: агранулоцитоз, отсутствие Т и Влимфоцитов
III. Комбинированные иммунодефициты Тяжелый комбинированный иммунодефицит с ретикулярной дисгенезией Нарушена дифференцировка и пролиферация гемопоэтической стволовой клетки в лимфоидную и миелоидную стволовую клетку Клиническая картина типична: после нескольких недель благополучия у ребенка происходит остановка роста и развития, возникают неукротимый понос, рвота, обширная молочница, нарастающая одышка, сухой кашель Дети погибают в первые месяцы жизни от септического процесса. Без радикальной иммунореконструктивной терапии (пересадка HLAсовместимого костного мозга) заболевание инвариантно заканчивается летально на 1 -м году жизни. Лабораторные данные: агранулоцитоз, отсутствие Т и Влимфоцитов
 III. Комбинированные иммунодефициты Недостаточность аденозин-дезаминазы Дефицит этого фермента в эритроцитах и лимфоцитах ведет к накоплению дезоксиаденозина, токсично действующего на Тлимфоциты Клинически проявляется сразу после рождения, сочетается с с аномалиями развития скелета (деформация, окостенение), выявляются признаки инволюции вилочковой железы Лабораторные данные: лимфоцитопения, недостаточность преимущественно Т-лимфоцитов
III. Комбинированные иммунодефициты Недостаточность аденозин-дезаминазы Дефицит этого фермента в эритроцитах и лимфоцитах ведет к накоплению дезоксиаденозина, токсично действующего на Тлимфоциты Клинически проявляется сразу после рождения, сочетается с с аномалиями развития скелета (деформация, окостенение), выявляются признаки инволюции вилочковой железы Лабораторные данные: лимфоцитопения, недостаточность преимущественно Т-лимфоцитов
 IV. ДЕФЕКТЫ ФАГОЦИТОЗА ХРОНИЧЕСКАЯ ГРАНУЛЕМАТОЗНАЯ БОЛЕЗНЬ Преобладает X-сцепленный тип наследования (80% больных – мужского пола), существует аутосомно-рецессивная форма заболевания В основе лежит нарушение бактерицидной функции нейтрофилов (неспособность вырабатывать активные формы кислорода) Клиническая картина: Манифестирует в раннем детстве, изредка – в подростковом возрасте • гнойные инфекции кожи и подкожной клетчатки; • БЦЖ-ит; • абсцессы печени, частые лимфадениты, легочные инфекции; • афтозный стоматит, множественный кариес Рецидивирующие инфекции, обусловленные микроорганизмами, вырабатывающими каталазу (Staph. aureus, Escherichia, Pseudomonas), а также различными видами Aspergillus, вызывающими пневмонии и Candida с поражением мягких тканей Лабораторные данные: определение фагоцитарного индекса НСТ-теста
IV. ДЕФЕКТЫ ФАГОЦИТОЗА ХРОНИЧЕСКАЯ ГРАНУЛЕМАТОЗНАЯ БОЛЕЗНЬ Преобладает X-сцепленный тип наследования (80% больных – мужского пола), существует аутосомно-рецессивная форма заболевания В основе лежит нарушение бактерицидной функции нейтрофилов (неспособность вырабатывать активные формы кислорода) Клиническая картина: Манифестирует в раннем детстве, изредка – в подростковом возрасте • гнойные инфекции кожи и подкожной клетчатки; • БЦЖ-ит; • абсцессы печени, частые лимфадениты, легочные инфекции; • афтозный стоматит, множественный кариес Рецидивирующие инфекции, обусловленные микроорганизмами, вырабатывающими каталазу (Staph. aureus, Escherichia, Pseudomonas), а также различными видами Aspergillus, вызывающими пневмонии и Candida с поражением мягких тканей Лабораторные данные: определение фагоцитарного индекса НСТ-теста
 V. Дефицит комплимента Локализация дефекта Развивающаяся патология С 1 СКВ, васкулит, гломерулонефрит С 2 СКВ, дискоидная волчанка, дерматомиозит, гломерулонефрит, геморрагический васкулит С 3 Рецидивирующие бактериальные инфекции: пневмония, менингит, отит, сепсис С 4 СКВ С 5 СКВ, васкулит, гломерулонефрит, опоясывающий лишай, гоно- и менингококковый сепсис, экзема С 6 Синдром Рейно, гоно- и менингококковый сепсис С 7 Синдром Рейно, инфекция мочевыводящих путей, менингит, сепсис С 8 СКВ, стафило- и гонококковые инфекции, сепсис С 9 Перемежающаяся лихорадка
V. Дефицит комплимента Локализация дефекта Развивающаяся патология С 1 СКВ, васкулит, гломерулонефрит С 2 СКВ, дискоидная волчанка, дерматомиозит, гломерулонефрит, геморрагический васкулит С 3 Рецидивирующие бактериальные инфекции: пневмония, менингит, отит, сепсис С 4 СКВ С 5 СКВ, васкулит, гломерулонефрит, опоясывающий лишай, гоно- и менингококковый сепсис, экзема С 6 Синдром Рейно, гоно- и менингококковый сепсис С 7 Синдром Рейно, инфекция мочевыводящих путей, менингит, сепсис С 8 СКВ, стафило- и гонококковые инфекции, сепсис С 9 Перемежающаяся лихорадка
 Дефекты регуляции системы комплимента Наследственный ангионевротический отек * (НАО) передается по аутосомно-доминантному признаку и проявляется дефицитом (I тип) или функциональной неполноценностью (II тип) фермента – эстеразы, функция которого состоит в инактивации первого компонента комплимента (С 1 q-ингибитора) В отличие от отека Квинке: • провоцирующие факторы – микротравма, операция, стресс • отек формируется в течении нескольких часов, не сопровождается крапивницей и зудом • лечение антигистаминными препаратами, ГКС – не эффективно • базисная патогенетическая терапия включает прием даназола и станозола, стимулирующих синтез С 1 -ингибитора. Идеальную форму заместительной терапии представляет очищенный С 1 -ингибитор, вводимый при острых эпизодах. В качестве источника С 1 -ингибитора можно использовать свежезамороженную плазму.
Дефекты регуляции системы комплимента Наследственный ангионевротический отек * (НАО) передается по аутосомно-доминантному признаку и проявляется дефицитом (I тип) или функциональной неполноценностью (II тип) фермента – эстеразы, функция которого состоит в инактивации первого компонента комплимента (С 1 q-ингибитора) В отличие от отека Квинке: • провоцирующие факторы – микротравма, операция, стресс • отек формируется в течении нескольких часов, не сопровождается крапивницей и зудом • лечение антигистаминными препаратами, ГКС – не эффективно • базисная патогенетическая терапия включает прием даназола и станозола, стимулирующих синтез С 1 -ингибитора. Идеальную форму заместительной терапии представляет очищенный С 1 -ингибитор, вводимый при острых эпизодах. В качестве источника С 1 -ингибитора можно использовать свежезамороженную плазму.
 V. Иммунодефициты, связанные с другими крупными дефектами СИНДРОМ ВИСКОТТА-ОЛДРИЧА X-сцепленное заболевание, проявляющееся в младенческом или раннем детском возрасте Клиническая картина: - Тромбоцитопения (носовые кровотечения, петехиально-пятнистый тип кровоточивости) - Экзема (атипичный атопический дерматит) - Рецидивирующие, резистентные к лечению инфекции (гнойные и вирусные) Лабораторные данные: Прогрессирующая Т-лимоцитопения, умеренное снижение сывороточных Ig (преимущественно Ig. M)
V. Иммунодефициты, связанные с другими крупными дефектами СИНДРОМ ВИСКОТТА-ОЛДРИЧА X-сцепленное заболевание, проявляющееся в младенческом или раннем детском возрасте Клиническая картина: - Тромбоцитопения (носовые кровотечения, петехиально-пятнистый тип кровоточивости) - Экзема (атипичный атопический дерматит) - Рецидивирующие, резистентные к лечению инфекции (гнойные и вирусные) Лабораторные данные: Прогрессирующая Т-лимоцитопения, умеренное снижение сывороточных Ig (преимущественно Ig. M)
 V. Иммунодефициты, связанные с другими крупными дефектами АТАКСИЯ-ТЕЛЕАНГИОЭКТАЗИЯ (Синдром Луи-Бара) Аутосомно-рецессивный тип наследования Клиническая картина: • прогрессирующая мозжечковая атаксия, • мелкие телеангиоэктазы (преимущественно на склерах), • рецидивирующие сино-пульмональные инфекции • высокая предрасположенность к злокачественным новообразованиям Лабораторные данные: Вариабельное снижение сывороточных иммуноглобулинов. Количество Тлимфоцитов снижено
V. Иммунодефициты, связанные с другими крупными дефектами АТАКСИЯ-ТЕЛЕАНГИОЭКТАЗИЯ (Синдром Луи-Бара) Аутосомно-рецессивный тип наследования Клиническая картина: • прогрессирующая мозжечковая атаксия, • мелкие телеангиоэктазы (преимущественно на склерах), • рецидивирующие сино-пульмональные инфекции • высокая предрасположенность к злокачественным новообразованиям Лабораторные данные: Вариабельное снижение сывороточных иммуноглобулинов. Количество Тлимфоцитов снижено
 ЛЕЧЕНИЕ ПЕРВИЧНОЙ ИММУННОЙ НЕДОСТАТОЧНОСТИ особенности антимикробной терапии (включает антибиотики, противогрибковые и противовирусные средства ) - раннее назначение - препараты широкого спектра действия в максимальных возрастных дозировках - парентеральное введение препаратов - продолжительность курсов 2 -4 недели и более (сроки назначения в 2 -3 раза превосходят стандартные) - многие иммунодефициты, в первую очередь комбинированные и Т-клеточные, требуют постоянной антимикробной терапии, в первую очередь, для профилактики инфицирования условно-патогенной флорой (например, комбинация триметоприм/сульфаметоксазол + кетоконазол + ацикловир).
ЛЕЧЕНИЕ ПЕРВИЧНОЙ ИММУННОЙ НЕДОСТАТОЧНОСТИ особенности антимикробной терапии (включает антибиотики, противогрибковые и противовирусные средства ) - раннее назначение - препараты широкого спектра действия в максимальных возрастных дозировках - парентеральное введение препаратов - продолжительность курсов 2 -4 недели и более (сроки назначения в 2 -3 раза превосходят стандартные) - многие иммунодефициты, в первую очередь комбинированные и Т-клеточные, требуют постоянной антимикробной терапии, в первую очередь, для профилактики инфицирования условно-патогенной флорой (например, комбинация триметоприм/сульфаметоксазол + кетоконазол + ацикловир).
 ЛЕЧЕНИЕ ПЕРВИЧНОЙ ИММУННОЙ НЕДОСТАТОЧНОСТИ Иммунореконструктивные операции - Трансплантация костного мозга - При дефиците аденозиндезаминазы 5 больным (2 в США и 3 в Европе) проведена пересадка гена, кодирующего аденозиндезаминазу с вариабельным эффектом Иммунокоррекция Показана при неглубоких дефектах (селективный Ig. A дефицит)
ЛЕЧЕНИЕ ПЕРВИЧНОЙ ИММУННОЙ НЕДОСТАТОЧНОСТИ Иммунореконструктивные операции - Трансплантация костного мозга - При дефиците аденозиндезаминазы 5 больным (2 в США и 3 в Европе) проведена пересадка гена, кодирующего аденозиндезаминазу с вариабельным эффектом Иммунокоррекция Показана при неглубоких дефектах (селективный Ig. A дефицит)
 Заместительная терапия - При гуморальных иммунодефицитах проводится иммуноглобулинами для внутривенного введения (сандоглобулин, октагам, гамунекс, интратект, габриглобин, иммуноглобулин нормальный человеческий для внутривенного введения) • В режиме насыщения - до достижения уровня Ig. G не ниже 8 -10 г/л- 2 раза в неделю • В поддерживающем режиме - 1 раз в месяц в дозе 0, 8 г/кг - Замещение ряда других факторов показано при специфических иммунодефицитах: • например, полиэтиленгликоль-аденозиндезаминазы при тяжелой комбинированной иммунной недостаточности, обусловленной дефицитом аденозиндезаминазы; • С 1 INH при семейном ангионевротическом отеке; • ростковых факторов (G-CSF или GM-CSF) при синдроме Костманна, циклической нейтропении или гипер-Ig. M-синдроме.
Заместительная терапия - При гуморальных иммунодефицитах проводится иммуноглобулинами для внутривенного введения (сандоглобулин, октагам, гамунекс, интратект, габриглобин, иммуноглобулин нормальный человеческий для внутривенного введения) • В режиме насыщения - до достижения уровня Ig. G не ниже 8 -10 г/л- 2 раза в неделю • В поддерживающем режиме - 1 раз в месяц в дозе 0, 8 г/кг - Замещение ряда других факторов показано при специфических иммунодефицитах: • например, полиэтиленгликоль-аденозиндезаминазы при тяжелой комбинированной иммунной недостаточности, обусловленной дефицитом аденозиндезаминазы; • С 1 INH при семейном ангионевротическом отеке; • ростковых факторов (G-CSF или GM-CSF) при синдроме Костманна, циклической нейтропении или гипер-Ig. M-синдроме.
 ВТОРИЧНАЯ ИММУННАЯ НЕДОСТАТОЧНОСТЬ
ВТОРИЧНАЯ ИММУННАЯ НЕДОСТАТОЧНОСТЬ
 ИММУННАЯ НЕДОСТАТОЧНОСТЬ ПЕРВИЧНАЯ ВТОРИЧНАЯ § Повышенная чувствительность к инфекциям § Опухоли § Аутоиммунные заболевания § Аллергия
ИММУННАЯ НЕДОСТАТОЧНОСТЬ ПЕРВИЧНАЯ ВТОРИЧНАЯ § Повышенная чувствительность к инфекциям § Опухоли § Аутоиммунные заболевания § Аллергия
 Неиммунные причины повышенной чувствительности к инфекциям (1) o Нарушения микроциркуляции: диабет, пороки сердца, васкулит и др. o Морфологические дефекты: стеноз уретры, пиелоэктазия, БЭБ и др. o Нарушение защитных барьеров: ожоги, экзема, дефекты мукоцилиарного механизма и др.
Неиммунные причины повышенной чувствительности к инфекциям (1) o Нарушения микроциркуляции: диабет, пороки сердца, васкулит и др. o Морфологические дефекты: стеноз уретры, пиелоэктазия, БЭБ и др. o Нарушение защитных барьеров: ожоги, экзема, дефекты мукоцилиарного механизма и др.
 Неиммунные причины повышенной чувствительности к инфекциям (2) o Необычные инфекционные факторы: - хронические очаги инфекции при отсутствии адекватной терапии, - постоянное реинфицирование (контаминированная вода, ингаляционное оборудование), - «больничная» флора o Инородные тела: венозные катетеры, искусственные клапаны, аспирация инородных тел
Неиммунные причины повышенной чувствительности к инфекциям (2) o Необычные инфекционные факторы: - хронические очаги инфекции при отсутствии адекватной терапии, - постоянное реинфицирование (контаминированная вода, ингаляционное оборудование), - «больничная» флора o Инородные тела: венозные катетеры, искусственные клапаны, аспирация инородных тел
 ВТОРИЧНАЯ ИММУННАЯ НЕДОСТАТОЧНОСТЬ клинико-лабораторный синдром недостаточности эффекторных функций иммунокомпетентных клеток, сочетающийся с осложненным течением - воспалительных заболеваний и травм, - повышенным риском развития аутоиммунных, - аллергических заболеваний и - новообразований Развиваются в позднем постнатальном периоде или у взрослых и не являются результатом генетических дефектов
ВТОРИЧНАЯ ИММУННАЯ НЕДОСТАТОЧНОСТЬ клинико-лабораторный синдром недостаточности эффекторных функций иммунокомпетентных клеток, сочетающийся с осложненным течением - воспалительных заболеваний и травм, - повышенным риском развития аутоиммунных, - аллергических заболеваний и - новообразований Развиваются в позднем постнатальном периоде или у взрослых и не являются результатом генетических дефектов
 ФОРМЫ ВТОРИЧНОЙ ИММУННОЙ НЕДОСТАТОЧНОСТИ приобретенная (Синдром приобретенного иммунодефицита) индуцированная (воздействие рентгеновского излучения, цитостатической терапии, применение кортикостероидов, травмы и хирургические вмешательства, а также нарушения иммунитета, развивающиеся вторично по отношению к основному заболеванию – диабет, заболевания печени, почек, злокачественные новообразования) спонтанная (отсутствие явной причины, вызвавшей нарушение иммунной реактивности) По характеру течения: - острый, транзиторный - хронический (более 6 мес. ) По типу поражения иммунной системы: - Недостаточность В-клеточного иммунитета - Недостаточность Т-клеточного иммунитета - Недостаточность системы фагоцитов - Недостаточность системы комплимента и др.
ФОРМЫ ВТОРИЧНОЙ ИММУННОЙ НЕДОСТАТОЧНОСТИ приобретенная (Синдром приобретенного иммунодефицита) индуцированная (воздействие рентгеновского излучения, цитостатической терапии, применение кортикостероидов, травмы и хирургические вмешательства, а также нарушения иммунитета, развивающиеся вторично по отношению к основному заболеванию – диабет, заболевания печени, почек, злокачественные новообразования) спонтанная (отсутствие явной причины, вызвавшей нарушение иммунной реактивности) По характеру течения: - острый, транзиторный - хронический (более 6 мес. ) По типу поражения иммунной системы: - Недостаточность В-клеточного иммунитета - Недостаточность Т-клеточного иммунитета - Недостаточность системы фагоцитов - Недостаточность системы комплимента и др.
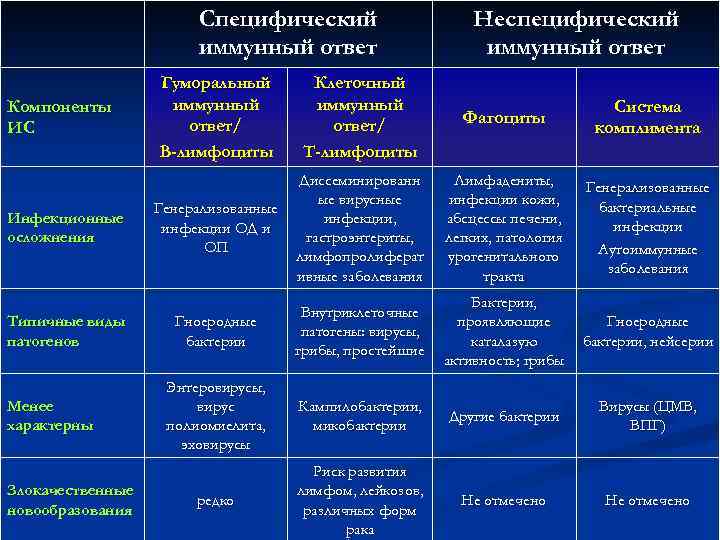 Специфический иммунный ответ Компоненты ИС Инфекционные осложнения Типичные виды патогенов Менее характерны Злокачественные новообразования Неспецифический иммунный ответ Гуморальный иммунный ответ/ В-лимфоциты Клеточный иммунный ответ/ Т-лимфоциты Фагоциты Система комплимента Генерализованные инфекции ОД и ОП Диссеминированн ые вирусные инфекции, гастроэнтериты, лимфопролиферат ивные заболевания Лимфадениты, инфекции кожи, абсцессы печени, легких, патология урогенитального тракта Генерализованные бактериальные инфекции Аутоиммунные заболевания Гноеродные бактерии Внутриклеточные патогены: вирусы, грибы, простейшие Бактерии, проявляющие каталазую активность; грибы Гноеродные бактерии, нейсерии Энтеровирусы, вирус полиомиелита, эховирусы Кампилобактерии, микобактерии Другие бактерии Вирусы (ЦМВ, ВПГ) редко Риск развития лимфом, лейкозов, различных форм рака Не отмечено
Специфический иммунный ответ Компоненты ИС Инфекционные осложнения Типичные виды патогенов Менее характерны Злокачественные новообразования Неспецифический иммунный ответ Гуморальный иммунный ответ/ В-лимфоциты Клеточный иммунный ответ/ Т-лимфоциты Фагоциты Система комплимента Генерализованные инфекции ОД и ОП Диссеминированн ые вирусные инфекции, гастроэнтериты, лимфопролиферат ивные заболевания Лимфадениты, инфекции кожи, абсцессы печени, легких, патология урогенитального тракта Генерализованные бактериальные инфекции Аутоиммунные заболевания Гноеродные бактерии Внутриклеточные патогены: вирусы, грибы, простейшие Бактерии, проявляющие каталазую активность; грибы Гноеродные бактерии, нейсерии Энтеровирусы, вирус полиомиелита, эховирусы Кампилобактерии, микобактерии Другие бактерии Вирусы (ЦМВ, ВПГ) редко Риск развития лимфом, лейкозов, различных форм рака Не отмечено
 ГРУППЫ ПАЦИЕНТОВ Больные, имеющие клинические признаки нарушения иммунитета в сочетании с 1. выявленными изменениями в параметрах иммунного статуса Больные, имеющие только клинические признаки 2. иммунной недостаточности без изменений в параметрах иммунного статуса Больные, имеющие только изменения в 3. параметрах иммунного статуса без клинических признаков иммунной недостаточности
ГРУППЫ ПАЦИЕНТОВ Больные, имеющие клинические признаки нарушения иммунитета в сочетании с 1. выявленными изменениями в параметрах иммунного статуса Больные, имеющие только клинические признаки 2. иммунной недостаточности без изменений в параметрах иммунного статуса Больные, имеющие только изменения в 3. параметрах иммунного статуса без клинических признаков иммунной недостаточности
 Клинические маркеры вторичной иммунной недостаточности Основные: появление нового очага инфекции на фоне текущего острого воспалительного заболевания вялое, затяжное течение острых инфекционно-воспалительных заболеваний наличие политопных очагов хронической инфекции (трех и более) рецидивирующее течение бактериально-вирусных заболеваний (ОРВИ более 4 раз в год, рецидивирующий герпес, хроническая вирусная инфекция и др. ) грибковая инфекция с поражением слизистых, бронхов, кишечника, половых органов, глубокие микозы хроническая протозойная инфекция персистирующая паразитарная инвазия гастоэнтеропатия с диареей и дисбактериозом, синдром мальабсорбции выраженные нарушения обмена веществ: кахексия, ожирение III ст. , сахарный диабет, гипотиреоз, врожденные энзимопатии состояние после лучевой и химиотерапии у онкологических больных длительное (более 3 месяцев) применение глюкокортикоидов и иммуносупрессивных препаратов больными с аутоиммунными, аллергическими, миело- и лимфопролифератиными заболеваниями
Клинические маркеры вторичной иммунной недостаточности Основные: появление нового очага инфекции на фоне текущего острого воспалительного заболевания вялое, затяжное течение острых инфекционно-воспалительных заболеваний наличие политопных очагов хронической инфекции (трех и более) рецидивирующее течение бактериально-вирусных заболеваний (ОРВИ более 4 раз в год, рецидивирующий герпес, хроническая вирусная инфекция и др. ) грибковая инфекция с поражением слизистых, бронхов, кишечника, половых органов, глубокие микозы хроническая протозойная инфекция персистирующая паразитарная инвазия гастоэнтеропатия с диареей и дисбактериозом, синдром мальабсорбции выраженные нарушения обмена веществ: кахексия, ожирение III ст. , сахарный диабет, гипотиреоз, врожденные энзимопатии состояние после лучевой и химиотерапии у онкологических больных длительное (более 3 месяцев) применение глюкокортикоидов и иммуносупрессивных препаратов больными с аутоиммунными, аллергическими, миело- и лимфопролифератиными заболеваниями
 Факторы, способствующие развитию ВИН старческий возраст (старше 60 лет) длительное проживание в экологически неблагоприятных регионах (регионы экологических катастроф, радиационных аварий, с высоким уровнем загрязнения местности промышленными отходами и т. д. ) хронический стресс работа в условиях профвредностей перенесенные генерализованные инфекции: инфекционно-токсический шок, сепсис, менингит, разлитой перитонит и др. состояние после обширных хирургических вмешательств и тяжелых травм генетическая предрасположенность к развитию иммунопатологических заболеваний
Факторы, способствующие развитию ВИН старческий возраст (старше 60 лет) длительное проживание в экологически неблагоприятных регионах (регионы экологических катастроф, радиационных аварий, с высоким уровнем загрязнения местности промышленными отходами и т. д. ) хронический стресс работа в условиях профвредностей перенесенные генерализованные инфекции: инфекционно-токсический шок, сепсис, менингит, разлитой перитонит и др. состояние после обширных хирургических вмешательств и тяжелых травм генетическая предрасположенность к развитию иммунопатологических заболеваний


