698d0cef6ae54bdd27a4f32f389f6fab.ppt
- Количество слайдов: 65
 Перспективы использования фототрофных микроорганизмов для генной инженерии
Перспективы использования фототрофных микроорганизмов для генной инженерии
 Разноообразие микроводорослей и их метаболических путей - Еда - Пищевые добавки - Лекарства - Направленный биосинтез - Биотопливо
Разноообразие микроводорослей и их метаболических путей - Еда - Пищевые добавки - Лекарства - Направленный биосинтез - Биотопливо
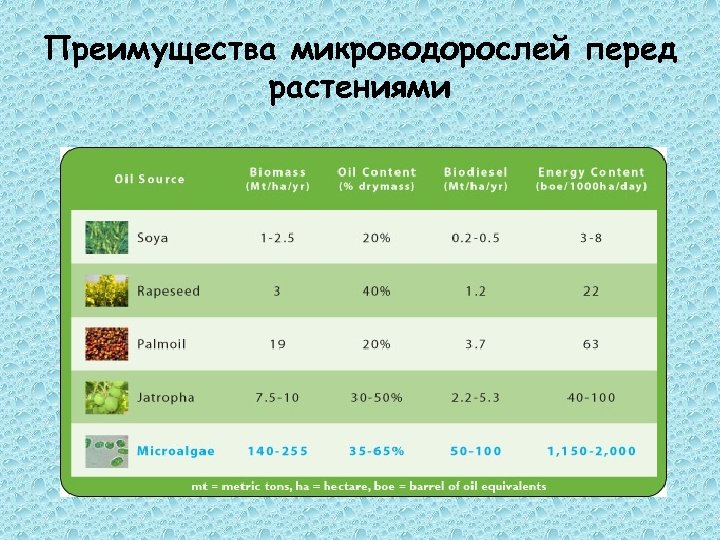 Преимущества микроводорослей перед растениями
Преимущества микроводорослей перед растениями
 Альгологический рай Дешевая еда Дешевая энергия Биотопливо
Альгологический рай Дешевая еда Дешевая энергия Биотопливо
 Производство биотоплива? Энергия Солнца напрямую конвертируется в биотопливо Исключается использование сельхозугодий и сельхозпродуктов Возможности масштабирования процесса Сносные цены на электроэнергию Отсутствие негативного влияния на окружающую среду
Производство биотоплива? Энергия Солнца напрямую конвертируется в биотопливо Исключается использование сельхозугодий и сельхозпродуктов Возможности масштабирования процесса Сносные цены на электроэнергию Отсутствие негативного влияния на окружающую среду
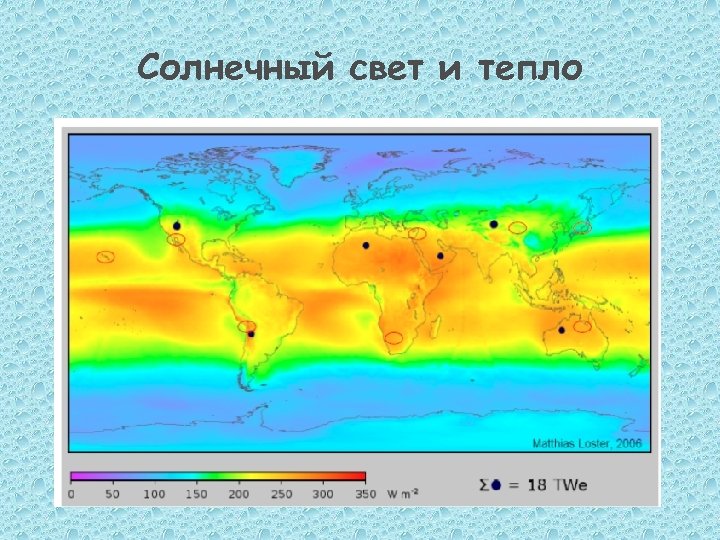 Солнечный свет и тепло
Солнечный свет и тепло
 Трудности производства топлива из микроводорослей Сбор биомассы Получение топлива Улучшенные штаммы
Трудности производства топлива из микроводорослей Сбор биомассы Получение топлива Улучшенные штаммы
 Что можно использовать в качестве топлива? - Триглицериды, жирные килоты - Липиды (диглицериды), длинные углеводороды - Углеводы: сахара и крахмал - Этанол и другие спирты - Целлюлоза
Что можно использовать в качестве топлива? - Триглицериды, жирные килоты - Липиды (диглицериды), длинные углеводороды - Углеводы: сахара и крахмал - Этанол и другие спирты - Целлюлоза
 Как это сделать? (a) Идентифицировать штаммы с нужными свойствами - один природный штамм вряд ли будет обладать всеми необходимыми свойствами (б) Модифицировать найденные штаммы - для получения высокого выхода продукта; - для удобного сбора биомассы - для удобной процедуры экстракции - для соблюдения норм биобезопасности
Как это сделать? (a) Идентифицировать штаммы с нужными свойствами - один природный штамм вряд ли будет обладать всеми необходимыми свойствами (б) Модифицировать найденные штаммы - для получения высокого выхода продукта; - для удобного сбора биомассы - для удобной процедуры экстракции - для соблюдения норм биобезопасности
 «Одомашнивание микроводорослей» Кукуруза «одомашнена» 4000 лет до н. э. Стальной плуг, масштабное с/х – 1837 Сорта кукурузы - 1863 «Зелёная революция» - 1944 ГМ-кукуруза – 2000 Микроводоросли – то же процесс, но гораздо быстрее!
«Одомашнивание микроводорослей» Кукуруза «одомашнена» 4000 лет до н. э. Стальной плуг, масштабное с/х – 1837 Сорта кукурузы - 1863 «Зелёная революция» - 1944 ГМ-кукуруза – 2000 Микроводоросли – то же процесс, но гораздо быстрее!
 Что нужно? - Глубокие знания генетики, физиологии и биохимии микроводорослей; - Знания о разных видах и штаммах микроводорослей на уровне генома, протеома, метаболома; - Новые способы трансформации, скрещивания и селекции; - Новые векторы для трансформации и экспрессии; - Новые способы направленного мутагенеза; - Способы массового культивирования, сбора и обработки биомассы
Что нужно? - Глубокие знания генетики, физиологии и биохимии микроводорослей; - Знания о разных видах и штаммах микроводорослей на уровне генома, протеома, метаболома; - Новые способы трансформации, скрещивания и селекции; - Новые векторы для трансформации и экспрессии; - Новые способы направленного мутагенеза; - Способы массового культивирования, сбора и обработки биомассы
 Что есть на данный момент? - Разные виды микроводорослей с разным потенциалом для дальнейшего использования; плохо охарактеризованные - Способы культивирования в ограниченных масштабах - Несколько геномов с известной последовательностью ДНК - Несколько способов трансформации модельных видов
Что есть на данный момент? - Разные виды микроводорослей с разным потенциалом для дальнейшего использования; плохо охарактеризованные - Способы культивирования в ограниченных масштабах - Несколько геномов с известной последовательностью ДНК - Несколько способов трансформации модельных видов
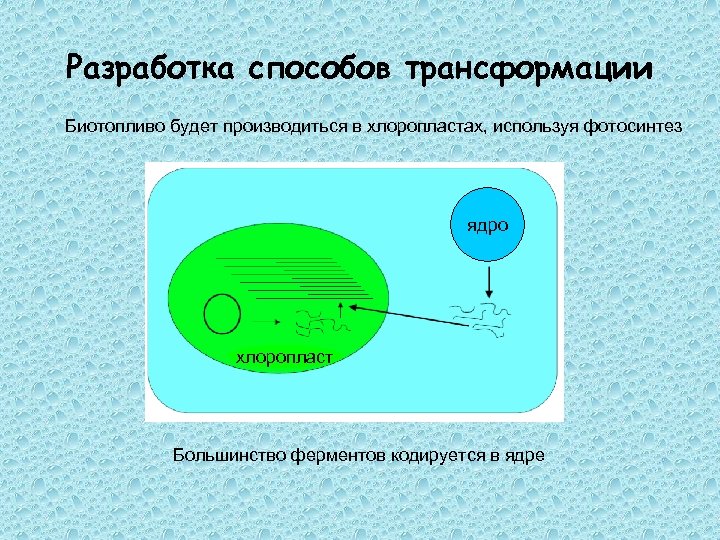 Разработка способов трансформации Биотопливо будет производиться в хлоропластах, используя фотосинтез ядро хлоропласт Большинство ферментов кодируется в ядре
Разработка способов трансформации Биотопливо будет производиться в хлоропластах, используя фотосинтез ядро хлоропласт Большинство ферментов кодируется в ядре
 Трансформация требует видоспецифичных маркеров для селекции ядро хлоропласт
Трансформация требует видоспецифичных маркеров для селекции ядро хлоропласт
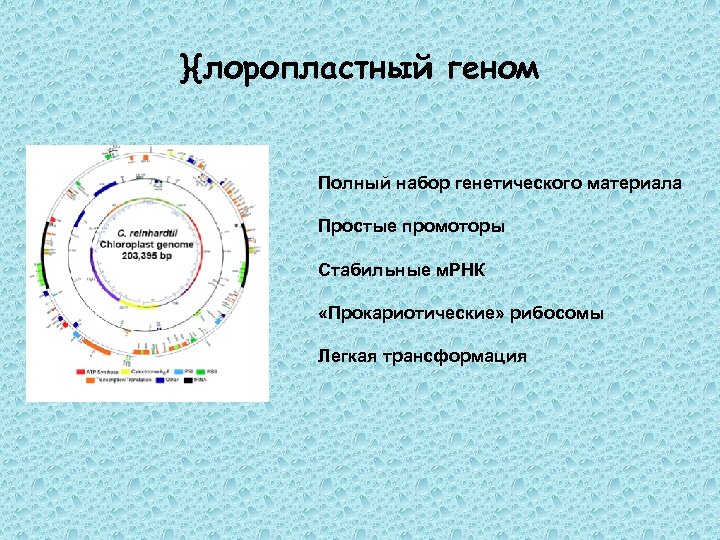 }{лоропластный геном Полный набор генетического материала Простые промоторы Стабильные м. РНК «Прокариотические» рибосомы Легкая трансформация
}{лоропластный геном Полный набор генетического материала Простые промоторы Стабильные м. РНК «Прокариотические» рибосомы Легкая трансформация
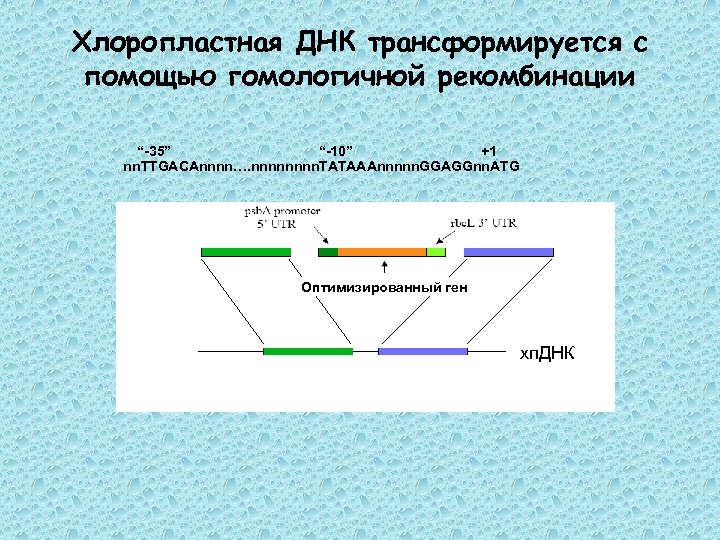 Хлоропластная ДНК трансформируется с помощью гомологичной рекомбинации “-35” “-10” +1 nn. TTGACAnnnn…. nnnn. TATAAAnnnnn. GGAGGnn. ATG Оптимизированный ген хп. ДНК
Хлоропластная ДНК трансформируется с помощью гомологичной рекомбинации “-35” “-10” +1 nn. TTGACAnnnn…. nnnn. TATAAAnnnnn. GGAGGnn. ATG Оптимизированный ген хп. ДНК
 Оптимизация использования кодонов GFP под хлоропластный геном
Оптимизация использования кодонов GFP под хлоропластный геном
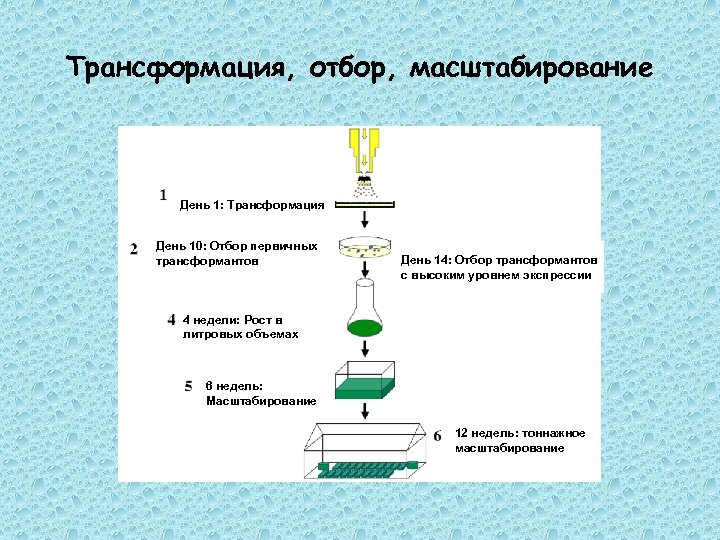 Трансформация, отбор, масштабирование День 1: Трансформация День 10: Отбор первичных трансформантов День 14: Отбор трансформантов с высоким уровнем экспрессии 4 недели: Рост в литровых объемах 6 недель: Масштабирование 12 недель: тоннажное масштабирование
Трансформация, отбор, масштабирование День 1: Трансформация День 10: Отбор первичных трансформантов День 14: Отбор трансформантов с высоким уровнем экспрессии 4 недели: Рост в литровых объемах 6 недель: Масштабирование 12 недель: тоннажное масштабирование
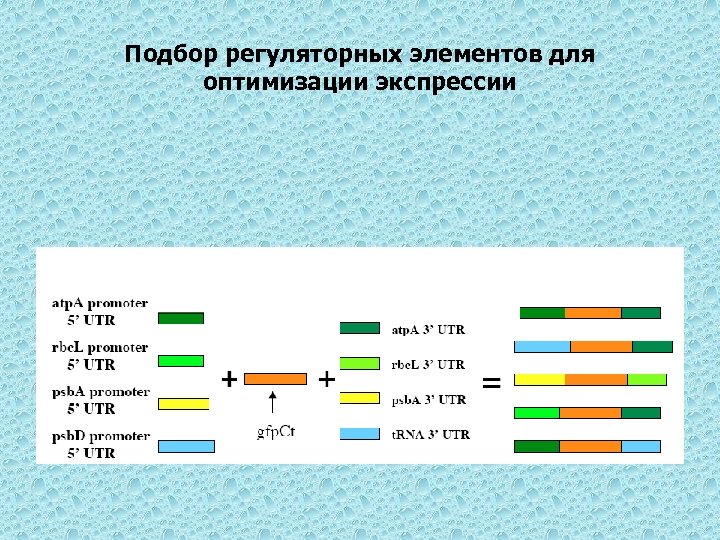 Подбор регуляторных элементов для оптимизации экспрессии
Подбор регуляторных элементов для оптимизации экспрессии
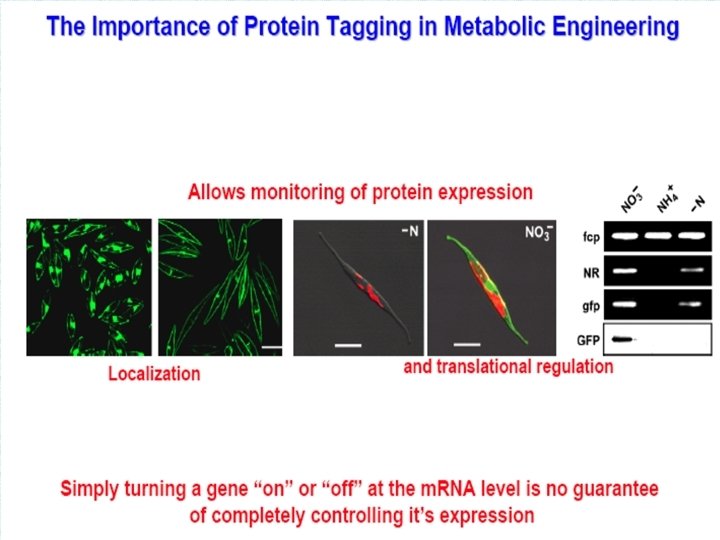
 Продукция GFP в трансгенных линиях
Продукция GFP в трансгенных линиях
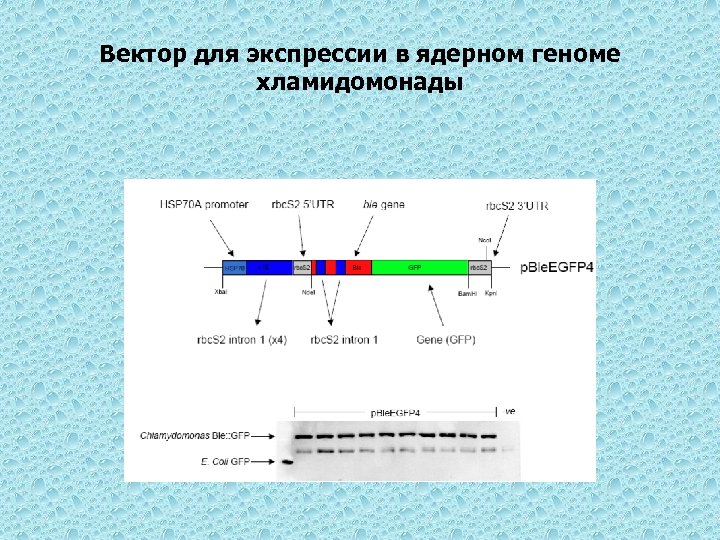 Вектор для экспрессии в ядерном геноме хламидомонады
Вектор для экспрессии в ядерном геноме хламидомонады
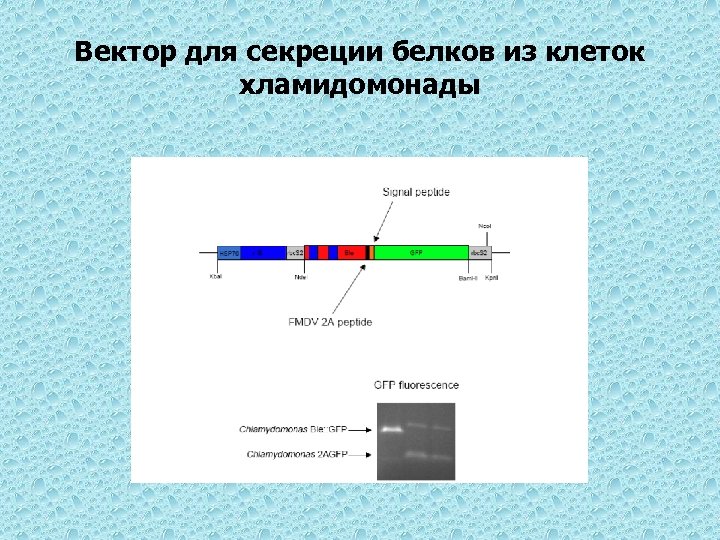 Вектор для секреции белков из клеток хламидомонады
Вектор для секреции белков из клеток хламидомонады
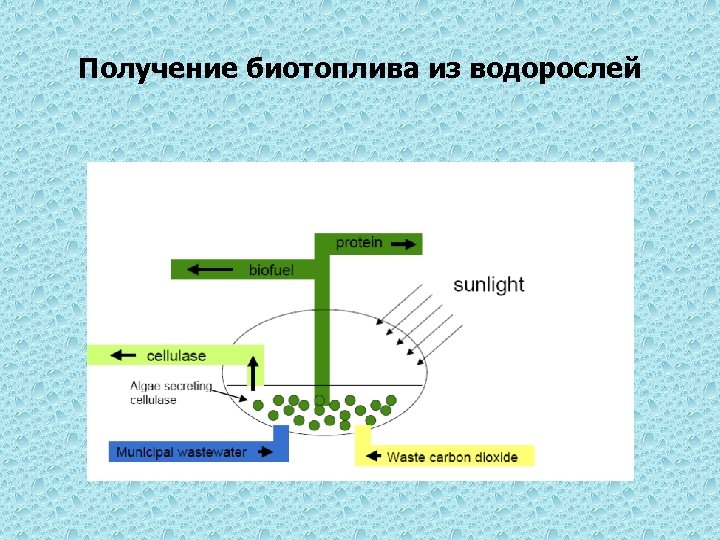 Получение биотоплива из водорослей
Получение биотоплива из водорослей
 Жирные кислоты для биотоплива
Жирные кислоты для биотоплива
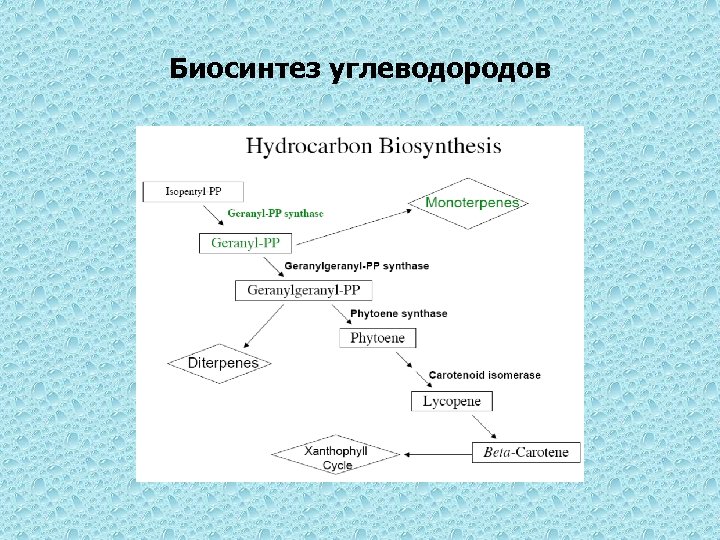 Биосинтез углеводородов
Биосинтез углеводородов

 Mutant Algae Is Hydrogen Factory Sam Jaffe 02. 23. 06 Researchers at the University of California at Berkeley have engineered a strain of pond scum that could, with further refinements, produce vast amounts of hydrogen through photosynthesis. The work, led by plant physiologist Tasios Melis, is so far unpublished. But if it proves correct, it would mean a major breakthrough in using algae as an industrial factory, not only for hydrogen, but for a wide range of products, from biodiesel to cosmetics. The new strain of algae, known as C. reinhardtii, has truncated chlorophyll antennae within the chloroplasts of the cells, which serves to increase the organism's energy efficiency. In addition, it makes the algae a lighter shade of green, which in turn allows more sunlight deeper into an algal culture and therefore allows more cells to photosynthesize. "An increase in solar conversion efficiency to 10 percent. . . is thought to be enough to make the mass culture of algae viable, " says Juergen Polle, a former student of Melis’ who now does research on algae at the City University of New York, Brooklyn. Polle points out that Melis has probably already reached that 10 percent threshold. But further refinements are still required before C. reinhardtii farms would be efficient enough to produce the world’s hydrogen, which is Melis’ eventual goal. Currently, the algae cells cycle between photosynthesis and hydrogen production because the hydrogenase enzyme which makes the hydrogen can’t function in the presence of oxygen. Researchers hope to further boost hydrogen production by using genetic engineering to close up pores that oxygen seeps through. Melis got involved in this research when he and Michael Seibert, a scientist at the National Renewable Energy Laboratory in Golden, Colorado, figured out how to get hydrogen out of green algae by restricting sulfur from their diet. The plant cells flicked a long-dormant genetic switch to produce hydrogen instead of carbon dioxide. But the quantities of hydrogen they produced were nowhere near enough to scale up the process commercially and profitably. "When we discovered the sulfur switch, we increased hydrogen production by a factor of 100, 000, " says Seibert. "But to make it a commercial technology, we still had to increase the efficiency of the process by another factor of 100. " Melis’ truncated antennae mutants are a big step in that direction. Now Seibert and others (including James Lee at Oak Ridge National Laboratories and J. Craig Venter at the Venter Institute in Rockville, Maryland) are trying to adjust the hydrogen-producing pathway so that it can produce hydrogen 100 percent of the time. A bigger challenge, and one that’s further down the road to solving, is improving the efficiency of the hydrogenase itself. "Right now the electron chain that goes into the system should produce a lot more hydrogen than comes out, and we don’t know what’s causing the bottleneck, " says Seibert. "More basic research is needed to better understand exactly what’s happening in there. " Seibert also points out that there are plenty of naturally occurring hydrogenases in microbes, most of which haven’t been studied and some of which might be much more efficient than the one used by C. reinhardtii. Whether or not scientists can find solutions for those two problems will have a lot to do with realizing the vision of a hydrogen-powered economy based on algae farms in desert areas. But algae can do a lot more than produce hydrogen. They are already used widely in the cosmetics industry to produce key chemicals used in make-up and perfume. And pharmaceutical companies have long viewed algae as a potential way to produce drugs in a cheap and environmentally friendly manner. Some algae are also viewed as an ideal source for biodiesel because they can produce oils at a much higher rate than other plants (which can then be converted into vehicle fuel without adding any carbon dioxide to the environment). For all these applications, Melis’ antenna-truncated algae should be a major breakthrough, allowing higher rates of production and thus making the end product more cheaply.
Mutant Algae Is Hydrogen Factory Sam Jaffe 02. 23. 06 Researchers at the University of California at Berkeley have engineered a strain of pond scum that could, with further refinements, produce vast amounts of hydrogen through photosynthesis. The work, led by plant physiologist Tasios Melis, is so far unpublished. But if it proves correct, it would mean a major breakthrough in using algae as an industrial factory, not only for hydrogen, but for a wide range of products, from biodiesel to cosmetics. The new strain of algae, known as C. reinhardtii, has truncated chlorophyll antennae within the chloroplasts of the cells, which serves to increase the organism's energy efficiency. In addition, it makes the algae a lighter shade of green, which in turn allows more sunlight deeper into an algal culture and therefore allows more cells to photosynthesize. "An increase in solar conversion efficiency to 10 percent. . . is thought to be enough to make the mass culture of algae viable, " says Juergen Polle, a former student of Melis’ who now does research on algae at the City University of New York, Brooklyn. Polle points out that Melis has probably already reached that 10 percent threshold. But further refinements are still required before C. reinhardtii farms would be efficient enough to produce the world’s hydrogen, which is Melis’ eventual goal. Currently, the algae cells cycle between photosynthesis and hydrogen production because the hydrogenase enzyme which makes the hydrogen can’t function in the presence of oxygen. Researchers hope to further boost hydrogen production by using genetic engineering to close up pores that oxygen seeps through. Melis got involved in this research when he and Michael Seibert, a scientist at the National Renewable Energy Laboratory in Golden, Colorado, figured out how to get hydrogen out of green algae by restricting sulfur from their diet. The plant cells flicked a long-dormant genetic switch to produce hydrogen instead of carbon dioxide. But the quantities of hydrogen they produced were nowhere near enough to scale up the process commercially and profitably. "When we discovered the sulfur switch, we increased hydrogen production by a factor of 100, 000, " says Seibert. "But to make it a commercial technology, we still had to increase the efficiency of the process by another factor of 100. " Melis’ truncated antennae mutants are a big step in that direction. Now Seibert and others (including James Lee at Oak Ridge National Laboratories and J. Craig Venter at the Venter Institute in Rockville, Maryland) are trying to adjust the hydrogen-producing pathway so that it can produce hydrogen 100 percent of the time. A bigger challenge, and one that’s further down the road to solving, is improving the efficiency of the hydrogenase itself. "Right now the electron chain that goes into the system should produce a lot more hydrogen than comes out, and we don’t know what’s causing the bottleneck, " says Seibert. "More basic research is needed to better understand exactly what’s happening in there. " Seibert also points out that there are plenty of naturally occurring hydrogenases in microbes, most of which haven’t been studied and some of which might be much more efficient than the one used by C. reinhardtii. Whether or not scientists can find solutions for those two problems will have a lot to do with realizing the vision of a hydrogen-powered economy based on algae farms in desert areas. But algae can do a lot more than produce hydrogen. They are already used widely in the cosmetics industry to produce key chemicals used in make-up and perfume. And pharmaceutical companies have long viewed algae as a potential way to produce drugs in a cheap and environmentally friendly manner. Some algae are also viewed as an ideal source for biodiesel because they can produce oils at a much higher rate than other plants (which can then be converted into vehicle fuel without adding any carbon dioxide to the environment). For all these applications, Melis’ antenna-truncated algae should be a major breakthrough, allowing higher rates of production and thus making the end product more cheaply.
 • ". . . engineering studies do not conclude that we can or will actually be able to produce algal oil/biodiesel. They conclude that the R&D to develop such processes can be justified, at least until it can be demonstrated to be impossible" Dr. John Benemann, Benemann Associates
• ". . . engineering studies do not conclude that we can or will actually be able to produce algal oil/biodiesel. They conclude that the R&D to develop such processes can be justified, at least until it can be demonstrated to be impossible" Dr. John Benemann, Benemann Associates

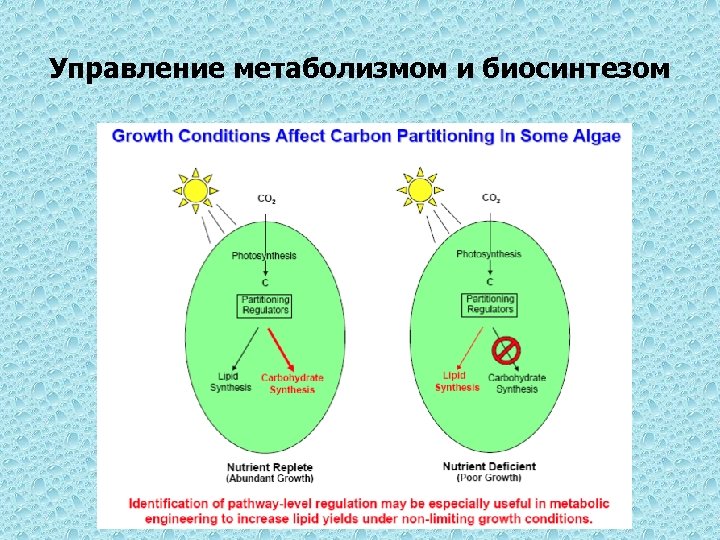 Управление метаболизмом и биосинтезом
Управление метаболизмом и биосинтезом
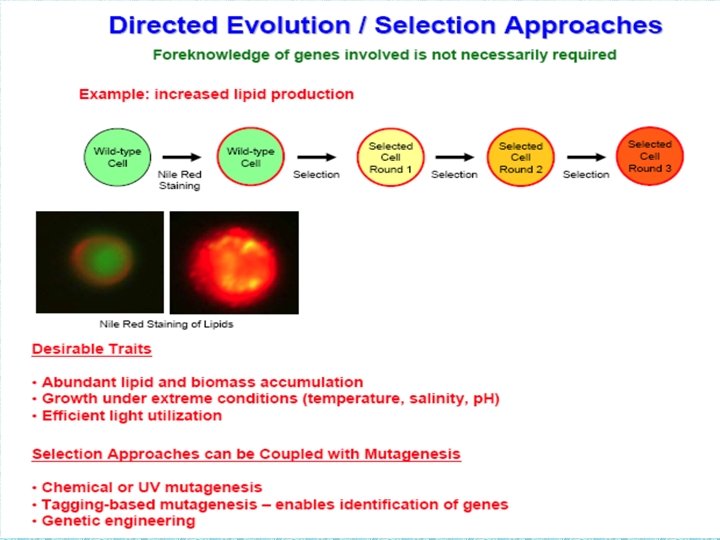
 Генно-инженерные подходы
Генно-инженерные подходы



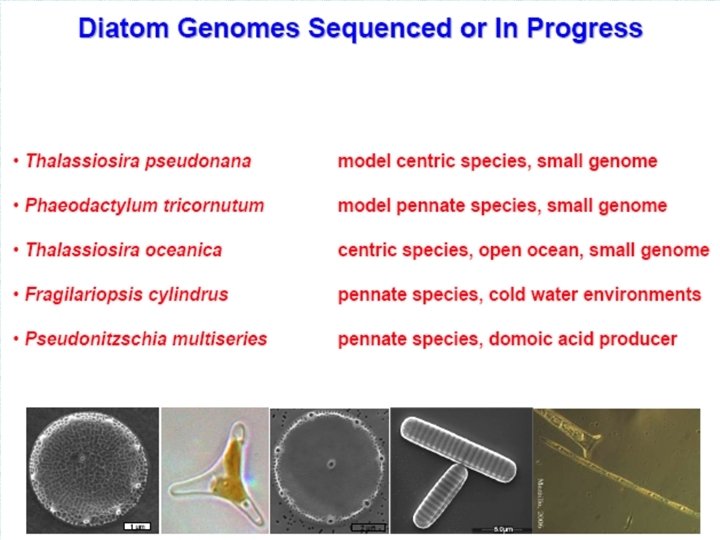
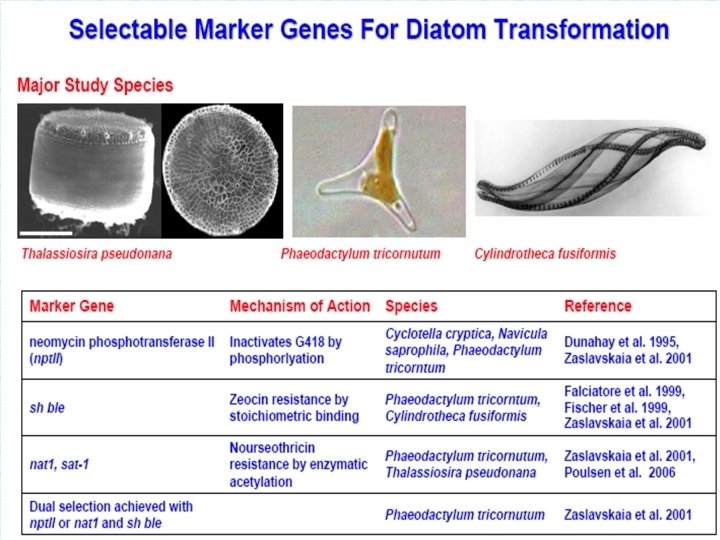
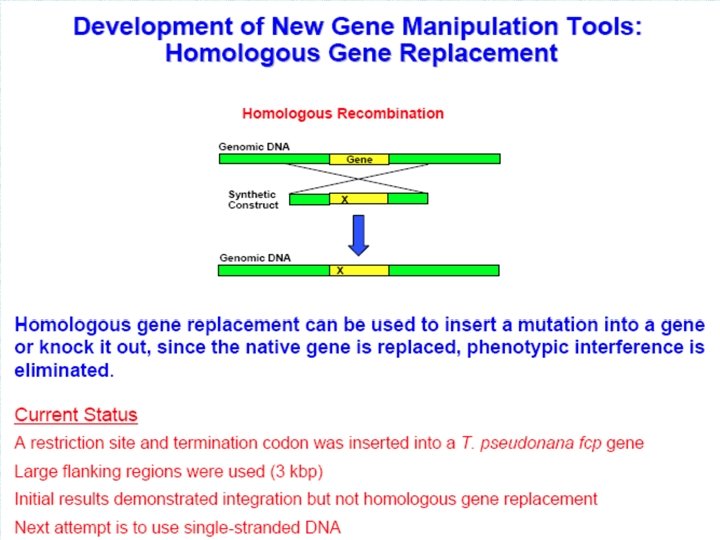
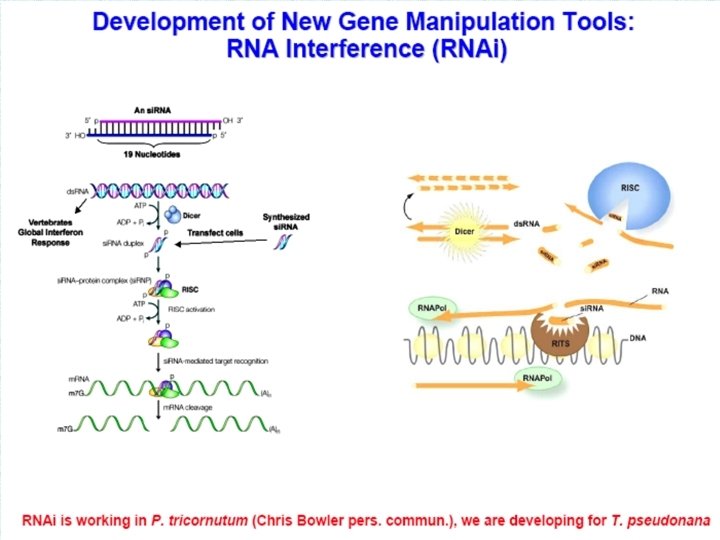
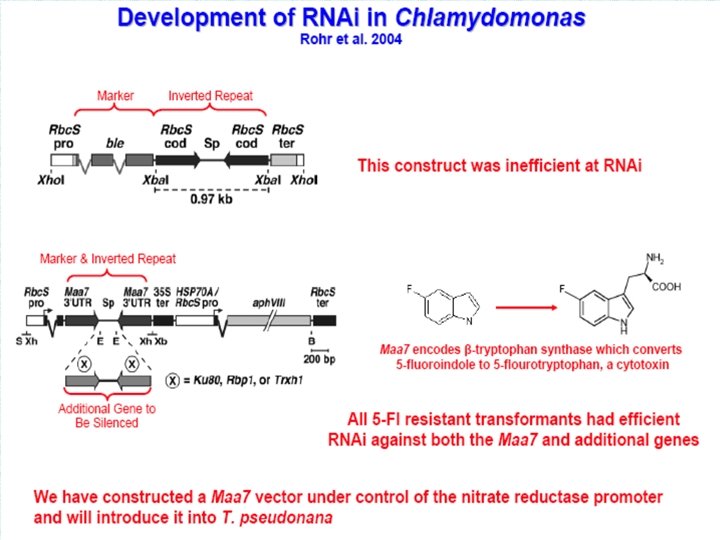

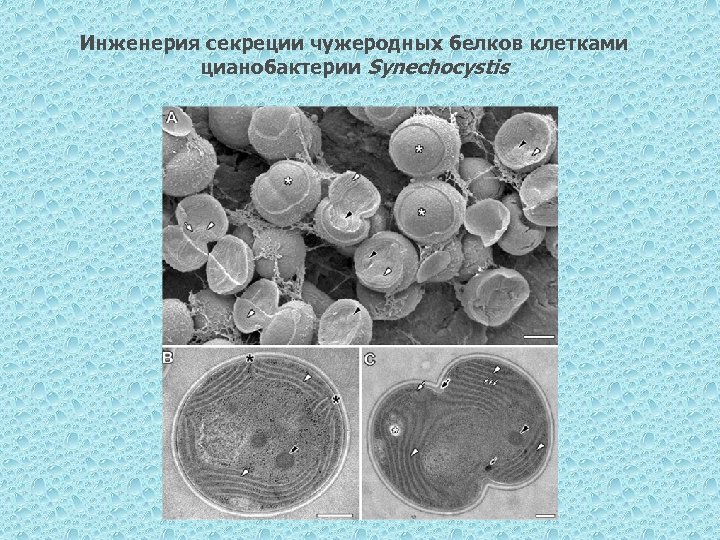 Инженерия секреции чужеродных белков клетками цианобактерии Synechocystis
Инженерия секреции чужеродных белков клетками цианобактерии Synechocystis
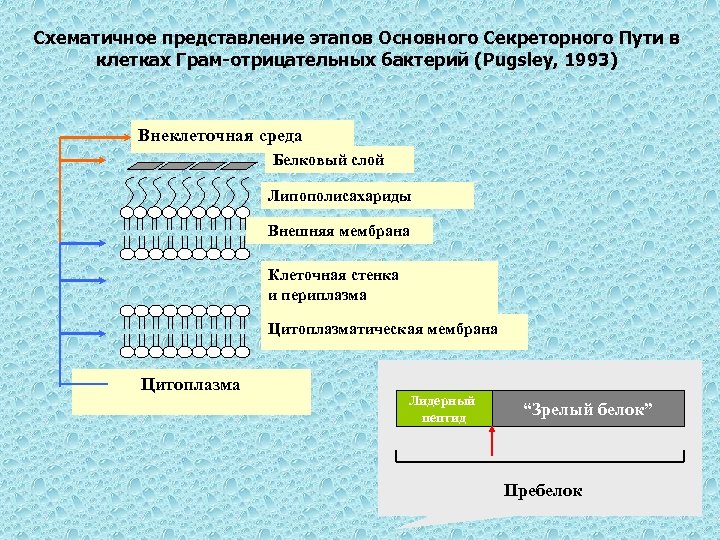 Схематичное представление этапов Основного Секреторного Пути в клетках Грам-отрицательных бактерий (Pugsley, 1993) Внеклеточная среда Белковый слой Липополисахариды Внешняя мембрана Клеточная стенка и периплазма Цитоплазматическая мембрана Цитоплазма Лидерный пептид “Зрелый белок” Пребелок
Схематичное представление этапов Основного Секреторного Пути в клетках Грам-отрицательных бактерий (Pugsley, 1993) Внеклеточная среда Белковый слой Липополисахариды Внешняя мембрана Клеточная стенка и периплазма Цитоплазматическая мембрана Цитоплазма Лидерный пептид “Зрелый белок” Пребелок
 Электрофоретическое разделение белков, секретируемых цианобактерией Synechocystis 1 2 3 к. Да - 90 - 65 - 46 - 30 - 16
Электрофоретическое разделение белков, секретируемых цианобактерией Synechocystis 1 2 3 к. Да - 90 - 65 - 46 - 30 - 16
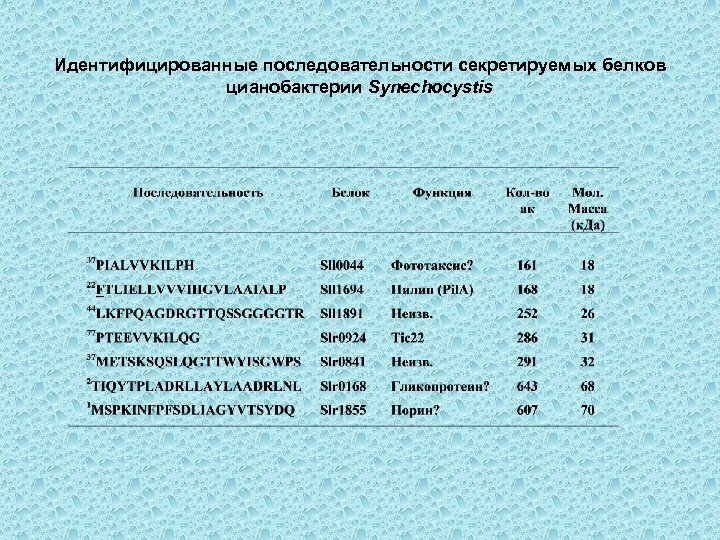 Идентифицированные последовательности секретируемых белков цианобактерии Synechocystis
Идентифицированные последовательности секретируемых белков цианобактерии Synechocystis
 Электрофоретическое разделение белков, секретируемых цианобактерией Synechocystis 1 Slr 0168 Slr 1855 2 3 к. Да - 90 - 65 - 46 Sll 0841 Blocked Tic 22 Sll 1891 Pil. A Sll 0044 - 30 - 16
Электрофоретическое разделение белков, секретируемых цианобактерией Synechocystis 1 Slr 0168 Slr 1855 2 3 к. Да - 90 - 65 - 46 Sll 0841 Blocked Tic 22 Sll 1891 Pil. A Sll 0044 - 30 - 16
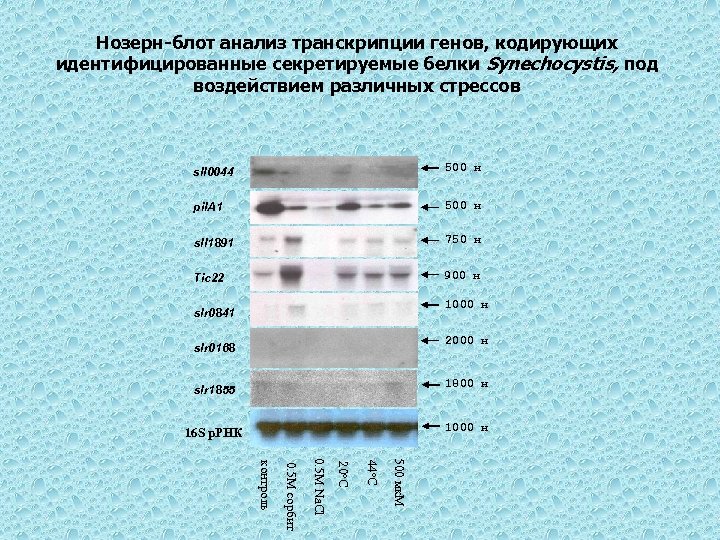 Нозерн-блот анализ транскрипции генов, кодирующих идентифицированные секретируемые белки Synechocystis, под воздействием различных стрессов sll 0044 500 н pil. A 1 500 н sll 1891 750 н Tic 22 900 н 1000 н slr 0841 2000 н slr 0168 slr 1855 1800 н 16 S р. РНК 1000 н 500 мк. М 44 o. C 20 o. C 0. 5 М Na. Cl 0. 5 М сорбит контроль
Нозерн-блот анализ транскрипции генов, кодирующих идентифицированные секретируемые белки Synechocystis, под воздействием различных стрессов sll 0044 500 н pil. A 1 500 н sll 1891 750 н Tic 22 900 н 1000 н slr 0841 2000 н slr 0168 slr 1855 1800 н 16 S р. РНК 1000 н 500 мк. М 44 o. C 20 o. C 0. 5 М Na. Cl 0. 5 М сорбит контроль
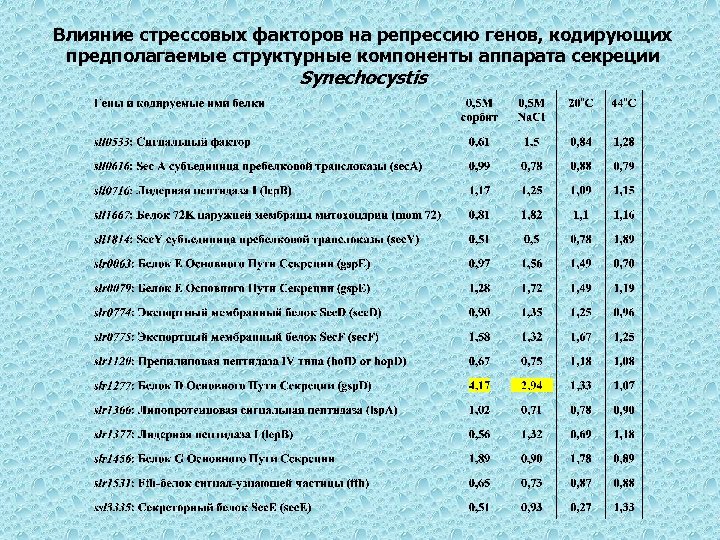 Влияние стрессовых факторов на репрессию генов, кодирующих предполагаемые структурные компоненты аппарата секреции Synechocystis
Влияние стрессовых факторов на репрессию генов, кодирующих предполагаемые структурные компоненты аппарата секреции Synechocystis
 Сравнение аминокислотных последовательностей белков Synechocystis, гомологичных секретируемому белку Pil. A Сайт процессинга MAS-NFKFKLLS-QLSKK-R-----AEGG MKA-QFSIGSSSNCRHFN-G---TR-QRG VNSSKTAFRGHNVFLLRH-A---LACSTG MSAKQ-LWKIF-NPRPMK-----GG MYKSPF-FKLRSILLLAR-NDQRTAPVSG M-KPSIVYKLFFLVSAPKF---KQKNNRG MV---MKLPNPTFLLKLVFNPHPSTSSQG MA---YK-NELIKALKLCLFTQKSTS--G Предполагаемый лидерный пептид (положительно заряженный) FTLIELLVVVIIIGI-LAAI--AL FTLLELLVVVIILGV-LGAM--TL FTLLEILVVVIVIGI-LGAI--AV FTLTENLVSLIVLSITLTAMLPAF YTLMELVVVVVVIGI-LSGI--VV VSLIELIVGVIIGGI-LIQL--AY WTLIEIGVVTVIVGI-LAAM--AF WTLIEIGVVTTIVGI-LASV--AF Pil. A Sll 1695 Slr 1456 Slr 2015 Slr 2017 Slr 1929 Slr 1930 N-концевая часть белка после процессинга (ярко выраженная гиброфобность) G – остаток глицина, предположительно являющегося последней аминокислотой лидерного пептида. F – остаток фенилаланина, предположительно являющийся первой аминокислотой зрелого белка после процессинга и секреции. F – метилированный фенилаланин в Pil. A. Стрелкой показан возможный сайт процессинга по аналогии с белком Pil. A.
Сравнение аминокислотных последовательностей белков Synechocystis, гомологичных секретируемому белку Pil. A Сайт процессинга MAS-NFKFKLLS-QLSKK-R-----AEGG MKA-QFSIGSSSNCRHFN-G---TR-QRG VNSSKTAFRGHNVFLLRH-A---LACSTG MSAKQ-LWKIF-NPRPMK-----GG MYKSPF-FKLRSILLLAR-NDQRTAPVSG M-KPSIVYKLFFLVSAPKF---KQKNNRG MV---MKLPNPTFLLKLVFNPHPSTSSQG MA---YK-NELIKALKLCLFTQKSTS--G Предполагаемый лидерный пептид (положительно заряженный) FTLIELLVVVIIIGI-LAAI--AL FTLLELLVVVIILGV-LGAM--TL FTLLEILVVVIVIGI-LGAI--AV FTLTENLVSLIVLSITLTAMLPAF YTLMELVVVVVVIGI-LSGI--VV VSLIELIVGVIIGGI-LIQL--AY WTLIEIGVVTVIVGI-LAAM--AF WTLIEIGVVTTIVGI-LASV--AF Pil. A Sll 1695 Slr 1456 Slr 2015 Slr 2017 Slr 1929 Slr 1930 N-концевая часть белка после процессинга (ярко выраженная гиброфобность) G – остаток глицина, предположительно являющегося последней аминокислотой лидерного пептида. F – остаток фенилаланина, предположительно являющийся первой аминокислотой зрелого белка после процессинга и секреции. F – метилированный фенилаланин в Pil. A. Стрелкой показан возможный сайт процессинга по аналогии с белком Pil. A.
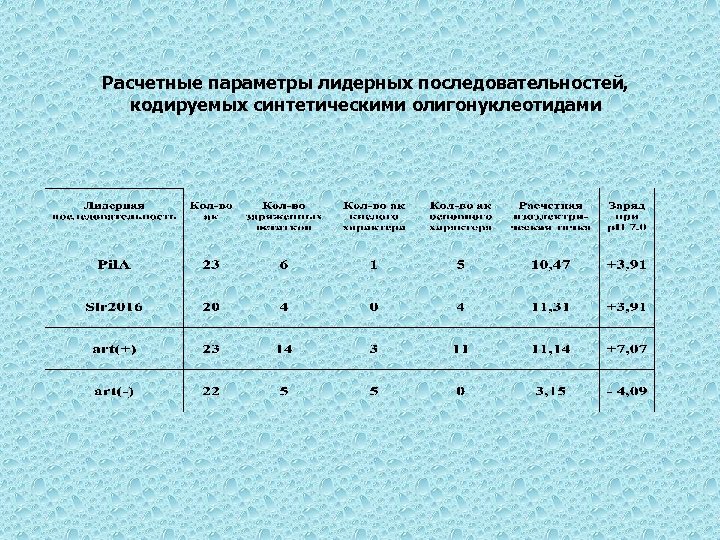 Расчетные параметры лидерных последовательностей, кодируемых синтетическими олигонуклеотидами
Расчетные параметры лидерных последовательностей, кодируемых синтетическими олигонуклеотидами
 Синтетические нуклеотидные и кодируемые ими аминокислотные последовательности, использовавшиеся для клонирования лидерных пептидов Nco I Bam HI 5'-CATGGCTAGTAATTTTAAATTCAAACTCCTCTCTCAACTCTCCAAAAAACGGGCAGAAGGTGGTATGG-3' pil. A-F 3'-CGATCATTAAAATTTAAGTTTGAGGAGAGAGTTGAGAGGTTTTTTGCCCGTCTTCCACCATACCTAG-5' pil. A-R M A S N F K L L S Q L S K K R A E G G M G Nco I Bam HI 5'-CATGGCAGCAAAACAACTATGGAAAATTTTCAATCCTAGACCGATGAAGGGTGGAATGG-3' 3'-CGTCGTTTTGTTGATACCTTTTAAAAGTTAGGATCTGGCTACTTCCCACCTTACCTAG-5' M S A K Q L W K I F N P R P M K G G M G 2016 -F 2016 -R Nco I Bam HI 5'-CATGGATAGAAAGCACGTGCTCCGGAAAAAAGAAGACTCTGCGCGGAAAAAACAAAAAGGTGGTATGG-3' art(+)-F 3'-CTATCTTTCGTGCACGAGGCCTTTTTTCTTCTGAGACGCGCCTTTTTTGTTTTTCCACCATACCTAG-5’art(+)-R M D R K H V L R K K E D S R R K K Q K G G M G Nco I Bam HI 5'-CATGGAAATTGACGGTTTTGGTGGTATTCTCTACACGTCTGATGAAGCAATTCTCGGTGGTATGG-3' 3'-CTTTAACTGCCAAAACCACCATAAGAGATGTGCAGACTACTTCGTTAAGAGCCACCATACCTAG-5' M E I D G F G G I L Y T S D E A I L G G M G art(-)-F art(-)-R
Синтетические нуклеотидные и кодируемые ими аминокислотные последовательности, использовавшиеся для клонирования лидерных пептидов Nco I Bam HI 5'-CATGGCTAGTAATTTTAAATTCAAACTCCTCTCTCAACTCTCCAAAAAACGGGCAGAAGGTGGTATGG-3' pil. A-F 3'-CGATCATTAAAATTTAAGTTTGAGGAGAGAGTTGAGAGGTTTTTTGCCCGTCTTCCACCATACCTAG-5' pil. A-R M A S N F K L L S Q L S K K R A E G G M G Nco I Bam HI 5'-CATGGCAGCAAAACAACTATGGAAAATTTTCAATCCTAGACCGATGAAGGGTGGAATGG-3' 3'-CGTCGTTTTGTTGATACCTTTTAAAAGTTAGGATCTGGCTACTTCCCACCTTACCTAG-5' M S A K Q L W K I F N P R P M K G G M G 2016 -F 2016 -R Nco I Bam HI 5'-CATGGATAGAAAGCACGTGCTCCGGAAAAAAGAAGACTCTGCGCGGAAAAAACAAAAAGGTGGTATGG-3' art(+)-F 3'-CTATCTTTCGTGCACGAGGCCTTTTTTCTTCTGAGACGCGCCTTTTTTGTTTTTCCACCATACCTAG-5’art(+)-R M D R K H V L R K K E D S R R K K Q K G G M G Nco I Bam HI 5'-CATGGAAATTGACGGTTTTGGTGGTATTCTCTACACGTCTGATGAAGCAATTCTCGGTGGTATGG-3' 3'-CTTTAACTGCCAAAACCACCATAAGAGATGTGCAGACTACTTCGTTAAGAGCCACCATACCTAG-5' M E I D G F G G I L Y T S D E A I L G G M G art(-)-F art(-)-R
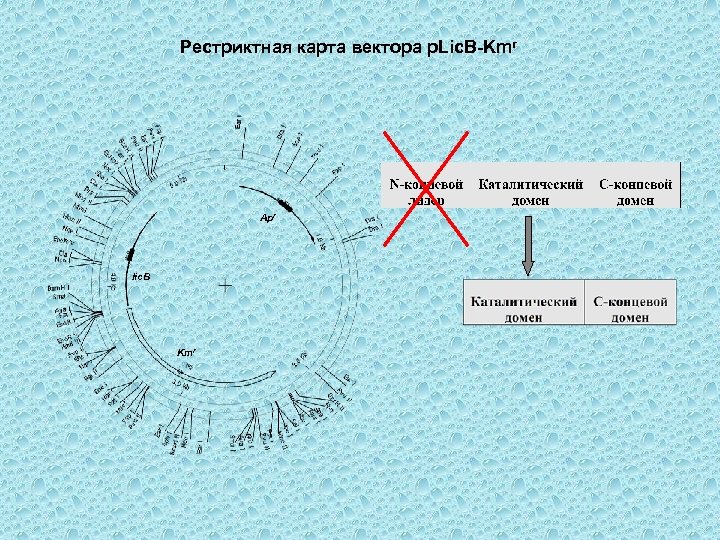 Рестриктная карта вектора p. Lic. B-Kmr Apr lic. B Kmr
Рестриктная карта вектора p. Lic. B-Kmr Apr lic. B Kmr
 Схема интеграции плазмид, несущих различные конструкции для экспресии гена lic. B в геноме Synechocystis Ecl 137 I/Sma. I Hind. III/Ehe. I Kmr Участок интеграции Ampr Геномная ДНК Synechocystis Nco I Bam. HI Ecl 137 I lic. B Ptrc лидер Участок интеграции ori
Схема интеграции плазмид, несущих различные конструкции для экспресии гена lic. B в геноме Synechocystis Ecl 137 I/Sma. I Hind. III/Ehe. I Kmr Участок интеграции Ampr Геномная ДНК Synechocystis Nco I Bam. HI Ecl 137 I lic. B Ptrc лидер Участок интеграции ori
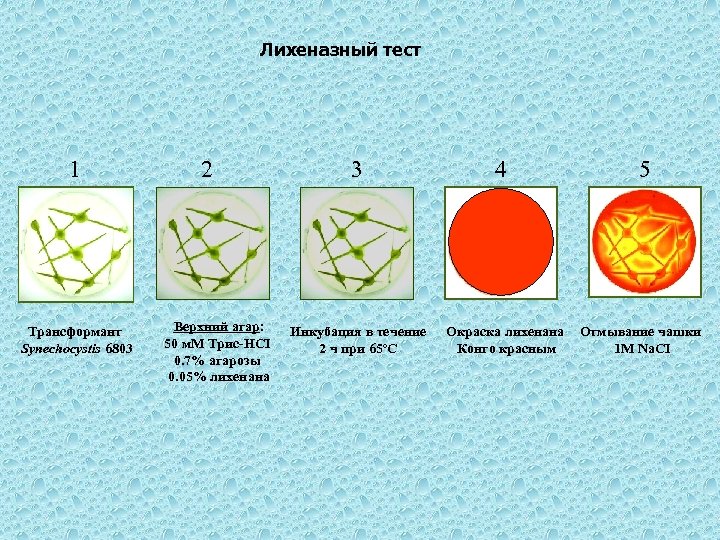 Лихеназный тест 1 Трансформант Synechocystis 6803 2 Верхний агар: 50 м. М Трис-НCI 0. 7% агарозы 0. 05% лихенана 3 Инкубация в течение 2 ч при 65 о. С 4 Окраска лихенана Конго красным 5 Отмывание чашки 1 М Na. CI
Лихеназный тест 1 Трансформант Synechocystis 6803 2 Верхний агар: 50 м. М Трис-НCI 0. 7% агарозы 0. 05% лихенана 3 Инкубация в течение 2 ч при 65 о. С 4 Окраска лихенана Конго красным 5 Отмывание чашки 1 М Na. CI
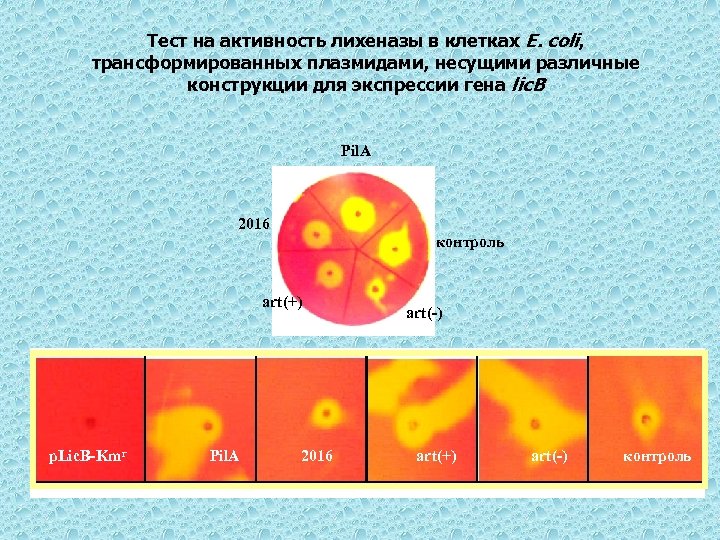 Тест на активность лихеназы в клетках E. coli, трансформированных плазмидами, несущими различные конструкции для экспрессии гена lic. B Pil. A 2016 контроль art(+) p. Lic. B-Kmr Pil. A 2016 art(-) art(+) art(-) контроль
Тест на активность лихеназы в клетках E. coli, трансформированных плазмидами, несущими различные конструкции для экспрессии гена lic. B Pil. A 2016 контроль art(+) p. Lic. B-Kmr Pil. A 2016 art(-) art(+) art(-) контроль
 Тест на активность лихеназы в культуральной среде клеток E. coli lic. B/pil. A lic. B/2016 E. coli lic. B/art(+) E. coli lic. B/art(-) E. coli lic. B/control E. coli
Тест на активность лихеназы в культуральной среде клеток E. coli lic. B/pil. A lic. B/2016 E. coli lic. B/art(+) E. coli lic. B/art(-) E. coli lic. B/control E. coli
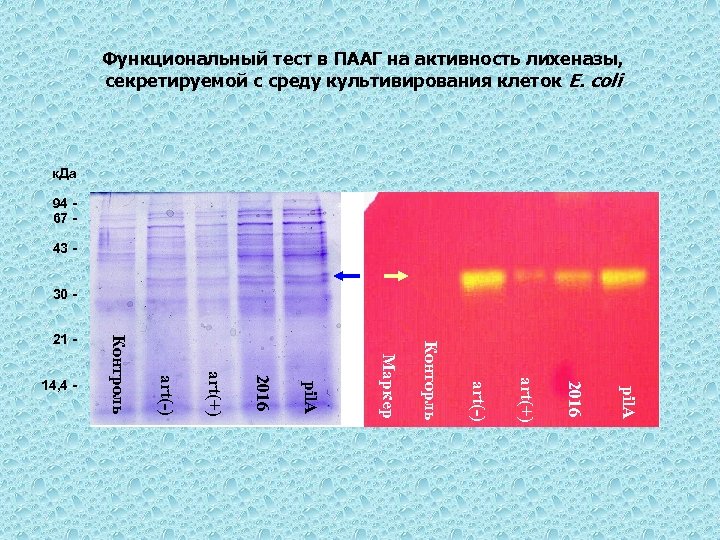 Функциональный тест в ПААГ на активность лихеназы, секретируемой с среду культивирования клеток E. coli к. Да 94 67 43 30 - pil. A 2016 art(+) art(-) Конторль Маркер pil. A 2016 art(+) art(-) 14, 4 - Контроль 21 -
Функциональный тест в ПААГ на активность лихеназы, секретируемой с среду культивирования клеток E. coli к. Да 94 67 43 30 - pil. A 2016 art(+) art(-) Конторль Маркер pil. A 2016 art(+) art(-) 14, 4 - Контроль 21 -
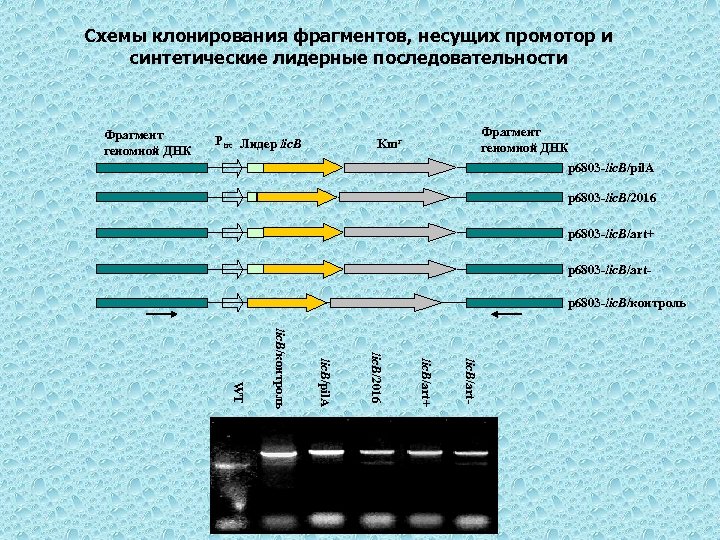 Схемы клонирования фрагментов, несущих промотор и синтетические лидерные последовательности Фрагмент геномной ДНК Ptrc Лидер lic. B Фрагмент геномной ДНК Kmr p 6803 -lic. B/pil. A p 6803 -lic. B/2016 p 6803 -lic. B/art+ p 6803 -lic. B/artp 6803 -lic. B/контроль lic. B/art- lic. B/art+ lic. B/2016 lic. B/pil. A lic. B/контроль WT
Схемы клонирования фрагментов, несущих промотор и синтетические лидерные последовательности Фрагмент геномной ДНК Ptrc Лидер lic. B Фрагмент геномной ДНК Kmr p 6803 -lic. B/pil. A p 6803 -lic. B/2016 p 6803 -lic. B/art+ p 6803 -lic. B/artp 6803 -lic. B/контроль lic. B/art- lic. B/art+ lic. B/2016 lic. B/pil. A lic. B/контроль WT
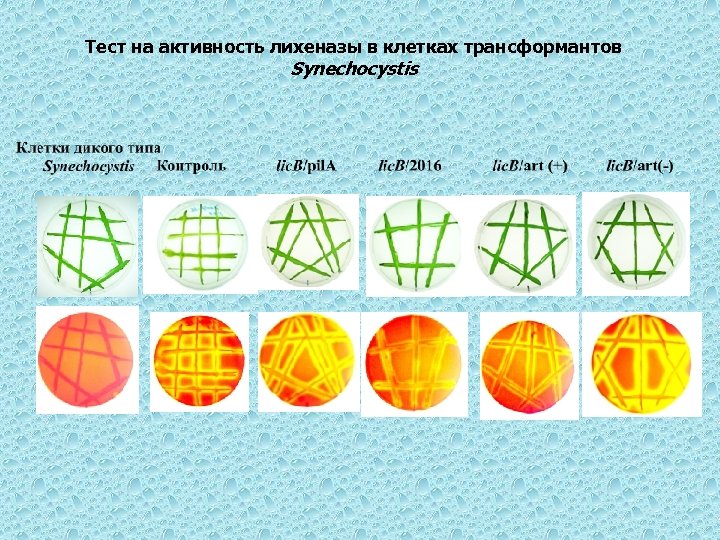 Тест на активность лихеназы в клетках трансформантов Synechocystis
Тест на активность лихеназы в клетках трансформантов Synechocystis
 Проверка лихеназной активности в культуральной среде клеток трансформантов Synechocystis WT 6803 lic. B/контроль WT 6803 lic. B/pil. A lic. B/2016 WT 6803 lic. B/art(+) WT 6803 lic. B/art(-)
Проверка лихеназной активности в культуральной среде клеток трансформантов Synechocystis WT 6803 lic. B/контроль WT 6803 lic. B/pil. A lic. B/2016 WT 6803 lic. B/art(+) WT 6803 lic. B/art(-)
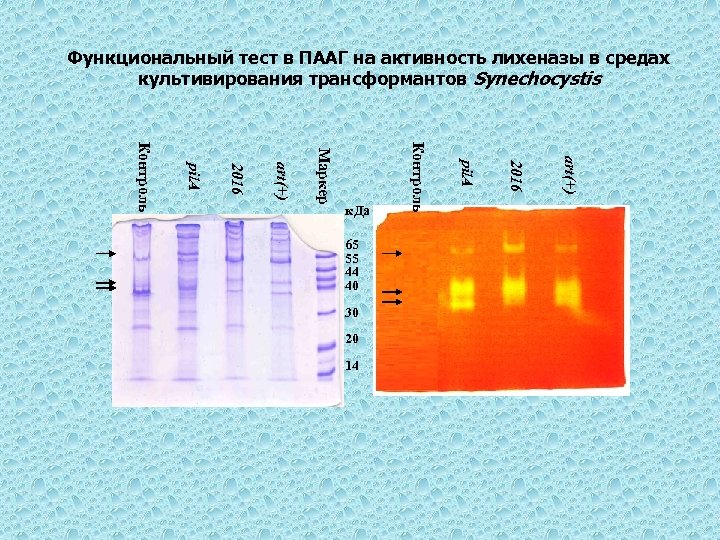 Функциональный тест в ПААГ на активность лихеназы в средах культивирования трансформантов Synechocystis 14 art(+) 20 2016 30 pil. A 65 55 44 40 Контроль Маркер art(+) 2016 pil. A Контроль к. Да
Функциональный тест в ПААГ на активность лихеназы в средах культивирования трансформантов Synechocystis 14 art(+) 20 2016 30 pil. A 65 55 44 40 Контроль Маркер art(+) 2016 pil. A Контроль к. Да

 Заключение Генетическая инженерия может всё! Или почти всё… Но для её применения необходимо знать много другого: - Физиологию и биохимию - Метаболизм конкретного организма * Желательно знать нуклеотидную последовательность всего генома
Заключение Генетическая инженерия может всё! Или почти всё… Но для её применения необходимо знать много другого: - Физиологию и биохимию - Метаболизм конкретного организма * Желательно знать нуклеотидную последовательность всего генома


