Перспективи розвитку вірусології в 21 сторіччі Поліщук Валерій

































Перспективи.ppt
- Количество слайдов: 48
 Перспективи розвитку вірусології в 21 сторіччі Поліщук Валерій Петрович Професор Завідувач кафедpи вірусології Біологічного факультету Київського національного університету імені Тараса Шевченка
Перспективи розвитку вірусології в 21 сторіччі Поліщук Валерій Петрович Професор Завідувач кафедpи вірусології Біологічного факультету Київського національного університету імені Тараса Шевченка
 Коротка історія розвитку вірусології (L. W. Enquist, JOURNAL OF VIROLOGY, June 2009) n Protovirology (1798 -1885) n Auroravirology (1892 -1933) n Meridiovirology (1934 -1955) n Janovirology (1956 -1975) n Neovirology (1976 -20. . . )
Коротка історія розвитку вірусології (L. W. Enquist, JOURNAL OF VIROLOGY, June 2009) n Protovirology (1798 -1885) n Auroravirology (1892 -1933) n Meridiovirology (1934 -1955) n Janovirology (1956 -1975) n Neovirology (1976 -20. . . )
 Protovirology n 1798 Коров’яча віспа була використана для вакцинації проти віспи людини (Дженнер) n 1882 Передача хвороби тютюнової мозаїки з безклітинних екстрактів (Maйєр) n 1885 Створення вакцини проти сказу (Пастер, Ру)
Protovirology n 1798 Коров’яча віспа була використана для вакцинації проти віспи людини (Дженнер) n 1882 Передача хвороби тютюнової мозаїки з безклітинних екстрактів (Maйєр) n 1885 Створення вакцини проти сказу (Пастер, Ру)
 Auroravirology n 1892 - Описано інфекційний агент, що фільтрується - ВТМ (Івановський) n 1911 - Відкриття першого вірусу, що викликає пухлини RSV (Раус) n 1933 - Виявлення вірусу грипу людини (Smith)
Auroravirology n 1892 - Описано інфекційний агент, що фільтрується - ВТМ (Івановський) n 1911 - Відкриття першого вірусу, що викликає пухлини RSV (Раус) n 1933 - Виявлення вірусу грипу людини (Smith)
 Meridiovirology n 1935 - Кристалізація ВТМ (Стенлі) n 1943 - Відкриття генетичного походження мутацій у бактеріофагів ( Лурія, Дельбрюк) n 1952 - Вірусний геном складається з нуклеїнові кислоти (Херші , Чейз) n - Визначення гену (цис-транс-тест) у бактеріофагів (Бензер)
Meridiovirology n 1935 - Кристалізація ВТМ (Стенлі) n 1943 - Відкриття генетичного походження мутацій у бактеріофагів ( Лурія, Дельбрюк) n 1952 - Вірусний геном складається з нуклеїнові кислоти (Херші , Чейз) n - Визначення гену (цис-транс-тест) у бактеріофагів (Бензер)
 Janovirology n 1957 – Відкриття інтерферону (Айзекс, Ліндеман) n 1958 – Відкриття механізму регулювання геному бактеріофага (Парді, Якоб, Моно, Львов) n 1970 - Відкриття зворотної транскриптази у ретровірусів (Темин, Балтімор) n 1972 - Отримання першої рекомбінантної молекули (фаг лямда, SV 40) (Берг) n 1974 - Отримання першої трансгенної миші (SV 40) (Мінтц)
Janovirology n 1957 – Відкриття інтерферону (Айзекс, Ліндеман) n 1958 – Відкриття механізму регулювання геному бактеріофага (Парді, Якоб, Моно, Львов) n 1970 - Відкриття зворотної транскриптази у ретровірусів (Темин, Балтімор) n 1972 - Отримання першої рекомбінантної молекули (фаг лямда, SV 40) (Берг) n 1974 - Отримання першої трансгенної миші (SV 40) (Мінтц)
 Neovirology n 1977 - Перший сиквенс ДНК – геноми вірусів лямда, ф. X 174, SV 40 (Сенжер, Ферс, Вайсман) n - Відкриття сплайсингу РНК у аденовірусів (Робертс, Шарп) n - Відкриття пухлинного супресору р53 у SV 40 (Левін, Крауфорд) n 1979 - Декларація ВООЗ про ліквідацію віспи n 1982 - Відкриття пріонів (Прузінер)
Neovirology n 1977 - Перший сиквенс ДНК – геноми вірусів лямда, ф. X 174, SV 40 (Сенжер, Ферс, Вайсман) n - Відкриття сплайсингу РНК у аденовірусів (Робертс, Шарп) n - Відкриття пухлинного супресору р53 у SV 40 (Левін, Крауфорд) n 1979 - Декларація ВООЗ про ліквідацію віспи n 1982 - Відкриття пріонів (Прузінер)
 Neovirology n 1983 - Відкриття ВІЛ (Монтан’є, Бар-Сінуссі) n 1988 - Відкриття IRES (Віннер, Соненберг) n - Відкриття вірусу гепатиту С (Хаутон) n 1990 - Перша генна терапія людини з ретровірусним вектором (Aндерсон, Блез) n 1998 - Відкриття si РНК (Файр та ін. ) n 2001 - Відкриття кавеосом (Геленіус) n 2002 - Створення штучного вірусу поліомієліту n 2005 – реконструкція геному “іспанки” (Таутенбергер)
Neovirology n 1983 - Відкриття ВІЛ (Монтан’є, Бар-Сінуссі) n 1988 - Відкриття IRES (Віннер, Соненберг) n - Відкриття вірусу гепатиту С (Хаутон) n 1990 - Перша генна терапія людини з ретровірусним вектором (Aндерсон, Блез) n 1998 - Відкриття si РНК (Файр та ін. ) n 2001 - Відкриття кавеосом (Геленіус) n 2002 - Створення штучного вірусу поліомієліту n 2005 – реконструкція геному “іспанки” (Таутенбергер)
 Перспективи n Прикладна вірусологія n Фундаментальна вірусологія
Перспективи n Прикладна вірусологія n Фундаментальна вірусологія
 Прикладна вірусологія n Розробка новітніх сучасних методів діагностики вірусних інфекцій n Створення нових хіміотерапевтичних антивірусних препаратів n Створення високоефективних та безпечних вакцин нового покоління n Застосування вірусів у біотехнологічних та нанотехнологічних процесах n Використання вірусів для лікування онкозахворювань n Використання бактеріофагів для боротьтби з бактеріальними інфекціями n Розробка стратегій боротьби з вірусними інфекціями в медицині, ветеринарії та рослинництві
Прикладна вірусологія n Розробка новітніх сучасних методів діагностики вірусних інфекцій n Створення нових хіміотерапевтичних антивірусних препаратів n Створення високоефективних та безпечних вакцин нового покоління n Застосування вірусів у біотехнологічних та нанотехнологічних процесах n Використання вірусів для лікування онкозахворювань n Використання бактеріофагів для боротьтби з бактеріальними інфекціями n Розробка стратегій боротьби з вірусними інфекціями в медицині, ветеринарії та рослинництві
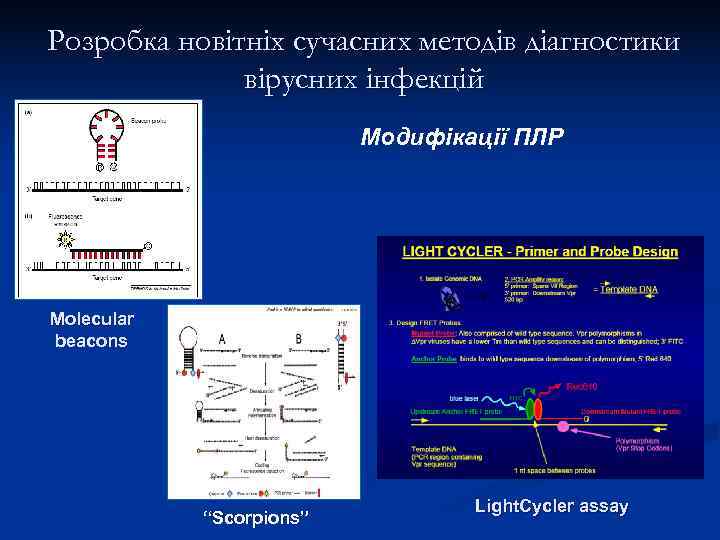
 Розробка новітніх сучасних методів діагностики вірусних інфекцій Модифікації ПЛР Molecular beacons Light. Cycler assay “Scorpions”
Розробка новітніх сучасних методів діагностики вірусних інфекцій Модифікації ПЛР Molecular beacons Light. Cycler assay “Scorpions”
 Розробка новітніх сучасних методів діагностики вірусних інфекцій Атомно-силова мікроскопія АСМ вірусу гепатиту С
Розробка новітніх сучасних методів діагностики вірусних інфекцій Атомно-силова мікроскопія АСМ вірусу гепатиту С
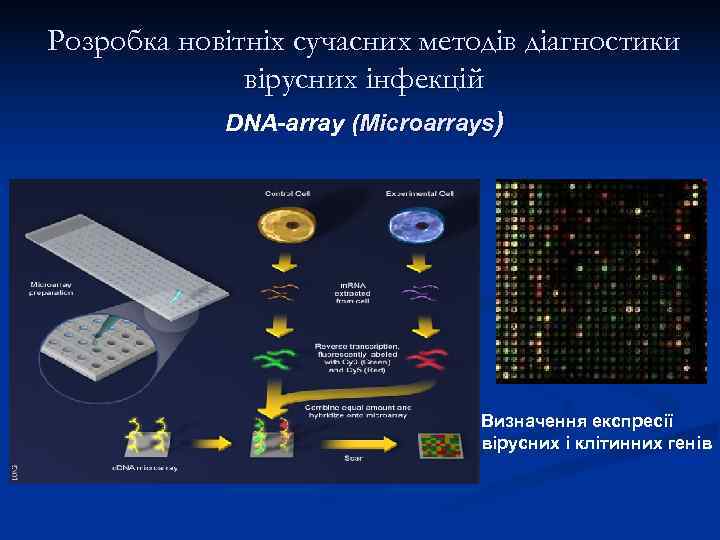
 Розробка новітніх сучасних методів діагностики вірусних інфекцій DNA-array (Microarrays) Визначення експресії вірусних і клітинних генів
Розробка новітніх сучасних методів діагностики вірусних інфекцій DNA-array (Microarrays) Визначення експресії вірусних і клітинних генів
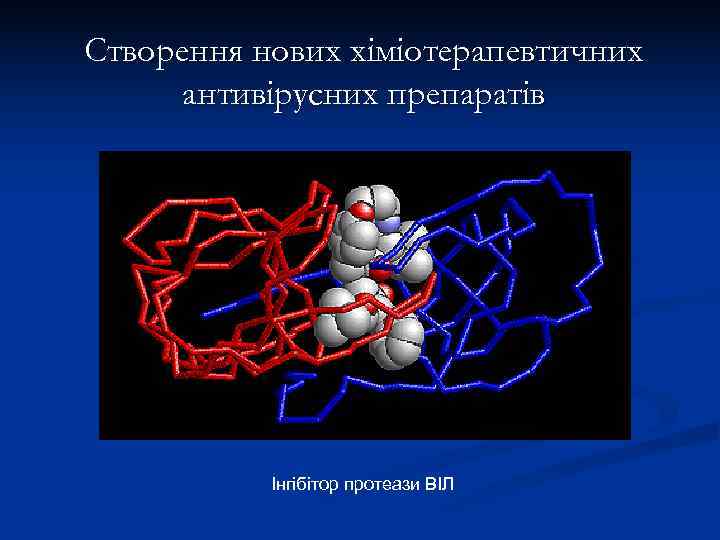
 Створення нових хіміотерапевтичних антивірусних препаратів Інгібітор протеази ВІЛ
Створення нових хіміотерапевтичних антивірусних препаратів Інгібітор протеази ВІЛ
 Створення високоефективних та безпечних вакцин нового покоління Людський ізолят ПЛР-копії вірусного Лабораторний штам A/HK/213/03 (H 5 N 1) геному, клоновані в плазміду p. HW 2000 A/PR/8/34 (H 1 N 1) ∆HA Вакцинний штам Ф/РЛ/21303(∆H 5 N 1)XA/P PQRERRRKKRGL R/8/34 Трансфекція клітин VERO, PQIETRGL сертифікованих для Клонування ПЛР-копії гену виробництва вакцини НА в плазміду p. HW 2000 та заміна сайт-специфічним мутагенезом мульти-основного сайту нарізання на моноосновний Створення прототипного вакцинного штаму з модифікованим HA проти вірусу А/НК/213 (H 5 N 1) з використанням плазмідної системи
Створення високоефективних та безпечних вакцин нового покоління Людський ізолят ПЛР-копії вірусного Лабораторний штам A/HK/213/03 (H 5 N 1) геному, клоновані в плазміду p. HW 2000 A/PR/8/34 (H 1 N 1) ∆HA Вакцинний штам Ф/РЛ/21303(∆H 5 N 1)XA/P PQRERRRKKRGL R/8/34 Трансфекція клітин VERO, PQIETRGL сертифікованих для Клонування ПЛР-копії гену виробництва вакцини НА в плазміду p. HW 2000 та заміна сайт-специфічним мутагенезом мульти-основного сайту нарізання на моноосновний Створення прототипного вакцинного штаму з модифікованим HA проти вірусу А/НК/213 (H 5 N 1) з використанням плазмідної системи
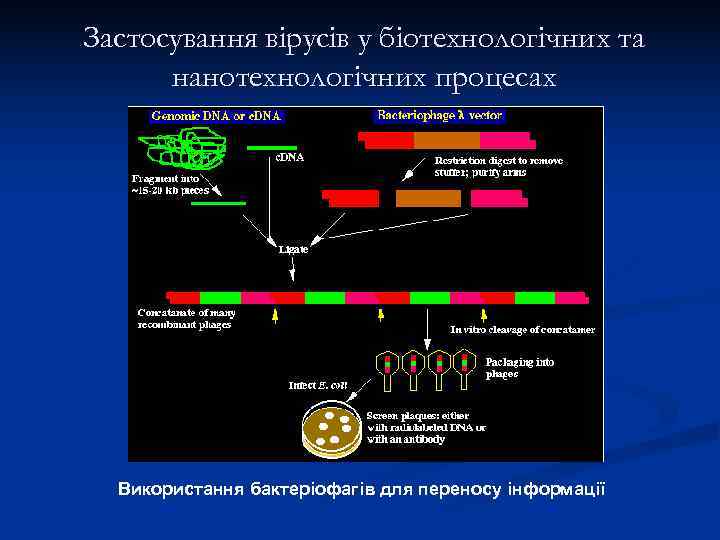
 Застосування вірусів у біотехнологічних та нанотехнологічних процесах Використання бактеріофагів для переносу інформації
Застосування вірусів у біотехнологічних та нанотехнологічних процесах Використання бактеріофагів для переносу інформації
 Застосування вірусів у біотехнологічних та нанотехнологічних процесах Схема переносу генів з використанням ретровірусних векторів
Застосування вірусів у біотехнологічних та нанотехнологічних процесах Схема переносу генів з використанням ретровірусних векторів
 Застосування вірусів у біотехнологічних та нанотехнологічних процесах ВТМ проти ВІЛ В лабораторії Біотехнології Томас Джефферсон Університету (Філадельфія, США) створений шпинат для виготовлення вакцини проти ВІЛ. Ген білку Tat був вбудований в вірус- вектор (ВТМ). Рослини можуть виробляти його в значних кількостях
Застосування вірусів у біотехнологічних та нанотехнологічних процесах ВТМ проти ВІЛ В лабораторії Біотехнології Томас Джефферсон Університету (Філадельфія, США) створений шпинат для виготовлення вакцини проти ВІЛ. Ген білку Tat був вбудований в вірус- вектор (ВТМ). Рослини можуть виробляти його в значних кількостях
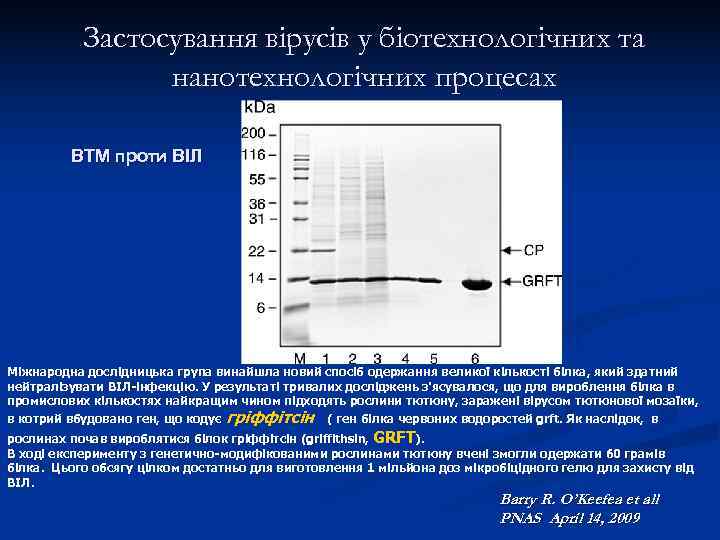
 Застосування вірусів у біотехнологічних та нанотехнологічних процесах ВТМ проти ВІЛ Міжнародна дослідницька група винайшла новий спосіб одержання великої кількості білка, який здатний нейтралізувати ВІЛ-інфекцію. У результаті тривалих досліджень з'ясувалося, що для вироблення білка в промислових кількостях найкращим чином підходять рослини тютюну, заражені вірусом тютюнової мозаїки, в котрий вбудовано ген, що кодує гріффітсін ( ген білка червоних водоростей grft. Як наслідок, в рослинах почав вироблятися білок гріффітсін (griffithsin, GRFT). В ході експерименту з генетично-модифікованими рослинами тютюну вчені змогли одержати 60 грамів білка. Цього обсягу цілком достатньо для виготовлення 1 мільйона доз мікробіцідного гелю для захисту від ВІЛ. Barry R. O’Keefea et all PNAS April 14, 2009
Застосування вірусів у біотехнологічних та нанотехнологічних процесах ВТМ проти ВІЛ Міжнародна дослідницька група винайшла новий спосіб одержання великої кількості білка, який здатний нейтралізувати ВІЛ-інфекцію. У результаті тривалих досліджень з'ясувалося, що для вироблення білка в промислових кількостях найкращим чином підходять рослини тютюну, заражені вірусом тютюнової мозаїки, в котрий вбудовано ген, що кодує гріффітсін ( ген білка червоних водоростей grft. Як наслідок, в рослинах почав вироблятися білок гріффітсін (griffithsin, GRFT). В ході експерименту з генетично-модифікованими рослинами тютюну вчені змогли одержати 60 грамів білка. Цього обсягу цілком достатньо для виготовлення 1 мільйона доз мікробіцідного гелю для захисту від ВІЛ. Barry R. O’Keefea et all PNAS April 14, 2009
 Застосування вірусів у біотехнологічних та нанотехнологічних процесах Фагова нанобіотехнологія • Фагозалежне розпізнавання в біосенсорах • Фаговий транспорт генів та ліків до клітини • Фагозалежні пацієнт-специфічні навігаційні системи • Синтез неорганічних наноречовин за допомогою фагів • Сайт-специфічна хімічна модифікація фагових частинок
Застосування вірусів у біотехнологічних та нанотехнологічних процесах Фагова нанобіотехнологія • Фагозалежне розпізнавання в біосенсорах • Фаговий транспорт генів та ліків до клітини • Фагозалежні пацієнт-специфічні навігаційні системи • Синтез неорганічних наноречовин за допомогою фагів • Сайт-специфічна хімічна модифікація фагових частинок
 Використання вірусів для лікування онкозахворювань Вірусотерапія Ттранскрипційний - використовує віруси, в геном яких по Ттранскрипційний Ттрансдукційний - передбачає створення таких різновидів сусідству з одним з життєво важливих генів вбудований звичайних вірусів (наприклад, штамів аденовірусів, що пухлиноспецифічний промотор. Він включаєтся тільки в викликають гостру респіраторну інфекцію), які вибірково ракових клітинах, і тільки в них може транскрибуватися інфікують та вбивають ракові клітини. Вирости на білковій вірусна ДНК. Мільйони дочірніх вірусних часток, що оболонці цих вірусів мають адапторні молекули або утворюються в раковій клітині, в кінців її лізують та модифіковані білки, які не дозволяють вірусним часточкам інфікують інші ракові клітини. Нормальні клітини також зв’язуватися зі звичайними клітинами, однак допомагать зв’ інфіууються, однак вірус там не розмножується. розпізнаванню ними пухлинних клітин.
Використання вірусів для лікування онкозахворювань Вірусотерапія Ттранскрипційний - використовує віруси, в геном яких по Ттранскрипційний Ттрансдукційний - передбачає створення таких різновидів сусідству з одним з життєво важливих генів вбудований звичайних вірусів (наприклад, штамів аденовірусів, що пухлиноспецифічний промотор. Він включаєтся тільки в викликають гостру респіраторну інфекцію), які вибірково ракових клітинах, і тільки в них може транскрибуватися інфікують та вбивають ракові клітини. Вирости на білковій вірусна ДНК. Мільйони дочірніх вірусних часток, що оболонці цих вірусів мають адапторні молекули або утворюються в раковій клітині, в кінців її лізують та модифіковані білки, які не дозволяють вірусним часточкам інфікують інші ракові клітини. Нормальні клітини також зв’язуватися зі звичайними клітинами, однак допомагать зв’ інфіууються, однак вірус там не розмножується. розпізнаванню ними пухлинних клітин.
 Використання вірусів для лікування онкозахворювань Аденовіруси і меланома Рак шкіри - меланома - одне з найбільш агресивних онкологічних захворювань. В його основі лежить безконтрольний поділ пігментованих клітин шкіри - меланоцитів. Вчені намагаються боротися зі смертельно небезпечною недугою за допомогою вірусів, що знищують клітини меланоми. Поки вони проводять досліди на штучній шкірі людини, яку вирощують у лабораторних чашках. Шкіра складається з меланомних клітин (темні плями на лівій мікрофотографії), нормальних клітин (кератиноцитів) і колагену. Групі вчених під керівництвом Дірка Неттелбека (Dirk M. Nettlebeck) вдалося сконструювати аденовірус, який може розмножуватися тільки в клітинах меланоми. Нормальні кератиноцити на мікрофотографіях пофарбовані червоним, а клітини шкіри, інфіковані вірусом, - зеленим. Мікрофотографія в центрі відображає ситуацію, коли вірус не був специфічний відносно меланомних клітин. Він міг інфікувати нормальні клітини, на фотографіях вони виглядають жовтими. Навпаки, вірус, націлений на пухлинні клітини, в нормальних клітинах не реплікується, і на фото справа немає жодної жовтої клітини. Hum Gene Ther. 2007; 18(1): 51 -62
Використання вірусів для лікування онкозахворювань Аденовіруси і меланома Рак шкіри - меланома - одне з найбільш агресивних онкологічних захворювань. В його основі лежить безконтрольний поділ пігментованих клітин шкіри - меланоцитів. Вчені намагаються боротися зі смертельно небезпечною недугою за допомогою вірусів, що знищують клітини меланоми. Поки вони проводять досліди на штучній шкірі людини, яку вирощують у лабораторних чашках. Шкіра складається з меланомних клітин (темні плями на лівій мікрофотографії), нормальних клітин (кератиноцитів) і колагену. Групі вчених під керівництвом Дірка Неттелбека (Dirk M. Nettlebeck) вдалося сконструювати аденовірус, який може розмножуватися тільки в клітинах меланоми. Нормальні кератиноцити на мікрофотографіях пофарбовані червоним, а клітини шкіри, інфіковані вірусом, - зеленим. Мікрофотографія в центрі відображає ситуацію, коли вірус не був специфічний відносно меланомних клітин. Він міг інфікувати нормальні клітини, на фотографіях вони виглядають жовтими. Навпаки, вірус, націлений на пухлинні клітини, в нормальних клітинах не реплікується, і на фото справа немає жодної жовтої клітини. Hum Gene Ther. 2007; 18(1): 51 -62
 Використання бактеріофагів для боротьтби з бактеріальними інфекціями
Використання бактеріофагів для боротьтби з бактеріальними інфекціями
 Розробка стратегій боротьби з вірусними інфекціями в медицині, ветеринарії та рослинництві SARS F&MD HIV PPV
Розробка стратегій боротьби з вірусними інфекціями в медицині, ветеринарії та рослинництві SARS F&MD HIV PPV
 Вірус мозаїки вігни (CPMV) n Створення електроактивних наноматеріалів
Вірус мозаїки вігни (CPMV) n Створення електроактивних наноматеріалів
 Створення наноматеріалів з унікальними властивостями -Можливість використання для створення світлозбиральних елементів Фотографія отримана за допомогою електронного мікроскопа
Створення наноматеріалів з унікальними властивостями -Можливість використання для створення світлозбиральних елементів Фотографія отримана за допомогою електронного мікроскопа
 Застосування вірусів у біотехнологічних та нанотехнологічних процесах Синтез нанопровідника на бактеріофазі М 13– одна из робіт лабораторії біомолекулярних матеріалів MIT (Професор Анжела Белчер, belcher 10. mit. edu). PNAS Jul 2008
Застосування вірусів у біотехнологічних та нанотехнологічних процесах Синтез нанопровідника на бактеріофазі М 13– одна из робіт лабораторії біомолекулярних матеріалів MIT (Професор Анжела Белчер, belcher 10. mit. edu). PNAS Jul 2008
 M 13 та створення літій іонних батарей
M 13 та створення літій іонних батарей
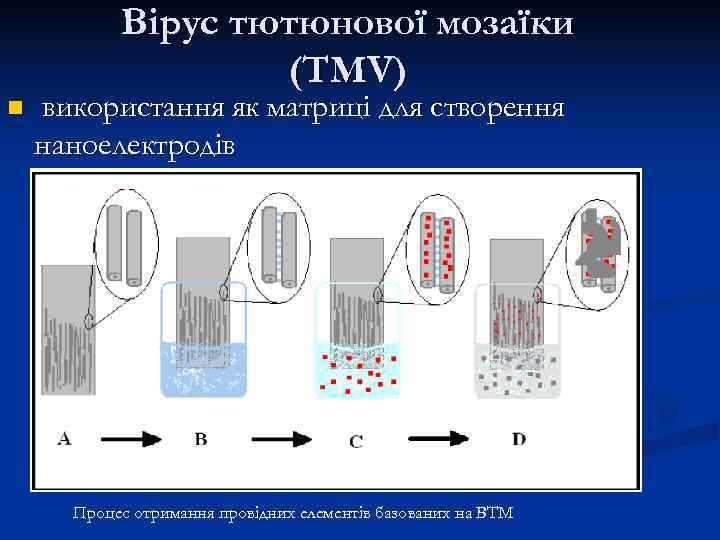
 Вірус тютюнової мозаїки (TMV) n використання як матриці для створення наноелектродів Процес отримання провідних елементів базованих на ВТМ
Вірус тютюнової мозаїки (TMV) n використання як матриці для створення наноелектродів Процес отримання провідних елементів базованих на ВТМ
 Перспективи: n Створення ефективних методів лікування онкологічних та інфекційних захворювань n Створення міцних матеріалів на основі вірусів n Розширення апаратних можливостей електронних приладів
Перспективи: n Створення ефективних методів лікування онкологічних та інфекційних захворювань n Створення міцних матеріалів на основі вірусів n Розширення апаратних можливостей електронних приладів
 Фундаментальна вірусологія n З’ясування молекулярних механізмів взаємодії вірусу і організму-хазяїна n Відкриття та аналіз нових, раніше невідомих вірусів n Вивчення походження та еволюції вірусів n З’ясування ролі вірусів в екологічних нішах та в еволюції всього живого n Інтеграція вірусології в системну біологію
Фундаментальна вірусологія n З’ясування молекулярних механізмів взаємодії вірусу і організму-хазяїна n Відкриття та аналіз нових, раніше невідомих вірусів n Вивчення походження та еволюції вірусів n З’ясування ролі вірусів в екологічних нішах та в еволюції всього живого n Інтеграція вірусології в системну біологію
 З’ясування молекулярних механізмів взаємодії вірусу і організму-хазяїна База даних по генним сіткам інтерферонової індукції противірусної відповіді у эукариот Інтерферонова регуляція противірусної відповіді (генна сітка "Antiviral response") 108 білків 85 генів 219 взаємодій 339 публикацій Дані по 4 організмам: людина, мыша, пацюк, курка
З’ясування молекулярних механізмів взаємодії вірусу і організму-хазяїна База даних по генним сіткам інтерферонової індукції противірусної відповіді у эукариот Інтерферонова регуляція противірусної відповіді (генна сітка "Antiviral response") 108 білків 85 генів 219 взаємодій 339 публикацій Дані по 4 організмам: людина, мыша, пацюк, курка
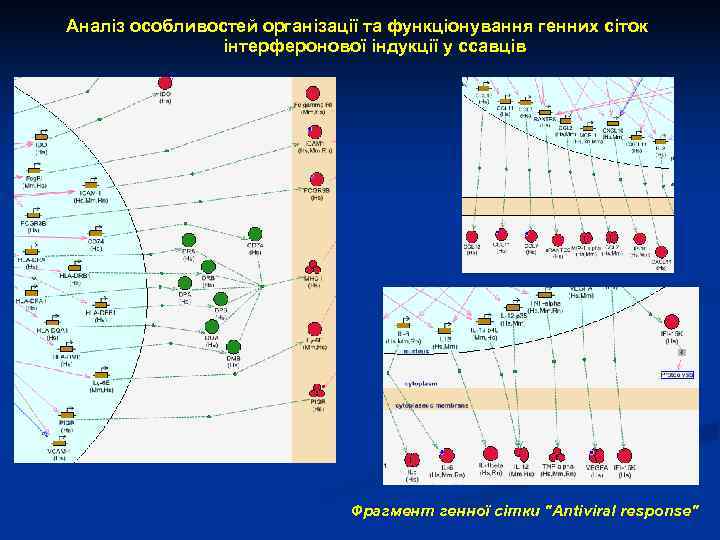
 Аналіз особливостей організації та функціонування генних сіток інтерферонової індукції у ссавців Хемокіни Цитокіни Комплекс гістосумісності, поверхневі рецептори Фрагмент генної сітки "Antiviral response"
Аналіз особливостей організації та функціонування генних сіток інтерферонової індукції у ссавців Хемокіни Цитокіни Комплекс гістосумісності, поверхневі рецептори Фрагмент генної сітки "Antiviral response"
 Білки безпеки n Віруси не мають особливого «бажання» бути небезпечними, тобто шкодочинними, щоб вбивати їх господарів. Патогенні властивості вірусу не є обов'язковою умовою для вірусних пристосувань (fitness). Фактично, найбільш серйозна шкода при вірусній інфекції відбувається не від вірусної репродукції, а від (іноді помилкової) відповіді імунного захисту. Пошкодження клітини-хазіїна або навіть суїцидальні оборонної реакції включають деградацію РНК, інгібування трансляції, і індукцію стресу ендоплазматичного ретикулума, апоптоз, аутофагію та запалення, і ці реакції спрямовані на обмеження вірусної репродукції та розповсюдження. n Як природна реакція, віруси розвивалися як інструменти, спрямовані не тільки на подолання конкретної вродженої і набутої імунної відповіді, але і на інгібування загальних хазяйських метаболічних функцій, , на яких ці конкретні способи оборони засновані, - це такі процеси, як транскрипція і трансляція, клітинні сигнали та внутрішньоклітинні взаємодії (trafficking). Інгібування цих процесів є основною функцією білків безпеки. Відповідно, здатність витримувати відповідь захисних сил організму, , а не вірулентність (здатність завдавати шкоди хазяїну) як така, є властивістю, що вибирається вірусами для еволюції. Довгострокова спільна еволюція вірусу і хазяїна, ймовірно, призведе до їх взаємної адаптації, що супроводжувитиметься зменшенням вірусної вірулентності.
Білки безпеки n Віруси не мають особливого «бажання» бути небезпечними, тобто шкодочинними, щоб вбивати їх господарів. Патогенні властивості вірусу не є обов'язковою умовою для вірусних пристосувань (fitness). Фактично, найбільш серйозна шкода при вірусній інфекції відбувається не від вірусної репродукції, а від (іноді помилкової) відповіді імунного захисту. Пошкодження клітини-хазіїна або навіть суїцидальні оборонної реакції включають деградацію РНК, інгібування трансляції, і індукцію стресу ендоплазматичного ретикулума, апоптоз, аутофагію та запалення, і ці реакції спрямовані на обмеження вірусної репродукції та розповсюдження. n Як природна реакція, віруси розвивалися як інструменти, спрямовані не тільки на подолання конкретної вродженої і набутої імунної відповіді, але і на інгібування загальних хазяйських метаболічних функцій, , на яких ці конкретні способи оборони засновані, - це такі процеси, як транскрипція і трансляція, клітинні сигнали та внутрішньоклітинні взаємодії (trafficking). Інгібування цих процесів є основною функцією білків безпеки. Відповідно, здатність витримувати відповідь захисних сил організму, , а не вірулентність (здатність завдавати шкоди хазяїну) як така, є властивістю, що вибирається вірусами для еволюції. Довгострокова спільна еволюція вірусу і хазяїна, ймовірно, призведе до їх взаємної адаптації, що супроводжувитиметься зменшенням вірусної вірулентності.
 Білки безпеки (на прикладі пікорнавірусів) Функціонально ці білки (L, L * і 2 А) були охарактеризовані детально тільки для деяких пікорнавірусів і в цьому випадку було показано, що протидія захисним силам організму є їх основною функцією забезпечуючи тим самим оптимальні умови для вірусної репродукції
Білки безпеки (на прикладі пікорнавірусів) Функціонально ці білки (L, L * і 2 А) були охарактеризовані детально тільки для деяких пікорнавірусів і в цьому випадку було показано, що протидія захисним силам організму є їх основною функцією забезпечуючи тим самим оптимальні умови для вірусної репродукції
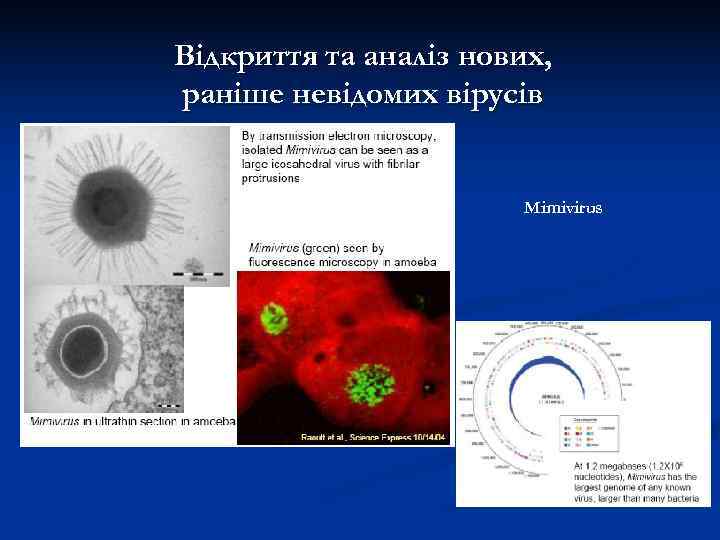
 Відкриття та аналіз нових, раніше невідомих вірусів Mimivirus
Відкриття та аналіз нових, раніше невідомих вірусів Mimivirus
 Valeriy Polischuk Virology Department Kyiv National Taras Shevchenko University
Valeriy Polischuk Virology Department Kyiv National Taras Shevchenko University
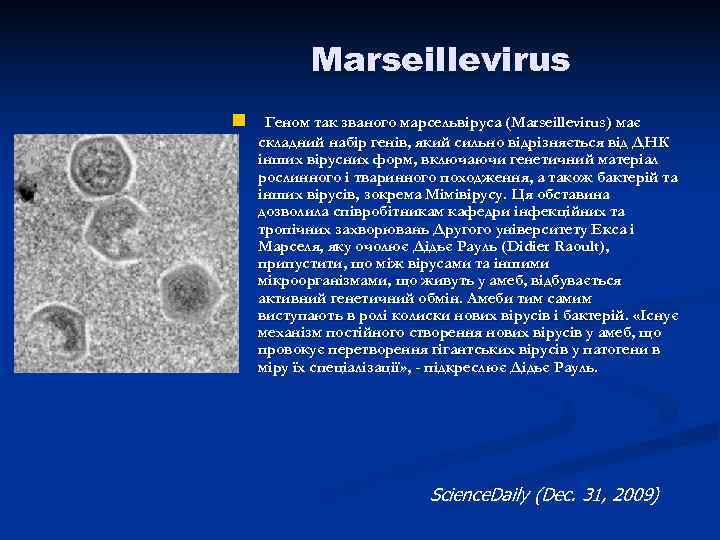
 Marseillevirus n Геном так званого марсельвіруса (Marseillevirus) має складний набір генів, який сильно відрізняється від ДНК інших вірусних форм, включаючи генетичний матеріал рослинного і тваринного походження, а також бактерій та інших вірусів, зокрема Мімівірусу. Ця обставина дозволила співробітникам кафедри інфекційних та тропічних захворювань Другого університету Екса і Марселя, яку очолює Дідьє Рауль (Didier Raoult), припустити, що між вірусами та іншими мікроорганізмами, що живуть у амеб, відбувається активний генетичний обмін. Амеби тим самим виступають в ролі колиски нових вірусів і бактерій. «Існує механізм постійного створення нових вірусів у амеб, що провокує перетворення гігантських вірусів у патогени в міру їх спеціалізації» , - підкреслює Дідьє Рауль. Science. Daily (Dec. 31, 2009)
Marseillevirus n Геном так званого марсельвіруса (Marseillevirus) має складний набір генів, який сильно відрізняється від ДНК інших вірусних форм, включаючи генетичний матеріал рослинного і тваринного походження, а також бактерій та інших вірусів, зокрема Мімівірусу. Ця обставина дозволила співробітникам кафедри інфекційних та тропічних захворювань Другого університету Екса і Марселя, яку очолює Дідьє Рауль (Didier Raoult), припустити, що між вірусами та іншими мікроорганізмами, що живуть у амеб, відбувається активний генетичний обмін. Амеби тим самим виступають в ролі колиски нових вірусів і бактерій. «Існує механізм постійного створення нових вірусів у амеб, що провокує перетворення гігантських вірусів у патогени в міру їх спеціалізації» , - підкреслює Дідьє Рауль. Science. Daily (Dec. 31, 2009)
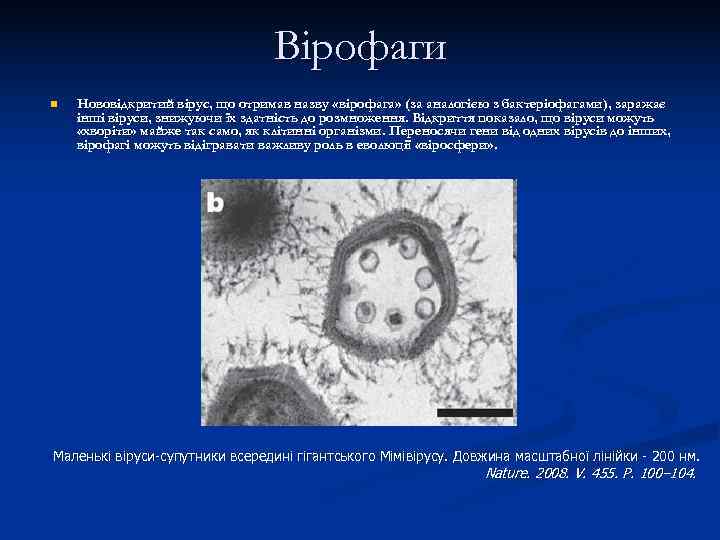
 Вірофаги n Нововідкритий вірус, що отримав назву «вірофага» (за аналогією з бактеріофагами), заражає інші віруси, знижуючи їх здатність до розмноження. Відкриття показало, що віруси можуть «хворіти» майже так само, як клітинні організми. Переносячи гени від одних вірусів до інших, вірофагі можуть відігравати важливу роль в еволюції «віросфери» . Маленькі віруси-супутники всередині гігантського Мімівірусу. Довжина масштабної лінійки - 200 нм. Nature. 2008. V. 455. P. 100– 104.
Вірофаги n Нововідкритий вірус, що отримав назву «вірофага» (за аналогією з бактеріофагами), заражає інші віруси, знижуючи їх здатність до розмноження. Відкриття показало, що віруси можуть «хворіти» майже так само, як клітинні організми. Переносячи гени від одних вірусів до інших, вірофагі можуть відігравати важливу роль в еволюції «віросфери» . Маленькі віруси-супутники всередині гігантського Мімівірусу. Довжина масштабної лінійки - 200 нм. Nature. 2008. V. 455. P. 100– 104.
 n Геном віруса-супутника представляє собою кільцеву молекулу ДНК. Вона складається з 18 343 пар нуклеотидів і містить 21 білок-кодуючий ген. Три з них, очевидно, порівняно недавно були «запозичені» супутником у Мімівірусу, тобто придбані в результаті горизонтального обміну генами - це явище дуже поширене у світі вірусів. Ще один ген явно походить від вірусів - паразитів архей, два інших - від поки ще не описаного сімейства морських вірусів, про існування якого стало відомо в результаті широкомасштабних досліджень вірусної ДНК, ізольованої з морської води. Таким чином, супутник має химерну природу; він «зібрав» свій геном як мінімум з трьох різних джерел. Можливо, багато яких інших вірусів також утворилися в такий спосіб, тобто «зібралися» зі шматочків ДНК інших вірусів і клітинних організмів, але у супутника ознаки химерного походження особливо очевидні.
n Геном віруса-супутника представляє собою кільцеву молекулу ДНК. Вона складається з 18 343 пар нуклеотидів і містить 21 білок-кодуючий ген. Три з них, очевидно, порівняно недавно були «запозичені» супутником у Мімівірусу, тобто придбані в результаті горизонтального обміну генами - це явище дуже поширене у світі вірусів. Ще один ген явно походить від вірусів - паразитів архей, два інших - від поки ще не описаного сімейства морських вірусів, про існування якого стало відомо в результаті широкомасштабних досліджень вірусної ДНК, ізольованої з морської води. Таким чином, супутник має химерну природу; він «зібрав» свій геном як мінімум з трьох різних джерел. Можливо, багато яких інших вірусів також утворилися в такий спосіб, тобто «зібралися» зі шматочків ДНК інших вірусів і клітинних організмів, але у супутника ознаки химерного походження особливо очевидні.
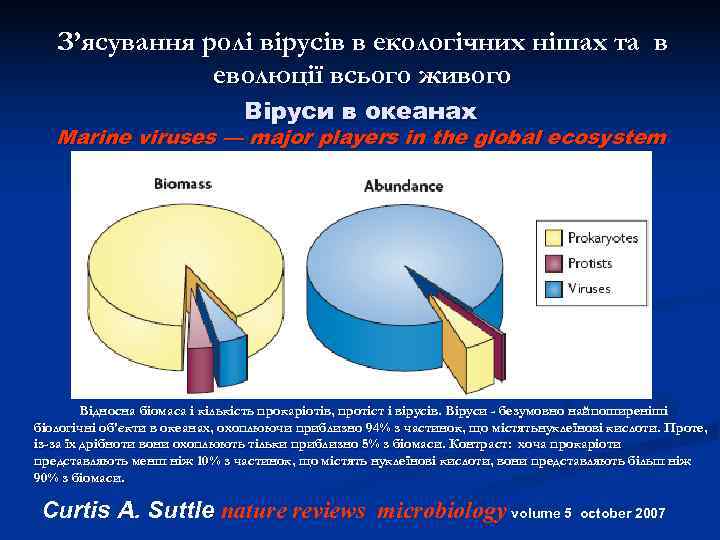
 З’ясування ролі вірусів в екологічних нішах та в еволюції всього живого Віруси в океанах Marine viruses — major players in the global ecosystem Відносна біомаса і кількість прокаріотів, протіст і вірусів. Віруси - безумовно найпоширеніші біологічні об'єкти в океанах, охоплюючи приблизно 94% з частинок, що містятьнуклеїнові кислоти. Проте, із-за їх дрібноти вони охоплюють тільки приблизно 5% з біомаси. Контраст: хоча прокаріоти представляють менш ніж 10% з частинок, що містять нуклеїнові кислоти, вони представляють більш ніж 90% з біомаси. Curtis A. Suttle nature reviews microbiology volume 5 october 2007
З’ясування ролі вірусів в екологічних нішах та в еволюції всього живого Віруси в океанах Marine viruses — major players in the global ecosystem Відносна біомаса і кількість прокаріотів, протіст і вірусів. Віруси - безумовно найпоширеніші біологічні об'єкти в океанах, охоплюючи приблизно 94% з частинок, що містятьнуклеїнові кислоти. Проте, із-за їх дрібноти вони охоплюють тільки приблизно 5% з біомаси. Контраст: хоча прокаріоти представляють менш ніж 10% з частинок, що містять нуклеїнові кислоти, вони представляють більш ніж 90% з біомаси. Curtis A. Suttle nature reviews microbiology volume 5 october 2007
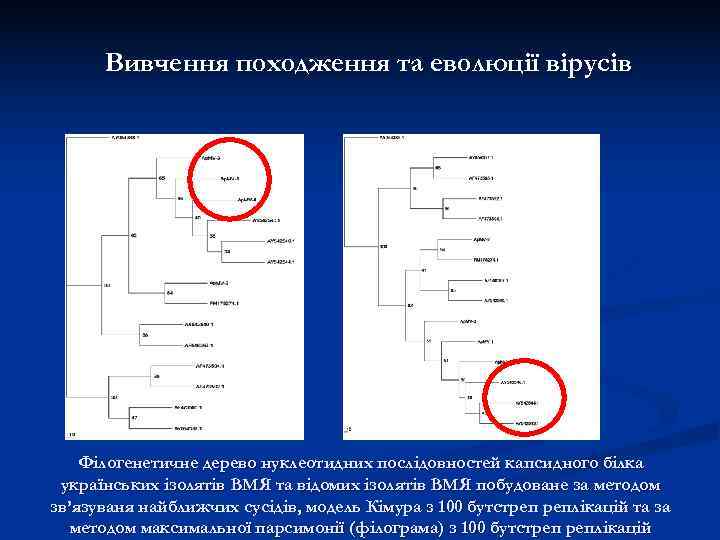
 Вивчення походження та еволюції вірусів Філогенетичне дерево нуклеотидних послідовностей капсидного білка українських ізолятів ВМЯ та відомих ізолятів ВМЯ побудоване за методом зв’язуваня найближчих сусідів, модель Кімура з 100 бутстреп реплікацій та за методом максимальної парсимонії (філограма) з 100 бутстреп реплікацій
Вивчення походження та еволюції вірусів Філогенетичне дерево нуклеотидних послідовностей капсидного білка українських ізолятів ВМЯ та відомих ізолятів ВМЯ побудоване за методом зв’язуваня найближчих сусідів, модель Кімура з 100 бутстреп реплікацій та за методом максимальної парсимонії (філограма) з 100 бутстреп реплікацій
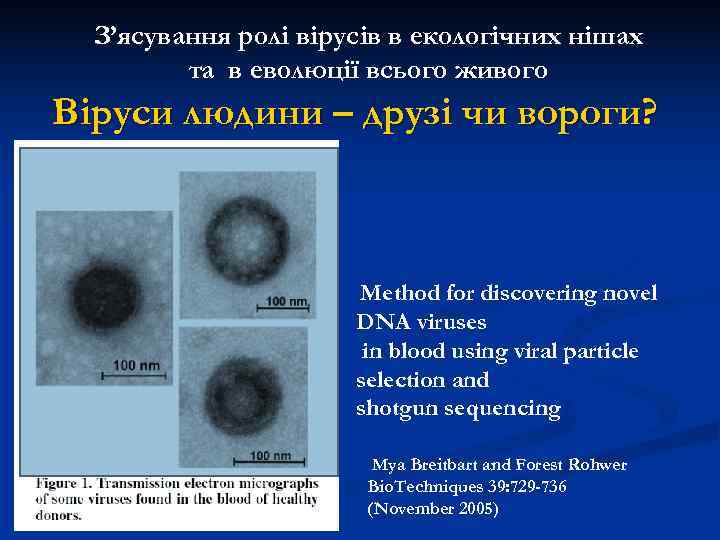
 З’ясування ролі вірусів в екологічних нішах та в еволюції всього живого Віруси людини – друзі чи вороги? Method for discovering novel DNA viruses in blood using viral particle selection and shotgun sequencing Mya Breitbart and Forest Rohwer Bio. Techniques 39: 729 -736 (November 2005)
З’ясування ролі вірусів в екологічних нішах та в еволюції всього живого Віруси людини – друзі чи вороги? Method for discovering novel DNA viruses in blood using viral particle selection and shotgun sequencing Mya Breitbart and Forest Rohwer Bio. Techniques 39: 729 -736 (November 2005)
 Віруси рослин – друзі чи вороги? Non-cultivated plants of the Tallgrass Prairie Preserve of northeastern Oklahoma frequently contain virus-like sequences in particulate fractions Vijay Muthukumara, Ulrich Melcher∗, Marlee Piercea, Graham B. Wileyb, Bruce A. Roeb, Michael. W. Palmerc, Vaskar Thapac, Akhtar Ali d, Tao Dinga Virus Research 141 (2009) 169– 173 Melburne 2010 Date: November 16 -19, 2010 Theme: Plant viruses - Friend or Foe?
Віруси рослин – друзі чи вороги? Non-cultivated plants of the Tallgrass Prairie Preserve of northeastern Oklahoma frequently contain virus-like sequences in particulate fractions Vijay Muthukumara, Ulrich Melcher∗, Marlee Piercea, Graham B. Wileyb, Bruce A. Roeb, Michael. W. Palmerc, Vaskar Thapac, Akhtar Ali d, Tao Dinga Virus Research 141 (2009) 169– 173 Melburne 2010 Date: November 16 -19, 2010 Theme: Plant viruses - Friend or Foe?
 Віруси і віруси “Спеціалісти вважають, що комп’ютерні та людські віруси ведуть себе дуже подібно, і значних збитків від ураження вірусами цифрових пристроїв можна запобігти за допомогою методів, що застосовуються в медицині. “ "Вірус, з'явившись в Азії, доходить до Європи і США, вже маючи серйо імпульс, - говорить Джек Кларк, консультант з компанії Mc. Afee, - Антивірусне програмне забезпечення і людська імунна система працюю схожим принципом, вивчаючи можливості боротьби з новими типами ві в Valeriy Polischuk Virology Department Kyiv National Taras Shevchenko University
Віруси і віруси “Спеціалісти вважають, що комп’ютерні та людські віруси ведуть себе дуже подібно, і значних збитків від ураження вірусами цифрових пристроїв можна запобігти за допомогою методів, що застосовуються в медицині. “ "Вірус, з'явившись в Азії, доходить до Європи і США, вже маючи серйо імпульс, - говорить Джек Кларк, консультант з компанії Mc. Afee, - Антивірусне програмне забезпечення і людська імунна система працюю схожим принципом, вивчаючи можливості боротьби з новими типами ві в Valeriy Polischuk Virology Department Kyiv National Taras Shevchenko University
 n Суперечки про те, чи можна вважати віруси живими істотами, тривають вже не одне десятиліття. Зрозуміло, відповідь в кінцевому рахунку залежить від того, як ми визначимо поняття «життя» (а думок з цього приводу існує безліч). В останні роки отримано багато нових даних, що свідчать про величезну різноманітність вірусів і про несподівано велику роль, яку грає «віросфера» в економіці природи
n Суперечки про те, чи можна вважати віруси живими істотами, тривають вже не одне десятиліття. Зрозуміло, відповідь в кінцевому рахунку залежить від того, як ми визначимо поняття «життя» (а думок з цього приводу існує безліч). В останні роки отримано багато нових даних, що свідчать про величезну різноманітність вірусів і про несподівано велику роль, яку грає «віросфера» в економіці природи
 ОСВІТА Важливим в плані майбутнього вірусології як науки є підготовка нового покоління вчених, здатних до проведення дослідженнь на сучасному рівні. Для цього буде потрібно більше різноманітних пропонованих курсів, розширення можливостей професійної підготовки, особливо за участю міждисциплінарного співробітництва та використання обчислювальних методів, а також навчання роботи в інтернаціональній команді. Для України це означатиме розробку нового концептуального підходу до підготовки фахівців- вірусологів в області біології, медицини та сільського господарства.
ОСВІТА Важливим в плані майбутнього вірусології як науки є підготовка нового покоління вчених, здатних до проведення дослідженнь на сучасному рівні. Для цього буде потрібно більше різноманітних пропонованих курсів, розширення можливостей професійної підготовки, особливо за участю міждисциплінарного співробітництва та використання обчислювальних методів, а також навчання роботи в інтернаціональній команді. Для України це означатиме розробку нового концептуального підходу до підготовки фахівців- вірусологів в області біології, медицини та сільського господарства.
 ДЯКУЮ ЗА УВАГУ!!
ДЯКУЮ ЗА УВАГУ!!

