Пер1од_закон.ppt
- Количество слайдов: 23
 ПЕРІОДИЧНИЙ ЗАКОН ТА ПЕРІОДИЧНА СИСТЕМА 6. Історія відкриття періодичного закону. Періодичний закон у формулюванні Д. І. Менделєєва. Періодична система елементів та її структура. Періодичний закон і електронна будова елементів. Енергетичні характеристики атомів. Атомні та іонні радіуси. 7. Поширення елементів у природі. 1. 2. 3. 4. 5. 1
ПЕРІОДИЧНИЙ ЗАКОН ТА ПЕРІОДИЧНА СИСТЕМА 6. Історія відкриття періодичного закону. Періодичний закон у формулюванні Д. І. Менделєєва. Періодична система елементів та її структура. Періодичний закон і електронна будова елементів. Енергетичні характеристики атомів. Атомні та іонні радіуси. 7. Поширення елементів у природі. 1. 2. 3. 4. 5. 1
 Спроби класифікації хімічних елементів o o o o поділ на метали і неметали (Лавуазьє, Берцеліус); правило тріад Деберейнера, 1829 р. ; радіально-колова таблиця Гінрікса, 1857 р. ; спіраль де Шанкуртуа, 1863 р. ; правило октав Ньюлендса (8 груп елементів у порядку зростання атомних мас), 1864 р. ; таблиця Одлінга (6 груп елементів), 1864 р. ; таблиця Мейера (9 груп елементів), 1864 р. 2
Спроби класифікації хімічних елементів o o o o поділ на метали і неметали (Лавуазьє, Берцеліус); правило тріад Деберейнера, 1829 р. ; радіально-колова таблиця Гінрікса, 1857 р. ; спіраль де Шанкуртуа, 1863 р. ; правило октав Ньюлендса (8 груп елементів у порядку зростання атомних мас), 1864 р. ; таблиця Одлінга (6 груп елементів), 1864 р. ; таблиця Мейера (9 груп елементів), 1864 р. 2
 Правило тріад Й. Деберейнера o o o Літій Li - 6, 94 Натрій Na - 23, 00 Калій K - 39, 1 o Фосфор P - 31, 04 Арсен As - 74, 96 Стибій Sb - 121, 8 o o o o Кальцій Ca - 40, 07 Стронцій Sr - 87, 63 Барій Ba - 137, 37 Сульфур S - 32, 06 Селен Se - 79, 2 Телур Te - 127, 5 Хлор Cl - 35, 5 Бром Br - 80, 0 Йод I - 127, 0 3
Правило тріад Й. Деберейнера o o o Літій Li - 6, 94 Натрій Na - 23, 00 Калій K - 39, 1 o Фосфор P - 31, 04 Арсен As - 74, 96 Стибій Sb - 121, 8 o o o o Кальцій Ca - 40, 07 Стронцій Sr - 87, 63 Барій Ba - 137, 37 Сульфур S - 32, 06 Селен Se - 79, 2 Телур Te - 127, 5 Хлор Cl - 35, 5 Бром Br - 80, 0 Йод I - 127, 0 3
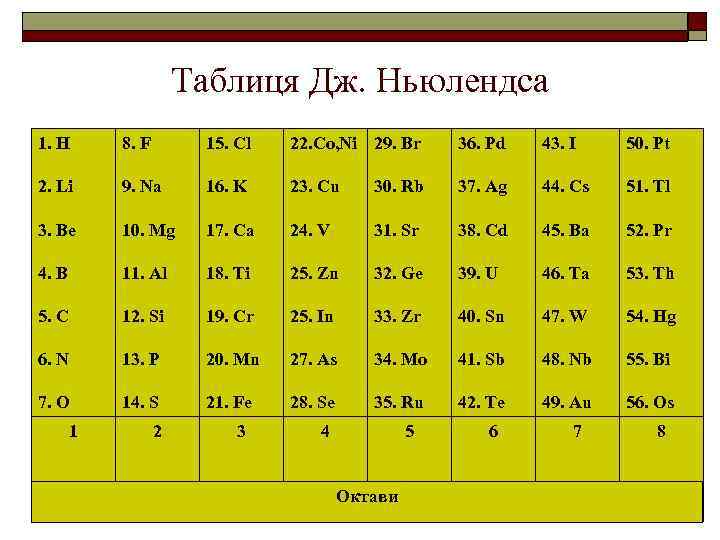 Таблиця Дж. Ньюлендса 1. H 8. F 15. Cl 22. Co, Ni 29. Br 36. Pd 43. I 50. Pt 2. Li 9. Na 16. K 23. Cu 30. Rb 37. Ag 44. Cs 51. Tl 3. Be 10. Mg 17. Ca 24. V 31. Sr 38. Cd 45. Ba 52. Pr 4. B 11. Al 18. Ti 25. Zn 32. Ge 39. U 46. Ta 53. Th 5. C 12. Si 19. Cr 25. In 33. Zr 40. Sn 47. W 54. Hg 6. N 13. P 20. Mn 27. As 34. Mo 41. Sb 48. Nb 55. Bi 7. O 14. S 21. Fe 28. Se 35. Ru 42. Te 49. Au 56. Os 1 2 3 4 5 Октави 6 7 8 4
Таблиця Дж. Ньюлендса 1. H 8. F 15. Cl 22. Co, Ni 29. Br 36. Pd 43. I 50. Pt 2. Li 9. Na 16. K 23. Cu 30. Rb 37. Ag 44. Cs 51. Tl 3. Be 10. Mg 17. Ca 24. V 31. Sr 38. Cd 45. Ba 52. Pr 4. B 11. Al 18. Ti 25. Zn 32. Ge 39. U 46. Ta 53. Th 5. C 12. Si 19. Cr 25. In 33. Zr 40. Sn 47. W 54. Hg 6. N 13. P 20. Mn 27. As 34. Mo 41. Sb 48. Nb 55. Bi 7. O 14. S 21. Fe 28. Se 35. Ru 42. Te 49. Au 56. Os 1 2 3 4 5 Октави 6 7 8 4
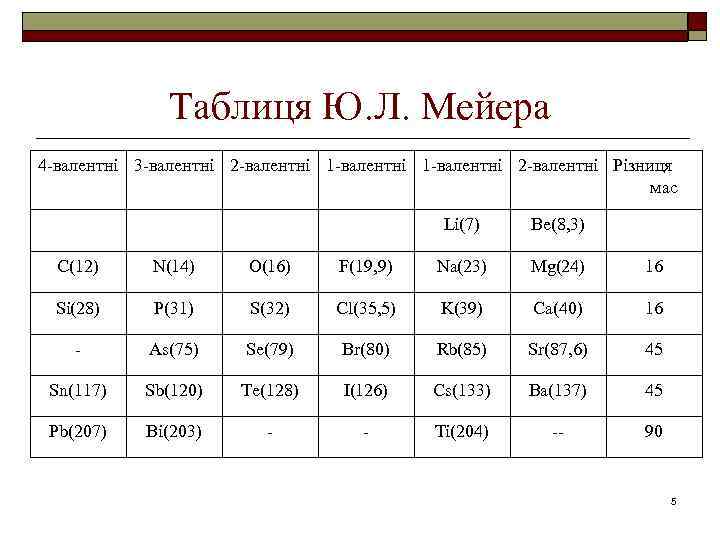 Таблиця Ю. Л. Мейера 4 -валентні 3 -валентні 2 -валентні 1 -валентні 2 -валентні Різниця мас Li(7) Be(8, 3) C(12) N(14) O(16) F(19, 9) Na(23) Mg(24) 16 Si(28) P(31) S(32) Cl(35, 5) K(39) Ca(40) 16 - As(75) Se(79) Br(80) Rb(85) Sr(87, 6) 45 Sn(117) Sb(120) Te(128) I(126) Cs(133) Ba(137) 45 Pb(207) Bi(203) - - Ti(204) -- 90 5
Таблиця Ю. Л. Мейера 4 -валентні 3 -валентні 2 -валентні 1 -валентні 2 -валентні Різниця мас Li(7) Be(8, 3) C(12) N(14) O(16) F(19, 9) Na(23) Mg(24) 16 Si(28) P(31) S(32) Cl(35, 5) K(39) Ca(40) 16 - As(75) Se(79) Br(80) Rb(85) Sr(87, 6) 45 Sn(117) Sb(120) Te(128) I(126) Cs(133) Ba(137) 45 Pb(207) Bi(203) - - Ti(204) -- 90 5
 Періодичний закон у формулюванні Д. І. Менделєєва (1869 р. ): o властивості простих тіл, а також форми і властивості сполук елементів перебувають у періодичній залежності від величини атомних мас елементів. o Сучасне трактування: властивості елементів є періодичною функцією позитивно зарядженого ядра атомів елементів. o Періодична система хімічних елементів – це табличний вираз періодичного закону. 6
Періодичний закон у формулюванні Д. І. Менделєєва (1869 р. ): o властивості простих тіл, а також форми і властивості сполук елементів перебувають у періодичній залежності від величини атомних мас елементів. o Сучасне трактування: властивості елементів є періодичною функцією позитивно зарядженого ядра атомів елементів. o Періодична система хімічних елементів – це табличний вираз періодичного закону. 6
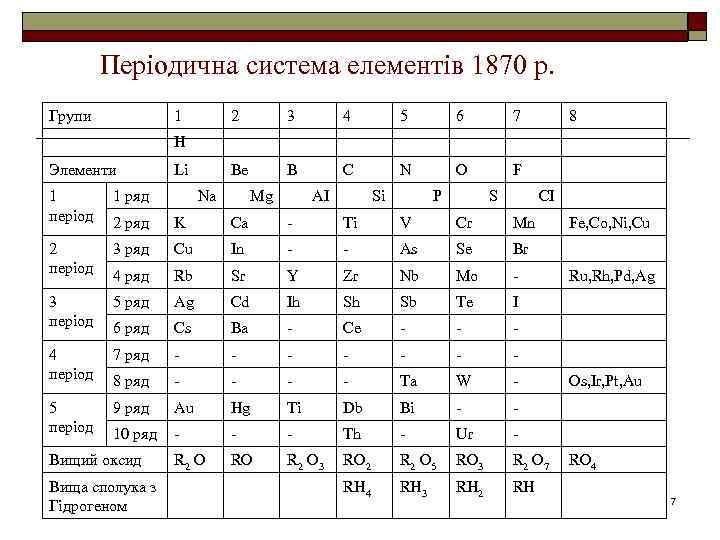 Періодична система елементів 1870 р. Групи 1 2 3 4 5 6 7 Be B C N O 8 F H Элементи Li 1 період 1 ряд 2 ряд K Ca - Ti V Cr Mn 2 період 3 ряд Cu In - - As Se Br 4 ряд Rb Sr Y Zr Nb Mo - 3 період 5 ряд Ag Cd Ih Sh Sb Te I 6 ряд Cs Ba - Ce - - - 4 період 7 ряд - - - - 8 ряд - - Ta W - 5 період 9 ряд Au Hg Ti Db Bi - - 10 ряд - - - Th - Ur - R 2 O RO R 2 O 3 RO 2 R 2 O 5 RO 3 R 2 O 7 RH 4 RH 3 RH 2 RH Вищий оксид Вища сполука з Гідрогеном Na Mg AI Si P S CI Fe, Co, Ni, Cu Ru, Rh, Pd, Ag Os, Ir, Pt, Au RO 4 7
Періодична система елементів 1870 р. Групи 1 2 3 4 5 6 7 Be B C N O 8 F H Элементи Li 1 період 1 ряд 2 ряд K Ca - Ti V Cr Mn 2 період 3 ряд Cu In - - As Se Br 4 ряд Rb Sr Y Zr Nb Mo - 3 період 5 ряд Ag Cd Ih Sh Sb Te I 6 ряд Cs Ba - Ce - - - 4 період 7 ряд - - - - 8 ряд - - Ta W - 5 період 9 ряд Au Hg Ti Db Bi - - 10 ряд - - - Th - Ur - R 2 O RO R 2 O 3 RO 2 R 2 O 5 RO 3 R 2 O 7 RH 4 RH 3 RH 2 RH Вищий оксид Вища сполука з Гідрогеном Na Mg AI Si P S CI Fe, Co, Ni, Cu Ru, Rh, Pd, Ag Os, Ir, Pt, Au RO 4 7
 Структура періодичної системи o Період – це горизонтальний ряд хімічних елементів, розміщених за зростанням їхніх протонних чисел, який починається із лужного металу (1 період – з Гідрогену) і закінчується шляхетним газом. У періодах простежується поступове послаблення металічних властивостей елементів і наростання неметалічних з переходом до шляхетних газів. o Великі періоди поділяються на два ряди – парний і непарний, в яких проявляється подвійна періодичність зміни властивостей. 8
Структура періодичної системи o Період – це горизонтальний ряд хімічних елементів, розміщених за зростанням їхніх протонних чисел, який починається із лужного металу (1 період – з Гідрогену) і закінчується шляхетним газом. У періодах простежується поступове послаблення металічних властивостей елементів і наростання неметалічних з переходом до шляхетних газів. o Великі періоди поділяються на два ряди – парний і непарний, в яких проявляється подвійна періодичність зміни властивостей. 8
 Структура періодичної системи o Група – вертикальний стовпчик подібних елементів, що належать до різних періодів. o Кожна група складається з головної і побічної підгрупи, і містить по одному елементу з малих періодів і по два – з великих. o Номер групи вказує на вищу валентність елемента за Оксигеном. Винятки: Сu, Ag, Au; F; елементи VIII групи, крім Os, Ru i Xe. o Валентність елемента у летких сполуках з Гідрогеном (тільки для елементів головних підгруп IV–VII груп) дорівнює: 8 – номер групи. o У групах із зростанням атомних мас елементів посилюються їхні металічні властивості. 9
Структура періодичної системи o Група – вертикальний стовпчик подібних елементів, що належать до різних періодів. o Кожна група складається з головної і побічної підгрупи, і містить по одному елементу з малих періодів і по два – з великих. o Номер групи вказує на вищу валентність елемента за Оксигеном. Винятки: Сu, Ag, Au; F; елементи VIII групи, крім Os, Ru i Xe. o Валентність елемента у летких сполуках з Гідрогеном (тільки для елементів головних підгруп IV–VII груп) дорівнює: 8 – номер групи. o У групах із зростанням атомних мас елементів посилюються їхні металічні властивості. 9
 Структура періодичної системи o Родини - ряди подібних елементів, які розміщені в одній і тій самій групі і в одному періоді (за винятком платиноїдів). Родина Феруму - Fe, Co і Ni; родина платиноїдів – Ru, Rh, Pd, Os, Ir i Pt. o У VI періоді, відразу за Лантаном, розташовані 14 елементів (порядкові номери 58– 71, Ce–Lu), що називаються лантаноїдами. Хімічні властивості лантаноїдів дуже подібні. o 14 елементів VII періоду (з номерами 90– 103) утворюють родину актиноїдів. Актиноїди значно відрізняються між собою за хімічними властивостями. 10
Структура періодичної системи o Родини - ряди подібних елементів, які розміщені в одній і тій самій групі і в одному періоді (за винятком платиноїдів). Родина Феруму - Fe, Co і Ni; родина платиноїдів – Ru, Rh, Pd, Os, Ir i Pt. o У VI періоді, відразу за Лантаном, розташовані 14 елементів (порядкові номери 58– 71, Ce–Lu), що називаються лантаноїдами. Хімічні властивості лантаноїдів дуже подібні. o 14 елементів VII періоду (з номерами 90– 103) утворюють родину актиноїдів. Актиноїди значно відрізняються між собою за хімічними властивостями. 10
 Періодичний закон і електронна будова елементів 1. Номер періоду співпадає із значенням головного квантового числа n і відповідає кількості електронних рівнів, що заповнюються у елементів цього періоду: І період – 1 рівень, II період – 2, III – 3 рівні і т. д. 2. Кожен період починається із заповнення s-підрівня нового квантового рівня і закінчується заповненням p-підрівня того ж рівня. 3. У кожному великому періоді, починаючи з елементів ІІІ групи Sc, Y, La і Ac, відбувається заповнення передостаннього d-підрівня. Наприклад, 21 Sc 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 1. 11
Періодичний закон і електронна будова елементів 1. Номер періоду співпадає із значенням головного квантового числа n і відповідає кількості електронних рівнів, що заповнюються у елементів цього періоду: І період – 1 рівень, II період – 2, III – 3 рівні і т. д. 2. Кожен період починається із заповнення s-підрівня нового квантового рівня і закінчується заповненням p-підрівня того ж рівня. 3. У кожному великому періоді, починаючи з елементів ІІІ групи Sc, Y, La і Ac, відбувається заповнення передостаннього d-підрівня. Наприклад, 21 Sc 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 1. 11
 Періодичний закон і електронна будова елементів 4. У лантаноїдів та актиноїдів відбувається заповнення третього з кінця f-підрівня. Електрони зовнішнього шару, які відщеплюються при хімічних реакціях або беруть участь в утворенні ковалентного зв’язку, називаються валентними електронами. 5. Атоми елементів І–ІІІ періодів на зовнішньому рівні містять таку кількість електронів на s- i p-орбіталях, яка відповідає номеру групи (валентні електрони). 12
Періодичний закон і електронна будова елементів 4. У лантаноїдів та актиноїдів відбувається заповнення третього з кінця f-підрівня. Електрони зовнішнього шару, які відщеплюються при хімічних реакціях або беруть участь в утворенні ковалентного зв’язку, називаються валентними електронами. 5. Атоми елементів І–ІІІ періодів на зовнішньому рівні містять таку кількість електронів на s- i p-орбіталях, яка відповідає номеру групи (валентні електрони). 12
 Періодичний закон і електронна будова елементів 6. В атомів елементів непарних рядів великих періодів на зовнішньому рівні також міститься така кількість s- i p-електронів, яка дорівнює номеру групи. 7. Атоми елементів парних рядів великих періодів містять не більше двох електронів на зовнішньому s-підрівні. Ці елементи мають металічні властивості (перехідні метали). 8. У елементів головних підгруп валентними можуть бути лише електрони s- i p-підрівнів зовнішнього рівня. Електронна конфігурація зовнішнього рівня змінюється від ns 1 до ns 2 np 6 (для першого періоду від 1 s 1 до 1 s 2). 13
Періодичний закон і електронна будова елементів 6. В атомів елементів непарних рядів великих періодів на зовнішньому рівні також міститься така кількість s- i p-електронів, яка дорівнює номеру групи. 7. Атоми елементів парних рядів великих періодів містять не більше двох електронів на зовнішньому s-підрівні. Ці елементи мають металічні властивості (перехідні метали). 8. У елементів головних підгруп валентними можуть бути лише електрони s- i p-підрівнів зовнішнього рівня. Електронна конфігурація зовнішнього рівня змінюється від ns 1 до ns 2 np 6 (для першого періоду від 1 s 1 до 1 s 2). 13
 Періодичний закон і електронна будова елементів 9. У елементів побічних підгруп валентними можуть бути s-електрони зовнішнього і d-електрони передостаннього рівня. Наприклад, у атома V - 3 d 3 4 s 2. 10. У лантаноїдів та актиноїдів електронами валентними можуть бути s-електрони зовнішнього рівня, 1 електрон, розміщений на d-орбіталі, та певна кількість електронів, розміщених на f-орбіталі. Наприклад, в атома U - 5 f 3 6 d 1 7 s 2. 11. Атоми шляхетних газів містять на зовнішньому рівні 8 електронів (2 s i 6 p), тому вони розташовані в кінці періодів у VIII групі. 14
Періодичний закон і електронна будова елементів 9. У елементів побічних підгруп валентними можуть бути s-електрони зовнішнього і d-електрони передостаннього рівня. Наприклад, у атома V - 3 d 3 4 s 2. 10. У лантаноїдів та актиноїдів електронами валентними можуть бути s-електрони зовнішнього рівня, 1 електрон, розміщений на d-орбіталі, та певна кількість електронів, розміщених на f-орбіталі. Наприклад, в атома U - 5 f 3 6 d 1 7 s 2. 11. Атоми шляхетних газів містять на зовнішньому рівні 8 електронів (2 s i 6 p), тому вони розташовані в кінці періодів у VIII групі. 14
 Періодичний закон і електронна будова елементів o Отже, при послідовному збільшенні зарядів атомних ядер періодично повторюється конфігурація електронних оболонок і, як наслідок, періодично повторюються хімічні властивості елементів. o Фізичний зміст періодичного закону полягає в тому, що періодична зміна властивостей елементів і їхніх сполук є функцією періодично повторюваних на більш високих енергетичних рівнях подібних електронних структур (Бор, 1921 р. ). 15
Періодичний закон і електронна будова елементів o Отже, при послідовному збільшенні зарядів атомних ядер періодично повторюється конфігурація електронних оболонок і, як наслідок, періодично повторюються хімічні властивості елементів. o Фізичний зміст періодичного закону полягає в тому, що періодична зміна властивостей елементів і їхніх сполук є функцією періодично повторюваних на більш високих енергетичних рівнях подібних електронних структур (Бор, 1921 р. ). 15
 Енергетичні характеристики атомів o Енергія іонізації, І – це енергія, яку потрібно затратити для відщеплення електрона від електронейтрального атома з перетворенням його на позитивно заряджений іон. І = [к. Дж/моль] або [е. В/атом]. o Потенціал іонізації - це найменша різниця потенціалів, яку повинен пройти електрон в електричному полі, щоб отримати кінетичну енергію, достатню для іонізації частинки. Потенціал іонізації виражають у вольтах (В). Значення енергії іонізації в е. В чисельно дорівнює потенціалу іонізації у В. o Чим менший потенціал іонізації елемента, тим сильніше виражені його металічні властивості. 16
Енергетичні характеристики атомів o Енергія іонізації, І – це енергія, яку потрібно затратити для відщеплення електрона від електронейтрального атома з перетворенням його на позитивно заряджений іон. І = [к. Дж/моль] або [е. В/атом]. o Потенціал іонізації - це найменша різниця потенціалів, яку повинен пройти електрон в електричному полі, щоб отримати кінетичну енергію, достатню для іонізації частинки. Потенціал іонізації виражають у вольтах (В). Значення енергії іонізації в е. В чисельно дорівнює потенціалу іонізації у В. o Чим менший потенціал іонізації елемента, тим сильніше виражені його металічні властивості. 16
 Зміна першого потенціалу іонізації у групах і періодах 17
Зміна першого потенціалу іонізації у групах і періодах 17
 Енергетичні характеристики атомів o Спорідненість до електрона, F, – це енергія, що виділяється або поглинається у процесі приєднання електрона до нейтрального атома. F = [к. Дж/моль] або [е. В]. o Електронегативність, – це здатність атомів елемента відтягувати спільну електронну густину порівняно з іншими елементами у сполуці. Кількісно міра електронегативності атома – це півсума його енергії іонізації та спорідненості до електрона (Маллікен): χ = (І + F). 18
Енергетичні характеристики атомів o Спорідненість до електрона, F, – це енергія, що виділяється або поглинається у процесі приєднання електрона до нейтрального атома. F = [к. Дж/моль] або [е. В]. o Електронегативність, – це здатність атомів елемента відтягувати спільну електронну густину порівняно з іншими елементами у сполуці. Кількісно міра електронегативності атома – це півсума його енергії іонізації та спорідненості до електрона (Маллікен): χ = (І + F). 18
 Зміна спорідненості до електрона у групах і періодах 19
Зміна спорідненості до електрона у групах і періодах 19
 Атомні та іонні радіуси o Радіус вільного атома – теоретично розраховане положення головного максимуму густини зовнішньої електронної орбіталі (орбітальний радіус, r 0) або така віддаль від ядра, що охоплює 90% електронної густини (r 1) o Ефективні радіуси визначають при вивченні молекул або кристалів (половина найкоротшої відстані між ядрами сусідніх атомів дорівнює радіусу атома). 20
Атомні та іонні радіуси o Радіус вільного атома – теоретично розраховане положення головного максимуму густини зовнішньої електронної орбіталі (орбітальний радіус, r 0) або така віддаль від ядра, що охоплює 90% електронної густини (r 1) o Ефективні радіуси визначають при вивченні молекул або кристалів (половина найкоротшої відстані між ядрами сусідніх атомів дорівнює радіусу атома). 20
 Поширення елементів у природі Геохімічні групи елементів за Гольдшмідтом (1924 р. ): o o атмофільні елементи – входять до складу атмосфери (O, N, H, шляхетні гази та ін. ); літофільні елементи – входять до складу кам’янистої оболонки Землі (до 120 км углиб) – галогени, O, Al, B, Si, Mg, лужні та лужноземельні метали; РЗЕ; P, Nb, Ta, Ti, Cr, V, W і т. д. ; o халькофільні елементи – входять до складу халькосфери (до 1200 км углиб) – S, Se, Te, Pb, Cu, Ga, In, Tl, Ge та ін. ; o сидерофільні елементи – входять до складу сидеросфери (ядро Землі) – Fe, Ni, Co, Pt i платиноїди, Mo, Re та ін. 21
Поширення елементів у природі Геохімічні групи елементів за Гольдшмідтом (1924 р. ): o o атмофільні елементи – входять до складу атмосфери (O, N, H, шляхетні гази та ін. ); літофільні елементи – входять до складу кам’янистої оболонки Землі (до 120 км углиб) – галогени, O, Al, B, Si, Mg, лужні та лужноземельні метали; РЗЕ; P, Nb, Ta, Ti, Cr, V, W і т. д. ; o халькофільні елементи – входять до складу халькосфери (до 1200 км углиб) – S, Se, Te, Pb, Cu, Ga, In, Tl, Ge та ін. ; o сидерофільні елементи – входять до складу сидеросфери (ядро Землі) – Fe, Ni, Co, Pt i платиноїди, Mo, Re та ін. 21
 Елементи у складі живих організмів o До складу живих організмів входять 18 елементів періодичної системи. o Органогени – C, O, H, N, P i S – є основою всіх біологічних систем, входять до складу білків та нуклеїнових кислот. Загальний масовий відсоток їх в живих організмах ~97, 5%. o 12 інших елементів також необхідні для нормальної життєдіяльності живих організмів. Це 2 неметали – Сl та І, і 10 металів – Na, K, Mg, Ca, Zn, Mn, Fe, Co, Cu, Mo (метали життя або біометали). 22
Елементи у складі живих організмів o До складу живих організмів входять 18 елементів періодичної системи. o Органогени – C, O, H, N, P i S – є основою всіх біологічних систем, входять до складу білків та нуклеїнових кислот. Загальний масовий відсоток їх в живих організмах ~97, 5%. o 12 інших елементів також необхідні для нормальної життєдіяльності живих організмів. Це 2 неметали – Сl та І, і 10 металів – Na, K, Mg, Ca, Zn, Mn, Fe, Co, Cu, Mo (метали життя або біометали). 22
 Елементи вчення про біосферу o В. Вернадський вперше науково обґрунтував роль живої речовини в міграції хімічних елементів земної кори, а також значення хімічних елементів в життєдіяльності живих організмів. o Частина планети, в якій виявляється життя у всій різноманітності, - це біосфера. o Живі організми безперервно викликають міграцію хімічних елементів (біогенна міграція). o Біогеохімічні провінції - зони, в яких організми концентрують один або декілька елементів. 23
Елементи вчення про біосферу o В. Вернадський вперше науково обґрунтував роль живої речовини в міграції хімічних елементів земної кори, а також значення хімічних елементів в життєдіяльності живих організмів. o Частина планети, в якій виявляється життя у всій різноманітності, - це біосфера. o Живі організми безперервно викликають міграцію хімічних елементів (біогенна міграція). o Біогеохімічні провінції - зони, в яких організми концентрують один або декілька елементів. 23


