ПЗ и ПС обзорная.ppt
- Количество слайдов: 62
 Периодический закон. Периодическая система. Периодичность изменения свойств химических элементов
Периодический закон. Периодическая система. Периодичность изменения свойств химических элементов
 Периодический закон • свойства химических элементов и образуемых ими соединений находятся в периодической зависимости от зарядов ядер атомов.
Периодический закон • свойства химических элементов и образуемых ими соединений находятся в периодической зависимости от зарядов ядер атомов.
 Периодическая система • единственная классификация элементов согласно закономерностям строения электронных оболочек их атомов; • период - последовательный ряд элементов, в атомах которых происходит заполнение электронами одинакового числа электронных слоев; • группа –объединяет элементы, имеющие одинаковое строение внешних электронных оболочек атомов.
Периодическая система • единственная классификация элементов согласно закономерностям строения электронных оболочек их атомов; • период - последовательный ряд элементов, в атомах которых происходит заполнение электронами одинакового числа электронных слоев; • группа –объединяет элементы, имеющие одинаковое строение внешних электронных оболочек атомов.
 Периодическая таблица • Принципиальный подход к построению таблиц : элементы располагаются в порядке возрастания заряда ядер их атомов. • Периодических таблиц известно более 500.
Периодическая таблица • Принципиальный подход к построению таблиц : элементы располагаются в порядке возрастания заряда ядер их атомов. • Периодических таблиц известно более 500.
 Периодическая таблица, составленная Д. И. Менделеевым Автограф полной таблицы элементов Д. И. Менделеева, переписанной набело для отправки в типографию 17 февраля 1869 г. Листок с «Опытом системы элементов» Д. И. Менделеева отпечатан. На французском языке для рассылки иностранным ученым
Периодическая таблица, составленная Д. И. Менделеевым Автограф полной таблицы элементов Д. И. Менделеева, переписанной набело для отправки в типографию 17 февраля 1869 г. Листок с «Опытом системы элементов» Д. И. Менделеева отпечатан. На французском языке для рассылки иностранным ученым
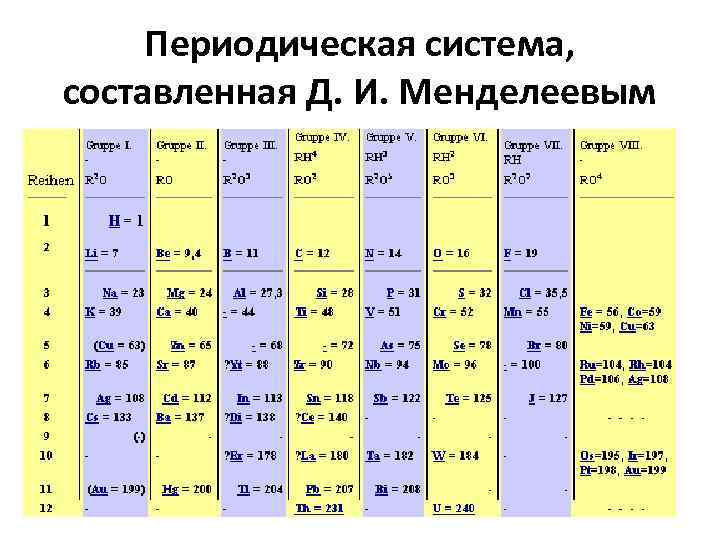 Периодическая система, составленная Д. И. Менделеевым
Периодическая система, составленная Д. И. Менделеевым
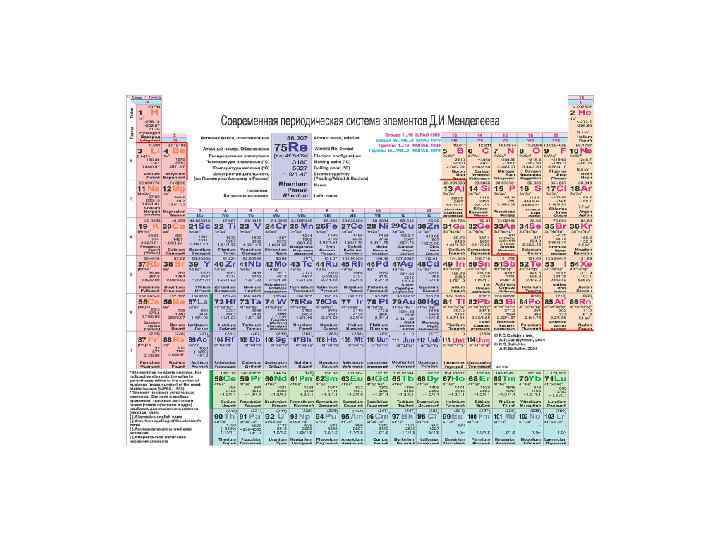
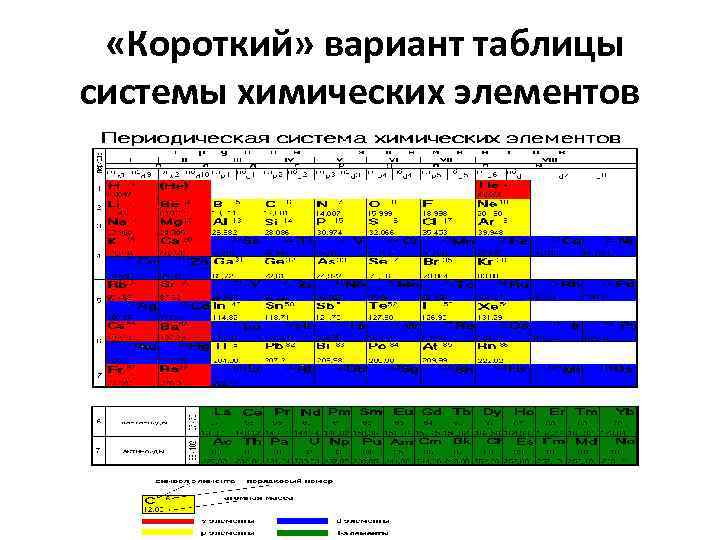 «Короткий» вариант таблицы системы химических элементов
«Короткий» вариант таблицы системы химических элементов
 Квантовомеханическая интерпретация периодической системы
Квантовомеханическая интерпретация периодической системы
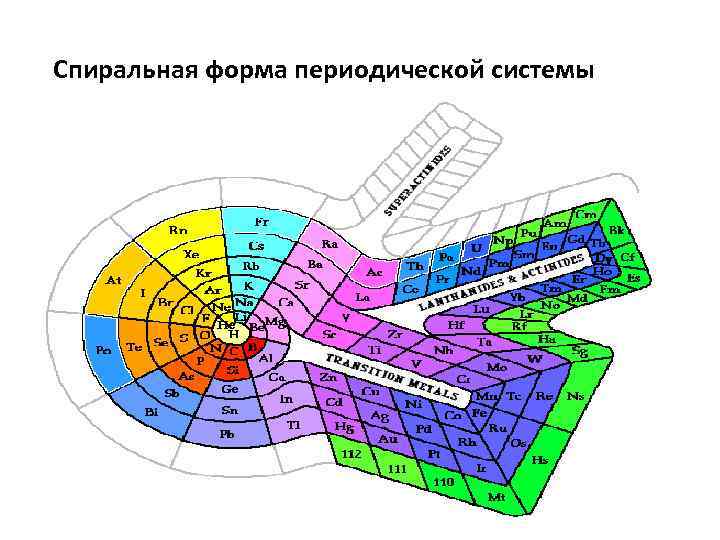 Спиральная форма периодической системы
Спиральная форма периодической системы
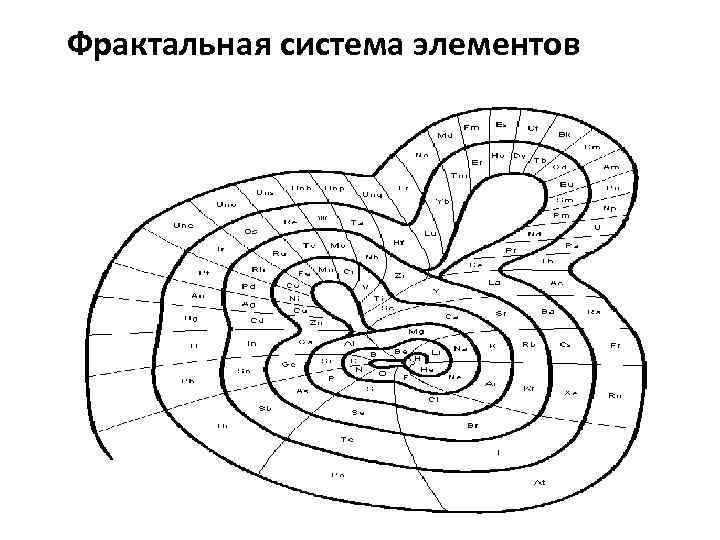 Фрактальная система элементов
Фрактальная система элементов
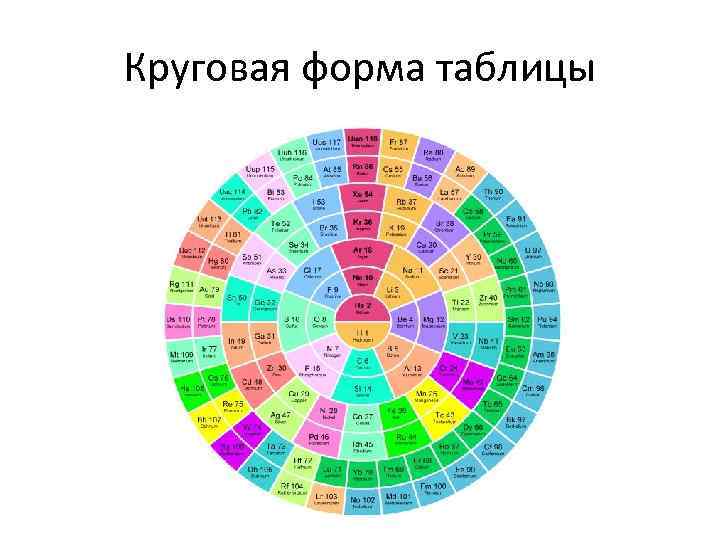 Круговая форма таблицы
Круговая форма таблицы
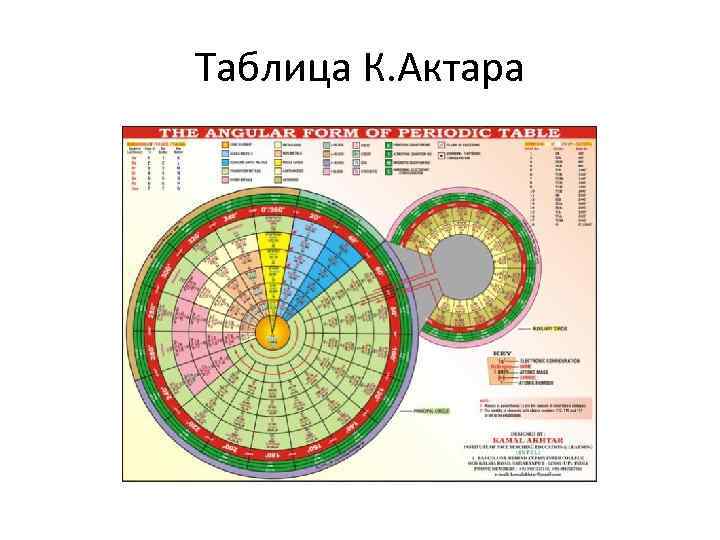 Таблица К. Актара
Таблица К. Актара
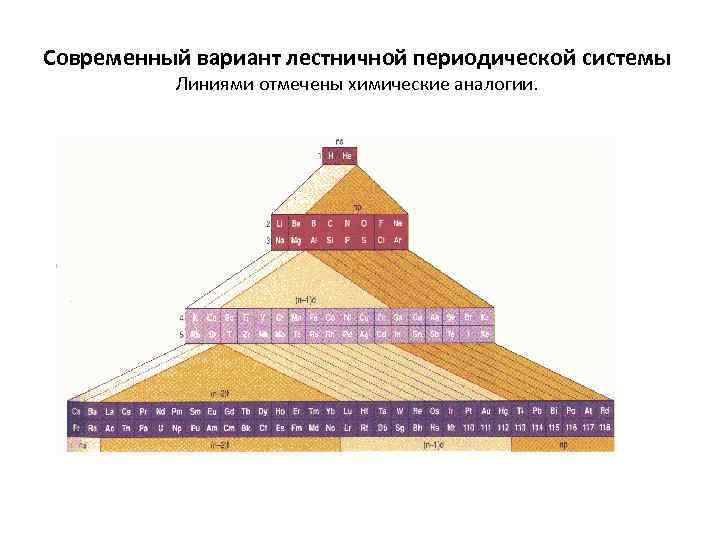 Современный вариант лестничной периодической системы Линиями отмечены химические аналогии.
Современный вариант лестничной периодической системы Линиями отмечены химические аналогии.
 Вариант таблицы Альберта Тарантолы
Вариант таблицы Альберта Тарантолы
 Периодическая таблица • В 2008 г. в Японии вышла книга под названием Периодическая таблица: Изучение основ химии при помощи "мoэ", героинями которого являются 118 девочекэлементов.
Периодическая таблица • В 2008 г. в Японии вышла книга под названием Периодическая таблица: Изучение основ химии при помощи "мoэ", героинями которого являются 118 девочекэлементов.
 ПЕРИОДИЧНОСТЬ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ • заряд ядра • структура внешней (предвнешней) электронной оболочки • размеры атома • энергия ионизации • энергия сродства к электрону • электроотрицательность
ПЕРИОДИЧНОСТЬ СВОЙСТВ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ • заряд ядра • структура внешней (предвнешней) электронной оболочки • размеры атома • энергия ионизации • энергия сродства к электрону • электроотрицательность
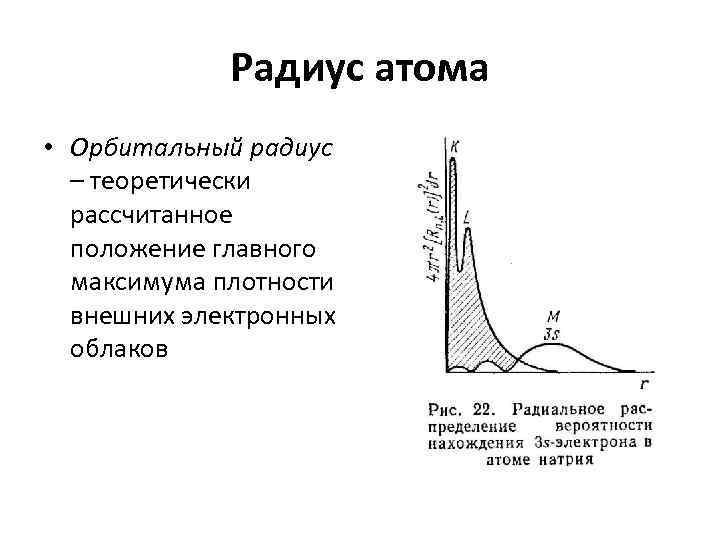 Радиус атома • Орбитальный радиус – теоретически рассчитанное положение главного максимума плотности внешних электронных облаков
Радиус атома • Орбитальный радиус – теоретически рассчитанное положение главного максимума плотности внешних электронных облаков
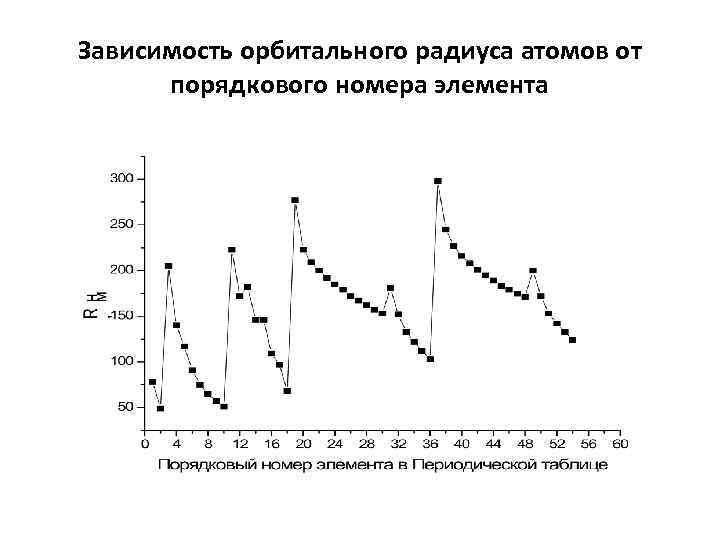 Зависимость орбитального радиуса атомов от порядкового номера элемента
Зависимость орбитального радиуса атомов от порядкового номера элемента
 Эффективный радиус атома • • ковалентный металлический ионный Ван-дер-Ваальсовский
Эффективный радиус атома • • ковалентный металлический ионный Ван-дер-Ваальсовский
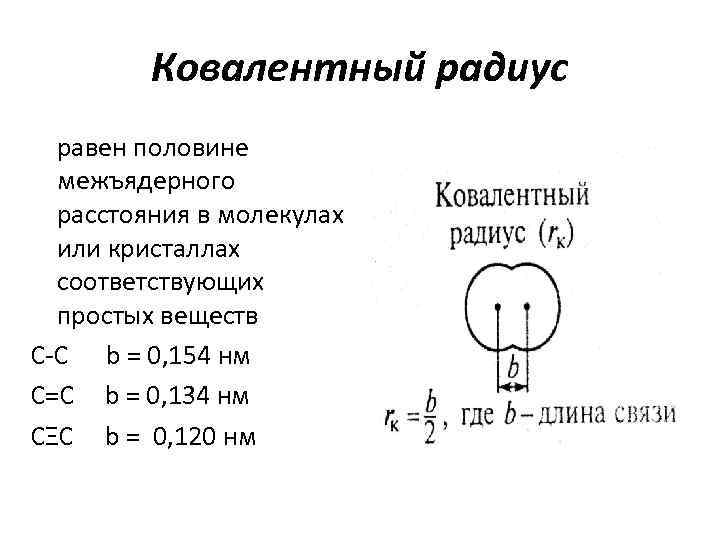 Ковалентный радиус равен половине межъядерного расстояния в молекулах или кристаллах соответствующих простых веществ C-C b = 0, 154 нм C=C b = 0, 134 нм CΞC b = 0, 120 нм
Ковалентный радиус равен половине межъядерного расстояния в молекулах или кристаллах соответствующих простых веществ C-C b = 0, 154 нм C=C b = 0, 134 нм CΞC b = 0, 120 нм
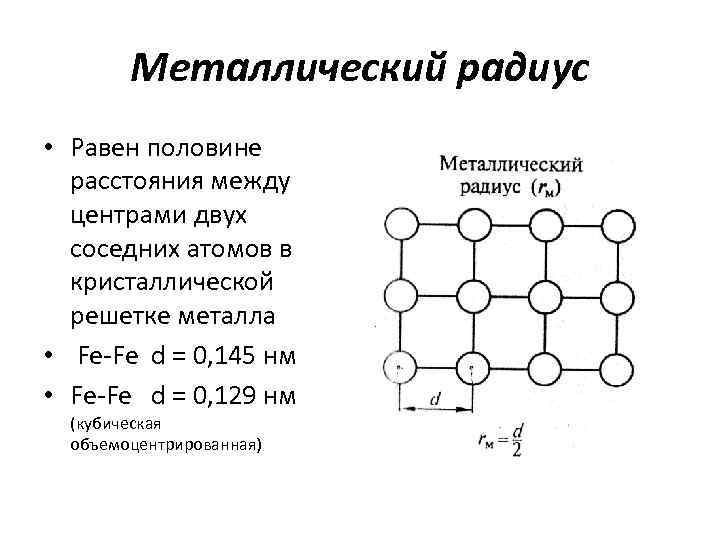 Металлический радиус • Равен половине расстояния между центрами двух соседних атомов в кристаллической решетке металла • Fe-Fe d = 0, 145 нм • Fe-Fe d = 0, 129 нм (кубическая объемоцентрированная)
Металлический радиус • Равен половине расстояния между центрами двух соседних атомов в кристаллической решетке металла • Fe-Fe d = 0, 145 нм • Fe-Fe d = 0, 129 нм (кубическая объемоцентрированная)
 Для золота Au • орбитальный радиус атома – 0, 119 нм; • ковалентный радиус атома – 0, 134 нм; • металлический радиус атома – 0, 146 нм.
Для золота Au • орбитальный радиус атома – 0, 119 нм; • ковалентный радиус атома – 0, 134 нм; • металлический радиус атома – 0, 146 нм.
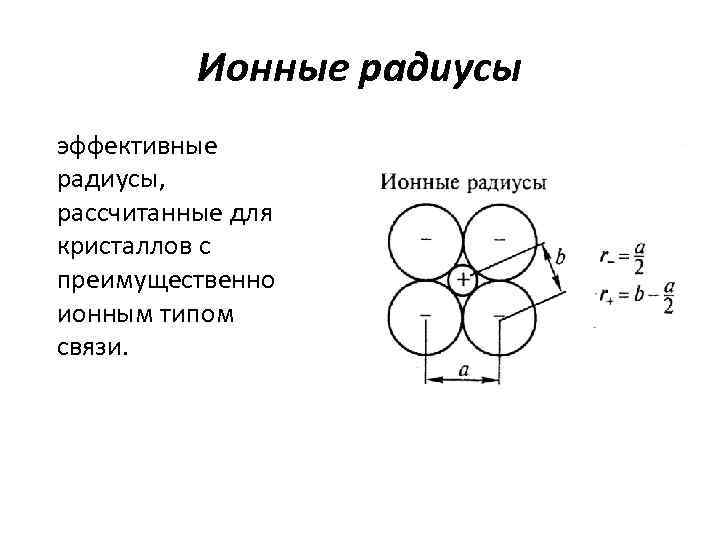 Ионные радиусы эффективные радиусы, рассчитанные для кристаллов с преимущественно ионным типом связи.
Ионные радиусы эффективные радиусы, рассчитанные для кристаллов с преимущественно ионным типом связи.
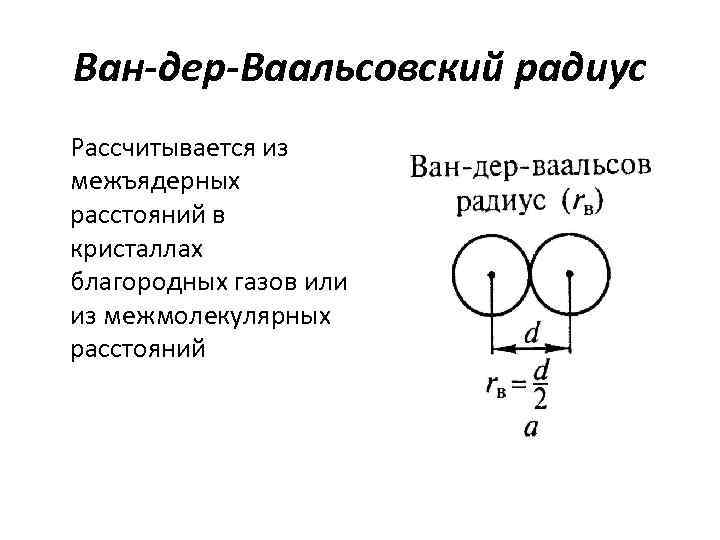 Ван-дер-Ваальсовский радиус Рассчитывается из межъядерных расстояний в кристаллах благородных газов или из межмолекулярных расстояний
Ван-дер-Ваальсовский радиус Рассчитывается из межъядерных расстояний в кристаллах благородных газов или из межмолекулярных расстояний
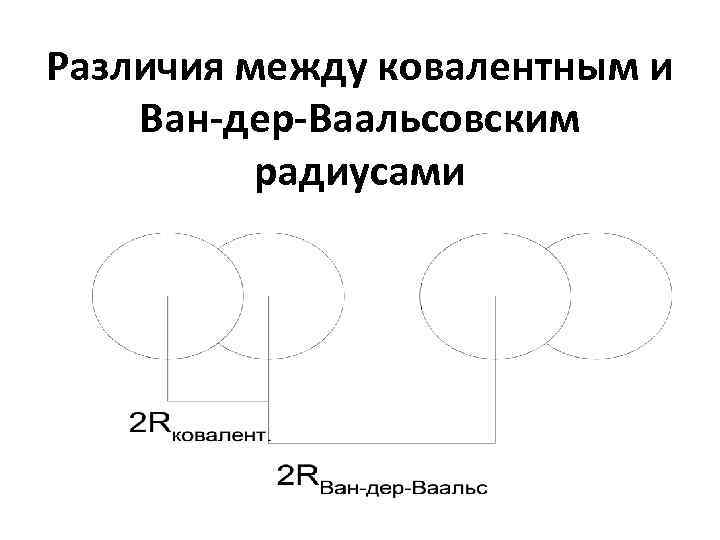 Различия между ковалентным и Ван дер Ваальсовским радиусами
Различия между ковалентным и Ван дер Ваальсовским радиусами
 ЭНЕРГИЯ ИОНИЗАЦИИ • Энергия ионизации – энергия, необходимая для превращения 1 моль атомов в газовой фазе в 1 моль катионов в газовой фазе. Единицы измерения- к. Дж/моль, э. В/атом. • Потенциал ионизации - наименьшее напряжение электрического поля, при котором происходит отрыв электрона от невозбужденного атома. Единицы измерения – В.
ЭНЕРГИЯ ИОНИЗАЦИИ • Энергия ионизации – энергия, необходимая для превращения 1 моль атомов в газовой фазе в 1 моль катионов в газовой фазе. Единицы измерения- к. Дж/моль, э. В/атом. • Потенциал ионизации - наименьшее напряжение электрического поля, при котором происходит отрыв электрона от невозбужденного атома. Единицы измерения – В.
 Величина энергии ионизации определяется: эффективным зарядом ядра; радиусом атома; конфигурацией электронной оболочки; эффектом экранирования электронной оболочки; • проникающей способностью электронов внешнего слоя. • Li – e- = Li⁺ E₁ = 5, 39 э. В Li⁺ – e- = Li⁺⁺ E₂ = 75, 65 э. В Li⁺⁺ – e- = Li⁺⁺⁺ E₃ = 122, 42 э. В • •
Величина энергии ионизации определяется: эффективным зарядом ядра; радиусом атома; конфигурацией электронной оболочки; эффектом экранирования электронной оболочки; • проникающей способностью электронов внешнего слоя. • Li – e- = Li⁺ E₁ = 5, 39 э. В Li⁺ – e- = Li⁺⁺ E₂ = 75, 65 э. В Li⁺⁺ – e- = Li⁺⁺⁺ E₃ = 122, 42 э. В • •
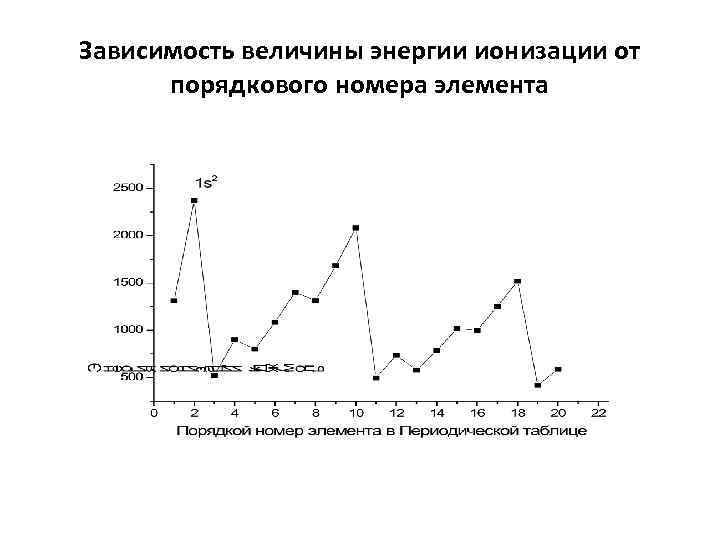 Зависимость величины энергии ионизации от порядкового номера элемента
Зависимость величины энергии ионизации от порядкового номера элемента
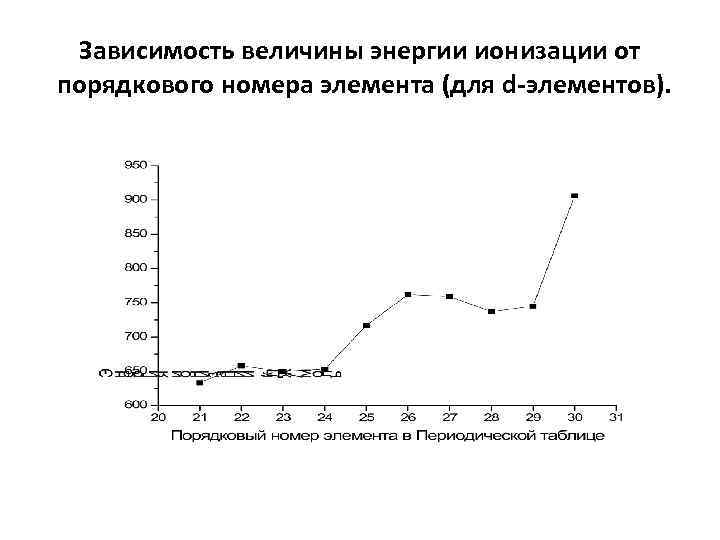 Зависимость величины энергии ионизации от порядкового номера элемента (для d элементов).
Зависимость величины энергии ионизации от порядкового номера элемента (для d элементов).
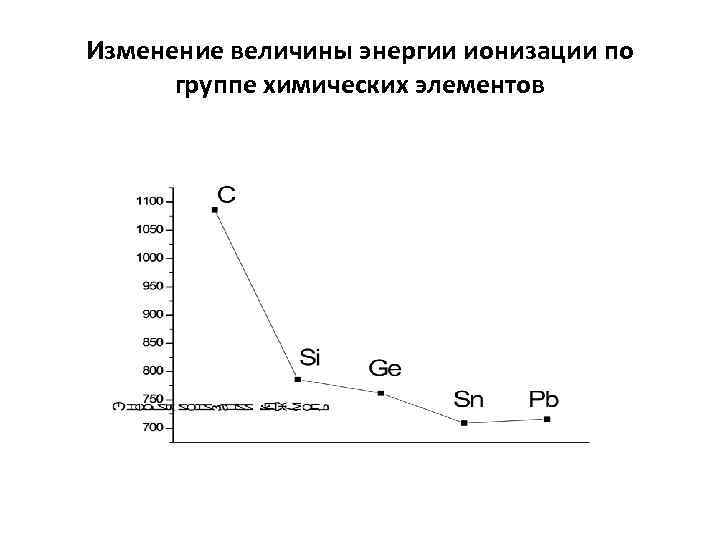 Изменение величины энергии ионизации по группе химических элементов
Изменение величины энергии ионизации по группе химических элементов
 ЭНЕРГИЯ СРОДСТВА К ЭЛЕКТРОНУ • Сродством к электрону F называется энергетический эффект присоединения электрона к нейтральному атому Э с превращением его в отрицательный ион Э-: • Э + e- = Э-+ F; H + e- = H-; E = 0, 75 э. В. • Энергия сродства к электрону = f(заряд ядра (Z), ra, электронной конфигурации).
ЭНЕРГИЯ СРОДСТВА К ЭЛЕКТРОНУ • Сродством к электрону F называется энергетический эффект присоединения электрона к нейтральному атому Э с превращением его в отрицательный ион Э-: • Э + e- = Э-+ F; H + e- = H-; E = 0, 75 э. В. • Энергия сродства к электрону = f(заряд ядра (Z), ra, электронной конфигурации).
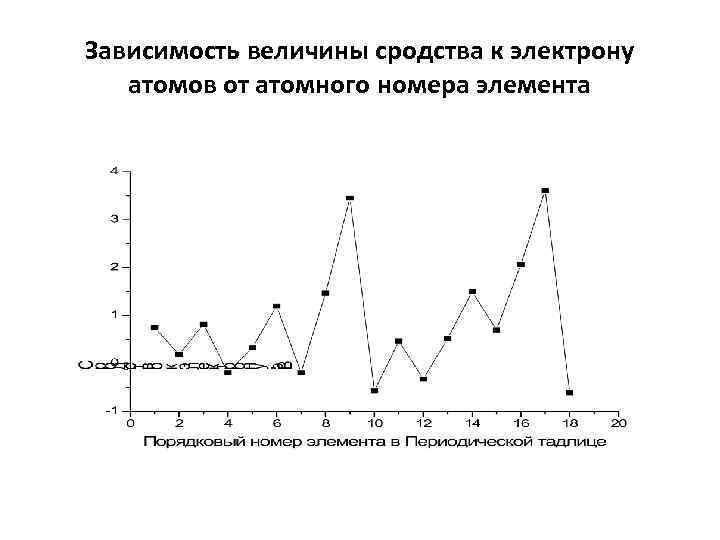 Зависимость величины сродства к электрону атомов от атомного номера элемента
Зависимость величины сродства к электрону атомов от атомного номера элемента
 Сродство к электрону для молекул • Pt. F 6 Е=6, 8 э. В, т. е. он способен отнимать электроны даже у молекулы кислорода, превращая ее в ион O 2+ (образуются кристаллы [O 2 Pt. F 6]
Сродство к электрону для молекул • Pt. F 6 Е=6, 8 э. В, т. е. он способен отнимать электроны даже у молекулы кислорода, превращая ее в ион O 2+ (образуются кристаллы [O 2 Pt. F 6]
 ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ характеристика (условная величина) способности атома в химическом соединении смещать электронную плотность в свою сторону • По Полингу шкала электроотрицательности рассчитана на основании экспериментальных значений энтальпии образования связей в двухатомных молекулах; • наибольшее значение электроотрицательности имеет самый активный неметалл – фтор (χ=4, 0), а наименьшее значение – щелочные металлы – церий и франций (χ=0, 7)
ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ характеристика (условная величина) способности атома в химическом соединении смещать электронную плотность в свою сторону • По Полингу шкала электроотрицательности рассчитана на основании экспериментальных значений энтальпии образования связей в двухатомных молекулах; • наибольшее значение электроотрицательности имеет самый активный неметалл – фтор (χ=4, 0), а наименьшее значение – щелочные металлы – церий и франций (χ=0, 7)
 ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ • По Малликену: χ =1/2(Еиониз+Еср-ва к электрону). • По шкале Оллреда-Рохова электроотрицательность определяется электрическим полем на поверхности атома; ее величина фактически является мерой стабильности электронной оболочки атома. Для атома Не χ = 5, 50.
ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬ • По Малликену: χ =1/2(Еиониз+Еср-ва к электрону). • По шкале Оллреда-Рохова электроотрицательность определяется электрическим полем на поверхности атома; ее величина фактически является мерой стабильности электронной оболочки атома. Для атома Не χ = 5, 50.
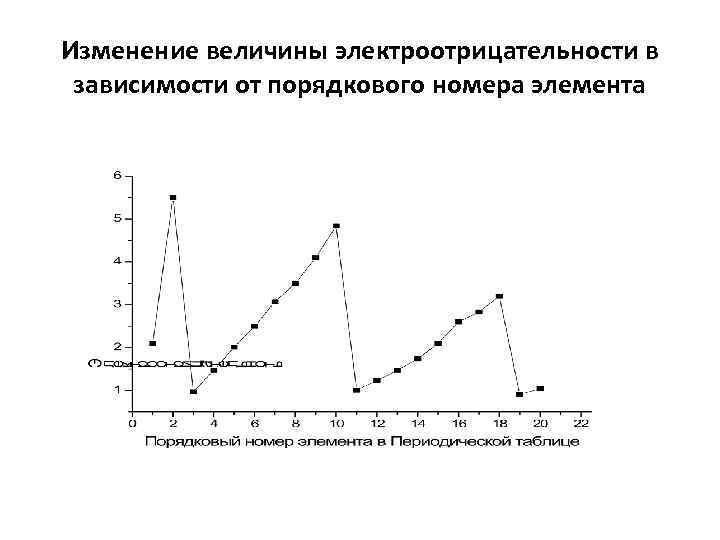 Изменение величины электроотрицательности в зависимости от порядкового номера элемента
Изменение величины электроотрицательности в зависимости от порядкового номера элемента
 Внутренняя периодичность • немонотонное изменение свойств химических элементов по периоду
Внутренняя периодичность • немонотонное изменение свойств химических элементов по периоду
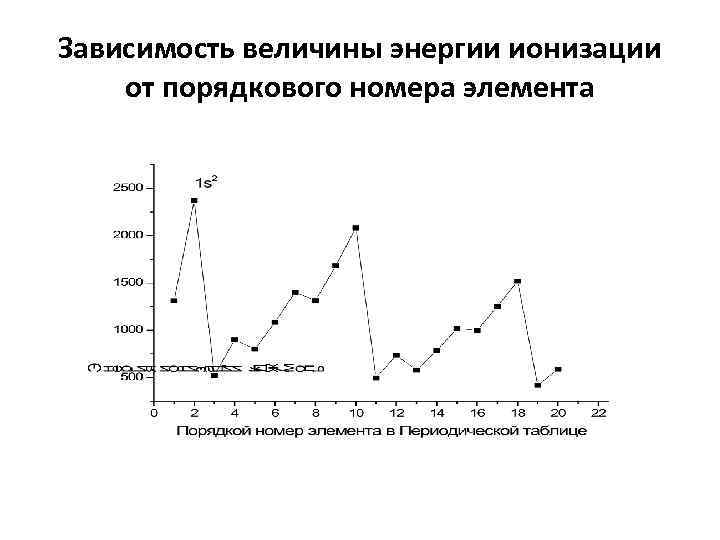 Зависимость величины энергии ионизации от порядкового номера элемента
Зависимость величины энергии ионизации от порядкового номера элемента
 В периодах (с увеличением порядкового номера): • увеличивается заряд ядра, • увеличивается число электронов на внешних атомных орбиталях, • уменьшается радиус атомов, • увеличивается прочность связи электронов с ядром (энергия ионизации), • увеличивается электроотрицательность.
В периодах (с увеличением порядкового номера): • увеличивается заряд ядра, • увеличивается число электронов на внешних атомных орбиталях, • уменьшается радиус атомов, • увеличивается прочность связи электронов с ядром (энергия ионизации), • увеличивается электроотрицательность.
 В группах (с увеличением порядкового номера): • увеличивается заряд ядра, • увеличивается радиус атомов (только в Агруппах), • уменьшается прочность связи электронов с ядром (энергия ионизации; только в Агруппах), • уменьшается электроотрицательность (только в А-группах).
В группах (с увеличением порядкового номера): • увеличивается заряд ядра, • увеличивается радиус атомов (только в Агруппах), • уменьшается прочность связи электронов с ядром (энергия ионизации; только в Агруппах), • уменьшается электроотрицательность (только в А-группах).
 Вторичная периодичность • немонотонное изменение свойств химических элементов по группе Энергия сродства к электрону F 3, 50 э. В Cl 3, 61 э. В Br 3, 54 э. В I 3, 29 э. В
Вторичная периодичность • немонотонное изменение свойств химических элементов по группе Энергия сродства к электрону F 3, 50 э. В Cl 3, 61 э. В Br 3, 54 э. В I 3, 29 э. В
 Диагональная периодичность • Li - Mg (реакции с азотом и углеродом; карбонаты и фосфаты нерастворимы); • Be - Al (взаимодействуют со щелочами, гидроксиды амфотерны, соединения склонны к полимеризации); • B - Si (простые вещества инертны и тугоплавки, образуют кислотные оксиды, галогениды подвергаются гидролизу) • Ионный потенциал = отношение заряда иона к радиусу иона (Z/R) (Be – 5, 9; Al – 5, 9).
Диагональная периодичность • Li - Mg (реакции с азотом и углеродом; карбонаты и фосфаты нерастворимы); • Be - Al (взаимодействуют со щелочами, гидроксиды амфотерны, соединения склонны к полимеризации); • B - Si (простые вещества инертны и тугоплавки, образуют кислотные оксиды, галогениды подвергаются гидролизу) • Ионный потенциал = отношение заряда иона к радиусу иона (Z/R) (Be – 5, 9; Al – 5, 9).
 Диагональная периодичность • Особенно часто диагональное сходство элементов проявляется в явлении изоморфного замещения одними элементами других в кристаллах – гетеровалентный изоморфизм • Примером является диагональ Na+-Ca 2+-Y 3+ с ионными радиусами 0, 98; 1, 06 и 1, 06 Å.
Диагональная периодичность • Особенно часто диагональное сходство элементов проявляется в явлении изоморфного замещения одними элементами других в кристаллах – гетеровалентный изоморфизм • Примером является диагональ Na+-Ca 2+-Y 3+ с ионными радиусами 0, 98; 1, 06 и 1, 06 Å.
 «Звездная» периодичность ( «геохимическая звезда» )
«Звездная» периодичность ( «геохимическая звезда» )
 ХАРАКТЕР ИЗМЕНЕНИЯ СВОЙСТВ СОЕДИНЕНИЙ ЭЛЕМЕНТОВ В ПЕРИОДАХ • Свойства простых веществ и их соединений (оксидов, гидроксидов, водородных соединений) по периоду изменяются от металлических через амфотерные к неметаллическим. Номер группы I II IV V VI VII оксид Na 2 O Mg. O Al 2 O 3 Si. O 2 P 2 O 5 SO 3 Cl 2 O 7 H 2 Si. O 3 H 3 PO 4 H 2 SO 4 HCl. O 4 гидроксид Na. OH Mg(OH)2 Al(OH)3
ХАРАКТЕР ИЗМЕНЕНИЯ СВОЙСТВ СОЕДИНЕНИЙ ЭЛЕМЕНТОВ В ПЕРИОДАХ • Свойства простых веществ и их соединений (оксидов, гидроксидов, водородных соединений) по периоду изменяются от металлических через амфотерные к неметаллическим. Номер группы I II IV V VI VII оксид Na 2 O Mg. O Al 2 O 3 Si. O 2 P 2 O 5 SO 3 Cl 2 O 7 H 2 Si. O 3 H 3 PO 4 H 2 SO 4 HCl. O 4 гидроксид Na. OH Mg(OH)2 Al(OH)3
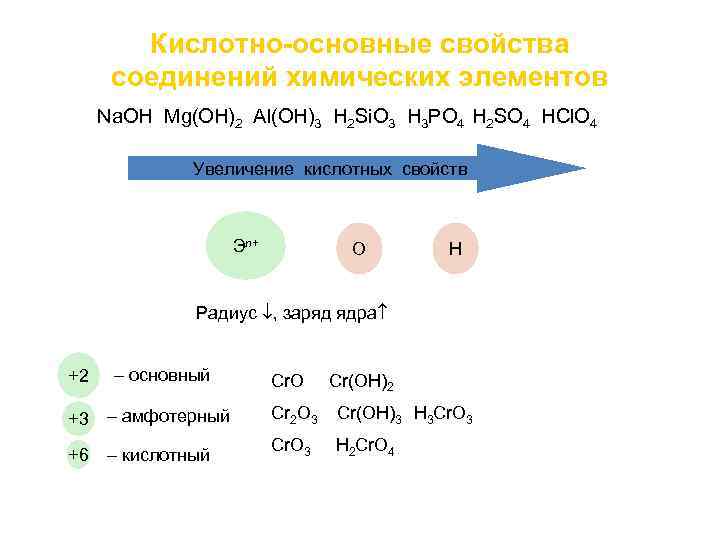 Кислотно-основные свойства соединений химических элементов Na. OН Mg(OH)2 Al(OH)3 H 2 Si. O 3 H 3 PO 4 H 2 SO 4 HСl. O 4 Увеличение кислотных свойств Эn+ О Н Радиус , заряд ядра +2 – основный Cr. O Cr(OH)2 +3 – амфотерный Cr 2 O 3 Cr(OH)3 H 3 Cr. O 3 +6 – кислотный Cr. O 3 H 2 Cr. O 4
Кислотно-основные свойства соединений химических элементов Na. OН Mg(OH)2 Al(OH)3 H 2 Si. O 3 H 3 PO 4 H 2 SO 4 HСl. O 4 Увеличение кислотных свойств Эn+ О Н Радиус , заряд ядра +2 – основный Cr. O Cr(OH)2 +3 – амфотерный Cr 2 O 3 Cr(OH)3 H 3 Cr. O 3 +6 – кислотный Cr. O 3 H 2 Cr. O 4
 В периодах (с увеличением порядкового номера): • усиливаются окислительные свойства простых веществ ("неметалличность"); • ослабевают восстановительные свойства простых веществ ("металличность"); • ослабевает основный характер гидроксидов и соответствующих оксидов; • возрастает кислотный характер гидроксидов и соответствующих оксидов.
В периодах (с увеличением порядкового номера): • усиливаются окислительные свойства простых веществ ("неметалличность"); • ослабевают восстановительные свойства простых веществ ("металличность"); • ослабевает основный характер гидроксидов и соответствующих оксидов; • возрастает кислотный характер гидроксидов и соответствующих оксидов.
 ХАРАКТЕР ИЗМЕНЕНИЯ СВОЙСТВ СОЕДИНЕНИЙ ЭЛЕМЕНТОВ В ГРУППАХ • Элементы второго периода аналогов не имеют. • В каждой А-группе (кроме VIII) металлические свойства простых веществ и основный характер соединений (вследствие увеличения радиуса атома) сверху вниз усиливаются. Оксид B 2 O 3 Гидроксид H 3 BO 3 свойства кислота Al 2 O 3 Ga 2 O 3 Al(OH)3 Ga(OH)3 In(OH)3 Tl(OH)3 амфотерные In 2 O 3 Tl 2 O 3 основание
ХАРАКТЕР ИЗМЕНЕНИЯ СВОЙСТВ СОЕДИНЕНИЙ ЭЛЕМЕНТОВ В ГРУППАХ • Элементы второго периода аналогов не имеют. • В каждой А-группе (кроме VIII) металлические свойства простых веществ и основный характер соединений (вследствие увеличения радиуса атома) сверху вниз усиливаются. Оксид B 2 O 3 Гидроксид H 3 BO 3 свойства кислота Al 2 O 3 Ga 2 O 3 Al(OH)3 Ga(OH)3 In(OH)3 Tl(OH)3 амфотерные In 2 O 3 Tl 2 O 3 основание
 В группах А (с увеличением порядкового номера): • ослабевают окислительные свойства простых веществ ( «неметалличность» ), • усиливаются восстановительные свойства простых веществ ("металличность» ), • возрастает основный характер гидроксидов и соответствующих оксидов; • ослабевает кислотный характер гидроксидов и соответствующих оксидов; • снижается устойчивость водородных соединений (повышается их восстановительная активность).
В группах А (с увеличением порядкового номера): • ослабевают окислительные свойства простых веществ ( «неметалличность» ), • усиливаются восстановительные свойства простых веществ ("металличность» ), • возрастает основный характер гидроксидов и соответствующих оксидов; • ослабевает кислотный характер гидроксидов и соответствующих оксидов; • снижается устойчивость водородных соединений (повышается их восстановительная активность).
 ХАРАКТЕР ИЗМЕНЕНИЯ СВОЙСТВ СОЕДИНЕНИЙ ЭЛЕМЕНТОВ В ГРУППАХ • Сходство между элементами групп А и групп В (главных и побочных подгрупп) наглядно проявляется в соединениях с максимальной степенью окисления. Например, Cl 2 O 7 и Mn 2 O 7 – кислотные оксиды (хотя Mn. О – основный оксид).
ХАРАКТЕР ИЗМЕНЕНИЯ СВОЙСТВ СОЕДИНЕНИЙ ЭЛЕМЕНТОВ В ГРУППАХ • Сходство между элементами групп А и групп В (главных и побочных подгрупп) наглядно проявляется в соединениях с максимальной степенью окисления. Например, Cl 2 O 7 и Mn 2 O 7 – кислотные оксиды (хотя Mn. О – основный оксид).
 ХАРАКТЕР ИЗМЕНЕНИЯ СВОЙСТВ СОЕДИНЕНИЙ В ЗАВИСИМОСТИ ОТ СТЕПЕНИ ОКИСЛЕНИЯ ЭЛЕМЕНТА Оксиды Cr. O Cr 2 O 3 Cr. O 3 Гидроксиды Cr(OH)2 Cr(OH)3; HCr. O 2 H 2 Cr. O 4 свойства амфотер кислота основание → усиление кислотных свойств
ХАРАКТЕР ИЗМЕНЕНИЯ СВОЙСТВ СОЕДИНЕНИЙ В ЗАВИСИМОСТИ ОТ СТЕПЕНИ ОКИСЛЕНИЯ ЭЛЕМЕНТА Оксиды Cr. O Cr 2 O 3 Cr. O 3 Гидроксиды Cr(OH)2 Cr(OH)3; HCr. O 2 H 2 Cr. O 4 свойства амфотер кислота основание → усиление кислотных свойств
 Границы периодической системы «Будущее не грозит периодическому закону разрушением, а только надстройки и развитие обещает» (Д. И. Менделеев, 1905 г. )
Границы периодической системы «Будущее не грозит периодическому закону разрушением, а только надстройки и развитие обещает» (Д. И. Менделеев, 1905 г. )
 Верхняя граница периодической системы наличие электронов в атоме релятивистский эффект Z = 200 радиоактивный распад элементов количество синтезируемых элементов 110 Э – 5 атомов • проблемы идентификации • • •
Верхняя граница периодической системы наличие электронов в атоме релятивистский эффект Z = 200 радиоактивный распад элементов количество синтезируемых элементов 110 Э – 5 атомов • проблемы идентификации • • •
 Проблема синтеза трансурановых элементов: • наличие электронов в атоме – релятивистский эффект; • радиоактивный распад элементов; • количество синтезируемых элементов (5 -10 атомов) и проблемы их идентификации • Верхняя граница ≈200
Проблема синтеза трансурановых элементов: • наличие электронов в атоме – релятивистский эффект; • радиоактивный распад элементов; • количество синтезируемых элементов (5 -10 атомов) и проблемы их идентификации • Верхняя граница ≈200
 Нижняя граница периодической системы • Ньютоний – Д. И. Менделеев • Протон – супруги Кюри
Нижняя граница периодической системы • Ньютоний – Д. И. Менделеев • Протон – супруги Кюри
 Нижняя граница периодической системы • Позитроний (Ps) – электрон и позитрон, вращающиеся вокруг общего центра тяжести перед тем как аннигилировать. «Атомный» вес 1/920, время жизни 10 -10 -10 -7 с. Энергия связи электрона и позитрона = 6, 8 э. В
Нижняя граница периодической системы • Позитроний (Ps) – электрон и позитрон, вращающиеся вокруг общего центра тяжести перед тем как аннигилировать. «Атомный» вес 1/920, время жизни 10 -10 -10 -7 с. Энергия связи электрона и позитрона = 6, 8 э. В
 Нижняя граница периодической системы • Мюоний (Mu) μ⁺ мезон (мюон) и электрон вокруг него масса μ+ мезона = 200 масс электрона, атомный» вес – 1/9, время жизни ~2·10 -6 с. Рисунок из http: //www. arxiv. org/abs/1311. 6431
Нижняя граница периодической системы • Мюоний (Mu) μ⁺ мезон (мюон) и электрон вокруг него масса μ+ мезона = 200 масс электрона, атомный» вес – 1/9, время жизни ~2·10 -6 с. Рисунок из http: //www. arxiv. org/abs/1311. 6431
 Нижняя граница периодической системы • Мезоатомы (нет электронов) μ⁻ мюон (заряд как у электрона, масса в 207 раз больше) может замещать электрон. Радиус орбиты мюона в 207 раз меньше, чем радиус орбиты электрона в атоме водорода. В тяжелых атомах орбита μ ⁻ мюона может находится даже внутри ядра. • Протоний – протон + анти-протон
Нижняя граница периодической системы • Мезоатомы (нет электронов) μ⁻ мюон (заряд как у электрона, масса в 207 раз больше) может замещать электрон. Радиус орбиты мюона в 207 раз меньше, чем радиус орбиты электрона в атоме водорода. В тяжелых атомах орбита μ ⁻ мюона может находится даже внутри ядра. • Протоний – протон + анти-протон
 Распространенность элементов во Вселенной На 1000 атомов: 928 H 71 He 1 остальные
Распространенность элементов во Вселенной На 1000 атомов: 928 H 71 He 1 остальные
 Распространенность элементов в земной коре • Кларк элемента – среднее содержание в земной коре (в %) • О - 47 % • Si – 29, 5 % • Al – 8, 05 % • Fe – 4, 65 % • Ca – 2, 96 % • Na – 2, 50 % • K – 2, 50 % • Mg – 1, 65 %
Распространенность элементов в земной коре • Кларк элемента – среднее содержание в земной коре (в %) • О - 47 % • Si – 29, 5 % • Al – 8, 05 % • Fe – 4, 65 % • Ca – 2, 96 % • Na – 2, 50 % • K – 2, 50 % • Mg – 1, 65 %
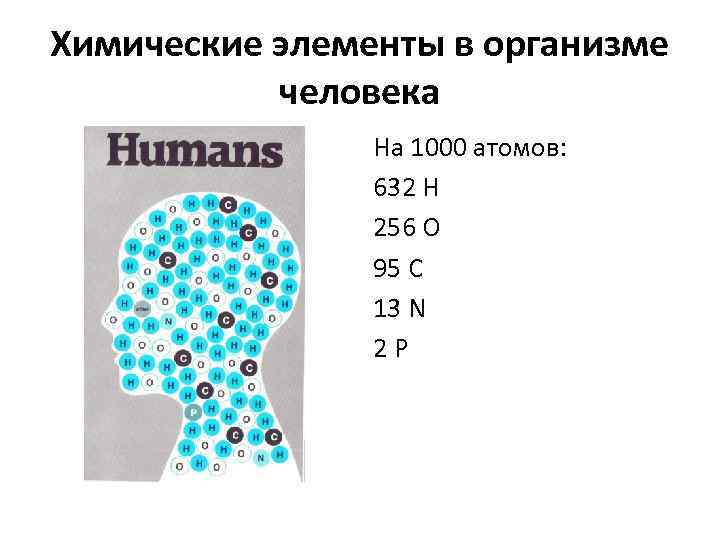 Химические элементы в организме человека На 1000 атомов: 632 H 256 O 95 C 13 N 2 P
Химические элементы в организме человека На 1000 атомов: 632 H 256 O 95 C 13 N 2 P


