Периодический закон.ppt
- Количество слайдов: 12
 Периодический закон Менделеев Д. И. 1869 г.
Периодический закон Менделеев Д. И. 1869 г.
 1. Формулировка Д. И. Менделеева: Свойства простых тел, а также свойства и формы соединений элементов находятся в периодической зависимости от величины атомных весов элементов. 2. Современная формулировка: Свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда ядер их атомов.
1. Формулировка Д. И. Менделеева: Свойства простых тел, а также свойства и формы соединений элементов находятся в периодической зависимости от величины атомных весов элементов. 2. Современная формулировка: Свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины заряда ядер их атомов.
 Структура ПС Графическое отражение периодического закона – периодическая система (ПС). Известно 500 форм ПС, чаще используется 3: 1. Короткая, 8 –клеточная 2. Полудлинная, 18 -клеточная 3. Длиннопериодная, 32 -клеточная
Структура ПС Графическое отражение периодического закона – периодическая система (ПС). Известно 500 форм ПС, чаще используется 3: 1. Короткая, 8 –клеточная 2. Полудлинная, 18 -клеточная 3. Длиннопериодная, 32 -клеточная
 Принципиальный подход к построениюэлементы располагаются в порядке возрастания заряда ядер их атомов. Физическая основа структурыопределенная последовательность формирования электронных конфигураций атомов по мере роста порядкового номера элемента Z.
Принципиальный подход к построениюэлементы располагаются в порядке возрастания заряда ядер их атомов. Физическая основа структурыопределенная последовательность формирования электронных конфигураций атомов по мере роста порядкового номера элемента Z.
 В зависимости от того, какой энергетический подуровень заполняется последним различают 4 типа элементов: 1. s-элементы 3. d-элементы 2. p-элементы 4. f-элементы Элементы со сходной электронной конфигурацией внешних энергетических уровней обладают сходными химическими свойствами.
В зависимости от того, какой энергетический подуровень заполняется последним различают 4 типа элементов: 1. s-элементы 3. d-элементы 2. p-элементы 4. f-элементы Элементы со сходной электронной конфигурацией внешних энергетических уровней обладают сходными химическими свойствами.
 Период- ряд элементов у которых электронная конфигурация внешнего энергетического уровня изменяется от ns 1 до ns 2 np 6 (для первого периода 1 s 1 и 1 s 2). Начинает период щелочной металл, заканчивает инертный газ. Идет изменение свойств от металлических к типично неметаллическим.
Период- ряд элементов у которых электронная конфигурация внешнего энергетического уровня изменяется от ns 1 до ns 2 np 6 (для первого периода 1 s 1 и 1 s 2). Начинает период щелочной металл, заканчивает инертный газ. Идет изменение свойств от металлических к типично неметаллическим.
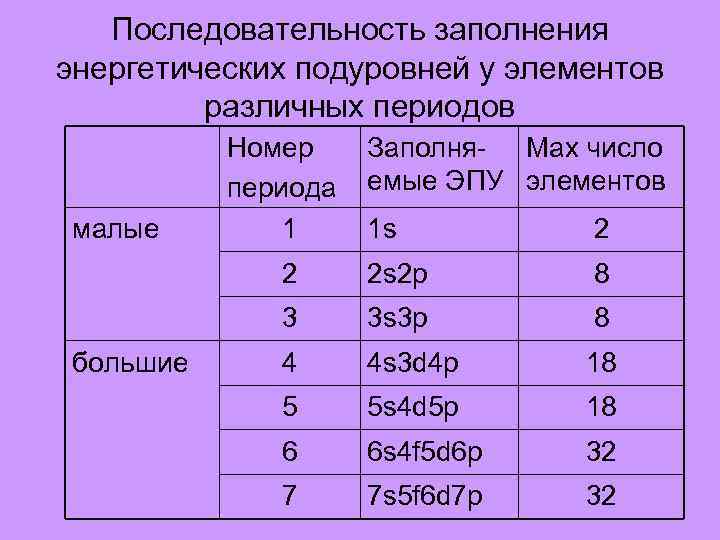 Последовательность заполнения энергетических подуровней у элементов различных периодов малые Номер периода 1 Заполня- Max число емые ЭПУ элементов 2 2 2 s 2 p 8 3 большие 1 s 3 s 3 p 8 4 4 s 3 d 4 p 18 5 5 s 4 d 5 p 18 6 6 s 4 f 5 d 6 p 32 7 7 s 5 f 6 d 7 p 32
Последовательность заполнения энергетических подуровней у элементов различных периодов малые Номер периода 1 Заполня- Max число емые ЭПУ элементов 2 2 2 s 2 p 8 3 большие 1 s 3 s 3 p 8 4 4 s 3 d 4 p 18 5 5 s 4 d 5 p 18 6 6 s 4 f 5 d 6 p 32 7 7 s 5 f 6 d 7 p 32
 В группах (вертикальные колонки) объединены элементы, имеющие сходное электронное строение. В коротком варианте таблицы 8 групп, каждая состоит из главной(А) и побочной (В) подгрупп. В главных идет заполнение s- и р-подуровней внешних энергетических уровней. В побочных заполняются внутренние (n-1)d – и (n-2) f–подуровней при наличии на внешнем уровне 1 -2 электронов.
В группах (вертикальные колонки) объединены элементы, имеющие сходное электронное строение. В коротком варианте таблицы 8 групп, каждая состоит из главной(А) и побочной (В) подгрупп. В главных идет заполнение s- и р-подуровней внешних энергетических уровней. В побочных заполняются внутренние (n-1)d – и (n-2) f–подуровней при наличии на внешнем уровне 1 -2 электронов.
 Элементы главной и побочной подгрупп различаются по химическим свойствам, объединяет их номер группы. Его физический смысл – указывает число электронов, которое, как правило, может участвовать в образовании химической связи. С 1985 г. Международный союз теоретической и прикладной химии (IUPAC)рекомендует использовать полудлинный вариант ПС со сквозной нумерацией вертикальных колонок (от 1 до 18 ).
Элементы главной и побочной подгрупп различаются по химическим свойствам, объединяет их номер группы. Его физический смысл – указывает число электронов, которое, как правило, может участвовать в образовании химической связи. С 1985 г. Международный союз теоретической и прикладной химии (IUPAC)рекомендует использовать полудлинный вариант ПС со сквозной нумерацией вертикальных колонок (от 1 до 18 ).
 Периодичность свойств ХЭ Атомный радиус (АР) Ковалентный – половина межъядерного расстояния в молекулах; Металлический- половина расстояния между центрами двух соседних атомов в кристаллической решетке. 1. В периодах по мере роста заряда АР уменьшаются 2. В группах – увеличиваются (в А – больше, чем в В).
Периодичность свойств ХЭ Атомный радиус (АР) Ковалентный – половина межъядерного расстояния в молекулах; Металлический- половина расстояния между центрами двух соседних атомов в кристаллической решетке. 1. В периодах по мере роста заряда АР уменьшаются 2. В группах – увеличиваются (в А – больше, чем в В).
 Потенциал ионизации (Еион) и сродство к электрону (Еср) Потенциал(энергия) ионизации минимальная энергия, необходимая для отрыва наименее связанного электрона от невозбужденного атома. Сродство к электрону – минимальная энергия, необходимая для присоединения электрона к нейтральному атому.
Потенциал ионизации (Еион) и сродство к электрону (Еср) Потенциал(энергия) ионизации минимальная энергия, необходимая для отрыва наименее связанного электрона от невозбужденного атома. Сродство к электрону – минимальная энергия, необходимая для присоединения электрона к нейтральному атому.
 Электроотрицательность Полусумма Еион и Еср; =0, 5 (Еион+ Еср) Введена условная относительная шкала (Полинг), самый э/о элемент – фтор (4, 1), наименее э/о элемент – франций (0, 86). 1. В периоде слева направо растут , Еион и Еср. 2. В группе сверху вниз падает , Еион и Еср.
Электроотрицательность Полусумма Еион и Еср; =0, 5 (Еион+ Еср) Введена условная относительная шкала (Полинг), самый э/о элемент – фтор (4, 1), наименее э/о элемент – франций (0, 86). 1. В периоде слева направо растут , Еион и Еср. 2. В группе сверху вниз падает , Еион и Еср.


