2 Виды аналогий.ppt
- Количество слайдов: 27
 Периодический закон как основа химической систематики Виды аналогий
Периодический закон как основа химической систематики Виды аналогий
![Групповая, типовая, слоевая аналогии. Электронная аналогия и кайносимметрия N [He] 2 s 22 p Групповая, типовая, слоевая аналогии. Электронная аналогия и кайносимметрия N [He] 2 s 22 p](https://present5.com/presentation/14884915_68581561/image-2.jpg) Групповая, типовая, слоевая аналогии. Электронная аналогия и кайносимметрия N [He] 2 s 22 p 3 P [Ne] 3 s 23 p 3 V [Ar] 4 s 23 d 3 Nb [Kr] 5 s 14 d 4 Sb [Kr] 4 d 105 s 25 p 3 Ta [Xe] 6 s 25 d 3 2 As [Ar] 3 d 104 s 24 p 3 Bi [Xe] 5 d 106 s 26 p 3
Групповая, типовая, слоевая аналогии. Электронная аналогия и кайносимметрия N [He] 2 s 22 p 3 P [Ne] 3 s 23 p 3 V [Ar] 4 s 23 d 3 Nb [Kr] 5 s 14 d 4 Sb [Kr] 4 d 105 s 25 p 3 Ta [Xe] 6 s 25 d 3 2 As [Ar] 3 d 104 s 24 p 3 Bi [Xe] 5 d 106 s 26 p 3
 Типические элементы II и III периодов s p N 2 P 3 3 d
Типические элементы II и III периодов s p N 2 P 3 3 d
 Переходные элементы. Контракционная аналогия. Вторичная периодичность Атомные орбитальные радиусы элементов 4
Переходные элементы. Контракционная аналогия. Вторичная периодичность Атомные орбитальные радиусы элементов 4
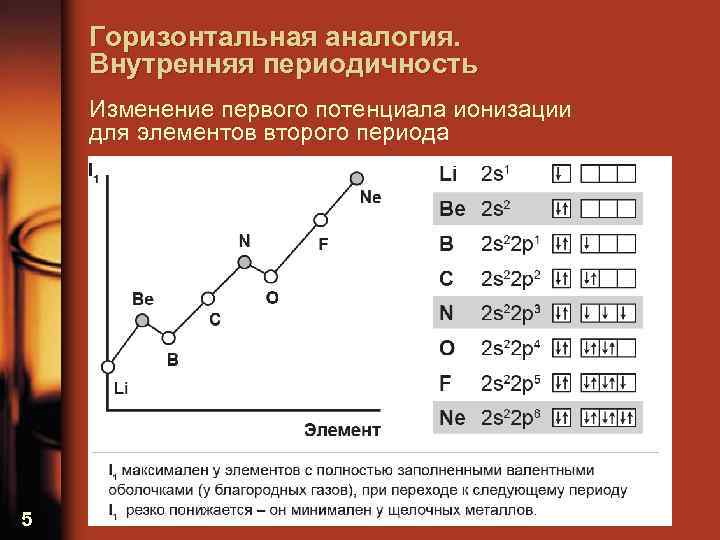 Горизонтальная аналогия. Внутренняя периодичность Изменение первого потенциала ионизации для элементов второго периода 5
Горизонтальная аналогия. Внутренняя периодичность Изменение первого потенциала ионизации для элементов второго периода 5
 Горизонтальная аналогия. Внутренняя периодичность Зависимость металлических радиусов элементов от их порядкового номера 6
Горизонтальная аналогия. Внутренняя периодичность Зависимость металлических радиусов элементов от их порядкового номера 6
 Горизонтальная аналогия • Аналогия в триадах VIIIB-группы Fe — Co — Ni Ru — Ph — Pd Os — Ir — Pt • Аналогия элементов 2 -ой семерки лантаноидов (Tb — Lu) Ho — Er — Tm • Аналогия элементов 2 -ой семерки актинидов (кюриды) • Аналогия p-элементов больших периодов (Ge — As, Pb — Bi) 7
Горизонтальная аналогия • Аналогия в триадах VIIIB-группы Fe — Co — Ni Ru — Ph — Pd Os — Ir — Pt • Аналогия элементов 2 -ой семерки лантаноидов (Tb — Lu) Ho — Er — Tm • Аналогия элементов 2 -ой семерки актинидов (кюриды) • Аналогия p-элементов больших периодов (Ge — As, Pb — Bi) 7
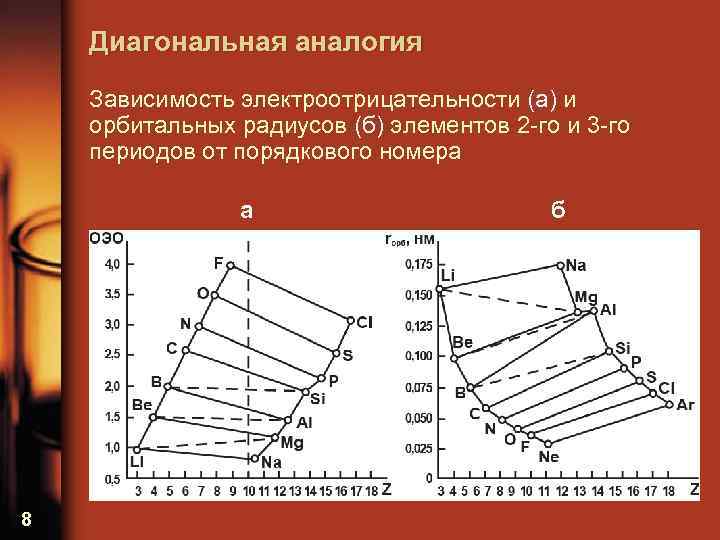 Диагональная аналогия Зависимость электроотрицательности (а) и орбитальных радиусов (б) элементов 2 -го и 3 -го периодов от порядкового номера а 8 б
Диагональная аналогия Зависимость электроотрицательности (а) и орбитальных радиусов (б) элементов 2 -го и 3 -го периодов от порядкового номера а 8 б
 Диагональная аналогия В широком смысле – сходство общего химического характера элементов Li Be Mg 2 Li + ½ O 2 = Li 2 O Mg + ½O 2 = Mg. O 3 Li + ½N 2 = Li 3 N 3 Mg + N 2 = Mg 3 N 2 Гидроксиды Li и Mg – плохо растворимы в H 2 O 9 B Al [Be(OH)4]2– [Al(OH)4]– [Al(OH)6 ]3– Гидриды не солеобразны Be. H 2 – полимер Al. H 3 – димер Si B 2 H 6, Si. H 4 B 2 O 3, Si. O 2 Кислотный характер оксидов и гидроксидов. Стеклообразование оксидов, образование полимерных структур
Диагональная аналогия В широком смысле – сходство общего химического характера элементов Li Be Mg 2 Li + ½ O 2 = Li 2 O Mg + ½O 2 = Mg. O 3 Li + ½N 2 = Li 3 N 3 Mg + N 2 = Mg 3 N 2 Гидроксиды Li и Mg – плохо растворимы в H 2 O 9 B Al [Be(OH)4]2– [Al(OH)4]– [Al(OH)6 ]3– Гидриды не солеобразны Be. H 2 – полимер Al. H 3 – димер Si B 2 H 6, Si. H 4 B 2 O 3, Si. O 2 Кислотный характер оксидов и гидроксидов. Стеклообразование оксидов, образование полимерных структур
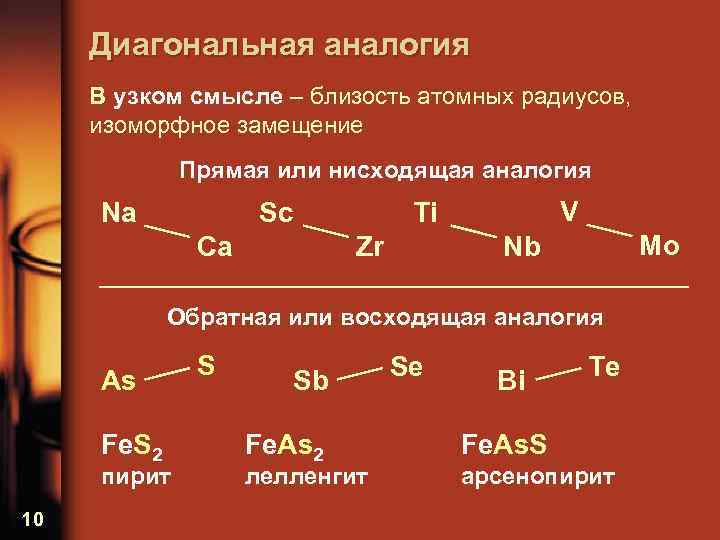 Диагональная аналогия В узком смысле – близость атомных радиусов, изоморфное замещение Прямая или нисходящая аналогия Na Sc Ca V Ti Zr Mo Nb Обратная или восходящая аналогия As Fe. S 2 пирит 10 S Sb Fe. As 2 лелленгит Se Bi Te Fe. As. S арсенопирит
Диагональная аналогия В узком смысле – близость атомных радиусов, изоморфное замещение Прямая или нисходящая аналогия Na Sc Ca V Ti Zr Mo Nb Обратная или восходящая аналогия As Fe. S 2 пирит 10 S Sb Fe. As 2 лелленгит Se Bi Te Fe. As. S арсенопирит
 Простые вещества
Простые вещества
 Особенности • Отсутствуют эффекты, связанные с разностью электроотрицательностей, реализуются либо металлические, либо неполярные ковалентные связи • Отсутствует понятие «состав» элемент простое вещество кислород – O 2 углерод – С алмаз – С, графит – С железо – Fe • Граница Цинтля проходит между IIIA и IVA группами, отделяет элементы с дефицитом электронов от элементов с их достаточным количеством. • Кристаллохимическое правило Юм-Розери 8 – N 12
Особенности • Отсутствуют эффекты, связанные с разностью электроотрицательностей, реализуются либо металлические, либо неполярные ковалентные связи • Отсутствует понятие «состав» элемент простое вещество кислород – O 2 углерод – С алмаз – С, графит – С железо – Fe • Граница Цинтля проходит между IIIA и IVA группами, отделяет элементы с дефицитом электронов от элементов с их достаточным количеством. • Кристаллохимическое правило Юм-Розери 8 – N 12
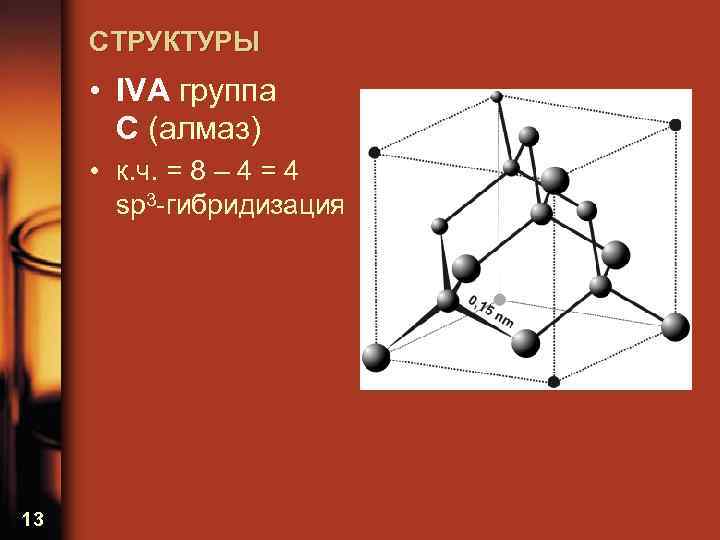 СТРУКТУРЫ • IVА группа С (алмаз) • к. ч. = 8 – 4 = 4 sp 3 -гибридизация 13
СТРУКТУРЫ • IVА группа С (алмаз) • к. ч. = 8 – 4 = 4 sp 3 -гибридизация 13
 СТРУКТУРЫ • VА группа As, Sb, Bi • к. ч. = 8 – 5 = 3 sp 2 -гибридизация 14
СТРУКТУРЫ • VА группа As, Sb, Bi • к. ч. = 8 – 5 = 3 sp 2 -гибридизация 14
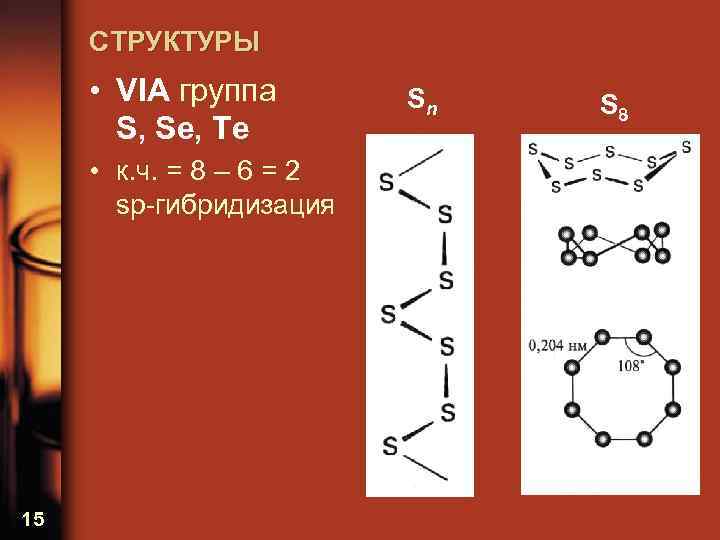 СТРУКТУРЫ • VIА группа S, Se, Te • к. ч. = 8 – 6 = 2 sp-гибридизация 15 Sn S 8
СТРУКТУРЫ • VIА группа S, Se, Te • к. ч. = 8 – 6 = 2 sp-гибридизация 15 Sn S 8
 СТРУКТУРЫ • VIIА группа Cl 2, Br 2, I 2 • к. ч. = 8 – 7 = 1 молекулярная решетка 16
СТРУКТУРЫ • VIIА группа Cl 2, Br 2, I 2 • к. ч. = 8 – 7 = 1 молекулярная решетка 16
 СТРУКТУРЫ • VIIIА группа кристаллы благородных газов • к. ч. = 8 – 8 = 0 одноатомные молекулы 17
СТРУКТУРЫ • VIIIА группа кристаллы благородных газов • к. ч. = 8 – 8 = 0 одноатомные молекулы 17
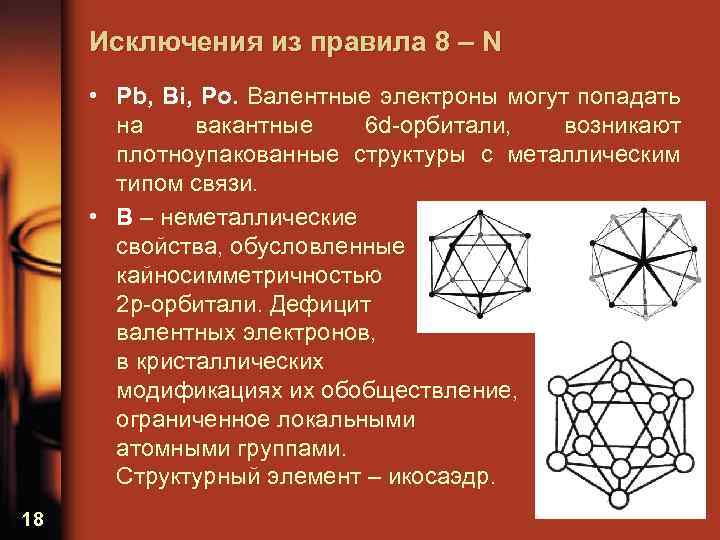 Исключения из правила 8 – N • Pb, Bi, Po. Валентные электроны могут попадать на вакантные 6 d-орбитали, возникают плотноупакованные структуры с металлическим типом связи. • B – неметаллические свойства, обусловленные кайносимметричностью 2 p-орбитали. Дефицит валентных электронов, в кристаллических модификациях их обобществление, ограниченное локальными атомными группами. Структурный элемент – икосаэдр. 18
Исключения из правила 8 – N • Pb, Bi, Po. Валентные электроны могут попадать на вакантные 6 d-орбитали, возникают плотноупакованные структуры с металлическим типом связи. • B – неметаллические свойства, обусловленные кайносимметричностью 2 p-орбитали. Дефицит валентных электронов, в кристаллических модификациях их обобществление, ограниченное локальными атомными группами. Структурный элемент – икосаэдр. 18
 • Диагональная граница между металлами и неметаллами проходит от B к At между элементами: B – Al, Si – Ge, As – Sb, Te – Po. 19 • Al, Ga, In, Sb, As – расположены вблизи диагональной границы и одними свойствами напоминают металлы, по другим – неметаллы.
• Диагональная граница между металлами и неметаллами проходит от B к At между элементами: B – Al, Si – Ge, As – Sb, Te – Po. 19 • Al, Ga, In, Sb, As – расположены вблизи диагональной границы и одними свойствами напоминают металлы, по другим – неметаллы.
 Физические свойства простых веществ
Физические свойства простых веществ
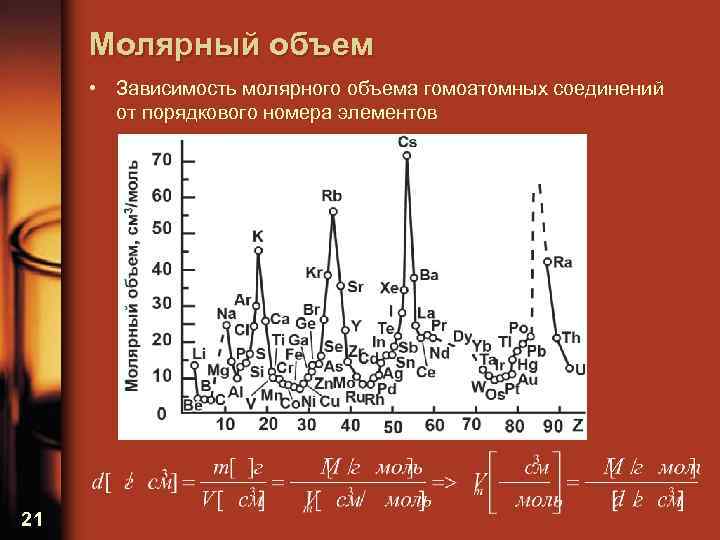 Молярный объем • Зависимость молярного объема гомоатомных соединений от порядкового номера элементов 21
Молярный объем • Зависимость молярного объема гомоатомных соединений от порядкового номера элементов 21
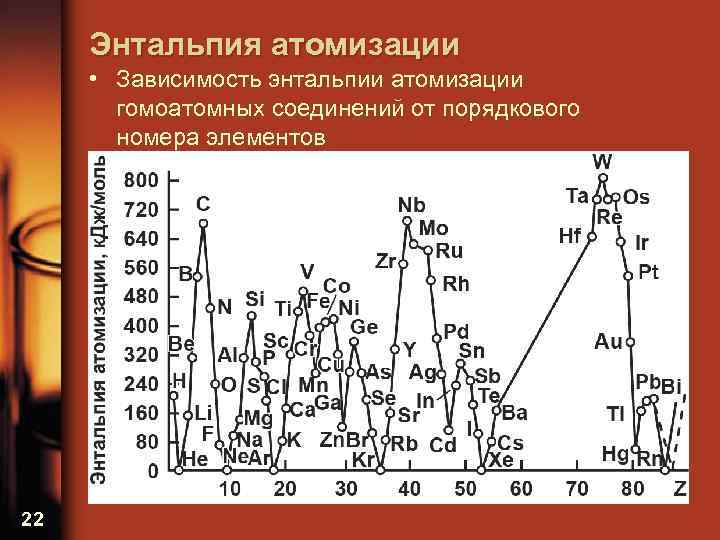 Энтальпия атомизации • Зависимость энтальпии атомизации гомоатомных соединений от порядкового номера элементов 22
Энтальпия атомизации • Зависимость энтальпии атомизации гомоатомных соединений от порядкового номера элементов 22
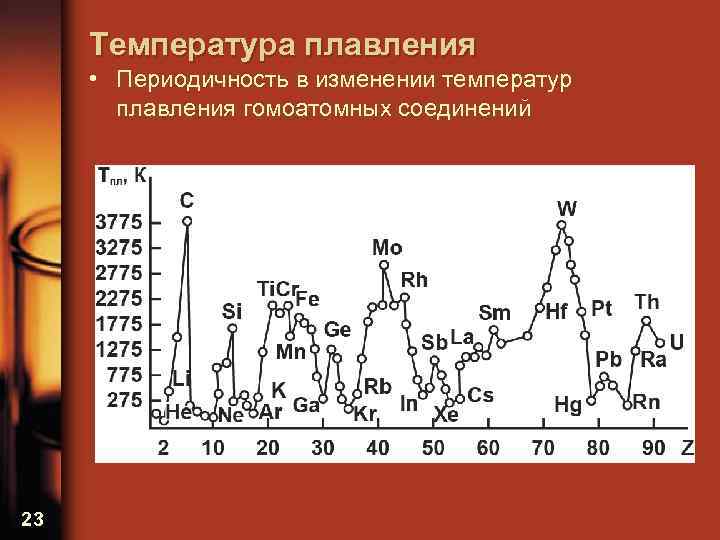 Температура плавления • Периодичность в изменении температур плавления гомоатомных соединений 23
Температура плавления • Периодичность в изменении температур плавления гомоатомных соединений 23
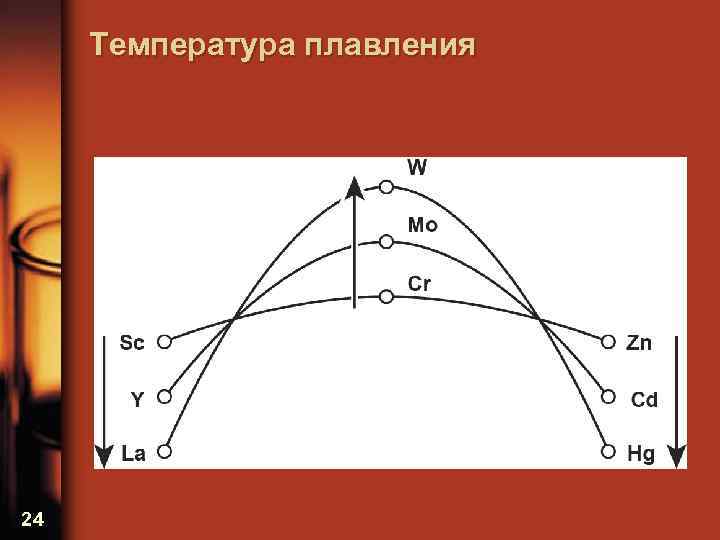 Температура плавления 24
Температура плавления 24
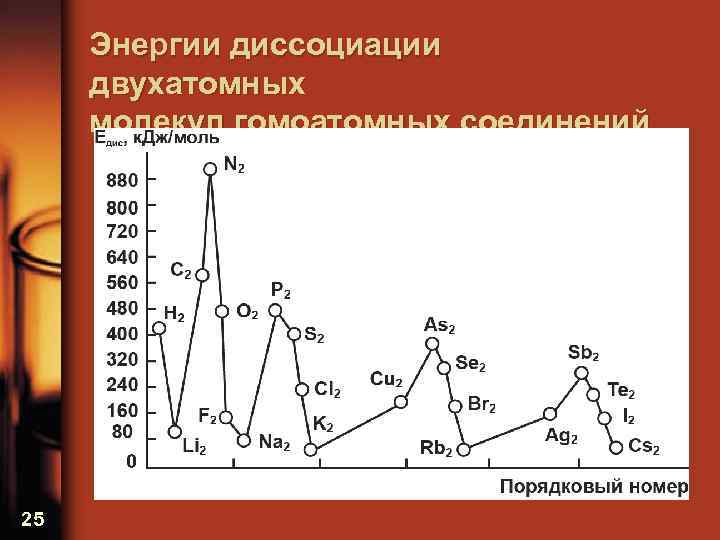 Энергии диссоциации двухатомных молекул гомоатомных соединений 25
Энергии диссоциации двухатомных молекул гомоатомных соединений 25
 Химические свойства простых веществ
Химические свойства простых веществ
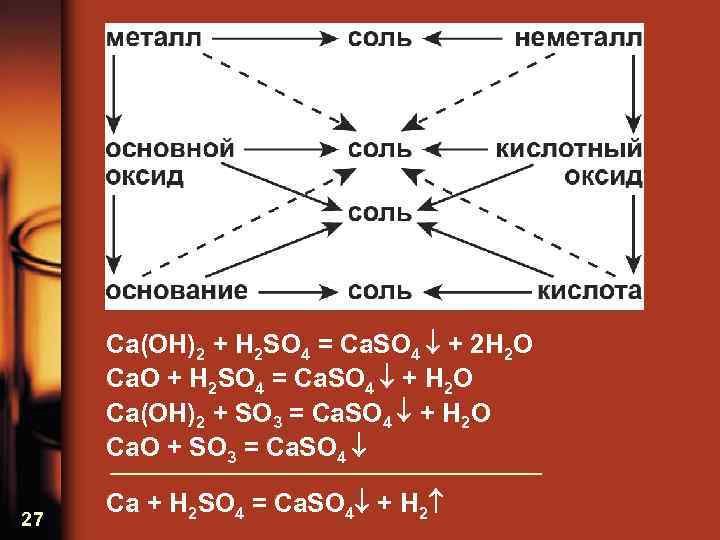 Ca(OH)2 + H 2 SO 4 = Ca. SO 4 + 2 H 2 O Ca. O + H 2 SO 4 = Ca. SO 4 + H 2 O Ca(OH)2 + SO 3 = Ca. SO 4 + H 2 O Ca. O + SO 3 = Ca. SO 4 27 Ca + H 2 SO 4 = Ca. SO 4 + H 2
Ca(OH)2 + H 2 SO 4 = Ca. SO 4 + 2 H 2 O Ca. O + H 2 SO 4 = Ca. SO 4 + H 2 O Ca(OH)2 + SO 3 = Ca. SO 4 + H 2 O Ca. O + SO 3 = Ca. SO 4 27 Ca + H 2 SO 4 = Ca. SO 4 + H 2


