 Периодический закон и Периодическая система химических элементов Д. И. Менделеева. 1
Периодический закон и Периодическая система химических элементов Д. И. Менделеева. 1
 Иоганн Вольфганг Дёберейнер Закон триад (1829 г. ) Cl – 35. 5 Br – 80 I – 125 P – 31 As – 75 Sb – 122 S – 32 Se – 79 Te – 129 Ca – 41 Sr – 88 Ba – 137 Li – 7 Na – 23 K – 39 Атомный вес среднего элемента триады примерно равен полусумме атомных весов двух крайних элементов 2
Иоганн Вольфганг Дёберейнер Закон триад (1829 г. ) Cl – 35. 5 Br – 80 I – 125 P – 31 As – 75 Sb – 122 S – 32 Se – 79 Te – 129 Ca – 41 Sr – 88 Ba – 137 Li – 7 Na – 23 K – 39 Атомный вес среднего элемента триады примерно равен полусумме атомных весов двух крайних элементов 2
 Леопольд Гмелин Таблица химически сходных элементов (1843 г. ) Три "базисных" элемента – кислород, азот и водород 3
Леопольд Гмелин Таблица химически сходных элементов (1843 г. ) Три "базисных" элемента – кислород, азот и водород 3
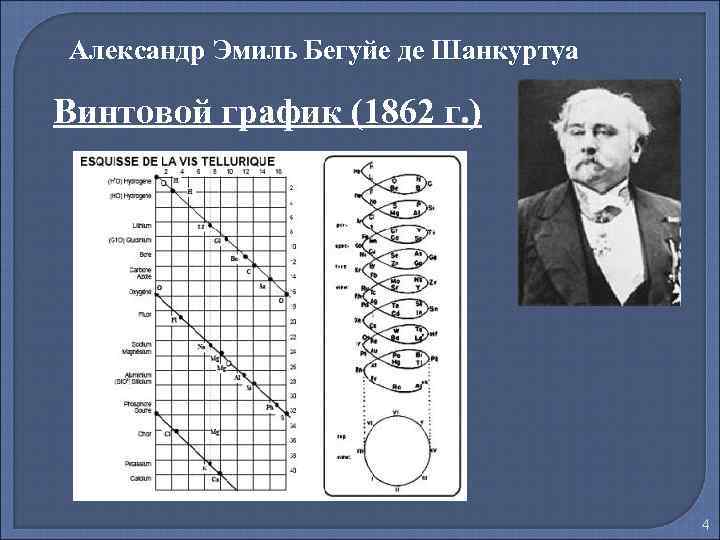 Александр Эмиль Бегуйе де Шанкуртуа Винтовой график (1862 г. ) 4
Александр Эмиль Бегуйе де Шанкуртуа Винтовой график (1862 г. ) 4
 Джон Александр Рейна Ньюлендс Закон октав (1864 г. ) В ряду элементы размещены в порядке возрастания атомных весов, свойства восьмого элемента сходны со свойствами первого. 5
Джон Александр Рейна Ньюлендс Закон октав (1864 г. ) В ряду элементы размещены в порядке возрастания атомных весов, свойства восьмого элемента сходны со свойствами первого. 5
 Юлиус Лотар Мейер Таблица Мейера (1864 г. ) Таблица состояла из девяти вертикальных столбцов, сходные элементы располагались в горизонтальных рядах; некоторые ячейки таблицы Мейер оставил незаполненными. 6
Юлиус Лотар Мейер Таблица Мейера (1864 г. ) Таблица состояла из девяти вертикальных столбцов, сходные элементы располагались в горизонтальных рядах; некоторые ячейки таблицы Мейер оставил незаполненными. 6
 Дмитрий Иванович Менделеев Таблица Менделеева (1869 г. ) 7
Дмитрий Иванович Менделеев Таблица Менделеева (1869 г. ) 7
 Формулировка Периодического закона «Свойства химических элементов, а также формы и свойства соединений элементов находятся в периодической зависимости от величины заряда ядер их атомов» . 8
Формулировка Периодического закона «Свойства химических элементов, а также формы и свойства соединений элементов находятся в периодической зависимости от величины заряда ядер их атомов» . 8
 Периодическая система и периодическая таблица Периодическая система – система классификации химических элементов, позволяющая выявлять связи между элементами, характеризующими их различие и сходство Периодический закон и основанную на нём периодическую систему можно выразить в форме таблицы. Периодическая таблица – графическое изображение периодической системы. 9
Периодическая система и периодическая таблица Периодическая система – система классификации химических элементов, позволяющая выявлять связи между элементами, характеризующими их различие и сходство Периодический закон и основанную на нём периодическую систему можно выразить в форме таблицы. Периодическая таблица – графическое изображение периодической системы. 9
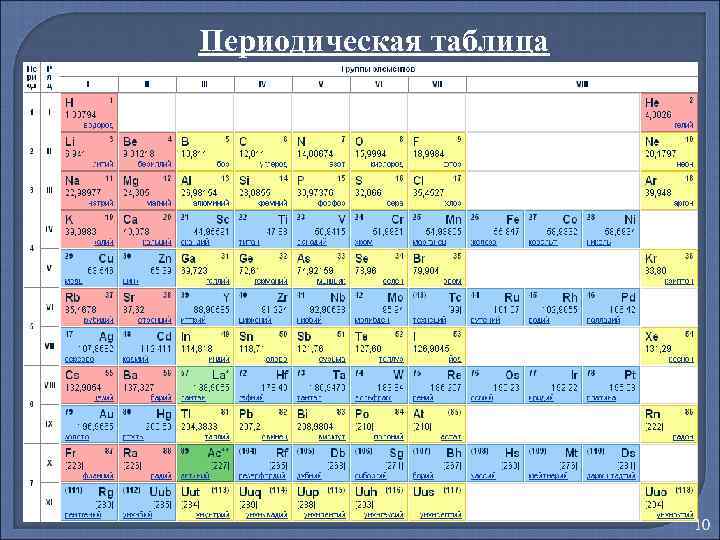 Периодическая таблица 10
Периодическая таблица 10
 11
11
 12
12
 13
13
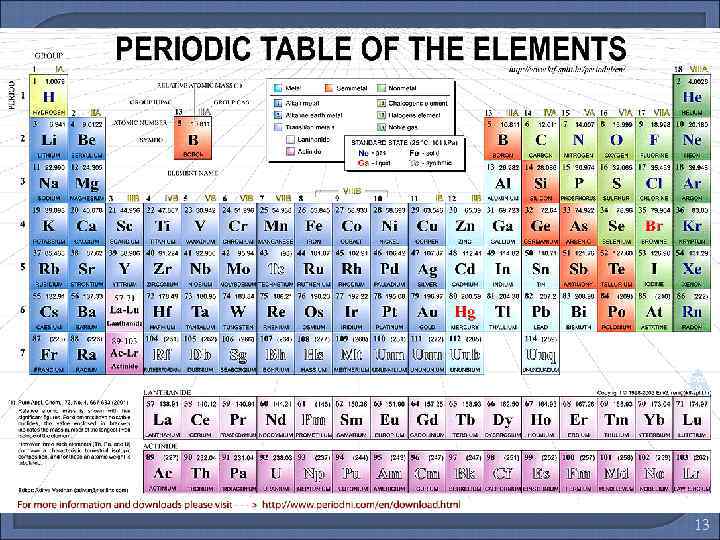
 Периодическая таблица Периоды – горизонтальные ряды элементов, расположенных в порядке возрастания их атомных масс, начинающиеся щелочным металлом и заканчивающиеся инертным газом. Группы – вертикальные столбцы элементов, расположенные в порядке возрастания их атомных масс. Главная подгруппа – подгруппа, элементами и малых, и больших периодов. образованная Побочная подгруппа – подгруппа из элементов только больших периодов. 14
Периодическая таблица Периоды – горизонтальные ряды элементов, расположенных в порядке возрастания их атомных масс, начинающиеся щелочным металлом и заканчивающиеся инертным газом. Группы – вертикальные столбцы элементов, расположенные в порядке возрастания их атомных масс. Главная подгруппа – подгруппа, элементами и малых, и больших периодов. образованная Побочная подгруппа – подгруппа из элементов только больших периодов. 14
 Химический знак (символ) 15
Химический знак (символ) 15
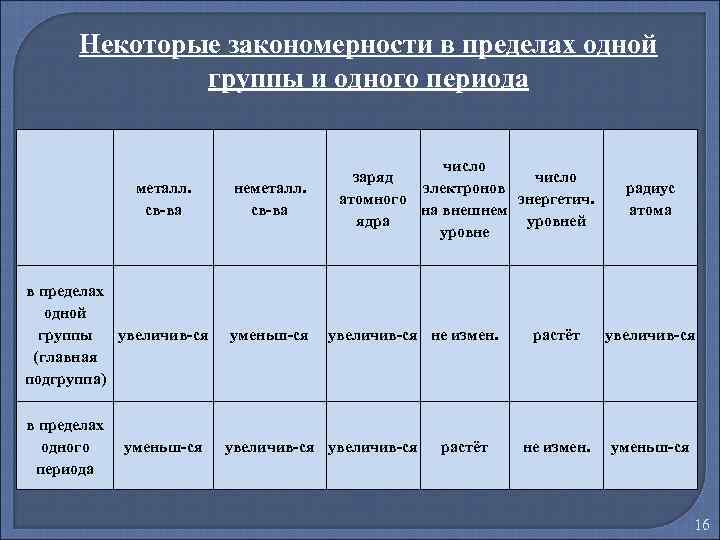 Некоторые закономерности в пределах одной группы и одного периода металл. св-ва в пределах одной группы увеличив-ся (главная подгруппа) в пределах одного периода уменьш-ся неметалл. св-ва уменьш-ся число заряд число электронов атомного энергетич. на внешнем ядра уровней уровне увеличив-ся не измен. увеличив-ся растёт радиус атома растёт увеличив-ся не измен. уменьш-ся 16
Некоторые закономерности в пределах одной группы и одного периода металл. св-ва в пределах одной группы увеличив-ся (главная подгруппа) в пределах одного периода уменьш-ся неметалл. св-ва уменьш-ся число заряд число электронов атомного энергетич. на внешнем ядра уровней уровне увеличив-ся не измен. увеличив-ся растёт радиус атома растёт увеличив-ся не измен. уменьш-ся 16
 План характеристики элемента: Ø Период: • большой или • малый. Ø Ряд: • четный или • нечетный. Ø Группа. Ø Подгруппа: • главная или • побочная. Дать характеристику элементов водород (H), магний (Mg), кислород (O) по положению в ПСХЭ. 17
План характеристики элемента: Ø Период: • большой или • малый. Ø Ряд: • четный или • нечетный. Ø Группа. Ø Подгруппа: • главная или • побочная. Дать характеристику элементов водород (H), магний (Mg), кислород (O) по положению в ПСХЭ. 17
 Характеристика элемента по положению в ПСХЭ: Водород (H): I малый период, I нечетный ряд, I группа, главная подгруппа. Магний (Mg): III малый период, III нечетный ряд, II группа, главная подгруппа. Кислород (O): II малый период, II четный ряд, VI группа, главная подгруппа. 18
Характеристика элемента по положению в ПСХЭ: Водород (H): I малый период, I нечетный ряд, I группа, главная подгруппа. Магний (Mg): III малый период, III нечетный ряд, II группа, главная подгруппа. Кислород (O): II малый период, II четный ряд, VI группа, главная подгруппа. 18