периодический закoн и cвoйcтвa элементов.ppt
- Количество слайдов: 25
 Периодический закон и периодическая система химических элементов
Периодический закон и периодическая система химических элементов
 Естественный ряд химических элементов 1 Н, 2 Не, 3 Li…… 108 Hs, 109 Mt образует систему с периодическим изменением электронной конфигурации и свойств химических элементов, а также образуемых ими простых и сложных веществ.
Естественный ряд химических элементов 1 Н, 2 Не, 3 Li…… 108 Hs, 109 Mt образует систему с периодическим изменением электронной конфигурации и свойств химических элементов, а также образуемых ими простых и сложных веществ.
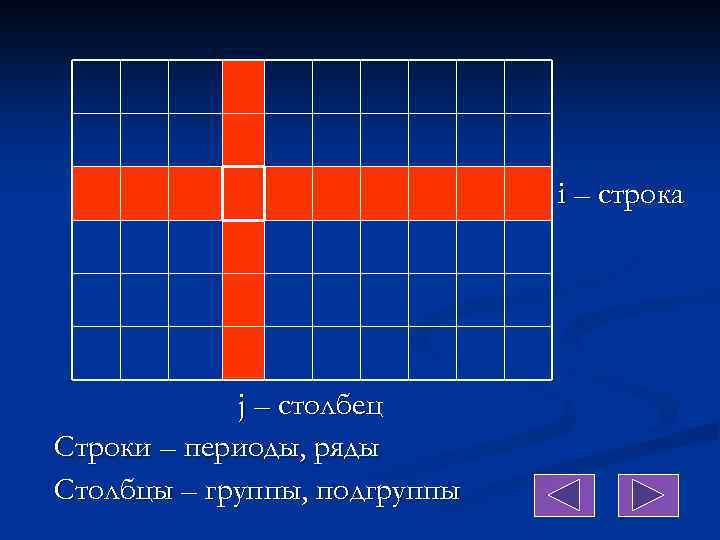 i – строка j – столбец Строки – периоды, ряды Столбцы – группы, подгруппы
i – строка j – столбец Строки – периоды, ряды Столбцы – группы, подгруппы
 Периодические элементов : nспираль де таблицы химических Шанкуртуа (1862) nоктавы Ньюлендса (1865) nтаблица Одлинга и Л. Мейера n. Таблица Менделеева (1869) n. Коротко- и длиннопериодные варианты (всего ~ 700), Киплинг IUPAC version (18 columns) USA: I A – VII A, I B – VII B, VIII – З и О Россия: I – VIII группы
Периодические элементов : nспираль де таблицы химических Шанкуртуа (1862) nоктавы Ньюлендса (1865) nтаблица Одлинга и Л. Мейера n. Таблица Менделеева (1869) n. Коротко- и длиннопериодные варианты (всего ~ 700), Киплинг IUPAC version (18 columns) USA: I A – VII A, I B – VII B, VIII – З и О Россия: I – VIII группы
 Химические и физические варианты Периодичность свойств ↔ периодичность заселения электронных уровней Элементы – полные электронные аналоги – сходство во всех СО Неполные электронные аналоги – не во всех СО О…… 2 s 22 p 4, S…… 3 s 23 p 4 O Se, Te, Po… (n-1)d 10 ns 2 np 4 S Cr, Mo, W…. (n-1)d 5 ns 1 Cr Se Mo Te W Po
Химические и физические варианты Периодичность свойств ↔ периодичность заселения электронных уровней Элементы – полные электронные аналоги – сходство во всех СО Неполные электронные аналоги – не во всех СО О…… 2 s 22 p 4, S…… 3 s 23 p 4 O Se, Te, Po… (n-1)d 10 ns 2 np 4 S Cr, Mo, W…. (n-1)d 5 ns 1 Cr Se Mo Te W Po
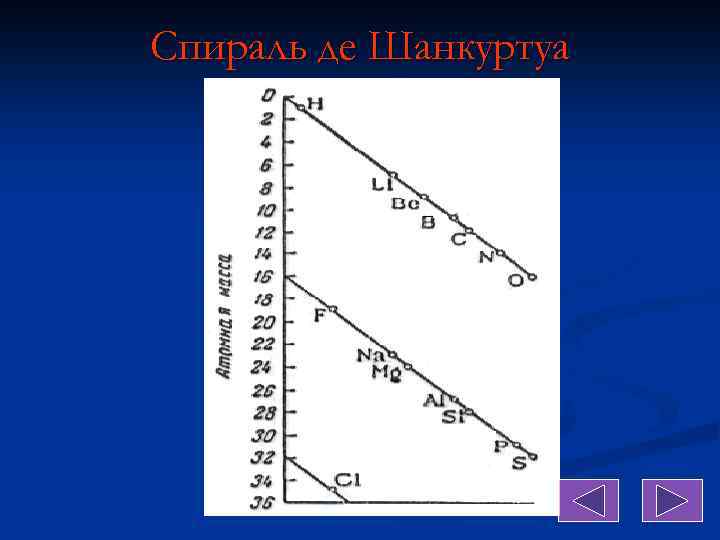 Спираль де Шанкуртуа
Спираль де Шанкуртуа
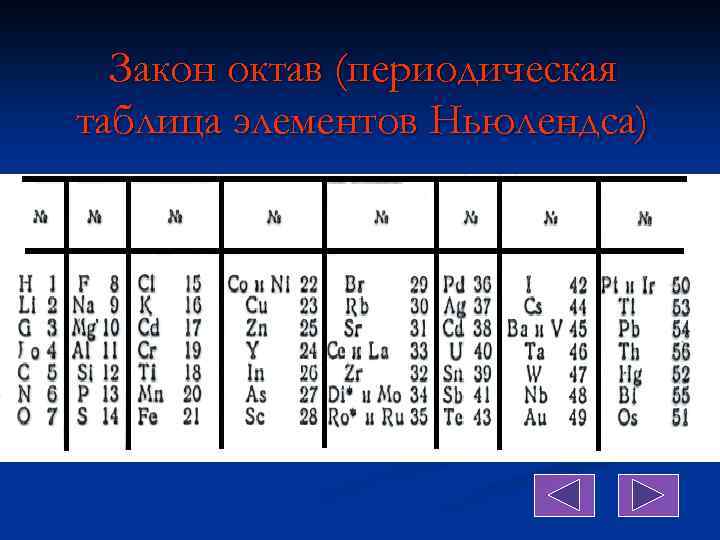 Закон октав (периодическая таблица элементов Ньюлендса)
Закон октав (периодическая таблица элементов Ньюлендса)
 Классификация элементов по Одлингу
Классификация элементов по Одлингу
 Первоначальная периодическая таблица Д. И. Менделеева
Первоначальная периодическая таблица Д. И. Менделеева
 Периодическая таблица Д. И. Менделеева (1871 г. )
Периодическая таблица Д. И. Менделеева (1871 г. )
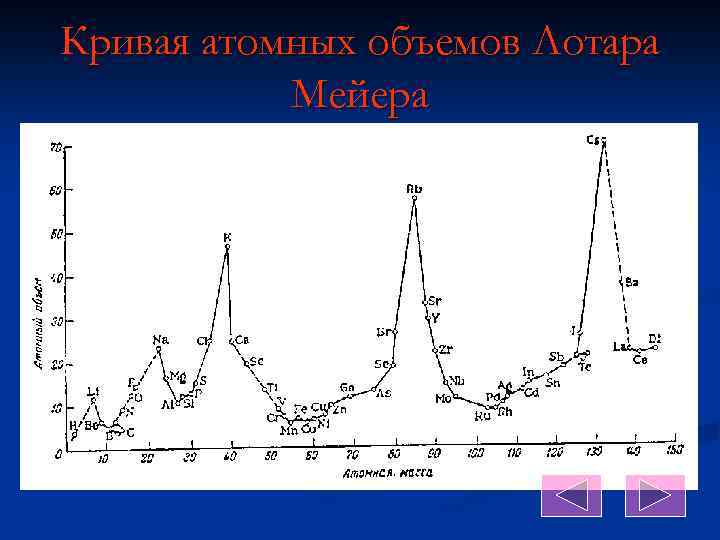 Кривая атомных объемов Лотара Мейера
Кривая атомных объемов Лотара Мейера
 Характеристики атомов. Периодические свойства элементов. n Орбитальный радиус атома ra Размер электронного облака атома с учетом взаимодействий электронов между собой и с ядром n Потенциал ионизации Ii Aгаз = А+газ + е. I 1 A+газ = А 2+газ + е. I 2 I 1< I 2< I 3< …
Характеристики атомов. Периодические свойства элементов. n Орбитальный радиус атома ra Размер электронного облака атома с учетом взаимодействий электронов между собой и с ядром n Потенциал ионизации Ii Aгаз = А+газ + е. I 1 A+газ = А 2+газ + е. I 2 I 1< I 2< I 3< …
 n n Сродство к электрону Ае Aгаз + е- = А-газ Ае Магнитный момент µэфф Электроотрицательность χ Мера смещения электронной плотности при взаимодействии с другим атомом. Шкалы: Полинга χР, Оллреда – Рохова χАR, Малликена χМ n
n n Сродство к электрону Ае Aгаз + е- = А-газ Ае Магнитный момент µэфф Электроотрицательность χ Мера смещения электронной плотности при взаимодействии с другим атомом. Шкалы: Полинга χР, Оллреда – Рохова χАR, Малликена χМ n
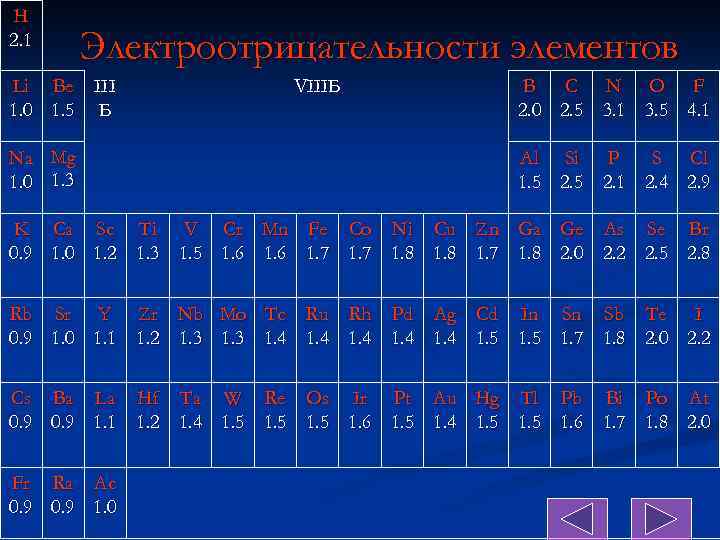 Н 2. 1 Электроотрицательности элементов Li Be III 1. 0 1. 5 Б VIIIБ B C N O F 2. 0 2. 5 3. 1 3. 5 4. 1 Na Mg 1. 0 1. 3 Al Si P S Cl 1. 5 2. 1 2. 4 2. 9 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br 0. 9 1. 0 1. 2 1. 3 1. 5 1. 6 1. 7 1. 8 2. 0 2. 2 2. 5 2. 8 Rb Sr Y Zr 0. 9 1. 0 1. 1 1. 2 Nb 1. 3 Mo 1. 3 Tc 1. 4 Ru 1. 4 Rh Pd 1. 4 Ag 1. 4 Cd In Sn Sb Te I 1. 5 1. 7 1. 8 2. 0 2. 2 Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At 0. 9 1. 1 1. 2 1. 4 1. 5 1. 6 1. 5 1. 4 1. 5 1. 6 1. 7 1. 8 2. 0 Fr Ra Ac 0. 9 1. 0
Н 2. 1 Электроотрицательности элементов Li Be III 1. 0 1. 5 Б VIIIБ B C N O F 2. 0 2. 5 3. 1 3. 5 4. 1 Na Mg 1. 0 1. 3 Al Si P S Cl 1. 5 2. 1 2. 4 2. 9 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br 0. 9 1. 0 1. 2 1. 3 1. 5 1. 6 1. 7 1. 8 2. 0 2. 2 2. 5 2. 8 Rb Sr Y Zr 0. 9 1. 0 1. 1 1. 2 Nb 1. 3 Mo 1. 3 Tc 1. 4 Ru 1. 4 Rh Pd 1. 4 Ag 1. 4 Cd In Sn Sb Te I 1. 5 1. 7 1. 8 2. 0 2. 2 Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At 0. 9 1. 1 1. 2 1. 4 1. 5 1. 6 1. 5 1. 4 1. 5 1. 6 1. 7 1. 8 2. 0 Fr Ra Ac 0. 9 1. 0
 Шкала электроотрицательностей по Полингу
Шкала электроотрицательностей по Полингу
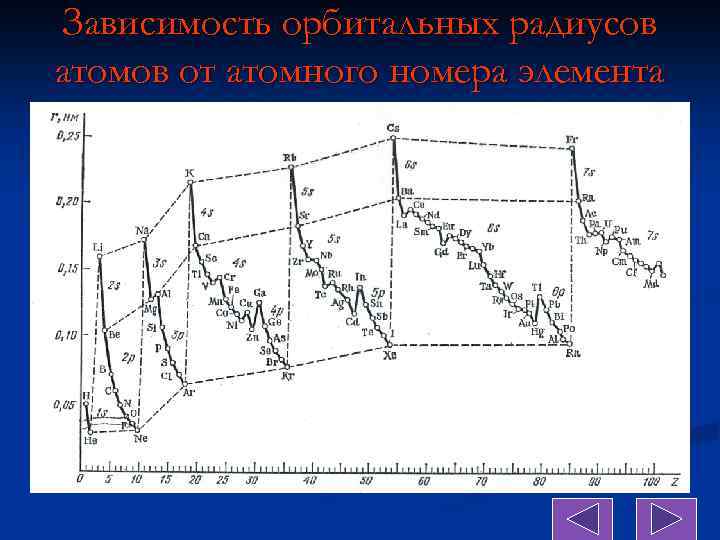 Зависимость орбитальных радиусов атомов от атомного номера элемента
Зависимость орбитальных радиусов атомов от атомного номера элемента
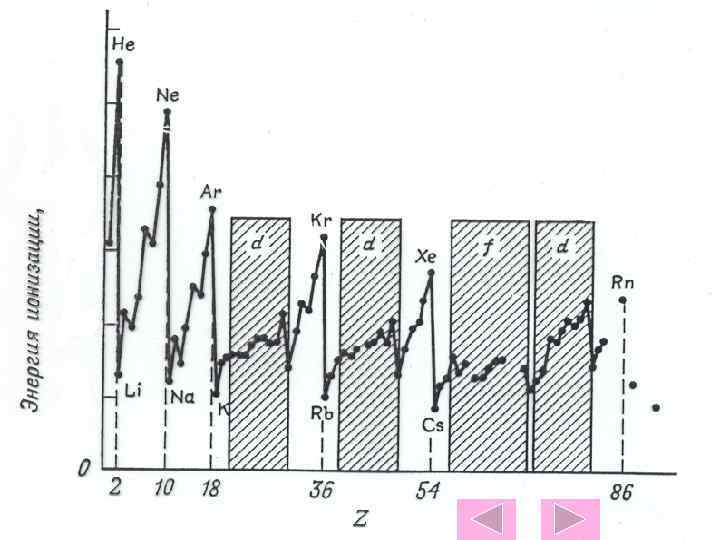
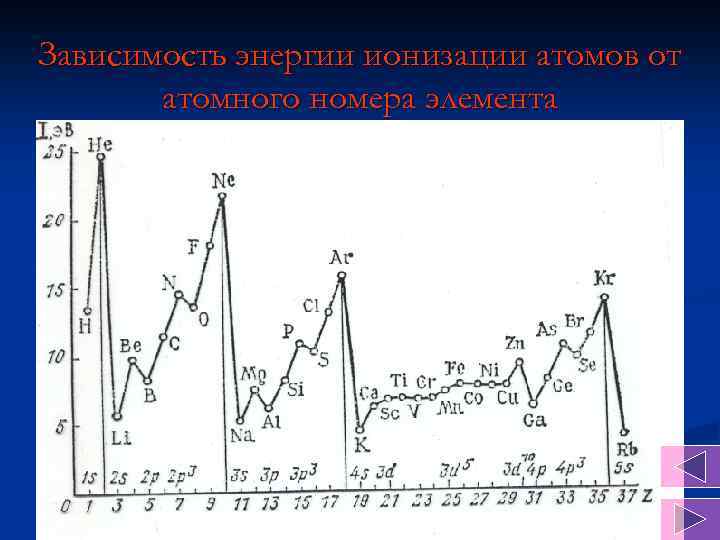 Зависимость энергии ионизации атомов от атомного номера элемента
Зависимость энергии ионизации атомов от атомного номера элемента
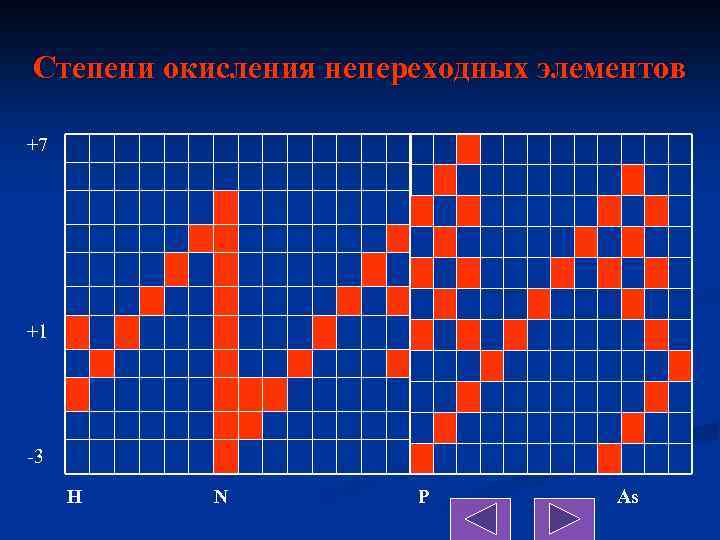 Степени окисления непереходных элементов +7 +1 -3 H N P As
Степени окисления непереходных элементов +7 +1 -3 H N P As
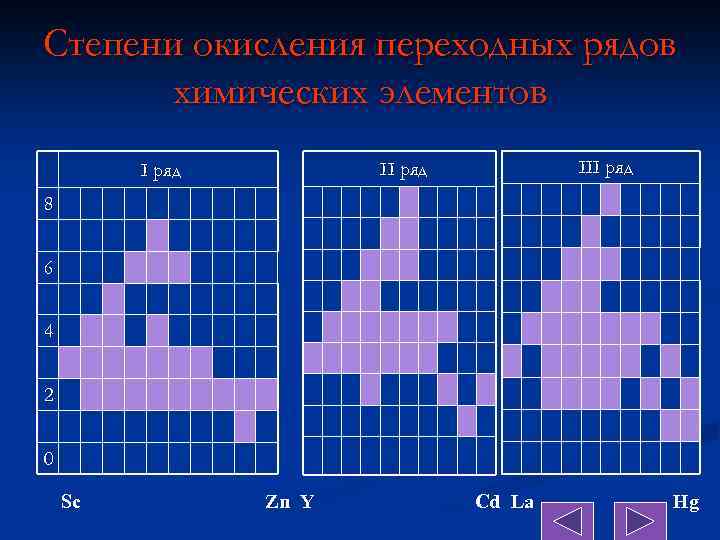 Степени окисления переходных рядов химических элементов III ряд 8 6 4 2 0 Sc Zn Y Cd La Hg
Степени окисления переходных рядов химических элементов III ряд 8 6 4 2 0 Sc Zn Y Cd La Hg
![I A: Li, Na, K, Rb, Cs, Fr 1 [ ] ns 1 щелочные I A: Li, Na, K, Rb, Cs, Fr 1 [ ] ns 1 щелочные](https://present5.com/presentation/3/22232948_85782574.pdf-img/22232948_85782574.pdf-21.jpg) I A: Li, Na, K, Rb, Cs, Fr 1 [ ] ns 1 щелочные металлы n II A: Be, Mg, Ca, Sr, Ba, Ra [ ] ns 2 щелочноземельные металлы 2 n III A: B, Al, Ga, In, Tl 3 [ ] ns 2 np 1 n IV A: C, Si, Ge, Sn, Pb 4 [ ] ns 2 np 2 n V A: N, P, As, Sb, Bi [ ] ns 2 np 3 пниктогены 5 n VI A: O, S, Se, Te, Po [ ] ns 2 np 4 халькогены 6 n
I A: Li, Na, K, Rb, Cs, Fr 1 [ ] ns 1 щелочные металлы n II A: Be, Mg, Ca, Sr, Ba, Ra [ ] ns 2 щелочноземельные металлы 2 n III A: B, Al, Ga, In, Tl 3 [ ] ns 2 np 1 n IV A: C, Si, Ge, Sn, Pb 4 [ ] ns 2 np 2 n V A: N, P, As, Sb, Bi [ ] ns 2 np 3 пниктогены 5 n VI A: O, S, Se, Te, Po [ ] ns 2 np 4 халькогены 6 n
![n VII A: F, Cl, Br, I, At [ ] ns 2 np 5 n VII A: F, Cl, Br, I, At [ ] ns 2 np 5](https://present5.com/presentation/3/22232948_85782574.pdf-img/22232948_85782574.pdf-22.jpg) n VII A: F, Cl, Br, I, At [ ] ns 2 np 5 галогены n VIII A: He, Ne, Ar, Kr, Xe, Rn 8 1 s 2; [ ] ns 2 np 6 инертные газы (благородные) 7
n VII A: F, Cl, Br, I, At [ ] ns 2 np 5 галогены n VIII A: He, Ne, Ar, Kr, Xe, Rn 8 1 s 2; [ ] ns 2 np 6 инертные газы (благородные) 7
 3 12 3 d – элементы (Sc → Zn) 4 d – элементы (Y → Cd) 5 d – элементы (La → Hg) 6 d – элементы (Ac, Th, Lr → Mt) 4 f – элементы (Ce → Lu) 5 f – элементы (Pa → No)
3 12 3 d – элементы (Sc → Zn) 4 d – элементы (Y → Cd) 5 d – элементы (La → Hg) 6 d – элементы (Ac, Th, Lr → Mt) 4 f – элементы (Ce → Lu) 5 f – элементы (Pa → No)
 Периодическая система в нечетном периоде в четном периоде Первый период → 2 электрона Второй и третий периоды → 8 электронов Четвертый и пятый периоды → 18 электронов Шестой и седьмой периоды → 32 электрона
Периодическая система в нечетном периоде в четном периоде Первый период → 2 электрона Второй и третий периоды → 8 электронов Четвертый и пятый периоды → 18 электронов Шестой и седьмой периоды → 32 электрона
 Число главных подгрупп = число s + p электронов = 8 Число переходных элементов = максимальное число d элементов = 10 21 Sc → 30 Zn 39 Y → 48 Cd 57 La и 72 Hf → 80 Hg Число лантаноидов = максимальное число f элементов = 14 Предсказать свойства 72 Hf (не РЗЭ, Zr - аналог)
Число главных подгрупп = число s + p электронов = 8 Число переходных элементов = максимальное число d элементов = 10 21 Sc → 30 Zn 39 Y → 48 Cd 57 La и 72 Hf → 80 Hg Число лантаноидов = максимальное число f элементов = 14 Предсказать свойства 72 Hf (не РЗЭ, Zr - аналог)


