Периодический закон и строение атома.ppt
- Количество слайдов: 15
 ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА
ПЕРИОДИЧЕСКИЙ ЗАКОН Д. И. МЕНДЕЛЕЕВА
 «Периодическому закону будущее не грозит разрушением, а только надстройка и развитие обещаются» (Д. И. Менделеев).
«Периодическому закону будущее не грозит разрушением, а только надстройка и развитие обещаются» (Д. И. Менделеев).
 В 1875 г. Поль Эмиль Лекок де Буабодран (Франция) открыл галлий, предсказанный Менделеевым (экаалюминий – подобный алюминию). n В 1879 г. Ларс Фредерик Нильсон (Швеция) открыл скандий, предсказанный Менделеевым (экабор – подобный бору). n В 1886 г. Клеменс Александр Винклер (Германия) открыл германий, предсказанный Менделеевым (экасилиций – подобный кремнию). n
В 1875 г. Поль Эмиль Лекок де Буабодран (Франция) открыл галлий, предсказанный Менделеевым (экаалюминий – подобный алюминию). n В 1879 г. Ларс Фредерик Нильсон (Швеция) открыл скандий, предсказанный Менделеевым (экабор – подобный бору). n В 1886 г. Клеменс Александр Винклер (Германия) открыл германий, предсказанный Менделеевым (экасилиций – подобный кремнию). n
 n n 1. 1869 г. Свойства простых тел, а также формы и свойства простых и сложных соединений элементов находятся в периодической зависимости от относительных атомных масс элементов. (ОТ ЗАРЯДА ЯДРА АТОМА) 2. На основе периодического закона изображена его графическая структура – периодическая система химических элементов (ПСХЭ). В настоящее время известно более 800 вариантов ПСХЭ. Это различные формы передачи периодического закона. Наиболее распространена короткая форма.
n n 1. 1869 г. Свойства простых тел, а также формы и свойства простых и сложных соединений элементов находятся в периодической зависимости от относительных атомных масс элементов. (ОТ ЗАРЯДА ЯДРА АТОМА) 2. На основе периодического закона изображена его графическая структура – периодическая система химических элементов (ПСХЭ). В настоящее время известно более 800 вариантов ПСХЭ. Это различные формы передачи периодического закона. Наиболее распространена короткая форма.
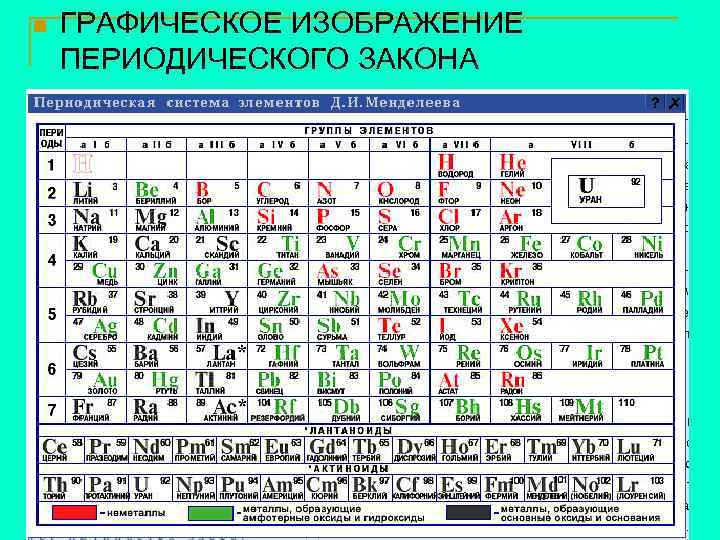 n ГРАФИЧЕСКОЕ ИЗОБРАЖЕНИЕ ПЕРИОДИЧЕСКОГО ЗАКОНА
n ГРАФИЧЕСКОЕ ИЗОБРАЖЕНИЕ ПЕРИОДИЧЕСКОГО ЗАКОНА
 n Каждый элемент, изображенный соответствующим символом, имеет порядковый номер и занимает определенную клетку – это занумерованное место элемента в ПСХЭ, его координаты. n n Горизонтальный ряд элементов, расположенных по возрастанию порядковых номеров, в котором закономерно изменяются свойства при переходе от металлов к неметаллам, называется периодом. В ПСХЭ семь периодов, из них 1 -й, 2 -й, 3 -й – малые, 4 -й, 5 -й, 6 -й, 7 -й – большие.
n Каждый элемент, изображенный соответствующим символом, имеет порядковый номер и занимает определенную клетку – это занумерованное место элемента в ПСХЭ, его координаты. n n Горизонтальный ряд элементов, расположенных по возрастанию порядковых номеров, в котором закономерно изменяются свойства при переходе от металлов к неметаллам, называется периодом. В ПСХЭ семь периодов, из них 1 -й, 2 -й, 3 -й – малые, 4 -й, 5 -й, 6 -й, 7 -й – большие.
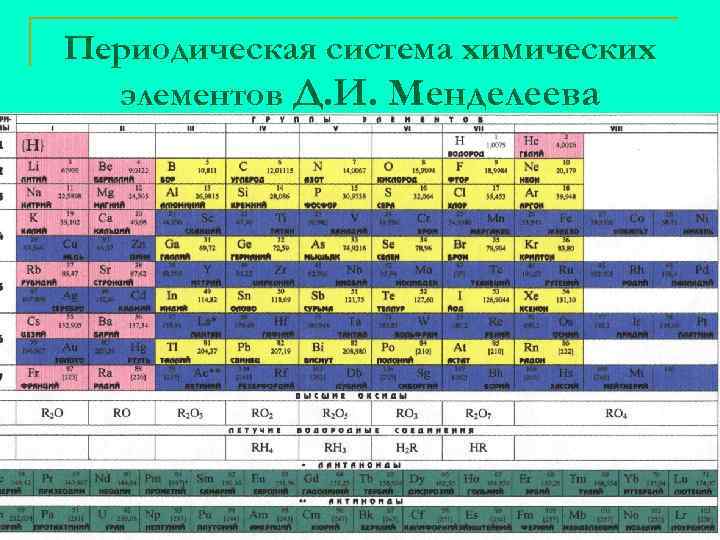 Периодическая система химических элементов Д. И. Менделеева 7
Периодическая система химических элементов Д. И. Менделеева 7
 Структура периодической системы: n n n Формулировка периодического закона «Свойства простых тел находятся в периодической зависимости от заряда атомного ядра» . Принцип построения периодической системы «Периодическая система построена в порядке возрастания атомной массы» . Принцип периодичности «Периодичность - это повторение химических свойств через каждые семь элементов на восьмой Понятие периода n n n А) В периодической системе всего 7 периодов, 1, 2, 3 малые и 4, 5, 6, 7 большие. Б) Период начинается с щелочного металла и заканчивается инертном газом. В) Период – это расположение элементов по горизонтали. Г) Период показывает количество энергетических уровней. Д) Количество элементов на периодах: 1 -2, 2 -8, 3 -8, 4 -18, 518, 6 -32, 7 -28. В настоящее время в периодической системе находится 116 элементов. 8
Структура периодической системы: n n n Формулировка периодического закона «Свойства простых тел находятся в периодической зависимости от заряда атомного ядра» . Принцип построения периодической системы «Периодическая система построена в порядке возрастания атомной массы» . Принцип периодичности «Периодичность - это повторение химических свойств через каждые семь элементов на восьмой Понятие периода n n n А) В периодической системе всего 7 периодов, 1, 2, 3 малые и 4, 5, 6, 7 большие. Б) Период начинается с щелочного металла и заканчивается инертном газом. В) Период – это расположение элементов по горизонтали. Г) Период показывает количество энергетических уровней. Д) Количество элементов на периодах: 1 -2, 2 -8, 3 -8, 4 -18, 518, 6 -32, 7 -28. В настоящее время в периодической системе находится 116 элементов. 8
 Структура периодической системы: Понятие группы n n n А) Группа – это расположение элементов по вертикали. Б) В периодической системе всего 8 групп, каждая группа подразделяется на: главную, в которой происходит заполнение электронов на внешнем энергетическом уровне и побочную в которой происходит заполнение предвнешнего энергетического уровня. В) Группа показывает количество электронов на внешнем энергетическом уровне только в главных подгруппах. Г) Группа показывает наивысшую валентность по кислороду. Понятие порядкового номера n n n Порядковый номер показывает: А) Заряд ядра атома. Б) Количество электронов, которые движутся вокруг атома и несут отрицательный заряд. В) Количество протонов. Г) Количество нейтронов, которые вычисляются между разностью молярной масс и порядковым номером. 9
Структура периодической системы: Понятие группы n n n А) Группа – это расположение элементов по вертикали. Б) В периодической системе всего 8 групп, каждая группа подразделяется на: главную, в которой происходит заполнение электронов на внешнем энергетическом уровне и побочную в которой происходит заполнение предвнешнего энергетического уровня. В) Группа показывает количество электронов на внешнем энергетическом уровне только в главных подгруппах. Г) Группа показывает наивысшую валентность по кислороду. Понятие порядкового номера n n n Порядковый номер показывает: А) Заряд ядра атома. Б) Количество электронов, которые движутся вокруг атома и несут отрицательный заряд. В) Количество протонов. Г) Количество нейтронов, которые вычисляются между разностью молярной масс и порядковым номером. 9
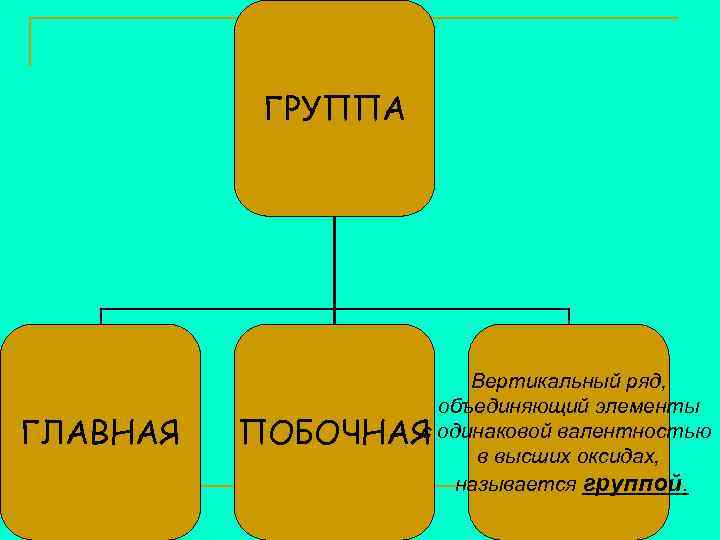 ГРУППА ГЛАВНАЯ Вертикальный ряд, объединяющий элементы с ПОБОЧНАЯ одинаковой валентностью в высших оксидах, называется группой.
ГРУППА ГЛАВНАЯ Вертикальный ряд, объединяющий элементы с ПОБОЧНАЯ одинаковой валентностью в высших оксидах, называется группой.
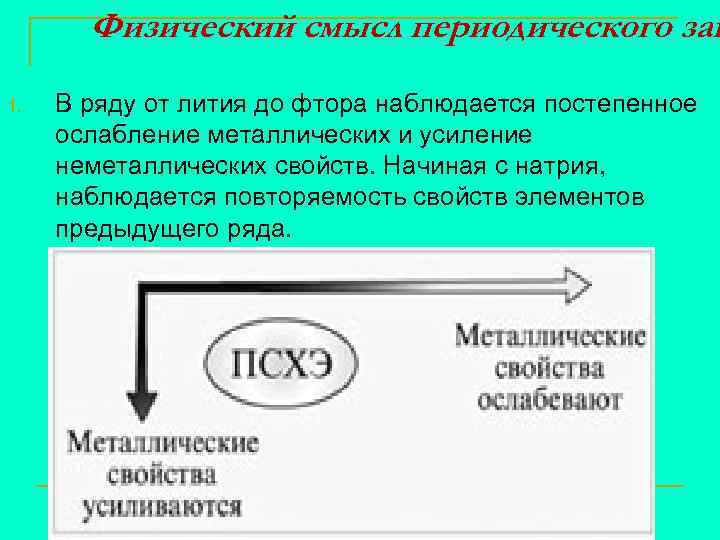 Физический смысл периодического зак 1. В ряду от лития до фтора наблюдается постепенное ослабление металлических и усиление неметаллических свойств. Начиная с натрия, наблюдается повторяемость свойств элементов предыдущего ряда.
Физический смысл периодического зак 1. В ряду от лития до фтора наблюдается постепенное ослабление металлических и усиление неметаллических свойств. Начиная с натрия, наблюдается повторяемость свойств элементов предыдущего ряда.
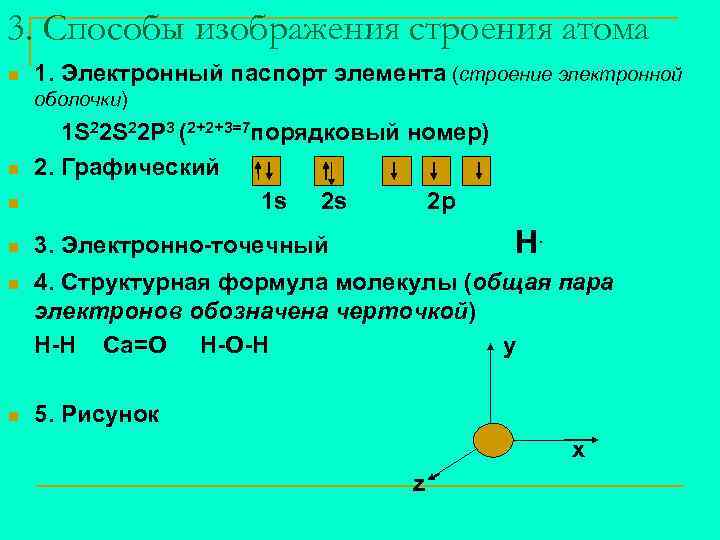 3. Способы изображения строения атома n 1. Электронный паспорт элемента (строение электронной оболочки) n 1 S 22 P 3 (2+2+3=7 порядковый номер) 2. Графический 1 s 2 s 2 p n 3. Электронно-точечный n 4. Структурная формула молекулы (общая пара электронов обозначена черточкой) Н-Н Са=О Н-О-Н y n 5. Рисунок n Н. x z
3. Способы изображения строения атома n 1. Электронный паспорт элемента (строение электронной оболочки) n 1 S 22 P 3 (2+2+3=7 порядковый номер) 2. Графический 1 s 2 s 2 p n 3. Электронно-точечный n 4. Структурная формула молекулы (общая пара электронов обозначена черточкой) Н-Н Са=О Н-О-Н y n 5. Рисунок n Н. x z
 4. Характеристика по положению в ПСХЭ 5. Радиоактивность n Ослабление неметаллических св-в в пятерках элементов N Si P S As n n Kr Усиление металлических св-в в пятерках элементов n K n n Mg Ca Sc Sr n Альфа-распад. n 226 Ra n Se Cl Br I 88 = 4 He + 2 222 Rn 86 Zn Al Ga In Ge
4. Характеристика по положению в ПСХЭ 5. Радиоактивность n Ослабление неметаллических св-в в пятерках элементов N Si P S As n n Kr Усиление металлических св-в в пятерках элементов n K n n Mg Ca Sc Sr n Альфа-распад. n 226 Ra n Se Cl Br I 88 = 4 He + 2 222 Rn 86 Zn Al Ga In Ge
 6. V 111 группа. n Главная п/группа – инертные газы He Ne Ar Kr Xe Rn 2 е, 8 e, правило октета n Побочная п/группа n n триады Fe Co Ni Ru Rh Pd Os Ir Pt Общее в строении – на внешнем е-уровне 2 е, заполняется предвнешний d-уровень сходство в св-вах и образованных соединениях
6. V 111 группа. n Главная п/группа – инертные газы He Ne Ar Kr Xe Rn 2 е, 8 e, правило октета n Побочная п/группа n n триады Fe Co Ni Ru Rh Pd Os Ir Pt Общее в строении – на внешнем е-уровне 2 е, заполняется предвнешний d-уровень сходство в св-вах и образованных соединениях
 Закончить фразу n n n n Положительно заряженные частицы называются……. . Масса ядра атома численно равна………. . Максимальное число s, p, d-электронов на уровне равно……. Заряд электрона равен……. Число электронов в атоме соответствует……. . Число электронных уровней в атоме соответствует……… В периоде слева направо металлические свойства…………
Закончить фразу n n n n Положительно заряженные частицы называются……. . Масса ядра атома численно равна………. . Максимальное число s, p, d-электронов на уровне равно……. Заряд электрона равен……. Число электронов в атоме соответствует……. . Число электронных уровней в атоме соответствует……… В периоде слева направо металлические свойства…………


