3. Периодическая система.ppt
- Количество слайдов: 17

Периодическая таблица Д. И. Менделеева
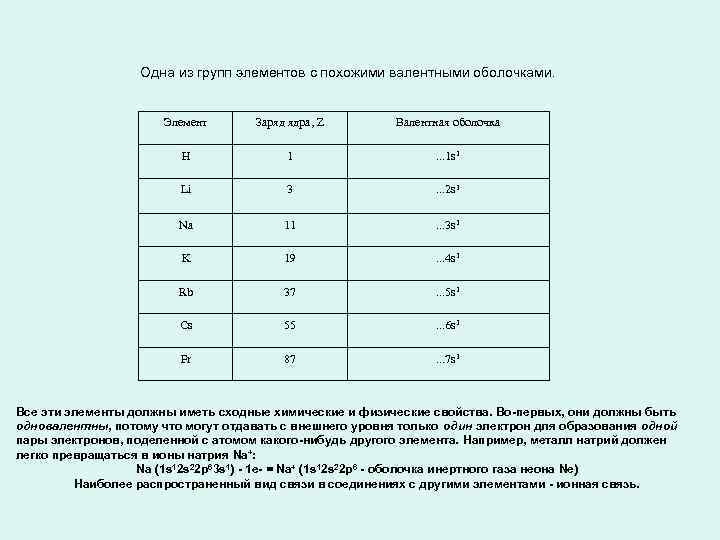
Одна из групп элементов с похожими валентными оболочками. Элемент Заряд ядра, Z Валентная оболочка H 1 . . . 1 s 1 Li 3 . . . 2 s 1 Na 11 . . . 3 s 1 K 19 . . . 4 s 1 Rb 37 . . . 5 s 1 Cs 55 . . . 6 s 1 Fr 87 . . . 7 s 1 Все эти элементы должны иметь сходные химические и физические свойства. Во-первых, они должны быть одновалентны, потому что могут отдавать с внешнего уровня только один электрон для образования одной пары электронов, поделенной с атомом какого-нибудь другого элемента. Например, металл натрий должен легко превращаться в ионы натрия Na+: Na (1 s 12 s 22 p 63 s 1) - 1 e- = Na+ (1 s 12 s 22 p 6 - оболочка инертного газа неона Ne) Наиболее распространенный вид связи в соединениях с другими элементами - ионная связь.
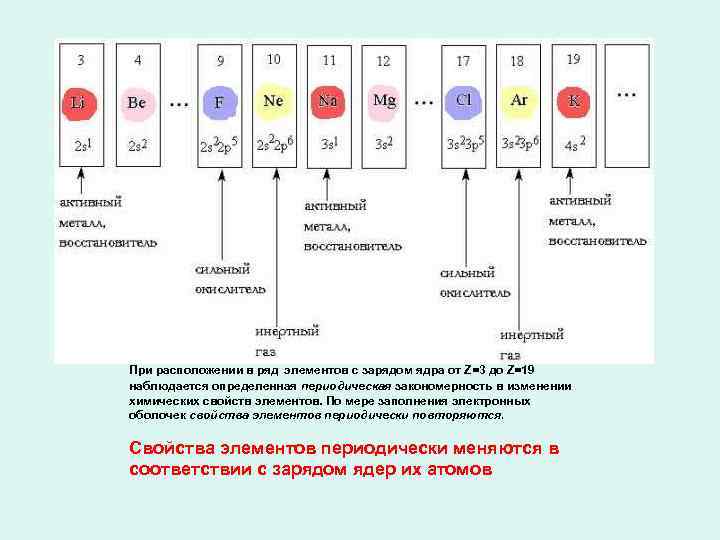
При расположении в ряд элементов с зарядом ядра от Z=3 до Z=19 наблюдается определенная периодическая закономерность в изменении химических свойств элементов. По мере заполнения электронных оболочек свойства элементов периодически повторяются. Свойства элементов периодически меняются в соответствии с зарядом ядер их атомов
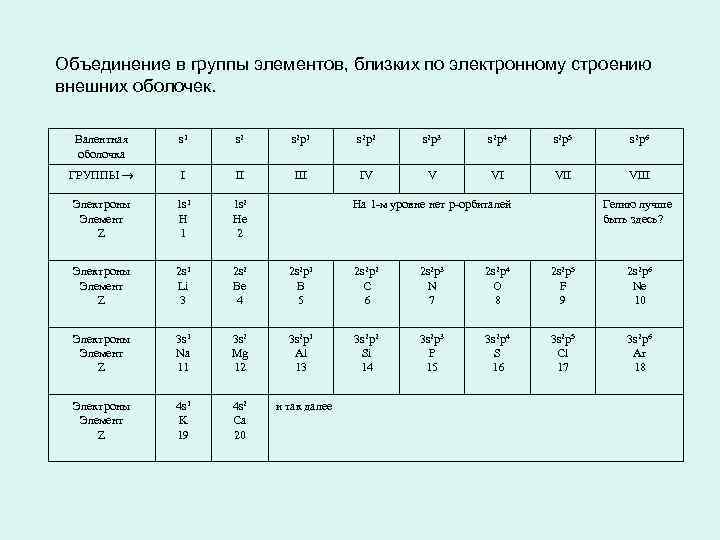
Объединение в группы элементов, близких по электронному строению внешних оболочек. Валентная оболочка s 1 s 2 p 2 s 2 p 3 s 2 p 4 s 2 p 5 s 2 p 6 ГРУППЫ ® I II IV V VI VIII Электроны Элемент Z 1 s 1 H 1 1 s 2 He 2 Электроны Элемент Z 2 s 1 Li 3 2 s 2 Be 4 2 s 2 p 1 B 5 2 s 2 p 2 C 6 2 s 2 p 3 N 7 2 s 2 p 4 O 8 2 s 2 p 5 F 9 2 s 2 p 6 Ne 10 Электроны Элемент Z 3 s 1 Na 11 3 s 2 Mg 12 3 s 2 p 1 Al 13 3 s 2 p 2 Si 14 3 s 2 p 3 P 15 3 s 2 p 4 S 16 3 s 2 p 5 Cl 17 3 s 2 p 6 Ar 18 Электроны Элемент Z 4 s 1 K 19 4 s 2 Ca 20 и так далее На 1 -м уровне нет p-орбиталей Гелию лучше быть здесь?
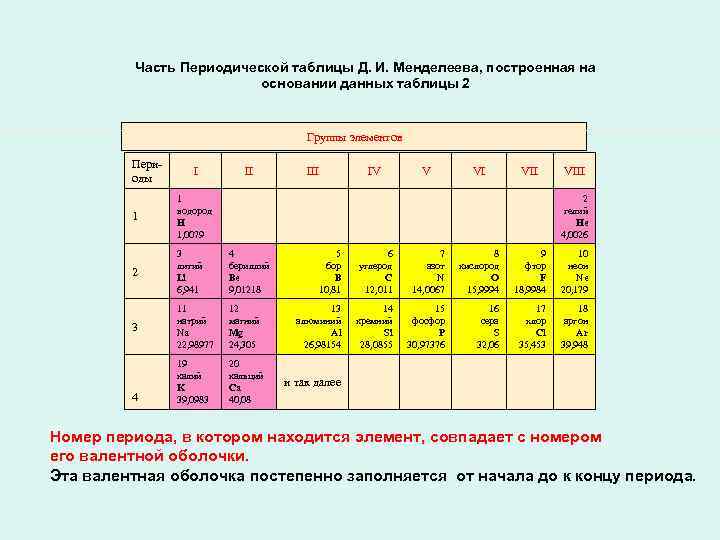
Часть Периодической таблицы Д. И. Менделеева, построенная на основании данных таблицы 2 Группы элементов Периоды I II 1 2 4 бериллий Be 9, 01218 3 11 натрий Na 22, 98977 12 магний Mg 24, 305 19 калий K 39, 0983 20 кальций Ca 40, 08 IV V VI VII 1 водород H 1, 0079 3 литий Li 6, 941 III 4 VIII 2 гелий He 4, 0026 5 бор B 10, 81 6 углерод C 12, 011 7 азот N 14, 0067 8 кислород O 15, 9994 9 фтор F 18, 9984 10 неон Ne 20, 179 13 алюминий Al 26, 98154 14 кремний Si 28, 0855 15 фосфор P 30, 97376 16 сера S 32, 06 17 хлор Cl 35, 453 18 аргон Ar 39, 948 и так далее Номер периода, в котором находится элемент, совпадает с номером его валентной оболочки. Эта валентная оболочка постепенно заполняется от начала до к концу периода.

В левой части периодов элементы проявляют ярко выраженные восстановительные свойства. Большинство из этих элементов являются металлами (Li, Na, Mg, Ca). В правой части собраны типичные неметаллы, обладающие окислительными свойствами (O, F, Cl). В середине периодов располагаются элементы, обладающие как восстановительными так и окислительными свойствами. Эти свойства зависят от того, с какими элементами они реагируют. Если сера (S) реагирует с сильным окислителем (кислородом), то проявляет восстановительные свойства: А при взаимодействии с сильным восстановителем (например, с железом) сера играет роль окислителя: Каждый период начинается активным металлом и заканчивается инертным газом Номера групп совпадают с числом валентных электронов, которые могут участвовать в образовании химических связей.
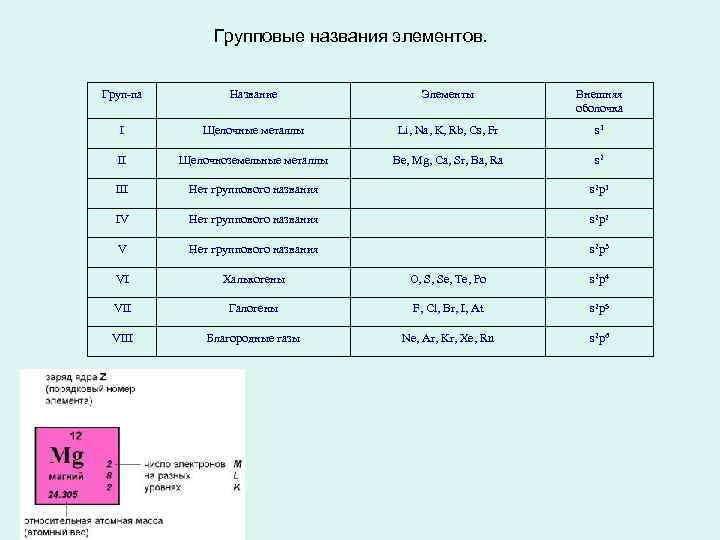
Групповые названия элементов. Груп-па Название Элементы Внешняя оболочка I Щелочные металлы Li, Na, K, Rb, Cs, Fr s 1 II Щелочноземельные металлы Be, Mg, Ca, Sr, Ba, Ra s 2 III Нет группового названия s 2 p 1 IV Нет группового названия s 2 p 2 V Нет группового названия s 2 p 3 VI Халькогены O, S, Se, Te, Po s 2 p 4 VII Галогены F, Cl, Br, I, At s 2 p 5 VIII Благородные газы Ne, Ar, Kr, Xe, Rn s 2 p 6
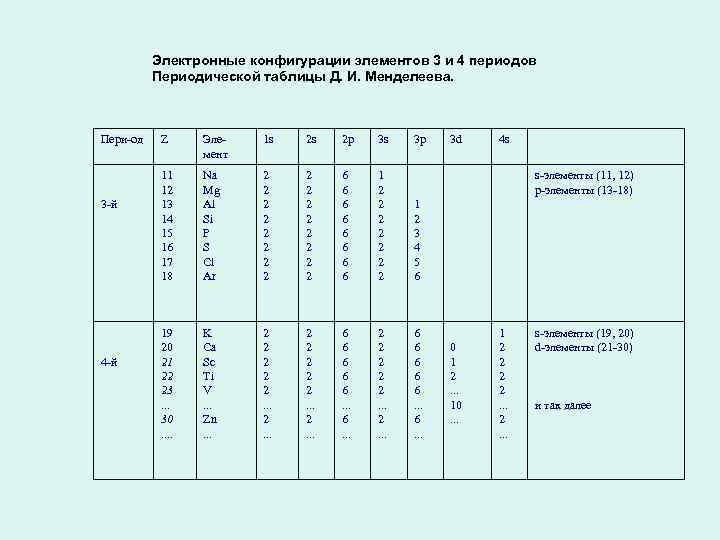
Электронные конфигурации элементов 3 и 4 периодов Периодической таблицы Д. И. Менделеева. Пери-од Z Элемент 1 s 2 s 2 p 3 s 3 p 3 d 4 s 3 -й 11 12 13 14 15 16 17 18 Na Mg Al Si P S Cl Ar 2 2 2 2 6 6 6 6 1 2 2 2 2 1 2 3 4 5 6 s-элементы (11, 12) p-элементы (13 -18) 4 -й 19 20 21 22 23. . . 30. . K Ca Sc Ti V. . . Zn. . . 2 2 2 2 2. . . 6 6 6. . . 0 1 2. . . 10. . . 1 2 2. . . s-элементы (19, 20) d-элементы (21 -30) и так далее
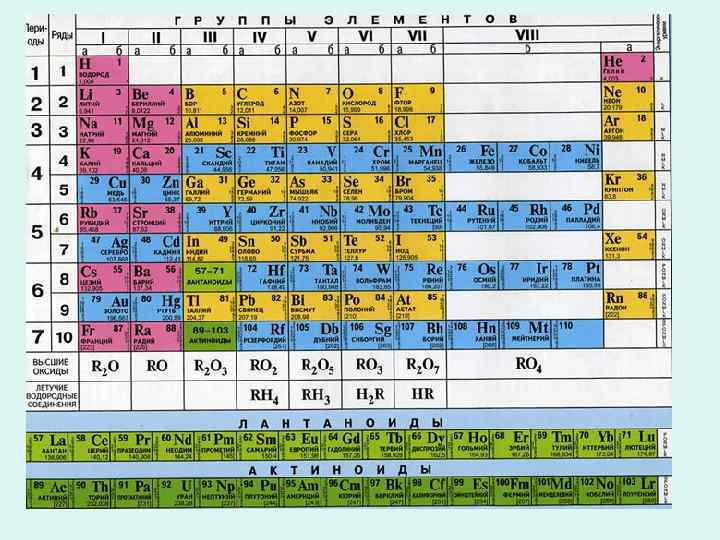

Подгруппы, в которых расположены s- и p-элементы, называют ГЛАВНЫМИ, а подгруппы с d-элементами - ПОБОЧНЫМИ ПОДГРУППАМИ. Главные и побочные подгруппы иногда обозначают соответственно буквами "А" и "Б", или "А" и "В", или "а" и "б". Элементы побочных подгрупп (d-элементы) называют ПЕРЕХОДНЫМИ элементами или переходными металлами (все dэлементы - металлы). Электронное строение и химические свойства элементов главных и побочных подгрупп могут не иметь ничего общего.
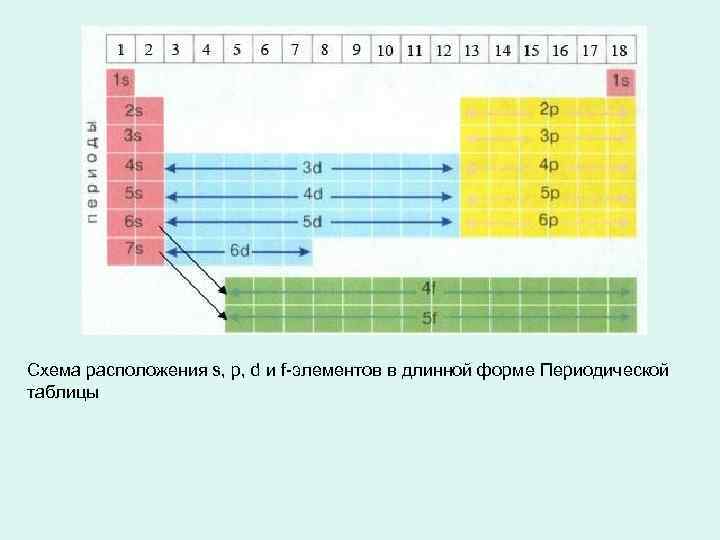
Схема расположения s, p, d и f-элементов в длинной форме Периодической таблицы




Полумета ллы (металлоиды, амфотерные металлы) — химические элементы, расположенные в периодической системе на границе между металлами и неметаллами. Для них характерно образование ковалентной кристаллической решётки и наличие металлической проводимости. В физике твёрдого тела полуметаллами называются различные вещества, занимающие по электрическим свойствам промежуточное положение между металлами и полупроводниками.

IA IIIB IVB VB VIIB VIIIB IB IIIA IVA VA VIIA VIIIA 2 1 1 He H 1. 00794 4. 00260 2 4 3 2 Be Li 6. 941 2 11 3 12 Na 24. 3050 4 K 39. 0983 40. 078 Ti 44. 95591 Ca 22 47. 8 2 37 5 38 Sr Y 85. 4678 87. 62 55 6 132. 905 (223) Mo 95. 94 74 75 W Re 137. 327 73 Ta 178. 180. 9478 49 8 104 Ra (226) 183. 84 105 98. 9063 186. 207 4 Rh 101. 0 102. 9055 7 190. 2 3 0 192. 217 33 34 Se 195. 08 4 107. 8682 Ds (281) Rg (280) 60 Nd 138. 90 140. 11 140. 90 144. 24 765 90 91 92 Th Pa U 232. 03 231. 03 238. 02 2 (276) 63 Sm 150. 36 93 94 95 96 Np (237) Pu (244) Am (243) Cm (247) 64 Gd 157. 25 204. 3833 127. 60 0 67 68 69 Ho Er Tm 158. 92 162. 50 164. 93 167. 25 168. 93 032 97 98 Bk (247) Cf 0 (251) 117 Uus (290) 71 Yb Lu 421 100 101 102 Es (252) Fm (257) Md (258) No (259) 9 (210) 173. 04 Xe 131. 293 86 70 99 At Uu h (293) Uup (288) 85 116 115 Dy 126. 90447 Po (209) 66 535 54 84 208. 9804 Uu q (289) Uut (284) Bi 114 113 83. 798 I Tb Pm (145) 4 200. 59 Kr 53 83 Pb 207. 2 36 79. 904 Te 65 62 151. 96 Tl 52 121. 760 82 Uu b (285) 61 Eu 81 112 111 Mt 0 78. 96 Sb 118. 71 Hg Au Hs (277) 114. 818 51 Sn In 74. 92160 50 49 112. 41 1 80 79 Bh (270) 69. 723 Cd 196. 966569 48 Ag 110 Pr 6 65. 409 20. 1797 39. 948 Br Ne Ar 35 As Pd Pt Ir 35. 453 Ge 72. 64 47 78 77 2 32 46 32. 065 18 Ga 63. 546 106. 42 5 Cl 31 109 59 Ac (227) 30. 97376 17 S Zn 108 Ce 89 28. 085 16 30 107 58 5 45 Os La 547 P Cu Sg (271) Db (267) (268) 5 15 18. 9984032 29 106 Rf 58. 693 76 57 58. 93319 Ru Tc 92. 90638 Ni 44 Nb 91. 2 24 43 Hf 88 Fr 1 28 Co 55. 84 54. 938045 42 72 Ba 87 7 88. 90585 51. 996 27 Fe Mn 41 Zr 56 Cs 4519 50. 9415 26 25 Cr V 40 39 Rb 67 24 23 4 Si 26. 9815386 Sc 20 10 F 15. 999 14 Al 21 19 7 14. 007 9 O N 12. 010 13 Mg 22. 9897 6928 10. 811 8 7 C B 9. 01218 6 5 174. 96 7 103 Lr (262) Rn (222) 118 Uuo (294)
3. Периодическая система.ppt