Периодическая таблица.ppt
- Количество слайдов: 20
 Период Ёмкость периода I 1 s 2 II 2 s 22 p 6 III 3 s 23 p 6 IV 4 s 2 3 d 104 p 6 V 5 s 2 4 d 105 p 6 VI 6 s 2 5 d 1(La 57)4 f 14 5 d 10 -16 p 6 VII 7 s 2 6 d 1(Ac 89) 5 f 14 6 d 2….
Период Ёмкость периода I 1 s 2 II 2 s 22 p 6 III 3 s 23 p 6 IV 4 s 2 3 d 104 p 6 V 5 s 2 4 d 105 p 6 VI 6 s 2 5 d 1(La 57)4 f 14 5 d 10 -16 p 6 VII 7 s 2 6 d 1(Ac 89) 5 f 14 6 d 2….
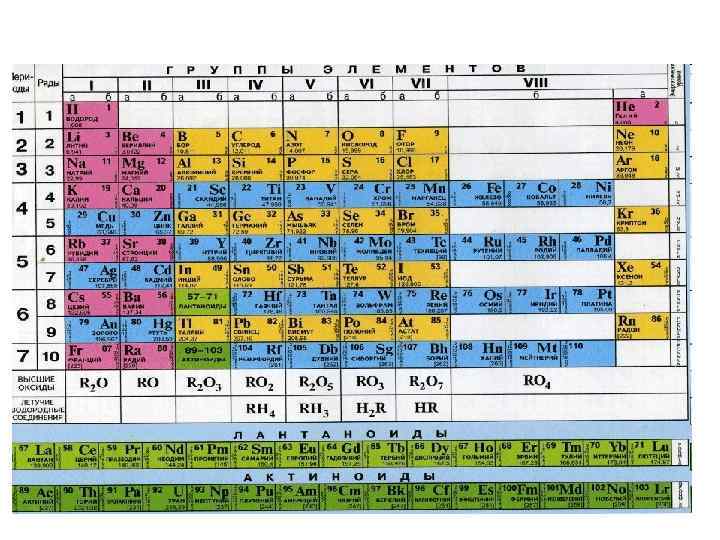
 Каждый период начинается с s-элементов, которые располагаются в IA –IIA главных подгруппах. Валентные электроны - внешние s-электроны. Все периоды заканчиваются р-элементами, которые располагаются в IIIA –VIIIA главных подгруппах. Валентными являются внешние s-и р-электроны. Их число соответствует номеру группы.
Каждый период начинается с s-элементов, которые располагаются в IA –IIA главных подгруппах. Валентные электроны - внешние s-электроны. Все периоды заканчиваются р-элементами, которые располагаются в IIIA –VIIIA главных подгруппах. Валентными являются внешние s-и р-электроны. Их число соответствует номеру группы.
 11 Na 12 Mg 1 s 22 p 63 s 1 1 s 22 p 63 s 2 13 Al 1 s 22 p 63 s 23 p 1 14 Si 1 s 22 p 63 s 23 p 2 15 P 16 S 17 Cl 18 Ar 1 s 22 p 63 s 23 p 3 1 s 22 p 63 s 23 p 4 1 s 22 p 63 s 23 p 5 1 s 22 p 63 s 23 p 6
11 Na 12 Mg 1 s 22 p 63 s 1 1 s 22 p 63 s 2 13 Al 1 s 22 p 63 s 23 p 1 14 Si 1 s 22 p 63 s 23 p 2 15 P 16 S 17 Cl 18 Ar 1 s 22 p 63 s 23 p 3 1 s 22 p 63 s 23 p 4 1 s 22 p 63 s 23 p 5 1 s 22 p 63 s 23 p 6
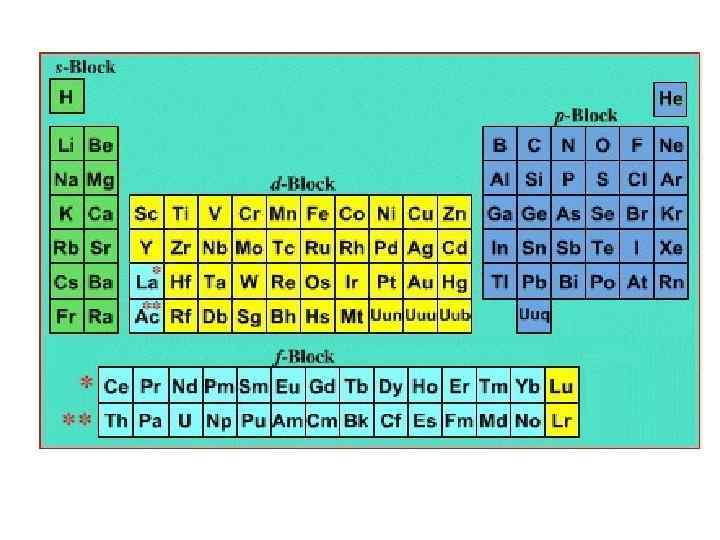
 d-элементами называются элементы, у которых последний электрон попадает на d-подуровень. Валентные электроны: внешние s- и предвнешние dэлектроны. Их число соответствует номеру группы. d-элементы расположены во всех побочных подгруппах: IIIB-VIIB, IIB. I-ый d-элемент в таблице– скандий Sc 21
d-элементами называются элементы, у которых последний электрон попадает на d-подуровень. Валентные электроны: внешние s- и предвнешние dэлектроны. Их число соответствует номеру группы. d-элементы расположены во всех побочных подгруппах: IIIB-VIIB, IIB. I-ый d-элемент в таблице– скандий Sc 21
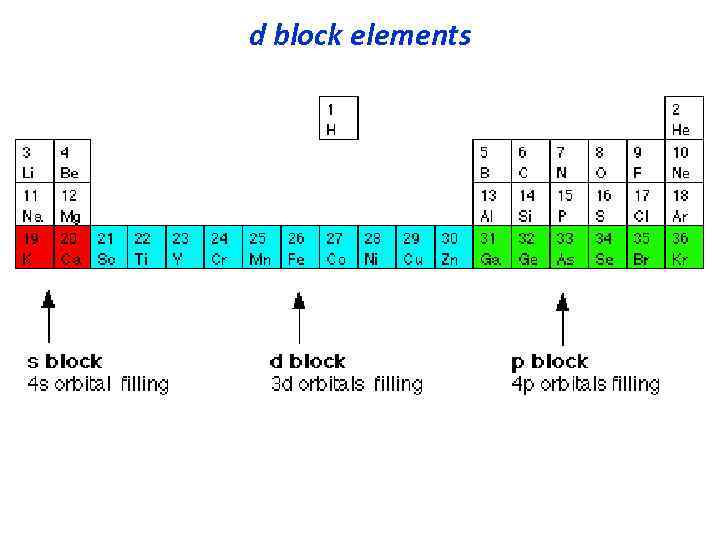 d block elements
d block elements
 19 K 20 Ca 1 s 22 p 63 s 23 p 64 s 1 1 s 22 p 63 s 23 p 64 s 2 21 Sc 1 s 22 p 63 s 23 p 64 s 23 d 1 22 Ti 1 s 22 p 63 s 23 p 64 s 23 d 2 23 V 1 s 22 p 63 s 23 p 64 s 23 d 3 24 Cr 1 s 22 p 63 s 23 p 64 s 13 d 5
19 K 20 Ca 1 s 22 p 63 s 23 p 64 s 1 1 s 22 p 63 s 23 p 64 s 2 21 Sc 1 s 22 p 63 s 23 p 64 s 23 d 1 22 Ti 1 s 22 p 63 s 23 p 64 s 23 d 2 23 V 1 s 22 p 63 s 23 p 64 s 23 d 3 24 Cr 1 s 22 p 63 s 23 p 64 s 13 d 5
 Проскок электронов у Cr 24, Mo 42, Cu 29, Ag 47 Полностью или наполовину заполненный dподуровень обладает повышенной устойчивостью. Поэтому у четвертых и девятых элементов d-декад происходит перескок электронов с 4 s на 3 d –подуровень (Cr 24, Cu 29); с 5 s на 4 d - подуровень (Mo 42, Ag 47).
Проскок электронов у Cr 24, Mo 42, Cu 29, Ag 47 Полностью или наполовину заполненный dподуровень обладает повышенной устойчивостью. Поэтому у четвертых и девятых элементов d-декад происходит перескок электронов с 4 s на 3 d –подуровень (Cr 24, Cu 29); с 5 s на 4 d - подуровень (Mo 42, Ag 47).
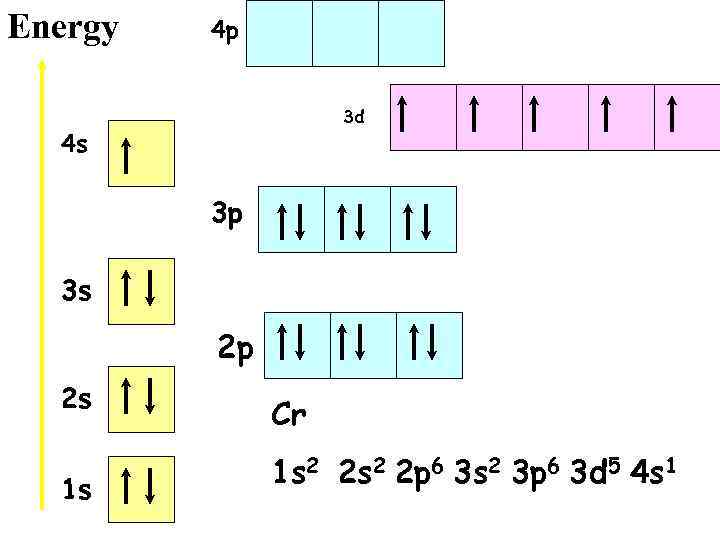 Energy 4 p 3 d 4 s 3 p 3 s 2 p 2 s 1 s Cr 1 s 2 2 p 6 3 s 2 3 p 6 3 d 5 4 s 1
Energy 4 p 3 d 4 s 3 p 3 s 2 p 2 s 1 s Cr 1 s 2 2 p 6 3 s 2 3 p 6 3 d 5 4 s 1
 25 Mn 1 s 22 p 63 s 23 p 64 s 23 d 5 26 Fe 1 s 22 p 63 s 23 p 64 s 23 d 6 27 Co 1 s 22 p 63 s 23 p 64 s 23 d 7 28 Ni 1 s 22 p 63 s 23 p 64 s 23 d 8 29 Cu 1 s 22 p 63 s 23 p 64 s 13 d 10 30 Zn 1 s 22 p 63 s 23 p 64 s 23 d 10
25 Mn 1 s 22 p 63 s 23 p 64 s 23 d 5 26 Fe 1 s 22 p 63 s 23 p 64 s 23 d 6 27 Co 1 s 22 p 63 s 23 p 64 s 23 d 7 28 Ni 1 s 22 p 63 s 23 p 64 s 23 d 8 29 Cu 1 s 22 p 63 s 23 p 64 s 13 d 10 30 Zn 1 s 22 p 63 s 23 p 64 s 23 d 10
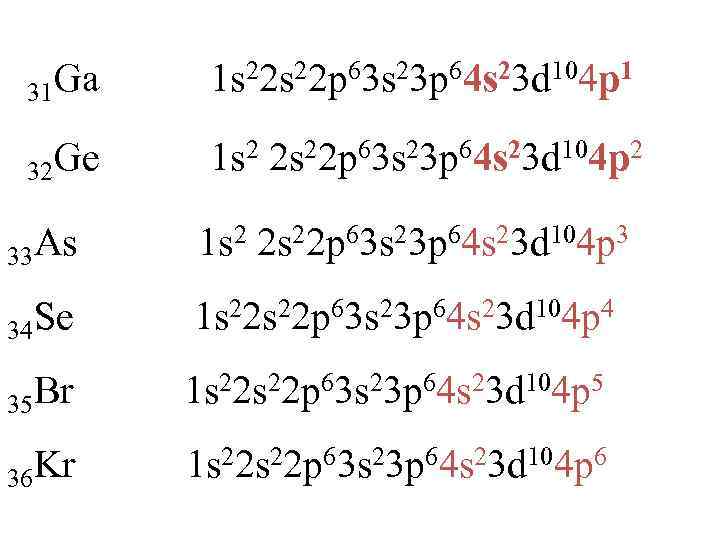 31 Ga 1 s 22 p 63 s 23 p 64 s 23 d 104 p 1 32 Ge 1 s 2 2 s 22 p 63 s 23 p 64 s 23 d 104 p 2 33 As 1 s 2 2 s 22 p 63 s 23 p 64 s 23 d 104 p 3 34 Se 1 s 22 p 63 s 23 p 64 s 23 d 104 p 4 35 Br 1 s 22 p 63 s 23 p 64 s 23 d 104 p 5 36 Kr 1 s 22 p 63 s 23 p 64 s 23 d 104 p 6
31 Ga 1 s 22 p 63 s 23 p 64 s 23 d 104 p 1 32 Ge 1 s 2 2 s 22 p 63 s 23 p 64 s 23 d 104 p 2 33 As 1 s 2 2 s 22 p 63 s 23 p 64 s 23 d 104 p 3 34 Se 1 s 22 p 63 s 23 p 64 s 23 d 104 p 4 35 Br 1 s 22 p 63 s 23 p 64 s 23 d 104 p 5 36 Kr 1 s 22 p 63 s 23 p 64 s 23 d 104 p 6
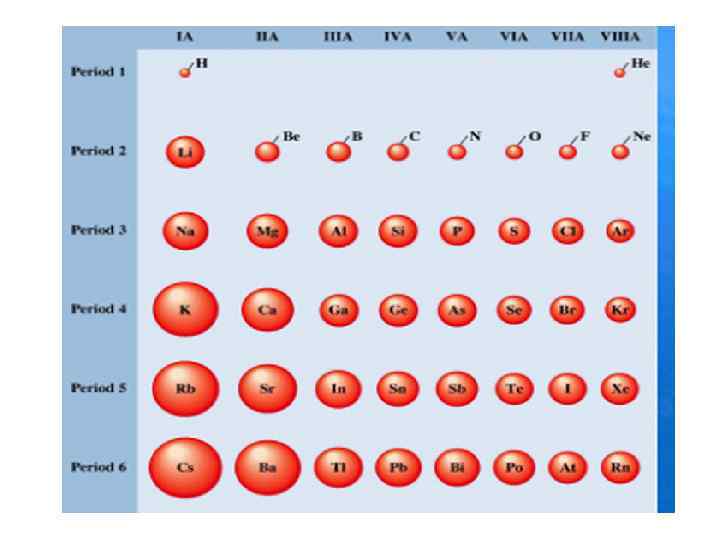
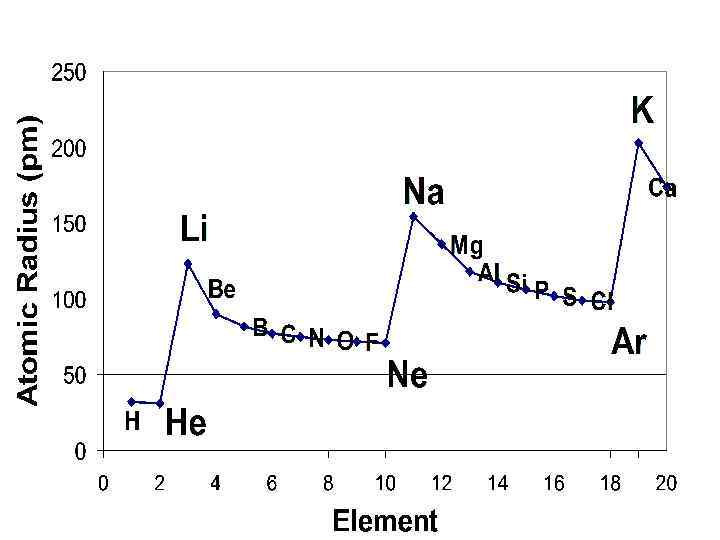
 В периодах орбитальные атомные радиусы по мере увеличения заряда ядра Z уменьшаются вследствие увеличения силы взаимодействия внешних электронов с ядром. Наибольшее уменьшение радиусов происходит в малых периодах. Уменьшение радиусов у d- и fэлементов называется d- и f-сжатием В главных подгруппах радиусы увеличиваются из-за возрастания числа электронных оболочек.
В периодах орбитальные атомные радиусы по мере увеличения заряда ядра Z уменьшаются вследствие увеличения силы взаимодействия внешних электронов с ядром. Наибольшее уменьшение радиусов происходит в малых периодах. Уменьшение радиусов у d- и fэлементов называется d- и f-сжатием В главных подгруппах радиусы увеличиваются из-за возрастания числа электронных оболочек.
 Энергия (потенциал) ионизации атома Ii ─минимальная энергия, необходимая для удаления электрона из атома на бесконечность в соответствии с уравнением: Э 0 + Ii = Э+ + ē. Энергия ионизации в периодах возрастает, а в главных подгруппах сверху вниз уменьшается. Ii характеризует восстановительную способность элемента: чем меньше энергия ионизации, тем больше восстановительная способность. Самым сильным восстановителем является цезий Cs 55.
Энергия (потенциал) ионизации атома Ii ─минимальная энергия, необходимая для удаления электрона из атома на бесконечность в соответствии с уравнением: Э 0 + Ii = Э+ + ē. Энергия ионизации в периодах возрастает, а в главных подгруппах сверху вниз уменьшается. Ii характеризует восстановительную способность элемента: чем меньше энергия ионизации, тем больше восстановительная способность. Самым сильным восстановителем является цезий Cs 55.
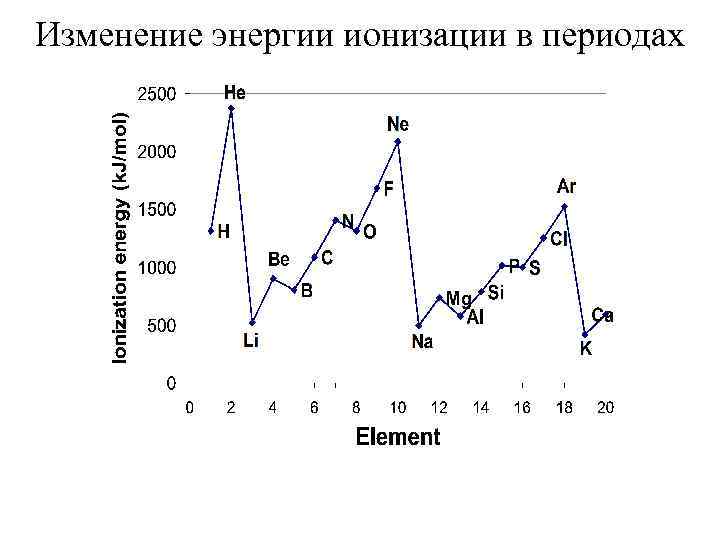 Изменение энергии ионизации в периодах
Изменение энергии ионизации в периодах
 Сродство к электрону - это энергия (к. Дж/моль), которая выделяется или поглощается присоединении к атому электрона и образовании при этом отрицательного иона: Э 0 + ē = Э- Eср Сродство к электрону характеризует окислительную способность элемента: чем больше Eср , тем сильнее его окислительная способность. Окислительная способность нейтральных атомов повышается в периодах слева направо и в группах снизу вверх. Для элементов главных подгрупп сродство к электрону возрастает в периодах слева направо и уменьшается в группах сверху вниз. Максимальное значение сродства к электрону имеет фтор.
Сродство к электрону - это энергия (к. Дж/моль), которая выделяется или поглощается присоединении к атому электрона и образовании при этом отрицательного иона: Э 0 + ē = Э- Eср Сродство к электрону характеризует окислительную способность элемента: чем больше Eср , тем сильнее его окислительная способность. Окислительная способность нейтральных атомов повышается в периодах слева направо и в группах снизу вверх. Для элементов главных подгрупп сродство к электрону возрастает в периодах слева направо и уменьшается в группах сверху вниз. Максимальное значение сродства к электрону имеет фтор.
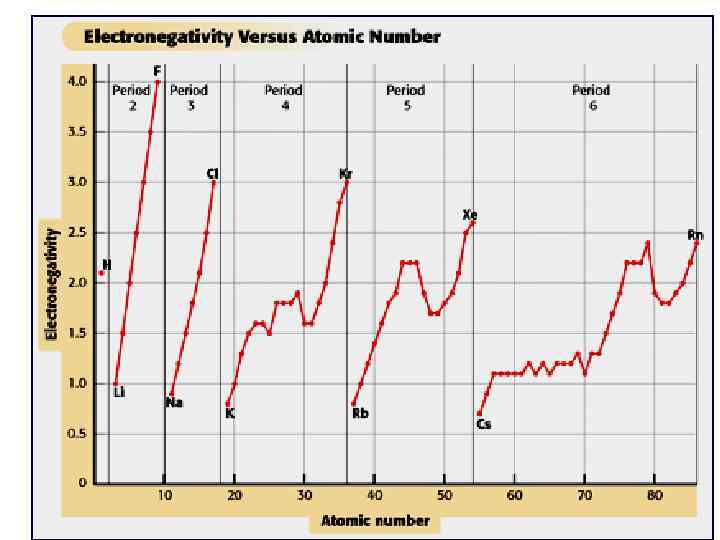
 Электроотрицательность (ЭО) –это способность атома смещать в свою сторону электронное облако при образовании химической связи. ЭО служит мерой неметалличности элементов. Чем больше относительная ЭО, тем сильнее элемент проявляет неметаллические свойства.
Электроотрицательность (ЭО) –это способность атома смещать в свою сторону электронное облако при образовании химической связи. ЭО служит мерой неметалличности элементов. Чем больше относительная ЭО, тем сильнее элемент проявляет неметаллические свойства.