14-Переносчики кислорода (30).ppt
- Количество слайдов: 61
 Переносчики кислорода При 25 о. С растворяется 31, 6 мл О 2 в 1 л Н 2 О. С участием гемоглобина при 37 о. С растворяется 200 мл О 2 в 1 л крови.
Переносчики кислорода При 25 о. С растворяется 31, 6 мл О 2 в 1 л Н 2 О. С участием гемоглобина при 37 о. С растворяется 200 мл О 2 в 1 л крови.
 Метаболизм О 2 Процессы в использовании О 2 : Поглощение Транспорт Запасание Контролированное превращение Контроль образования побочных продуктов
Метаболизм О 2 Процессы в использовании О 2 : Поглощение Транспорт Запасание Контролированное превращение Контроль образования побочных продуктов
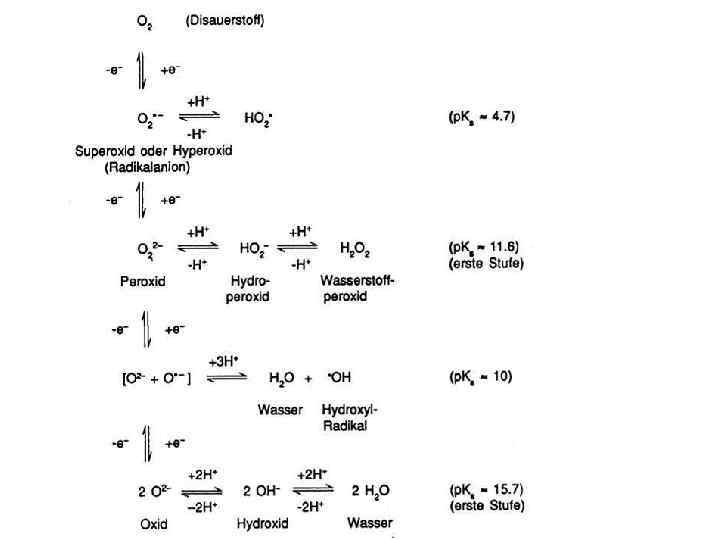
 Редокс-потенциалы и редокс-процессы
Редокс-потенциалы и редокс-процессы
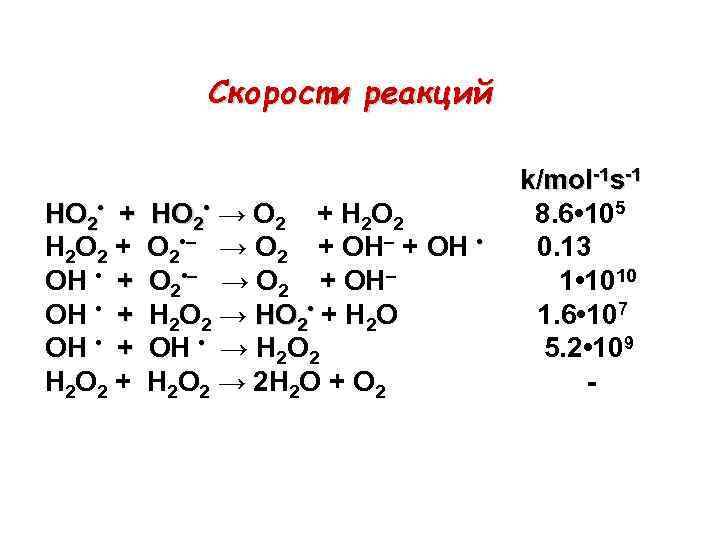 Скорости реакций HO 2 • + H 2 O 2 + OH • + H 2 O 2 + HO 2 • → O 2 + H 2 O 2 • – → O 2 + OH– + OH • O 2 • – → O 2 + OH– H 2 O 2 → HO 2 • + H 2 O OH • → H 2 O 2 → 2 H 2 O + O 2 k/mol-1 s-1 8. 6 • 105 0. 13 1 • 1010 1. 6 • 107 5. 2 • 109 -
Скорости реакций HO 2 • + H 2 O 2 + OH • + H 2 O 2 + HO 2 • → O 2 + H 2 O 2 • – → O 2 + OH– + OH • O 2 • – → O 2 + OH– H 2 O 2 → HO 2 • + H 2 O OH • → H 2 O 2 → 2 H 2 O + O 2 k/mol-1 s-1 8. 6 • 105 0. 13 1 • 1010 1. 6 • 107 5. 2 • 109 -
![Активные формы кислорода (АФК) [Активные метаболиты кислорода (АМК)] Reactive Oxygen Species ROS Активные формы кислорода (АФК) [Активные метаболиты кислорода (АМК)] Reactive Oxygen Species ROS](https://present5.com/presentation/6624959_133364530/image-7.jpg) Активные формы кислорода (АФК) [Активные метаболиты кислорода (АМК)] Reactive Oxygen Species ROS
Активные формы кислорода (АФК) [Активные метаболиты кислорода (АМК)] Reactive Oxygen Species ROS
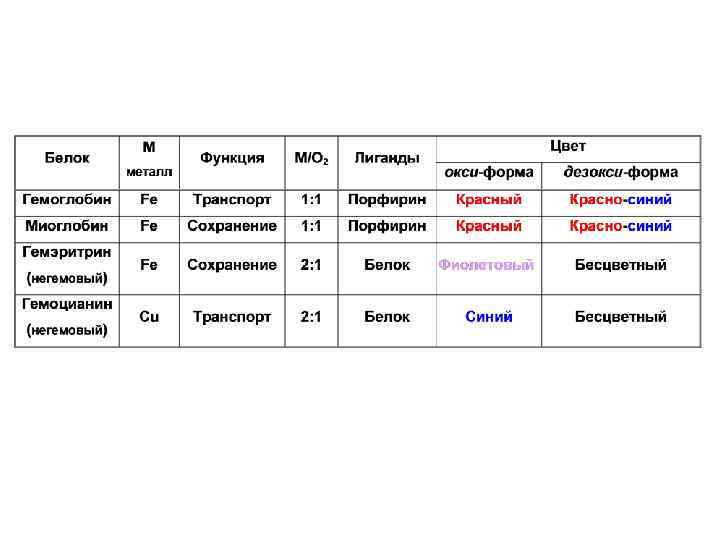
 In hemoglobin and myoglobin, O 2 binds as a superoxide: Fe. III – (O 2)-.
In hemoglobin and myoglobin, O 2 binds as a superoxide: Fe. III – (O 2)-.
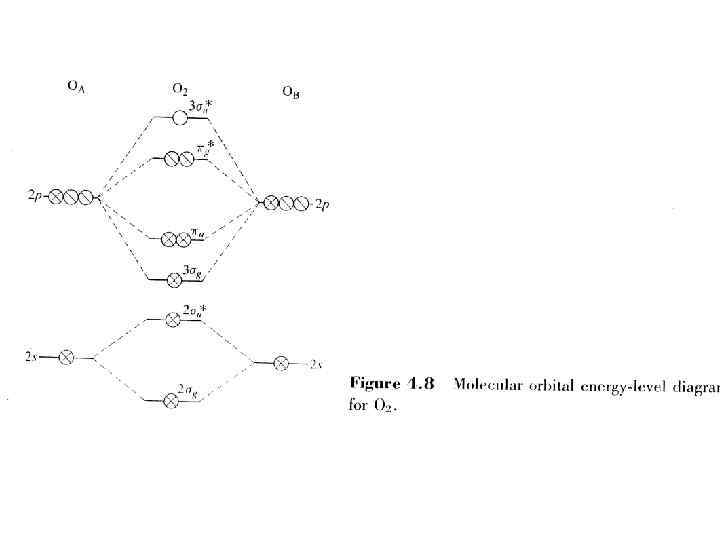
 О 2 О 2. - О 22 - 2 1, 5 1 Длина связи (Å) 1, 21 ~1, 28 ~1, 49 max см-1 1560 1150 -1100 Порядок связи 850 -740
О 2 О 2. - О 22 - 2 1, 5 1 Длина связи (Å) 1, 21 ~1, 28 ~1, 49 max см-1 1560 1150 -1100 Порядок связи 850 -740
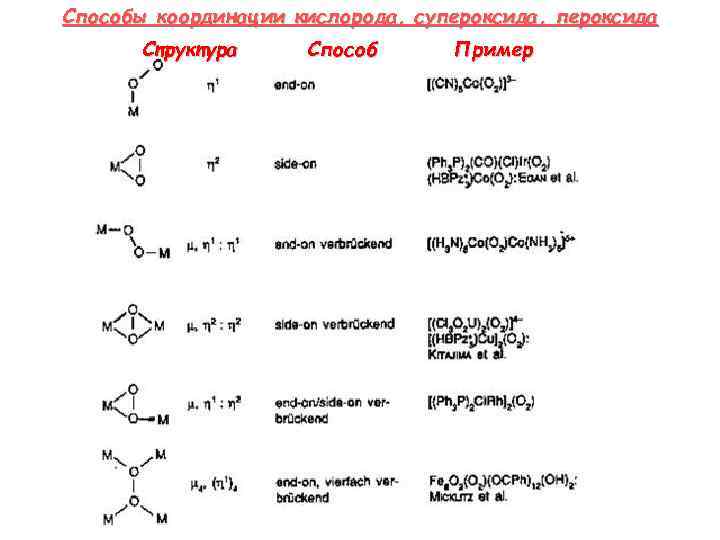 Способы координации кислорода, супероксида, пероксида Структура Способ Пример
Способы координации кислорода, супероксида, пероксида Структура Способ Пример
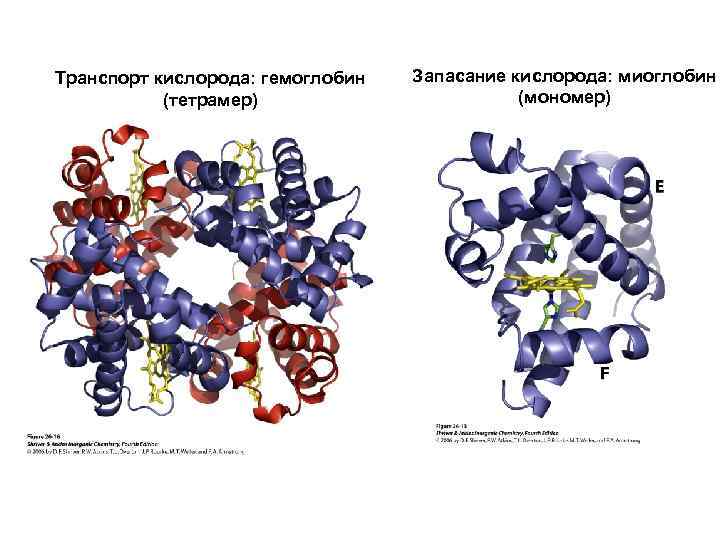 Транспорт кислорода: гемоглобин (тетрамер) Запасание кислорода: миоглобин (мономер)
Транспорт кислорода: гемоглобин (тетрамер) Запасание кислорода: миоглобин (мономер)
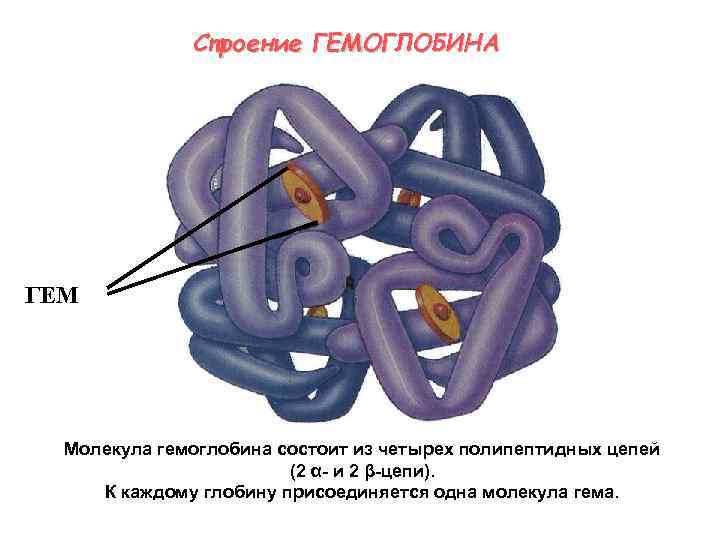 Строение ГЕМОГЛОБИНА ГЕМ Молекула гемоглобина состоит из четырех полипептидных цепей (2 α- и 2 β-цепи). К каждому глобину присоединяется одна молекула гема.
Строение ГЕМОГЛОБИНА ГЕМ Молекула гемоглобина состоит из четырех полипептидных цепей (2 α- и 2 β-цепи). К каждому глобину присоединяется одна молекула гема.
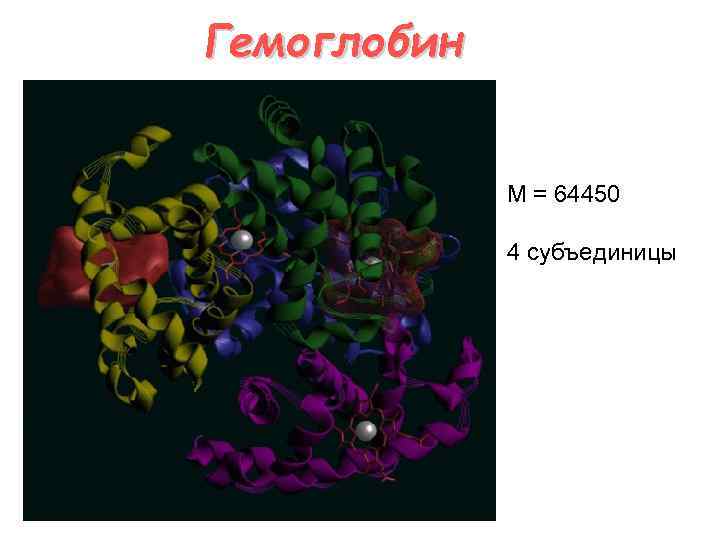 Гемоглобин M = 64450 4 субъединицы
Гемоглобин M = 64450 4 субъединицы
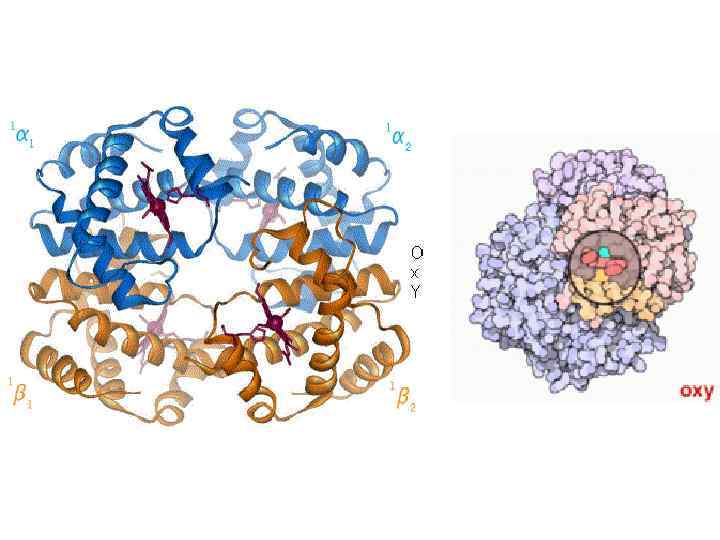
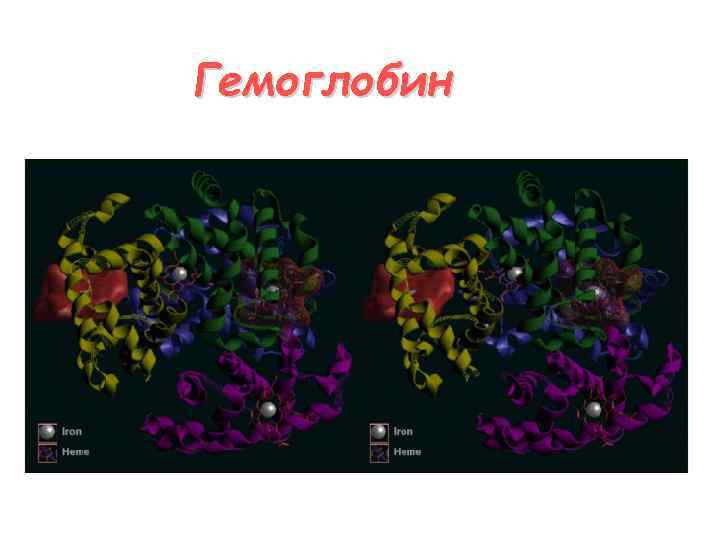 Гемоглобин
Гемоглобин
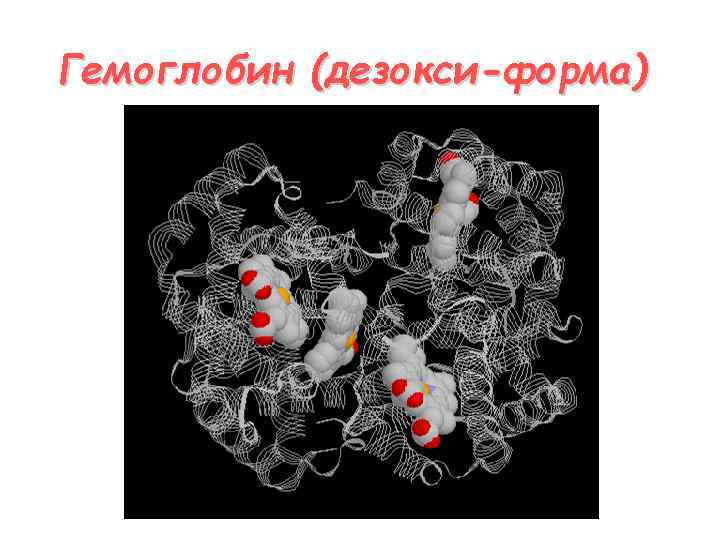 Гемоглобин (дезокси-форма)
Гемоглобин (дезокси-форма)
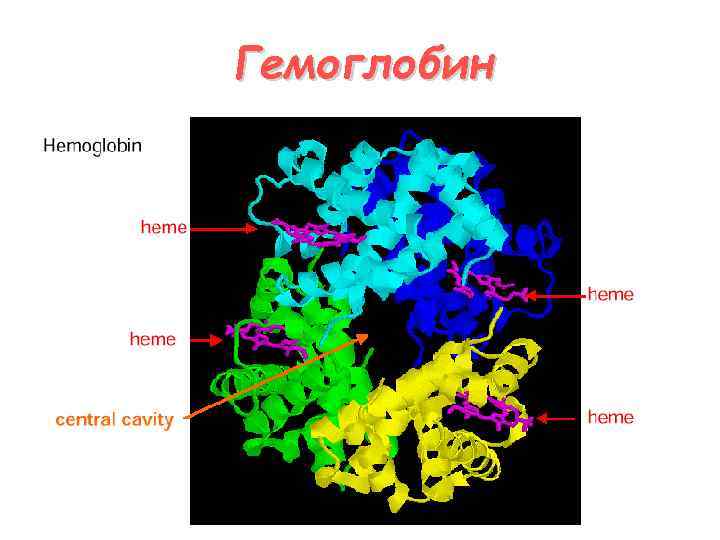 Гемоглобин
Гемоглобин
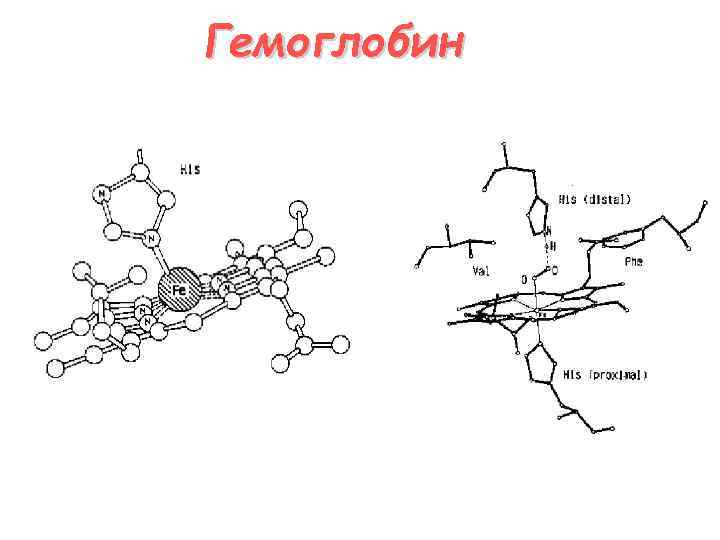 Гемоглобин
Гемоглобин
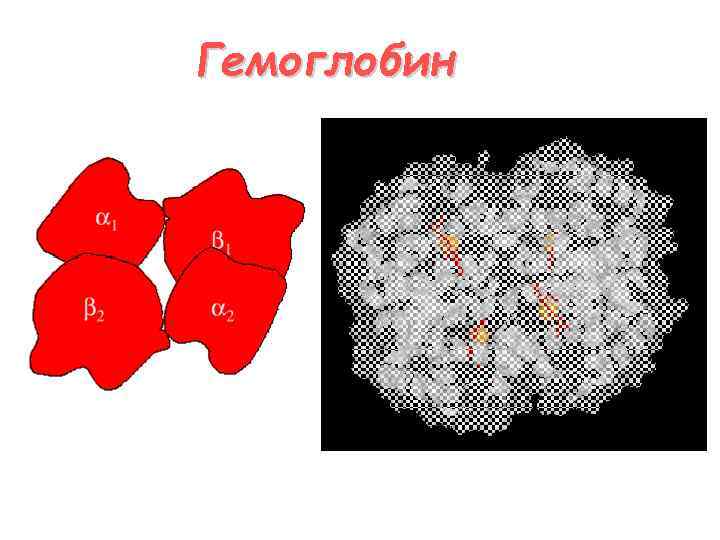 Гемоглобин
Гемоглобин
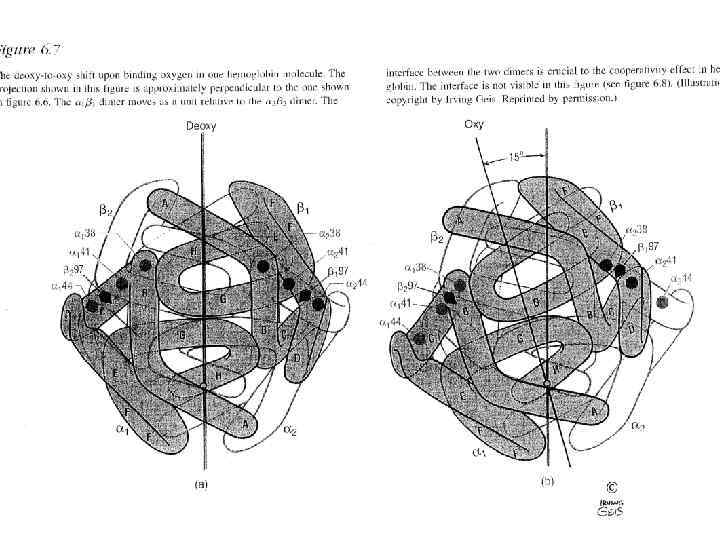
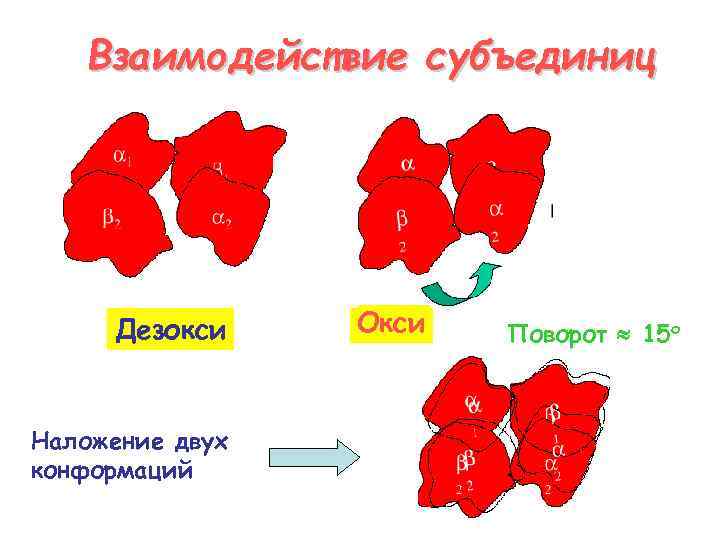 Взаимодействие субъединиц Дезокси Наложение двух конформаций Окси Поворот 15 о
Взаимодействие субъединиц Дезокси Наложение двух конформаций Окси Поворот 15 о
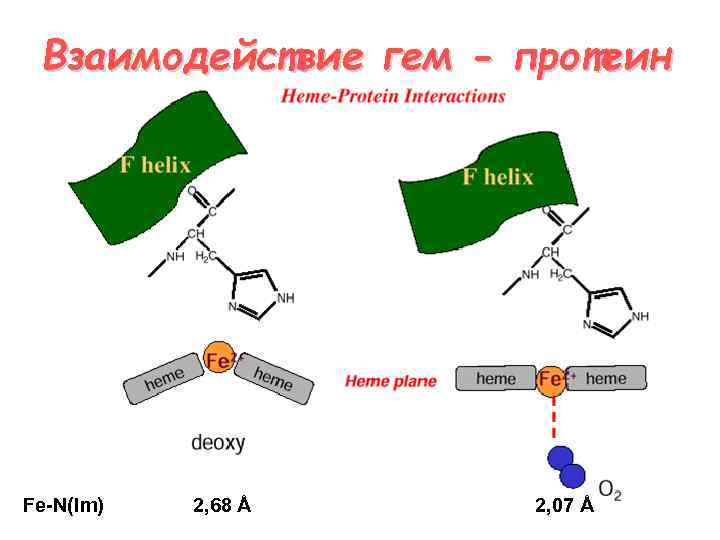 Взаимодействие гем - протеин Fe-N(Im) 2, 68 Å 2, 07 Å
Взаимодействие гем - протеин Fe-N(Im) 2, 68 Å 2, 07 Å
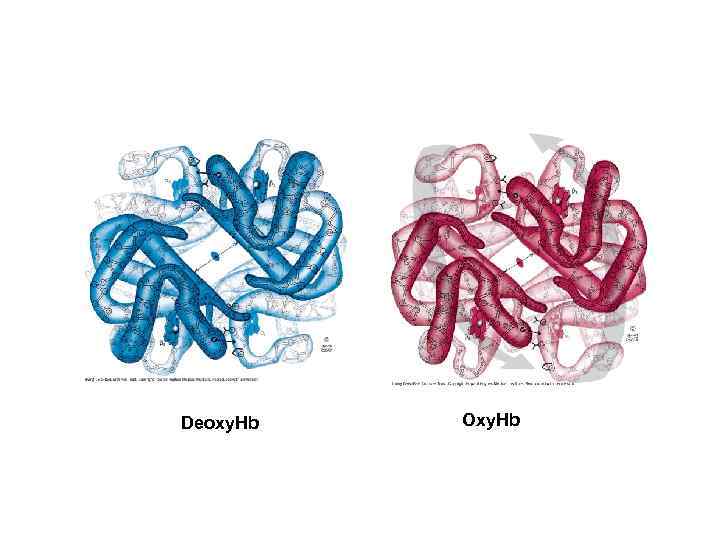 Deoxy. Hb Oxy. Hb
Deoxy. Hb Oxy. Hb
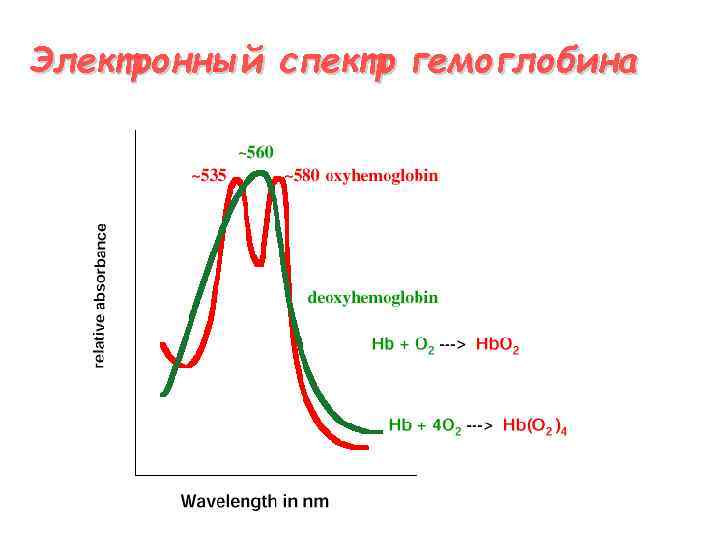 Электронный спектр гемоглобина
Электронный спектр гемоглобина
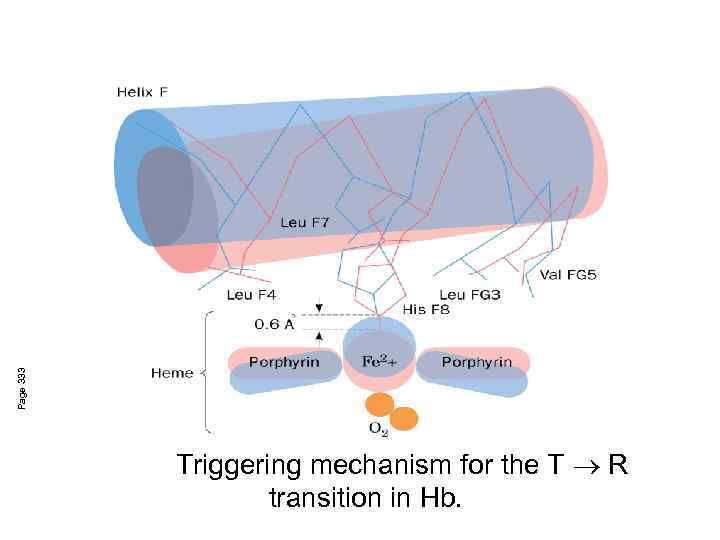 Page 333 Triggering mechanism for the T ® R transition in Hb.
Page 333 Triggering mechanism for the T ® R transition in Hb.
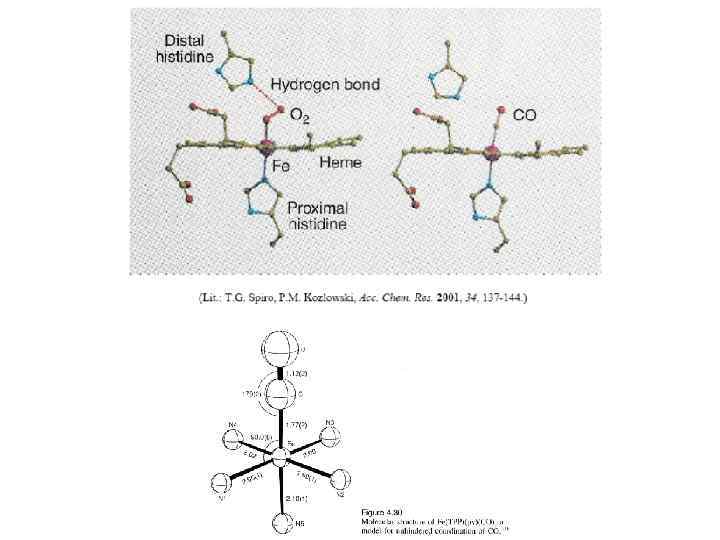
 Нарушение транспорта О 2 гемоглобином ИНИБИТОРЫ: NO 2‾ окисляет Fe(II) до Fe(III) и образуется метгемоглобин, который не способен связывать О 2. СО блокирует гемоглобин ( константа связывания в 320 раз выше) ¼ об. % СО во выдыхаемом воздухе ингибирует 25% гемоглобина, ½ об. % СО во выдыхаемом воздухе ингибирует 90% гемоглобина
Нарушение транспорта О 2 гемоглобином ИНИБИТОРЫ: NO 2‾ окисляет Fe(II) до Fe(III) и образуется метгемоглобин, который не способен связывать О 2. СО блокирует гемоглобин ( константа связывания в 320 раз выше) ¼ об. % СО во выдыхаемом воздухе ингибирует 25% гемоглобина, ½ об. % СО во выдыхаемом воздухе ингибирует 90% гемоглобина
 ГЕМОГЛОБИН Нормальный уровень гемоглобина для мужчин ~ 135 - 180 г/л; для женщин ~ 115 - 165 г/л
ГЕМОГЛОБИН Нормальный уровень гемоглобина для мужчин ~ 135 - 180 г/л; для женщин ~ 115 - 165 г/л
 Миоглобин
Миоглобин
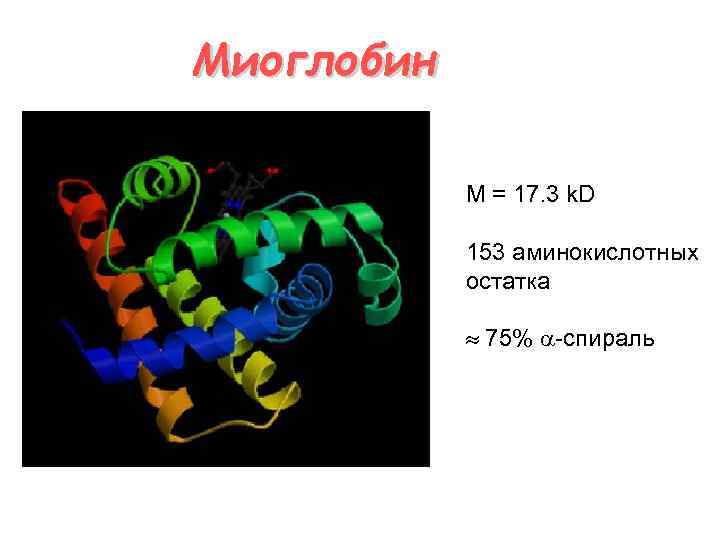 Миоглобин M = 17. 3 k. D 153 аминокислотных остатка 75% -спираль
Миоглобин M = 17. 3 k. D 153 аминокислотных остатка 75% -спираль
 Феноменология связывания кислорода гемоглобином 1. Увеличение эффективности связывания каждой последующей молекулы О 2 (позитивный кооперативный эффект). Соотношение констант образования 1 : 4 : 24 : 9 для моно-, ди-, три- и тетраоксигемоглобина. 2. Изменение магнитных свойств присоединении кислорода (дезоксигемоглобин – парамагнитний, оксигемоглобин – диамагнитний).
Феноменология связывания кислорода гемоглобином 1. Увеличение эффективности связывания каждой последующей молекулы О 2 (позитивный кооперативный эффект). Соотношение констант образования 1 : 4 : 24 : 9 для моно-, ди-, три- и тетраоксигемоглобина. 2. Изменение магнитных свойств присоединении кислорода (дезоксигемоглобин – парамагнитний, оксигемоглобин – диамагнитний).
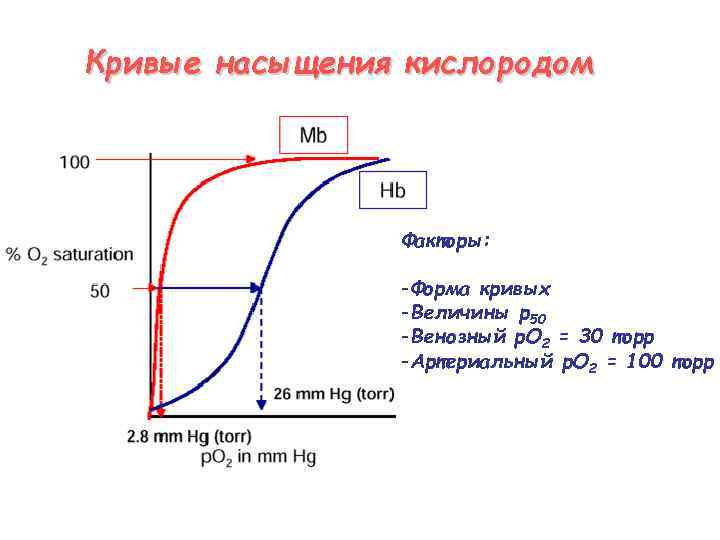 Кривые насыщения кислородом Факторы: -Форма кривых -Величины p 50 -Венозный p. O 2 = 30 торр -Артериальный p. O 2 = 100 торр
Кривые насыщения кислородом Факторы: -Форма кривых -Величины p 50 -Венозный p. O 2 = 30 торр -Артериальный p. O 2 = 100 торр
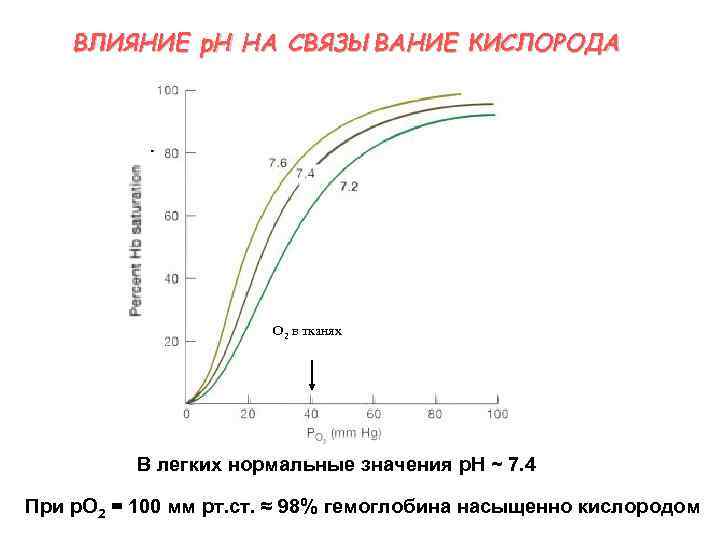 ВЛИЯНИЕ p. H НА СВЯЗЫВАНИЕ КИСЛОРОДА O 2 в тканях В легких нормальные значения p. H ~ 7. 4 При р. O 2 = 100 мм рт. ст. ≈ 98% гемоглобина насыщенно кислородом
ВЛИЯНИЕ p. H НА СВЯЗЫВАНИЕ КИСЛОРОДА O 2 в тканях В легких нормальные значения p. H ~ 7. 4 При р. O 2 = 100 мм рт. ст. ≈ 98% гемоглобина насыщенно кислородом
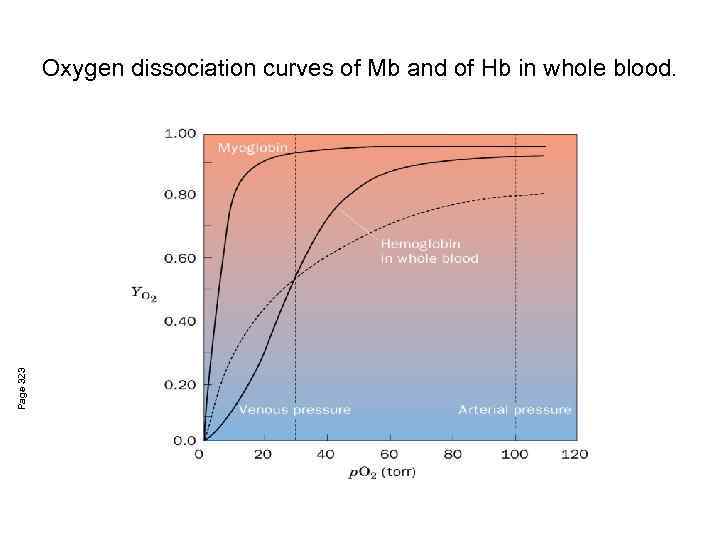 Page 323 Oxygen dissociation curves of Mb and of Hb in whole blood.
Page 323 Oxygen dissociation curves of Mb and of Hb in whole blood.
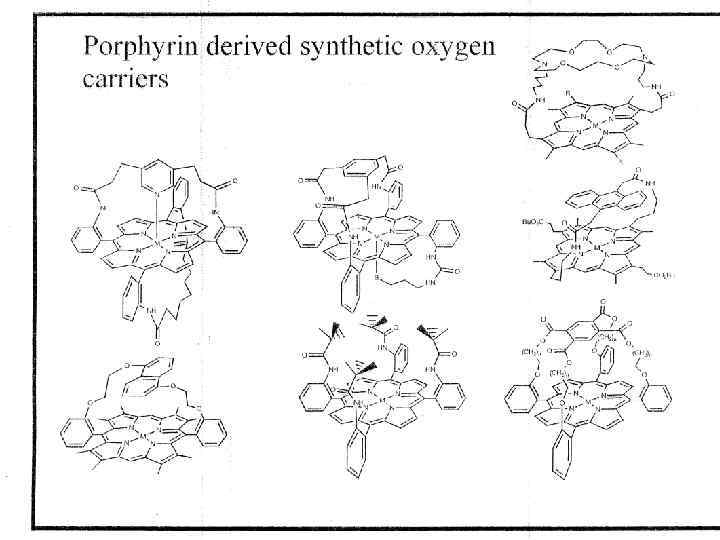
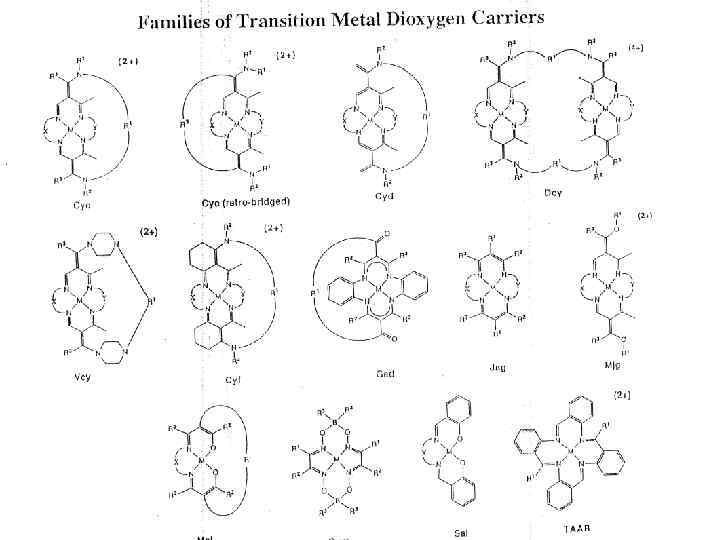
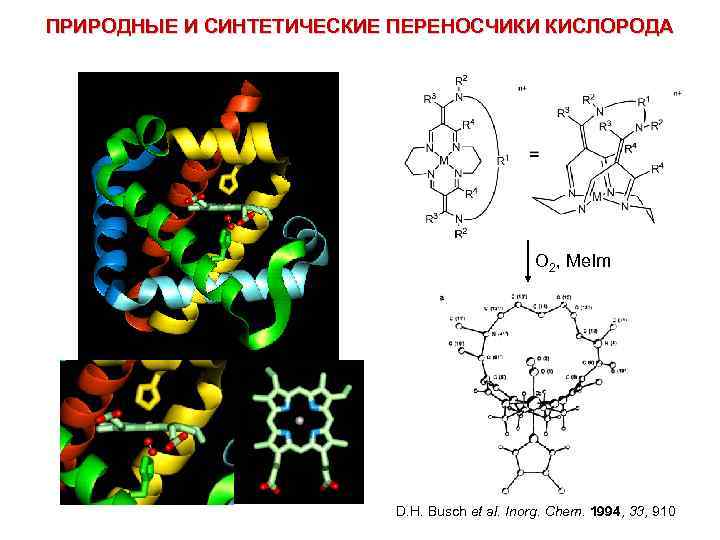 ПРИРОДНЫЕ И СИНТЕТИЧЕСКИЕ ПЕРЕНОСЧИКИ КИСЛОРОДА O 2, Me. Im D. H. Busch et al. Inorg. Chem. 1994, 33, 910
ПРИРОДНЫЕ И СИНТЕТИЧЕСКИЕ ПЕРЕНОСЧИКИ КИСЛОРОДА O 2, Me. Im D. H. Busch et al. Inorg. Chem. 1994, 33, 910
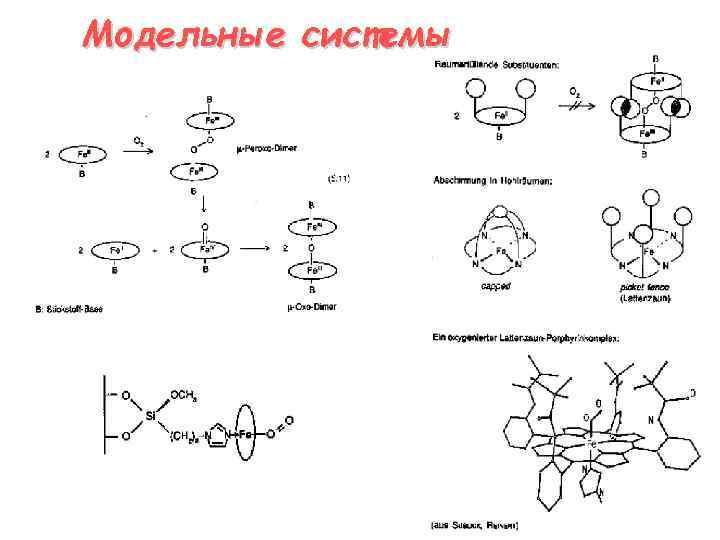 Модельные системы
Модельные системы
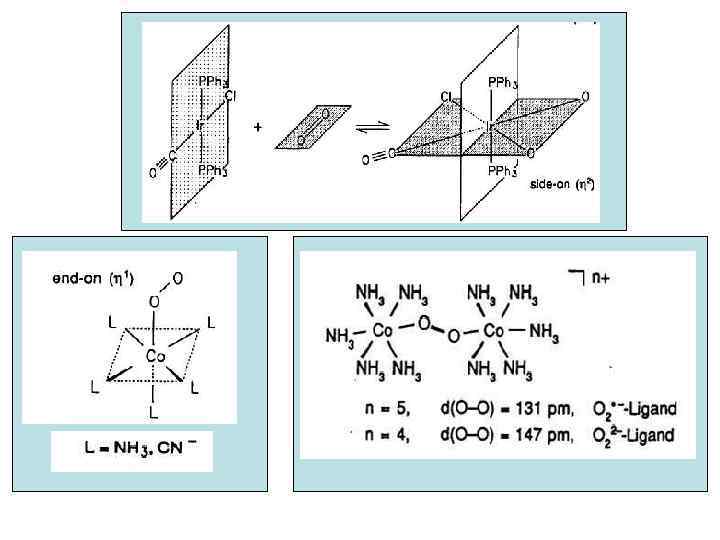
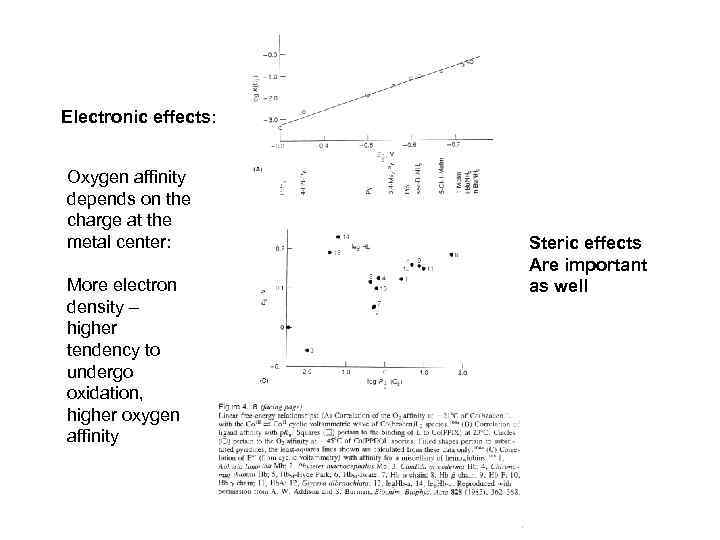 Electronic effects: Oxygen affinity depends on the charge at the metal center: More electron density – higher tendency to undergo oxidation, higher oxygen affinity Steric effects Are important as well
Electronic effects: Oxygen affinity depends on the charge at the metal center: More electron density – higher tendency to undergo oxidation, higher oxygen affinity Steric effects Are important as well
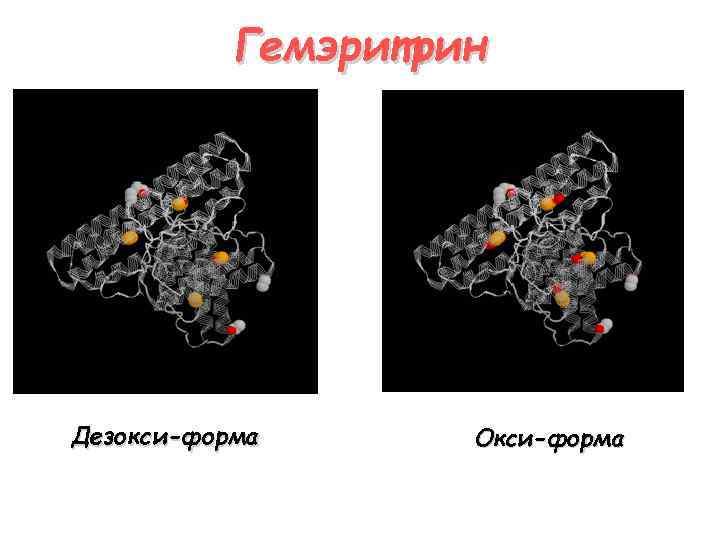 Гемэритрин Дезокси-форма Окси-форма
Гемэритрин Дезокси-форма Окси-форма
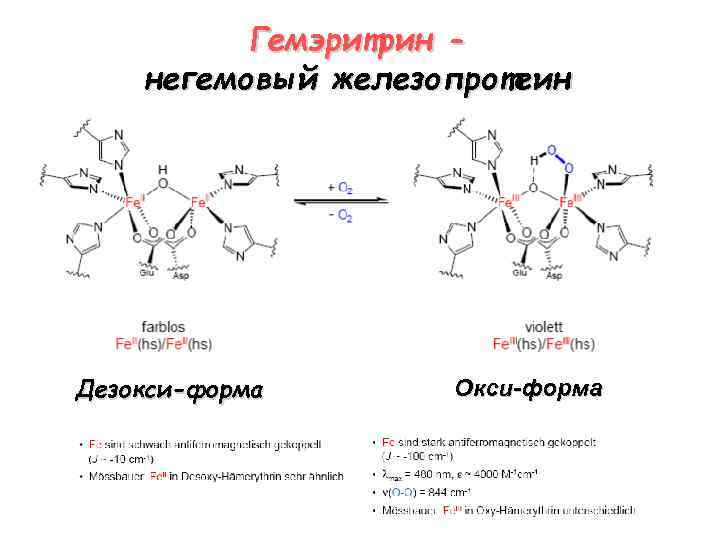 Гемэритрин негемовый железопротеин Дезокси-форма Окси-форма
Гемэритрин негемовый железопротеин Дезокси-форма Окси-форма
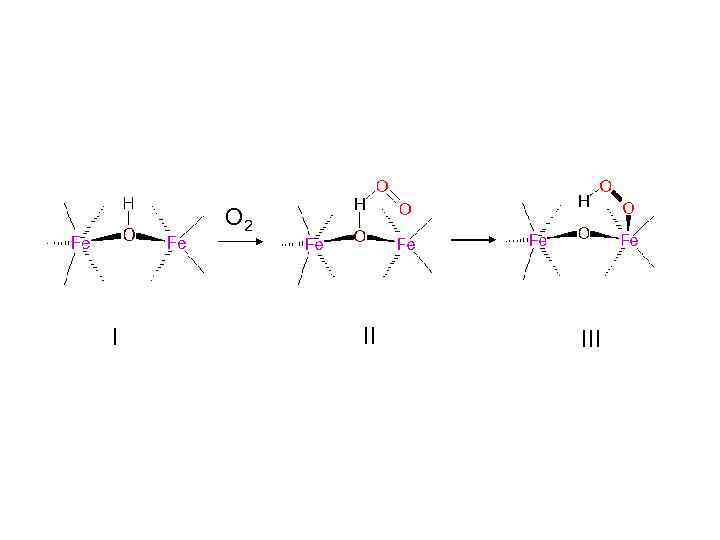 O 2 I II III
O 2 I II III
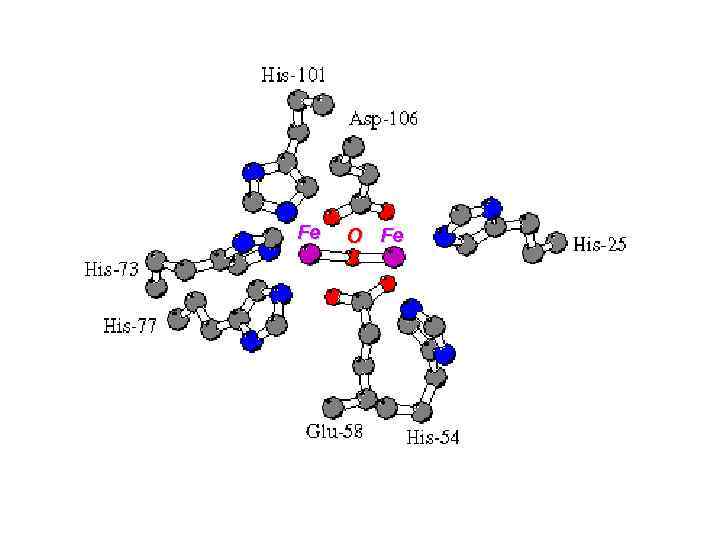 Fe O Fe
Fe O Fe
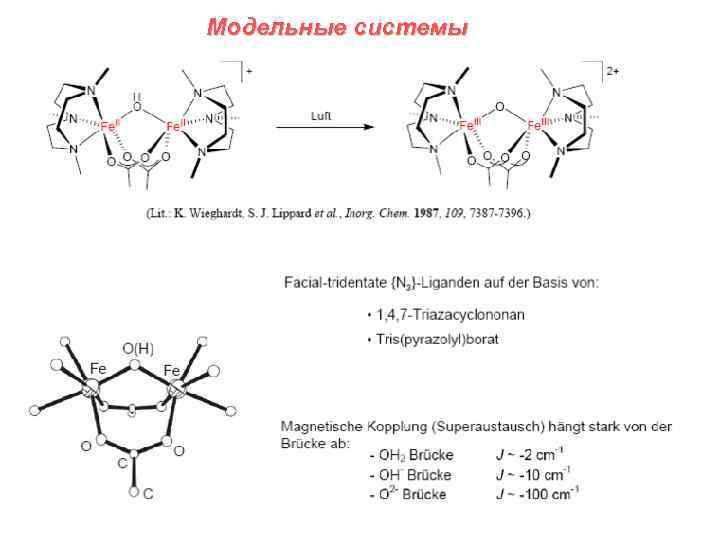 Модельные системы
Модельные системы

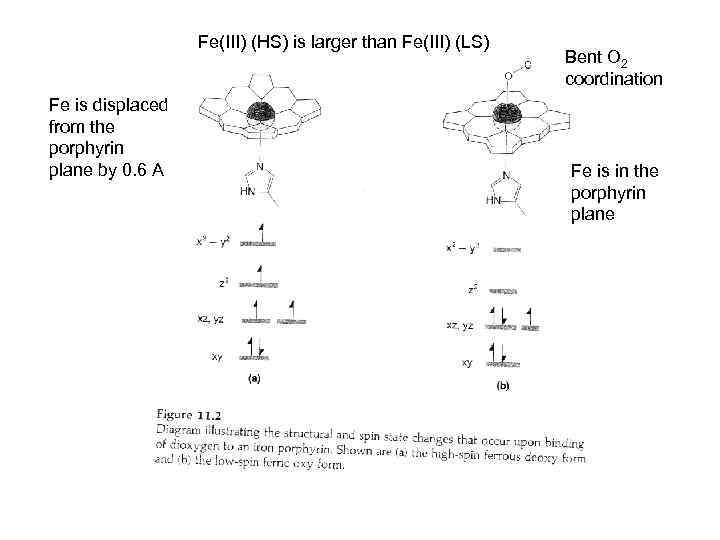 Fe(III) (HS) is larger than Fe(III) (LS) Fe is displaced from the porphyrin plane by 0. 6 A Bent O 2 coordination Fe is in the porphyrin plane
Fe(III) (HS) is larger than Fe(III) (LS) Fe is displaced from the porphyrin plane by 0. 6 A Bent O 2 coordination Fe is in the porphyrin plane




 protein Heme complexes: CO binds MUCH stronger than O 2
protein Heme complexes: CO binds MUCH stronger than O 2





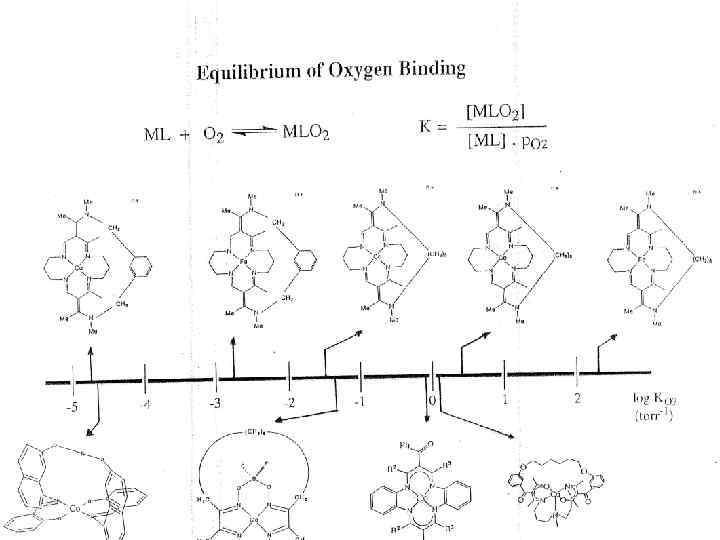
 REVERSIBLE DIOXYGEN BINDING
REVERSIBLE DIOXYGEN BINDING



