04 Обмен белков.ppt
- Количество слайдов: 30
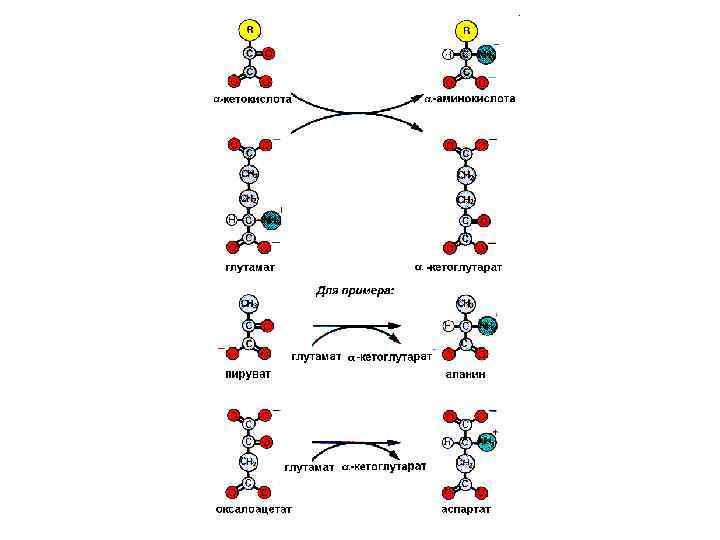
 ПЕРЕАМИНИРОВАНИЕ Аминотрансферазы содержат в качестве кофермента производные витамина В 6 - пиридоксаль-5'-фосфат (I) и пиридоксамин-5'-фосфат (II). В основе каталитической активности пиридоксаль-5'-фосфата лежит способность его формильной группы образовывать с аминокислотами шиффовы основания, легко гидролизующиеся до пиридоксамин-5'-фосфата и a-кетокислоты. Общая схема переаминирования с участием аминотрансфераз представляет собой сумму двух полуреакций:
ПЕРЕАМИНИРОВАНИЕ Аминотрансферазы содержат в качестве кофермента производные витамина В 6 - пиридоксаль-5'-фосфат (I) и пиридоксамин-5'-фосфат (II). В основе каталитической активности пиридоксаль-5'-фосфата лежит способность его формильной группы образовывать с аминокислотами шиффовы основания, легко гидролизующиеся до пиридоксамин-5'-фосфата и a-кетокислоты. Общая схема переаминирования с участием аминотрансфераз представляет собой сумму двух полуреакций:
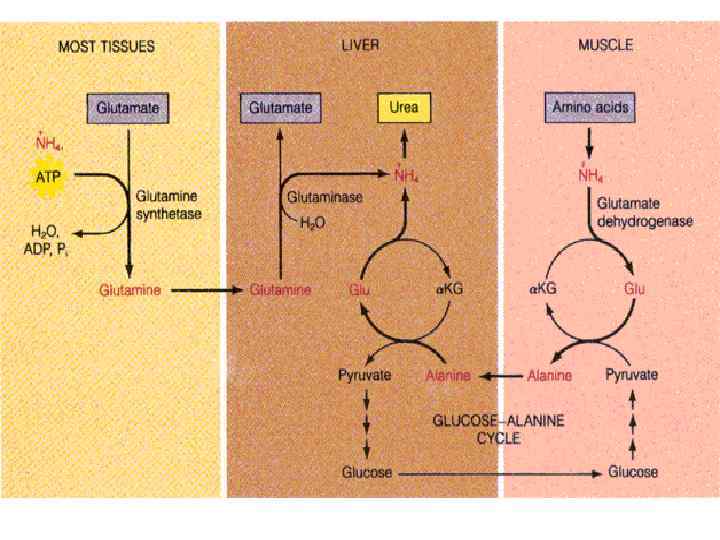
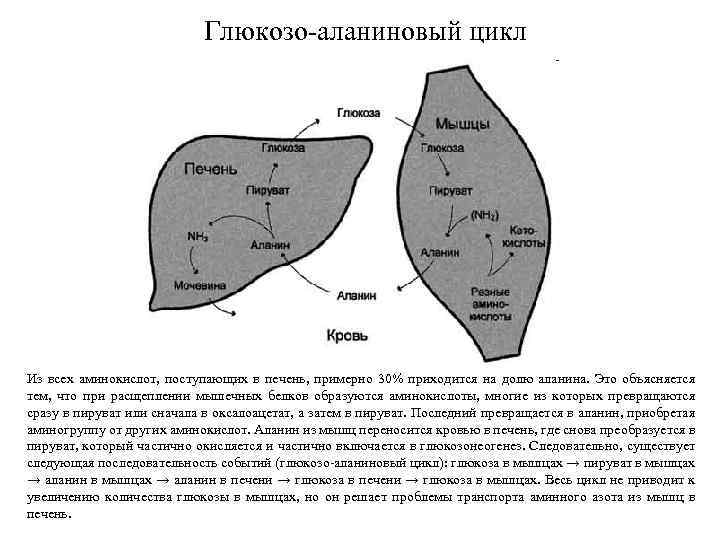 Глюкозо-аланиновый цикл Из всех аминокислот, поступающих в печень, примерно 30% приходится на долю аланина. Это объясняется тем, что при расщеплении мышечных белков образуются аминокислоты, многие из которых превращаются сразу в пируват или сначала в оксалоацетат, а затем в пируват. Последний превращается в аланин, приобретая аминогруппу от других аминокислот. Аланин из мышц переносится кровью в печень, где снова преобразуется в пируват, который частично окисляется и частично включается в глюкозонеогенез. Следовательно, существует следующая последовательность событий (глюкозо-аланиновый цикл): глюкоза в мышцах → пируват в мышцах → аланин в печени → глюкоза в мышцах. Весь цикл не приводит к увеличению количества глюкозы в мышцах, но он решает проблемы транспорта аминного азота из мышц в печень.
Глюкозо-аланиновый цикл Из всех аминокислот, поступающих в печень, примерно 30% приходится на долю аланина. Это объясняется тем, что при расщеплении мышечных белков образуются аминокислоты, многие из которых превращаются сразу в пируват или сначала в оксалоацетат, а затем в пируват. Последний превращается в аланин, приобретая аминогруппу от других аминокислот. Аланин из мышц переносится кровью в печень, где снова преобразуется в пируват, который частично окисляется и частично включается в глюкозонеогенез. Следовательно, существует следующая последовательность событий (глюкозо-аланиновый цикл): глюкоза в мышцах → пируват в мышцах → аланин в печени → глюкоза в мышцах. Весь цикл не приводит к увеличению количества глюкозы в мышцах, но он решает проблемы транспорта аминного азота из мышц в печень.
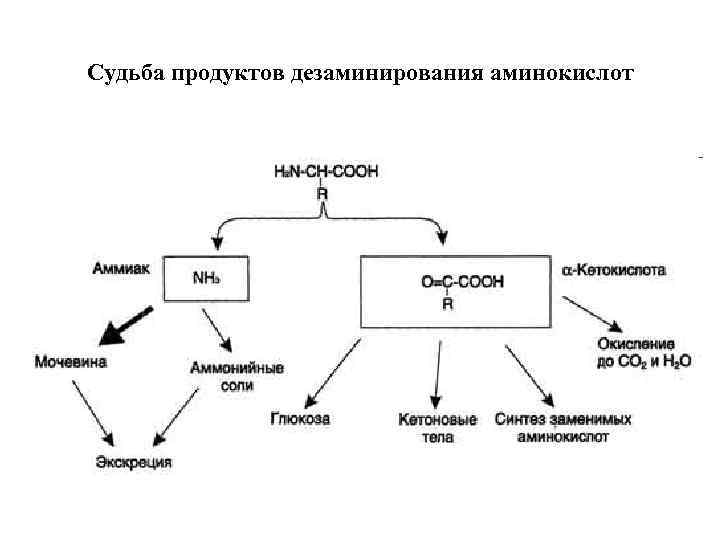 Судьба продуктов дезаминирования аминокислот
Судьба продуктов дезаминирования аминокислот
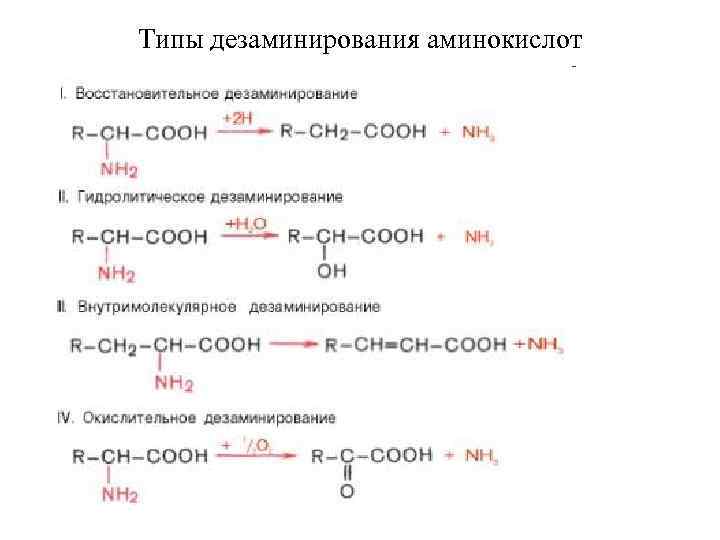 Типы дезаминирования аминокислот
Типы дезаминирования аминокислот
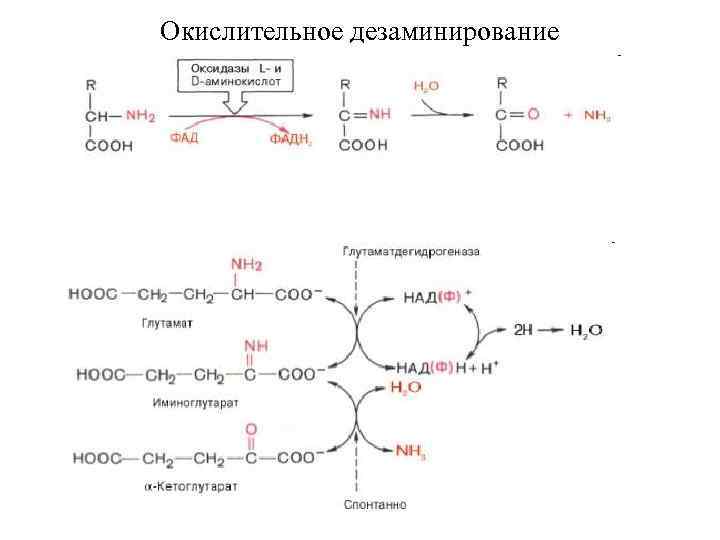 Окислительное дезаминирование
Окислительное дезаминирование
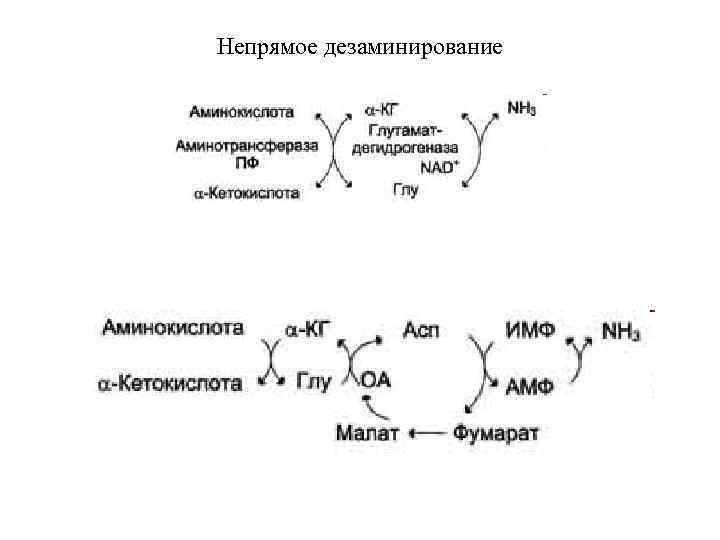 Непрямое дезаминирование
Непрямое дезаминирование
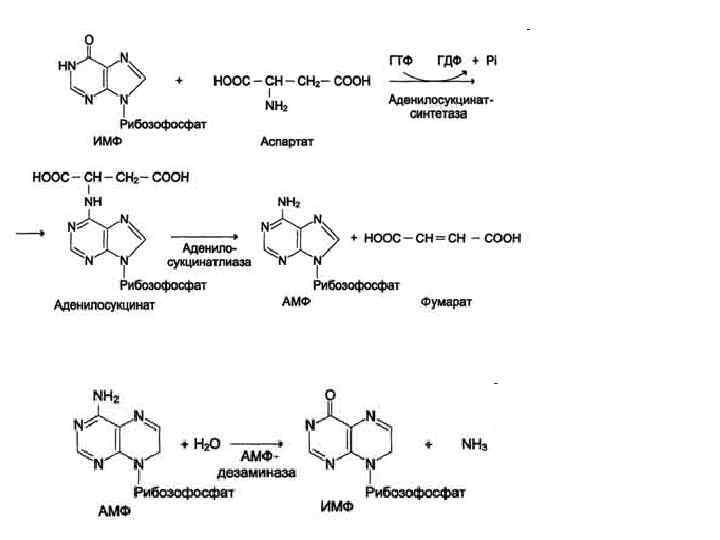
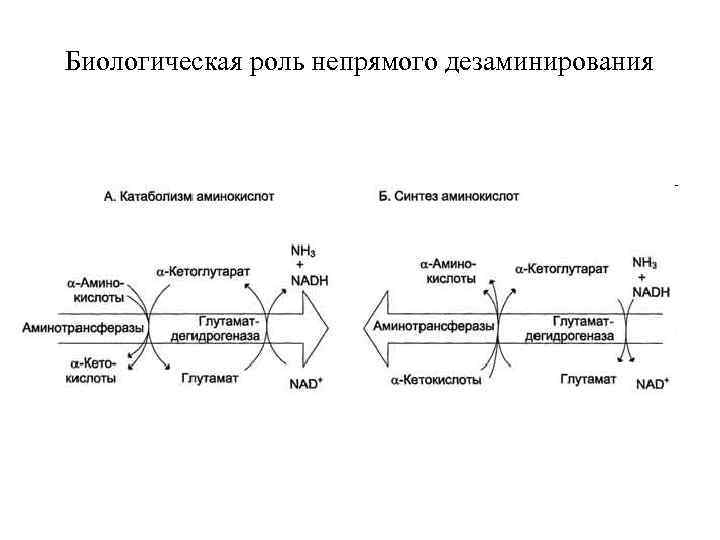 Биологическая роль непрямого дезаминирования
Биологическая роль непрямого дезаминирования
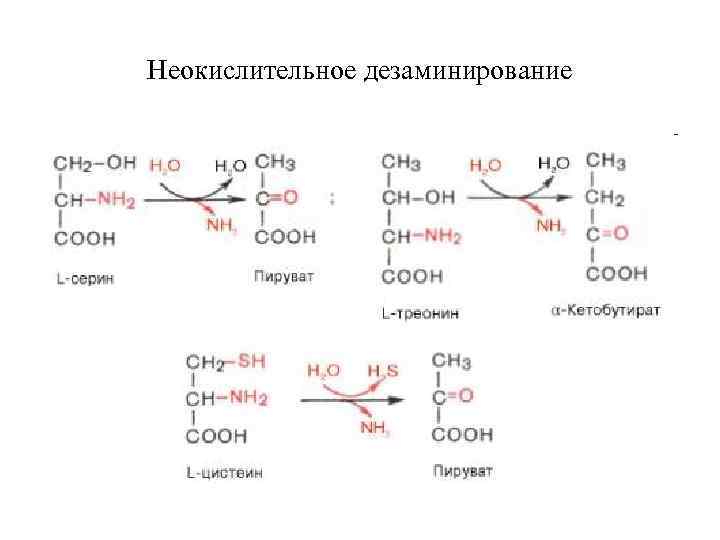 Неокислительное дезаминирование
Неокислительное дезаминирование
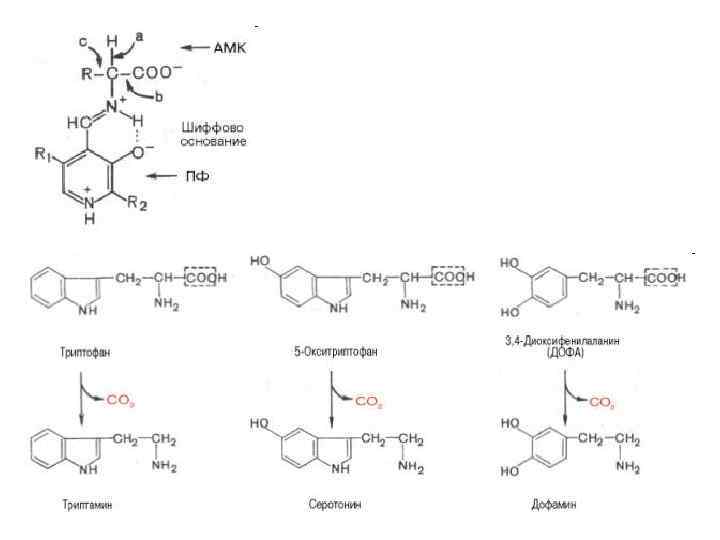
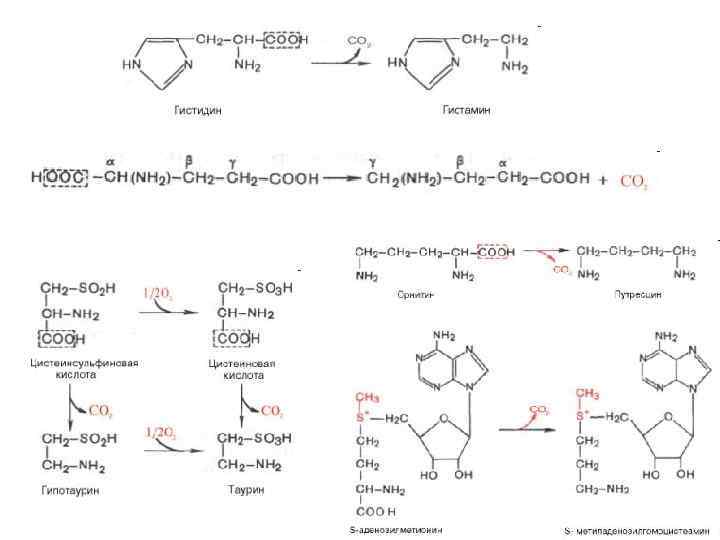
 Декарбоксилирование аминокислот α-Декарбоксилирование, характерное для тканей животных. Продуктами реакции являются СО 2 и биогенные амины ω-Декарбоксилирование, свойственное микроорганизмам Декарбоксилирование, связанное с реакцией трансаминирования Декарбоксилирование, связанное с реакцией конденсации двух молекул
Декарбоксилирование аминокислот α-Декарбоксилирование, характерное для тканей животных. Продуктами реакции являются СО 2 и биогенные амины ω-Декарбоксилирование, свойственное микроорганизмам Декарбоксилирование, связанное с реакцией трансаминирования Декарбоксилирование, связанное с реакцией конденсации двух молекул
 Источники аммиака в организме Источник Процесс Ферменты Локализация процесса Аминокислоты Непрямое дезаминирование (основной путь дезаминирования аминокислот) Аминотрансферазы, ПФ Глутаматдегидрогеназа, NAD+ Все ткани Окислительное дезаминирование Глутамата Глутаматдегидрогеназа, NAD+ Все ткани Неокислительное дезаминирование Гис, Сер, Тре Гистидаза-Серин, треониндегидратазы, ПФ Преимущественно печень Окислительное дезаминирование аминокислот (малозначимый путь дезаминирования) Оксидаза L-аминокислот, FMN Печень и почки Биогенные амины Окислительное дезаминирование (путь инактивации биогенных аминов) Аминооксидазы, FAD Все ткани АМФ Гидролитическое дезаминирование АМФ-дезаминаза Интенсивно Работающая мышца
Источники аммиака в организме Источник Процесс Ферменты Локализация процесса Аминокислоты Непрямое дезаминирование (основной путь дезаминирования аминокислот) Аминотрансферазы, ПФ Глутаматдегидрогеназа, NAD+ Все ткани Окислительное дезаминирование Глутамата Глутаматдегидрогеназа, NAD+ Все ткани Неокислительное дезаминирование Гис, Сер, Тре Гистидаза-Серин, треониндегидратазы, ПФ Преимущественно печень Окислительное дезаминирование аминокислот (малозначимый путь дезаминирования) Оксидаза L-аминокислот, FMN Печень и почки Биогенные амины Окислительное дезаминирование (путь инактивации биогенных аминов) Аминооксидазы, FAD Все ткани АМФ Гидролитическое дезаминирование АМФ-дезаминаза Интенсивно Работающая мышца
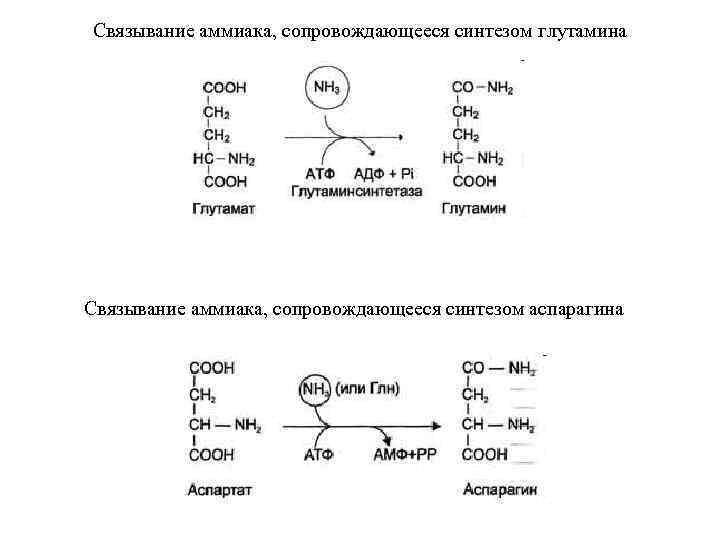 Связывание аммиака, сопровождающееся синтезом глутамина Связывание аммиака, сопровождающееся синтезом аспарагина
Связывание аммиака, сопровождающееся синтезом глутамина Связывание аммиака, сопровождающееся синтезом аспарагина
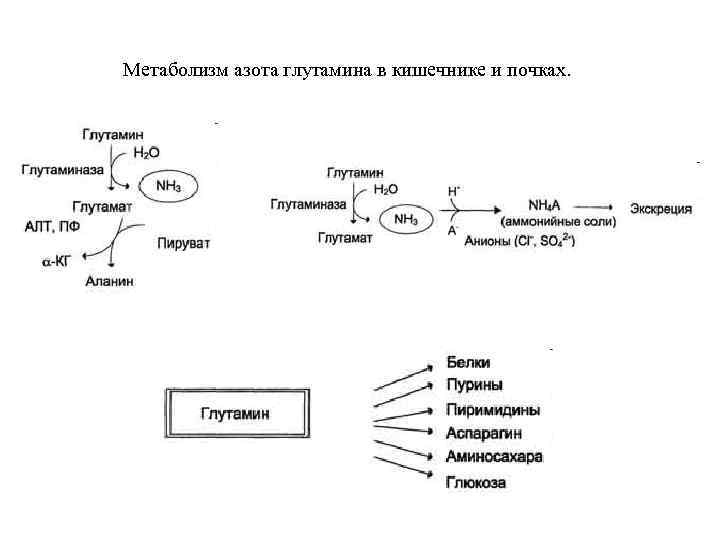 Метаболизм азота глутамина в кишечнике и почках.
Метаболизм азота глутамина в кишечнике и почках.
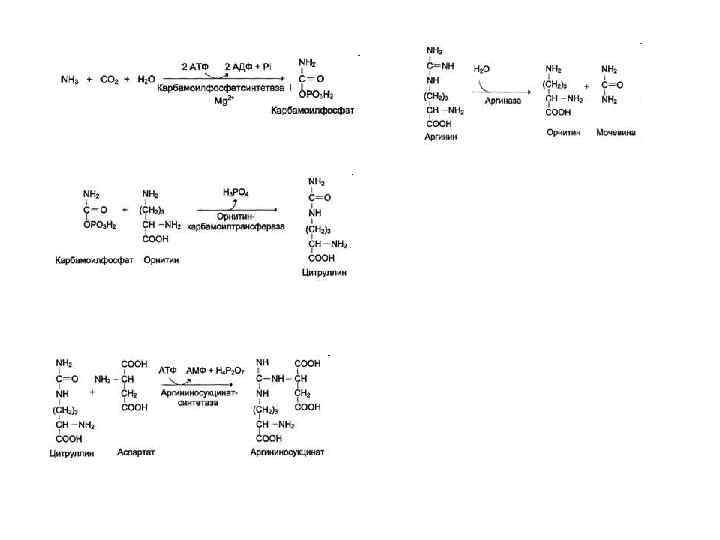
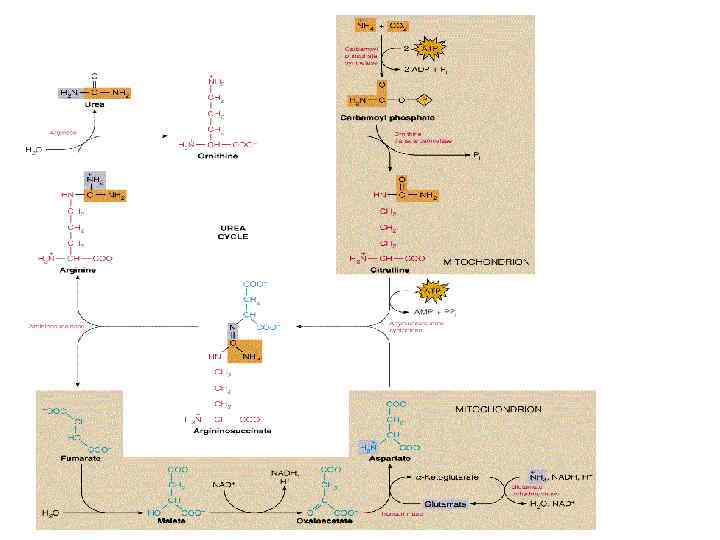
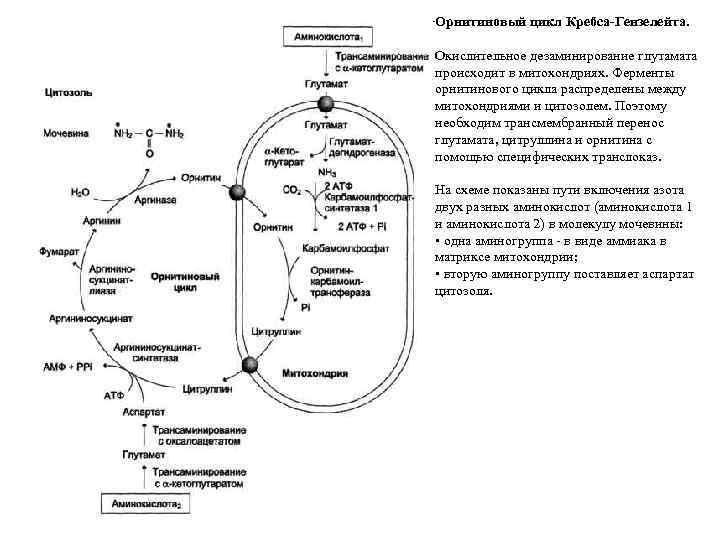 Орнитиновый цикл Кребса-Гензелейта. Окислительное дезаминирование глутамата происходит в митохондриях. Ферменты орнитинового цикла распределены между митохондриями и цитозолем. Поэтому необходим трансмембранный перенос глутамата, цитруллина и орнитина с помощью специфических транслоказ. На схеме показаны пути включения азота двух разных аминокислот (аминокислота 1 и аминокислота 2) в молекулу мочевины: • одна аминогруппа - в виде аммиака в матриксе митохондрии; • вторую аминогруппу поставляет аспартат цитозоля.
Орнитиновый цикл Кребса-Гензелейта. Окислительное дезаминирование глутамата происходит в митохондриях. Ферменты орнитинового цикла распределены между митохондриями и цитозолем. Поэтому необходим трансмембранный перенос глутамата, цитруллина и орнитина с помощью специфических транслоказ. На схеме показаны пути включения азота двух разных аминокислот (аминокислота 1 и аминокислота 2) в молекулу мочевины: • одна аминогруппа - в виде аммиака в матриксе митохондрии; • вторую аминогруппу поставляет аспартат цитозоля.
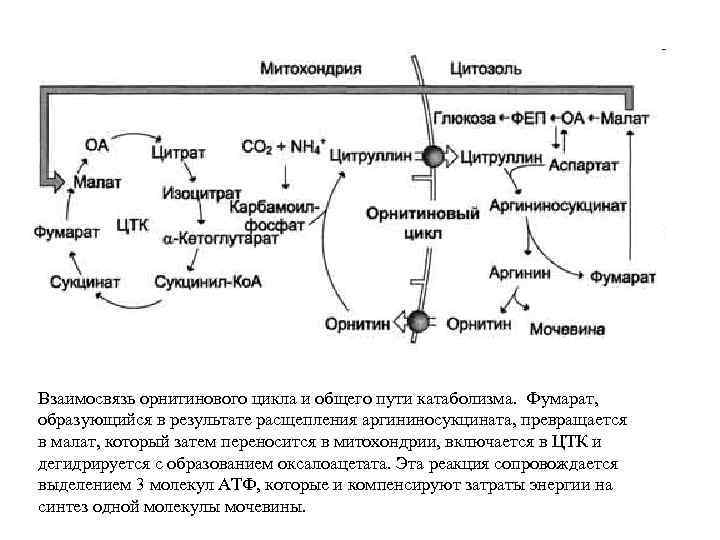 Взаимосвязь орнитинового цикла и общего пути катаболизма. Фумарат, образующийся в результате расщепления аргининосукцината, превращается в малат, который затем переносится в митохондрии, включается в ЦТК и дегидрируется с образованием оксалоацетата. Эта реакция сопровождается выделением 3 молекул АТФ, которые и компенсируют затраты энергии на синтез одной молекулы мочевины.
Взаимосвязь орнитинового цикла и общего пути катаболизма. Фумарат, образующийся в результате расщепления аргининосукцината, превращается в малат, который затем переносится в митохондрии, включается в ЦТК и дегидрируется с образованием оксалоацетата. Эта реакция сопровождается выделением 3 молекул АТФ, которые и компенсируют затраты энергии на синтез одной молекулы мочевины.
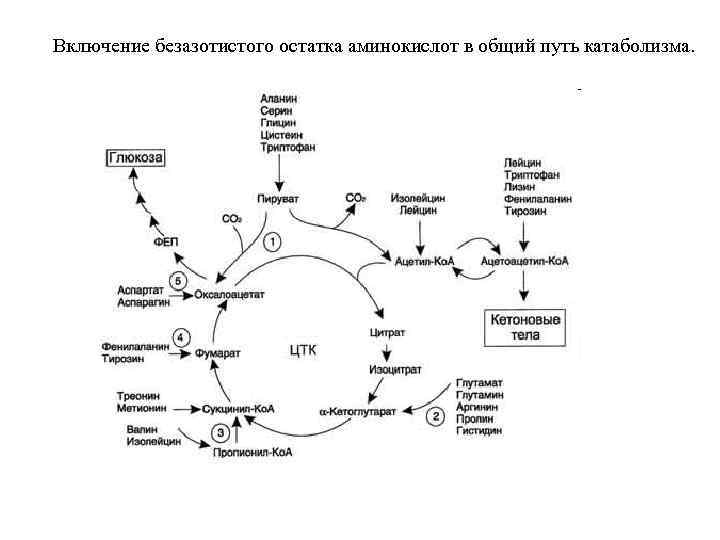 Включение безазотистого остатка аминокислот в общий путь катаболизма.
Включение безазотистого остатка аминокислот в общий путь катаболизма.
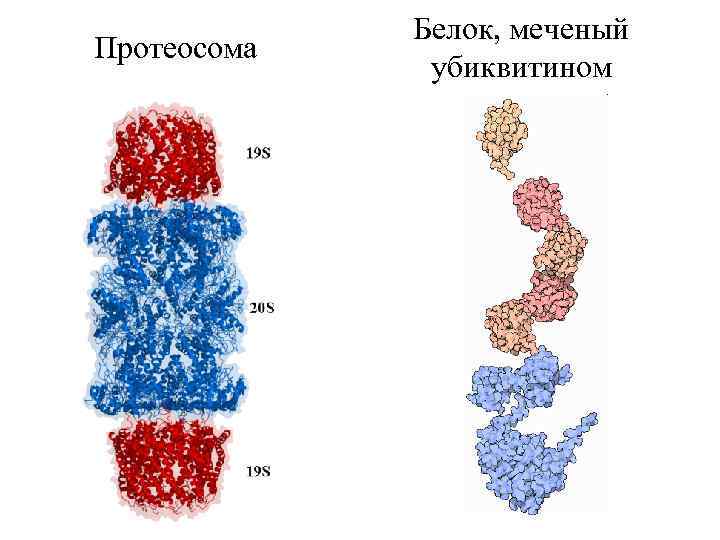 Протеосома Белок, меченый убиквитином
Протеосома Белок, меченый убиквитином
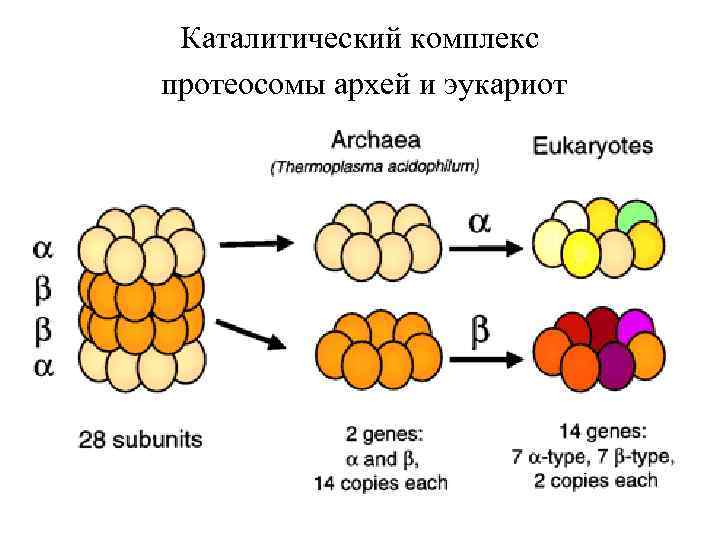 Каталитический комплекс протеосомы архей и эукариот
Каталитический комплекс протеосомы архей и эукариот
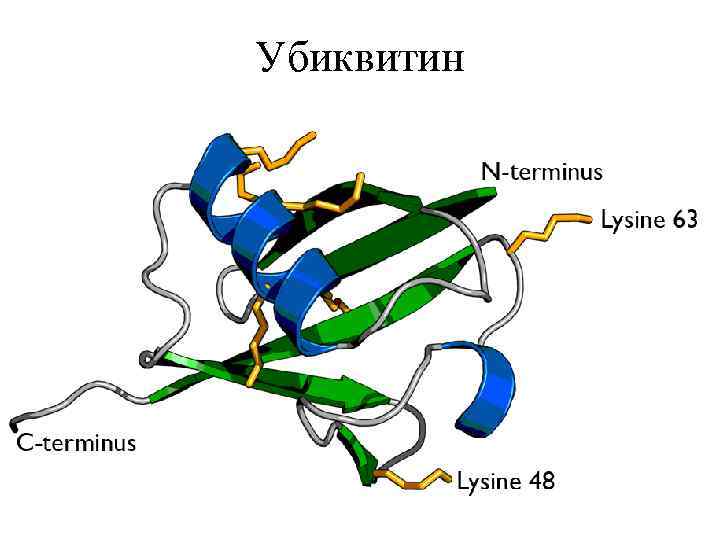 Убиквитин
Убиквитин
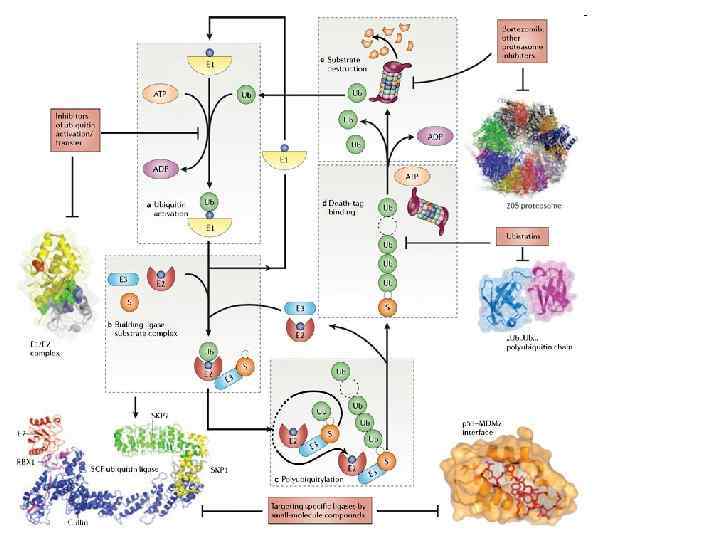
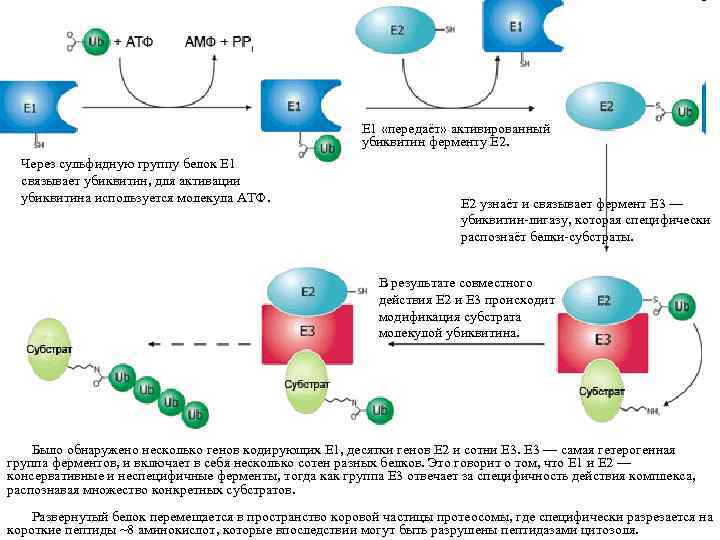 Е 1 «передаёт» активированный убиквитин ферменту Е 2. Через сульфидную группу белок Е 1 связывает убиквитин, для активации убиквитина используется молекула АТФ. Е 2 узнаёт и связывает фермент Е 3 — убиквитин-лигазу, которая специфически распознаёт белки-субстраты. В результате совместного действия Е 2 и Е 3 происходит модификация субстрата молекулой убиквитина. Было обнаружено несколько генов кодирующих Е 1, десятки генов Е 2 и сотни Е 3 — самая гетерогенная группа ферментов, и включает в себя несколько сотен разных белков. Это говорит о том, что Е 1 и Е 2 — консервативные и неспецифичные ферменты, тогда как группа Е 3 отвечает за специфичность действия комплекса, распознавая множество конкретных субстратов. Развернутый белок перемещается в пространство коровой частицы протеосомы, где специфически разрезается на короткие пептиды ~8 аминокислот, которые впоследствии могут быть разрушены пептидазами цитозоля.
Е 1 «передаёт» активированный убиквитин ферменту Е 2. Через сульфидную группу белок Е 1 связывает убиквитин, для активации убиквитина используется молекула АТФ. Е 2 узнаёт и связывает фермент Е 3 — убиквитин-лигазу, которая специфически распознаёт белки-субстраты. В результате совместного действия Е 2 и Е 3 происходит модификация субстрата молекулой убиквитина. Было обнаружено несколько генов кодирующих Е 1, десятки генов Е 2 и сотни Е 3 — самая гетерогенная группа ферментов, и включает в себя несколько сотен разных белков. Это говорит о том, что Е 1 и Е 2 — консервативные и неспецифичные ферменты, тогда как группа Е 3 отвечает за специфичность действия комплекса, распознавая множество конкретных субстратов. Развернутый белок перемещается в пространство коровой частицы протеосомы, где специфически разрезается на короткие пептиды ~8 аминокислот, которые впоследствии могут быть разрушены пептидазами цитозоля.
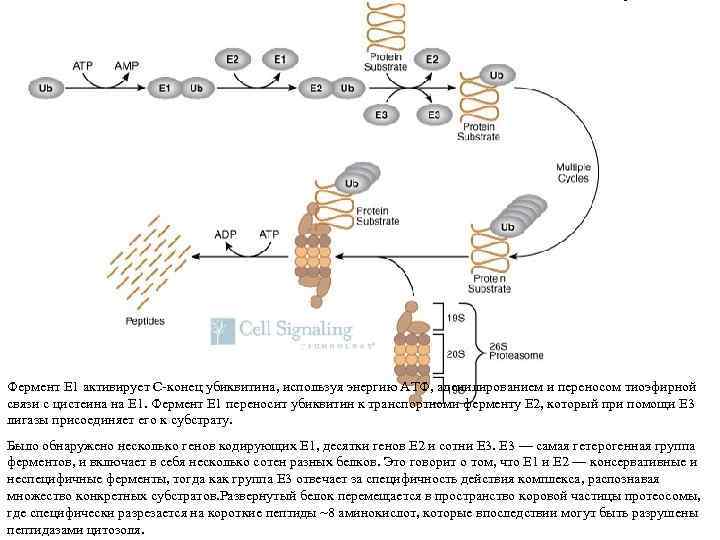 Фермент Е 1 активирует С-конец убиквитина, используя энергию АТФ, аденилированием и переносом тиоэфирной связи с цистеина на E 1. Фермент Е 1 переносит убиквитин к транспортноми ферменту Е 2, который при помощи Е 3 лигазы присоединяет его к субстрату. Было обнаружено несколько генов кодирующих Е 1, десятки генов Е 2 и сотни Е 3 — самая гетерогенная группа ферментов, и включает в себя несколько сотен разных белков. Это говорит о том, что Е 1 и Е 2 — консервативные и неспецифичные ферменты, тогда как группа Е 3 отвечает за специфичность действия комплекса, распознавая множество конкретных субстратов. Развернутый белок перемещается в пространство коровой частицы протеосомы, где специфически разрезается на короткие пептиды ~8 аминокислот, которые впоследствии могут быть разрушены пептидазами цитозоля.
Фермент Е 1 активирует С-конец убиквитина, используя энергию АТФ, аденилированием и переносом тиоэфирной связи с цистеина на E 1. Фермент Е 1 переносит убиквитин к транспортноми ферменту Е 2, который при помощи Е 3 лигазы присоединяет его к субстрату. Было обнаружено несколько генов кодирующих Е 1, десятки генов Е 2 и сотни Е 3 — самая гетерогенная группа ферментов, и включает в себя несколько сотен разных белков. Это говорит о том, что Е 1 и Е 2 — консервативные и неспецифичные ферменты, тогда как группа Е 3 отвечает за специфичность действия комплекса, распознавая множество конкретных субстратов. Развернутый белок перемещается в пространство коровой частицы протеосомы, где специфически разрезается на короткие пептиды ~8 аминокислот, которые впоследствии могут быть разрушены пептидазами цитозоля.
 Классификация протеаз по типу строения активного центра 1. аспартильные (пепсин, ренин, катепсины D, Е и ряд других) 2. серниновые (трипсин, химотрипсин, эластаза, подавляющее большинство протеаз плазмы крови (факторы свертывания крови, фибринолиза, системы комплемента, кининовой системы), многие внутриклеточные и бактериальные протеазы) 3. цистеиновые (катепсины: В, H, L, ряд бактериальных и растительных ферментов, из которых наиболее хорошо изучен папаин) 4. металлопротеазы (чаще всего содержат Zn)(коллагеназа, термолизин) 5. треониновые 6. глютаминовые
Классификация протеаз по типу строения активного центра 1. аспартильные (пепсин, ренин, катепсины D, Е и ряд других) 2. серниновые (трипсин, химотрипсин, эластаза, подавляющее большинство протеаз плазмы крови (факторы свертывания крови, фибринолиза, системы комплемента, кининовой системы), многие внутриклеточные и бактериальные протеазы) 3. цистеиновые (катепсины: В, H, L, ряд бактериальных и растительных ферментов, из которых наиболее хорошо изучен папаин) 4. металлопротеазы (чаще всего содержат Zn)(коллагеназа, термолизин) 5. треониновые 6. глютаминовые
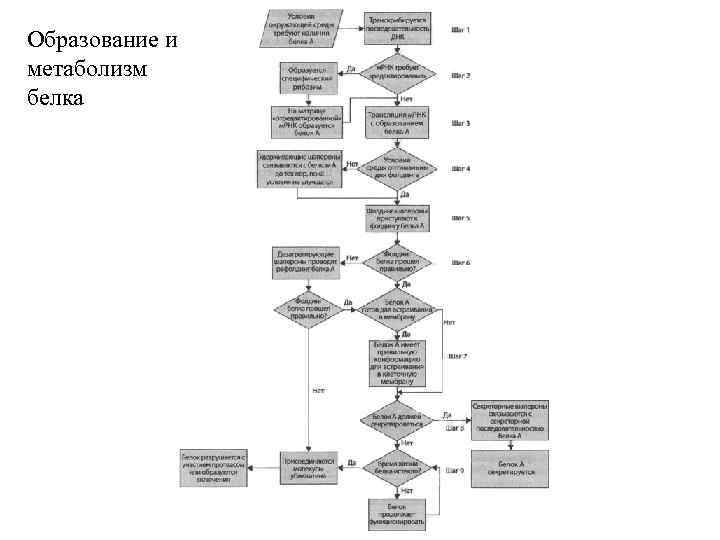 Образование и метаболизм белка
Образование и метаболизм белка


