COJ-lek03-2006 Белки.ppt
- Количество слайдов: 79

ПЕПТИДЫ И БЕЛКИ Спирали встречаются во многих областях: в архитектуре, в макромолекулах белков, нуклеиновых кислот и даже в полисахаридах (Loretto Chapel, Santa Fe, 1 NM/© Sarbo )

ОБЩИЕ СВЕДЕНИЯ О БЕЛКАХ У каждого вида организмов имеются тысячи различных белков, а число самих видов, вероятно, составляет около 10 миллионов. Можно ли всего из 20 аминокислот построить, скажем, 1011 (или более) различных последовательностей? Дипептид – 2 изомера Трипептид (из трех аминокислот – А, В и С) – 3!=1· 2· 3=6 изомеров (ABC, АСВ, ВАС, ВСА, CAB и СВА) 2

ОБЩИЕ СВЕДЕНИЯ О БЕЛКАХ Тетрапептид - 4! = 4· 3· 2· 1=24 различные последовательности Полипептида из 20 различных аминокислот – 20!≈2· 1018 изомеров (Mr ≈2600). Белок с Mr ≈34000, состоящий из 12 аминокислот в равных соотношениях, имеет 10300 возможных последовательностей. 3

ОБЩИЕ СВЕДЕНИЯ О БЕЛКАХ Garrett R. H. , Grisham C. M. Biochemistry. 2 ed. , 1999. 851 s. 4

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ 5

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ Garrett R. H. , Grisham C. M. Biochemistry. 2 ed. , 1999. 851 s. 6

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ 7
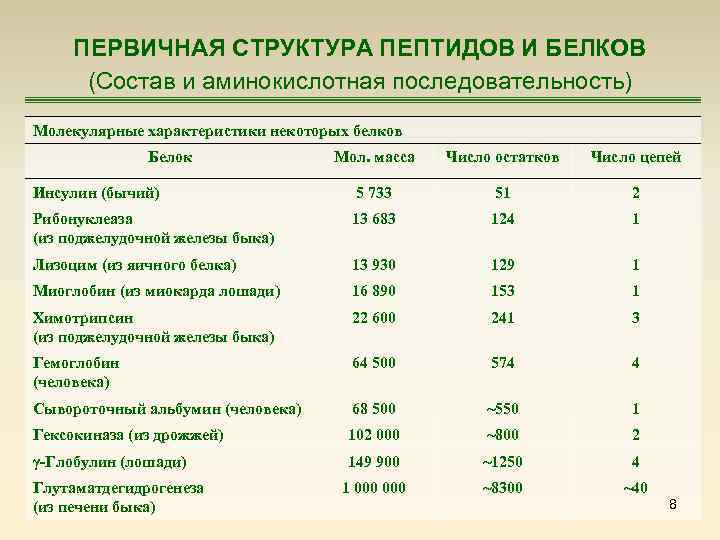
ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Состав и аминокислотная последовательность) Молекулярные характеристики некоторых белков Белок Мол. масса Число остатков Число цепей Инсулин (бычий) 5 733 51 2 Рибонуклеаза (из поджелудочной железы быка) 13 683 124 1 Лизоцим (из яичного белка) 13 930 129 1 Миоглобин (из миокарда лошади) 16 890 153 1 Химотрипсин (из поджелудочной железы быка) 22 600 241 3 Гемоглобин (человека) 64 500 574 4 Сывороточный альбумин (человека) 68 500 ~550 1 Гексокиназа (из дрожжей) 102 000 ~800 2 γ-Глобулин (лошади) 149 900 ~1250 4 1 000 ~8300 ~40 Глутаматдегидрогенеза (из печени быка) 8

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Выделение и очистка белков) Диализ Мембрана, окружающая раствор белка, свободно пропускает воду и низкомолекулярные соединения, такие, как Na. Cl или глюкоза, но не пропускает большие молекулы в частности молекулы белка. Малые молекулы диффундируют из диализного мешочка во внешний сосуд, так как в процессе диффузии молекулы стремятся перейти в зону с более низкой концентрацией. Заменяя несколько раз водную фазу во внешнем сосуде на дистиллированную воду, можно снизить концентрацию низкомолекулярных соединений в растворе белка до сколь угодно малой величины. Garrett R. H. , Grisham C. M. Biochemistry. 2 ed. , 1999. 851 s. 9

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Выделение и очистка белков) Гель-фильтрация Разделение белков в соответствии с размерами их молекул методом гельфильтрации. Раствор, содержащий смесь белков, пропускают через колонку, заполненную очень мелкими пористыми гранулами гидрофильного полимера: широко используют для этой цели производные декстрана. Молекулы малых белков проникают внутрь гранул, тогда как более крупные молекулы не могут туда проникнуть. Молекулярную массу белка можно определить путем сравнения скорости его прохождения через колонку со скоростями прохождения других белков с известными молекулярными массами. Garrett R. H. , Grisham C. M. Biochemistry. 2 ed. , 1999. 851 s. 10

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Выделение и очистка белков) Гель-электрофорез Garrett R. H. , Grisham C. M. Biochemistry. 2 ed. , 1999. 851 s. 11

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 1: Определение аминокислотного состава 12
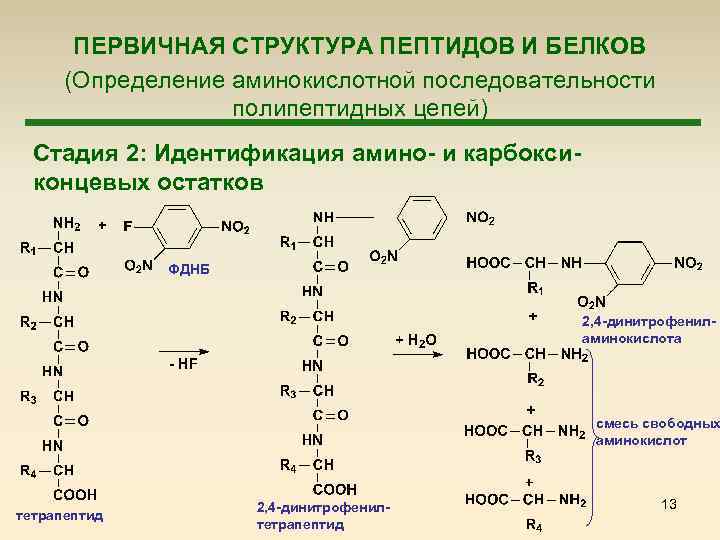
ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 2: Идентификация амино- и карбоксиконцевых остатков ФДНБ 2, 4 -динитрофениламинокислота смесь свободных аминокислот тетрапептид 2, 4 -динитрофенилтетрапептид 13
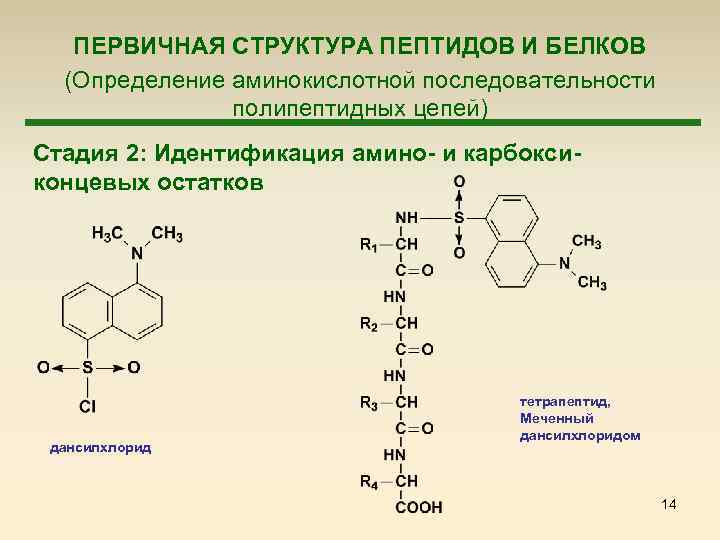
ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 2: Идентификация амино- и карбоксиконцевых остатков дансилхлорид тетрапептид, Меченный дансилхлоридом 14

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 3: Расщепление полипептидной цепи на фрагменты Специфичность, свойственная четырем важным методам фрагментации полипептидных цепей Обработка Точки расщепления (остатки, которым принадлежит карбонильная группа расщепляемой пептидной связи) Трипсин Лизин Аргинин Химотрипсин Фенилаланин Триптофан Тирозин Пепсин Фенилаланин Триптофан Тирозин Некоторые другие остатки Бромциан Метионин 15

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 3: Расщепление полипептидной цепи на фрагменты Garrett R. H. , Grisham C. M. Biochemistry. 2 ed. , 1999. 851 s. 16

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 3: Расщепление полипептидной цепи на фрагменты Активный центр химотрипсина а) в отсутствии субстрата 17

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 3: Расщепление полипептидной цепи на фрагменты Активный центр химотрипсина б) в присутствии субстрата 18

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 3: Расщепление полипептидной цепи на фрагменты Расщепление пептидной связи (стадия ацилирования) 19

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 3: Расщепление полипептидной цепи на фрагменты Стадия деацилирования 20
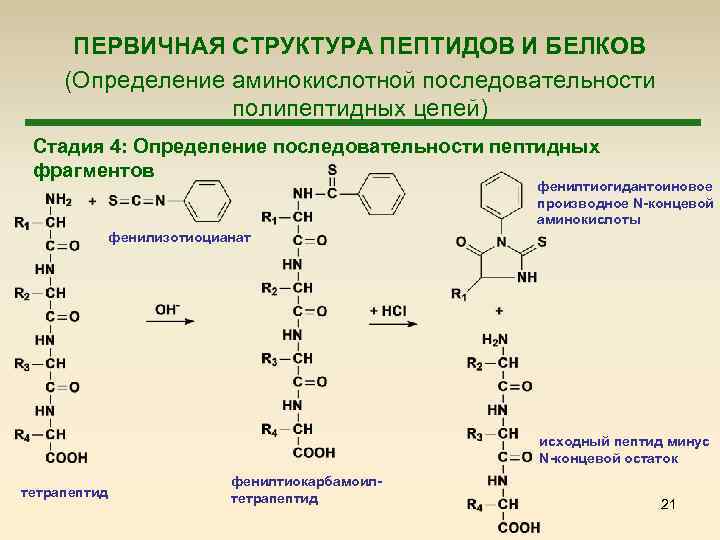
ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 4: Определение последовательности пептидных фрагментов фенилтиогидантоиновое производное N-концевой аминокислоты фенилизотиоцианат исходный пептид минус N-концевой остаток тетрапептид фенилтиокарбамоилтетрапептид 21

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 4: Определение последовательности пептидных фрагментов Garrett R. H. , Grisham C. M. Biochemistry. 2 ed. , 1999. 851 s. 22

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 5: Расщепление исходной полипептидной цепи еще одним способом Garrett R. H. , Grisham C. M. Biochemistry. 2 ed. , 1999. 851 s. 23

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Стадия 6: Установление порядка расположения пептидных фрагментов по перекрывающимся участкам Garrett R. H. , Grisham C. M. Biochemistry. 2 ed. , 1999. 851 s. 24

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) 25

ПЕРВИЧНАЯ СТРУКТУРА ПЕПТИДОВ И БЕЛКОВ (Определение аминокислотной последовательности полипептидных цепей) Аминокислотная последовательность, т. е. порядок чередования -аминокислотных остатков, составляет первичную структуру пептидов и белков. 26

СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ 27

СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ Дипептиды Каркозин ( -аланил-L-гистидин) Ансерин 28 ( -аланил-N-метил-L-гистидин)

СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ Трипептиды 29

СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ Трипептиды 30

СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ Пептидные антибиотики Bacillus brevis Г. Ф. Граузе и М. Г. Бражникова (1942) L-орнитин 31

СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ Пептидные гормоны В. Дю Виньо (1953 г. ) 32
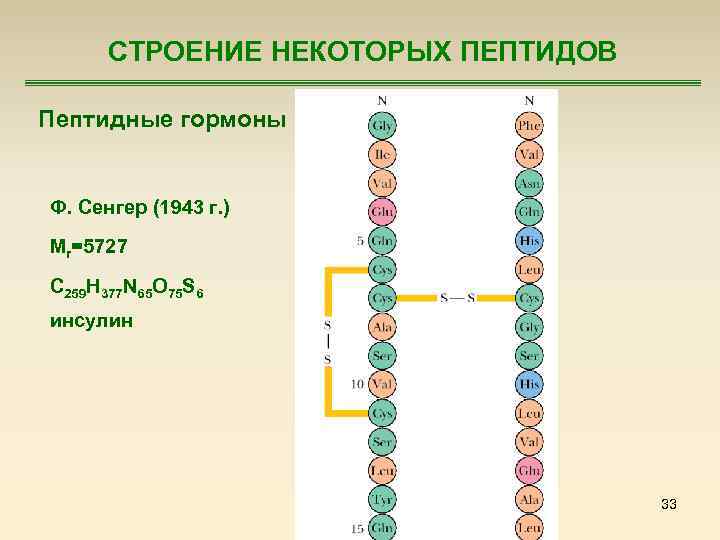
СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ Пептидные гормоны Ф. Сенгер (1943 г. ) Mr=5727 С 259 Н 377 N 65 O 75 S 6 инсулин 33

СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ Пептидные токсины 34

СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ Нейропептиды 35

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ 36

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ 37

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Синтез дипептида аланилвалина 1 -ый компонент – Аланин Защита NH 2 -группы: 38

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Синтез дипептида аланилвалина 1 -ый компонент – Аланин Активация COOH-группы: 39

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Синтез дипептида аланилвалина 2 -ый компонент – Валин Защита COOH-группы: 40

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Синтез дипептида аланилвалина Образование амидной связи 41
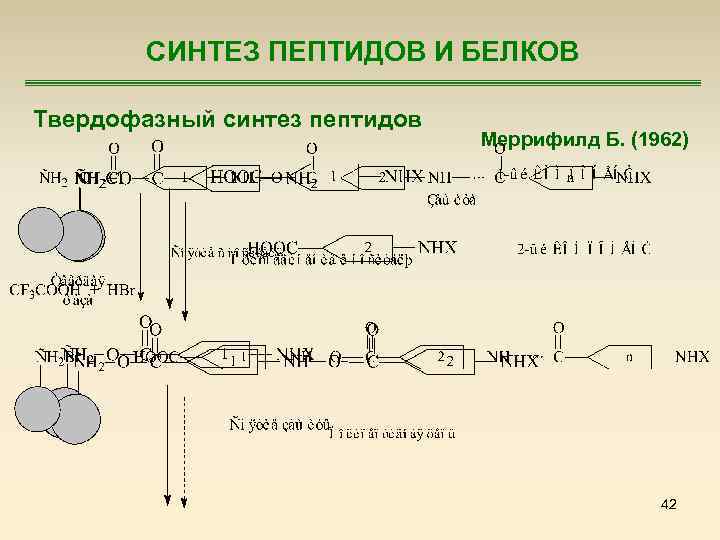
СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Твердофазный синтез пептидов Меррифилд Б. (1962) 42

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Твердофазный синтез пептидов Меррифилд Б. (1962) Garrett R. H. , Grisham C. M. Biochemistry. 2 ed. , 1999. 851 s. 43

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Твердофазный синтез пептидов Меррифилд Б. (1962) Этим методом были синтезированы цепи А и Б инсулина (1967), апоферритин (1968), рибонуклеаза А (1969). В синтезе рибонуклеазы были соединены 124 аминокислотных остатка, что потребовало проведения 369 химических реакций и 1131 автоматических операций (промывки и т. п. ) без промежуточного выделения продуктов. ЖИДКОФАЗНЫЙ СИНТЕЗ Акад. М. М. Шемякин 44

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Applied Biosystems model 430 A peptide synthesizer 45

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Biosearch Peptide Synthesizer (New Brunswick) model 9600 46

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ ABI model 431 a peptide synthesizer, made by applied Biosystems 47

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Applied Biosystems 433 A Peptide Synthesizer 48

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Applied Biosystems 433 A Peptide Synthesizer 49

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Applied Biosystems 433 A Peptide Synthesizer 50

СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Applied Biosystems 433 A Peptide Synthesizer 51
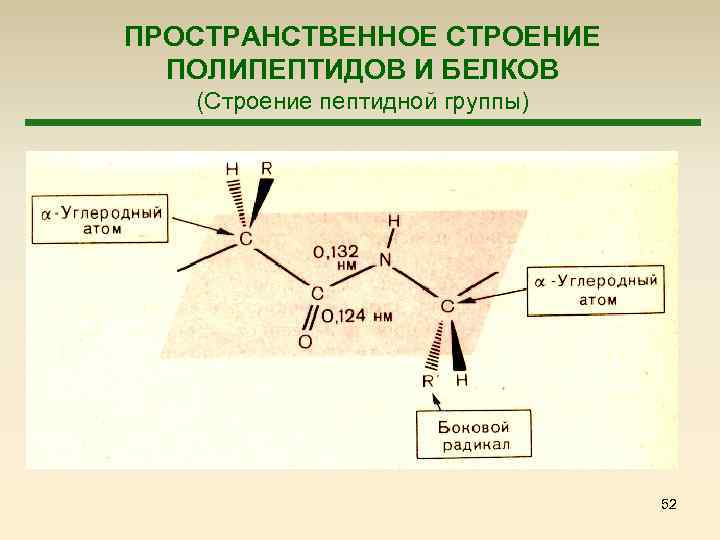
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Строение пептидной группы) 52

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Строение пептидной группы) Garrett R. H. , Grisham C. M. Biochemistry. 2 ed. , 1999. 851 s. 53

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Строение пептидной группы) 54

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Строение пептидной группы) Garrett R. H. , Grisham C. M. Biochemistry. 2 ed. , 1999. 851 s. 55
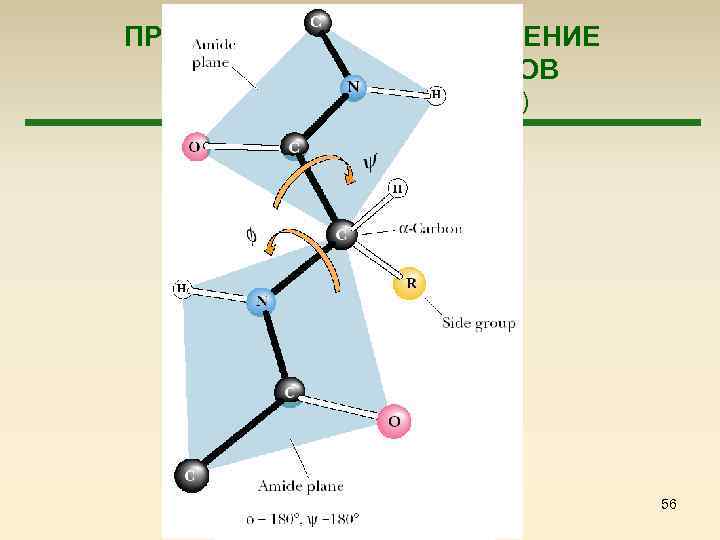
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Строение пептидной группы) 56
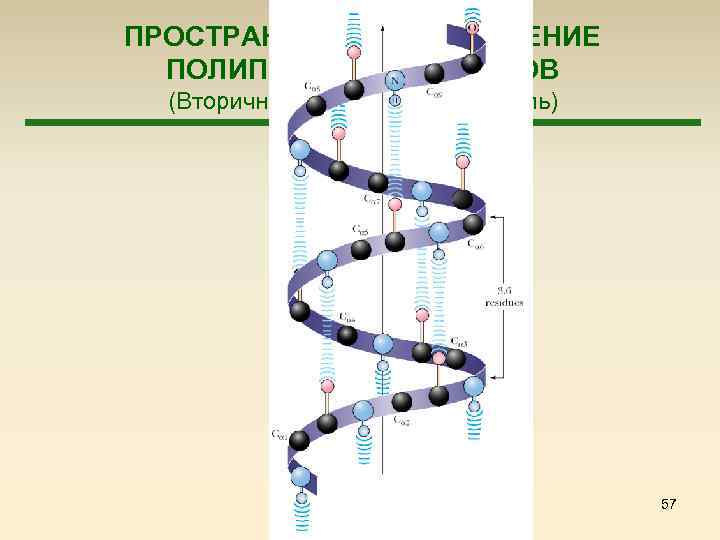
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Вторичная структура – α-спираль) 57

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Вторичная структура – α-спираль) 58
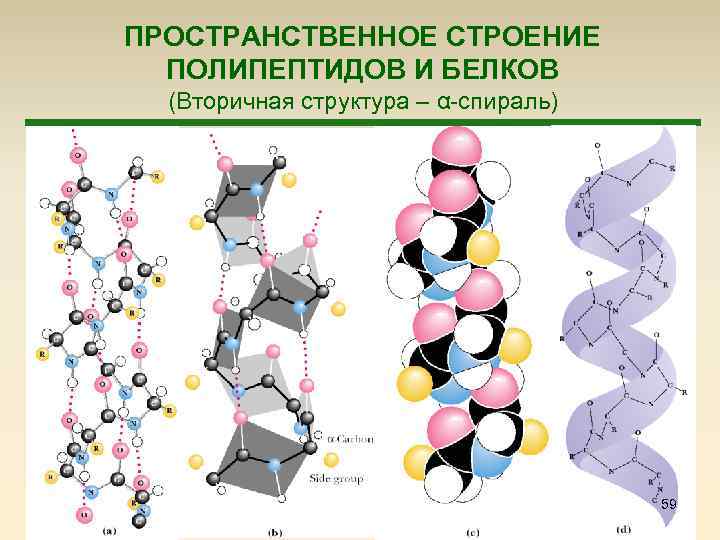
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Вторичная структура – α-спираль) 59
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Вторичная структура – α-спираль) 60
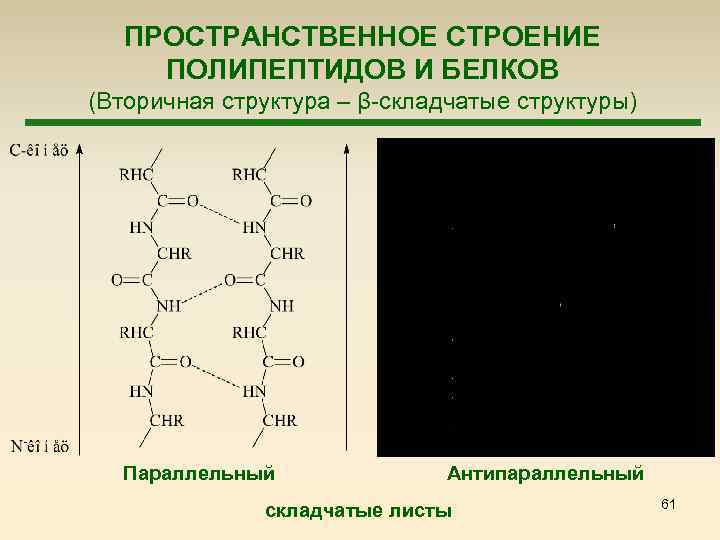
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Вторичная структура – β-складчатые структуры) Параллельный Антипараллельный складчатые листы 61
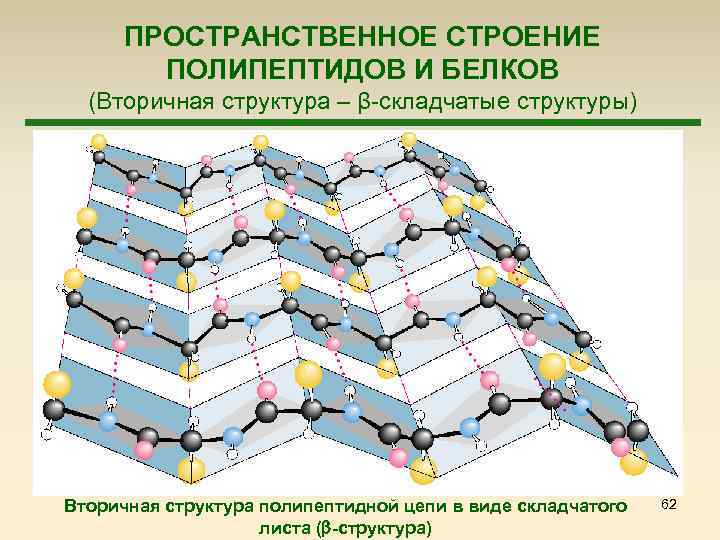
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Вторичная структура – β-складчатые структуры) Вторичная структура полипептидной цепи в виде складчатого листа ( -структура) 62
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Вторичная структура – β-складчатые структуры) 63

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Третичная структура) Фибрилярные белки Глобулярные белки 64

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Третичная структура) 65

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Третичная структура) 66

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Третичная структура) 67

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Фибриллярные белки) Коллаген 68

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Фибриллярные белки) Модель строения спирали коллагена 69

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Фибриллярные белки) "Сшивание" тропоколлагеновых цепей в коллагене 70

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Фибриллярные белки) "Сшивание" тропоколлагеновых цепей в коллагене 71
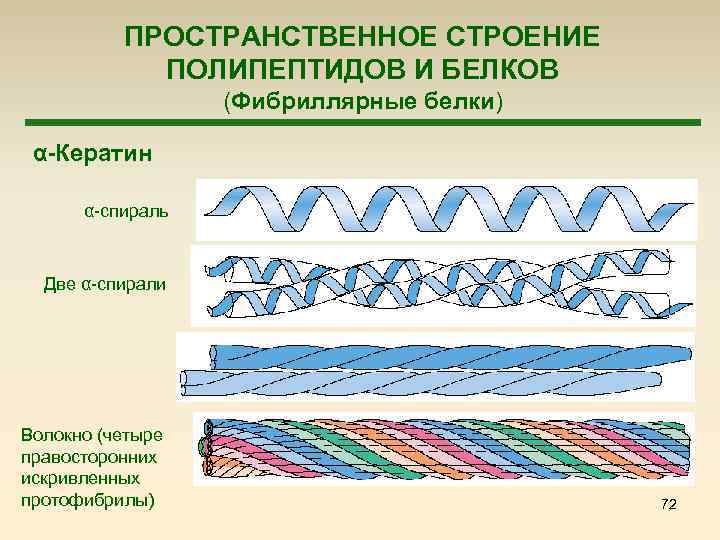
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Фибриллярные белки) α-Кератин α-спираль Две α-спирали Волокно (четыре правосторонних искривленных протофибрилы) 72
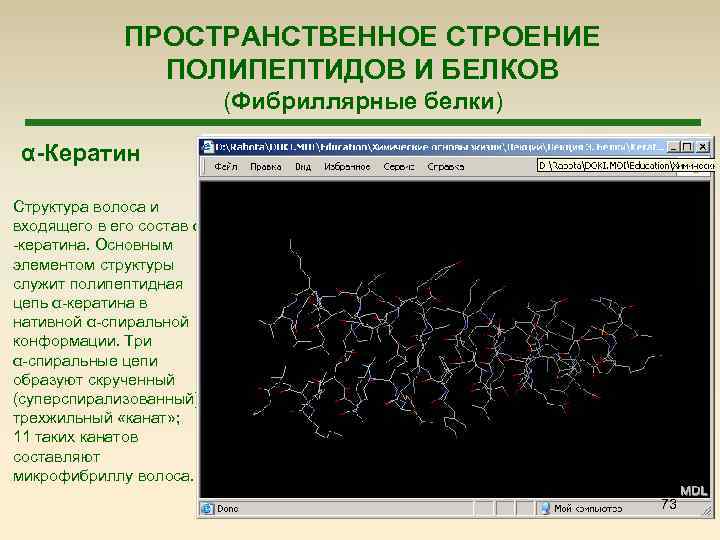
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Фибриллярные белки) α-Кератин Структура волоса и входящего в его состав α -кератина. Основным элементом структуры служит полипептидная цепь α-кератина в нативной α-спиральной конформации. Три α-спиральные цепи образуют скрученный (суперспирализованный) трехжильный «канат» ; 11 таких канатов составляют микрофибриллу волоса. 73

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Фибриллярные белки) β-Кератин фиброин β-Конформация полипептидных цепей в βкератинах. А. Три цепи, образующие складчатый слой (вид сверху); показано расположение поперечных водородных связей между соседними цепями. R-группы выделены красным цветом. Б. Та же структура (вид сбоку): показано расположение R-групп, выступающих по обе стороны складчатого слоя. 74
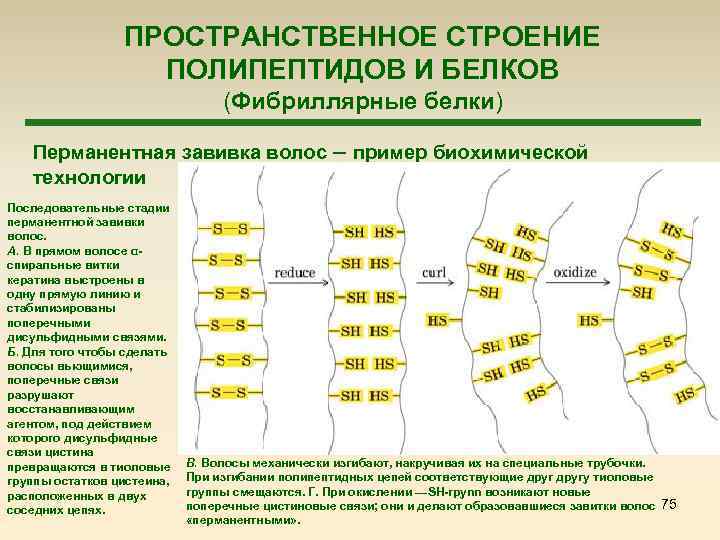
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Фибриллярные белки) Перманентная завивка волос – пример биохимической технологии Последовательные стадии перманентной завивки волос. А. В прямом волосе αспиральные витки кератина выстроены в одну прямую линию и стабилизированы поперечными дисульфидными связями. Б. Для того чтобы сделать волосы вьющимися, поперечные связи разрушают восстанавливающим агентом, под действием которого дисульфидные связи цистина превращаются в тиоловые группы остатков цистеина, расположенных в двух соседних цепях. В. Волосы механически изгибают, накручивая их на специальные трубочки. При изгибании полипептидных цепей соответствующие другу тиоловые группы смещаются. Г. При окислении —SH-rpynn возникают новые поперечные цистиновые связи; они и делают образовавшиеся завитки волос 75 «перманентными» .
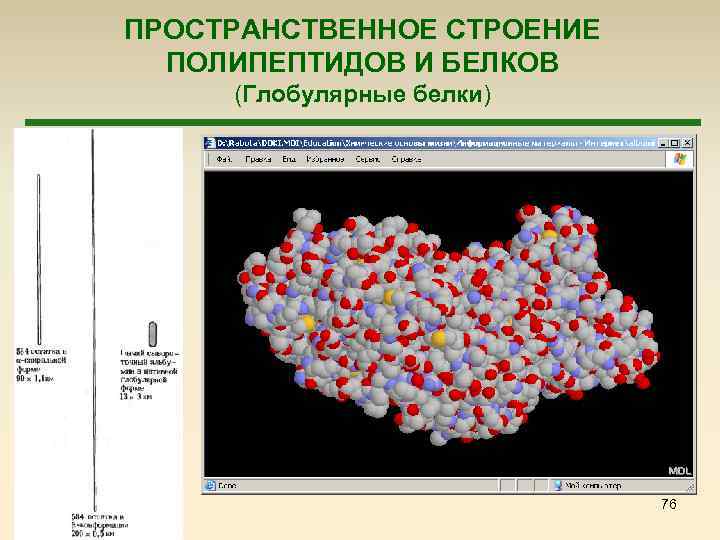
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Глобулярные белки) 76

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Глобулярные белки) Лизоцим 1965 г. 129 аминокислотных остатков Mr = 14 600 77

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Денатурация и ренатурация) 78
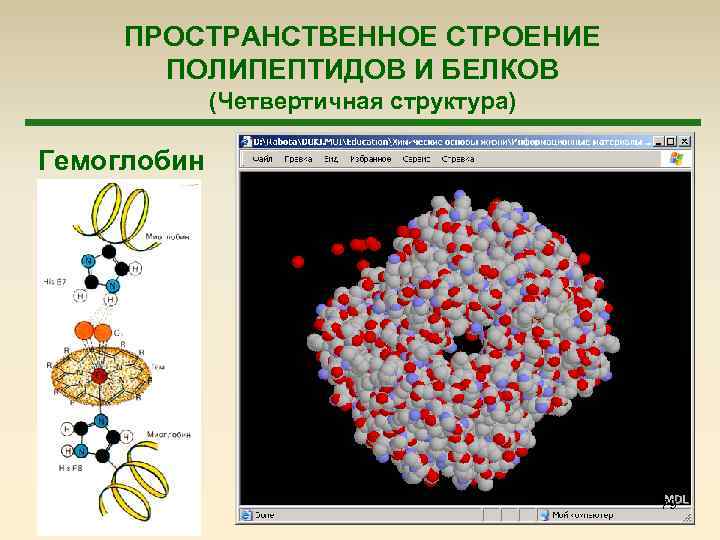
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ (Четвертичная структура) Гемоглобин 79
COJ-lek03-2006 Белки.ppt