Лекция 3 Пентозный цикл.pptx
- Количество слайдов: 112
 ПЕНТОЗНЫЙ ЦИКЛ
ПЕНТОЗНЫЙ ЦИКЛ
 Глюконеогенез • Мозг, эритроциты и некоторые другие ткани требуют постоянно глюкозу • Если с пищей и за счет расщепления гликогена глюкозы не хватает, то активируется глюконеогенез – синтез глюкозы новой • Глюконеогенез идет в печени и почечных канальцах синтезируется до 250 г глюкозы в сутки. • Процесс идет в цитоплазме, митохондриях, эндоплазматической сети
Глюконеогенез • Мозг, эритроциты и некоторые другие ткани требуют постоянно глюкозу • Если с пищей и за счет расщепления гликогена глюкозы не хватает, то активируется глюконеогенез – синтез глюкозы новой • Глюконеогенез идет в печени и почечных канальцах синтезируется до 250 г глюкозы в сутки. • Процесс идет в цитоплазме, митохондриях, эндоплазматической сети
 Факторы, влияющие на глюконеогенез Усиливают: • Субстраты 1. лактат (молочная кислота) из мышечной ткани и эритроцитов 2. аминокислоты из ЖКТ (глюкогенные) и аланин из мышц 3. глицерин из жиров ткани 4. оксалоацетат 5. пируват • Гормоны кортизол, глюкагон, адреналин • Ферменты те же, что и в гликолизе
Факторы, влияющие на глюконеогенез Усиливают: • Субстраты 1. лактат (молочная кислота) из мышечной ткани и эритроцитов 2. аминокислоты из ЖКТ (глюкогенные) и аланин из мышц 3. глицерин из жиров ткани 4. оксалоацетат 5. пируват • Гормоны кортизол, глюкагон, адреналин • Ферменты те же, что и в гликолизе
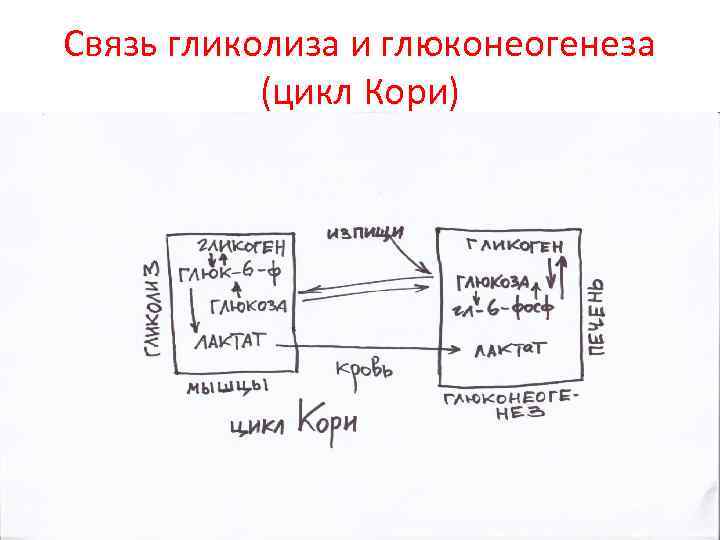 Связь гликолиза и глюконеогенеза (цикл Кори)
Связь гликолиза и глюконеогенеза (цикл Кори)
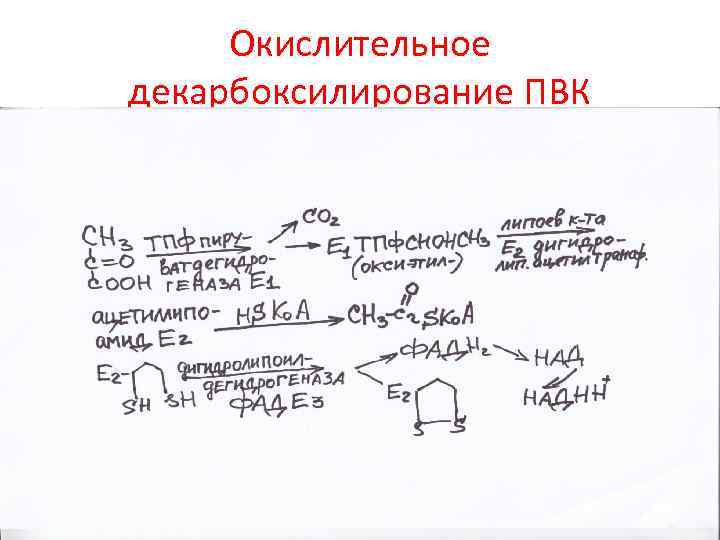 Окислительное декарбоксилирование ПВК
Окислительное декарбоксилирование ПВК
 Состав мультиферментного комплекса окисления ПВК • 3 фермента пируватдегидрогеназа, дигидролипоилтрансфераза, дигидролипоилдегидрогеназа • 5 коферментов ТПФ, липоевая кислота (Е 2), коэнзим А, ФАД (Е 3), НАД
Состав мультиферментного комплекса окисления ПВК • 3 фермента пируватдегидрогеназа, дигидролипоилтрансфераза, дигидролипоилдегидрогеназа • 5 коферментов ТПФ, липоевая кислота (Е 2), коэнзим А, ФАД (Е 3), НАД
 Пентозный цикл (он же апотомический, фосфоглюконатный, пентозофосфатный) • • Это распад глюкозы с отщеплением первого атома углерода в виде СО 2 (в цитоплазме) Роль процесса: Синтез НАДФН для использования его в синтезе жирных кислот и холестерина. Синтез пентоз для нуклеиновых кислот и коферментов Синтез НАДФН для монооксигеназных реакций и др. процессов. Возможность переключения пентозного пути на энергетическую функцию
Пентозный цикл (он же апотомический, фосфоглюконатный, пентозофосфатный) • • Это распад глюкозы с отщеплением первого атома углерода в виде СО 2 (в цитоплазме) Роль процесса: Синтез НАДФН для использования его в синтезе жирных кислот и холестерина. Синтез пентоз для нуклеиновых кислот и коферментов Синтез НАДФН для монооксигеназных реакций и др. процессов. Возможность переключения пентозного пути на энергетическую функцию
 Особенности пентозного пути • Есть окислительная стадия и (при необходимости) восстановительная (поэтому цикл) • В основном идет в печени, надпочечниках, эмбриональной ткани, молочной железе, семенниках, лейкоцитах, жировой ткани. • Значение пентозного цикла возрастает в растущих, делящихся клетках, детском возрасте, восстановлении после болезней, кровопотерь и т. п.
Особенности пентозного пути • Есть окислительная стадия и (при необходимости) восстановительная (поэтому цикл) • В основном идет в печени, надпочечниках, эмбриональной ткани, молочной железе, семенниках, лейкоцитах, жировой ткани. • Значение пентозного цикла возрастает в растущих, делящихся клетках, детском возрасте, восстановлении после болезней, кровопотерь и т. п.
 • Цикл не ведет к синтезу АТФ и протекает анаэробно, но при необходимости через глицероальдегидфосфат из второй части процесса есть связь с гликолизом, а значит освобождением энергии и синтеза АТФ (через ПВК и ацетил-Ко. А). • На гликолиз из пентозного пути может переключиться и фруктозо-6 -фосфат, получающийся во второй стадии цикла. • Пентозный цикл зависит от кислорода: мало кислорода, значит мало АТФ, значит замедление синтезов, а значит и снижение апотомического распада глюкозы.
• Цикл не ведет к синтезу АТФ и протекает анаэробно, но при необходимости через глицероальдегидфосфат из второй части процесса есть связь с гликолизом, а значит освобождением энергии и синтеза АТФ (через ПВК и ацетил-Ко. А). • На гликолиз из пентозного пути может переключиться и фруктозо-6 -фосфат, получающийся во второй стадии цикла. • Пентозный цикл зависит от кислорода: мало кислорода, значит мало АТФ, значит замедление синтезов, а значит и снижение апотомического распада глюкозы.
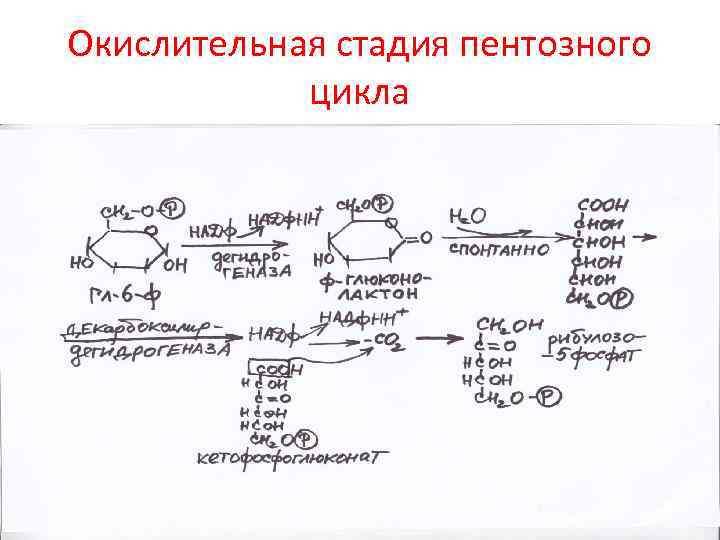 Окислительная стадия пентозного цикла
Окислительная стадия пентозного цикла
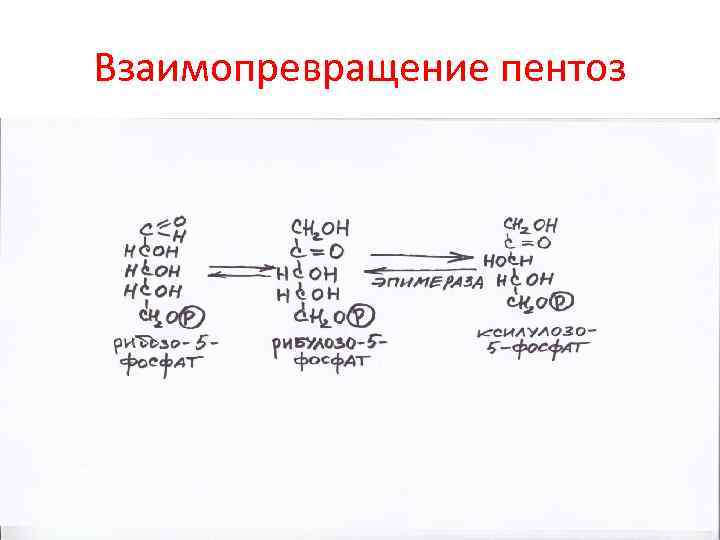 Взаимопревращение пентоз
Взаимопревращение пентоз
 Реакции второй (неокислительной) стадии пентозного цикла
Реакции второй (неокислительной) стадии пентозного цикла
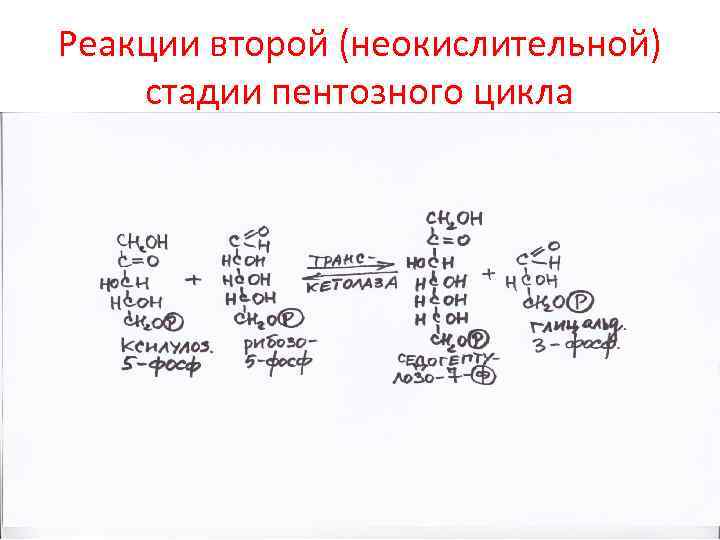 Реакции второй (неокислительной) стадии пентозного цикла
Реакции второй (неокислительной) стадии пентозного цикла
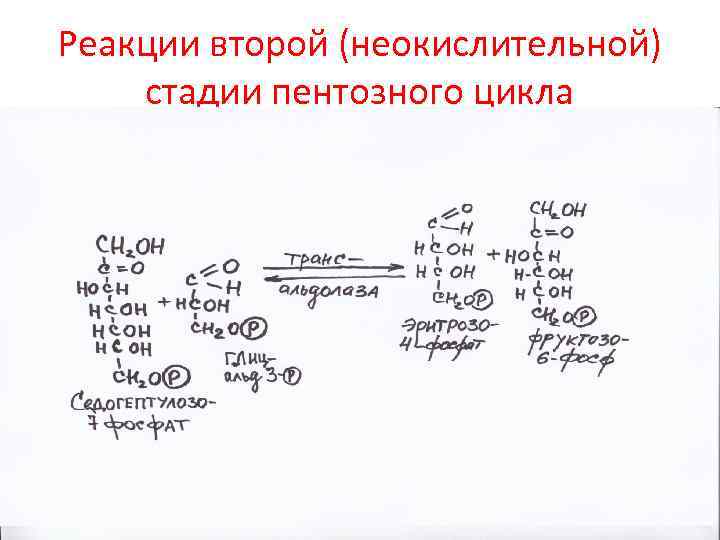 Реакции второй (неокислительной) стадии пентозного цикла
Реакции второй (неокислительной) стадии пентозного цикла
 Патология углеводного обмена.
Патология углеводного обмена.
 Регуляция обмена углеводов (А) • • • В основе – регуляция активности ферментов (концентрациями субстратов, продуктами, кислородом, ингибиторами и т. п. ) Гликолиз регулируется гексокиназой, фруктокиназой, пируваткиназой, ингибируется АТФ и цитратом, активируется АМФ Интенсивность цикла Кребса зависит от потребности в АТФ Активация гликолиза приводит к снижению активности глюконеогенеза и наоборот Низкая глюкоза крови (3, 4 ммоля) возбуждает ЦНС (гипоталамус), что продуцирует гормоны и активирует мобилизацию гликогена Соотношение НАДН – НАДФН координирует взаимодействие гликолитического и пентозного пути глюкозы
Регуляция обмена углеводов (А) • • • В основе – регуляция активности ферментов (концентрациями субстратов, продуктами, кислородом, ингибиторами и т. п. ) Гликолиз регулируется гексокиназой, фруктокиназой, пируваткиназой, ингибируется АТФ и цитратом, активируется АМФ Интенсивность цикла Кребса зависит от потребности в АТФ Активация гликолиза приводит к снижению активности глюконеогенеза и наоборот Низкая глюкоза крови (3, 4 ммоля) возбуждает ЦНС (гипоталамус), что продуцирует гормоны и активирует мобилизацию гликогена Соотношение НАДН – НАДФН координирует взаимодействие гликолитического и пентозного пути глюкозы
 Регуляция обмена углеводов (Б) • Преимущество аэробного пути в тканях сердечной мышцы и почек обеспечивается тем, что ЛДГ 1 и ЛДГ 2 в этих тканях ингибируется ПВК и она, не превращаясь в лактат, идет в цикл Кребса. А для ЛДГ 4 и ЛДГ 5 в скелетных мышцах ингибирования со стороны ПВК не наблюдается и легко образуется лактат. • В печени активность глюкокиназы в 10 раз превышает активность гексокиназы, к тому же глюкокиназа имеет высокое значение Км, что практически выравнивает содержание глюкозы в крови и в печени. Глюкокиназа не ингибируется глюкозо-6 фосфатом.
Регуляция обмена углеводов (Б) • Преимущество аэробного пути в тканях сердечной мышцы и почек обеспечивается тем, что ЛДГ 1 и ЛДГ 2 в этих тканях ингибируется ПВК и она, не превращаясь в лактат, идет в цикл Кребса. А для ЛДГ 4 и ЛДГ 5 в скелетных мышцах ингибирования со стороны ПВК не наблюдается и легко образуется лактат. • В печени активность глюкокиназы в 10 раз превышает активность гексокиназы, к тому же глюкокиназа имеет высокое значение Км, что практически выравнивает содержание глюкозы в крови и в печени. Глюкокиназа не ингибируется глюкозо-6 фосфатом.
 Сахарный диабет Широко распространенное заболевание, которое наблюдается при абсолютном или относительном дефиците инсулина. Страдает обмен углеводов и липидов. Диабет встречается в 2 -х формах: 1 типа (инсулинзависимый) – уже в раннем возрасте происходит гибель инсулинсинтезирующих клеток. Менее тяжелый диабет 2 типа (инсулиннезависимый) проявляется в пожилом возрасте. Причины разные: снижение секреции инсулина, нарушение рецепторной функции клеток-мишеней. Опасен осложнениями. Парализует работу жизненно важных систем и органов.
Сахарный диабет Широко распространенное заболевание, которое наблюдается при абсолютном или относительном дефиците инсулина. Страдает обмен углеводов и липидов. Диабет встречается в 2 -х формах: 1 типа (инсулинзависимый) – уже в раннем возрасте происходит гибель инсулинсинтезирующих клеток. Менее тяжелый диабет 2 типа (инсулиннезависимый) проявляется в пожилом возрасте. Причины разные: снижение секреции инсулина, нарушение рецепторной функции клеток-мишеней. Опасен осложнениями. Парализует работу жизненно важных систем и органов.
 Причины диабета • Снижение продукции инсулина (не всегда ясны мотивы) • Нарушено превращение проинсулина в инсулин • Избыточное образование диабетогенных метаболитов (триптофана) • Врожденное или приобретенное снижение количества инсулиновых рецепторов • Блокирование рецепторов антителами • Продукция генетически измененного инсулина с низкой активностью • Наличие антагонистов инсулина • Увеличение содержание белковосвязанного инсулина и уменьшение свободного (активного)
Причины диабета • Снижение продукции инсулина (не всегда ясны мотивы) • Нарушено превращение проинсулина в инсулин • Избыточное образование диабетогенных метаболитов (триптофана) • Врожденное или приобретенное снижение количества инсулиновых рецепторов • Блокирование рецепторов антителами • Продукция генетически измененного инсулина с низкой активностью • Наличие антагонистов инсулина • Увеличение содержание белковосвязанного инсулина и уменьшение свободного (активного)
 Симптомы диабета • Гипергликемия с разными причинами: - эмоциональное возбуждение ЦНС - гиперфункция аденогипофиза (избыток соматотропина, кортикотропина (болезнь Иценко-Кушинга – избыток АКТГ), кортизола (опухоль коры надпочечников), феохромоцитома (увеличение количества адреналина – опухоль мозговой части надпочечников) - избыток углеводов и липидов в пище
Симптомы диабета • Гипергликемия с разными причинами: - эмоциональное возбуждение ЦНС - гиперфункция аденогипофиза (избыток соматотропина, кортикотропина (болезнь Иценко-Кушинга – избыток АКТГ), кортизола (опухоль коры надпочечников), феохромоцитома (увеличение количества адреналина – опухоль мозговой части надпочечников) - избыток углеводов и липидов в пище
 Симптомы диабета • • • Глюкозурия Кетонемия Кетонурия Полидипсия (жажда) Высокая плотность мочи Сухость во рту Запах ацетона от больного Полифагия (избыток приема пищи)
Симптомы диабета • • • Глюкозурия Кетонемия Кетонурия Полидипсия (жажда) Высокая плотность мочи Сухость во рту Запах ацетона от больного Полифагия (избыток приема пищи)
 Симптомы диабета (продолжение) • Недостаток ПВК (а именно из него образуется оксалоацетат) приведет к остановке цикла Кребса, к избытку не вовлеченного в цикл ацетил -Ко. А и, следовательно, опять к ацидозу. • С мочой идет потеря ионов калия и натрия (т. е. щелочных эквивалентов). • Сдвигается в кислую сторону р. Н крови, развивается диабетическая кома.
Симптомы диабета (продолжение) • Недостаток ПВК (а именно из него образуется оксалоацетат) приведет к остановке цикла Кребса, к избытку не вовлеченного в цикл ацетил -Ко. А и, следовательно, опять к ацидозу. • С мочой идет потеря ионов калия и натрия (т. е. щелочных эквивалентов). • Сдвигается в кислую сторону р. Н крови, развивается диабетическая кома.
 Биохимические эффекты инсулина • Стимулирует проникновение глюкозы из крови в клетку ( а также аминокислот, ионов калия) – в мышцах, печени, жировой ткани, лейкоцитах. • Активирует гексокиназу, фосфофруктокиназу, пируватдегидрогеназу. • Тормозит (ингибирует) активность глюкозо-6 -фосфатазы, гликогенфосфорилазы, угнетает глюконеогенез и пируваткарбоксилазу. • Инсулин тормозит липолиз и активирует липогенез, усиливает синтез холестерина и синтез жиров. • Усиливает синтез белков, ДНК, РНК, подавляет распад белков (по сути – анаболик). • Роль хрома: осуществляет контакт инсулина с рецептором на мембране-мишени.
Биохимические эффекты инсулина • Стимулирует проникновение глюкозы из крови в клетку ( а также аминокислот, ионов калия) – в мышцах, печени, жировой ткани, лейкоцитах. • Активирует гексокиназу, фосфофруктокиназу, пируватдегидрогеназу. • Тормозит (ингибирует) активность глюкозо-6 -фосфатазы, гликогенфосфорилазы, угнетает глюконеогенез и пируваткарбоксилазу. • Инсулин тормозит липолиз и активирует липогенез, усиливает синтез холестерина и синтез жиров. • Усиливает синтез белков, ДНК, РНК, подавляет распад белков (по сути – анаболик). • Роль хрома: осуществляет контакт инсулина с рецептором на мембране-мишени.
 Осложнения сахарного диабета • Избыток ацетоуксусной кислоты ведет к образованию кетоновых тел, закислению внутренней среды – состояние ацидоза. • При диабете нарушается гликолиз, возникает энергетический голод тканей, несмотря на избыток глюкозы в крови. • Усиливается мобилизация жиров, в кровь поступают жирные кислоты. Они окисляются в ацетил-Ко. А, который идет в цикл Кребса.
Осложнения сахарного диабета • Избыток ацетоуксусной кислоты ведет к образованию кетоновых тел, закислению внутренней среды – состояние ацидоза. • При диабете нарушается гликолиз, возникает энергетический голод тканей, несмотря на избыток глюкозы в крови. • Усиливается мобилизация жиров, в кровь поступают жирные кислоты. Они окисляются в ацетил-Ко. А, который идет в цикл Кребса.
 Синтез ацетоуксусной кислоты (одно из кетоновых тел)
Синтез ацетоуксусной кислоты (одно из кетоновых тел)
 Формулы кетоновых тел
Формулы кетоновых тел
 Сахарная нагрузка – способ диагностики скрытого диабета • Измеряют натощак уровень сахара крови • Предлагают пациенту выпить 50 -100 г глюкозы в 200 мл воды • Через 15 минут с интервалами 30 минут измеряют уровень сахара крови в течение 2 -х часов. • Рисуют зависимость уровня глюкозы от времени измерения. • Оценивают (сравнивают с нормой) параметры: гликемическая кривая, время подъема уровня глюкозы, высота подъема, время и интенсивность снижения уровня до нормы.
Сахарная нагрузка – способ диагностики скрытого диабета • Измеряют натощак уровень сахара крови • Предлагают пациенту выпить 50 -100 г глюкозы в 200 мл воды • Через 15 минут с интервалами 30 минут измеряют уровень сахара крови в течение 2 -х часов. • Рисуют зависимость уровня глюкозы от времени измерения. • Оценивают (сравнивают с нормой) параметры: гликемическая кривая, время подъема уровня глюкозы, высота подъема, время и интенсивность снижения уровня до нормы.
 Лечение сахарного диабета • Диетотерапия (исключение ряда продуктов, замена сахара на сорбит, ксилит и др. ). • Замещение недостающего природного инсулина лекарственным препаратом. • Стимулирование клеток поджелудочной железы. • Ингибирование фермента инсулиназы. • Включение препаратов, увеличивающих проницаемость мембран для глюкозы, стимулирующих синтез гликогена, тормозящих глюконеогенез… (патогенетическая терапия).
Лечение сахарного диабета • Диетотерапия (исключение ряда продуктов, замена сахара на сорбит, ксилит и др. ). • Замещение недостающего природного инсулина лекарственным препаратом. • Стимулирование клеток поджелудочной железы. • Ингибирование фермента инсулиназы. • Включение препаратов, увеличивающих проницаемость мембран для глюкозы, стимулирующих синтез гликогена, тормозящих глюконеогенез… (патогенетическая терапия).
 Лечение некоторых осложнений диабета • При угрозе диабетической комы – инсулин внутривенно, бикарбонат натрия (сода) для снижения ацидоза, КСl для компенсации потери ионов с мочой, кровезаменители (р-р Рингера) для снижения дегидратации. • При гиперосмолярной – введение гипотонических растворов и инсулина для снижения уровня глюкозы. • При гипогликемической - внутривенно глюкоза. Введение адреналина для стимуляции мобилизации гликогена
Лечение некоторых осложнений диабета • При угрозе диабетической комы – инсулин внутривенно, бикарбонат натрия (сода) для снижения ацидоза, КСl для компенсации потери ионов с мочой, кровезаменители (р-р Рингера) для снижения дегидратации. • При гиперосмолярной – введение гипотонических растворов и инсулина для снижения уровня глюкозы. • При гипогликемической - внутривенно глюкоза. Введение адреналина для стимуляции мобилизации гликогена
 Гликогенозы Это наследственные заболевания, связанные с недостатком или полным отсутствием некоторых ферментов распада или синтеза гликогена. При этом в органах и тканях избыточно накапливаются гликоген или его продукты, парализуя жизнь клетки. • Болезнь Гирке – дефицит глюкозо-6 -фосфатазы, накапливается в печени и почках гликоген. • Болезнь Помпе – дефицит кислой глюкозидазы – те же симптомы. • Болезнь Кори – отсутствие гликогенветвящего фермента, образуются короткие фрагменты гликогена в печени и эритроцитах
Гликогенозы Это наследственные заболевания, связанные с недостатком или полным отсутствием некоторых ферментов распада или синтеза гликогена. При этом в органах и тканях избыточно накапливаются гликоген или его продукты, парализуя жизнь клетки. • Болезнь Гирке – дефицит глюкозо-6 -фосфатазы, накапливается в печени и почках гликоген. • Болезнь Помпе – дефицит кислой глюкозидазы – те же симптомы. • Болезнь Кори – отсутствие гликогенветвящего фермента, образуются короткие фрагменты гликогена в печени и эритроцитах
 Гликогенозы (продолжение) • Болезнь Андерсена – отсутствие глюкозилтрансферазы, образуется гликоген с редкими ветвлениями в печени, мышцах, лейкоцитах. • Болезнь Мак-Ардла – недостаточность фосфорилазы мышц, гликоген избыточно накапливается в скелетной мускулатуре. • Болезнь Герса – недостаток фосфорилазы печени. Гликоген накапливается в печени и лейкоцитах. • Всего известно 11 гликогенозов. • Агликогенозы – отсутствие гликогенсинтазы (гипогликемия, судороги, необходимость постоянного приема пищи).
Гликогенозы (продолжение) • Болезнь Андерсена – отсутствие глюкозилтрансферазы, образуется гликоген с редкими ветвлениями в печени, мышцах, лейкоцитах. • Болезнь Мак-Ардла – недостаточность фосфорилазы мышц, гликоген избыточно накапливается в скелетной мускулатуре. • Болезнь Герса – недостаток фосфорилазы печени. Гликоген накапливается в печени и лейкоцитах. • Всего известно 11 гликогенозов. • Агликогенозы – отсутствие гликогенсинтазы (гипогликемия, судороги, необходимость постоянного приема пищи).
 Химия и обмен липидов
Химия и обмен липидов
 Характеристика класса липидов Это нерастворимые в воде, но растворимые в органических растворителях соединения различной химической структуры, содержащие длинные (жирные) углеводородные радикалы. Одна из классификаций следующая: • Простые липиды: жиры (триглицериды) и воска. • Сложные – фосфолипиды (глицеро- и сфинголипиды), гликолипиды, стероиды, другие сложные (сульфо-, аминолипиды, липопротеины) • Предшественники и производные: жирные кислоты, жирные спирты, жирорастворимые витамины. гормоны и т. д.
Характеристика класса липидов Это нерастворимые в воде, но растворимые в органических растворителях соединения различной химической структуры, содержащие длинные (жирные) углеводородные радикалы. Одна из классификаций следующая: • Простые липиды: жиры (триглицериды) и воска. • Сложные – фосфолипиды (глицеро- и сфинголипиды), гликолипиды, стероиды, другие сложные (сульфо-, аминолипиды, липопротеины) • Предшественники и производные: жирные кислоты, жирные спирты, жирорастворимые витамины. гормоны и т. д.
 Простые липиды (жиры и воска)
Простые липиды (жиры и воска)
 Сложные липиды фосфолипиды (лецитины, кефалины, фосфатидилсерины, фосфатидилинозитолы)
Сложные липиды фосфолипиды (лецитины, кефалины, фосфатидилсерины, фосфатидилинозитолы)
 Фосфолипиды (плазмалогены) фосфатидальхолин
Фосфолипиды (плазмалогены) фосфатидальхолин
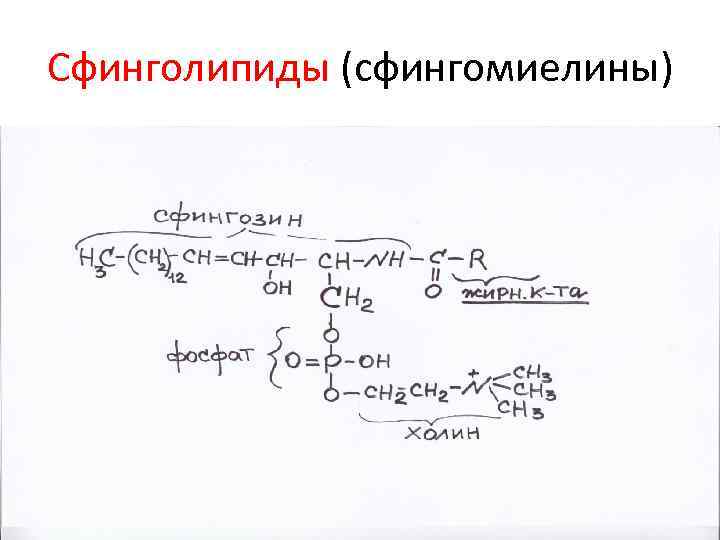 Сфинголипиды (сфингомиелины)
Сфинголипиды (сфингомиелины)
 Гликосфинголипиды (галактозилцерамид тканей мозга)
Гликосфинголипиды (галактозилцерамид тканей мозга)
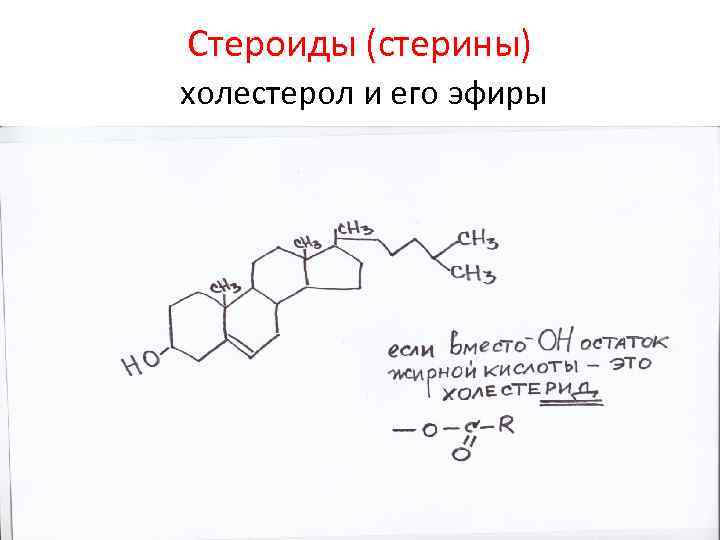 Стероиды (стерины) холестерол и его эфиры
Стероиды (стерины) холестерол и его эфиры
 Переваривание липидов в ЖКТ • В слюне нет ферментов для липидов ( у детей лингвалипаза) • В желудке нет ( у детей есть липаза с р. Н=6) • 12 -перстная кишка: нейтрализация НСl, перемешивание СО 2, эмульгирование желчью, парные желчные кислоты, липаза, колипаза, моноглицероизомераза (из бета-2 в альфа-1), фосфолипазы, холестеролэстераза • Кишечный сок – липаза, кишечная щелочная фосфатаза, гидролаза эфиров холестерина.
Переваривание липидов в ЖКТ • В слюне нет ферментов для липидов ( у детей лингвалипаза) • В желудке нет ( у детей есть липаза с р. Н=6) • 12 -перстная кишка: нейтрализация НСl, перемешивание СО 2, эмульгирование желчью, парные желчные кислоты, липаза, колипаза, моноглицероизомераза (из бета-2 в альфа-1), фосфолипазы, холестеролэстераза • Кишечный сок – липаза, кишечная щелочная фосфатаза, гидролаза эфиров холестерина.
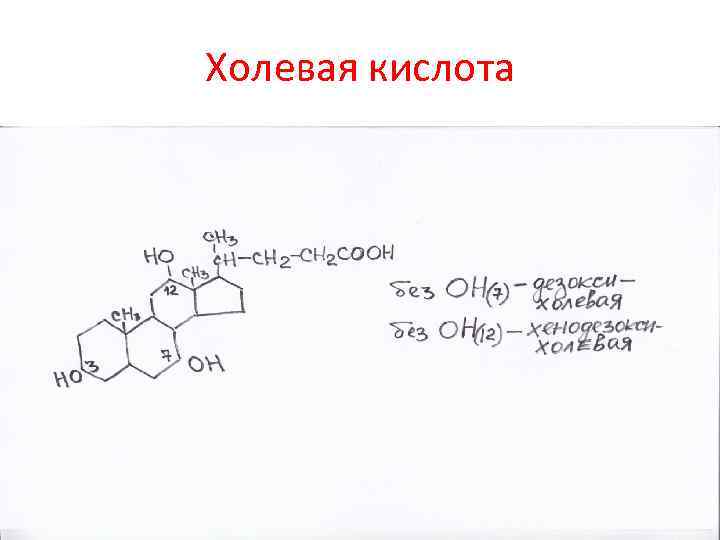 Холевая кислота
Холевая кислота
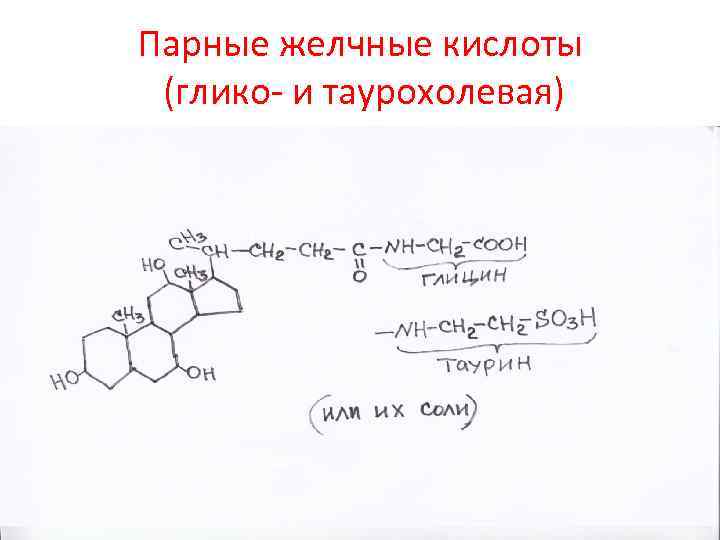 Парные желчные кислоты (глико- и таурохолевая)
Парные желчные кислоты (глико- и таурохолевая)
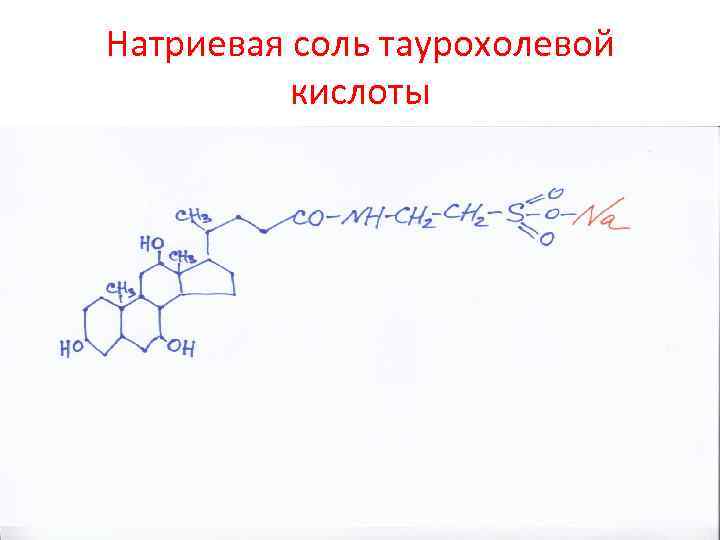 Натриевая соль таурохолевой кислоты
Натриевая соль таурохолевой кислоты
 Продукты переваривания пищевых липидов • Триглицериды (жиры) частично или полностью расщепляются до глицерина и свободных жирных кислот, проникают в энтероциты, портальную систему и в печень. Уже в стенке кишечника начинают синтезироваться собственные липиды • Фосфолипиды под действием кишечного сока гидролизуются и всасываются в виде лизофосфолипидов. Эфиры холестерина гидролизуются эстеразой, всасывается свободный холестерин • Частично могут всасываться недогидролизованные липиды
Продукты переваривания пищевых липидов • Триглицериды (жиры) частично или полностью расщепляются до глицерина и свободных жирных кислот, проникают в энтероциты, портальную систему и в печень. Уже в стенке кишечника начинают синтезироваться собственные липиды • Фосфолипиды под действием кишечного сока гидролизуются и всасываются в виде лизофосфолипидов. Эфиры холестерина гидролизуются эстеразой, всасывается свободный холестерин • Частично могут всасываться недогидролизованные липиды
 Всасывание продуктов расщепления липидов • Происходит в тонкой кишке. Очень мало всасывается в виде эмульгированного жира без гидролиза, коротких жирных кислот и глицерина. • Всасывание в виде мицелл. Гидрофобное ядро (жирные кислоты, холестерин, витамины, моноглицериды), а снаружи гидрофильные оболочки из жирных кислот и фосфолипидов. • Ресинтез липидов в кишечной стенке (комплекс из 3 -х ферментов – триглицеридсинтетаза) • Ресинтез фосфолипидов в кишечной стенке • Образование хиломикронов (ХМ) - 2% белка, 7% фосфолипидов, 8% холестерина, 80% триглицеридов) • Диффузия ХМ из кишечника в лимфатическую систему, а далее в кровь и печень.
Всасывание продуктов расщепления липидов • Происходит в тонкой кишке. Очень мало всасывается в виде эмульгированного жира без гидролиза, коротких жирных кислот и глицерина. • Всасывание в виде мицелл. Гидрофобное ядро (жирные кислоты, холестерин, витамины, моноглицериды), а снаружи гидрофильные оболочки из жирных кислот и фосфолипидов. • Ресинтез липидов в кишечной стенке (комплекс из 3 -х ферментов – триглицеридсинтетаза) • Ресинтез фосфолипидов в кишечной стенке • Образование хиломикронов (ХМ) - 2% белка, 7% фосфолипидов, 8% холестерина, 80% триглицеридов) • Диффузия ХМ из кишечника в лимфатическую систему, а далее в кровь и печень.
 Хиломикроны • Это транспортная форма липидов из кишечника в лимфу, а затем в кровь • Хиломикроны состоят из липидного ядра (98%), покрытого белковой оболочкой (2%). В ядре содердится до 85% жиров, фдсфолипиды, холестерин, витамины • Белковая гидрофильная оболочка позволяет хиломикронам хорошо растворяться и обеспечивать транспортные функции
Хиломикроны • Это транспортная форма липидов из кишечника в лимфу, а затем в кровь • Хиломикроны состоят из липидного ядра (98%), покрытого белковой оболочкой (2%). В ядре содердится до 85% жиров, фдсфолипиды, холестерин, витамины • Белковая гидрофильная оболочка позволяет хиломикронам хорошо растворяться и обеспечивать транспортные функции
 Липопротеины сыворотки крови • • Хиломикроны Содержат до 90% жиров, около 2% белков Образуются в эпителии кишечника Транспортируют липиды от кишечника к органам и тканям (в основном к жировой) Остатки хиломикронов из крови поглощаются печенью и идут на синтез липопротеинов низкой плотности
Липопротеины сыворотки крови • • Хиломикроны Содержат до 90% жиров, около 2% белков Образуются в эпителии кишечника Транспортируют липиды от кишечника к органам и тканям (в основном к жировой) Остатки хиломикронов из крови поглощаются печенью и идут на синтез липопротеинов низкой плотности
 Липопротеины низкой плотности – ЛПНП, беталипопротеины • Содержат до 45% холестерина, до 25% белков, это основные липопротеины сыворотки • Образуются из остатков хиломикронов и липопротеинов очень низкой плотности • Транспортируют холестерин к органам и тканям для формирования клеточных мембран • Поглощаются клетками путем эндоцитоза
Липопротеины низкой плотности – ЛПНП, беталипопротеины • Содержат до 45% холестерина, до 25% белков, это основные липопротеины сыворотки • Образуются из остатков хиломикронов и липопротеинов очень низкой плотности • Транспортируют холестерин к органам и тканям для формирования клеточных мембран • Поглощаются клетками путем эндоцитоза
 Липопротеины очень низкой плотности (ЛПОНП, пре-бета-липопротеины) • Содержат более 50% жиров и около 10% белков • Синтезируются, главным образом, в печени, небольшое количество образуется и эпителии кишечника вместе с хиломикронами • Обеспечивают транспорт собственных эндогенных жиров из печени в жировую ткань
Липопротеины очень низкой плотности (ЛПОНП, пре-бета-липопротеины) • Содержат более 50% жиров и около 10% белков • Синтезируются, главным образом, в печени, небольшое количество образуется и эпителии кишечника вместе с хиломикронами • Обеспечивают транспорт собственных эндогенных жиров из печени в жировую ткань
 Липопротеины высокой плотности (ЛПВП, альфалипопротеины) • Содержат более чем другие (до 50%) белков и фосфолипидов, много холестерина. Этой фракции в крови до 30% от всех липопротеинов • Возникают в печени, поступают в кровь, где достраиваются, поглощая хиломикроны и избыточный холестерин из органов и тканей, чтобы транспортировать его вновь в печень • Холестерин из этой фракции расходуется в печени на образование желчных кислот, а также выделяется с желчью в кишечник
Липопротеины высокой плотности (ЛПВП, альфалипопротеины) • Содержат более чем другие (до 50%) белков и фосфолипидов, много холестерина. Этой фракции в крови до 30% от всех липопротеинов • Возникают в печени, поступают в кровь, где достраиваются, поглощая хиломикроны и избыточный холестерин из органов и тканей, чтобы транспортировать его вновь в печень • Холестерин из этой фракции расходуется в печени на образование желчных кислот, а также выделяется с желчью в кишечник
 Гидролитическое расщепление фосфолипида
Гидролитическое расщепление фосфолипида
 Расщепление (окисление) липидов, т. е. липолиз • Стимулируют: катехоламины, глюкагон, тироксин, АКТГ, глюкокортикоиды, стрессы физическая нагрузка, холод, голодание, инсулин • Угнетают: активация фосфодиэстеразы (усиление гидролиза ц. АМФ), снижение активности аденилатциклазы
Расщепление (окисление) липидов, т. е. липолиз • Стимулируют: катехоламины, глюкагон, тироксин, АКТГ, глюкокортикоиды, стрессы физическая нагрузка, холод, голодание, инсулин • Угнетают: активация фосфодиэстеразы (усиление гидролиза ц. АМФ), снижение активности аденилатциклазы
 Гидролиз липидов в клетках • Триглицериды (жиры) расщепляются ферментами триацилглицероллипазой, диацилглицероллипазой, моноацилглицероллипазой • Другие липиды гидролизуются ферментами, локализованными в лизосомах: фосфолипазой А 1, фосфолипазой А 2, фосфолипазой С, фосфатазами, холестеролэстеразой, цереброзидсульфатазой и др. • Интенсивность липолиза в клетках регулируется гормонами, влияющими через ц-АМФ
Гидролиз липидов в клетках • Триглицериды (жиры) расщепляются ферментами триацилглицероллипазой, диацилглицероллипазой, моноацилглицероллипазой • Другие липиды гидролизуются ферментами, локализованными в лизосомах: фосфолипазой А 1, фосфолипазой А 2, фосфолипазой С, фосфатазами, холестеролэстеразой, цереброзидсульфатазой и др. • Интенсивность липолиза в клетках регулируется гормонами, влияющими через ц-АМФ
 Гидролиз фосфолипида
Гидролиз фосфолипида
 ОБМЕН ЛИПИДОВ продолжение
ОБМЕН ЛИПИДОВ продолжение
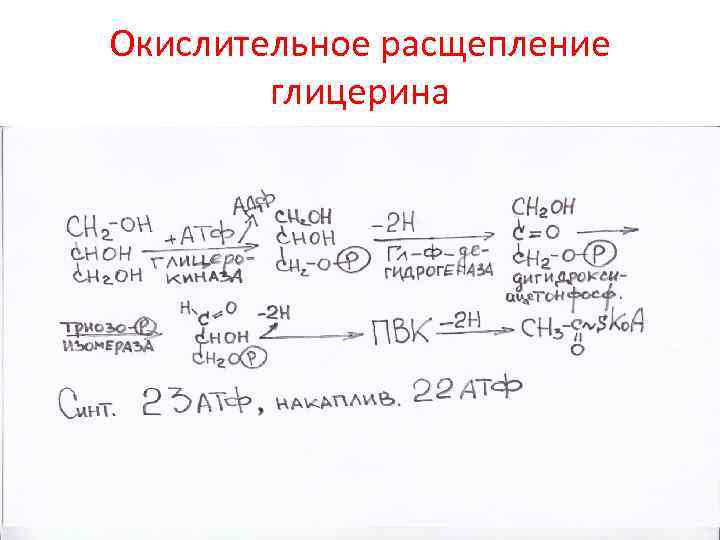 Окислительное расщепление глицерина
Окислительное расщепление глицерина
 Активирование жирной кислоты
Активирование жирной кислоты
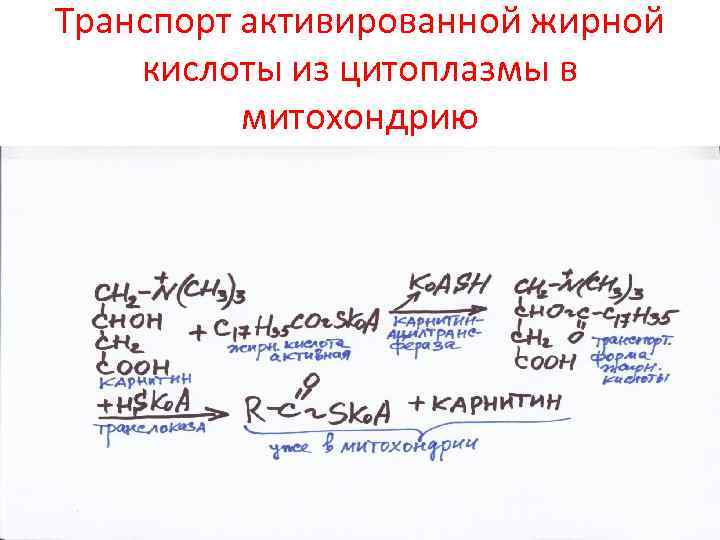 Транспорт активированной жирной кислоты из цитоплазмы в митохондрию
Транспорт активированной жирной кислоты из цитоплазмы в митохондрию
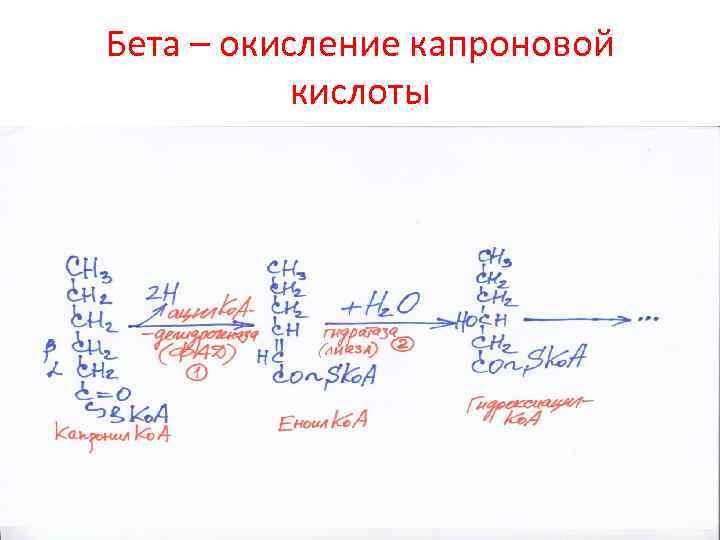 Бета – окисление капроновой кислоты
Бета – окисление капроновой кислоты
 Бета – окисление капроновой кислоты (продолжение)
Бета – окисление капроновой кислоты (продолжение)
 Схема окисления жирных кислот с нечетным числом С - атомов
Схема окисления жирных кислот с нечетным числом С - атомов
 Деградация жирных кислот в печени • Сначала в цитоплазме гепатоцитов жирные кислоты активируются, присоединяясь к коэнзиму А • Затем с помощью переносчика карнитина жирные кислоты транспортируются в митохондрии • В матриксе митохондрий идет бета-окисление до ацетил-Ко. А • Далее цикл Кребса до СО 2, Н 2 О и энергии АТФ • Если количество ацетильных остатков превосходит потребности, то образуются кетоновые тела (при голодании, диабете)
Деградация жирных кислот в печени • Сначала в цитоплазме гепатоцитов жирные кислоты активируются, присоединяясь к коэнзиму А • Затем с помощью переносчика карнитина жирные кислоты транспортируются в митохондрии • В матриксе митохондрий идет бета-окисление до ацетил-Ко. А • Далее цикл Кребса до СО 2, Н 2 О и энергии АТФ • Если количество ацетильных остатков превосходит потребности, то образуются кетоновые тела (при голодании, диабете)
 Расщепление жиров в жировой ткани • Жиры резервируются в клетках жировой ткани – адипоцитах • Их расщепление там (липолиз) катализируется гормонзависимой липазой (активируют глюкагон, адреналин, норадреналин, тормозит инсулин) • Освободившиеся жирные кислоты выходят в плазму крови (длинные с белком-альбумином) • Из плазмы крови жирные кислоты поступают в ткани на синтез новых жиров или окисляются для получения энергии (синтеза АТФ)
Расщепление жиров в жировой ткани • Жиры резервируются в клетках жировой ткани – адипоцитах • Их расщепление там (липолиз) катализируется гормонзависимой липазой (активируют глюкагон, адреналин, норадреналин, тормозит инсулин) • Освободившиеся жирные кислоты выходят в плазму крови (длинные с белком-альбумином) • Из плазмы крови жирные кислоты поступают в ткани на синтез новых жиров или окисляются для получения энергии (синтеза АТФ)
 Роль кетоновых тел • Ацетил Ко. А из окисления жирных кислот включается в цикл Кребса, если метаболизм в норме • Если расщепление жиров преобладает (голодание, диабет) – образуются кетоновые тела (т. к. оксалоацетата нет - он ушел в глюконеогенез) • Кетоновые тела – это топливо для мышц и почек, а печень не использует кетоновые тела для энергетики • При голодании и диабете мозг адаптируется к ацетоацетату, как к топливу (в норме это глюкоза) «Жиры сгорают в пламени углеводов»
Роль кетоновых тел • Ацетил Ко. А из окисления жирных кислот включается в цикл Кребса, если метаболизм в норме • Если расщепление жиров преобладает (голодание, диабет) – образуются кетоновые тела (т. к. оксалоацетата нет - он ушел в глюконеогенез) • Кетоновые тела – это топливо для мышц и почек, а печень не использует кетоновые тела для энергетики • При голодании и диабете мозг адаптируется к ацетоацетату, как к топливу (в норме это глюкоза) «Жиры сгорают в пламени углеводов»
 Другие пути окисления жирных кислот • У ненасыщенных жирных кислот двойные связи цис-конфигурации, а классическое бета окисление – транс-двоные связи: положение двойных связей должно быть 2 -3, а получаются при классическом окислении 3 -4. Эти особенности исправляет 3, 4 -цис-изомераза, далее обычный механизм окисления жирных кислот • Жирные кислоты с боковыми ответвлениями (растительные) разрушаются методом альфа-окисления. При этом сначала кислота гидроксилируется, отщепляется по одному атому С без участия Ко. А и без синтеза АТФ • Омега-окисление начинается с гидроксилирования метильного атома С, получаются дикарбоновые кислоты, окисление идет с обеих сторон, продукт выводится с мочой. • В пероксисомах окисляются длинные (более 20 С) жирные кислоты с образованием Н 2 О 2, ацетил Ко. А без синтеза
Другие пути окисления жирных кислот • У ненасыщенных жирных кислот двойные связи цис-конфигурации, а классическое бета окисление – транс-двоные связи: положение двойных связей должно быть 2 -3, а получаются при классическом окислении 3 -4. Эти особенности исправляет 3, 4 -цис-изомераза, далее обычный механизм окисления жирных кислот • Жирные кислоты с боковыми ответвлениями (растительные) разрушаются методом альфа-окисления. При этом сначала кислота гидроксилируется, отщепляется по одному атому С без участия Ко. А и без синтеза АТФ • Омега-окисление начинается с гидроксилирования метильного атома С, получаются дикарбоновые кислоты, окисление идет с обеих сторон, продукт выводится с мочой. • В пероксисомах окисляются длинные (более 20 С) жирные кислоты с образованием Н 2 О 2, ацетил Ко. А без синтеза
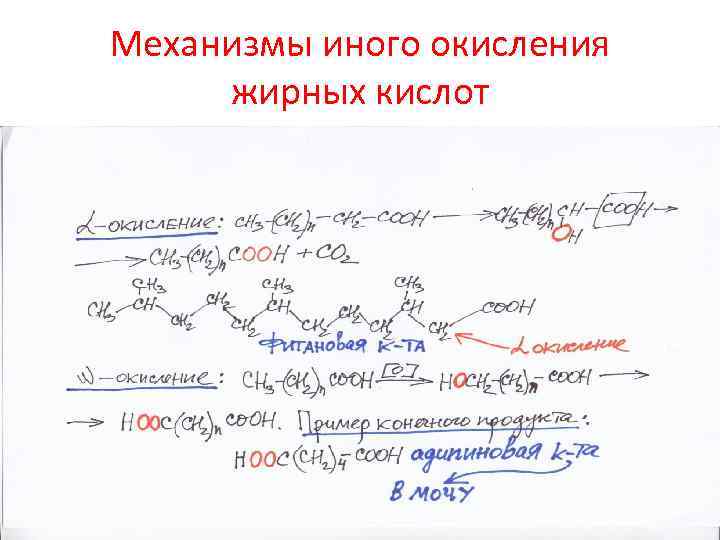 Механизмы иного окисления жирных кислот
Механизмы иного окисления жирных кислот
 Механизмы синтеза липидов
Механизмы синтеза липидов
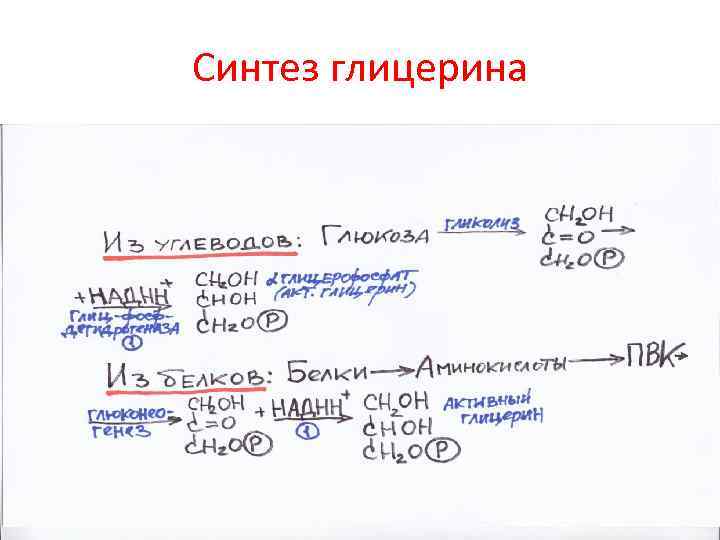 Синтез глицерина
Синтез глицерина
 Синтез жирных кислот • Синтез идет в цитоплазме до С 16, удлинение кислот продолжается в митохондриях • Синтез идет в печени, почках, мозге, легких, молочной железе, жировой ткани • Участники синтеза: НАДФН, АТФ, Мn+2, источник СО 2, ацетил Ко. А, ферментный комплекс – синтетаза жирных кислот (6 ферментов), ацилпереносящие белки (АПБ) • Пути синтеза и окисления жирных кислот не пересекаются и идут в разных структурах клетки
Синтез жирных кислот • Синтез идет в цитоплазме до С 16, удлинение кислот продолжается в митохондриях • Синтез идет в печени, почках, мозге, легких, молочной железе, жировой ткани • Участники синтеза: НАДФН, АТФ, Мn+2, источник СО 2, ацетил Ко. А, ферментный комплекс – синтетаза жирных кислот (6 ферментов), ацилпереносящие белки (АПБ) • Пути синтеза и окисления жирных кислот не пересекаются и идут в разных структурах клетки
 Карбоксилирование ацетил Ко-А – первый этап синтеза жирных кислот
Карбоксилирование ацетил Ко-А – первый этап синтеза жирных кислот
 Синтез жирной кислоты (продолжение)
Синтез жирной кислоты (продолжение)
 Синтез жирной кислоты (продолжение)
Синтез жирной кислоты (продолжение)
 Синтез жирной кислоты (продолжение)
Синтез жирной кислоты (продолжение)
 Образование ненасыщенных и удлинение (более С 16) жирных кислот • Превращение жирных кислот в ненасыщенные идет в микросомах печени и жировой ткани. Участвуют кислород, нуклеотиды, цитохром в 5, ферменты десатуразы, активированные насыщенные кислоты • Удлинение (элонгация) жирных кислот идет там же с участием ацетил. Ко. А, малонил. Ко. А и ферментов элонгаз • Жирные кислоты с нечетным числом углеродных атомов начинают синтезироваться с пропионил. Ко. А и далее обычным образом
Образование ненасыщенных и удлинение (более С 16) жирных кислот • Превращение жирных кислот в ненасыщенные идет в микросомах печени и жировой ткани. Участвуют кислород, нуклеотиды, цитохром в 5, ферменты десатуразы, активированные насыщенные кислоты • Удлинение (элонгация) жирных кислот идет там же с участием ацетил. Ко. А, малонил. Ко. А и ферментов элонгаз • Жирные кислоты с нечетным числом углеродных атомов начинают синтезироваться с пропионил. Ко. А и далее обычным образом
 Схема удлинения жирных кислот образования ненасыщенных
Схема удлинения жирных кислот образования ненасыщенных
 Синтез жиров • Синтез жира начинается с синтеза фосфатидной кислоты • Фосфатидная кислота – основа для последующего синтеза жиров, а также фосфатидилхолина (лецитина) и других форм фосфолипидов • На синтез одной молекулы жира расходуется 4 АТФ: 1 молекула идет на активирование глицерина и по 1 на активирование каждой жирной кислоты
Синтез жиров • Синтез жира начинается с синтеза фосфатидной кислоты • Фосфатидная кислота – основа для последующего синтеза жиров, а также фосфатидилхолина (лецитина) и других форм фосфолипидов • На синтез одной молекулы жира расходуется 4 АТФ: 1 молекула идет на активирование глицерина и по 1 на активирование каждой жирной кислоты
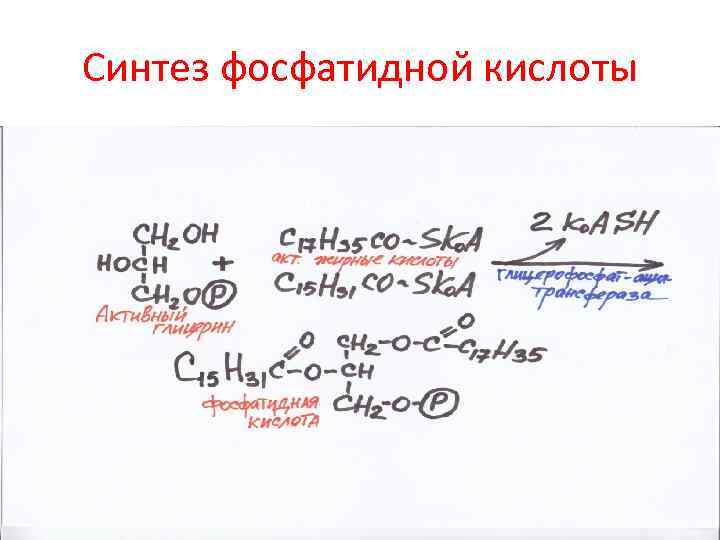 Синтез фосфатидной кислоты
Синтез фосфатидной кислоты
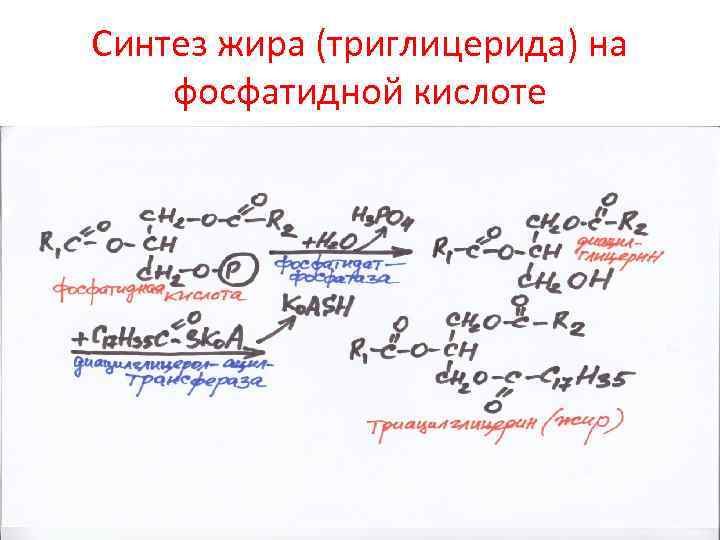 Синтез жира (триглицерида) на фосфатидной кислоте
Синтез жира (триглицерида) на фосфатидной кислоте
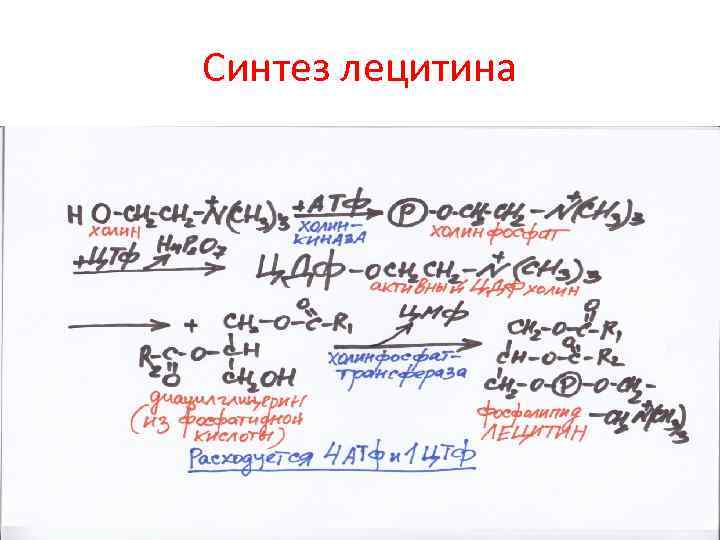 Синтез лецитина
Синтез лецитина
 Синтез эндогенного холестерина • Холестерин синтезируется в печени (более 80%), слизистой кишечника, надпочечниках, семенниках, яичниках, коже • Холестерин синтезируется из ацетил. Ко. А (18 молекул), НАДФН (17 молекул) с участием АТФ (18 молекул) и кислорода • В синтезе холестерина выделяют 3 стадии: 1 – превращение ацетил. Ко. А в мевалоновую кис-ту, 2 – образование сквалена из мевалоновой кислоты, 3 – циклизация сквалена в холестерин. Каждая стадия включает несколько реакций. • Синтезируется в сутки 1 грамм холестерина, поступает с пищей около 1 грамма, содержится в крови 200 мг в декалитре
Синтез эндогенного холестерина • Холестерин синтезируется в печени (более 80%), слизистой кишечника, надпочечниках, семенниках, яичниках, коже • Холестерин синтезируется из ацетил. Ко. А (18 молекул), НАДФН (17 молекул) с участием АТФ (18 молекул) и кислорода • В синтезе холестерина выделяют 3 стадии: 1 – превращение ацетил. Ко. А в мевалоновую кис-ту, 2 – образование сквалена из мевалоновой кислоты, 3 – циклизация сквалена в холестерин. Каждая стадия включает несколько реакций. • Синтезируется в сутки 1 грамм холестерина, поступает с пищей около 1 грамма, содержится в крови 200 мг в декалитре
 Синтез холестерина до мевалоновой кислоты
Синтез холестерина до мевалоновой кислоты
 Синтез сквалена из мевалоновой кислоты
Синтез сквалена из мевалоновой кислоты
 Синтез сквалена (продолжение)
Синтез сквалена (продолжение)
 Синтез холестерина из сквалена
Синтез холестерина из сквалена
 Особенности синтеза холестерина • До сквалена все продукты синтеза холестерина растворимы и свободны (ни с чем не связаны) • После сквалена все продукты связаны со стеринпереносящими белками, что обеспечивает их растворимость • Связь с белками облегчает вхождение холестерина в мембраны, окисление его в желчные кислоты, превращение в стероидные гормоны и др. продукты • Синтез холестерина лимитируется скоростью образования мевалоновой кислоты • Увеличивает синтез инсулин и тиреогормоны, снижает – глюкагон, глюкокортикоиды, голодание, тиреоидэктомия
Особенности синтеза холестерина • До сквалена все продукты синтеза холестерина растворимы и свободны (ни с чем не связаны) • После сквалена все продукты связаны со стеринпереносящими белками, что обеспечивает их растворимость • Связь с белками облегчает вхождение холестерина в мембраны, окисление его в желчные кислоты, превращение в стероидные гормоны и др. продукты • Синтез холестерина лимитируется скоростью образования мевалоновой кислоты • Увеличивает синтез инсулин и тиреогормоны, снижает – глюкагон, глюкокортикоиды, голодание, тиреоидэктомия
 Образование ненасыщенных и удлинение (более С 16) жирных кислот • Превращение жирных кислот в ненасыщенные идет в микросомах печени и жировой ткани. Участвуют кислород, нуклеотиды, цитохром в 5, ферменты десатуразы, активированные насыщенные кислоты • Удлинение (элонгация) жирных кислот идет там же с участием ацетил. Ко. А, малонил. Ко. А и ферментов элонгаз • Жирные кислоты с нечетным числом углеродных атомов начинают синтезироваться с пропионил. Ко. А и далее обычным образом
Образование ненасыщенных и удлинение (более С 16) жирных кислот • Превращение жирных кислот в ненасыщенные идет в микросомах печени и жировой ткани. Участвуют кислород, нуклеотиды, цитохром в 5, ферменты десатуразы, активированные насыщенные кислоты • Удлинение (элонгация) жирных кислот идет там же с участием ацетил. Ко. А, малонил. Ко. А и ферментов элонгаз • Жирные кислоты с нечетным числом углеродных атомов начинают синтезироваться с пропионил. Ко. А и далее обычным образом
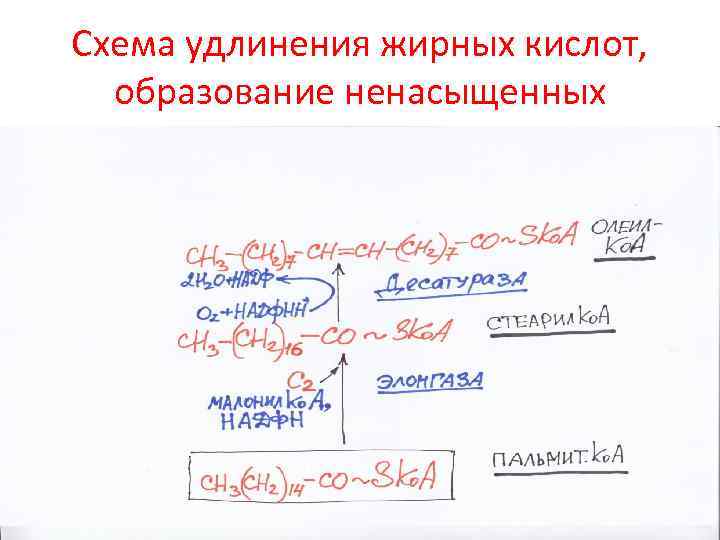 Схема удлинения жирных кислот, образование ненасыщенных
Схема удлинения жирных кислот, образование ненасыщенных
 Синтез жиров • Синтез жира начинается с синтеза фосфатидной кислоты • Фосфатидная кислота – основа для последующего синтеза жиров, а также фосфатидилхолина (лецитина) и других форм фосфолипидов • На синтез одной молекулы жира расходуется 4 АТФ: 1 молекула идет на активирование глицерина и по 1 на активирование каждой жирной кислоты
Синтез жиров • Синтез жира начинается с синтеза фосфатидной кислоты • Фосфатидная кислота – основа для последующего синтеза жиров, а также фосфатидилхолина (лецитина) и других форм фосфолипидов • На синтез одной молекулы жира расходуется 4 АТФ: 1 молекула идет на активирование глицерина и по 1 на активирование каждой жирной кислоты
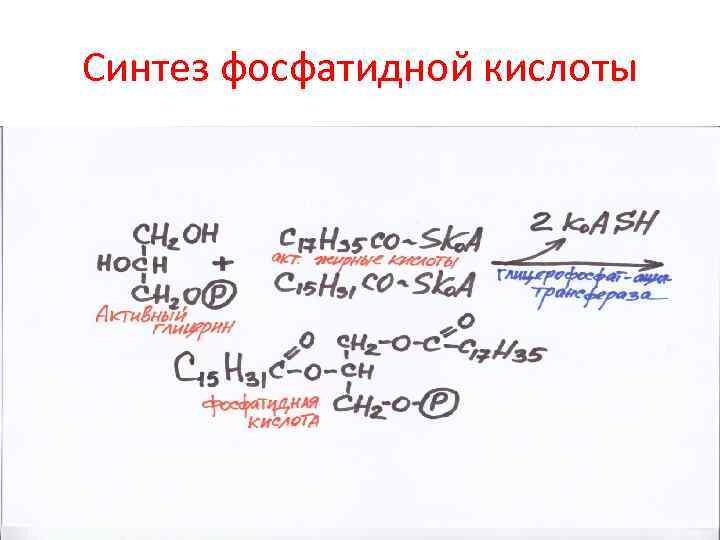 Синтез фосфатидной кислоты
Синтез фосфатидной кислоты
 Синтез жира (триглицерида) на фосфатидной кислоте
Синтез жира (триглицерида) на фосфатидной кислоте
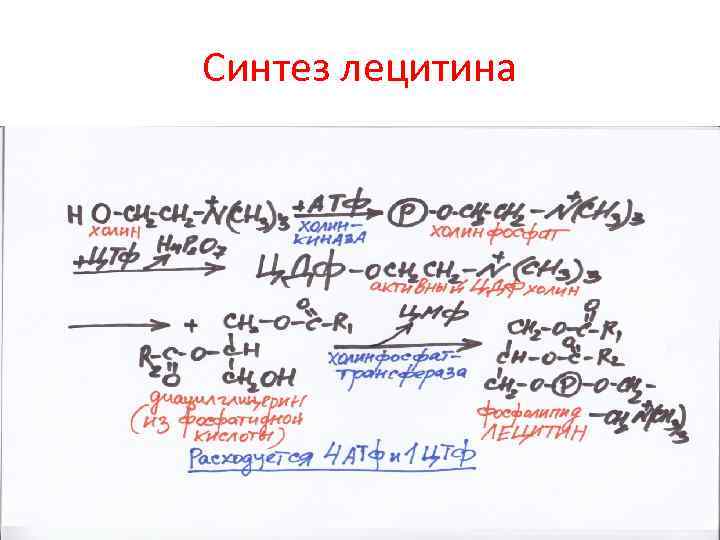 Синтез лецитина
Синтез лецитина
 Синтез эндогенного холестерина • Холестерин синтезируется в печени (более 80%), слизистой кишечника, надпочечниках, семенниках, яичниках, коже • Холестерин синтезируется из ацетил. Ко. А (18 молекул), НАДФН (17 молекул) с участием АТФ (18 молекул) и кислорода • В синтезе холестерина выделяют 3 стадии: 1 – превращение ацетил. Ко. А в мевалоновую кис-ту, 2 – образование сквалена из мевалоновой кислоты, 3 – циклизация сквалена в холестерин. Каждая стадия включает несколько реакций. • Синтезируется в сутки 1 грамм холестерина, поступает с пищей около 1 грамма, содержится в крови 200 мг в декалитре
Синтез эндогенного холестерина • Холестерин синтезируется в печени (более 80%), слизистой кишечника, надпочечниках, семенниках, яичниках, коже • Холестерин синтезируется из ацетил. Ко. А (18 молекул), НАДФН (17 молекул) с участием АТФ (18 молекул) и кислорода • В синтезе холестерина выделяют 3 стадии: 1 – превращение ацетил. Ко. А в мевалоновую кис-ту, 2 – образование сквалена из мевалоновой кислоты, 3 – циклизация сквалена в холестерин. Каждая стадия включает несколько реакций. • Синтезируется в сутки 1 грамм холестерина, поступает с пищей около 1 грамма, содержится в крови 200 мг в декалитре
 Синтез холестерина до мевалоновой кислоты
Синтез холестерина до мевалоновой кислоты
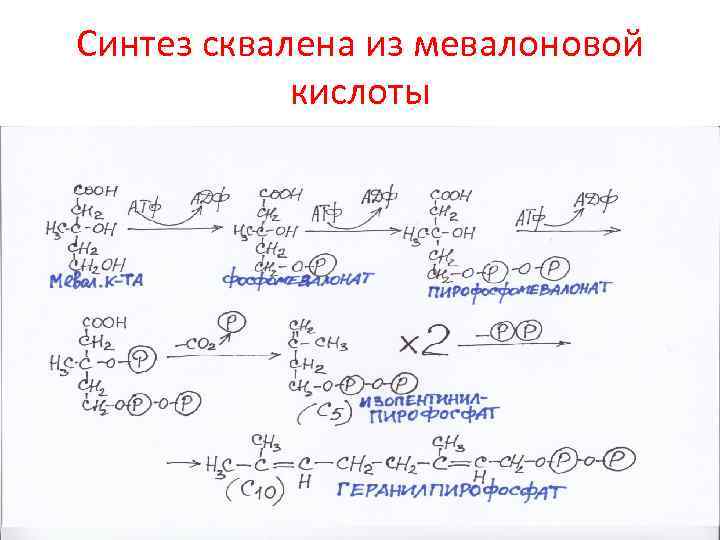 Синтез сквалена из мевалоновой кислоты
Синтез сквалена из мевалоновой кислоты
 Синтез сквалена (продолжение)
Синтез сквалена (продолжение)
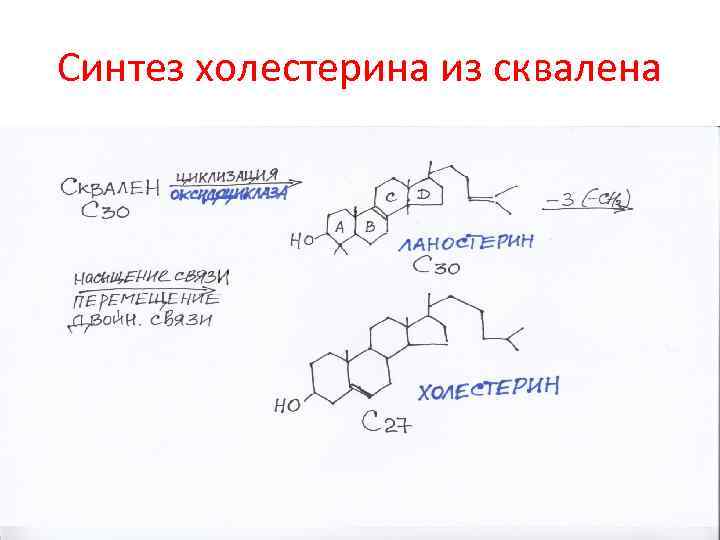 Синтез холестерина из сквалена
Синтез холестерина из сквалена
 Особенности синтеза холестерина • До сквалена все продукты синтеза холестерина растворимы и свободны (ни с чем не связаны) • После сквалена все продукты связаны со стеринпереносящими белками, что обеспечивает их растворимость • Связь с белками облегчает вхождение холестерина в мембраны, окисление его в желчные кислоты, превращение в стероидные гормоны и др. продукты • Синтез холестерина лимитируется скоростью образования мевалоновой кислоты • Увеличивает синтез инсулин и тиреогормоны, снижает – глюкагон, глюкокортикоиды, голодание, тиреоидэктомия
Особенности синтеза холестерина • До сквалена все продукты синтеза холестерина растворимы и свободны (ни с чем не связаны) • После сквалена все продукты связаны со стеринпереносящими белками, что обеспечивает их растворимость • Связь с белками облегчает вхождение холестерина в мембраны, окисление его в желчные кислоты, превращение в стероидные гормоны и др. продукты • Синтез холестерина лимитируется скоростью образования мевалоновой кислоты • Увеличивает синтез инсулин и тиреогормоны, снижает – глюкагон, глюкокортикоиды, голодание, тиреоидэктомия
 Регуляция липидного обмена • Обмен липидов регулируется ЦНС (кора – нижние отделы нервной системы – эндокринные железы – липидный обмен). Эмоциональный стресс – катехоамины в кровь – липолиз жировой ткани – мобилизация жирных кислот в кровь. В клетках адреналин – аденилатциклаза – ц. АМФ - протеинкиназа – фосфорилирование (активация) липазы. • Соматотропный гормон (гипофиз) влияет на обмен липидов: гипофункция стимулирует отложение жира (гипофизарное ожирение), повышение уровня СТГ стимулирует липолиз (гидролиз жиров). Адреналин стимулирует активность аденилатциклазы мгновенно, а СТГ индуцирует синтез новых молекул этого фермента (медленно), хотя и работают в одном направлении.
Регуляция липидного обмена • Обмен липидов регулируется ЦНС (кора – нижние отделы нервной системы – эндокринные железы – липидный обмен). Эмоциональный стресс – катехоамины в кровь – липолиз жировой ткани – мобилизация жирных кислот в кровь. В клетках адреналин – аденилатциклаза – ц. АМФ - протеинкиназа – фосфорилирование (активация) липазы. • Соматотропный гормон (гипофиз) влияет на обмен липидов: гипофункция стимулирует отложение жира (гипофизарное ожирение), повышение уровня СТГ стимулирует липолиз (гидролиз жиров). Адреналин стимулирует активность аденилатциклазы мгновенно, а СТГ индуцирует синтез новых молекул этого фермента (медленно), хотя и работают в одном направлении.
 Регуляция липидного обмена (продолжение) • Инсулин оказывает на липолиз действие, обратное адреналину и глюкагону. Инсулин – активация фосфодиэстеразы – расшепление (активация) ц. АМФ – активация гликолиза в жировой ткани. • Тироксин, половые гормоны влияют на липидный обмен. Механизм не всегда ясен. Кастрация у животных влечет избыток отложения жира. • Простагландины угнетают аденилатциклазу, ослабляют влияние адреналина на липидный обмен
Регуляция липидного обмена (продолжение) • Инсулин оказывает на липолиз действие, обратное адреналину и глюкагону. Инсулин – активация фосфодиэстеразы – расшепление (активация) ц. АМФ – активация гликолиза в жировой ткани. • Тироксин, половые гормоны влияют на липидный обмен. Механизм не всегда ясен. Кастрация у животных влечет избыток отложения жира. • Простагландины угнетают аденилатциклазу, ослабляют влияние адреналина на липидный обмен
 Нарушения липидного обмена • • Нарушение всасывания и переваривания Недостаточное поступление панкреатической липазы в кишечник Недостаток поступления в кишечник желчи Заболевания пищеварительного тракта (энтериты, гиповитаминозы) Повреждение эпителия кишечника, операции на кишечнике Следствие – недопереваривание жиров, много нерасщепленного жира в кале, его белесость, много не всосавшихся жирных кислот.
Нарушения липидного обмена • • Нарушение всасывания и переваривания Недостаточное поступление панкреатической липазы в кишечник Недостаток поступления в кишечник желчи Заболевания пищеварительного тракта (энтериты, гиповитаминозы) Повреждение эпителия кишечника, операции на кишечнике Следствие – недопереваривание жиров, много нерасщепленного жира в кале, его белесость, много не всосавшихся жирных кислот.
 Нарушения липидного обмена Нарушения перехода жира из крови в ткани • Иногда жирные кислоты из хиломикронов плазмы крови не расщепляются. Причина – низкая активность липопротеинлипазы крови (триглицериды не гидролизуются). Плазма крови имеет молочный цвет – много хиломикронов. • Подходы к лечению: заменить природные жиры с разными (особенно длинными жирными кислотами) на синтетические с радикалами не более 8 -10 атомов С. Такие жирные кислоты всасываются из кишечника в кровь без образования хиломикронов.
Нарушения липидного обмена Нарушения перехода жира из крови в ткани • Иногда жирные кислоты из хиломикронов плазмы крови не расщепляются. Причина – низкая активность липопротеинлипазы крови (триглицериды не гидролизуются). Плазма крови имеет молочный цвет – много хиломикронов. • Подходы к лечению: заменить природные жиры с разными (особенно длинными жирными кислотами) на синтетические с радикалами не более 8 -10 атомов С. Такие жирные кислоты всасываются из кишечника в кровь без образования хиломикронов.
 Кетонемия и кетонурия При голодании и у больных сахарным диабетом содержание кетоновых тел в крови повышается до 20 ммоль/л, а также сопровождается кетонурией. В норме в моче в сутки 40 мг, а при диабете – 50 г и более. Причина: усиление липолиза – мобилизация жирных кислот в печень из жировых депо – интенсивное образование кетоновых тел – выход их из печени в кровь – идут к тканям (как топливо) – ткани не успевают использовать (как топливо) - кетонемия
Кетонемия и кетонурия При голодании и у больных сахарным диабетом содержание кетоновых тел в крови повышается до 20 ммоль/л, а также сопровождается кетонурией. В норме в моче в сутки 40 мг, а при диабете – 50 г и более. Причина: усиление липолиза – мобилизация жирных кислот в печень из жировых депо – интенсивное образование кетоновых тел – выход их из печени в кровь – идут к тканям (как топливо) – ткани не успевают использовать (как топливо) - кетонемия
 Атеросклероз • Атеросклероз развивается при повышении в плазме крови ЛПНП и ЛПОНП. Сами липопротеины не атерогенны, но если они химически изменены (перекисное окисление), то диеновые и триеновые коньюгаты, гидроперекиси, малоновый альдегид атакуют аполипротеины и модифицируют их. Место модификации – артериальная стенка. Они приобретают аутоантигенные свойства, на них вырабатываются аутоантитела, образуются комплексы антиген-антитело. Макрофаги захватывают эти комплексы, трансформируются в пенистые клетки, которые (разрушаясь) изливают во внутреннюю оболочку артерии холестерин. Попытка изолировать холестерин путем образования соединительнотканной (фиброзной) капсулы приводит к образованию бляшки – главного элемента склеротического поражения артерий.
Атеросклероз • Атеросклероз развивается при повышении в плазме крови ЛПНП и ЛПОНП. Сами липопротеины не атерогенны, но если они химически изменены (перекисное окисление), то диеновые и триеновые коньюгаты, гидроперекиси, малоновый альдегид атакуют аполипротеины и модифицируют их. Место модификации – артериальная стенка. Они приобретают аутоантигенные свойства, на них вырабатываются аутоантитела, образуются комплексы антиген-антитело. Макрофаги захватывают эти комплексы, трансформируются в пенистые клетки, которые (разрушаясь) изливают во внутреннюю оболочку артерии холестерин. Попытка изолировать холестерин путем образования соединительнотканной (фиброзной) капсулы приводит к образованию бляшки – главного элемента склеротического поражения артерий.
 Атеросклероз (продолжение) • Липопротеины высокой плотности (ЛПВП) – антиатерогенны. Они осуществляют обратный транспорт холестерина (от тканей в печень), где холестерин окисляется в желчные кислоты. ЛПВП еще и протекторы перекисного окисления, т. е. работают как антиоксиданты. Поэтому высокий уровень ЛПВП – это показатель устойчивости, сопротивляемости развитию атеросклероза.
Атеросклероз (продолжение) • Липопротеины высокой плотности (ЛПВП) – антиатерогенны. Они осуществляют обратный транспорт холестерина (от тканей в печень), где холестерин окисляется в желчные кислоты. ЛПВП еще и протекторы перекисного окисления, т. е. работают как антиоксиданты. Поэтому высокий уровень ЛПВП – это показатель устойчивости, сопротивляемости развитию атеросклероза.
 Дислипопротеинемиии (ДЛП) Это изменение нормального соотношения липопротеинов: повышение, снижение, полное отсутствие или появление новых, необычных, патологических ЛП. • Гиперхиломикронемия – много ХМ, много триглицеридов в сыворотке крови. Клинически – ксантоматоз (избыточное отложение липидов под кожей). • Гипербеталипопротеинемия - много ЛПОНП и ЛПНП в крови, следовательно много холестерина (а иногда и триглицеридов). Клинически проявляется как атеросклероз и развивается ишемическая болезнь сердца (ИБС).
Дислипопротеинемиии (ДЛП) Это изменение нормального соотношения липопротеинов: повышение, снижение, полное отсутствие или появление новых, необычных, патологических ЛП. • Гиперхиломикронемия – много ХМ, много триглицеридов в сыворотке крови. Клинически – ксантоматоз (избыточное отложение липидов под кожей). • Гипербеталипопротеинемия - много ЛПОНП и ЛПНП в крови, следовательно много холестерина (а иногда и триглицеридов). Клинически проявляется как атеросклероз и развивается ишемическая болезнь сердца (ИБС).
 Дислипопротеинемиии (продолжение) • Дисбеталипопротеинемия – флотирующие липопротеины с большим содержанием холестерина. ЛПОНП не превращаются в ЛПНП. Клинически: атеросклероз, ИБС, поражение сосудов ног. • Гиперпребеталипопротеинемия. Много ЛПОНП, мало ХМ, много триглицеридов. Наблюдается при диабете, ожирении, ИБС. • Гиперпребеталипопротеинемия в сочетании с гиперхиломикронемией. Много ЛПОНП, много ХМ. Клинически проявляется ксантоматозом, сочетается со скрытым диабетом. ИБС не наблюдается при этом виде липопротеинемии.
Дислипопротеинемиии (продолжение) • Дисбеталипопротеинемия – флотирующие липопротеины с большим содержанием холестерина. ЛПОНП не превращаются в ЛПНП. Клинически: атеросклероз, ИБС, поражение сосудов ног. • Гиперпребеталипопротеинемия. Много ЛПОНП, мало ХМ, много триглицеридов. Наблюдается при диабете, ожирении, ИБС. • Гиперпребеталипопротеинемия в сочетании с гиперхиломикронемией. Много ЛПОНП, много ХМ. Клинически проявляется ксантоматозом, сочетается со скрытым диабетом. ИБС не наблюдается при этом виде липопротеинемии.
 Липопротеины при прогнозировании ИБС • Для предсказания ИБС уровень холестерина в ЛПВП в 8 раз чувствительнее, чем холестерин в ЛПНП. • Коэффициент атерогенности К : К = холестерин ЛПНП+холестерин ЛПОНП/холестерин ЛПВП • Более удобная модификация К = общий холестерин – холестерин ЛПВП/холестерин ЛПВП К у здоровых людей не более 3. Чем коэффициент выше – тем выше риск развития ИБС (или уже наличия ИБС).
Липопротеины при прогнозировании ИБС • Для предсказания ИБС уровень холестерина в ЛПВП в 8 раз чувствительнее, чем холестерин в ЛПНП. • Коэффициент атерогенности К : К = холестерин ЛПНП+холестерин ЛПОНП/холестерин ЛПВП • Более удобная модификация К = общий холестерин – холестерин ЛПВП/холестерин ЛПВП К у здоровых людей не более 3. Чем коэффициент выше – тем выше риск развития ИБС (или уже наличия ИБС).
 Липосомы – липидные искусственные частицы • Частицы состоят из фосфолипидных бислоев, разделенных водной фазой с размером от 25 до 10000 нм. • Получаются встряхиванием или ультразвуковой обработкой суспензии фосфолипидов (из природных или синтетических). • Сначала липосомы использовались для научных опытов как модели мембран. Теперь их используют как контейнеры для лекарств, ферментов, гормонов, витаминов, антибиотиков и т. д. • Преимущество: липосомы позволяют доставить в клетку вещества, которые сами не пройдут через клеточную мем -брану; присоединение к липосоме антител (адресвектор) позволяет найти клетку мишень; препарат, включенный в липосому, доставляется точно по адресу, а не растворяет-ся в крови и не проходит по желудочнокишечному тракту.
Липосомы – липидные искусственные частицы • Частицы состоят из фосфолипидных бислоев, разделенных водной фазой с размером от 25 до 10000 нм. • Получаются встряхиванием или ультразвуковой обработкой суспензии фосфолипидов (из природных или синтетических). • Сначала липосомы использовались для научных опытов как модели мембран. Теперь их используют как контейнеры для лекарств, ферментов, гормонов, витаминов, антибиотиков и т. д. • Преимущество: липосомы позволяют доставить в клетку вещества, которые сами не пройдут через клеточную мем -брану; присоединение к липосоме антител (адресвектор) позволяет найти клетку мишень; препарат, включенный в липосому, доставляется точно по адресу, а не растворяет-ся в крови и не проходит по желудочнокишечному тракту.
 Липосомы – липидные искусственные частицы (продолжение) • Есть 2 пути проникновения липосом в клетку: или липосома захватывается клеткой, а лизосомальные ферменты ее растворяют внутри клетки, или липосома сливается с клеточной мембраной, встраивается в нее, а препарат проникает из липосомы в цитоплазму клеток. • Основные пути введения: внутривенно, внутрибрюшинно, внутримышечно и попадают в печень или селезенку. • Ведутся поиски, метод новый и перспективный.
Липосомы – липидные искусственные частицы (продолжение) • Есть 2 пути проникновения липосом в клетку: или липосома захватывается клеткой, а лизосомальные ферменты ее растворяют внутри клетки, или липосома сливается с клеточной мембраной, встраивается в нее, а препарат проникает из липосомы в цитоплазму клеток. • Основные пути введения: внутривенно, внутрибрюшинно, внутримышечно и попадают в печень или селезенку. • Ведутся поиски, метод новый и перспективный.
 Ожирение • В норме в зависимости от пола у человека от 15 до 25% жировой ткани. • Ожирение – фактор риска развития инфаркта, инсульта, диабета, гипертонии, желчекаменной болезни. • Количество жировых клеток у взрослого постоянно, но они могут или «худеть» , или увеличиваться. • Первичное ожирение – это дисбаланс избыточной калорийности питания и сниженного расхода энергии (поддержание жизни, температуры тела и физической работы).
Ожирение • В норме в зависимости от пола у человека от 15 до 25% жировой ткани. • Ожирение – фактор риска развития инфаркта, инсульта, диабета, гипертонии, желчекаменной болезни. • Количество жировых клеток у взрослого постоянно, но они могут или «худеть» , или увеличиваться. • Первичное ожирение – это дисбаланс избыточной калорийности питания и сниженного расхода энергии (поддержание жизни, температуры тела и физической работы).
 Ожирение (продолжение) • Причины первичного ожирения – генетические нарушения, состав и количество пищи, тактика питания (перед сном), уровень активности, психологические факторы. Генетические (предопределяющие) факторы – это крен метаболизма в сторону рационального обмена (малый расход энергии). Переключение на «бесполезный» анаэробный гликолиз сжигает больше глюкозы и снижается ее переработка в жиры. А у склонных к ожирению лучше сопряжены дыхание и синтез АТФ. • Вторичное ожирение – развивается как следствие основного (чаще эндокринного) заболевания. Например, гипогонадизм, гипотиреоз, болезнь Иценко-Кушинга (повышение АКТГ при опухолях гипофиза или коры надпочечников).
Ожирение (продолжение) • Причины первичного ожирения – генетические нарушения, состав и количество пищи, тактика питания (перед сном), уровень активности, психологические факторы. Генетические (предопределяющие) факторы – это крен метаболизма в сторону рационального обмена (малый расход энергии). Переключение на «бесполезный» анаэробный гликолиз сжигает больше глюкозы и снижается ее переработка в жиры. А у склонных к ожирению лучше сопряжены дыхание и синтез АТФ. • Вторичное ожирение – развивается как следствие основного (чаще эндокринного) заболевания. Например, гипогонадизм, гипотиреоз, болезнь Иценко-Кушинга (повышение АКТГ при опухолях гипофиза или коры надпочечников).
 Роль лептина в ожирении У человека есть ген ожирения. Он кодирует белок лептин, который синтезируется адипоцитами, взаимодействует с рецепторами гипоталамуса, а он снижает секрецию нейропептида, который стимулирует пищевое поведение. У тучных людей лептина в 4 раза больше, а все равно нейропептид продолжает синтезироваться и стимулирует потребление пищи. Причина – нет рецепторов для лептина в гипоталамусе. Или мутации в гене лептина, которые приводят к ожирению (сопутствует ожирению, снижает физическую активность, стимулирует диабет 2 типа). Ожирение – полигенное заболевание, а не только переедание. Мало лептина в крови – это сигнал недостаточности количества жира в организме, а следовательно растет аппетит и растет масса тела.
Роль лептина в ожирении У человека есть ген ожирения. Он кодирует белок лептин, который синтезируется адипоцитами, взаимодействует с рецепторами гипоталамуса, а он снижает секрецию нейропептида, который стимулирует пищевое поведение. У тучных людей лептина в 4 раза больше, а все равно нейропептид продолжает синтезироваться и стимулирует потребление пищи. Причина – нет рецепторов для лептина в гипоталамусе. Или мутации в гене лептина, которые приводят к ожирению (сопутствует ожирению, снижает физическую активность, стимулирует диабет 2 типа). Ожирение – полигенное заболевание, а не только переедание. Мало лептина в крови – это сигнал недостаточности количества жира в организме, а следовательно растет аппетит и растет масса тела.


