9c54054e7bd0e18ff21401e66434c60e.ppt
- Количество слайдов: 36
 Pengilangan minyak dan produknya chemistry. slss. ie
Pengilangan minyak dan produknya chemistry. slss. ie
 Produk produk hidrokarbon Bensin (cair) gas Aspal (padat)
Produk produk hidrokarbon Bensin (cair) gas Aspal (padat)
 Petroleum • (petroleum, yunani: πέτρα (batuan) + oleum (minyak) • Terbentuk dalam lapisan bumi • Proses pengilangan membentuk bahan bakar • Terdiri dari senyawa hidrokarbon (senyawa organik) • Termasuk minyak mentah dan minyak olahan • Terbentuk dari fosil mahluk hidup seperti zooplankton dan alga yang mengalami tekanan dan panas
Petroleum • (petroleum, yunani: πέτρα (batuan) + oleum (minyak) • Terbentuk dalam lapisan bumi • Proses pengilangan membentuk bahan bakar • Terdiri dari senyawa hidrokarbon (senyawa organik) • Termasuk minyak mentah dan minyak olahan • Terbentuk dari fosil mahluk hidup seperti zooplankton dan alga yang mengalami tekanan dan panas
 Petroleum Campuran kompleks hidrokarbon yang terdapat pada lapisan bumi dalam bentuk gas (gas alam), cair (crude oil), padat (lilin , aspal). komposisi Minyak mentah Hidrokarbon padat Hidrokarbon cair : pentana dll Hidrokrbon gas: metana, propana, butana
Petroleum Campuran kompleks hidrokarbon yang terdapat pada lapisan bumi dalam bentuk gas (gas alam), cair (crude oil), padat (lilin , aspal). komposisi Minyak mentah Hidrokarbon padat Hidrokarbon cair : pentana dll Hidrokrbon gas: metana, propana, butana
 Apakah Minyak Mentah? • Minyak mentah merupakan campuran senyawa-senyawa hidrokarbon dari bahan organik. • Minyak mentah bervariasi tergatung komposisinya www. csub. edu/
Apakah Minyak Mentah? • Minyak mentah merupakan campuran senyawa-senyawa hidrokarbon dari bahan organik. • Minyak mentah bervariasi tergatung komposisinya www. csub. edu/
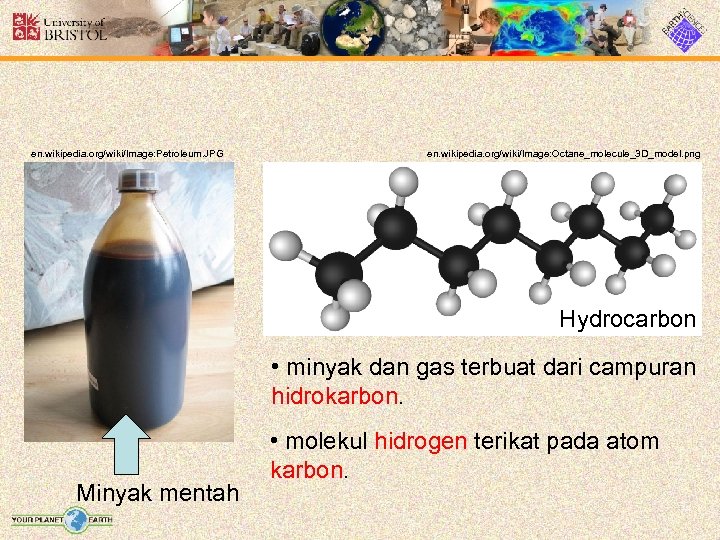 en. wikipedia. org/wiki/Image: Petroleum. JPG en. wikipedia. org/wiki/Image: Octane_molecule_3 D_model. png Hydrocarbon • minyak dan gas terbuat dari campuran hidrokarbon. Minyak mentah • molekul hidrogen terikat pada atom karbon.
en. wikipedia. org/wiki/Image: Petroleum. JPG en. wikipedia. org/wiki/Image: Octane_molecule_3 D_model. png Hydrocarbon • minyak dan gas terbuat dari campuran hidrokarbon. Minyak mentah • molekul hidrogen terikat pada atom karbon.
 Komposisi berdasar berat Unsur persentase karbon 83 to 85% Hidrogen 10 to 14% Nitrogen 0. 1 to 2% Oksigen 0. 05 to 1. 5% Sulfur 0. 05 to 6. 0% Logam < 0. 1%
Komposisi berdasar berat Unsur persentase karbon 83 to 85% Hidrogen 10 to 14% Nitrogen 0. 1 to 2% Oksigen 0. 05 to 1. 5% Sulfur 0. 05 to 6. 0% Logam < 0. 1%
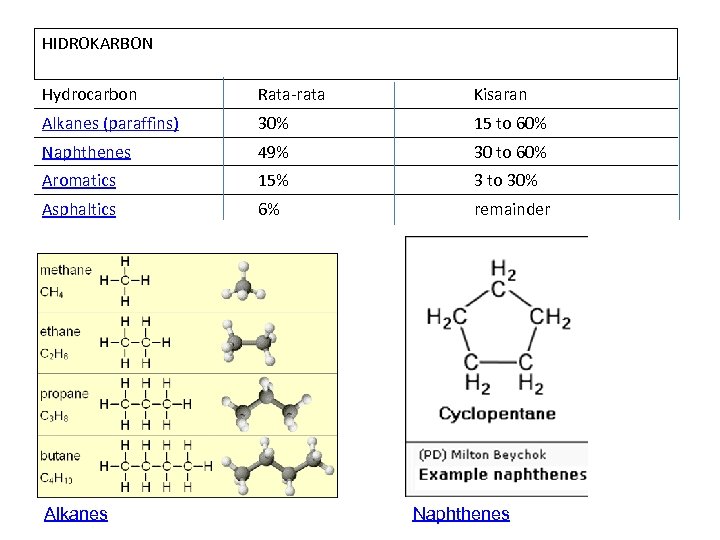 HIDROKARBON Hydrocarbon Rata-rata Kisaran Alkanes (paraffins) 30% 15 to 60% Naphthenes 49% 30 to 60% Aromatics 15% 3 to 30% Asphaltics 6% remainder Alkanes Naphthenes
HIDROKARBON Hydrocarbon Rata-rata Kisaran Alkanes (paraffins) 30% 15 to 60% Naphthenes 49% 30 to 60% Aromatics 15% 3 to 30% Asphaltics 6% remainder Alkanes Naphthenes
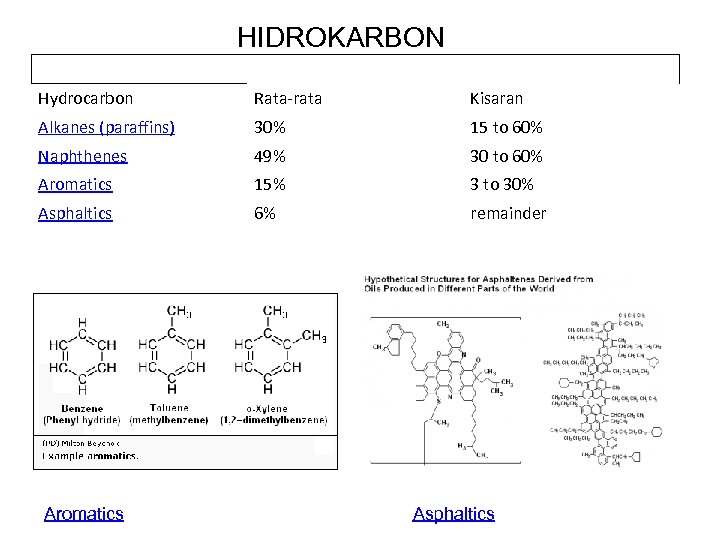 HIDROKARBON Hydrocarbon Rata-rata Kisaran Alkanes (paraffins) 30% 15 to 60% Naphthenes 49% 30 to 60% Aromatics 15% 3 to 30% Asphaltics 6% remainder Aromatics Asphaltics
HIDROKARBON Hydrocarbon Rata-rata Kisaran Alkanes (paraffins) 30% 15 to 60% Naphthenes 49% 30 to 60% Aromatics 15% 3 to 30% Asphaltics 6% remainder Aromatics Asphaltics
 Petrol and Crude Oil l Crude oil is separated by fractional distillation l works because the molecules have different boiling/condensation points l many of these hydrocarbons are alkanes, and are sorted into fractions l each fraction has a range of boiling points in the distillation l narrow boiling ranges of limited carbon number (eg light gasoline is C 5 to C 7 boiling point 25 C -75 C)
Petrol and Crude Oil l Crude oil is separated by fractional distillation l works because the molecules have different boiling/condensation points l many of these hydrocarbons are alkanes, and are sorted into fractions l each fraction has a range of boiling points in the distillation l narrow boiling ranges of limited carbon number (eg light gasoline is C 5 to C 7 boiling point 25 C -75 C)
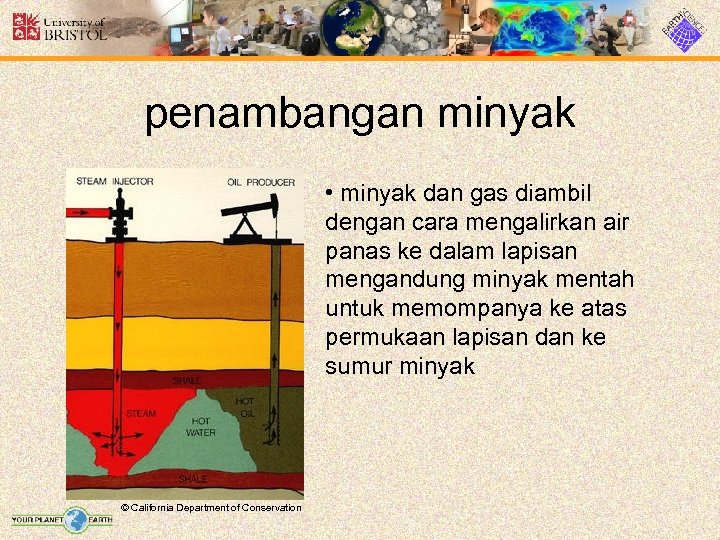 penambangan minyak • minyak dan gas diambil dengan cara mengalirkan air panas ke dalam lapisan mengandung minyak mentah untuk memompanya ke atas permukaan lapisan dan ke sumur minyak © California Department of Conservation
penambangan minyak • minyak dan gas diambil dengan cara mengalirkan air panas ke dalam lapisan mengandung minyak mentah untuk memompanya ke atas permukaan lapisan dan ke sumur minyak © California Department of Conservation
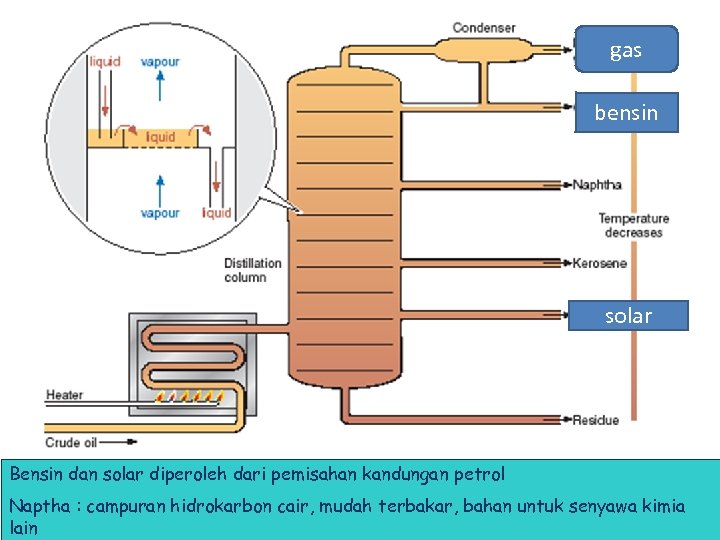 gas bensin solar Bensin dan solar diperoleh dari pemisahan kandungan petrol Naptha : campuran hidrokarbon cair, mudah terbakar, bahan untuk senyawa kimia lain
gas bensin solar Bensin dan solar diperoleh dari pemisahan kandungan petrol Naptha : campuran hidrokarbon cair, mudah terbakar, bahan untuk senyawa kimia lain
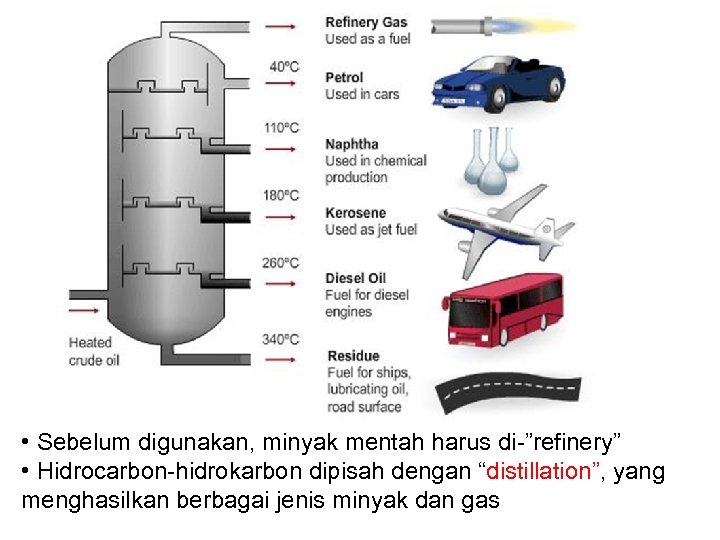 • Sebelum digunakan, minyak mentah harus di-”refinery” • Hidrocarbon-hidrokarbon dipisah dengan “distillation”, yang menghasilkan berbagai jenis minyak dan gas
• Sebelum digunakan, minyak mentah harus di-”refinery” • Hidrocarbon-hidrokarbon dipisah dengan “distillation”, yang menghasilkan berbagai jenis minyak dan gas
 Hasil Fraksionasi minyak mentah l l l Refinery Gas (LPG) Light Gasoline (Petrol) Naphtha (Petrol) Kerosene (Jet Fuel) Gas Oil (Diesel Fuel) Residue Fractions (Bitumen)
Hasil Fraksionasi minyak mentah l l l Refinery Gas (LPG) Light Gasoline (Petrol) Naphtha (Petrol) Kerosene (Jet Fuel) Gas Oil (Diesel Fuel) Residue Fractions (Bitumen)
 Gas alam l l l Domestik dan industri. methane, CH 4, (sedikitnya 85%), ethane, C 2 H 6, (sampai 10%) propane, C 3 H 8, butane, C 4 H 10.
Gas alam l l l Domestik dan industri. methane, CH 4, (sedikitnya 85%), ethane, C 2 H 6, (sampai 10%) propane, C 3 H 8, butane, C 4 H 10.
 Liquid Petroleum Gas (LPG) l l Gas dalam kemasan tabung (domestik). Propana dan butana (mudah berupa cair dalam tekanan tertentu)
Liquid Petroleum Gas (LPG) l l Gas dalam kemasan tabung (domestik). Propana dan butana (mudah berupa cair dalam tekanan tertentu)
 Mercaptans l l l Sangat bau, senyawa sulfur organik, disebut mercaptan Ditambahkan pada gas alam atau elpiji Mempermudah mendeteksi kebocoran gas
Mercaptans l l l Sangat bau, senyawa sulfur organik, disebut mercaptan Ditambahkan pada gas alam atau elpiji Mempermudah mendeteksi kebocoran gas
 Komposisi BENSIN l Campuran kompleks senyawa kimia l Senyawa utama : Hidrokarbon l Alkana bercabang l Senyawa Aromatik
Komposisi BENSIN l Campuran kompleks senyawa kimia l Senyawa utama : Hidrokarbon l Alkana bercabang l Senyawa Aromatik
 Bensin dalam Mesin Pembakaran l l l Menjadi uap Bercampur dgn udara Mengalami kompresi (tekanan) Terpercik api (oleh busi) dan terbakar Terbentuk gas yang mengembang Terbentuk tenaga
Bensin dalam Mesin Pembakaran l l l Menjadi uap Bercampur dgn udara Mengalami kompresi (tekanan) Terpercik api (oleh busi) dan terbakar Terbentuk gas yang mengembang Terbentuk tenaga
 Bensin dalam Mesin Pembakaran l Bilangan oktan adalah angka yang menunjukkan seberapa besar tekanan yang bisa diberikan sebelum bensin terbakar secara spontan.
Bensin dalam Mesin Pembakaran l Bilangan oktan adalah angka yang menunjukkan seberapa besar tekanan yang bisa diberikan sebelum bensin terbakar secara spontan.
 Pembakaran dini dalam mesin Di dalam mesin, campuran udara dan bensin (dalam bentuk gas) ditekan oleh piston sampai dengan volume yang sangat kecil Kemudian dibakar oleh percikan api oleh busi. Karena besarnya tekanan ini, campuran udara dan bensin juga bisa terbakar secara spontan sebelum percikan api dari busi keluar. Jika campuran gas ini terbakar karena tekanan yang tinggi (bukan karena percikan api dari busi), akan terjadi knocking atau ketukan di dalam mesin yg merusak mesin. kita hindari
Pembakaran dini dalam mesin Di dalam mesin, campuran udara dan bensin (dalam bentuk gas) ditekan oleh piston sampai dengan volume yang sangat kecil Kemudian dibakar oleh percikan api oleh busi. Karena besarnya tekanan ini, campuran udara dan bensin juga bisa terbakar secara spontan sebelum percikan api dari busi keluar. Jika campuran gas ini terbakar karena tekanan yang tinggi (bukan karena percikan api dari busi), akan terjadi knocking atau ketukan di dalam mesin yg merusak mesin. kita hindari
 Pembakaran dini l l l Problem: Auto-ignition (i. e. knocking or pinking) Effects: a) hilang tenaga b) kerusakan mesin Solusi: a) ditamah zat additives b) atur campuran dengan senyawa oktan tinggi
Pembakaran dini l l l Problem: Auto-ignition (i. e. knocking or pinking) Effects: a) hilang tenaga b) kerusakan mesin Solusi: a) ditamah zat additives b) atur campuran dengan senyawa oktan tinggi
 Bilangan Oktan l Mengukur kecenderungan ketahanan terbakar secara spontan atau Mengukur kecenderungan penyebab “knocking” l Makin rendah bilangan oktan, makin mudah terbakar secara spontan
Bilangan Oktan l Mengukur kecenderungan ketahanan terbakar secara spontan atau Mengukur kecenderungan penyebab “knocking” l Makin rendah bilangan oktan, makin mudah terbakar secara spontan
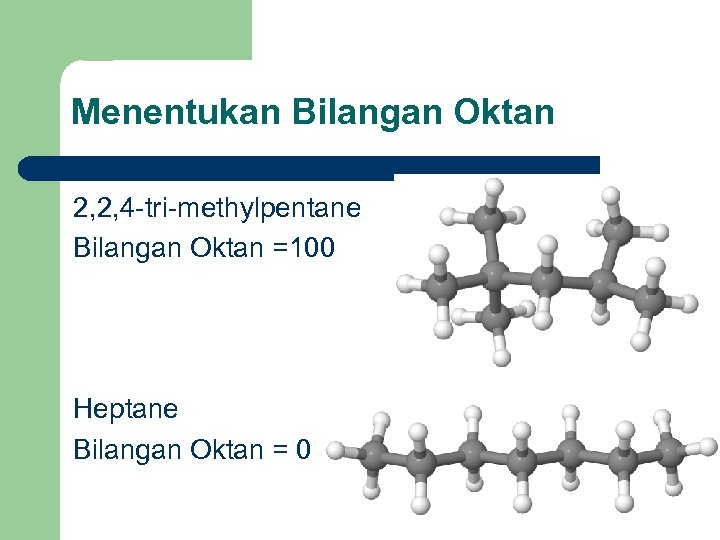 Menentukan Bilangan Oktan 2, 2, 4 -tri-methylpentane Bilangan Oktan =100 Heptane Bilangan Oktan = 0
Menentukan Bilangan Oktan 2, 2, 4 -tri-methylpentane Bilangan Oktan =100 Heptane Bilangan Oktan = 0
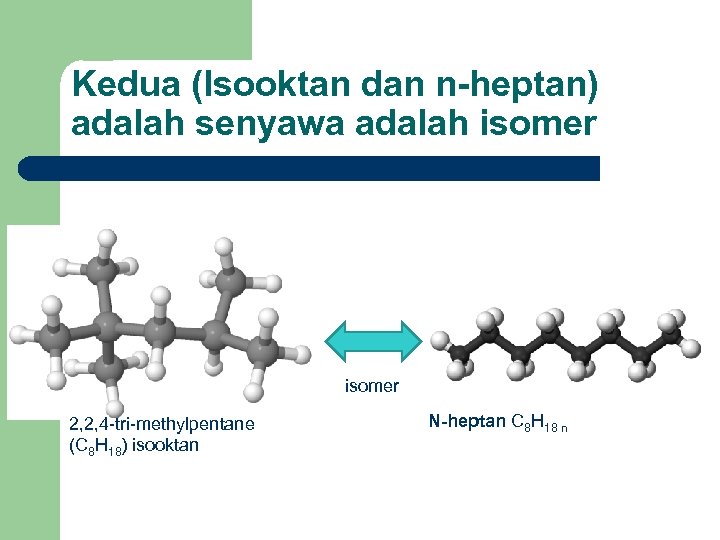 Kedua (Isooktan dan n-heptan) adalah senyawa adalah isomer 2, 2, 4 -tri-methylpentane (C 8 H 18) isooktan N-heptan C 8 H 18 n
Kedua (Isooktan dan n-heptan) adalah senyawa adalah isomer 2, 2, 4 -tri-methylpentane (C 8 H 18) isooktan N-heptan C 8 H 18 n
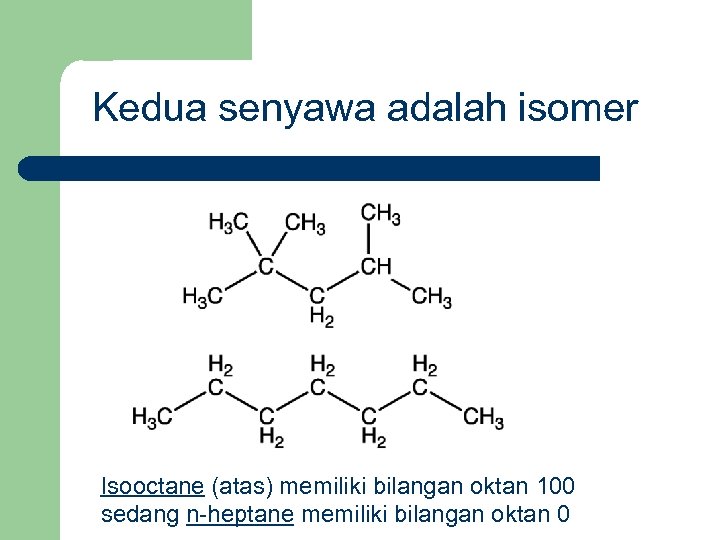 Kedua senyawa adalah isomer Isooctane (atas) memiliki bilangan oktan 100 sedang n-heptane memiliki bilangan oktan 0
Kedua senyawa adalah isomer Isooctane (atas) memiliki bilangan oktan 100 sedang n-heptane memiliki bilangan oktan 0
 SHATOX SX-200 PORTABLE OCTANE TESTER http: //www. shatox. com/octanetester. html
SHATOX SX-200 PORTABLE OCTANE TESTER http: //www. shatox. com/octanetester. html
 Dasar penetapan Bilangan Oktan • Bilangan oktan suatu bensin dapat ditentukan melalui uji pembakaran sampel bensin untuk memperoleh karakteristik pembakarannya. • Karakteristik tersebut kemudian dibandingkan dengan karakteristik pembakaran dari berbagai campuran n-heptana dan isooktana. • Jika ada karakteristik yang sesuai, maka kadar isooktana dalam campuran n-heptana dan isooktana tersebut digunakan untuk menyatakan nilai bilangan oktan dari bensin yang diuji.
Dasar penetapan Bilangan Oktan • Bilangan oktan suatu bensin dapat ditentukan melalui uji pembakaran sampel bensin untuk memperoleh karakteristik pembakarannya. • Karakteristik tersebut kemudian dibandingkan dengan karakteristik pembakaran dari berbagai campuran n-heptana dan isooktana. • Jika ada karakteristik yang sesuai, maka kadar isooktana dalam campuran n-heptana dan isooktana tersebut digunakan untuk menyatakan nilai bilangan oktan dari bensin yang diuji.
 Penambahan senyawa untuk tingkatkan bilangan oktan (i) l l l (ii) l l Timbal seperti “tetra ethyl lead” Melindungi reaksi pembakaran Dampak negatif terhadap lingkungan Dilarang sejak tahun 2000 Oksigenasi Naikkan bailangan oktan Polusi sedikit
Penambahan senyawa untuk tingkatkan bilangan oktan (i) l l l (ii) l l Timbal seperti “tetra ethyl lead” Melindungi reaksi pembakaran Dampak negatif terhadap lingkungan Dilarang sejak tahun 2000 Oksigenasi Naikkan bailangan oktan Polusi sedikit
 Campuran senyawa yang menaikkan bilangan oktan Molecular features: l Menambah jumlah cabang hidrokarbon l Memperpendek rantai hidrokarbon l Adanya cincin hidrokarbon
Campuran senyawa yang menaikkan bilangan oktan Molecular features: l Menambah jumlah cabang hidrokarbon l Memperpendek rantai hidrokarbon l Adanya cincin hidrokarbon
 31
31
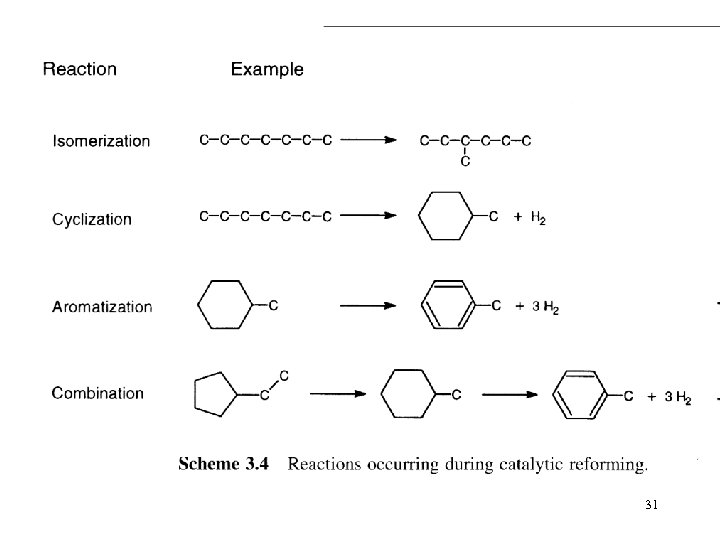
 untuk tingkatkan bilangan oktan, bisa juga dengan: 1. Isomerisation 2. Dehydrocyclisation 3. Catalytic cracking All three methods involve the use of catalysts
untuk tingkatkan bilangan oktan, bisa juga dengan: 1. Isomerisation 2. Dehydrocyclisation 3. Catalytic cracking All three methods involve the use of catalysts
 Isomerisasi l l alkana seperti : pentana C─C─C (O. N. 62) Panaskan Rantaian terputus Satukan lagi putusan rantai menjadi, msal: . 2 methylbutane C─C─C─C │ (O. N. 93) C
Isomerisasi l l alkana seperti : pentana C─C─C (O. N. 62) Panaskan Rantaian terputus Satukan lagi putusan rantai menjadi, msal: . 2 methylbutane C─C─C─C │ (O. N. 93) C
 Dehydrocyclisation l l l Rantai tidak bercabang : hexane (O. N. 25) Katalisator merubah heksana jadi cycloalkane (O. N. 83) C 6 H 14 → (CH 2)6 + H 2 Katalisator merubah cycloalkane menjadi senyawa aromatik ( benzene) (O. N. >100) (CH 2)6 → 3 H 2 + C 6 H 6 Benzene
Dehydrocyclisation l l l Rantai tidak bercabang : hexane (O. N. 25) Katalisator merubah heksana jadi cycloalkane (O. N. 83) C 6 H 14 → (CH 2)6 + H 2 Katalisator merubah cycloalkane menjadi senyawa aromatik ( benzene) (O. N. >100) (CH 2)6 → 3 H 2 + C 6 H 6 Benzene
 Pemecahan senyawa l l kerosine atau diesel yang kompleks Dengan suhu tinggi dan katalisator, menjadi senyawa yang sederhana Menjadi senyawa rantai jenuh (bilangan oktan jadi tinggi)
Pemecahan senyawa l l kerosine atau diesel yang kompleks Dengan suhu tinggi dan katalisator, menjadi senyawa yang sederhana Menjadi senyawa rantai jenuh (bilangan oktan jadi tinggi)
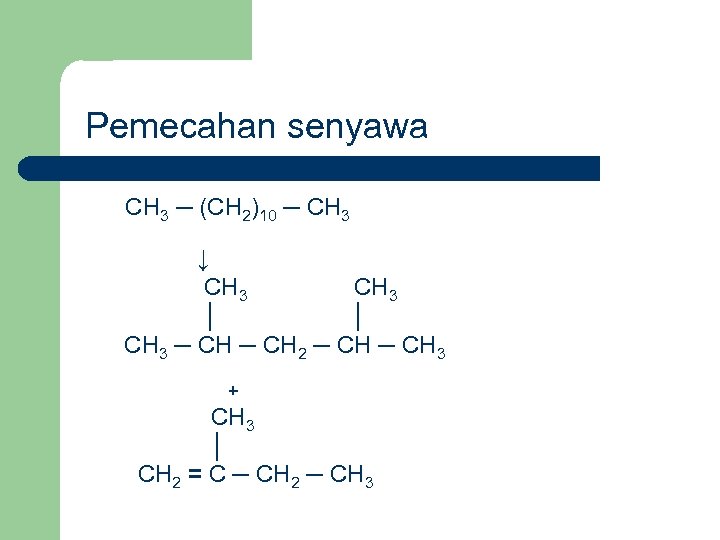 Pemecahan senyawa CH 3 ─ (CH 2)10 ─ CH 3 ↓ CH 3 │ │ CH 3 ─ CH 2 ─ CH 3 + CH 3 │ CH 2 = C ─ CH 2 ─ CH 3
Pemecahan senyawa CH 3 ─ (CH 2)10 ─ CH 3 ↓ CH 3 │ │ CH 3 ─ CH 2 ─ CH 3 + CH 3 │ CH 2 = C ─ CH 2 ─ CH 3


