простейшие 1.ppt
- Количество слайдов: 101
 Патогенные простейшие Зав. кафедрой д. м. н. , профессор Г. И. Чубенко
Патогенные простейшие Зав. кафедрой д. м. н. , профессор Г. И. Чубенко
 Общая характеристика Одноклеточные животные Эукариоты Размер от 2 до 100 мкм Размножение половое и бесполое Имеют жизненный цикл развития В неблагоприятных условиях образуют цисты
Общая характеристика Одноклеточные животные Эукариоты Размер от 2 до 100 мкм Размножение половое и бесполое Имеют жизненный цикл развития В неблагоприятных условиях образуют цисты
 Таксономия простейших Царство: Animalia Подцарство: Protozoa (7 типов) Тип: Ciliophora (реснитчатые) Apicomplexa (споровики) Sarcomastigophora (саркодовые и жгутиконосцы)
Таксономия простейших Царство: Animalia Подцарство: Protozoa (7 типов) Тип: Ciliophora (реснитчатые) Apicomplexa (споровики) Sarcomastigophora (саркодовые и жгутиконосцы)
 Таксономия простейших Класс: Sarcodina Роды: Entamoeba Acanthamoeba Negleria Класс: Mastigophora Роды: Trypanosoma Lamblia Trichomonas Giardia Leishmania Класс: Sporozoa Роды: Plasmodium Toxoplasma Jsospora Sarcocystis Cryptosporidium Cyclospora Babesia Класс: Kinetofragminophores Род: Balantidium Класс: Microsporea Род: Microspora
Таксономия простейших Класс: Sarcodina Роды: Entamoeba Acanthamoeba Negleria Класс: Mastigophora Роды: Trypanosoma Lamblia Trichomonas Giardia Leishmania Класс: Sporozoa Роды: Plasmodium Toxoplasma Jsospora Sarcocystis Cryptosporidium Cyclospora Babesia Класс: Kinetofragminophores Род: Balantidium Класс: Microsporea Род: Microspora

 Возбудители малярии природно эндемического заболевания с трансмиссивным путем передачи
Возбудители малярии природно эндемического заболевания с трансмиссивным путем передачи
 Малярия широко распространена во всех странах африканского континента и Южной Америки, в Азии и на островах Тихого Океана. в Африке ежегодно заболевают малярией 100 млн человек и около 1 млн больных умирают. В Индии и Бразилии ежегодно регистрируется до 2, 6 млн больных малярией
Малярия широко распространена во всех странах африканского континента и Южной Америки, в Азии и на островах Тихого Океана. в Африке ежегодно заболевают малярией 100 млн человек и около 1 млн больных умирают. В Индии и Бразилии ежегодно регистрируется до 2, 6 млн больных малярией
 В России ежегодно регистрируется более ста случаев малярии, в том числе и в Москве. В Приморье в 2000 г 6 сл. 2001 г. 4 сл. Завозные случаи тропической малярии в основном обусловливают и летальность.
В России ежегодно регистрируется более ста случаев малярии, в том числе и в Москве. В Приморье в 2000 г 6 сл. 2001 г. 4 сл. Завозные случаи тропической малярии в основном обусловливают и летальность.
 Малярия — собирательное название для группы инфекций, вызываемых простейшими рода Plasmodium.
Малярия — собирательное название для группы инфекций, вызываемых простейшими рода Plasmodium.
 Более 100 видов плазмодиев паразитирует у позвоночных животных: ящериц, птиц, грызунов, обезьян. Некоторые виды, паразитирующие у обезьян, морфологически близки к возбудителям у человека.
Более 100 видов плазмодиев паразитирует у позвоночных животных: ящериц, птиц, грызунов, обезьян. Некоторые виды, паразитирующие у обезьян, морфологически близки к возбудителям у человека.
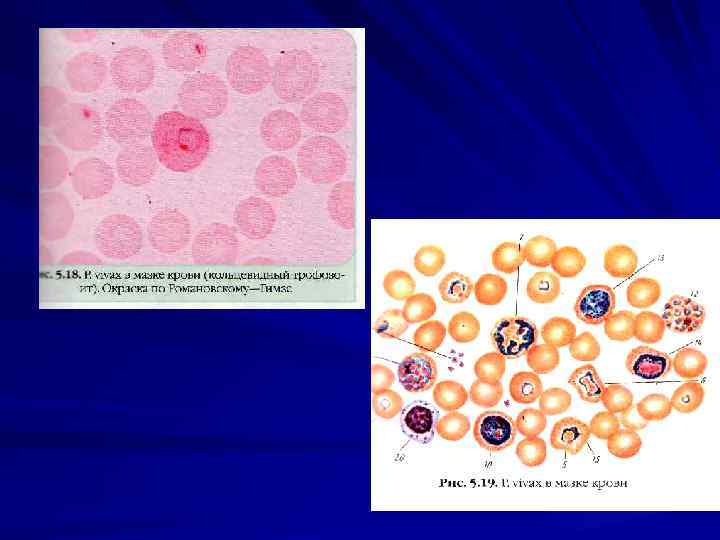
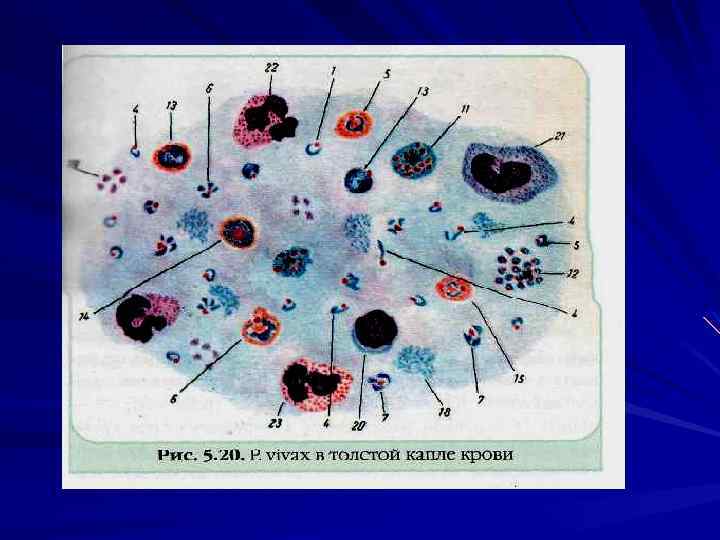
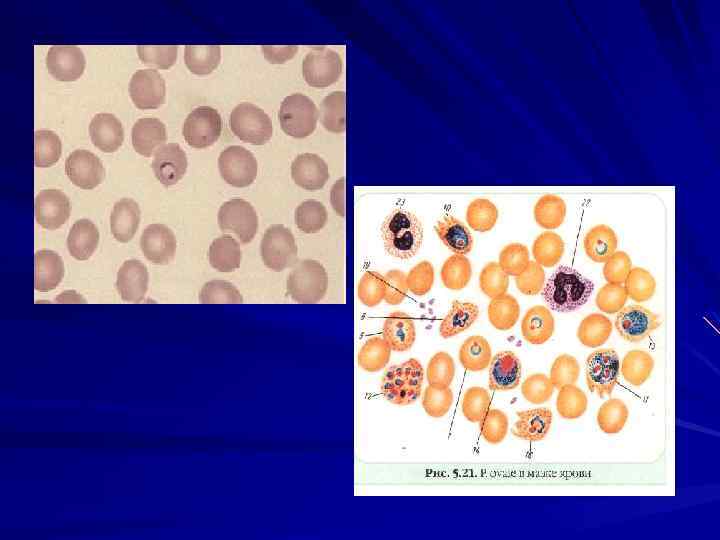
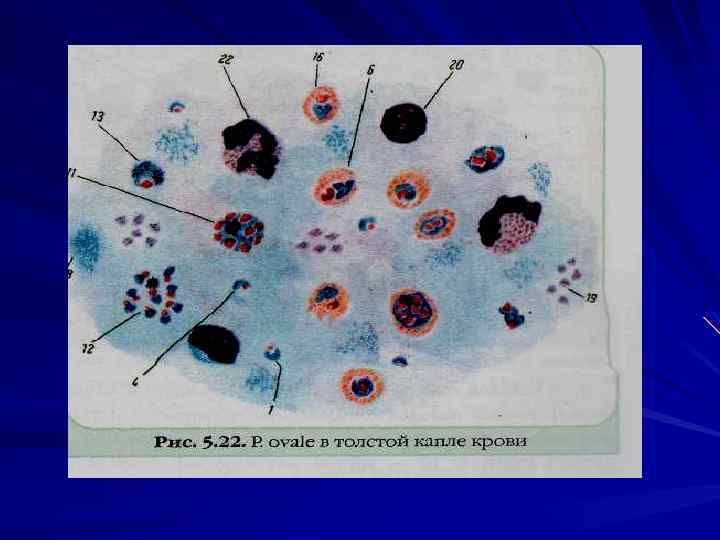
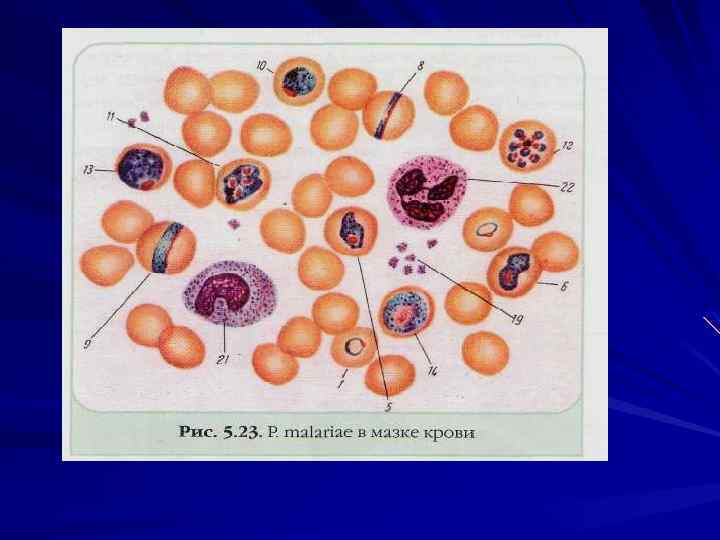
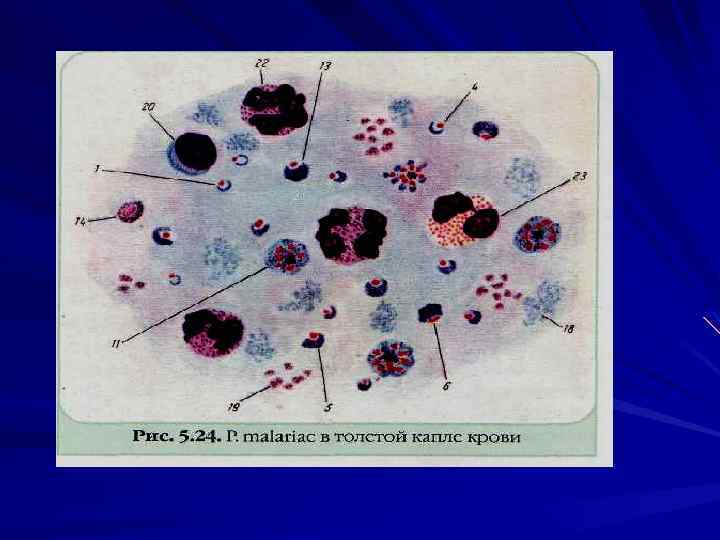
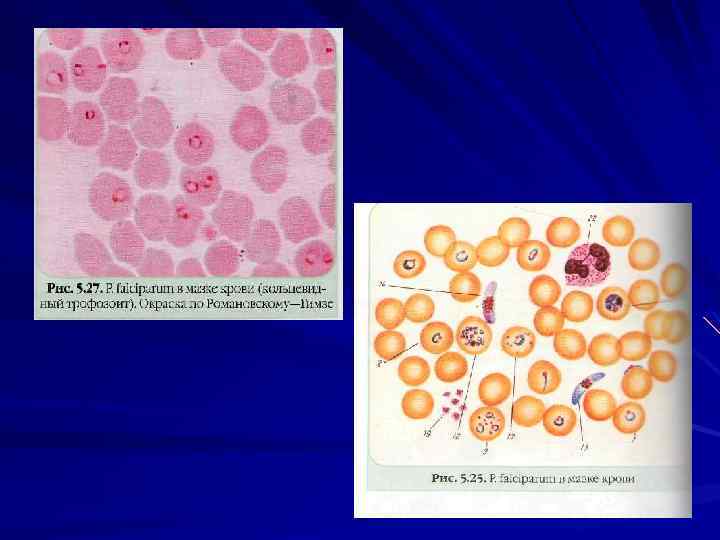
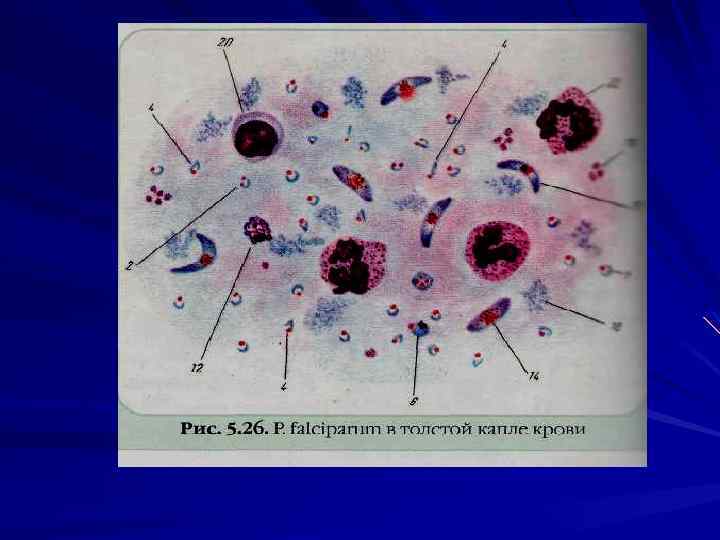
 У человека малярию вызывают 4 вида плазмодиев: P. vivax — возбудитель трехдневной малярии, P. malariae — возбудитель четырехдневной малярии, P. ovale — возбудитель особой формы малярии трехдневного типа, так называемой овале малярии P. falciparum — возбудитель тропической малярии.
У человека малярию вызывают 4 вида плазмодиев: P. vivax — возбудитель трехдневной малярии, P. malariae — возбудитель четырехдневной малярии, P. ovale — возбудитель особой формы малярии трехдневного типа, так называемой овале малярии P. falciparum — возбудитель тропической малярии.
 Переносчиком возбудителей малярии человека являются самки комаров рода Anopheles. Комары рода Anopheles встречаются практически во всех районах земного шара.
Переносчиком возбудителей малярии человека являются самки комаров рода Anopheles. Комары рода Anopheles встречаются практически во всех районах земного шара.
 Малярия характеризуется циклическим течением, в котором различают: A) Первичную атаку Б) Ближние рецидивы B) Латентный период Г) Отдаленные рецидивы
Малярия характеризуется циклическим течением, в котором различают: A) Первичную атаку Б) Ближние рецидивы B) Латентный период Г) Отдаленные рецидивы
 Жизненный цикл малярийных паразитов состоит из двух стадий: бесполый цикл (шизогония) в организме позвоночного хозяина половой цикл (спорогония) в организме беспозвоночного (комара).
Жизненный цикл малярийных паразитов состоит из двух стадий: бесполый цикл (шизогония) в организме позвоночного хозяина половой цикл (спорогония) в организме беспозвоночного (комара).

 Попав с укусом комара в организм человека, спорозоиты проникают и развиваются внутриклеточно в паренхиматозных клетках печени (так называемая экзоэритроцитарная шизогония). Внутриклеточно из спорозоита развивается шизонт (делящаяся клетка), который после многократного деления образует многочисленные мерозоиты.
Попав с укусом комара в организм человека, спорозоиты проникают и развиваются внутриклеточно в паренхиматозных клетках печени (так называемая экзоэритроцитарная шизогония). Внутриклеточно из спорозоита развивается шизонт (делящаяся клетка), который после многократного деления образует многочисленные мерозоиты.
 Длительность преэритроцитарной шизогонии зависит от вида паразита: P. vivax образует до 10 тыс. мерозоитов в течение 6 дней; P. malariae — 15 тыс. в течение 15 дней; P. ovale — до 10 тыс. в течение 9 дней P. falciparum — наибольшее число, до 40 тыс. в течение 8 дней.
Длительность преэритроцитарной шизогонии зависит от вида паразита: P. vivax образует до 10 тыс. мерозоитов в течение 6 дней; P. malariae — 15 тыс. в течение 15 дней; P. ovale — до 10 тыс. в течение 9 дней P. falciparum — наибольшее число, до 40 тыс. в течение 8 дней.
 При малярии, вызываемой P. vivax и P. ovale, часть паразитов, попавших в гепатоциты, задерживаются в развитии ( «дремлющая стадия» ), однако могут активизироваться спустя несколько месяцев или лет (до 2 лет)
При малярии, вызываемой P. vivax и P. ovale, часть паразитов, попавших в гепатоциты, задерживаются в развитии ( «дремлющая стадия» ), однако могут активизироваться спустя несколько месяцев или лет (до 2 лет)
 Образовавшиеся в гепатоцитах мерозоиты выходят в русло кровотока и внедряются в эритроциты. Эта стадия развития паразита называется эритроцитарной шизогонией. В процессе эритроцитарной шизогонии мерозоит превращается в трофозоит (растущую клетку), затем в эритроцитарный шизонт.
Образовавшиеся в гепатоцитах мерозоиты выходят в русло кровотока и внедряются в эритроциты. Эта стадия развития паразита называется эритроцитарной шизогонией. В процессе эритроцитарной шизогонии мерозоит превращается в трофозоит (растущую клетку), затем в эритроцитарный шизонт.
 Шизонты в результате деления вновь образуют мерозоиты, приводя к распаду эритроцита, а освободившиеся мерозоиты внедряются в новые эритроциты. Таким образом, цикл шизогонии вновь повторяется.
Шизонты в результате деления вновь образуют мерозоиты, приводя к распаду эритроцита, а освободившиеся мерозоиты внедряются в новые эритроциты. Таким образом, цикл шизогонии вновь повторяется.
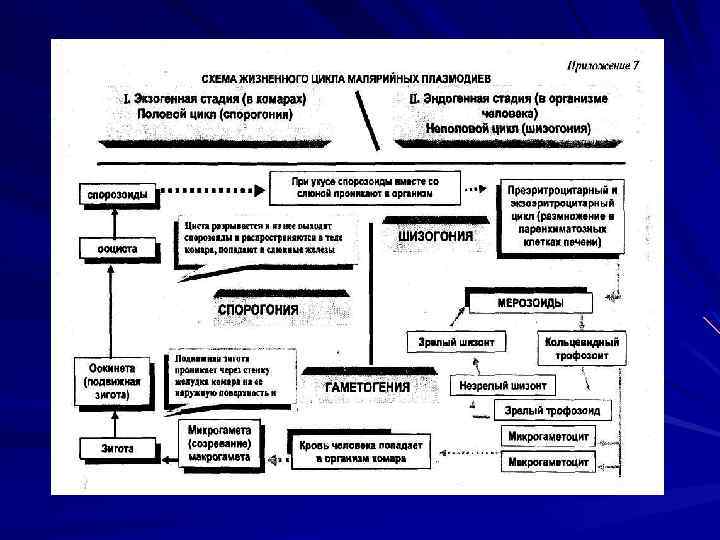
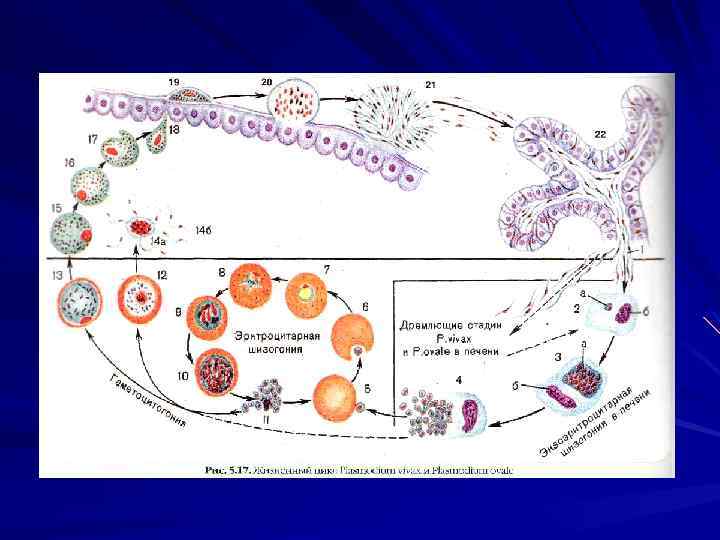
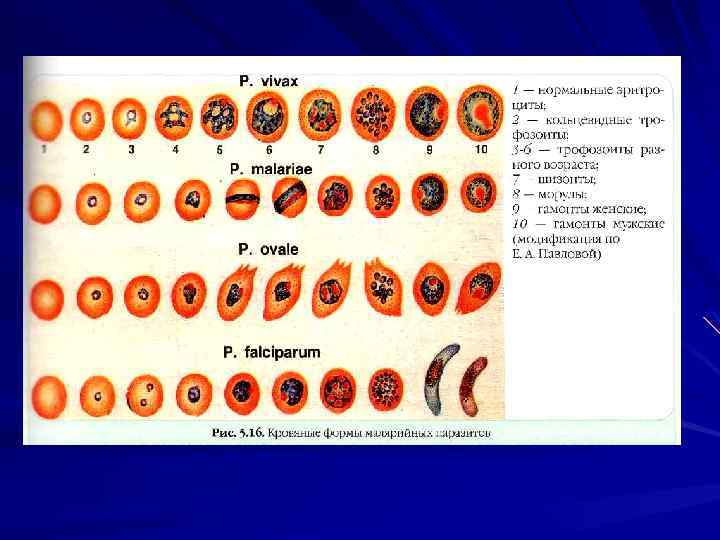
 С началом эритроцитарной шизогонии размножение возбудителя в печени прекращается.
С началом эритроцитарной шизогонии размножение возбудителя в печени прекращается.
 Заболевание проявляется с окончанием первых циклов эритроцитарной шизогонии, длительность которых: для Р. таlariае составляет 72 ч, для P. vivax, P. ovale и P. falciparum — 48 ч. 50 ч.
Заболевание проявляется с окончанием первых циклов эритроцитарной шизогонии, длительность которых: для Р. таlariае составляет 72 ч, для P. vivax, P. ovale и P. falciparum — 48 ч. 50 ч.
 При заражении P. vivax, P. ovale, P. malariae человек может стать источником заражения комаров с первых дней болезни до тех пор, пока паразиты находятся в крови.
При заражении P. vivax, P. ovale, P. malariae человек может стать источником заражения комаров с первых дней болезни до тех пор, пока паразиты находятся в крови.
 В организме человека сохраняются: P. falciparum до 1, 5 лет (некоторые африканские варианты — до 3 лет), P. vivax — до 3 лет, P. ovale — до 4, 5 лет, P. malariae в некоторых случаях сохраняется пожизненно без очевидных клинических проявлений и выявляются случайно при заболевании реципиентов, получавших кровь, зараженных малярией доноров (т. н. малярия, привитая кровью).
В организме человека сохраняются: P. falciparum до 1, 5 лет (некоторые африканские варианты — до 3 лет), P. vivax — до 3 лет, P. ovale — до 4, 5 лет, P. malariae в некоторых случаях сохраняется пожизненно без очевидных клинических проявлений и выявляются случайно при заболевании реципиентов, получавших кровь, зараженных малярией доноров (т. н. малярия, привитая кровью).
 Более длительно созревают мерозоиты P. falciparum. Образование гаметоцитов при тропической малярии происходит в глубоких сосудах в течение 9 11 дней. В периферической крови циркулируют только молодые бесполые формы паразитов (кольца). Человек при тропической малярии становится заразным для комаров через 10 12 дней после появления первых малярийных приступов, и остается источником заражения комаров после окончания эритроцирной шизогонии и исчезновения бесполых стадий паразита
Более длительно созревают мерозоиты P. falciparum. Образование гаметоцитов при тропической малярии происходит в глубоких сосудах в течение 9 11 дней. В периферической крови циркулируют только молодые бесполые формы паразитов (кольца). Человек при тропической малярии становится заразным для комаров через 10 12 дней после появления первых малярийных приступов, и остается источником заражения комаров после окончания эритроцирной шизогонии и исчезновения бесполых стадий паразита
 Малярийные приступы развиваются на выход в кровь огромного количества мерозоитов, явяющихся чужеродным белком. Число паразитов при этом составляет 100— 600 в 1 мкл крови.
Малярийные приступы развиваются на выход в кровь огромного количества мерозоитов, явяющихся чужеродным белком. Число паразитов при этом составляет 100— 600 в 1 мкл крови.
 Паразитемия может быть • невысокой десятки и сотни паразитов в 1 мкл, • умеренно высокой тысячи в 1 мкл • очень высокой 100 тысяч в 1 мкл и более.
Паразитемия может быть • невысокой десятки и сотни паразитов в 1 мкл, • умеренно высокой тысячи в 1 мкл • очень высокой 100 тысяч в 1 мкл и более.
 В повреждении внутренних органов участвует: токсинемия в период инвазии плазмодиев в макроорганизм с последующей сенсибилизацией тромбоцитов и эритроцитов и развитием в дальнейшем ДВС синдрома.
В повреждении внутренних органов участвует: токсинемия в период инвазии плазмодиев в макроорганизм с последующей сенсибилизацией тромбоцитов и эритроцитов и развитием в дальнейшем ДВС синдрома.
 В развитии анемии имеют значение: гемолиз инвазированных эритроцитов в внутрисосудистом русле фагоцитоз клетками ретикулоэндотелия селезенки как инвазированных, так и неинвазированных эритроцитов, поврежденных аутоантителами в результате иммуногенеза; секвестрация эритроцитов, содержащих зрелые паразиты в костном мозге.
В развитии анемии имеют значение: гемолиз инвазированных эритроцитов в внутрисосудистом русле фагоцитоз клетками ретикулоэндотелия селезенки как инвазированных, так и неинвазированных эритроцитов, поврежденных аутоантителами в результате иммуногенеза; секвестрация эритроцитов, содержащих зрелые паразиты в костном мозге.
 Во время приступов малярийной лихорадки отмечены гуморальные изменения: гиперадреналинемия, гипергликемия, гиперхолестеринемия, гиперкалиемия и относительная гипонатриемия.
Во время приступов малярийной лихорадки отмечены гуморальные изменения: гиперадреналинемия, гипергликемия, гиперхолестеринемия, гиперкалиемия и относительная гипонатриемия.
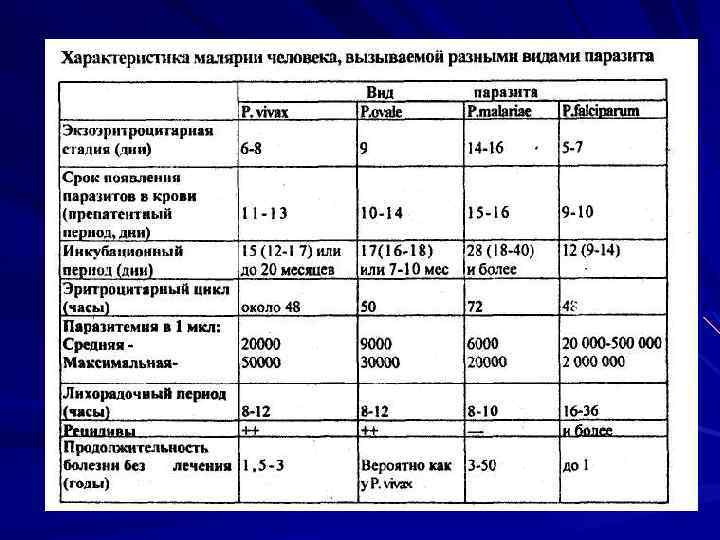
 Лабораторная диагностика Паразитологический метод Микроскопия мазков крови «тонкий мазок» , «толстая капля» (Романовскому Гимзе, Цилю Нильсону). Отрицательный результат, если паразиты не обнаружены после просмотра 100 полей зрения.
Лабораторная диагностика Паразитологический метод Микроскопия мазков крови «тонкий мазок» , «толстая капля» (Романовскому Гимзе, Цилю Нильсону). Отрицательный результат, если паразиты не обнаружены после просмотра 100 полей зрения.
 для экспресс диагностики на полоске стержне иммобилизированы моноклональные антитела, при погружении края полоски в каплю лизированной крови больного тропической малярией через 2 минуты появляется сплошная красная линия.
для экспресс диагностики на полоске стержне иммобилизированы моноклональные антитела, при погружении края полоски в каплю лизированной крови больного тропической малярией через 2 минуты появляется сплошная красная линия.
 Иммунологические методы диагностики основаны на обнаружении в сыворотке пациента антипаразитарных антител или выявлении в кровяном русле растворимых паразитарных антигенов. непрямая реакция иммунофлюоресценции (НРИФ). ИФА тест система, основанная на использовании растворимых антигенов малярийных плазмодиев (РЭМА и ELISA)
Иммунологические методы диагностики основаны на обнаружении в сыворотке пациента антипаразитарных антител или выявлении в кровяном русле растворимых паразитарных антигенов. непрямая реакция иммунофлюоресценции (НРИФ). ИФА тест система, основанная на использовании растворимых антигенов малярийных плазмодиев (РЭМА и ELISA)
 Иммунологические тест системы, основанные на выявлении антител, применяют для: определения уровня эндемии, доказательства или отсутствия малярии в очагах, определения границ малярийной зоны, установления сезонных изменений в передаче, выявления случаев завоза малярии на оздоравливаемые территории, оценки эффективности проводимых противомалярийных мероприятий.
Иммунологические тест системы, основанные на выявлении антител, применяют для: определения уровня эндемии, доказательства или отсутствия малярии в очагах, определения границ малярийной зоны, установления сезонных изменений в передаче, выявления случаев завоза малярии на оздоравливаемые территории, оценки эффективности проводимых противомалярийных мероприятий.
 Полимеразная цепная реакция (ПЦР), применяется в случаях очень низкой паразитемии. Метод чрезвычайно чувствителен.
Полимеразная цепная реакция (ПЦР), применяется в случаях очень низкой паразитемии. Метод чрезвычайно чувствителен.
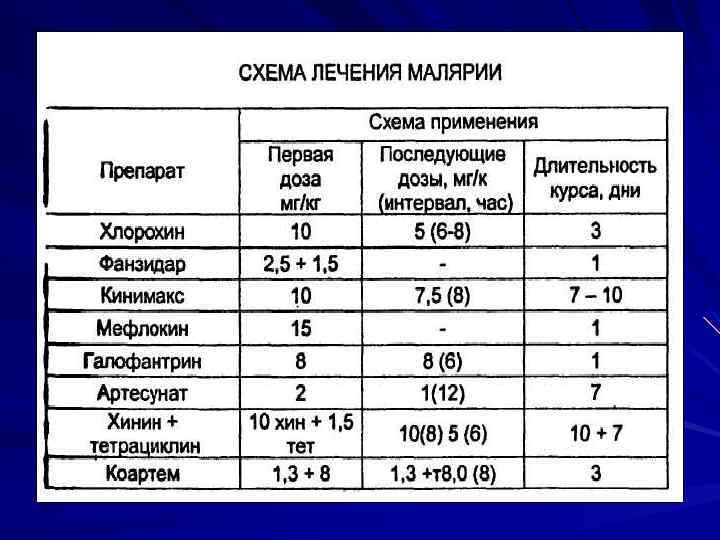
 Профилактика Цель воздействовать на сохраняющиеся в печени возбудители (гипнозоиты), дающие начало острым проявлениям в будущем. Единственным эффективным препаратом является примахин.
Профилактика Цель воздействовать на сохраняющиеся в печени возбудители (гипнозоиты), дающие начало острым проявлениям в будущем. Единственным эффективным препаратом является примахин.
 Профилактика Массовая химиопрофилактика населения может быть сезонной и межсезонной. Сезонная химиопрофилактика проводится в активных очагах только в период эффективной заражаемости комаров с целью перерыва передачи малярии.
Профилактика Массовая химиопрофилактика населения может быть сезонной и межсезонной. Сезонная химиопрофилактика проводится в активных очагах только в период эффективной заражаемости комаров с целью перерыва передачи малярии.
 Межсезонная химиопрофилактика проводится среди лиц, которые 1) в прошлом сезоне передачи малярии болели, но не лечились или лечились без примахина; 2) временно находились в высокоэндемичных зонах и прибыли на местность с высоким маляриогенным потенциалом; 3) получали сезонную химиопрофилактику в очаге
Межсезонная химиопрофилактика проводится среди лиц, которые 1) в прошлом сезоне передачи малярии болели, но не лечились или лечились без примахина; 2) временно находились в высокоэндемичных зонах и прибыли на местность с высоким маляриогенным потенциалом; 3) получали сезонную химиопрофилактику в очаге
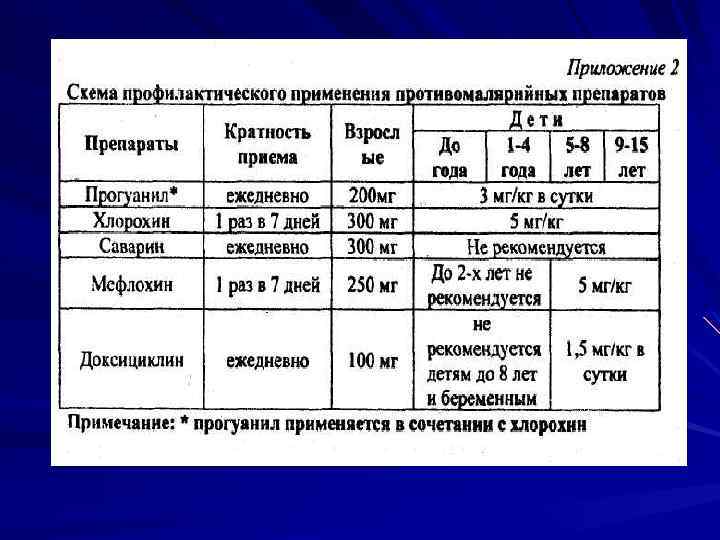
 Индивидуальная химиопрофилактика для персональной защиты лиц, выезжающих в страны Африки, Азии, Океании и др. (мефлохин, хлорохин)
Индивидуальная химиопрофилактика для персональной защиты лиц, выезжающих в страны Африки, Азии, Океании и др. (мефлохин, хлорохин)
 Возбудители криптоспоридиоза Криптоспоридиоз зооантропонозное паразитарное заболевание, вызываемое простейшими рода Cryptosporidium, которые поражают желудочно кишечный тракт.
Возбудители криптоспоридиоза Криптоспоридиоз зооантропонозное паразитарное заболевание, вызываемое простейшими рода Cryptosporidium, которые поражают желудочно кишечный тракт.
 Криптоспоридиоз является одной из причин диареи путешественников, внесен в число СПИД маркерных заболеваний. у иммунокомпетентных больных, у детей может протекать как остро с самоизлечением, так и в виде хронической диареи. бессимптомное паразитоносительство у здоровых лиц
Криптоспоридиоз является одной из причин диареи путешественников, внесен в число СПИД маркерных заболеваний. у иммунокомпетентных больных, у детей может протекать как остро с самоизлечением, так и в виде хронической диареи. бессимптомное паразитоносительство у здоровых лиц
 До недавнего времени инфекции, вызываемые криптоспоридиями, считались редкими среди животных, а у людей трактовались как результат заболевания, вызванного оппортунистическим микроорганизмом у иммунодефицитных людей.
До недавнего времени инфекции, вызываемые криптоспоридиями, считались редкими среди животных, а у людей трактовались как результат заболевания, вызванного оппортунистическим микроорганизмом у иммунодефицитных людей.
 За последние 10— 15 лет криптоспоридии стали широко распространенными агентами, часто вызывающими желудочно кишечные заболевания у животных и людей, особенно у детей.
За последние 10— 15 лет криптоспоридии стали широко распространенными агентами, часто вызывающими желудочно кишечные заболевания у животных и людей, особенно у детей.
 В структуре диарейных заболеваний криптоспоридиоз занимает 4 е место после кампилобактериоза, сальмонеллезов и ротавирусного гастроэнтерита. На сегодня он составляет 1— 2% всех регистрируемых острых кишечных инфекций (ОКИ)
В структуре диарейных заболеваний криптоспоридиоз занимает 4 е место после кампилобактериоза, сальмонеллезов и ротавирусного гастроэнтерита. На сегодня он составляет 1— 2% всех регистрируемых острых кишечных инфекций (ОКИ)
 В Европейской части России инфицированность криптоспоридиями выявлена в 3, 69% детей и в 0, 41% среди взрослых. Разницы между сельским и городским населением не отмечено.
В Европейской части России инфицированность криптоспоридиями выявлена в 3, 69% детей и в 0, 41% среди взрослых. Разницы между сельским и городским населением не отмечено.
 Более 80% заболеваний — спорадические случаи. Описаны вспышки криптоспоридиоза среди детей в закрытых коллективах, госпитальные инфекции, водные вспышки, в том числе значительные — более 2 тыс. человек. Число водных вспышек по различным регионам в последние годы возрастает (особенно в США, Великобритании, Италии, в Африкано Азиатских странах, Австралии, др. )
Более 80% заболеваний — спорадические случаи. Описаны вспышки криптоспоридиоза среди детей в закрытых коллективах, госпитальные инфекции, водные вспышки, в том числе значительные — более 2 тыс. человек. Число водных вспышек по различным регионам в последние годы возрастает (особенно в США, Великобритании, Италии, в Африкано Азиатских странах, Австралии, др. )
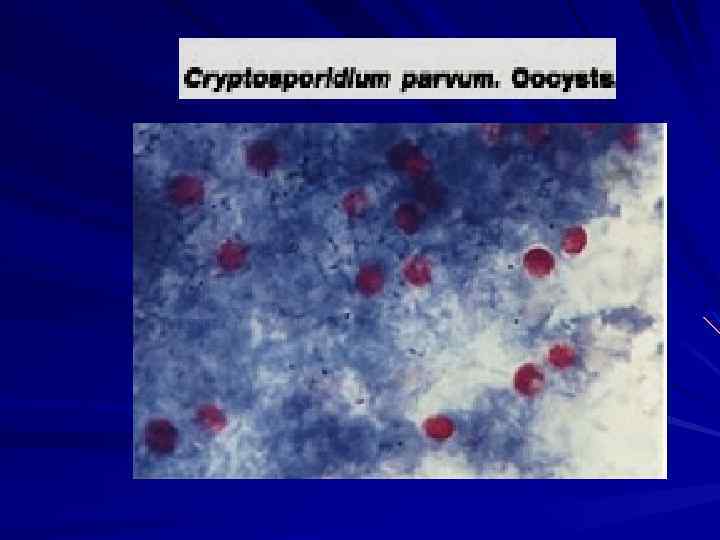
 Cryptosporidium возбудитель простейший паразит малых размеров (от 2 до 6 мкм), принадлежащий к кокцидиям. Впервые был описан в 1907 г.
Cryptosporidium возбудитель простейший паразит малых размеров (от 2 до 6 мкм), принадлежащий к кокцидиям. Впервые был описан в 1907 г.
 Описано несколько десятков видов криптоспоридий, однако считается, что млекопитающих и человека инфицируют в основном С. muris и С. pervum. Количество видов криптоспоридий, инфицирующих человека, возрастает.
Описано несколько десятков видов криптоспоридий, однако считается, что млекопитающих и человека инфицируют в основном С. muris и С. pervum. Количество видов криптоспоридий, инфицирующих человека, возрастает.
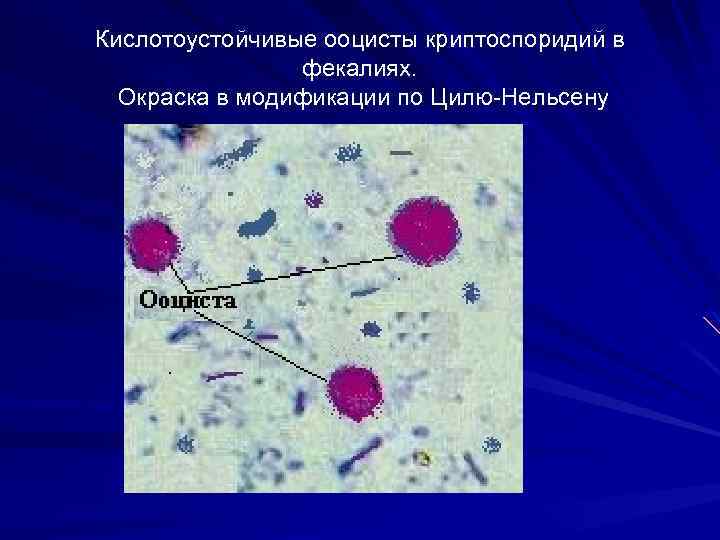 Кислотоустойчивые ооцисты криптоспоридий в фекалиях. Окраска в модификации по Цилю Нельсену
Кислотоустойчивые ооцисты криптоспоридий в фекалиях. Окраска в модификации по Цилю Нельсену
 Жизненный цикл С. parvum У людей он такой же как и у животных, но продолжается не 4— 7, а около 5 дней. Цикл от исходной ооцисты до ооцисты нового поколения осуществляется в одном организме.
Жизненный цикл С. parvum У людей он такой же как и у животных, но продолжается не 4— 7, а около 5 дней. Цикл от исходной ооцисты до ооцисты нового поколения осуществляется в одном организме.
 Человек заглатывает ооцисты с пищей и водой. В верхних отделах кишечника оболочка ооцисты разрушается, освобождая четыре подвижных червеобразных спорозоита. Они движутся к энтероцитам, достигают зоны микроворсинок и задерживаются под мембраной эпителиальных клеток, не погружаясь в их цитоплазму.
Человек заглатывает ооцисты с пищей и водой. В верхних отделах кишечника оболочка ооцисты разрушается, освобождая четыре подвижных червеобразных спорозоита. Они движутся к энтероцитам, достигают зоны микроворсинок и задерживаются под мембраной эпителиальных клеток, не погружаясь в их цитоплазму.
 Отличительная особенность — экстрацитоплазматическая локализация криптоспоридий. Затем, они внутри клетки образуют паразитоформную вакуоль. Такое возможно лишь в клетках, имеющих микроворсинки щеточной каймы (кишечник, легкие, почки, плацента). Вакуоль ограждает паразита от воздействия лизосом хозяина
Отличительная особенность — экстрацитоплазматическая локализация криптоспоридий. Затем, они внутри клетки образуют паразитоформную вакуоль. Такое возможно лишь в клетках, имеющих микроворсинки щеточной каймы (кишечник, легкие, почки, плацента). Вакуоль ограждает паразита от воздействия лизосом хозяина
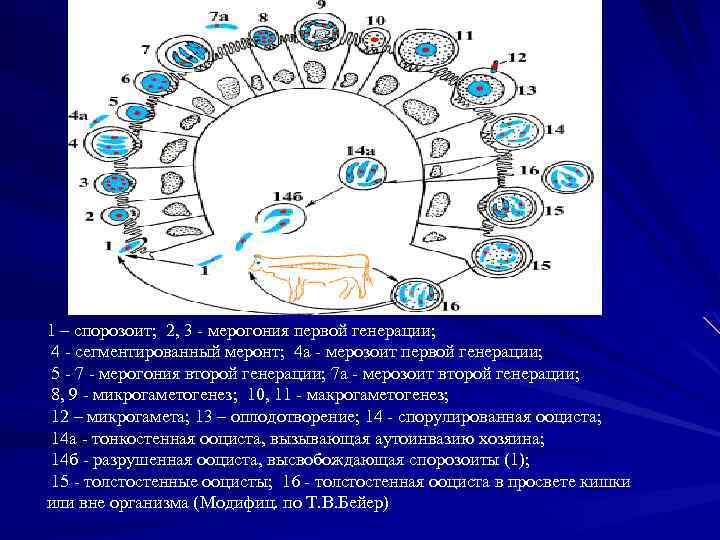 1 – спорозоит; 2, 3 - мерогония первой генерации; 4 - сегментированный меронт; 4 а - мерозоит первой генерации; 5 - 7 - мерогония второй генерации; 7 а - мерозоит второй генерации; 8, 9 - микрогаметогенез; 10, 11 - макрогаметогенез; 12 – микрогамета; 13 – оплодотворение; 14 - спорулированная ооциста; 14 а - тонкостенная ооциста, вызывающая аутоинвазию хозяина; 14 б - разрушенная ооциста, высвобождающая спорозоиты (1); 15 - толстостенные ооцисты; 16 - толстостенная ооциста в просвете кишки или вне организма (Модифиц. по Т. В. Бейер)
1 – спорозоит; 2, 3 - мерогония первой генерации; 4 - сегментированный меронт; 4 а - мерозоит первой генерации; 5 - 7 - мерогония второй генерации; 7 а - мерозоит второй генерации; 8, 9 - микрогаметогенез; 10, 11 - макрогаметогенез; 12 – микрогамета; 13 – оплодотворение; 14 - спорулированная ооциста; 14 а - тонкостенная ооциста, вызывающая аутоинвазию хозяина; 14 б - разрушенная ооциста, высвобождающая спорозоиты (1); 15 - толстостенные ооцисты; 16 - толстостенная ооциста в просвете кишки или вне организма (Модифиц. по Т. В. Бейер)
 Внутриклеточный трофозоит питается, увеличивается в размере и становится меронтом I типа. Размножение идет путем множественного деления (бесполое), с образованием 8 дочерних клеток.
Внутриклеточный трофозоит питается, увеличивается в размере и становится меронтом I типа. Размножение идет путем множественного деления (бесполое), с образованием 8 дочерних клеток.
 Из части мерозоитов формируются меронты II типа, которые реализуют половую фазу жизненного цикла. Идет образование макро и микрогамонтов. Гаметогония завершается оплодотворением и образованием зиготы, которая покрывается оболочкой и превращается в ооцисту.
Из части мерозоитов формируются меронты II типа, которые реализуют половую фазу жизненного цикла. Идет образование макро и микрогамонтов. Гаметогония завершается оплодотворением и образованием зиготы, которая покрывается оболочкой и превращается в ооцисту.
 Характерно также образование 2 типов ооцист (с толстыми и тонкими стенками), из которых последние способны вызывать аутоинвазию хозяина. Это обусловливает персистенцию возбудителя без повторных заражений, хроническое течение болезни, способность даже небольшой дозы инфекции вызвать заболевание и интенсивную инвазию.
Характерно также образование 2 типов ооцист (с толстыми и тонкими стенками), из которых последние способны вызывать аутоинвазию хозяина. Это обусловливает персистенцию возбудителя без повторных заражений, хроническое течение болезни, способность даже небольшой дозы инфекции вызвать заболевание и интенсивную инвазию.
 С. parvum значительно отличаются по фено и генотипам. Человеческий генотип 1 не выделяется от животных (генотип 2). Источником инвазии для человека являются животные (телята, ягнята, поросята, кошки, собаки и др. ), 2 вида рыб, 5 видов рептилий, 7 — птиц, 31 — млекопитающих, включая самого человека.
С. parvum значительно отличаются по фено и генотипам. Человеческий генотип 1 не выделяется от животных (генотип 2). Источником инвазии для человека являются животные (телята, ягнята, поросята, кошки, собаки и др. ), 2 вида рыб, 5 видов рептилий, 7 — птиц, 31 — млекопитающих, включая самого человека.
 Инкубационный период составляет от 3 до 8 сут. У лиц с нормальным иммунитетом преобладают субклинические и легкие формы инфекции.
Инкубационный период составляет от 3 до 8 сут. У лиц с нормальным иммунитетом преобладают субклинические и легкие формы инфекции.
 Резистентность Возбудитель высокоустойчив во внешней среде и ко многим широко используемым дезинфектантам.
Резистентность Возбудитель высокоустойчив во внешней среде и ко многим широко используемым дезинфектантам.
 Вакуоль ограждает паразита от воздействия лизосом хозяина ооцисты могут присутствовать в фекалиях до 2 нед после прекращения диареи.
Вакуоль ограждает паразита от воздействия лизосом хозяина ооцисты могут присутствовать в фекалиях до 2 нед после прекращения диареи.
 стадии развивающихся паразитов обнаруживаются в пищеварительном тракте на всем его протяжении, хотя наиболее инфицированным участком являлются проксимальные отделы тонкой кишки
стадии развивающихся паразитов обнаруживаются в пищеварительном тракте на всем его протяжении, хотя наиболее инфицированным участком являлются проксимальные отделы тонкой кишки
 звенья патогенеза персистенция инфекции и колонизация криптоспоридий на поверхности слизистой оболочки кишечни ка; присоединение к эпителиальным клеткам и их повреждение; нарушение всасывательной, секреторной и ферментативной функции кишечника с развитием диареи; формирование процессов иммуногенеза и развитие иммунитета; освобождение организма от возбудителя и регенерация пораженных участков слизистой оболочки кишечника.
звенья патогенеза персистенция инфекции и колонизация криптоспоридий на поверхности слизистой оболочки кишечни ка; присоединение к эпителиальным клеткам и их повреждение; нарушение всасывательной, секреторной и ферментативной функции кишечника с развитием диареи; формирование процессов иммуногенеза и развитие иммунитета; освобождение организма от возбудителя и регенерация пораженных участков слизистой оболочки кишечника.
 В пораженных участках отмечается атрофия ворсинок энтероцитов кишки, увеличение длины крипт, различной степени мононуклеарная клеточная инфильтрация собственной пластинки Связанная с этим мальабсорбция является основой диареи при криптоспоридиозе.
В пораженных участках отмечается атрофия ворсинок энтероцитов кишки, увеличение длины крипт, различной степени мононуклеарная клеточная инфильтрация собственной пластинки Связанная с этим мальабсорбция является основой диареи при криптоспоридиозе.
 Снижение выработки многих ферментов, включая расщепляющие дисахариды (сахарозу, лактозу, мальтозу), ведут к уменьшению всасывательной способности тонкой кишки (осмотическая диарея) С. parvum, обладает энтеротоксигенной активностью определяющей выраженность секреторной (холероподобной) диареи.
Снижение выработки многих ферментов, включая расщепляющие дисахариды (сахарозу, лактозу, мальтозу), ведут к уменьшению всасывательной способности тонкой кишки (осмотическая диарея) С. parvum, обладает энтеротоксигенной активностью определяющей выраженность секреторной (холероподобной) диареи.
 Предполагаемой невозможностью поступления антигенов паразита в клетку хозяина ввиду наличия мембранного слоя (паразитофорная вакуоль) объясняют отсутствие заметных морфологических изменений в цитоплазме зараженной клетки.
Предполагаемой невозможностью поступления антигенов паразита в клетку хозяина ввиду наличия мембранного слоя (паразитофорная вакуоль) объясняют отсутствие заметных морфологических изменений в цитоплазме зараженной клетки.
 Полагают, что резервуар в желчевыводящих путях может служить одной из причин упорного течения заболевания у иммунодефицитных больных
Полагают, что резервуар в желчевыводящих путях может служить одной из причин упорного течения заболевания у иммунодефицитных больных
 В ответ на инфекцию криптоспоридиями С. parvum в крови стимулируется выработка гамма интерферона и местная выработка Ig. A и Ig. M
В ответ на инфекцию криптоспоридиями С. parvum в крови стимулируется выработка гамма интерферона и местная выработка Ig. A и Ig. M
 клинические проявления острое начало заболевания, выраженная водянистая диарея, максимально проявляющаяся 2— 3 дня, спастические боли в животе (терминальный илеит), тошнота (2— 3 дня); рвота (2— 3 дня); субфебрильная температура (3— 7 дней), слабость, головная боль, снижение аппетита.
клинические проявления острое начало заболевания, выраженная водянистая диарея, максимально проявляющаяся 2— 3 дня, спастические боли в животе (терминальный илеит), тошнота (2— 3 дня); рвота (2— 3 дня); субфебрильная температура (3— 7 дней), слабость, головная боль, снижение аппетита.
 У иммунодефицитных лиц, особенно при СПИДе, заболевание становится прогрессивно тяжелым, приобретает пролонгированное, изнуряющее течение (месяцами) с потерей массы тела. Диарея нередко становится необратимой, а потери жидкости — значительными.
У иммунодефицитных лиц, особенно при СПИДе, заболевание становится прогрессивно тяжелым, приобретает пролонгированное, изнуряющее течение (месяцами) с потерей массы тела. Диарея нередко становится необратимой, а потери жидкости — значительными.
 Характерны также частые рецидивы, резистентность к лечению антибактериальными препаратами.
Характерны также частые рецидивы, резистентность к лечению антибактериальными препаратами.
 Случаи инфекции респираторного тракта, выражаются хроническим кашлем с одышкой, бронхитом и пневмонитом, часто в сочетании с цитомегаловирусной инфекцией, кандидами, пневмоцистами.
Случаи инфекции респираторного тракта, выражаются хроническим кашлем с одышкой, бронхитом и пневмонитом, часто в сочетании с цитомегаловирусной инфекцией, кандидами, пневмоцистами.
 Лабораторная диагностика микропическое обнаружение возбудителя (ооцист), в клиническом риале от больных (фекалии, рвотные массы и др. . (копроцитологические исследования), С применением методов окрашивания кислотоустойчивых микроорганизмов (чаще карболовым фуксином по Цилю— Нильсену, азуром и эозином по Романовскому—Гимзе)
Лабораторная диагностика микропическое обнаружение возбудителя (ооцист), в клиническом риале от больных (фекалии, рвотные массы и др. . (копроцитологические исследования), С применением методов окрашивания кислотоустойчивых микроорганизмов (чаще карболовым фуксином по Цилю— Нильсену, азуром и эозином по Романовскому—Гимзе)
 использование методов обогащения материала(чаще флотация и седиментации) позволяет почти в 2 раза увеличить число положительных находок Из иммунологических методов предложены МФА, отличающийся высокой чувствительностью ПЦР и иммуноблоттинг
использование методов обогащения материала(чаще флотация и седиментации) позволяет почти в 2 раза увеличить число положительных находок Из иммунологических методов предложены МФА, отличающийся высокой чувствительностью ПЦР и иммуноблоттинг
 Лечение Симптоматическое При среднетяжелом и тяжелом течении криптоспоридиоза показано проведение этиотропной терапии (фуразолидон, полимиксин, метронидазол) Эубиотики лактобациллы сдерживать развитие криптоспоридиозной инфекции
Лечение Симптоматическое При среднетяжелом и тяжелом течении криптоспоридиоза показано проведение этиотропной терапии (фуразолидон, полимиксин, метронидазол) Эубиотики лактобациллы сдерживать развитие криптоспоридиозной инфекции
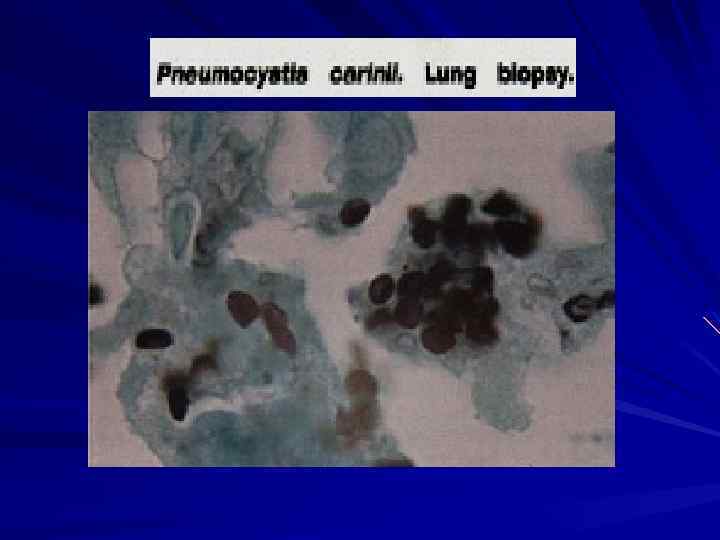
 Пневмоцистная пневмония (ПП) Pneumocystis carinii (P. jiroveci) Тип: простейших, подтип Sporozoa, класс Haplospora. Факторы риска: v CD 4<200 мкл 1 v в анамнезе пневмоцистная пневмония или кандидозный стоматит v лихорадка неясного генеза в течение 2 недель СПб МАПО Росздрава
Пневмоцистная пневмония (ПП) Pneumocystis carinii (P. jiroveci) Тип: простейших, подтип Sporozoa, класс Haplospora. Факторы риска: v CD 4<200 мкл 1 v в анамнезе пневмоцистная пневмония или кандидозный стоматит v лихорадка неясного генеза в течение 2 недель СПб МАПО Росздрава
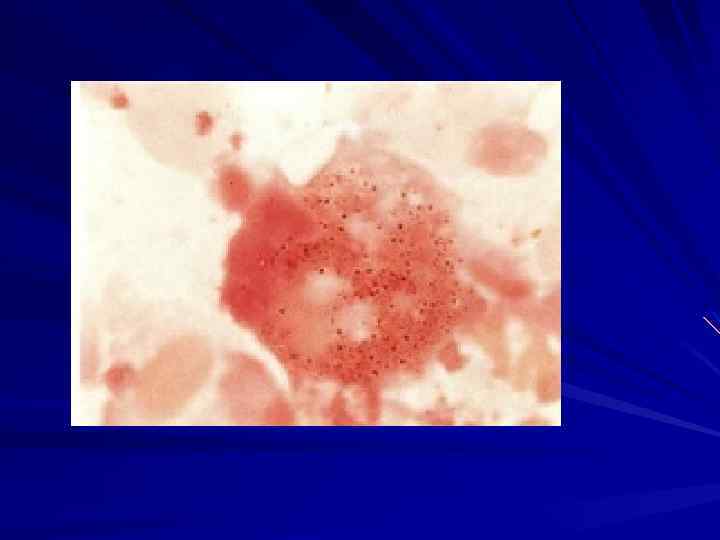
 основные формы микроорганизма: мелкие одноядерные трофозоиты (1 5 мкм) и, размножающиеся бинарным делением, цисты (10 мкм), имеющие толстую стенку и содержащие от 2 до 8 клеток (1 2 мкм), называющихся спорозоитами. Когда зрелая циста разрывается, спорозоиты либо продолжают цикл развития в альвеолах, и превращаются в трофозоит, либо выходят во внешнюю среду (с капельками слизи при кашле).
основные формы микроорганизма: мелкие одноядерные трофозоиты (1 5 мкм) и, размножающиеся бинарным делением, цисты (10 мкм), имеющие толстую стенку и содержащие от 2 до 8 клеток (1 2 мкм), называющихся спорозоитами. Когда зрелая циста разрывается, спорозоиты либо продолжают цикл развития в альвеолах, и превращаются в трофозоит, либо выходят во внешнюю среду (с капельками слизи при кашле).
 Пневмоцистная пневмония у детей У детей ПЦП чаще всего возникает в возрасте 3 месяцев, т. е. во время первого контакта с микроорганизмами окружающей среды. Пневмоцистная пневмония может развиться и у старших детей, у которых имеется быстрое снижение количества лимфоцитов CD 4+. В возрасте до 12 месяцев, у которых абсолютное количество лимфоцитов CD 4+ ниже 1500 клеток/мм-
Пневмоцистная пневмония у детей У детей ПЦП чаще всего возникает в возрасте 3 месяцев, т. е. во время первого контакта с микроорганизмами окружающей среды. Пневмоцистная пневмония может развиться и у старших детей, у которых имеется быстрое снижение количества лимфоцитов CD 4+. В возрасте до 12 месяцев, у которых абсолютное количество лимфоцитов CD 4+ ниже 1500 клеток/мм-
 Подтверждение диагноза: снижение функции внешнего дыхания у 90% РО 2 < 70 мм рт. ст. Микроскопический метод обнаружение цист возбудителя в мокроте – в 60% положительный результат из смывов при бронхоальвеолярном лаваже в 95% положительный результат РИФ, ПЦР, ИФА (моноклональные тест системы) СПб МАПО Росздрава
Подтверждение диагноза: снижение функции внешнего дыхания у 90% РО 2 < 70 мм рт. ст. Микроскопический метод обнаружение цист возбудителя в мокроте – в 60% положительный результат из смывов при бронхоальвеолярном лаваже в 95% положительный результат РИФ, ПЦР, ИФА (моноклональные тест системы) СПб МАПО Росздрава
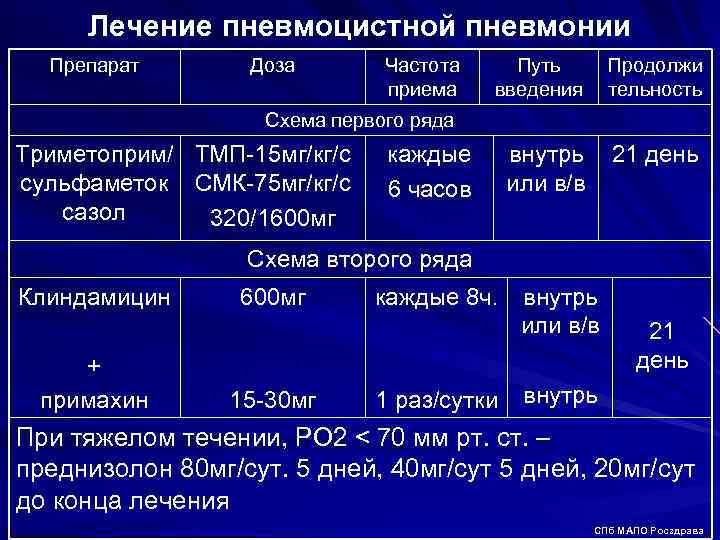 Лечение пневмоцистной пневмонии Препарат Доза Частота приема Путь введения Продолжи тельность Схема первого ряда Триметоприм/ ТМП 15 мг/кг/с сульфаметок СМК 75 мг/кг/с сазол 320/1600 мг каждые 6 часов внутрь 21 день или в/в Схема второго ряда Клиндамицин + примахин 600 мг 15 30 мг каждые 8 ч. 1 раз/сутки внутрь или в/в 21 день внутрь При тяжелом течении, РО 2 < 70 мм рт. ст. – преднизолон 80 мг/сут. 5 дней, 40 мг/сут 5 дней, 20 мг/сут до конца лечения СПб МАПО Росздрава
Лечение пневмоцистной пневмонии Препарат Доза Частота приема Путь введения Продолжи тельность Схема первого ряда Триметоприм/ ТМП 15 мг/кг/с сульфаметок СМК 75 мг/кг/с сазол 320/1600 мг каждые 6 часов внутрь 21 день или в/в Схема второго ряда Клиндамицин + примахин 600 мг 15 30 мг каждые 8 ч. 1 раз/сутки внутрь или в/в 21 день внутрь При тяжелом течении, РО 2 < 70 мм рт. ст. – преднизолон 80 мг/сут. 5 дней, 40 мг/сут 5 дней, 20 мг/сут до конца лечения СПб МАПО Росздрава
 Профилактика пневмоцистной пневмонии Первичная Показания Препараты первого ряда СD 4<200 Триметоприм/сульфаметоксазол 160/800 мг/сут внутрь ежедневно Альтернативные Дапсон 50 мг внутрь 2 раза в сутки Вторичная Триметоприм/сульфаметоксазол 160/800 мг/сут или 80/400 мг/сут внутрь ежедневно При CD 4>200 мкл 1 более 3 мес. профилактику можно прекратить СПб МАПО Росздрава
Профилактика пневмоцистной пневмонии Первичная Показания Препараты первого ряда СD 4<200 Триметоприм/сульфаметоксазол 160/800 мг/сут внутрь ежедневно Альтернативные Дапсон 50 мг внутрь 2 раза в сутки Вторичная Триметоприм/сульфаметоксазол 160/800 мг/сут или 80/400 мг/сут внутрь ежедневно При CD 4>200 мкл 1 более 3 мес. профилактику можно прекратить СПб МАПО Росздрава
 Первичная профилактика ПЦП у детей Триметоприм сульфаметоксазол: пероральный прием по 150 мг/м 2 в сутки 3' раза в неделю в течение трех последовательных дней. Дапсон: по 2 мг/кг перорально один раз в день. Пентамидин в виде аэрозоля: (дети старше 5 лет); по 300 мг назначают через ингалятор «Респригард 2» ежемесячно (MMWR 1995, 44, RR 4; 1 11).
Первичная профилактика ПЦП у детей Триметоприм сульфаметоксазол: пероральный прием по 150 мг/м 2 в сутки 3' раза в неделю в течение трех последовательных дней. Дапсон: по 2 мг/кг перорально один раз в день. Пентамидин в виде аэрозоля: (дети старше 5 лет); по 300 мг назначают через ингалятор «Респригард 2» ежемесячно (MMWR 1995, 44, RR 4; 1 11).
 Рекомендации CDC по профилактике ПЦП у детей От рождения до 6 недель - ребенок, контактный по ВИЧ-инфекции От 6 недель до 4 месяцев - ребенок, контактный по ВИЧ-инфекции От 4 до 12 месяцев - наличие ВИЧинфекции не уточнено или подтверждено От 4 до 12 месяцев Профилакти ка не проводится Профилакти ка проводится Проводится профилакти ка Профилакти
Рекомендации CDC по профилактике ПЦП у детей От рождения до 6 недель - ребенок, контактный по ВИЧ-инфекции От 6 недель до 4 месяцев - ребенок, контактный по ВИЧ-инфекции От 4 до 12 месяцев - наличие ВИЧинфекции не уточнено или подтверждено От 4 до 12 месяцев Профилакти ка не проводится Профилакти ка проводится Проводится профилакти ка Профилакти
 1 -2 года. У ВИЧ-инфицированного ребенка число лимфоцитов CD 4+ менее 750 клеток/мм 3 или меньше 15% 2 -5 лет, у ВИЧ-инфицированного ребенка число лимфоцитов CD 4 менее 500 клеток/мм 3 или меньше 15% От 5 лет, у ВИЧ-инфицированного ребенка число лимфоцитов CD 4+ менее 200 клеток/мм 3 или меньше 15% Ребенок любого возраста, болевший ранее ПЦП Проводится профилактика Рекомендуется пожизненная профилактика
1 -2 года. У ВИЧ-инфицированного ребенка число лимфоцитов CD 4+ менее 750 клеток/мм 3 или меньше 15% 2 -5 лет, у ВИЧ-инфицированного ребенка число лимфоцитов CD 4 менее 500 клеток/мм 3 или меньше 15% От 5 лет, у ВИЧ-инфицированного ребенка число лимфоцитов CD 4+ менее 200 клеток/мм 3 или меньше 15% Ребенок любого возраста, болевший ранее ПЦП Проводится профилактика Рекомендуется пожизненная профилактика
 Благодарим за внимание!
Благодарим за внимание!


