Heart lecture.ppt
- Количество слайдов: 49
 ПАТОФІЗІОЛОГІЯ СЕРЦЯ Лектор – Досенко Віктор Євгенович, д. м. н. , професор кафедри патофізіології НМУ ім. О. О. Богомольця, провідний науковий співробітник відділу загальної та молекулярної патофізіології Інституту фізіолоії ім. О. О. Богомольця НАН України
ПАТОФІЗІОЛОГІЯ СЕРЦЯ Лектор – Досенко Віктор Євгенович, д. м. н. , професор кафедри патофізіології НМУ ім. О. О. Богомольця, провідний науковий співробітник відділу загальної та молекулярної патофізіології Інституту фізіолоії ім. О. О. Богомольця НАН України

 НЕДОСТАТНІСТЬ СЕРЦЯ – неспроможність органу забезпечувати нормальний хвилинний об`єм крові 1. Недостатність серця від перевантаження 2. Недостатність серця через ушкодження міокарда 3. Змішана
НЕДОСТАТНІСТЬ СЕРЦЯ – неспроможність органу забезпечувати нормальний хвилинний об`єм крові 1. Недостатність серця від перевантаження 2. Недостатність серця через ушкодження міокарда 3. Змішана
 ПЕРЕВАНТАЖЕННЯ СЕРЦЯ Переднавантаження (об’ємом) Недостатність мітрального, аортального клапану, дефект міжпередсердної, міжшлуночкової перетинки та ін. Післянавантаження (тиском) Стеноз мітрального, аортального клапану, артеріальна гіпертензія, коарктація аорти та ін.
ПЕРЕВАНТАЖЕННЯ СЕРЦЯ Переднавантаження (об’ємом) Недостатність мітрального, аортального клапану, дефект міжпередсердної, міжшлуночкової перетинки та ін. Післянавантаження (тиском) Стеноз мітрального, аортального клапану, артеріальна гіпертензія, коарктація аорти та ін.
 МЕХАНІЗМИ КОМПЕНСАЦІЇ НЕГАЙНІ (термінові) ВІДДАЛЕНІ (довготермінові) - гетерометричний механізм компенсації за законом Франка. Старлінга - гомеометричний механізм - збільшення частоти серцевих скорочень ГІПЕРТРОФІЯ МІОКАРДА
МЕХАНІЗМИ КОМПЕНСАЦІЇ НЕГАЙНІ (термінові) ВІДДАЛЕНІ (довготермінові) - гетерометричний механізм компенсації за законом Франка. Старлінга - гомеометричний механізм - збільшення частоти серцевих скорочень ГІПЕРТРОФІЯ МІОКАРДА
 ГІПЕРТРОФІЯ МІОКАРДА – патофізіологічний процес, що виникає при перевантаженні серця (або окремих його відділів), та спричинює збільшення маси органу за рахунок збільшення об`єму кардіоміоцитів
ГІПЕРТРОФІЯ МІОКАРДА – патофізіологічний процес, що виникає при перевантаженні серця (або окремих його відділів), та спричинює збільшення маси органу за рахунок збільшення об`єму кардіоміоцитів
 МЕХАНІЗМИ ГІПЕРТРОФІЇ МІОКАРДА ГЕНЕТИЧНІ Microarray chip При “розтягненні” кардіоміоцитів змінюється експресія 185 генів (164 upregulated, 21 downregulated) За впливу норадреналіну змінюється експресія 450 генів (238 upregulated, 211 downregulated)
МЕХАНІЗМИ ГІПЕРТРОФІЇ МІОКАРДА ГЕНЕТИЧНІ Microarray chip При “розтягненні” кардіоміоцитів змінюється експресія 185 генів (164 upregulated, 21 downregulated) За впливу норадреналіну змінюється експресія 450 генів (238 upregulated, 211 downregulated)
 СТАДІЇ ГІПЕРТРОФІЇ МІОКАРДА (за Ф. З. Меєрсоном) 1. Аварійна А m = ІФС 2. Завершеної гіпертрофії та відносно стійкої гіперфункції А m = ІФС 3. Поступового виснаження і прогресуючого кардіосклерозу А m = ІФС
СТАДІЇ ГІПЕРТРОФІЇ МІОКАРДА (за Ф. З. Меєрсоном) 1. Аварійна А m = ІФС 2. Завершеної гіпертрофії та відносно стійкої гіперфункції А m = ІФС 3. Поступового виснаження і прогресуючого кардіосклерозу А m = ІФС
 ФАТАЛЬНІ ПАРАДОКСИ ГІПЕРТРОФІЇ МІОКАРДА V 3 → S 2 При збільшенні об`єму в кубі – площа збільшується лише в квадраті Кількість судин, що живлять серце, не збільшується Зменшення питомої поверхні клітин → погіршення транспорту речовин Погіршення оксигенації та трофічного забезпечення Кількість нервових закінчень у серці не збільшується Часткова денервація серця → підвищення чутливості до адренергічних впливів
ФАТАЛЬНІ ПАРАДОКСИ ГІПЕРТРОФІЇ МІОКАРДА V 3 → S 2 При збільшенні об`єму в кубі – площа збільшується лише в квадраті Кількість судин, що живлять серце, не збільшується Зменшення питомої поверхні клітин → погіршення транспорту речовин Погіршення оксигенації та трофічного забезпечення Кількість нервових закінчень у серці не збільшується Часткова денервація серця → підвищення чутливості до адренергічних впливів
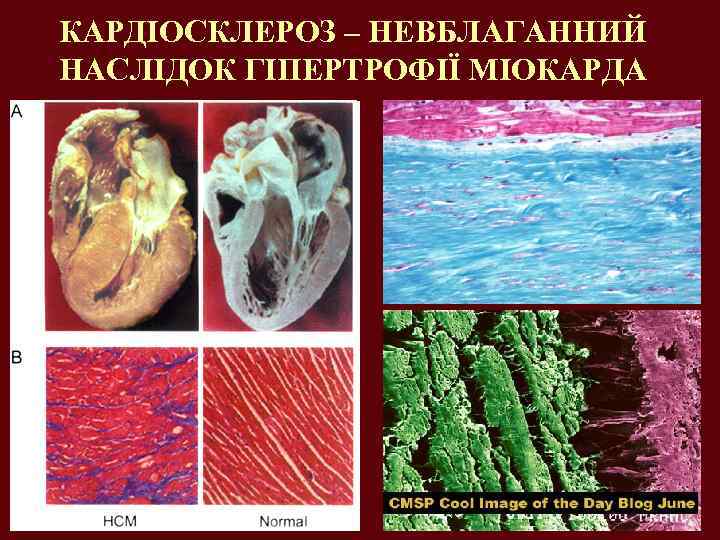 КАРДІОСКЛЕРОЗ – НЕВБЛАГАННИЙ НАСЛІДОК ГІПЕРТРОФІЇ МІОКАРДА
КАРДІОСКЛЕРОЗ – НЕВБЛАГАННИЙ НАСЛІДОК ГІПЕРТРОФІЇ МІОКАРДА
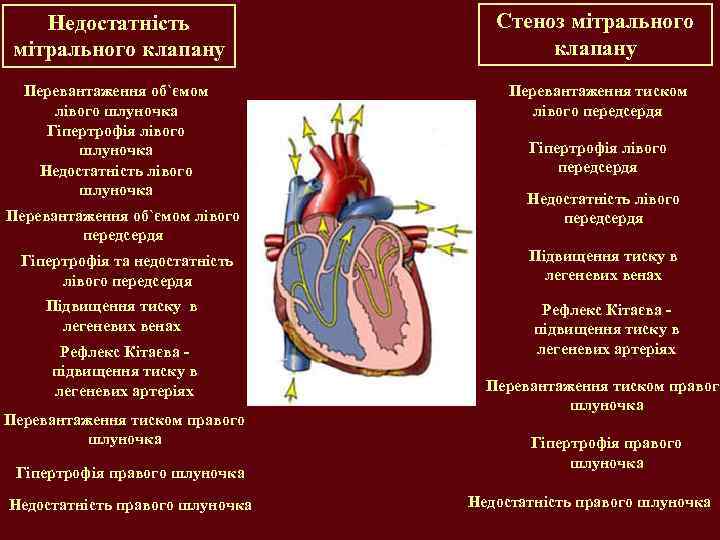 Недостатність мітрального клапану Стеноз мітрального клапану Перевантаження об`ємом лівого шлуночка Гіпертрофія лівого шлуночка Недостатність лівого шлуночка Перевантаження тиском лівого передсердя Перевантаження об`ємом лівого передсердя Гіпертрофія та недостатність лівого передсердя Підвищення тиску в легеневих венах Рефлекс Кітаєва підвищення тиску в легеневих артеріях Перевантаження тиском правого шлуночка Гіпертрофія правого шлуночка Недостатність правого шлуночка Гіпертрофія лівого передсердя Недостатність лівого передсердя Підвищення тиску в легеневих венах Рефлекс Кітаєва підвищення тиску в легеневих артеріях Перевантаження тиском правого шлуночка Гіпертрофія правого шлуночка Недостатність правого шлуночка
Недостатність мітрального клапану Стеноз мітрального клапану Перевантаження об`ємом лівого шлуночка Гіпертрофія лівого шлуночка Недостатність лівого шлуночка Перевантаження тиском лівого передсердя Перевантаження об`ємом лівого передсердя Гіпертрофія та недостатність лівого передсердя Підвищення тиску в легеневих венах Рефлекс Кітаєва підвищення тиску в легеневих артеріях Перевантаження тиском правого шлуночка Гіпертрофія правого шлуночка Недостатність правого шлуночка Гіпертрофія лівого передсердя Недостатність лівого передсердя Підвищення тиску в легеневих венах Рефлекс Кітаєва підвищення тиску в легеневих артеріях Перевантаження тиском правого шлуночка Гіпертрофія правого шлуночка Недостатність правого шлуночка
 НЕДОСТАТНІСТЬ СЕРЦЯ – неспроможність органу забезпечувати нормальний хвилинний об`єм крові 1. Недостатність серця від перевантаження 2. Недостатність серця через ушкодження міокарда 3. Змішана
НЕДОСТАТНІСТЬ СЕРЦЯ – неспроможність органу забезпечувати нормальний хвилинний об`єм крові 1. Недостатність серця від перевантаження 2. Недостатність серця через ушкодження міокарда 3. Змішана
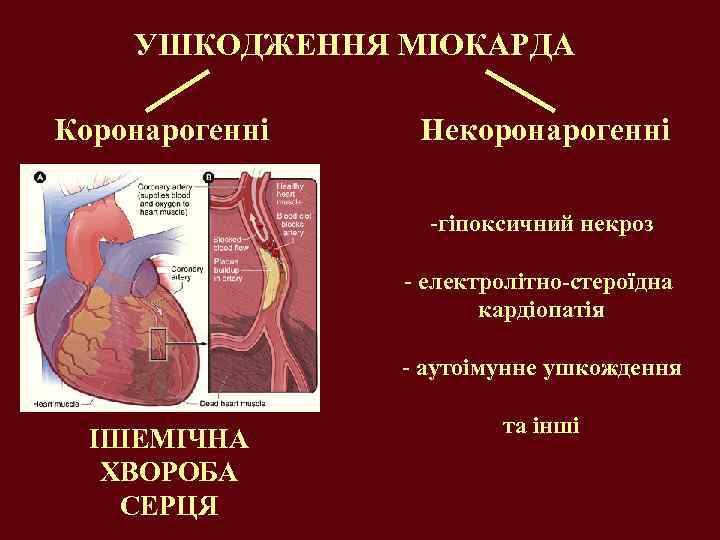 УШКОДЖЕННЯ МІОКАРДА Коронарогенні Некоронарогенні -гіпоксичний некроз - електролітно-стероїдна кардіопатія - аутоімунне ушкождення ІШЕМІЧНА ХВОРОБА СЕРЦЯ та інші
УШКОДЖЕННЯ МІОКАРДА Коронарогенні Некоронарогенні -гіпоксичний некроз - електролітно-стероїдна кардіопатія - аутоімунне ушкождення ІШЕМІЧНА ХВОРОБА СЕРЦЯ та інші
 ІШЕМІЧНА ХВОРОБА СЕРЦЯ – мультифакторне захворювання, що характеризується абсолютним або відносним порушенням кровопостачання міокарда внаслідок ураження коронарних артерій серця Клінічні форми ІХС 1. Раптова коронарна смерть 2. Стенокардія 3. Інфаркт міокарда 4. Аритмії 5. Постінфарктний кардіосклероз
ІШЕМІЧНА ХВОРОБА СЕРЦЯ – мультифакторне захворювання, що характеризується абсолютним або відносним порушенням кровопостачання міокарда внаслідок ураження коронарних артерій серця Клінічні форми ІХС 1. Раптова коронарна смерть 2. Стенокардія 3. Інфаркт міокарда 4. Аритмії 5. Постінфарктний кардіосклероз
 ФАКТОРИ РИЗИКУ ІШЕМІЧНОЇ ХВОРОБИ СЕРЦЯ ЕКЗОГЕННІ Переїдання (дисліпідемії, ожиріння, цукровий діабет ІІ типу) Стрес, “невідреаговані емоції” (артеріальна гіпертензія) Паління Гіподинамія ЕНДОГЕННІ Алельний поліморфізм генів - SNP
ФАКТОРИ РИЗИКУ ІШЕМІЧНОЇ ХВОРОБИ СЕРЦЯ ЕКЗОГЕННІ Переїдання (дисліпідемії, ожиріння, цукровий діабет ІІ типу) Стрес, “невідреаговані емоції” (артеріальна гіпертензія) Паління Гіподинамія ЕНДОГЕННІ Алельний поліморфізм генів - SNP
 Алельний поліморфізм – феномен, що визначає генетичну гетерогенність популяції та генетичну індивідуальність кожної людини ~ 23 млн. поліморфізмів на 3. 2 млрд. Нуклеотидів в геномі людини Кожний ген може бути представлений у більш ніж 700 варіантах
Алельний поліморфізм – феномен, що визначає генетичну гетерогенність популяції та генетичну індивідуальність кожної людини ~ 23 млн. поліморфізмів на 3. 2 млрд. Нуклеотидів в геномі людини Кожний ген може бути представлений у більш ніж 700 варіантах
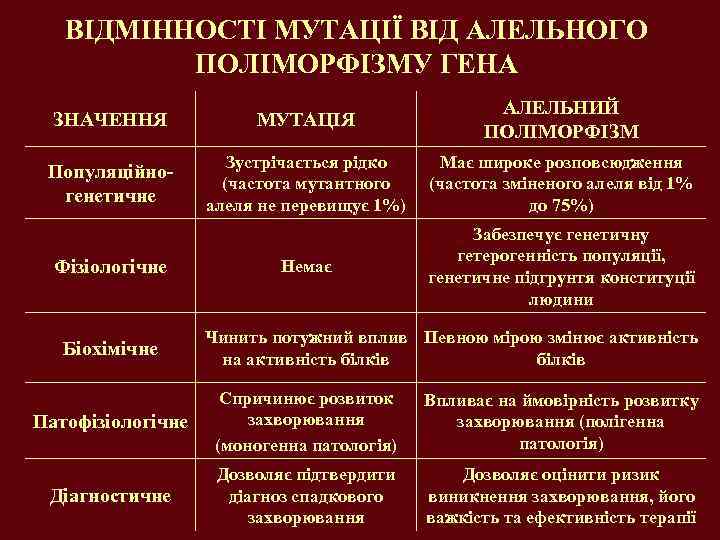 ВІДМІННОСТІ МУТАЦІЇ ВІД АЛЕЛЬНОГО ПОЛІМОРФІЗМУ ГЕНА ЗНАЧЕННЯ МУТАЦІЯ АЛЕЛЬНИЙ ПОЛІМОРФІЗМ Популяційногенетичне Зустрічається рідко (частота мутантного алеля не перевищує 1%) Має широке розповсюдження (частота зміненого алеля від 1% до 75%) Немає Забезпечує генетичну гетерогенність популяції, генетичне підгрунтя конституції людини Фізіологічне Біохімічне Чинить потужний вплив Певною мірою змінює активність на активність білків Патофізіологічне Спричинює розвиток захворювання (моногенна патологія) Впливає на ймовірність розвитку захворювання (полігенна патологія) Діагностичне Дозволяє підтвердити діагноз спадкового захворювання Дозволяє оцінити ризик виникнення захворювання, його важкість та ефективність терапії
ВІДМІННОСТІ МУТАЦІЇ ВІД АЛЕЛЬНОГО ПОЛІМОРФІЗМУ ГЕНА ЗНАЧЕННЯ МУТАЦІЯ АЛЕЛЬНИЙ ПОЛІМОРФІЗМ Популяційногенетичне Зустрічається рідко (частота мутантного алеля не перевищує 1%) Має широке розповсюдження (частота зміненого алеля від 1% до 75%) Немає Забезпечує генетичну гетерогенність популяції, генетичне підгрунтя конституції людини Фізіологічне Біохімічне Чинить потужний вплив Певною мірою змінює активність на активність білків Патофізіологічне Спричинює розвиток захворювання (моногенна патологія) Впливає на ймовірність розвитку захворювання (полігенна патологія) Діагностичне Дозволяє підтвердити діагноз спадкового захворювання Дозволяє оцінити ризик виникнення захворювання, його важкість та ефективність терапії
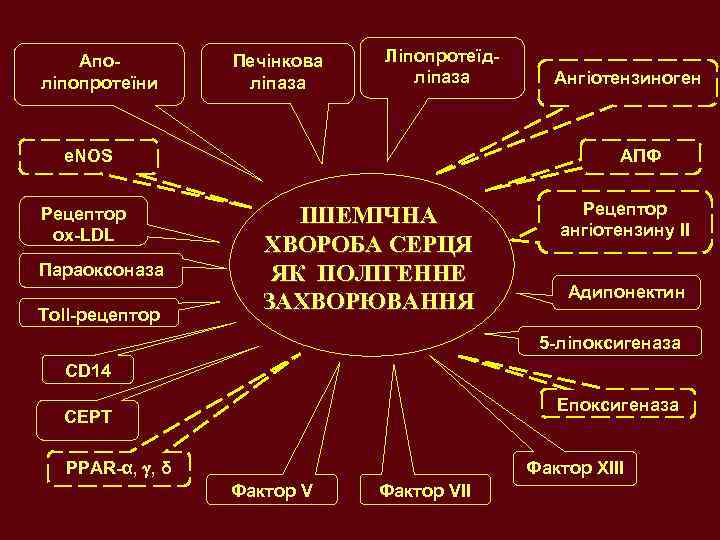 Аполіпопротеїни Печінкова ліпаза Ліпопротеїдліпаза e. NOS Рецептор ox-LDL Параоксоназа Toll-рецептор Ангіотензиноген AПФ ІШЕМІЧНА ХВОРОБА СЕРЦЯ ЯК ПОЛІГЕННЕ ЗАХВОРЮВАННЯ Рецептор ангіотензину ІІ Адипонектин 5 -ліпоксигеназа CD 14 Епоксигеназа CEPT PPAR-α, , δ Фактор XIII Фактор VII
Аполіпопротеїни Печінкова ліпаза Ліпопротеїдліпаза e. NOS Рецептор ox-LDL Параоксоназа Toll-рецептор Ангіотензиноген AПФ ІШЕМІЧНА ХВОРОБА СЕРЦЯ ЯК ПОЛІГЕННЕ ЗАХВОРЮВАННЯ Рецептор ангіотензину ІІ Адипонектин 5 -ліпоксигеназа CD 14 Епоксигеназа CEPT PPAR-α, , δ Фактор XIII Фактор VII
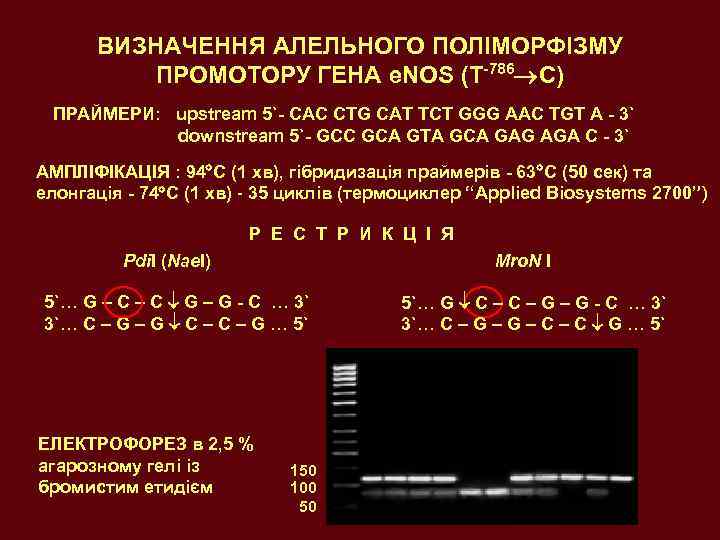 ВИЗНАЧЕННЯ АЛЕЛЬНОГО ПОЛІМОРФІЗМУ ПРОМОТОРУ ГЕНА e. NOS (T-786 C) ПРАЙМЕРИ: upstream 5`- CAC CTG CAT TCT GGG AAC TGT A - 3` downstream 5`- GCC GCA GTA GCA GAG AGA C - 3` АМПЛІФІКАЦІЯ : 94 С (1 хв), гібридизація праймерів - 63 С (50 cек) та елонгація - 74 С (1 хв) - 35 циклів (термоциклер “Applied Biosystems 2700”) Р Е С Т Р И К Ц І Я Pdi. I (Nae. I) Mro. N I 5`… G – C G – G - C … 3` 3`… C – G … 5` ЕЛЕКТРОФОРЕЗ в 2, 5 % агарозному гелі із бромистим етидієм 150 100 50 5`… G C – G – G - C … 3` 3`… C – G – C G … 5`
ВИЗНАЧЕННЯ АЛЕЛЬНОГО ПОЛІМОРФІЗМУ ПРОМОТОРУ ГЕНА e. NOS (T-786 C) ПРАЙМЕРИ: upstream 5`- CAC CTG CAT TCT GGG AAC TGT A - 3` downstream 5`- GCC GCA GTA GCA GAG AGA C - 3` АМПЛІФІКАЦІЯ : 94 С (1 хв), гібридизація праймерів - 63 С (50 cек) та елонгація - 74 С (1 хв) - 35 циклів (термоциклер “Applied Biosystems 2700”) Р Е С Т Р И К Ц І Я Pdi. I (Nae. I) Mro. N I 5`… G – C G – G - C … 3` 3`… C – G … 5` ЕЛЕКТРОФОРЕЗ в 2, 5 % агарозному гелі із бромистим етидієм 150 100 50 5`… G C – G – G - C … 3` 3`… C – G – C G … 5`
 ЗАСТОСУВАННЯ ПЛР В РЕАЛЬНОМУ ЧАСІ ДЛЯ ВИЗНАЧЕННЯ ПОЛІМОРФІЗМУ ПООДИНОКИХ НУКЛЕОТИДІВ
ЗАСТОСУВАННЯ ПЛР В РЕАЛЬНОМУ ЧАСІ ДЛЯ ВИЗНАЧЕННЯ ПОЛІМОРФІЗМУ ПООДИНОКИХ НУКЛЕОТИДІВ
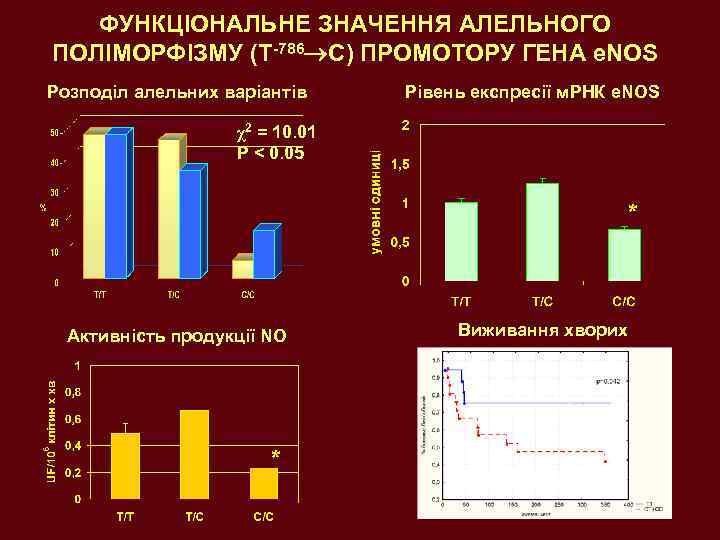 ФУНКЦІОНАЛЬНЕ ЗНАЧЕННЯ АЛЕЛЬНОГО ПОЛІМОРФІЗМУ (T-786 C) ПРОМОТОРУ ГЕНА е. NOS Розподіл алельних варіантів Рівень експресії м. РНК e. NOS χ2 = 10. 01 P < 0. 05 * Активність продукції NO * Виживання хворих
ФУНКЦІОНАЛЬНЕ ЗНАЧЕННЯ АЛЕЛЬНОГО ПОЛІМОРФІЗМУ (T-786 C) ПРОМОТОРУ ГЕНА е. NOS Розподіл алельних варіантів Рівень експресії м. РНК e. NOS χ2 = 10. 01 P < 0. 05 * Активність продукції NO * Виживання хворих
 МЕХАНІЗМИ ІШЕМІЧНОГО УШКОДЖЕННЯ КАРДІОМІОЦИТІВ Зменшення надходження кисню Пригнічення аеробних шляхів отримання енергії Активація гліколізу Накопичення лактату Накопичення жирових кислот Ацидоз Активація Na-H транспортеру Детергентоподібна дія вільних жирових кислот Инактивація мембранних ферментів Активація Na-Са транспортеру Накопичення Са++ в клітині Контрактури міофібрил Активація фосфоліпаз, ліпоксигеназ та ін. ферментів ЗАГИБЕЛЬ КЛІТИНИ
МЕХАНІЗМИ ІШЕМІЧНОГО УШКОДЖЕННЯ КАРДІОМІОЦИТІВ Зменшення надходження кисню Пригнічення аеробних шляхів отримання енергії Активація гліколізу Накопичення лактату Накопичення жирових кислот Ацидоз Активація Na-H транспортеру Детергентоподібна дія вільних жирових кислот Инактивація мембранних ферментів Активація Na-Са транспортеру Накопичення Са++ в клітині Контрактури міофібрил Активація фосфоліпаз, ліпоксигеназ та ін. ферментів ЗАГИБЕЛЬ КЛІТИНИ
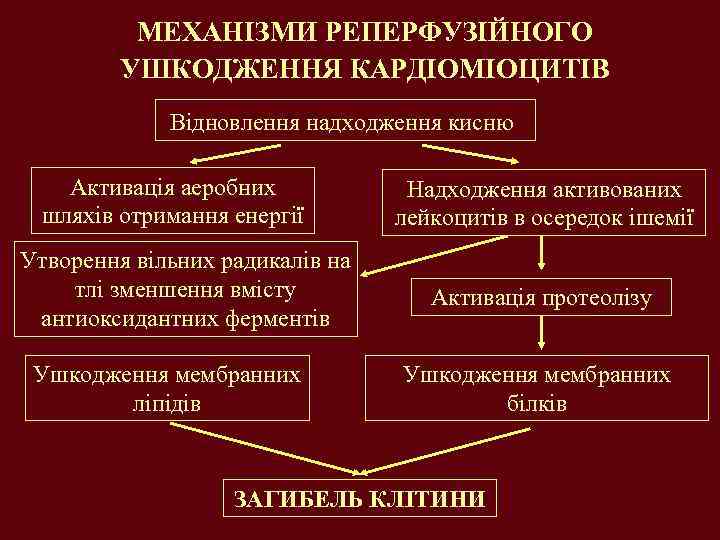 МЕХАНІЗМИ РЕПЕРФУЗІЙНОГО УШКОДЖЕННЯ КАРДІОМІОЦИТІВ Відновлення надходження кисню Активація аеробних шляхів отримання енергії Утворення вільних радикалів на тлі зменшення вмісту антиоксидантних ферментів Ушкодження мембранних ліпідів Надходження активованих лейкоцитів в осередок ішемії Активація протеолізу Ушкодження мембранних білків ЗАГИБЕЛЬ КЛІТИНИ
МЕХАНІЗМИ РЕПЕРФУЗІЙНОГО УШКОДЖЕННЯ КАРДІОМІОЦИТІВ Відновлення надходження кисню Активація аеробних шляхів отримання енергії Утворення вільних радикалів на тлі зменшення вмісту антиоксидантних ферментів Ушкодження мембранних ліпідів Надходження активованих лейкоцитів в осередок ішемії Активація протеолізу Ушкодження мембранних білків ЗАГИБЕЛЬ КЛІТИНИ
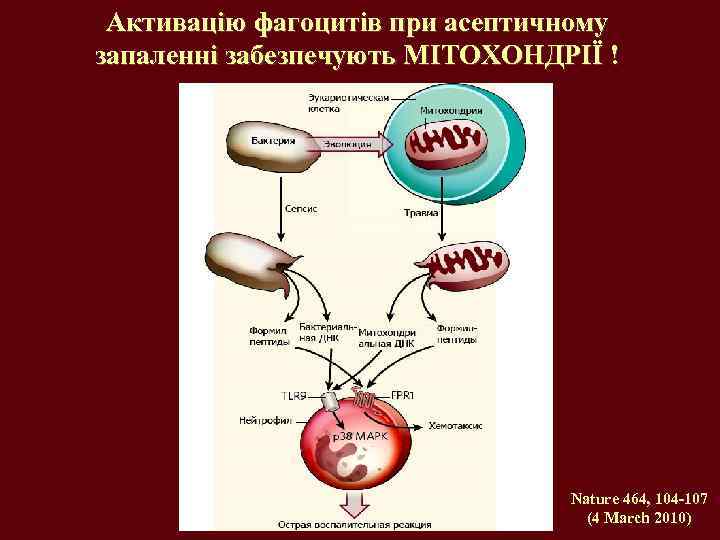 Активацію фагоцитів при асептичному запаленні забезпечують МІТОХОНДРІЇ ! Nature 464, 104 -107 (4 March 2010)
Активацію фагоцитів при асептичному запаленні забезпечують МІТОХОНДРІЇ ! Nature 464, 104 -107 (4 March 2010)
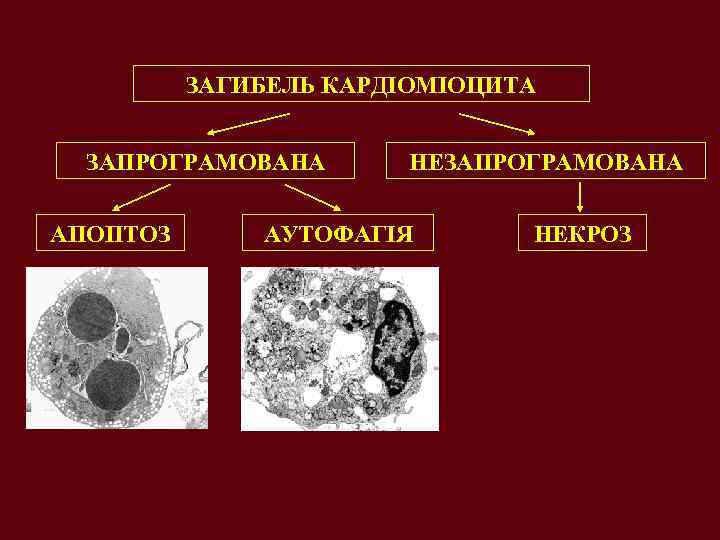 ЗАГИБЕЛЬ КАРДІОМІОЦИТА ЗАПРОГРАМОВАНА АПОПТОЗ НЕЗАПРОГРАМОВАНА АУТОФАГІЯ НЕКРОЗ
ЗАГИБЕЛЬ КАРДІОМІОЦИТА ЗАПРОГРАМОВАНА АПОПТОЗ НЕЗАПРОГРАМОВАНА АУТОФАГІЯ НЕКРОЗ
 НЕОНАТАЛЬНИЙ КАРДІОМІОЦИТ ЩУРА ПІСЛЯ 24 ГОДИН КУЛЬТИВУВАННЯ
НЕОНАТАЛЬНИЙ КАРДІОМІОЦИТ ЩУРА ПІСЛЯ 24 ГОДИН КУЛЬТИВУВАННЯ
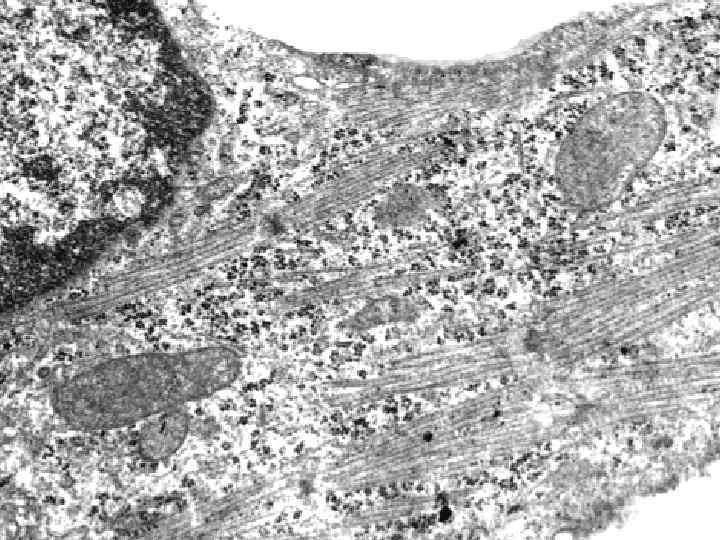
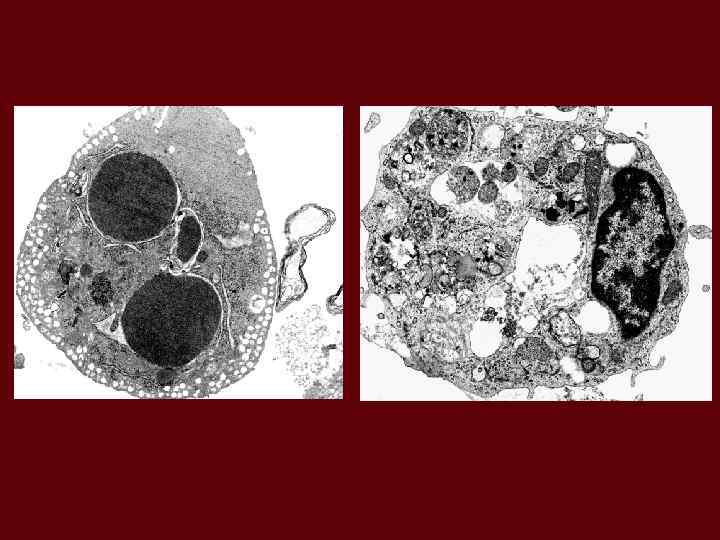
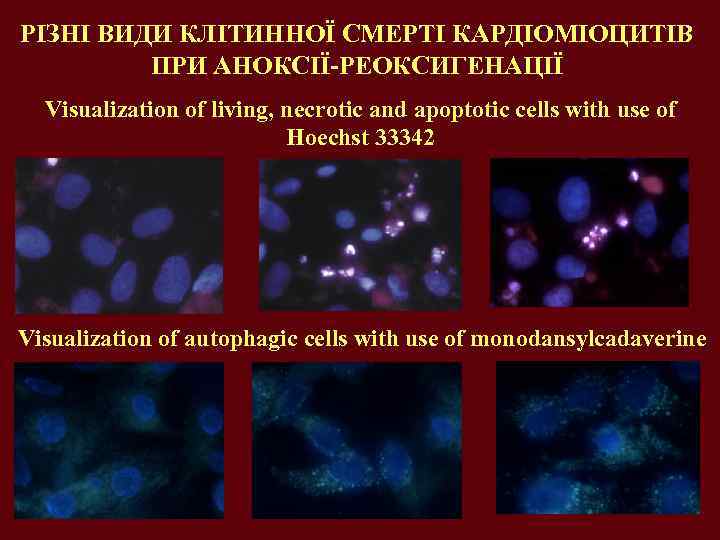 РІЗНІ ВИДИ КЛІТИННОЇ СМЕРТІ КАРДІОМІОЦИТІВ ПРИ АНОКСІЇ-РЕОКСИГЕНАЦІЇ Visualization of living, necrotic and apoptotic cells with use of Hoechst 33342 Visualization of autophagic cells with use of monodansylcadaverine
РІЗНІ ВИДИ КЛІТИННОЇ СМЕРТІ КАРДІОМІОЦИТІВ ПРИ АНОКСІЇ-РЕОКСИГЕНАЦІЇ Visualization of living, necrotic and apoptotic cells with use of Hoechst 33342 Visualization of autophagic cells with use of monodansylcadaverine
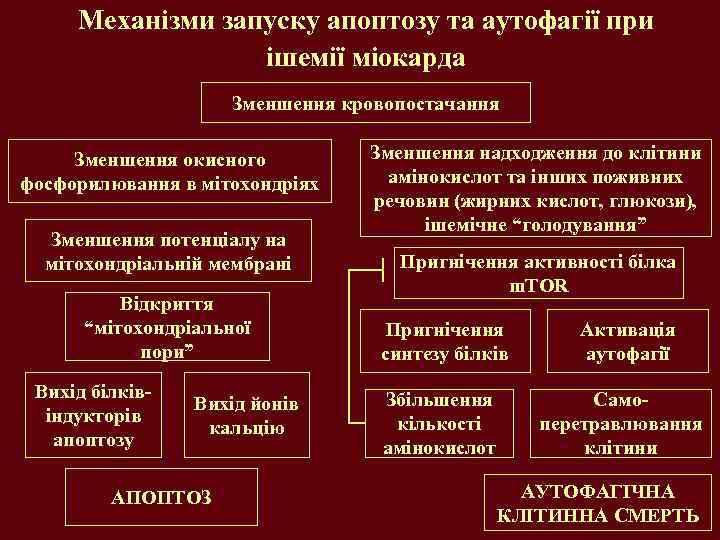 Механізми запуску апоптозу та аутофагії при ішемії міокарда Зменшення кровопостачання Зменшення окисного фосфорилювання в мітохондріях Зменшення потенціалу на мітохондріальній мембрані Відкриття “мітохондріальної пори” Вихід білківіндукторів апоптозу Вихід йонів кальцію АПОПТОЗ Зменшення надходження до клітини амінокислот та інших поживних речовин (жирних кислот, глюкози), ішемічне “голодування” Пригнічення активності білка m. TOR Пригнічення синтезу білків Збільшення кількості амінокислот Активація аутофагії Самоперетравлювання клітини АУТОФАГІЧНА КЛІТИННА СМЕРТЬ
Механізми запуску апоптозу та аутофагії при ішемії міокарда Зменшення кровопостачання Зменшення окисного фосфорилювання в мітохондріях Зменшення потенціалу на мітохондріальній мембрані Відкриття “мітохондріальної пори” Вихід білківіндукторів апоптозу Вихід йонів кальцію АПОПТОЗ Зменшення надходження до клітини амінокислот та інших поживних речовин (жирних кислот, глюкози), ішемічне “голодування” Пригнічення активності білка m. TOR Пригнічення синтезу білків Збільшення кількості амінокислот Активація аутофагії Самоперетравлювання клітини АУТОФАГІЧНА КЛІТИННА СМЕРТЬ
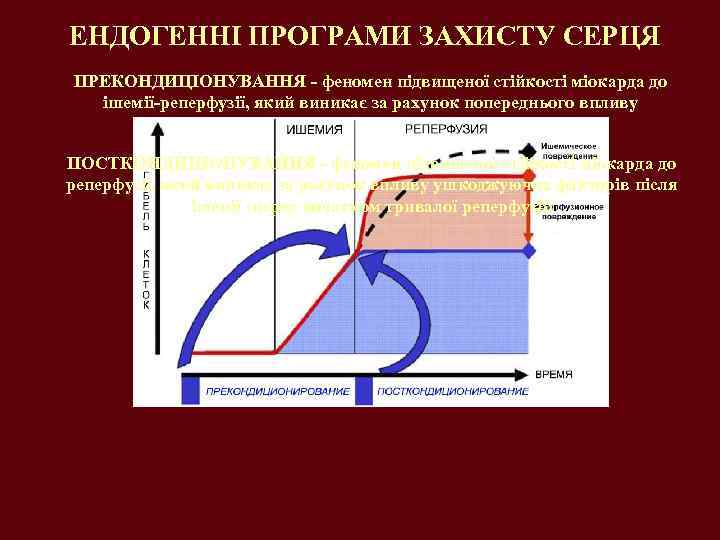 ЕНДОГЕННІ ПРОГРАМИ ЗАХИСТУ СЕРЦЯ ПРЕКОНДИЦІОНУВАННЯ - феномен підвищеної стійкості міокарда до ішемії-реперфузії, який виникає за рахунок попереднього впливу которкочасної ішемії або інших ушкоджуючих факторів ПОСТКОНДИЦІОНУВАННЯ - феномен підвищеної стійкості міокарда до реперфузії, який виникає за рахунок впливу ушкоджуючих факторів після ішемії (перед початком тривалої реперфузії)
ЕНДОГЕННІ ПРОГРАМИ ЗАХИСТУ СЕРЦЯ ПРЕКОНДИЦІОНУВАННЯ - феномен підвищеної стійкості міокарда до ішемії-реперфузії, який виникає за рахунок попереднього впливу которкочасної ішемії або інших ушкоджуючих факторів ПОСТКОНДИЦІОНУВАННЯ - феномен підвищеної стійкості міокарда до реперфузії, який виникає за рахунок впливу ушкоджуючих факторів після ішемії (перед початком тривалої реперфузії)
 ФАКТОРИ ІНДУКЦІЇ ПРЕ- ТА ПОСТКОНДИЦІОНУВАННЯ ЕКЗОГЕННІ: Фізичні – гіпоксія, гіпертермія Хімічні – засоби для інгаляційного наркозу (десфлуран, ізофлуран, галотан), опіати, інгібітори протеасоми активатори АТФчутливих калієвих каналів та ін. Біологічні – ліпополісахариди бактерій ЕНДОГЕННІ: ішемія, ішемія-реперфузія, аденозин, NO, брадикінін, ацетилхолін та ін.
ФАКТОРИ ІНДУКЦІЇ ПРЕ- ТА ПОСТКОНДИЦІОНУВАННЯ ЕКЗОГЕННІ: Фізичні – гіпоксія, гіпертермія Хімічні – засоби для інгаляційного наркозу (десфлуран, ізофлуран, галотан), опіати, інгібітори протеасоми активатори АТФчутливих калієвих каналів та ін. Біологічні – ліпополісахариди бактерій ЕНДОГЕННІ: ішемія, ішемія-реперфузія, аденозин, NO, брадикінін, ацетилхолін та ін.
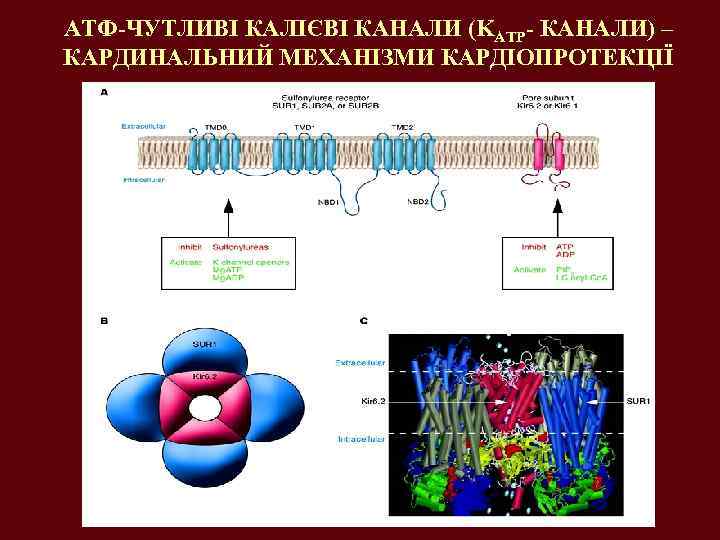 АТФ-ЧУТЛИВІ КАЛІЄВІ КАНАЛИ (KATP- КАНАЛИ) – КАРДИНАЛЬНИЙ МЕХАНІЗМИ КАРДІОПРОТЕКЦІЇ
АТФ-ЧУТЛИВІ КАЛІЄВІ КАНАЛИ (KATP- КАНАЛИ) – КАРДИНАЛЬНИЙ МЕХАНІЗМИ КАРДІОПРОТЕКЦІЇ
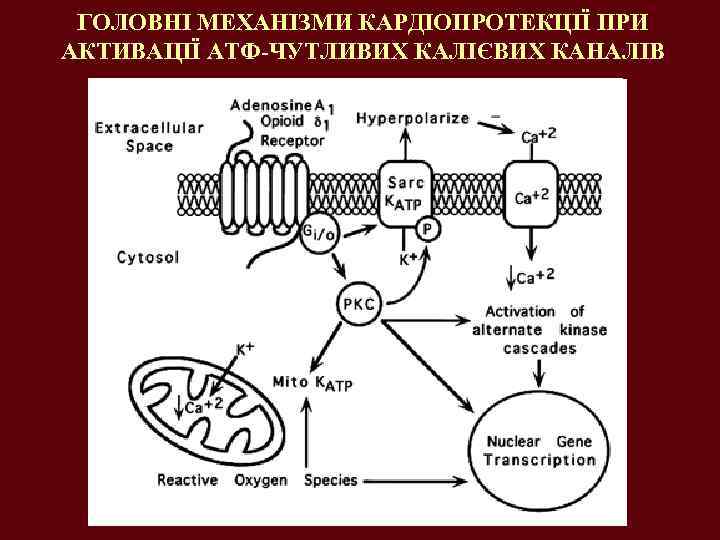 ГОЛОВНІ МЕХАНІЗМИ КАРДІОПРОТЕКЦІЇ ПРИ АКТИВАЦІЇ АТФ-ЧУТЛИВИХ КАЛІЄВИХ КАНАЛІВ
ГОЛОВНІ МЕХАНІЗМИ КАРДІОПРОТЕКЦІЇ ПРИ АКТИВАЦІЇ АТФ-ЧУТЛИВИХ КАЛІЄВИХ КАНАЛІВ
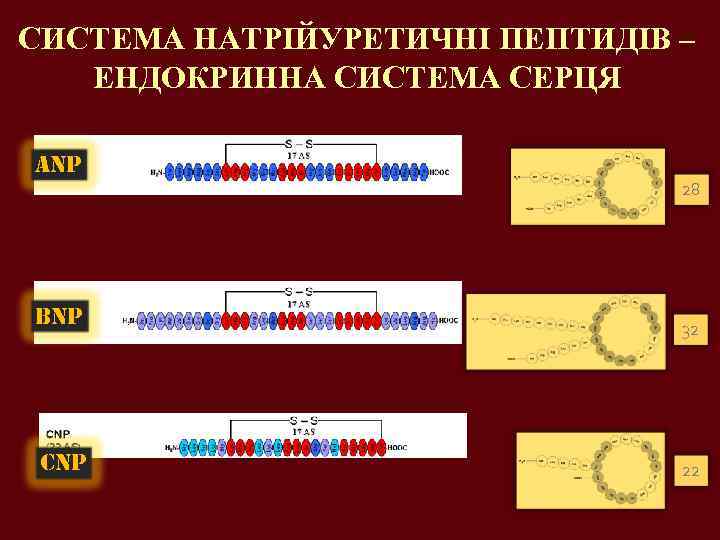 СИСТЕМА НАТРІЙУРЕТИЧНІ ПЕПТИДІВ – ЕНДОКРИННА СИСТЕМА СЕРЦЯ ANP BNP CNP 28 32 22
СИСТЕМА НАТРІЙУРЕТИЧНІ ПЕПТИДІВ – ЕНДОКРИННА СИСТЕМА СЕРЦЯ ANP BNP CNP 28 32 22
 ЕФЕКТИ NPS натрійурезу; діурезу; швидкості клубочкової фільтрації; кровообігу нирок.
ЕФЕКТИ NPS натрійурезу; діурезу; швидкості клубочкової фільтрації; кровообігу нирок.
 О. О. Мойбенко
О. О. Мойбенко
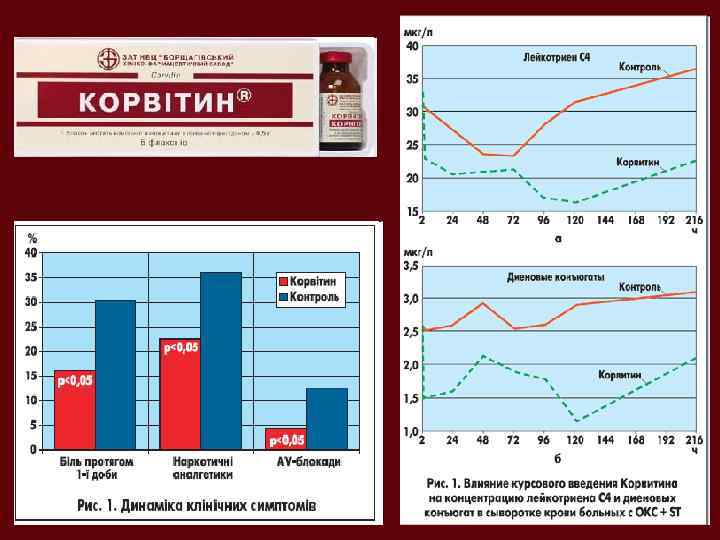

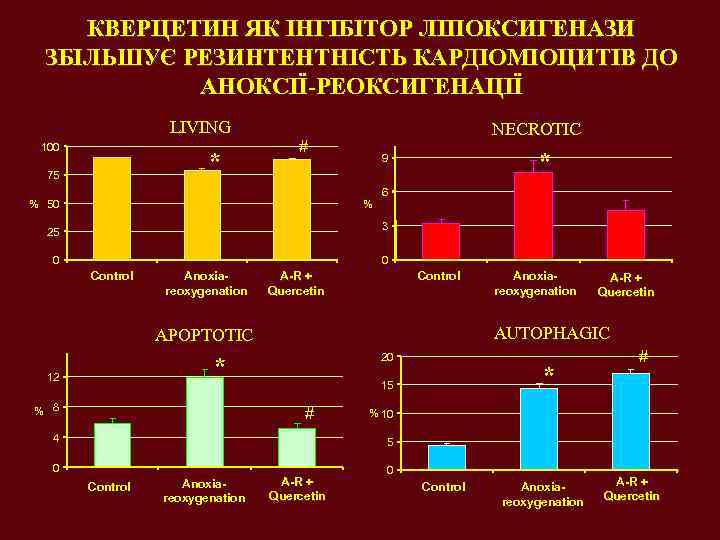 КВЕРЦЕТИН ЯК ІНГІБІТОР ЛІПОКСИГЕНАЗИ ЗБІЛЬШУЄ РЕЗИНТЕНТНІСТЬ КАРДІОМІОЦИТІВ ДО АНОКСІЇ-РЕОКСИГЕНАЦІЇ LIVING 100 * 75 NECROTIC # % 50 * 9 % 6 25 3 0 0 Control Anoxiareoxygenation A-R + Quercetin Control 20 * * 15 % 8 A-R + Quercetin AUTOPHAGIC APOPTOTIC 12 Anoxiareoxygenation # 4 # % 10 5 0 Control Anoxiareoxygenation A-R + Quercetin
КВЕРЦЕТИН ЯК ІНГІБІТОР ЛІПОКСИГЕНАЗИ ЗБІЛЬШУЄ РЕЗИНТЕНТНІСТЬ КАРДІОМІОЦИТІВ ДО АНОКСІЇ-РЕОКСИГЕНАЦІЇ LIVING 100 * 75 NECROTIC # % 50 * 9 % 6 25 3 0 0 Control Anoxiareoxygenation A-R + Quercetin Control 20 * * 15 % 8 A-R + Quercetin AUTOPHAGIC APOPTOTIC 12 Anoxiareoxygenation # 4 # % 10 5 0 Control Anoxiareoxygenation A-R + Quercetin
 ELECTROPORATION OF si. RNA IN NEONATAL CARDIOMYOCYTES Silencing ALOX 5 si. RNA GUACAGGAAGGGAACAUUUUU UUCAUGUCCUUCCCUUGUAAA Nonsilencing (scrambled) si. RNA UGUUCAGCGAAAUAUAACCUU UUACAAGUCGCUUUAUAUUGG
ELECTROPORATION OF si. RNA IN NEONATAL CARDIOMYOCYTES Silencing ALOX 5 si. RNA GUACAGGAAGGGAACAUUUUU UUCAUGUCCUUCCCUUGUAAA Nonsilencing (scrambled) si. RNA UGUUCAGCGAAAUAUAACCUU UUACAAGUCGCUUUAUAUUGG
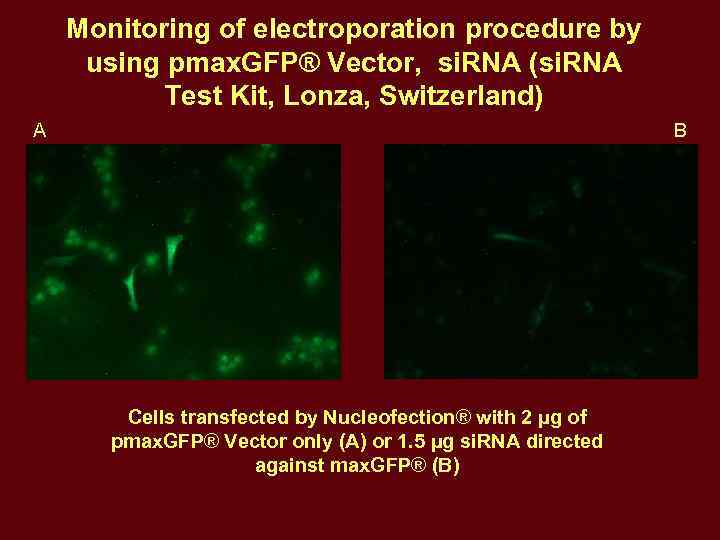 Monitoring of electroporation procedure by using pmax. GFP® Vector, si. RNA (si. RNA Test Kit, Lonza, Switzerland) A B Cells transfected by Nucleofection® with 2 µg of pmax. GFP® Vector only (A) or 1. 5 µg si. RNA directed against max. GFP® (B)
Monitoring of electroporation procedure by using pmax. GFP® Vector, si. RNA (si. RNA Test Kit, Lonza, Switzerland) A B Cells transfected by Nucleofection® with 2 µg of pmax. GFP® Vector only (A) or 1. 5 µg si. RNA directed against max. GFP® (B)
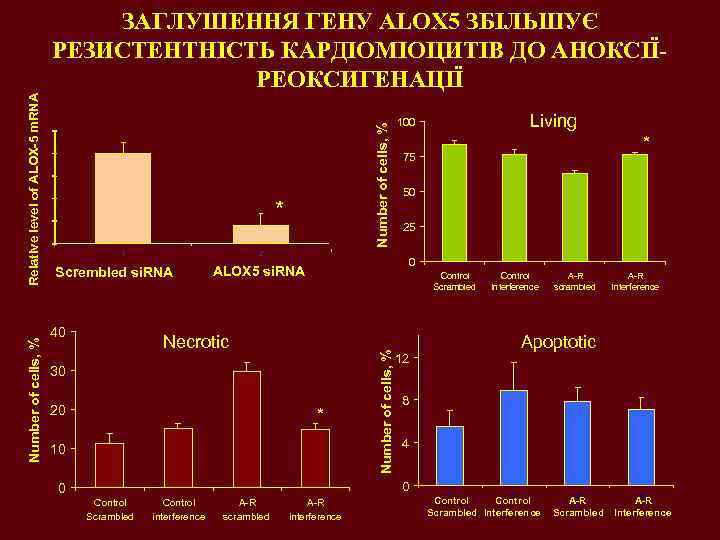 Number of cells, % * 1 Scrembled si. RNA 40 50 25 0 Control Scrambled Necrotic 30 * 10 Control interference A-R scrambled А-R interference Apoptotic 12 8 4 0 0 Control Scrambled * 75 ALOX 5 si. RNA 20 Living 100 2 Number of cells, % Relative level of ALOX-5 m. RNA ЗАГЛУШЕННЯ ГЕНУ ALOX 5 ЗБІЛЬШУЄ РЕЗИСТЕНТНІСТЬ КАРДІОМІОЦИТІВ ДО АНОКСІЇРЕОКСИГЕНАЦІЇ 1 2 Control Scrambled Interference 3 A-R Scrambled 4 A-R Interference
Number of cells, % * 1 Scrembled si. RNA 40 50 25 0 Control Scrambled Necrotic 30 * 10 Control interference A-R scrambled А-R interference Apoptotic 12 8 4 0 0 Control Scrambled * 75 ALOX 5 si. RNA 20 Living 100 2 Number of cells, % Relative level of ALOX-5 m. RNA ЗАГЛУШЕННЯ ГЕНУ ALOX 5 ЗБІЛЬШУЄ РЕЗИСТЕНТНІСТЬ КАРДІОМІОЦИТІВ ДО АНОКСІЇРЕОКСИГЕНАЦІЇ 1 2 Control Scrambled Interference 3 A-R Scrambled 4 A-R Interference
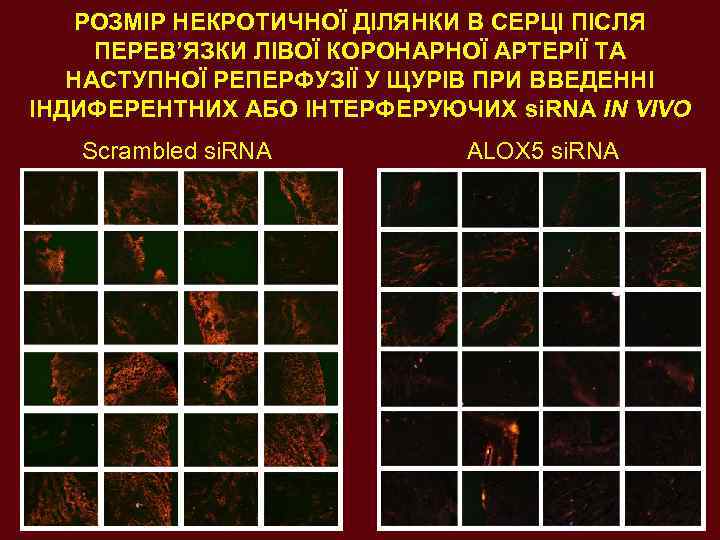 РОЗМІР НЕКРОТИЧНОЇ ДІЛЯНКИ В СЕРЦІ ПІСЛЯ ПЕРЕВ’ЯЗКИ ЛІВОЇ КОРОНАРНОЇ АРТЕРІЇ ТА НАСТУПНОЇ РЕПЕРФУЗІЇ У ЩУРІВ ПРИ ВВЕДЕННІ ІНДИФЕРЕНТНИХ АБО ІНТЕРФЕРУЮЧИХ si. RNA IN VIVO Scrambled si. RNA ALOX 5 si. RNA
РОЗМІР НЕКРОТИЧНОЇ ДІЛЯНКИ В СЕРЦІ ПІСЛЯ ПЕРЕВ’ЯЗКИ ЛІВОЇ КОРОНАРНОЇ АРТЕРІЇ ТА НАСТУПНОЇ РЕПЕРФУЗІЇ У ЩУРІВ ПРИ ВВЕДЕННІ ІНДИФЕРЕНТНИХ АБО ІНТЕРФЕРУЮЧИХ si. RNA IN VIVO Scrambled si. RNA ALOX 5 si. RNA
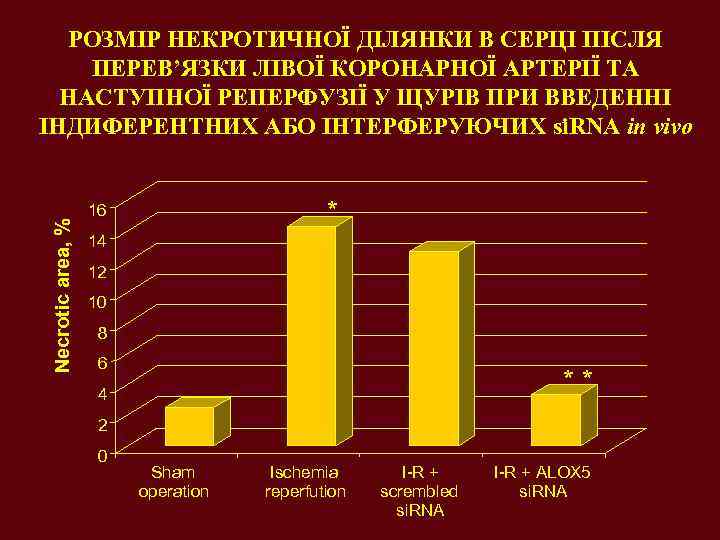 Necrotic area, % РОЗМІР НЕКРОТИЧНОЇ ДІЛЯНКИ В СЕРЦІ ПІСЛЯ ПЕРЕВ’ЯЗКИ ЛІВОЇ КОРОНАРНОЇ АРТЕРІЇ ТА НАСТУПНОЇ РЕПЕРФУЗІЇ У ЩУРІВ ПРИ ВВЕДЕННІ ІНДИФЕРЕНТНИХ АБО ІНТЕРФЕРУЮЧИХ si. RNA in vivo * 16 14 12 10 8 6 ** 4 2 0 Sham operation Ischemia reperfution І-R + scrembled si. RNA І-R + ALOX 5 si. RNA
Necrotic area, % РОЗМІР НЕКРОТИЧНОЇ ДІЛЯНКИ В СЕРЦІ ПІСЛЯ ПЕРЕВ’ЯЗКИ ЛІВОЇ КОРОНАРНОЇ АРТЕРІЇ ТА НАСТУПНОЇ РЕПЕРФУЗІЇ У ЩУРІВ ПРИ ВВЕДЕННІ ІНДИФЕРЕНТНИХ АБО ІНТЕРФЕРУЮЧИХ si. RNA in vivo * 16 14 12 10 8 6 ** 4 2 0 Sham operation Ischemia reperfution І-R + scrembled si. RNA І-R + ALOX 5 si. RNA
 Загальний принцип РНКінтерференції
Загальний принцип РНКінтерференції
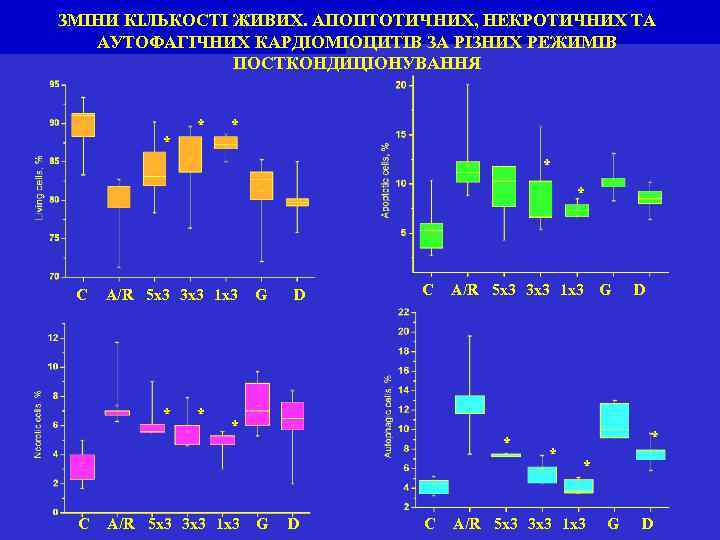 ЗМІНИ КІЛЬКОСТІ ЖИВИХ. АПОПТОТИЧНИХ, НЕКРОТИЧНИХ ТА АУТОФАГІЧНИХ КАРДІОМІОЦИТІВ ЗА РІЗНИХ РЕЖИМІВ ПОСТКОНДИЦІОНУВАННЯ * * * С А/R 5 x 3 3 x 3 1 x 3 * С * G D С * А/R 5 x 3 3 x 3 1 x 3 G * D С * D * * А/R 5 x 3 3 x 3 1 x 3 G D
ЗМІНИ КІЛЬКОСТІ ЖИВИХ. АПОПТОТИЧНИХ, НЕКРОТИЧНИХ ТА АУТОФАГІЧНИХ КАРДІОМІОЦИТІВ ЗА РІЗНИХ РЕЖИМІВ ПОСТКОНДИЦІОНУВАННЯ * * * С А/R 5 x 3 3 x 3 1 x 3 * С * G D С * А/R 5 x 3 3 x 3 1 x 3 G * D С * D * * А/R 5 x 3 3 x 3 1 x 3 G D