Патофизиология периферического нейромоторного аппарата












ПАТОФИЗИОЛОГИЯ Н-М АППАРАТА2013.ppt
- Количество слайдов: 35
 Патофизиология периферического нейромоторного аппарата человека
Патофизиология периферического нейромоторного аппарата человека
 Нервно-мышечные болезни – патологии скелетной мускулатуры и двигательной нервной системы (Гехт, Ильина, 1982). Классификация (в соответствии с местом первичного поражения) 1. Идиопатические, или первичномышечные миопатии (первичные) а) миодистрофии б) миопатии, обусловленные метаболическими или эндокринными нарушениями в) миотонии и периодические мышечные параличи г) миопатии, обусловленные воспалительными процессами в мышцах 2. Нейрогенные миопатии (вторичные) а) болезни моторного нейрона, или спинальные мышечные атрофии б) аксонопатии, или болезни периферического нерва в) полиневропатии (воспаление, токсикоз и др. патологии мотонейронов) 3. Болезни нервно-мышечного синапса Среди всех групп также различают 1. первичные миопатии, или наследственные, генетически детерминированные и 2. вторичные миопатии, или приобретенные, ненаследуемые формы
Нервно-мышечные болезни – патологии скелетной мускулатуры и двигательной нервной системы (Гехт, Ильина, 1982). Классификация (в соответствии с местом первичного поражения) 1. Идиопатические, или первичномышечные миопатии (первичные) а) миодистрофии б) миопатии, обусловленные метаболическими или эндокринными нарушениями в) миотонии и периодические мышечные параличи г) миопатии, обусловленные воспалительными процессами в мышцах 2. Нейрогенные миопатии (вторичные) а) болезни моторного нейрона, или спинальные мышечные атрофии б) аксонопатии, или болезни периферического нерва в) полиневропатии (воспаление, токсикоз и др. патологии мотонейронов) 3. Болезни нервно-мышечного синапса Среди всех групп также различают 1. первичные миопатии, или наследственные, генетически детерминированные и 2. вторичные миопатии, или приобретенные, ненаследуемые формы
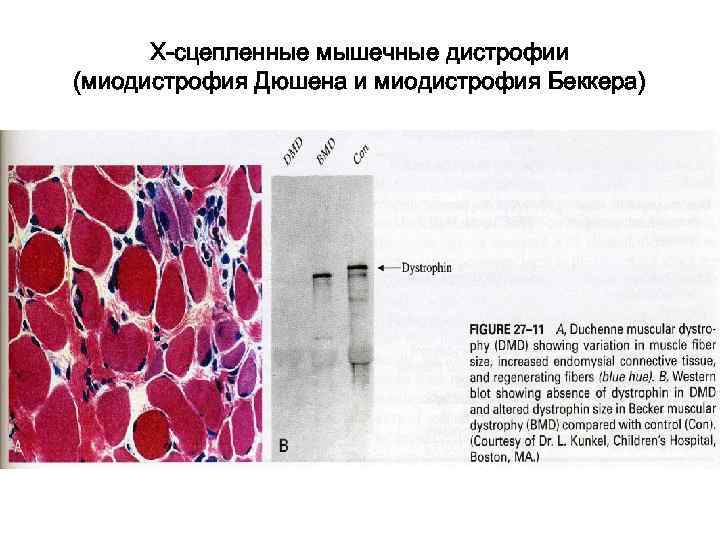
 Х-сцепленные мышечные дистрофии (миодистрофия Дюшена и миодистрофия Беккера) Эпидемиология. МДД - тяжелое летальное наследственное заболевание, сцепленное с полом, и встречается в среднем с частотой 1: 3500 (3000 - 5000) новорождённых мальчиков. Начало болезни в возрасте около 5 лет, к 10 -12 годам прикованы к инвалидному креслу и летальный исход до 20 лет. Единицы доживают до 30 лет. МДБ- начало в юном (10 -15 лет) или зрелом возрасте, медленно прогрессирует. Генетика. ►Дефект в 21 положении Х-хромосомы (Хр21) : делеции неравномерно по длине гена, чаще в его начале (5’-концевая область) и в середине. Реже встречаются мутации сдвига рамки считывания и точечные мутации. ► 2/3 мутаций – наследование по рецессивному типу, 1/3 – мутации de novo (для МДД). ►отсутствие фибриллярного белка дистрофина (427 к. Д) при миодистрофии Дюшена (описана в 1868 г французским врачом-неврологом Г. Дюшенном) и уменьшенное количество дистрофина (часто с аномальным молекулярным весом) при миодистрофии Беккера (описана в 1950 -х гг немецким врачом П. Беккером). Модель на животных – мыши линии mdx.
Х-сцепленные мышечные дистрофии (миодистрофия Дюшена и миодистрофия Беккера) Эпидемиология. МДД - тяжелое летальное наследственное заболевание, сцепленное с полом, и встречается в среднем с частотой 1: 3500 (3000 - 5000) новорождённых мальчиков. Начало болезни в возрасте около 5 лет, к 10 -12 годам прикованы к инвалидному креслу и летальный исход до 20 лет. Единицы доживают до 30 лет. МДБ- начало в юном (10 -15 лет) или зрелом возрасте, медленно прогрессирует. Генетика. ►Дефект в 21 положении Х-хромосомы (Хр21) : делеции неравномерно по длине гена, чаще в его начале (5’-концевая область) и в середине. Реже встречаются мутации сдвига рамки считывания и точечные мутации. ► 2/3 мутаций – наследование по рецессивному типу, 1/3 – мутации de novo (для МДД). ►отсутствие фибриллярного белка дистрофина (427 к. Д) при миодистрофии Дюшена (описана в 1868 г французским врачом-неврологом Г. Дюшенном) и уменьшенное количество дистрофина (часто с аномальным молекулярным весом) при миодистрофии Беккера (описана в 1950 -х гг немецким врачом П. Беккером). Модель на животных – мыши линии mdx.
 Х-сцепленные мышечные дистрофии (миодистрофия Дюшена и миодистрофия Беккера)
Х-сцепленные мышечные дистрофии (миодистрофия Дюшена и миодистрофия Беккера)
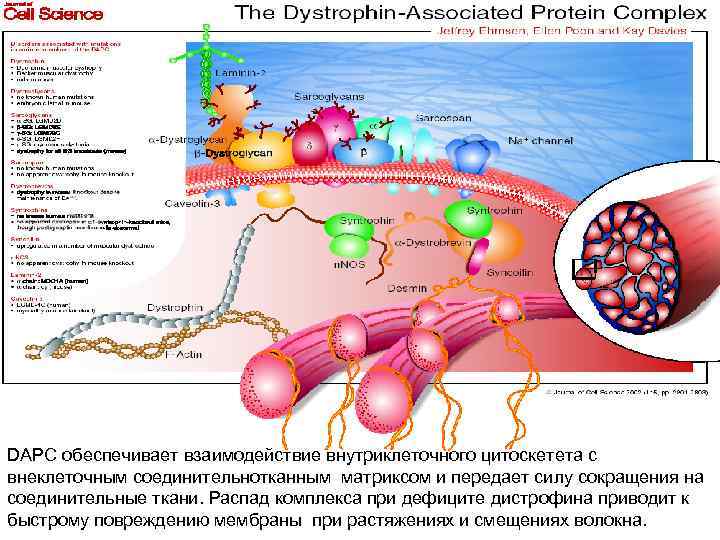
 DAPC обеспечивает взаимодействие внутриклеточного цитоскетета с внеклеточным соединительнотканным матриксом и передает силу сокращения на соединительные ткани. Распад комплекса при дефиците дистрофина приводит к быстрому повреждению мембраны при растяжениях и смещениях волокна.
DAPC обеспечивает взаимодействие внутриклеточного цитоскетета с внеклеточным соединительнотканным матриксом и передает силу сокращения на соединительные ткани. Распад комплекса при дефиците дистрофина приводит к быстрому повреждению мембраны при растяжениях и смещениях волокна.
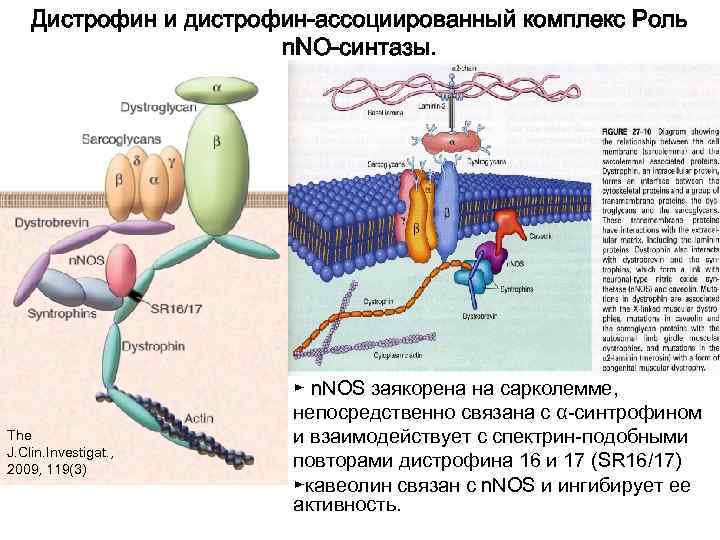
 Дистрофин и дистрофин-ассоциированный комплекс Роль n. NO-синтазы. ► n. NOS заякорена на сарколемме, непосредственно связана с α-синтрофином The и взаимодействует с спектрин-подобными J. Clin. Investigat. , 2009, 119(3) повторами дистрофина 16 и 17 (SR 16/17) ►кавеолин связан с n. NOS и ингибирует ее активность.
Дистрофин и дистрофин-ассоциированный комплекс Роль n. NO-синтазы. ► n. NOS заякорена на сарколемме, непосредственно связана с α-синтрофином The и взаимодействует с спектрин-подобными J. Clin. Investigat. , 2009, 119(3) повторами дистрофина 16 и 17 (SR 16/17) ►кавеолин связан с n. NOS и ингибирует ее активность.
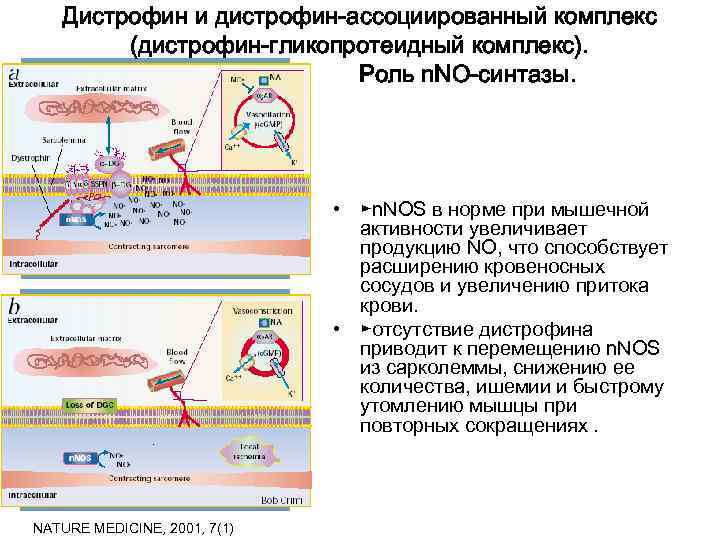
 Дистрофин и дистрофин-ассоциированный комплекс (дистрофин-гликопротеидный комплекс). Роль n. NO-синтазы. • ►n. NOS в норме при мышечной активности увеличивает продукцию NO, что способствует расширению кровеносных сосудов и увеличению притока крови. • ►отсутствие дистрофина приводит к перемещению n. NOS из сарколеммы, снижению ее количества, ишемии и быстрому утомлению мышцы при повторных сокращениях. NATURE MEDICINE, 2001, 7(1)
Дистрофин и дистрофин-ассоциированный комплекс (дистрофин-гликопротеидный комплекс). Роль n. NO-синтазы. • ►n. NOS в норме при мышечной активности увеличивает продукцию NO, что способствует расширению кровеносных сосудов и увеличению притока крови. • ►отсутствие дистрофина приводит к перемещению n. NOS из сарколеммы, снижению ее количества, ишемии и быстрому утомлению мышцы при повторных сокращениях. NATURE MEDICINE, 2001, 7(1)
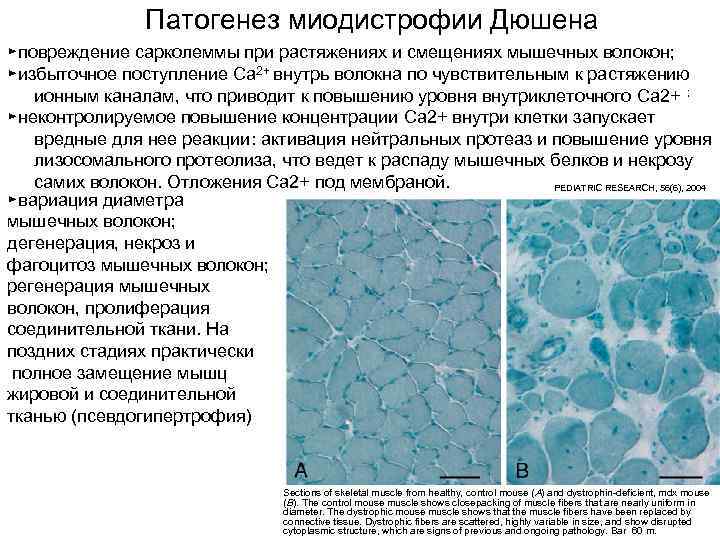
 Патогенез миодистрофии Дюшена ►повреждение сарколеммы при растяжениях и смещениях мышечных волокон; ►избыточное поступление Ca 2+ внутрь волокна по чувствительным к растяжению ионным каналам, что приводит к повышению уровня внутриклеточного Ca 2+ ; ►неконтролируемое повышение концентрации Ca 2+ внутри клетки запускает вредные для нее реакции: активация нейтральных протеаз и повышение уровня лизосомального протеолиза, что ведет к распаду мышечных белков и некрозу самих волокон. Отложения Са 2+ под мембраной. PEDIATRIC RESEARCH, 56(6), 2004 ►вариация диаметра мышечных волокон; дегенерация, некроз и фагоцитоз мышечных волокон; регенерация мышечных волокон, пролиферация соединительной ткани. На поздних стадиях практически полное замещение мышц жировой и соединительной тканью (псевдогипертрофия) Sections of skeletal muscle from healthy, control mouse (A) and dystrophin-deficient, mdx mouse (B). The control mouse muscle shows closepacking of muscle fibers that are nearly uniform in diameter. The dystrophic mouse muscle shows that the muscle fibers have been replaced by connective tissue. Dystrophic fibers are scattered, highly variable in size, and show disrupted cytoplasmic structure, which are signs of previous and ongoing pathology. Bar 60 m.
Патогенез миодистрофии Дюшена ►повреждение сарколеммы при растяжениях и смещениях мышечных волокон; ►избыточное поступление Ca 2+ внутрь волокна по чувствительным к растяжению ионным каналам, что приводит к повышению уровня внутриклеточного Ca 2+ ; ►неконтролируемое повышение концентрации Ca 2+ внутри клетки запускает вредные для нее реакции: активация нейтральных протеаз и повышение уровня лизосомального протеолиза, что ведет к распаду мышечных белков и некрозу самих волокон. Отложения Са 2+ под мембраной. PEDIATRIC RESEARCH, 56(6), 2004 ►вариация диаметра мышечных волокон; дегенерация, некроз и фагоцитоз мышечных волокон; регенерация мышечных волокон, пролиферация соединительной ткани. На поздних стадиях практически полное замещение мышц жировой и соединительной тканью (псевдогипертрофия) Sections of skeletal muscle from healthy, control mouse (A) and dystrophin-deficient, mdx mouse (B). The control mouse muscle shows closepacking of muscle fibers that are nearly uniform in diameter. The dystrophic mouse muscle shows that the muscle fibers have been replaced by connective tissue. Dystrophic fibers are scattered, highly variable in size, and show disrupted cytoplasmic structure, which are signs of previous and ongoing pathology. Bar 60 m.
 Клиническая картина • Мальчики нормальны при рождении, но поздно начинают ходить, не умеют бегать и прыгать. Слабость и атрофия мышц начинается с пояса нижних конечностей (трудно подниматься с пола, подниматься по лестнице, утиная и неустойчивая походка вперевалку, часто падают) и распространяется на пояс верхних конечностей. Увеличение икроножных мышц вместе с ослаблением – важный клинический признак (псевдогипертрофия). Атрофический процесс развивается и в сердце (кардиомиопатия). • Повышение концентрации фосфокреатинкиназы в сыворотке крови в первое десятилетие жизни и позже возвращение к норме (нет мышц). • Смерть в результате респираторной недостаточности, легочной инфекции, сердечной недостаточности. • Женщины-носительницы дюшеновского гена - нет клинических симптомов, но может быть повышена концентрация креатинкиназы в сыворотке крови и могут быть минимальные аномалии на мышечной биопсии. Риск развития дилятационной кардимиопатии. http: //www. mda. org/ disease/dmd. html Миодистрофия Беккера: доброкачественная форма миодистрофии. Частота миодистрофии Беккера у новорождённых мальчиков составляет 1: 20 000. По клиническим симптомам миодистрофия Беккера напоминает миодистрофию Дюшенна, но в менее выраженной форме. Начало болезни - не ранее 10 -15 лет, течение мягкое, больные сохраняют работоспособность в возрасте 20 -30 лет.
Клиническая картина • Мальчики нормальны при рождении, но поздно начинают ходить, не умеют бегать и прыгать. Слабость и атрофия мышц начинается с пояса нижних конечностей (трудно подниматься с пола, подниматься по лестнице, утиная и неустойчивая походка вперевалку, часто падают) и распространяется на пояс верхних конечностей. Увеличение икроножных мышц вместе с ослаблением – важный клинический признак (псевдогипертрофия). Атрофический процесс развивается и в сердце (кардиомиопатия). • Повышение концентрации фосфокреатинкиназы в сыворотке крови в первое десятилетие жизни и позже возвращение к норме (нет мышц). • Смерть в результате респираторной недостаточности, легочной инфекции, сердечной недостаточности. • Женщины-носительницы дюшеновского гена - нет клинических симптомов, но может быть повышена концентрация креатинкиназы в сыворотке крови и могут быть минимальные аномалии на мышечной биопсии. Риск развития дилятационной кардимиопатии. http: //www. mda. org/ disease/dmd. html Миодистрофия Беккера: доброкачественная форма миодистрофии. Частота миодистрофии Беккера у новорождённых мальчиков составляет 1: 20 000. По клиническим симптомам миодистрофия Беккера напоминает миодистрофию Дюшенна, но в менее выраженной форме. Начало болезни - не ранее 10 -15 лет, течение мягкое, больные сохраняют работоспособность в возрасте 20 -30 лет.
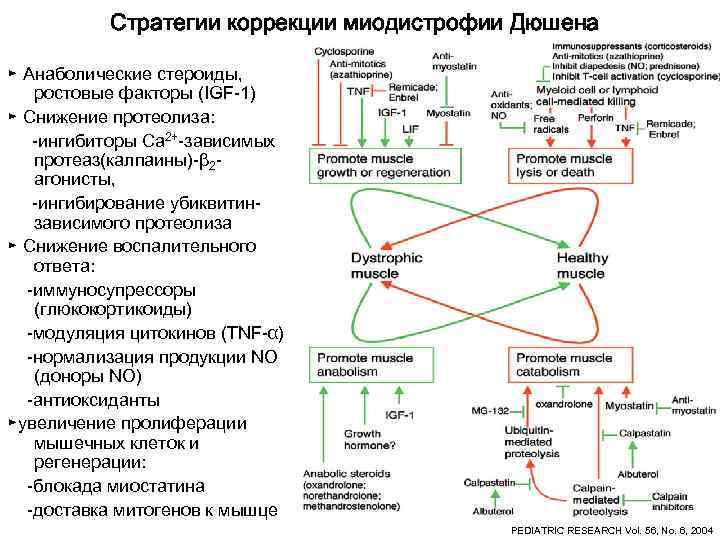
 Стратегии коррекции миодистрофии Дюшена ► Анаболические стероиды, ростовые факторы (IGF-1) ► Снижение протеолиза: -ингибиторы Ca 2+-зависимых протеаз(калпаины)-β 2 - агонисты, -ингибирование убиквитин- зависимого протеолиза ► Снижение воспалительного ответа: -иммуносупрессоры (глюкокортикоиды) -модуляция цитокинов (TNF-α) -нормализация продукции NO (доноры NO) -антиоксиданты ►увеличение пролиферации мышечных клеток и регенерации: -блокада миостатина -доставка митогенов к мышце PEDIATRIC RESEARCH Vol. 56, No. 6, 2004
Стратегии коррекции миодистрофии Дюшена ► Анаболические стероиды, ростовые факторы (IGF-1) ► Снижение протеолиза: -ингибиторы Ca 2+-зависимых протеаз(калпаины)-β 2 - агонисты, -ингибирование убиквитин- зависимого протеолиза ► Снижение воспалительного ответа: -иммуносупрессоры (глюкокортикоиды) -модуляция цитокинов (TNF-α) -нормализация продукции NO (доноры NO) -антиоксиданты ►увеличение пролиферации мышечных клеток и регенерации: -блокада миостатина -доставка митогенов к мышце PEDIATRIC RESEARCH Vol. 56, No. 6, 2004
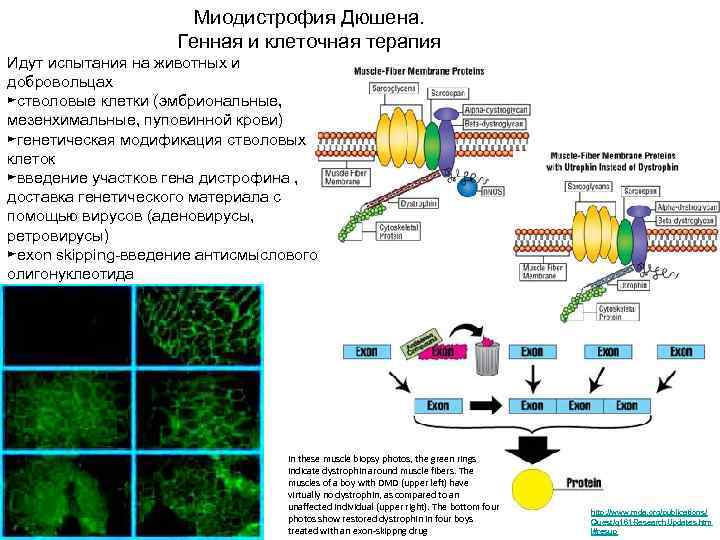
 Миодистрофия Дюшена. Генная и клеточная терапия Идут испытания на животных и добровольцах ►стволовые клетки (эмбриональные, мезенхимальные, пуповинной крови) ►генетическая модификация стволовых клеток ►введение участков гена дистрофина , доставка генетического материала с помощью вирусов (аденовирусы, ретровирусы) ►exon skipping-введение антисмыслового олигонуклеотида In these muscle biopsy photos, the green rings indicate dystrophin around muscle fibers. The muscles of a boy with DMD (upper left) have virtually no dystrophin, as compared to an unaffected individual (upper right). The bottom four http: //www. mda. org/publications/ photos show restored dystrophin in four boys Quest/q 161 Research. Updates. htm treated with an exon-skippng drug l#resup
Миодистрофия Дюшена. Генная и клеточная терапия Идут испытания на животных и добровольцах ►стволовые клетки (эмбриональные, мезенхимальные, пуповинной крови) ►генетическая модификация стволовых клеток ►введение участков гена дистрофина , доставка генетического материала с помощью вирусов (аденовирусы, ретровирусы) ►exon skipping-введение антисмыслового олигонуклеотида In these muscle biopsy photos, the green rings indicate dystrophin around muscle fibers. The muscles of a boy with DMD (upper left) have virtually no dystrophin, as compared to an unaffected individual (upper right). The bottom four http: //www. mda. org/publications/ photos show restored dystrophin in four boys Quest/q 161 Research. Updates. htm treated with an exon-skippng drug l#resup
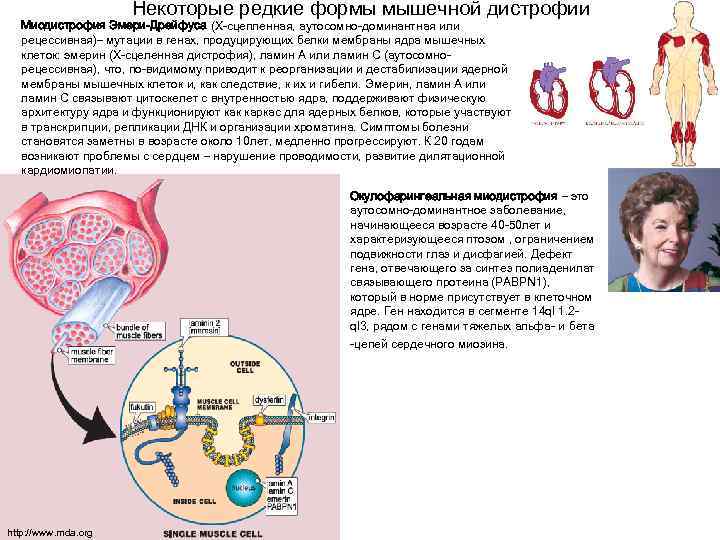
 Некоторые редкие формы мышечной дистрофии Миодистрофия Эмери-Дрейфуса (Х-сцепленная, аутосомно-доминантная или рецессивная)– мутации в генах, продуцирующих белки мембраны ядра мышечных клеток: эмерин (Х-сцеленная дистрофия), ламин А или ламин С (аутосомно- рецессивная), что, по-видимому приводит к реорганизации и дестабилизации ядерной мембраны мышечных клеток и, как следствие, к их и гибели. Эмерин, ламин А или ламин С связывают цитоскелет с внутренностью ядра, поддерживают физическую архитектуру ядра и функционируют как каркас для ядерных белков, которые участвуют в транскрипции, репликации ДНК и организации хроматина. Симптомы болезни становятся заметны в возрасте около 10 лет, медленно прогрессируют. К 20 годам возникают проблемы с сердцем – нарушение проводимости, развитие дилятационной кардиомиопатии. Окулофарингеальная миодистрофия – это аутосомно-доминантное заболевание, начинающееся возрасте 40 -50 лет и характеризующееся птозом , ограничением подвижности глаз и дисфагией. Дефект гена, отвечающего за синтез полиаденилат связывающего протеина (PABPN 1), который в норме присутствует в клеточном ядре. Ген находится в сегменте 14 ql 1. 2 - ql 3, рядом с генами тяжелых альфа- и бета -цепей сердечного миозина. http: //www. mda. org
Некоторые редкие формы мышечной дистрофии Миодистрофия Эмери-Дрейфуса (Х-сцепленная, аутосомно-доминантная или рецессивная)– мутации в генах, продуцирующих белки мембраны ядра мышечных клеток: эмерин (Х-сцеленная дистрофия), ламин А или ламин С (аутосомно- рецессивная), что, по-видимому приводит к реорганизации и дестабилизации ядерной мембраны мышечных клеток и, как следствие, к их и гибели. Эмерин, ламин А или ламин С связывают цитоскелет с внутренностью ядра, поддерживают физическую архитектуру ядра и функционируют как каркас для ядерных белков, которые участвуют в транскрипции, репликации ДНК и организации хроматина. Симптомы болезни становятся заметны в возрасте около 10 лет, медленно прогрессируют. К 20 годам возникают проблемы с сердцем – нарушение проводимости, развитие дилятационной кардиомиопатии. Окулофарингеальная миодистрофия – это аутосомно-доминантное заболевание, начинающееся возрасте 40 -50 лет и характеризующееся птозом , ограничением подвижности глаз и дисфагией. Дефект гена, отвечающего за синтез полиаденилат связывающего протеина (PABPN 1), который в норме присутствует в клеточном ядре. Ген находится в сегменте 14 ql 1. 2 - ql 3, рядом с генами тяжелых альфа- и бета -цепей сердечного миозина. http: //www. mda. org
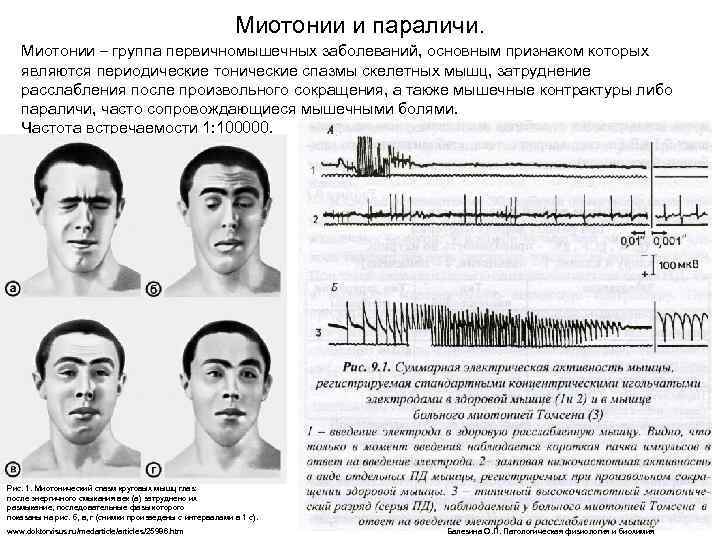
 Миотонии и параличи. Миотонии – группа первичномышечных заболеваний, основным признаком которых являются периодические тонические спазмы скелетных мышц, затруднение расслабления после произвольного сокращения, а также мышечные контрактуры либо параличи, часто сопровождающиеся мышечными болями. Частота встречаемости 1: 100000. Рис. 1. Миотонический спазм круговых мышц глаз: после энергичного смыкания век (а) затруднено их размыкание, последовательные фазы которого показаны на рис. б, в, г (снимки произведены с интервалами в 1 с). www. doktorvisus. ru/medarticle/articles/25986. htm Балезина О. П. Патологическая физиология и биохимия
Миотонии и параличи. Миотонии – группа первичномышечных заболеваний, основным признаком которых являются периодические тонические спазмы скелетных мышц, затруднение расслабления после произвольного сокращения, а также мышечные контрактуры либо параличи, часто сопровождающиеся мышечными болями. Частота встречаемости 1: 100000. Рис. 1. Миотонический спазм круговых мышц глаз: после энергичного смыкания век (а) затруднено их размыкание, последовательные фазы которого показаны на рис. б, в, г (снимки произведены с интервалами в 1 с). www. doktorvisus. ru/medarticle/articles/25986. htm Балезина О. П. Патологическая физиология и биохимия
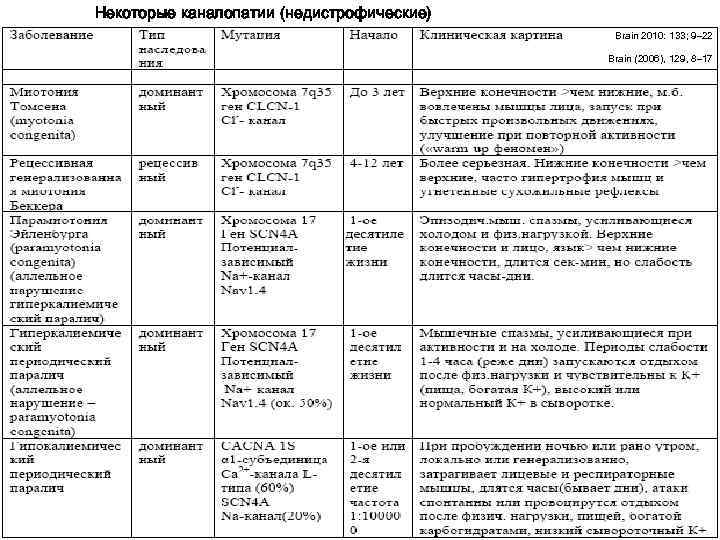
 Некоторые каналопатии (недистрофические) Миотонии и параличи. Brain 2010: 133; 9– 22 Brain (2006), 129, 8– 17 Каналопатии.
Некоторые каналопатии (недистрофические) Миотонии и параличи. Brain 2010: 133; 9– 22 Brain (2006), 129, 8– 17 Каналопатии.
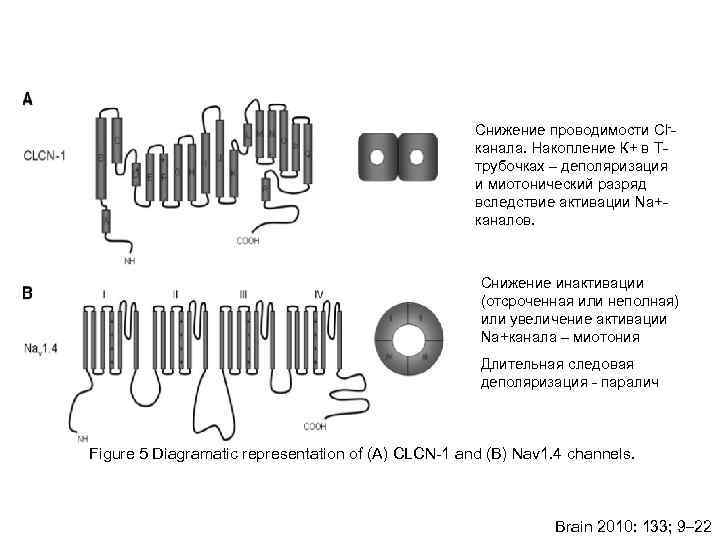
 Снижение проводимости Сl-- канала. Накопление К+ в Т- трубочках – деполяризация и миотонический разряд вследствие активации Na+- каналов. Снижение инактивации (отсроченная или неполная) или увеличение активации Na+канала – миотония Длительная следовая деполяризация - паралич Figure 5 Diagramatic representation of (A) CLCN-1 and (B) Nav 1. 4 channels. Brain 2010: 133; 9– 22
Снижение проводимости Сl-- канала. Накопление К+ в Т- трубочках – деполяризация и миотонический разряд вследствие активации Na+- каналов. Снижение инактивации (отсроченная или неполная) или увеличение активации Na+канала – миотония Длительная следовая деполяризация - паралич Figure 5 Diagramatic representation of (A) CLCN-1 and (B) Nav 1. 4 channels. Brain 2010: 133; 9– 22
 Миопатии, обусловленные воспалительными процессами в мышцах. Аутоиммунные заболевания, характеризующееся диффузным воспалением мышц и проявляющееся нарастающей слабостью и болезненностью мыщц шеи, гортани, глотки, плечевого и тазового поясов, проксимальных отделов конечностей, дыхательных мышц. Возможно присоединение миокардита и пневмонита http: //www. mda. org Дерматомиозиты - аутоимунная агрессия против мелких кровеносных сосудов, снабжающих мышцы и кожу Полимиозиты –аутоиммунная агрессия непосредственно против мышечных клеток Риск канцерогенеза В качестве этиологически значимых рассматривают вирусы гриппа, парагриппа, гепатита В, пикорнавирусы, парвовирус, а также простейшие (токсоплазма). Среди бактериальных возбудителей подчеркивают роль борелиоза и β-гемолитического стрептококка группы А. К другим предполагаемым этиологическим факторам относят некоторые вакцины (против тифа, холеры, кори, краснухи, паротита) и лекарственные вещества (D- пеницилламин, гормон роста).
Миопатии, обусловленные воспалительными процессами в мышцах. Аутоиммунные заболевания, характеризующееся диффузным воспалением мышц и проявляющееся нарастающей слабостью и болезненностью мыщц шеи, гортани, глотки, плечевого и тазового поясов, проксимальных отделов конечностей, дыхательных мышц. Возможно присоединение миокардита и пневмонита http: //www. mda. org Дерматомиозиты - аутоимунная агрессия против мелких кровеносных сосудов, снабжающих мышцы и кожу Полимиозиты –аутоиммунная агрессия непосредственно против мышечных клеток Риск канцерогенеза В качестве этиологически значимых рассматривают вирусы гриппа, парагриппа, гепатита В, пикорнавирусы, парвовирус, а также простейшие (токсоплазма). Среди бактериальных возбудителей подчеркивают роль борелиоза и β-гемолитического стрептококка группы А. К другим предполагаемым этиологическим факторам относят некоторые вакцины (против тифа, холеры, кори, краснухи, паротита) и лекарственные вещества (D- пеницилламин, гормон роста).
 Миопатии 1) При эндокринных нарушениях: Гипертиреоз Гипотиреоз 2) При диабете 3)Метаболические болезни мышц Группы мышечных болезней, как правило, связанные с наследственным дефицитом ферментов, участвующих в получении энергии из углеводов, жиров или транспортеров. Например, дефицит фосфорилазы, фосфофруктокиназы и т. д. 4)Алкогольная миопатия
Миопатии 1) При эндокринных нарушениях: Гипертиреоз Гипотиреоз 2) При диабете 3)Метаболические болезни мышц Группы мышечных болезней, как правило, связанные с наследственным дефицитом ферментов, участвующих в получении энергии из углеводов, жиров или транспортеров. Например, дефицит фосфорилазы, фосфофруктокиназы и т. д. 4)Алкогольная миопатия
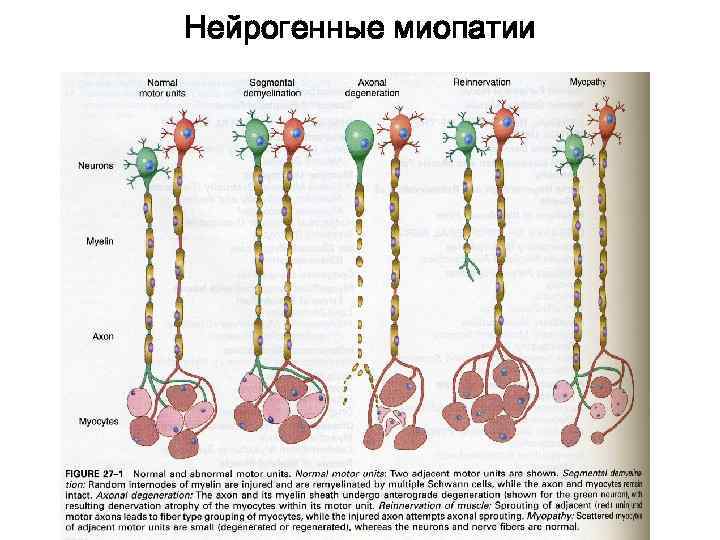
 Нейрогенные миопатии
Нейрогенные миопатии
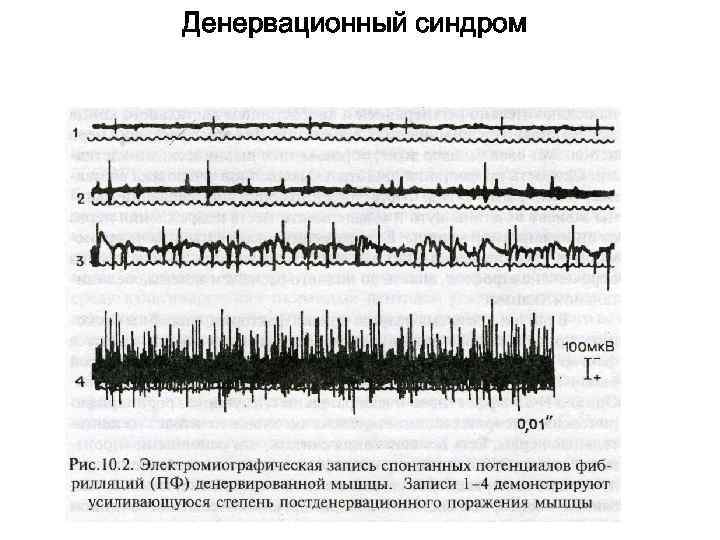
 Денервационный синдром
Денервационный синдром
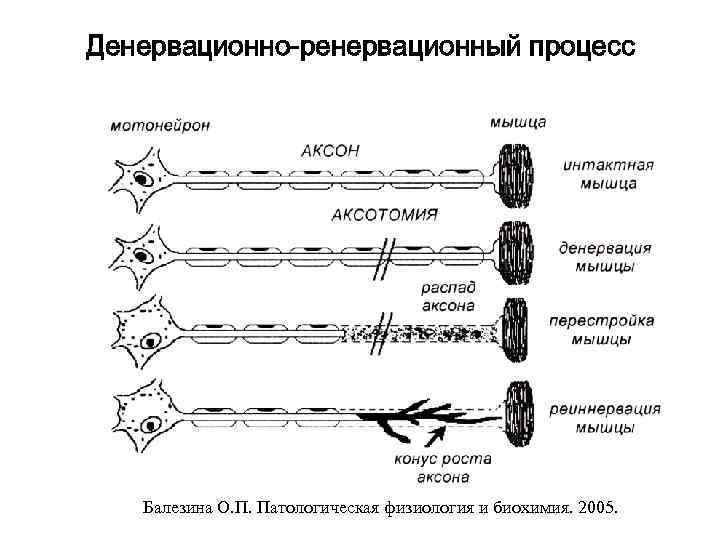
 Денервационно-ренервационный процесс Балезина О. П. Патологическая физиология и биохимия. 2005.
Денервационно-ренервационный процесс Балезина О. П. Патологическая физиология и биохимия. 2005.
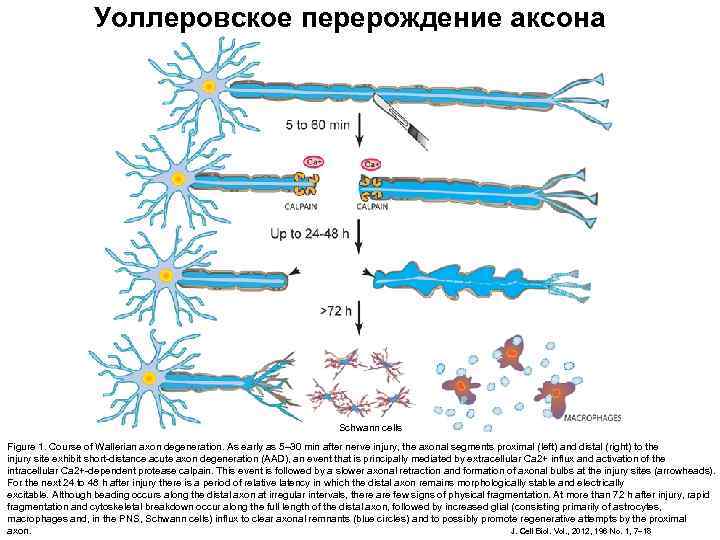
 Уоллеровское перерождение аксона Schwann cells Figure 1. Course of Wallerian axon degeneration. As early as 5– 30 min after nerve injury, the axonal segments proximal (left) and distal (right) to the injury site exhibit short-distance acute axon degeneration (AAD), an event that is principally mediated by extracellular Ca 2+ influx and activation of the intracellular Ca 2+-dependent protease calpain. This event is followed by a slower axonal retraction and formation of axonal bulbs at the injury sites (arrowheads). For the next 24 to 48 h after injury there is a period of relative latency in which the distal axon remains morphologically stable and electrically excitable. Although beading occurs along the distal axon at irregular intervals, there are few signs of physical fragmentation. At more than 72 h after injury, rapid fragmentation and cytoskeletal breakdown occur along the full length of the distal axon, followed by increased glial (consisting primarily of astrocytes, macrophages and, in the PNS, Schwann cells) influx to clear axonal remnants (blue circles) and to possibly promote regenerative attempts by the proximal axon. J. Cell Biol. Vol. , 2012, 196 No. 1, 7– 18
Уоллеровское перерождение аксона Schwann cells Figure 1. Course of Wallerian axon degeneration. As early as 5– 30 min after nerve injury, the axonal segments proximal (left) and distal (right) to the injury site exhibit short-distance acute axon degeneration (AAD), an event that is principally mediated by extracellular Ca 2+ influx and activation of the intracellular Ca 2+-dependent protease calpain. This event is followed by a slower axonal retraction and formation of axonal bulbs at the injury sites (arrowheads). For the next 24 to 48 h after injury there is a period of relative latency in which the distal axon remains morphologically stable and electrically excitable. Although beading occurs along the distal axon at irregular intervals, there are few signs of physical fragmentation. At more than 72 h after injury, rapid fragmentation and cytoskeletal breakdown occur along the full length of the distal axon, followed by increased glial (consisting primarily of astrocytes, macrophages and, in the PNS, Schwann cells) influx to clear axonal remnants (blue circles) and to possibly promote regenerative attempts by the proximal axon. J. Cell Biol. Vol. , 2012, 196 No. 1, 7– 18
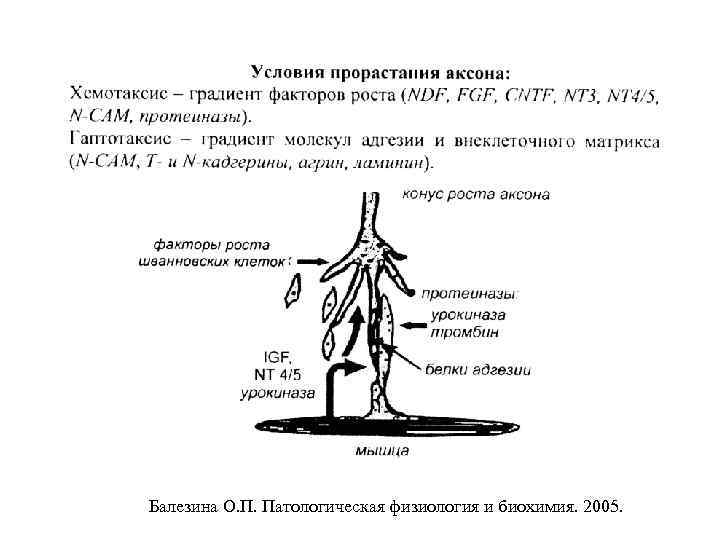
 Балезина О. П. Патологическая физиология и биохимия. 2005.
Балезина О. П. Патологическая физиология и биохимия. 2005.
 • За последние 10 -15 лет список ростовых факторов, стимулирующих прорастание аксонов мотонейронов, возрос и насчитывает более 10 наименований. К их числу принадлежат: • Мозговой нейротрофический фактор (BDNF) – белок, выделенный из мозгового экстракта; • Нейротрофины – 3 и -4, также выделенные из ткани мозга; • Цилиарный нейротрофический фактор (CNTF) из ткани ресничного ганглия; • Инсулиноподобные факторы роста; • Фактор роста фибробластов (FGF) – белок, высвобождающийся из фибробластов; • Пептиды семейства меланокортинов, в том числе –фрагменты АКТГ. Балезина О. П. Патологическая физиология и биохимия. 2005.
• За последние 10 -15 лет список ростовых факторов, стимулирующих прорастание аксонов мотонейронов, возрос и насчитывает более 10 наименований. К их числу принадлежат: • Мозговой нейротрофический фактор (BDNF) – белок, выделенный из мозгового экстракта; • Нейротрофины – 3 и -4, также выделенные из ткани мозга; • Цилиарный нейротрофический фактор (CNTF) из ткани ресничного ганглия; • Инсулиноподобные факторы роста; • Фактор роста фибробластов (FGF) – белок, высвобождающийся из фибробластов; • Пептиды семейства меланокортинов, в том числе –фрагменты АКТГ. Балезина О. П. Патологическая физиология и биохимия. 2005.
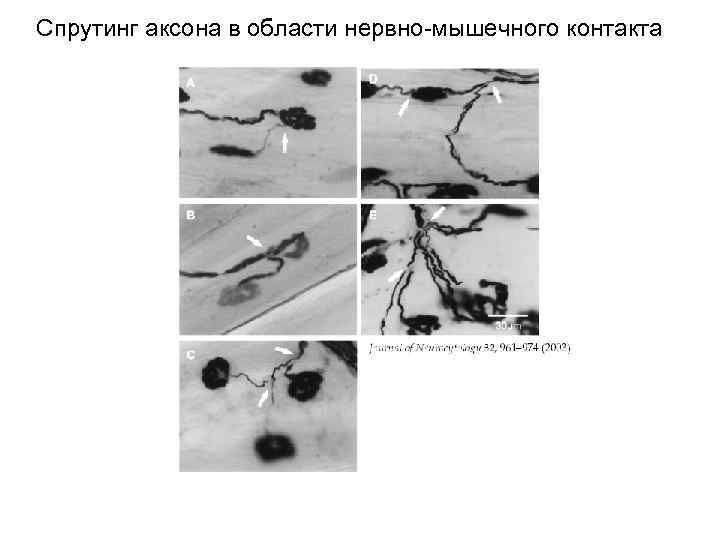
 Спрутинг аксона в области нервно-мышечного контакта
Спрутинг аксона в области нервно-мышечного контакта
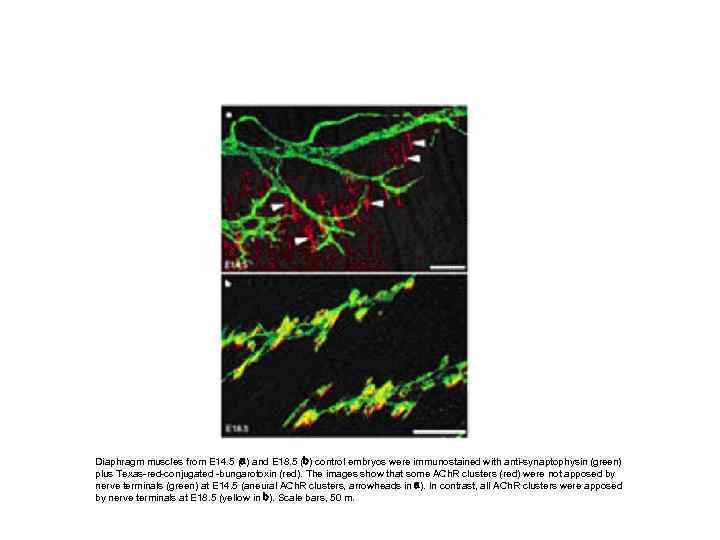
 Diaphragm muscles from E 14. 5 (a) and E 18. 5 (b) control embryos were immunostained with anti-synaptophysin (green) plus Texas-red-conjugated -bungarotoxin (red). The images show that some ACh. R clusters (red) were not apposed by nerve terminals (green) at E 14. 5 (aneural ACh. R clusters, arrowheads in a). In contrast, all ACh. R clusters were apposed by nerve terminals at E 18. 5 (yellow in b). Scale bars, 50 m.
Diaphragm muscles from E 14. 5 (a) and E 18. 5 (b) control embryos were immunostained with anti-synaptophysin (green) plus Texas-red-conjugated -bungarotoxin (red). The images show that some ACh. R clusters (red) were not apposed by nerve terminals (green) at E 14. 5 (aneural ACh. R clusters, arrowheads in a). In contrast, all ACh. R clusters were apposed by nerve terminals at E 18. 5 (yellow in b). Scale bars, 50 m.
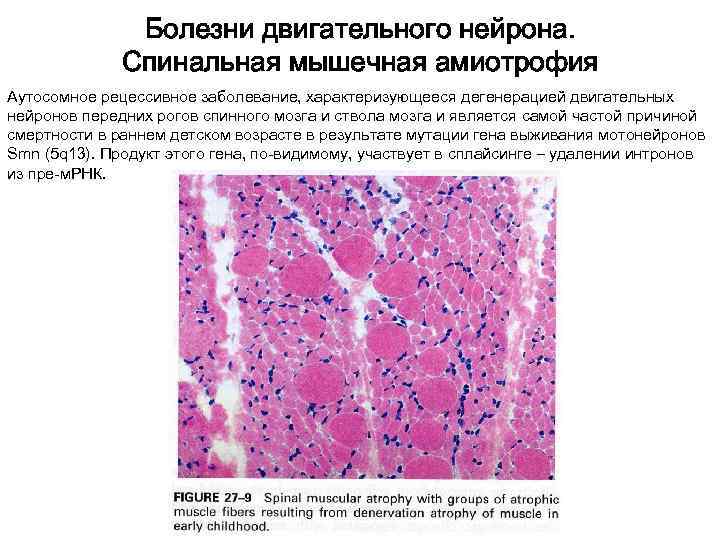
 Болезни двигательного нейрона. Спинальная мышечная амиотрофия Аутосомное рецессивное заболевание, характеризующееся дегенерацией двигательных нейронов передних рогов спинного мозга и ствола мозга и является самой частой причиной смертности в раннем детском возрасте в результате мутации гена выживания мотонейронов Smn (5 q 13). Продукт этого гена, по-видимому, участвует в сплайсинге – удалении интронов из пре-м. РНК.
Болезни двигательного нейрона. Спинальная мышечная амиотрофия Аутосомное рецессивное заболевание, характеризующееся дегенерацией двигательных нейронов передних рогов спинного мозга и ствола мозга и является самой частой причиной смертности в раннем детском возрасте в результате мутации гена выживания мотонейронов Smn (5 q 13). Продукт этого гена, по-видимому, участвует в сплайсинге – удалении интронов из пре-м. РНК.
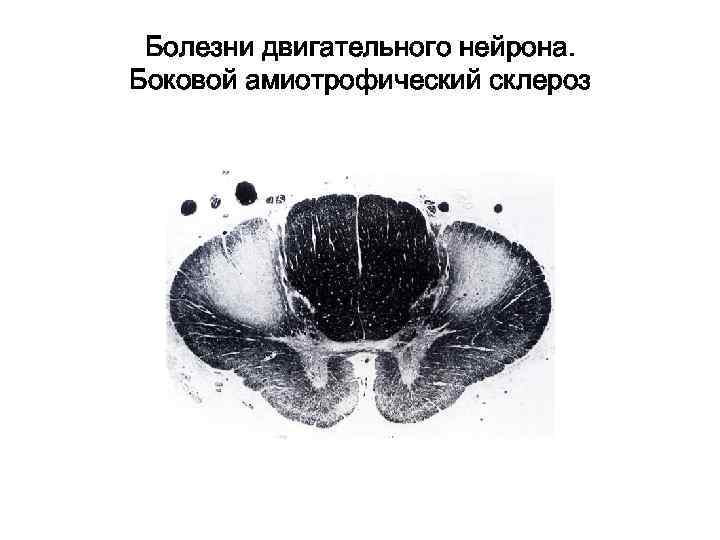
 Болезни двигательного нейрона. Боковой амиотрофический склероз
Болезни двигательного нейрона. Боковой амиотрофический склероз
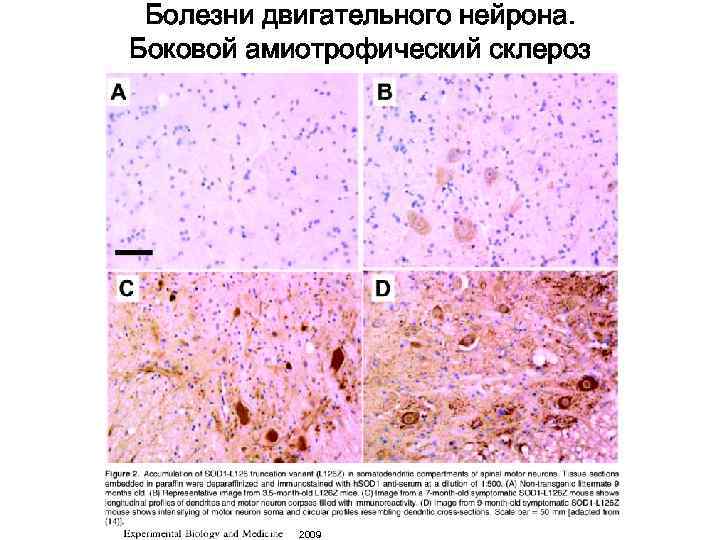
 • Боковой амиотрофический склероз (БАС) характеризуется прогрессирующей гибелью мотонейронов спинного мозга и ствола мозга. В 90% случая БАС является спорадической, а в 10% – семейной или наследственной. Частота встречаемости 2 -5: 100 000. • К клиническим проявлениям БДН относят признаки поражения периферических мотонейронов, такие как парезы и атрофии скелетных мышц с фасцикуляциями в них, а также признаки поражения центральных мотонейронов, такие как спастичность, гиперрефлексия и др. Дизартрия(нарушение речи), дисфагия(нарушение глотания) характерны при преимущественном поражении черепных нервов - это проявления прогрессирующего бульбарного паралича. • При наследственной патологии(до 20% случаев семейной формы БАС) установлен дефект гена, кодирующего медь и цинк содержащую супероксиддисмутазу (антиоксидантный фермент ), локализованного в 21 хромосоме (ген SOD 1 – 21 q 22. 1 -q 22. 2). Модель на животных – трансгенные мыши G 93 A (глицин замещен на аланин в позиции 93, выведена в США). Доказано, что БДН развивается не в силу снижения антиоксидантных свойств фермента и развития оксидантного стресса, а в результате новых цитотоксических свойств мутантного белка • Патогенез спорадической формы заболевания неясен. Вирусная инфекция и аутоиммунные реакции по механизму молекулярной мимикрии, дефицит трофических факторов – вероятные причины заболевания. Инфекционная и аутоиммунная теории происхождения БАС не получили подтверждения. Иммуносупрессанты и плазмоферез не привели к положительным результатам • Проблема лечения БДН состоит в том, что 80% мотонейронов погибает до клинических проявлений болезни. Возможно, подавляющее большинство испытанных препаратов различных групп оказались неэффективными потому, что 20% оставшихся "больных" мотонейронов уже не способны осуществить компенсацию функции погибших. Единственным препаратом, который достоверно продлевает жизнь больным в среднем на 3 мес, является рилузол – пресинаптический ингибитор высвобождения глутамата, исходно предложенный как противосудорожный препарат. по В. И. Скворцова, Г. Н. Левицкий Consilium Medicum Том 06/N 8/2004
• Боковой амиотрофический склероз (БАС) характеризуется прогрессирующей гибелью мотонейронов спинного мозга и ствола мозга. В 90% случая БАС является спорадической, а в 10% – семейной или наследственной. Частота встречаемости 2 -5: 100 000. • К клиническим проявлениям БДН относят признаки поражения периферических мотонейронов, такие как парезы и атрофии скелетных мышц с фасцикуляциями в них, а также признаки поражения центральных мотонейронов, такие как спастичность, гиперрефлексия и др. Дизартрия(нарушение речи), дисфагия(нарушение глотания) характерны при преимущественном поражении черепных нервов - это проявления прогрессирующего бульбарного паралича. • При наследственной патологии(до 20% случаев семейной формы БАС) установлен дефект гена, кодирующего медь и цинк содержащую супероксиддисмутазу (антиоксидантный фермент ), локализованного в 21 хромосоме (ген SOD 1 – 21 q 22. 1 -q 22. 2). Модель на животных – трансгенные мыши G 93 A (глицин замещен на аланин в позиции 93, выведена в США). Доказано, что БДН развивается не в силу снижения антиоксидантных свойств фермента и развития оксидантного стресса, а в результате новых цитотоксических свойств мутантного белка • Патогенез спорадической формы заболевания неясен. Вирусная инфекция и аутоиммунные реакции по механизму молекулярной мимикрии, дефицит трофических факторов – вероятные причины заболевания. Инфекционная и аутоиммунная теории происхождения БАС не получили подтверждения. Иммуносупрессанты и плазмоферез не привели к положительным результатам • Проблема лечения БДН состоит в том, что 80% мотонейронов погибает до клинических проявлений болезни. Возможно, подавляющее большинство испытанных препаратов различных групп оказались неэффективными потому, что 20% оставшихся "больных" мотонейронов уже не способны осуществить компенсацию функции погибших. Единственным препаратом, который достоверно продлевает жизнь больным в среднем на 3 мес, является рилузол – пресинаптический ингибитор высвобождения глутамата, исходно предложенный как противосудорожный препарат. по В. И. Скворцова, Г. Н. Левицкий Consilium Medicum Том 06/N 8/2004
 Болезни двигательного нейрона. Боковой амиотрофический склероз 2009
Болезни двигательного нейрона. Боковой амиотрофический склероз 2009
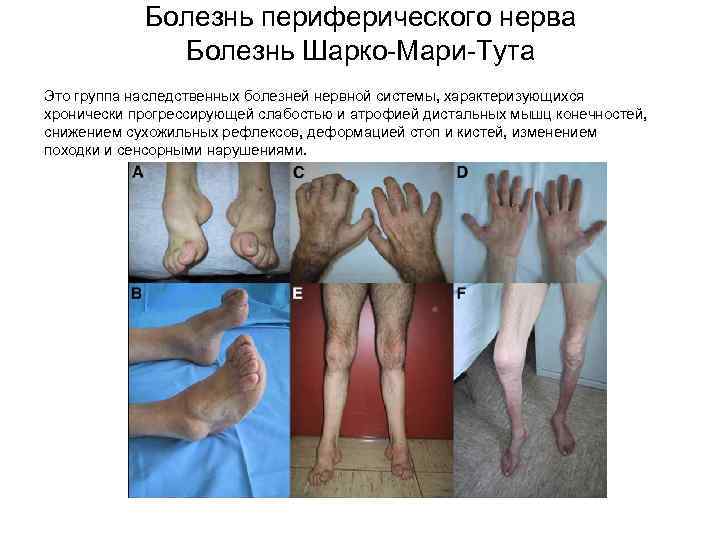
 Болезнь периферического нерва Болезнь Шарко-Мари-Тута Это группа наследственных болезней нервной системы, характеризующихся хронически прогрессирующей слабостью и атрофией дистальных мышц конечностей, снижением сухожильных рефлексов, деформацией стоп и кистей, изменением походки и сенсорными нарушениями.
Болезнь периферического нерва Болезнь Шарко-Мари-Тута Это группа наследственных болезней нервной системы, характеризующихся хронически прогрессирующей слабостью и атрофией дистальных мышц конечностей, снижением сухожильных рефлексов, деформацией стоп и кистей, изменением походки и сенсорными нарушениями.
 Болезнь периферического нерва Болезнь Шарко-Мари-Тута Ø Дегенерация двигательных и чувствительных волокон периферических нервов Ø Начало – первое или второе десятилетие жизни Ø Тип наследования – преимущественно аутосомно- доминантное, реже аутосомно-рецессивное Ø Частота – от 1: 10 000 до 1: 2500 Ø Типы: Биопсия n. suralis. Световая микроскопия. Признаки преимущественно аксональной Ø Миелинопатии [чаще] (скорость проведения импульса <38 м/с) невропатии: значительное уменьшение Ø Аксонопатии (скорость проведения импульса >38 м/с) площади аксона и его дегенеративные изменения в крупных миелинизированных Ø Генетика: 80% случаев – это мутации в генах и их белковых нервных волокнах, признаки вторичной продуктах: демиелинизации, отсутствие гипертрофических изменений в миелинизированных волокнах. PMP 22 (белок периферического миелина), (Атмосфера. Нервные болезни. 2005/2) MPZ (основной белок миелина P 0), GJB 1 (белок межклеточных контактов коннексин-32) и EGR 2 (ранний фактор транскрипции).
Болезнь периферического нерва Болезнь Шарко-Мари-Тута Ø Дегенерация двигательных и чувствительных волокон периферических нервов Ø Начало – первое или второе десятилетие жизни Ø Тип наследования – преимущественно аутосомно- доминантное, реже аутосомно-рецессивное Ø Частота – от 1: 10 000 до 1: 2500 Ø Типы: Биопсия n. suralis. Световая микроскопия. Признаки преимущественно аксональной Ø Миелинопатии [чаще] (скорость проведения импульса <38 м/с) невропатии: значительное уменьшение Ø Аксонопатии (скорость проведения импульса >38 м/с) площади аксона и его дегенеративные изменения в крупных миелинизированных Ø Генетика: 80% случаев – это мутации в генах и их белковых нервных волокнах, признаки вторичной продуктах: демиелинизации, отсутствие гипертрофических изменений в миелинизированных волокнах. PMP 22 (белок периферического миелина), (Атмосфера. Нервные болезни. 2005/2) MPZ (основной белок миелина P 0), GJB 1 (белок межклеточных контактов коннексин-32) и EGR 2 (ранний фактор транскрипции).
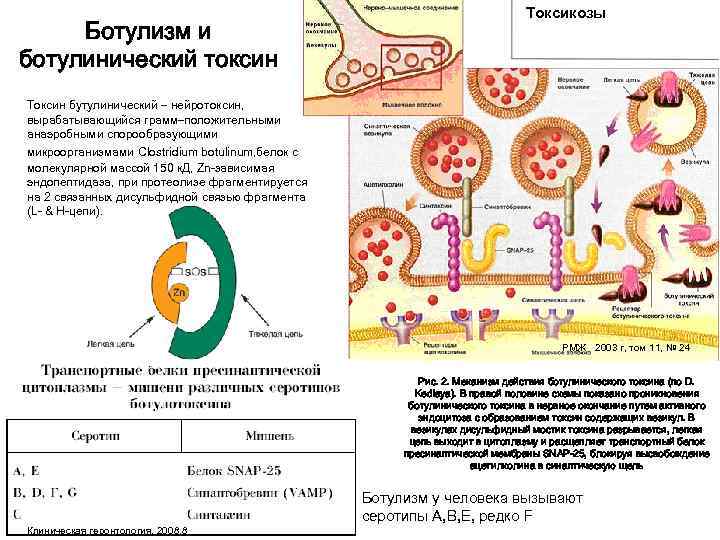
 Токсикозы Ботулизм и ботулинический токсин Токсин бутулинический – нейротоксин, вырабатывающийся грамм–положительными анаэробными спорообразующими микроорганизмами Clostridium botulinum, белок с молекулярной массой 150 к. Д, Zn-зависимая эндопептидаза, при протеолизе фрагментируется на 2 связанных дисульфидной связью фрагмента (L- & H-цепи). РМЖ 2003 г, том 11, № 24 Рис. 2. Механизм действия ботулинического токсина (по D. Kedlaya). В правой половине схемы показано проникновения ботулинического токсина в нервное окончание путем активного эндоцитоза с образованием токсин содержащих везикул. В везикулах дисульфидный мостик токсина разрывается, легкая цепь выходит в цитоплазму и расщепляет транспортный белок пресинаптической мембраны SNAP-25, блокируя высвобождение ацетилхолина в синаптическую щель Ботулизм у человека вызывают серотипы А, B, E, редко F Клиническая геронтология, 2008, 8
Токсикозы Ботулизм и ботулинический токсин Токсин бутулинический – нейротоксин, вырабатывающийся грамм–положительными анаэробными спорообразующими микроорганизмами Clostridium botulinum, белок с молекулярной массой 150 к. Д, Zn-зависимая эндопептидаза, при протеолизе фрагментируется на 2 связанных дисульфидной связью фрагмента (L- & H-цепи). РМЖ 2003 г, том 11, № 24 Рис. 2. Механизм действия ботулинического токсина (по D. Kedlaya). В правой половине схемы показано проникновения ботулинического токсина в нервное окончание путем активного эндоцитоза с образованием токсин содержащих везикул. В везикулах дисульфидный мостик токсина разрывается, легкая цепь выходит в цитоплазму и расщепляет транспортный белок пресинаптической мембраны SNAP-25, блокируя высвобождение ацетилхолина в синаптическую щель Ботулизм у человека вызывают серотипы А, B, E, редко F Клиническая геронтология, 2008, 8
 Применение ботулотоксина (серотип А, реже B) В урологии у неврологических больных с нарушением акта мочеиспукания вследствие не расслабляющегося поперечно–полосатого сфинктера уретры и у больных с снижением или отсутствием сокращения детрузора. В неврологии при локальных формах мышечной дистонии, спастичности различного происхождения. Например, для коррекции мышечного тонуса с целью снижения тонуса мышц, участвующих в построении патологического двигательного стереотипа у больных со спастическими формами ДЦП. Однако при длительном лечении и повторных введениях токсина развивается вторичная резистентность к его действию вследствие появления антител к токсину. В косметологии
Применение ботулотоксина (серотип А, реже B) В урологии у неврологических больных с нарушением акта мочеиспукания вследствие не расслабляющегося поперечно–полосатого сфинктера уретры и у больных с снижением или отсутствием сокращения детрузора. В неврологии при локальных формах мышечной дистонии, спастичности различного происхождения. Например, для коррекции мышечного тонуса с целью снижения тонуса мышц, участвующих в построении патологического двигательного стереотипа у больных со спастическими формами ДЦП. Однако при длительном лечении и повторных введениях токсина развивается вторичная резистентность к его действию вследствие появления антител к токсину. В косметологии
 Другие токсикозы: Столбняк (возбудитель – бактерия Clostridium tetani) Воспаление мотонейронов Полимиелит – вирусная инфекция Действие токсинов на нервно-мышечный синапс: Альфа-латротоксин (яд паука «черная вдова» ) Кураре (алкалоид растительного происхождения) Альфа-бунгаротоксин (яд кобры)
Другие токсикозы: Столбняк (возбудитель – бактерия Clostridium tetani) Воспаление мотонейронов Полимиелит – вирусная инфекция Действие токсинов на нервно-мышечный синапс: Альфа-латротоксин (яд паука «черная вдова» ) Кураре (алкалоид растительного происхождения) Альфа-бунгаротоксин (яд кобры)
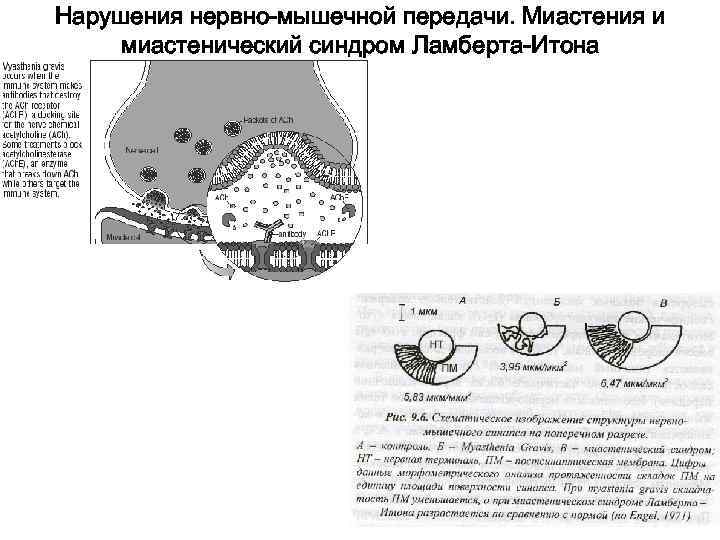
 Нарушения нервно-мышечной передачи. Миастения и миастенический синдром Ламберта-Итона
Нарушения нервно-мышечной передачи. Миастения и миастенический синдром Ламберта-Итона

