Патофизиология нервной системы Методы исследования













Патофизиология НС.ppt
- Количество слайдов: 49
 Патофизиология нервной системы
Патофизиология нервной системы
 Методы исследования нарушений функций нервной системы n Перерезка мозга и нервов n Удаление определенных структур мозга n Стереотаксическое разрушение определенных структур мозга n Стимуляция определенных структур мозга n Применение нейротропных препаратов n Электрофизиологические методы исследования функций мозга через электроды или с поверхности черепа n Исследование функций нейронов в культуре и на слайзах n Исследование экспрессии генов в нейронах и клетках глии n Иммуногистохимическое исследование определенных белков и нейромедиаторов в нейронах (в том числе маркеров активации клетки) n Использование ряда этих методов (6 -9) для поиска возможности медикаментозной и волновой коррекции дисфункций нервной системы
Методы исследования нарушений функций нервной системы n Перерезка мозга и нервов n Удаление определенных структур мозга n Стереотаксическое разрушение определенных структур мозга n Стимуляция определенных структур мозга n Применение нейротропных препаратов n Электрофизиологические методы исследования функций мозга через электроды или с поверхности черепа n Исследование функций нейронов в культуре и на слайзах n Исследование экспрессии генов в нейронах и клетках глии n Иммуногистохимическое исследование определенных белков и нейромедиаторов в нейронах (в том числе маркеров активации клетки) n Использование ряда этих методов (6 -9) для поиска возможности медикаментозной и волновой коррекции дисфункций нервной системы
 Патофизиология нервной системы. Повреждение Нарушение основных нервных Основные проявления (нарушение) процессов нарушений функций нервной функций системы нервных 1. Нарушение восприятия сигналов 1. Потеря или снижение структур определенного вида 2. Нарушение процессов передачи чувствительности. Рецепторного сигналов от периферии к центру аппарата 2. Частичная или полная 3. Нарушение процесса синаптической деафферентация. передачи сигналов к нейрону. Афферентных 3. Дефицит торможения нервных 4. Нарушение генерации нервного (Растормаживание). проводников импульса в нейроне. 4. Замена тормозных эффектов- Синаптического 5. Нарушение передачи импульса от возбуждающими. аппарата нервной клетки по аксонам и дендритам 5. Денервационый синдром нейрона (эфферентной передачи). 6. Спинальный шок Эфферентных 7. Нарушение различных форм 6. Нарушение передачи эфферентного проводниковых регуляции сигнала с нервных окончаний на клетку- путей мишень. 8. Выпадение функций Нервно- 7. Нарушение процессов интеграции в определенных структур мозга. мышечных и мозге. 9. Нарушение интегративной других синапсов 8. Нарушение процессов памяти деятельности нервной (фиксации, хранения, извлечения системы. информации).
Патофизиология нервной системы. Повреждение Нарушение основных нервных Основные проявления (нарушение) процессов нарушений функций нервной функций системы нервных 1. Нарушение восприятия сигналов 1. Потеря или снижение структур определенного вида 2. Нарушение процессов передачи чувствительности. Рецепторного сигналов от периферии к центру аппарата 2. Частичная или полная 3. Нарушение процесса синаптической деафферентация. передачи сигналов к нейрону. Афферентных 3. Дефицит торможения нервных 4. Нарушение генерации нервного (Растормаживание). проводников импульса в нейроне. 4. Замена тормозных эффектов- Синаптического 5. Нарушение передачи импульса от возбуждающими. аппарата нервной клетки по аксонам и дендритам 5. Денервационый синдром нейрона (эфферентной передачи). 6. Спинальный шок Эфферентных 7. Нарушение различных форм 6. Нарушение передачи эфферентного проводниковых регуляции сигнала с нервных окончаний на клетку- путей мишень. 8. Выпадение функций Нервно- 7. Нарушение процессов интеграции в определенных структур мозга. мышечных и мозге. 9. Нарушение интегративной других синапсов 8. Нарушение процессов памяти деятельности нервной (фиксации, хранения, извлечения системы. информации).
 Эндогенные причины повреждения нервной системы Патогенные факторы Нарушение жизнедеятельности Чрезмерная и структуры тканей, органов Нарушение теплового активация и систем, приводящие к гомеостаза организма СПОЛ расстройству: Дисбаланс биологически активных веществ и их Циркуляция Состава и реологии эффектов( нейромедиаторов, крови крови и ликвора гормонов, цитокинов) и ликвора в головном мозге Баланса ионов Обмена веществ и жидкости внутри в нейронах и вне нейронов
Эндогенные причины повреждения нервной системы Патогенные факторы Нарушение жизнедеятельности Чрезмерная и структуры тканей, органов Нарушение теплового активация и систем, приводящие к гомеостаза организма СПОЛ расстройству: Дисбаланс биологически активных веществ и их Циркуляция Состава и реологии эффектов( нейромедиаторов, крови крови и ликвора гормонов, цитокинов) и ликвора в головном мозге Баланса ионов Обмена веществ и жидкости внутри в нейронах и вне нейронов
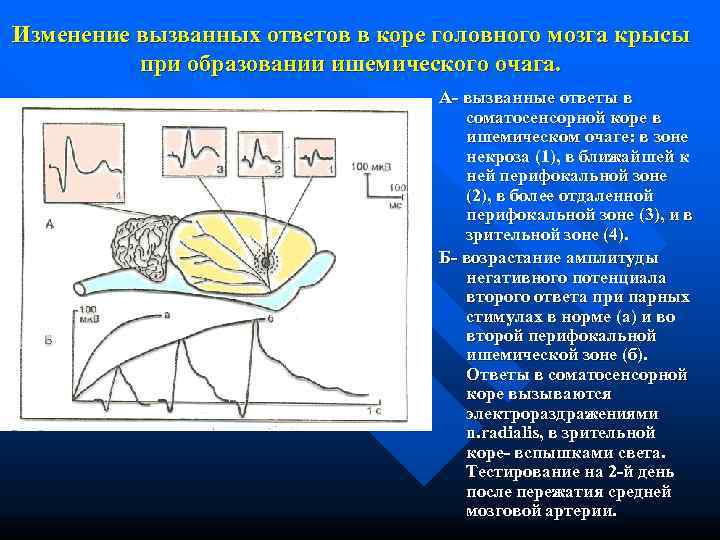
 Изменение вызванных ответов в коре головного мозга крысы при образовании ишемического очага. А- вызванные ответы в соматосенсорной коре в ишемическом очаге: в зоне некроза (1), в ближайшей к ней перифокальной зоне (2), в более отдаленной перифокальной зоне (3), и в зрительной зоне (4). Б- возрастание амплитуды негативного потенциала второго ответа при парных стимулах в норме (а) и во второй перифокальной ишемической зоне (б). Ответы в соматосенсорной коре вызываются электрораздражениями n. radialis, в зрительной коре- вспышками света. Тестирование на 2 -й день после пережатия средней мозговой артерии.
Изменение вызванных ответов в коре головного мозга крысы при образовании ишемического очага. А- вызванные ответы в соматосенсорной коре в ишемическом очаге: в зоне некроза (1), в ближайшей к ней перифокальной зоне (2), в более отдаленной перифокальной зоне (3), и в зрительной зоне (4). Б- возрастание амплитуды негативного потенциала второго ответа при парных стимулах в норме (а) и во второй перифокальной ишемической зоне (б). Ответы в соматосенсорной коре вызываются электрораздражениями n. radialis, в зрительной коре- вспышками света. Тестирование на 2 -й день после пережатия средней мозговой артерии.
 Основные механизмы повреждения нейронов (неспецифические) Неспецифические Повреждение мембран Апоптоз нейронов Дисбаланс ионов и жидкости Нарушение энергетического обеспечения Аутолиз компонентов нейронов Расстройства биосинтеза белка
Основные механизмы повреждения нейронов (неспецифические) Неспецифические Повреждение мембран Апоптоз нейронов Дисбаланс ионов и жидкости Нарушение энергетического обеспечения Аутолиз компонентов нейронов Расстройства биосинтеза белка
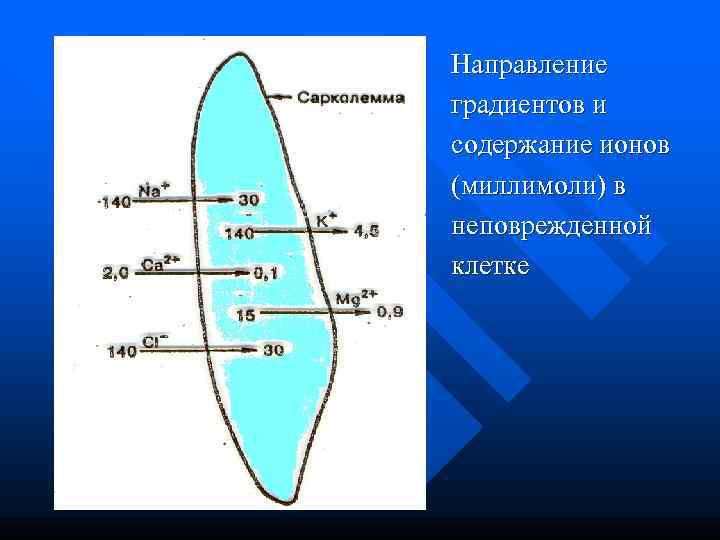
 Направление градиентов и содержание ионов (миллимоли) в неповрежденной клетке
Направление градиентов и содержание ионов (миллимоли) в неповрежденной клетке
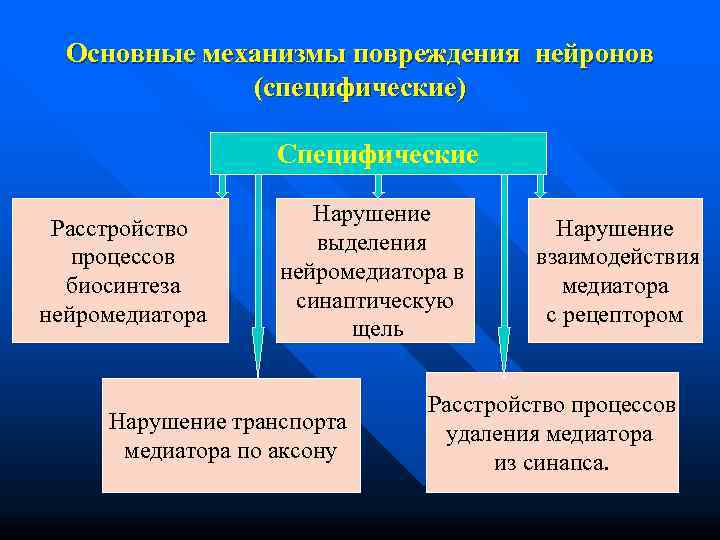
 Основные механизмы повреждения нейронов (специфические) Специфические Нарушение Расстройство Нарушение выделения процессов взаимодействия нейромедиатора в биосинтеза медиатора синаптическую нейромедиатора с рецептором щель Расстройство процессов Нарушение транспорта удаления медиатора по аксону из синапса.
Основные механизмы повреждения нейронов (специфические) Специфические Нарушение Расстройство Нарушение выделения процессов взаимодействия нейромедиатора в биосинтеза медиатора синаптическую нейромедиатора с рецептором щель Расстройство процессов Нарушение транспорта удаления медиатора по аксону из синапса.
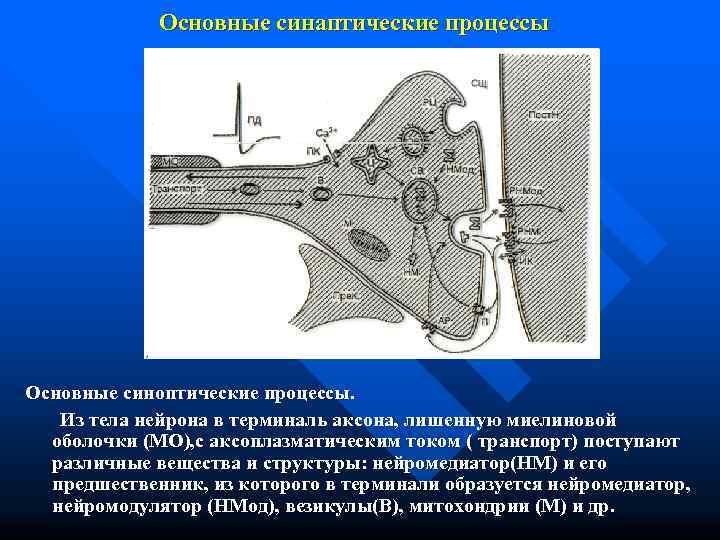
 Основные синаптические процессы Основные синоптические процессы. Из тела нейрона в терминаль аксона, лишенную миелиновой оболочки (МО), с аксоплазматическим током ( транспорт) поступают различные вещества и структуры: нейромедиатор(НМ) и его предшественник, из которого в терминали образуется нейромедиатор, нейромодулятор (НМод), везикулы(В), митохондрии (М) и др.
Основные синаптические процессы Основные синоптические процессы. Из тела нейрона в терминаль аксона, лишенную миелиновой оболочки (МО), с аксоплазматическим током ( транспорт) поступают различные вещества и структуры: нейромедиатор(НМ) и его предшественник, из которого в терминали образуется нейромедиатор, нейромодулятор (НМод), везикулы(В), митохондрии (М) и др.
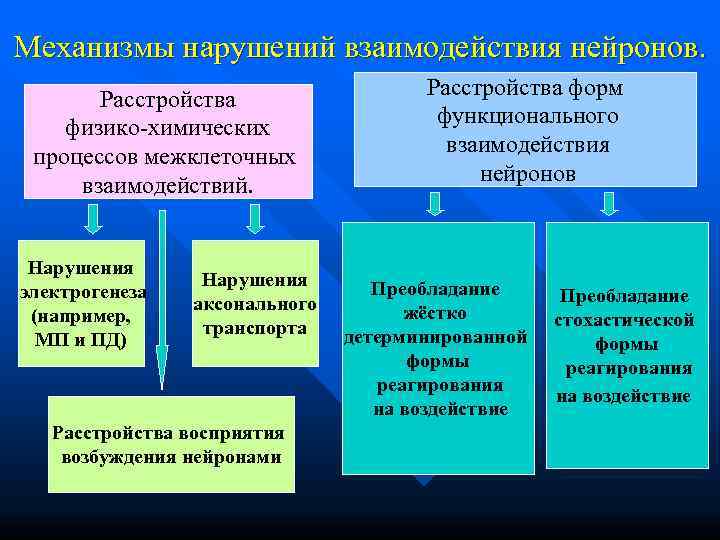
 Механизмы нарушений взаимодействия нейронов. Расстройства форм Расстройства функционального физико-химических взаимодействия процессов межклеточных нейронов взаимодействий. Нарушения Преобладание электрогенеза Преобладание аксонального жёстко (например, стохастической транспорта детерминированной МП и ПД) формы реагирования на воздействие Расстройства восприятия возбуждения нейронами
Механизмы нарушений взаимодействия нейронов. Расстройства форм Расстройства функционального физико-химических взаимодействия процессов межклеточных нейронов взаимодействий. Нарушения Преобладание электрогенеза Преобладание аксонального жёстко (например, стохастической транспорта детерминированной МП и ПД) формы реагирования на воздействие Расстройства восприятия возбуждения нейронами
 Воспроизведение экстензорных моносинаптических рефлексов при комбинированном моно-и полисинаптической стимуляции мышечного нерва в условиях локального одностороннего отравления столбнячным токсином люмбосакральных сегментов спинного мозга. Комбинированные моно- и полисинаптические ответы вызываются у кошки электрическими (специально подобранной силы) раздражениями нерва икроножной мышцы на стороне введения токсина (слева) и на противоположной стороне (справа). Частота раздражения (с) указывается цифрами. Калибровка 1 м. В, 20 мс.
Воспроизведение экстензорных моносинаптических рефлексов при комбинированном моно-и полисинаптической стимуляции мышечного нерва в условиях локального одностороннего отравления столбнячным токсином люмбосакральных сегментов спинного мозга. Комбинированные моно- и полисинаптические ответы вызываются у кошки электрическими (специально подобранной силы) раздражениями нерва икроножной мышцы на стороне введения токсина (слева) и на противоположной стороне (справа). Частота раздражения (с) указывается цифрами. Калибровка 1 м. В, 20 мс.
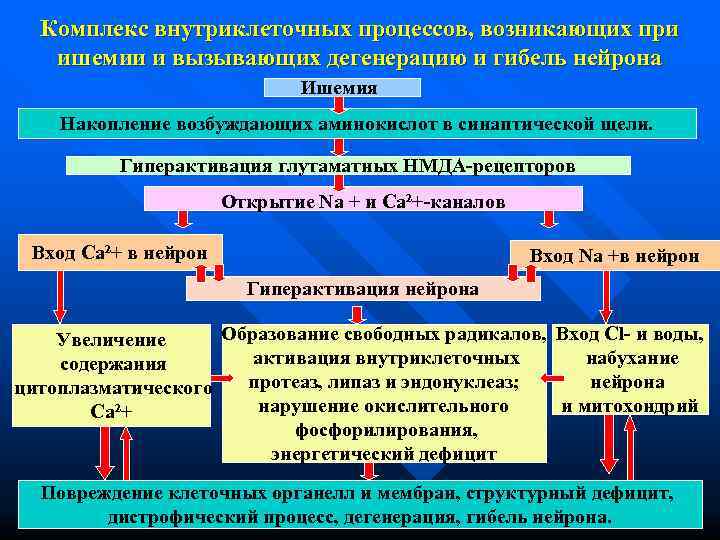
 Комплекс внутриклеточных процессов, возникающих при ишемии и вызывающих дегенерацию и гибель нейрона Ишемия Накопление возбуждающих аминокислот в синаптической щели. Гиперактивация глутаматных НМДА-рецепторов Открытие Na + и Ca²+-каналов Вход Ca²+ в нейрон Вход Na +в нейрон Гиперактивация нейрона Увеличение Образование свободных радикалов, Вход Cl- и воды, содержания активация внутриклеточных набухание цитоплазматического протеаз, липаз и эндонуклеаз; нейрона Ca²+ нарушение окислительного и митохондрий фосфорилирования, энергетический дефицит Повреждение клеточных органелл и мембран, структурный дефицит, дистрофический процесс, дегенерация, гибель нейрона.
Комплекс внутриклеточных процессов, возникающих при ишемии и вызывающих дегенерацию и гибель нейрона Ишемия Накопление возбуждающих аминокислот в синаптической щели. Гиперактивация глутаматных НМДА-рецепторов Открытие Na + и Ca²+-каналов Вход Ca²+ в нейрон Вход Na +в нейрон Гиперактивация нейрона Увеличение Образование свободных радикалов, Вход Cl- и воды, содержания активация внутриклеточных набухание цитоплазматического протеаз, липаз и эндонуклеаз; нейрона Ca²+ нарушение окислительного и митохондрий фосфорилирования, энергетический дефицит Повреждение клеточных органелл и мембран, структурный дефицит, дистрофический процесс, дегенерация, гибель нейрона.
 n Глюкоза является основным энергетическим субстратом нервных клеток. Аэробное расщепление субстратов обеспечивает образование примерно 80% энергии, потребляемой мозгом. n В норме головной мозг утилизирует около 20% глюкозы плазмы крови и всего потребляемого организмом кислорода. n Мозг чрезвычайно чувствителен к снижению поступления кислорода.
n Глюкоза является основным энергетическим субстратом нервных клеток. Аэробное расщепление субстратов обеспечивает образование примерно 80% энергии, потребляемой мозгом. n В норме головной мозг утилизирует около 20% глюкозы плазмы крови и всего потребляемого организмом кислорода. n Мозг чрезвычайно чувствителен к снижению поступления кислорода.
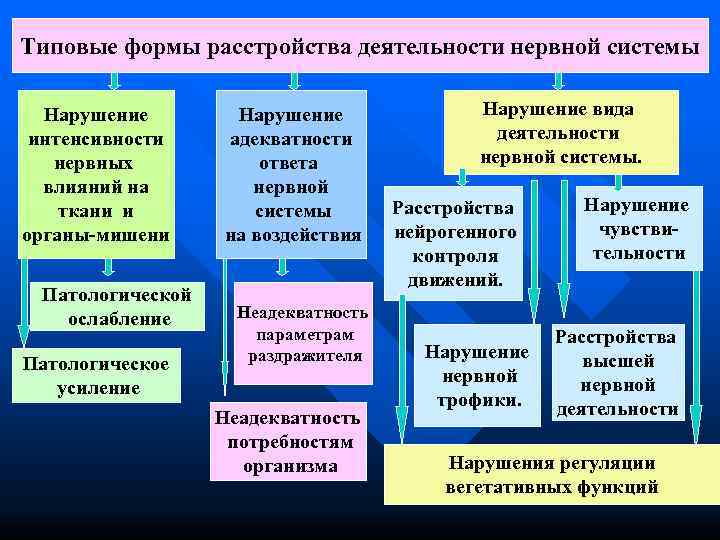
 Типовые формы расстройства деятельности нервной системы Нарушение вида интенсивности адекватности деятельности нервных ответа нервной системы. влияний на нервной ткани и системы Расстройства Нарушение органы-мишени на воздействия нейрогенного чувстви- контроля тельности движений. Патологической ослабление Неадекватность параметрам Расстройства раздражителя Нарушение высшей Патологическое нервной усиление трофики. деятельности Неадекватность потребностям организма Нарушения регуляции вегетативных функций
Типовые формы расстройства деятельности нервной системы Нарушение вида интенсивности адекватности деятельности нервных ответа нервной системы. влияний на нервной ткани и системы Расстройства Нарушение органы-мишени на воздействия нейрогенного чувстви- контроля тельности движений. Патологической ослабление Неадекватность параметрам Расстройства раздражителя Нарушение высшей Патологическое нервной усиление трофики. деятельности Неадекватность потребностям организма Нарушения регуляции вегетативных функций
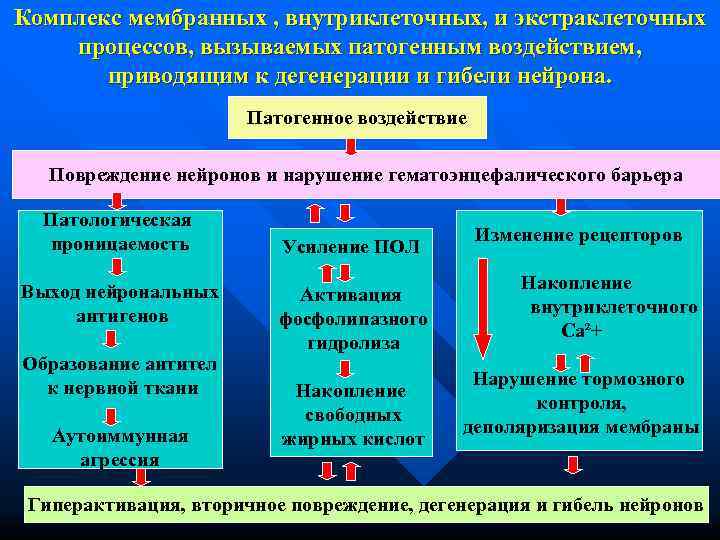
 Комплекс мембранных , внутриклеточных, и экстраклеточных процессов, вызываемых патогенным воздействием, приводящим к дегенерации и гибели нейрона. Патогенное воздействие Повреждение нейронов и нарушение гематоэнцефалического барьера Патологическая проницаемость Изменение рецепторов Усиление ПОЛ Выход нейрональных Накопление Активация антигенов внутриклеточного фосфолипазного Ca²+ гидролиза Образование антител к нервной ткани Нарушение тормозного Накопление контроля, свободных Аутоиммунная деполяризация мембраны жирных кислот агрессия Гиперактивация, вторичное повреждение, дегенерация и гибель нейронов
Комплекс мембранных , внутриклеточных, и экстраклеточных процессов, вызываемых патогенным воздействием, приводящим к дегенерации и гибели нейрона. Патогенное воздействие Повреждение нейронов и нарушение гематоэнцефалического барьера Патологическая проницаемость Изменение рецепторов Усиление ПОЛ Выход нейрональных Накопление Активация антигенов внутриклеточного фосфолипазного Ca²+ гидролиза Образование антител к нервной ткани Нарушение тормозного Накопление контроля, свободных Аутоиммунная деполяризация мембраны жирных кислот агрессия Гиперактивация, вторичное повреждение, дегенерация и гибель нейронов
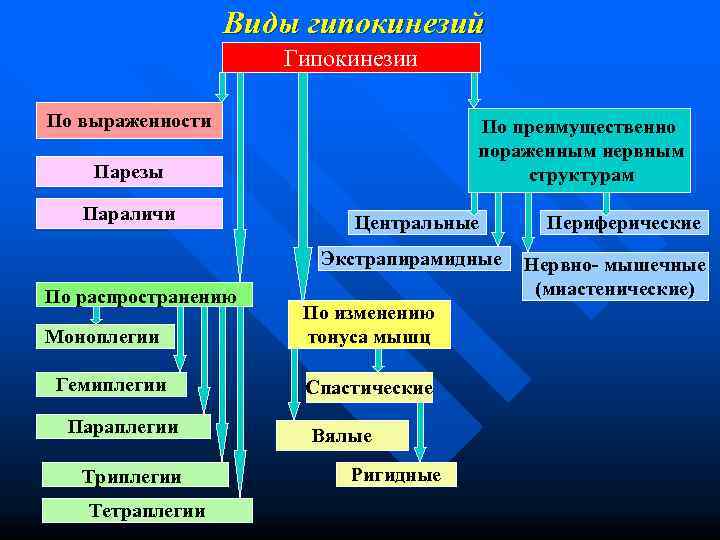
 Виды гипокинезий Гипокинезии По выраженности По преимущественно пораженным нервным Парезы структурам Параличи Центральные Периферические Экстрапирамидные Нервно- мышечные По распространению (миастенические) По изменению Моноплегии тонуса мышц Гемиплегии Спастические Параплегии Вялые Триплегии Ригидные Тетраплегии
Виды гипокинезий Гипокинезии По выраженности По преимущественно пораженным нервным Парезы структурам Параличи Центральные Периферические Экстрапирамидные Нервно- мышечные По распространению (миастенические) По изменению Моноплегии тонуса мышц Гемиплегии Спастические Параплегии Вялые Триплегии Ригидные Тетраплегии
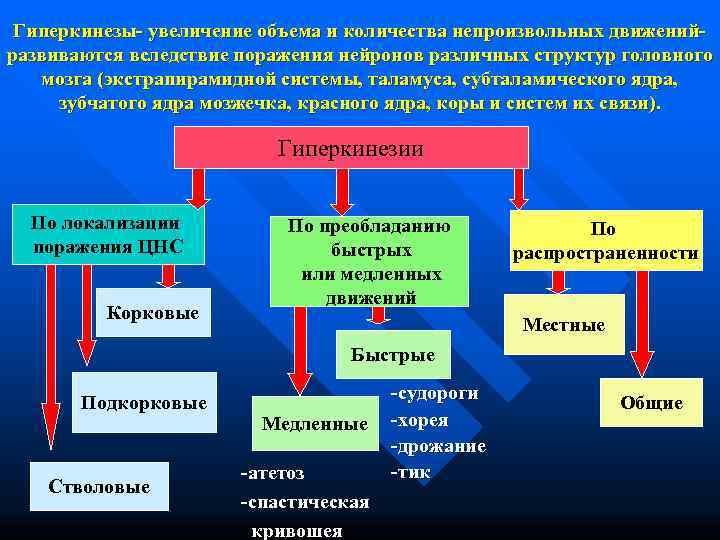
 Гиперкинезы- увеличение объема и количества непроизвольных движений- развиваются вследствие поражения нейронов различных структур головного мозга (экстрапирамидной системы, таламуса, субталамического ядра, зубчатого ядра мозжечка, красного ядра, коры и систем их связи). Гиперкинезии По локализации По преобладанию По поражения ЦНС быстрых распространенности или медленных движений Корковые Местные Быстрые -судороги Подкорковые Общие Медленные -хорея -дрожание -атетоз -тик Стволовые -спастическая кривошея
Гиперкинезы- увеличение объема и количества непроизвольных движений- развиваются вследствие поражения нейронов различных структур головного мозга (экстрапирамидной системы, таламуса, субталамического ядра, зубчатого ядра мозжечка, красного ядра, коры и систем их связи). Гиперкинезии По локализации По преобладанию По поражения ЦНС быстрых распространенности или медленных движений Корковые Местные Быстрые -судороги Подкорковые Общие Медленные -хорея -дрожание -атетоз -тик Стволовые -спастическая кривошея
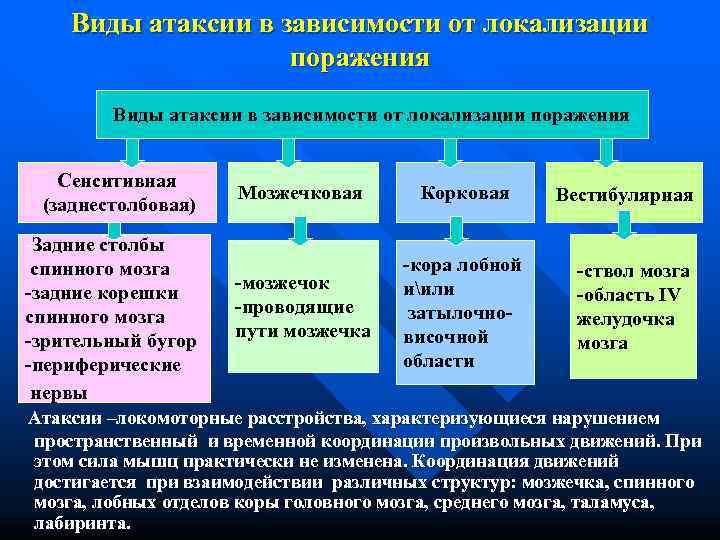
 Виды атаксии в зависимости от локализации поражения Виды атаксии в зависимости от локализации поражения Сенситивная Мозжечковая Корковая Вестибулярная (заднестолбовая) -Задние столбы спинного мозга -кора лобной -ствол мозга -задние корешки -мозжечок иили -область IV спинного мозга -проводящие затылочно- желудочка -зрительный бугор пути мозжечка височной мозга -периферические области нервы Атаксии –локомоторные расстройства, характеризующиеся нарушением пространственный и временной координации произвольных движений. При этом сила мышц практически не изменена. Координация движений достигается при взаимодействии различных структур: мозжечка, спинного мозга, лобных отделов коры головного мозга, среднего мозга, таламуса, лабиринта.
Виды атаксии в зависимости от локализации поражения Виды атаксии в зависимости от локализации поражения Сенситивная Мозжечковая Корковая Вестибулярная (заднестолбовая) -Задние столбы спинного мозга -кора лобной -ствол мозга -задние корешки -мозжечок иили -область IV спинного мозга -проводящие затылочно- желудочка -зрительный бугор пути мозжечка височной мозга -периферические области нервы Атаксии –локомоторные расстройства, характеризующиеся нарушением пространственный и временной координации произвольных движений. При этом сила мышц практически не изменена. Координация движений достигается при взаимодействии различных структур: мозжечка, спинного мозга, лобных отделов коры головного мозга, среднего мозга, таламуса, лабиринта.
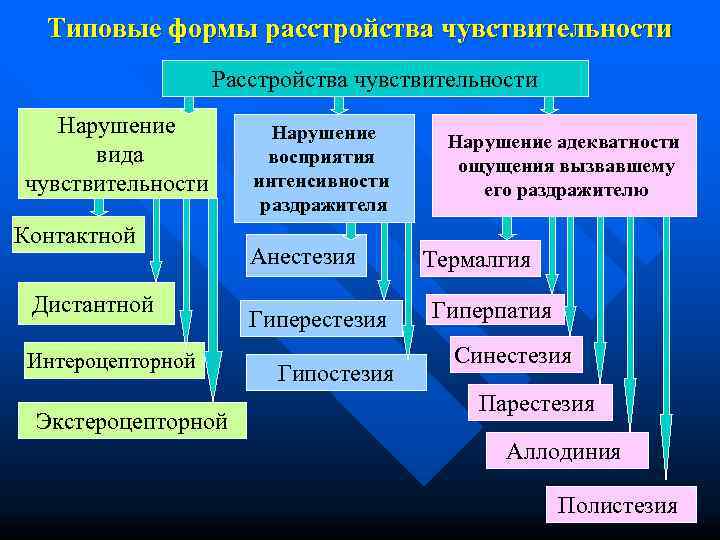
 Типовые формы расстройства чувствительности Расстройства чувствительности Нарушение адекватности вида восприятия ощущения вызвавшему чувствительности интенсивности его раздражителю раздражителя Контактной Анестезия Термалгия Дистантной Гиперпатия Гиперестезия Интероцепторной Синестезия Гипостезия Парестезия Экстероцепторной Аллодиния Полистезия
Типовые формы расстройства чувствительности Расстройства чувствительности Нарушение адекватности вида восприятия ощущения вызвавшему чувствительности интенсивности его раздражителю раздражителя Контактной Анестезия Термалгия Дистантной Гиперпатия Гиперестезия Интероцепторной Синестезия Гипостезия Парестезия Экстероцепторной Аллодиния Полистезия
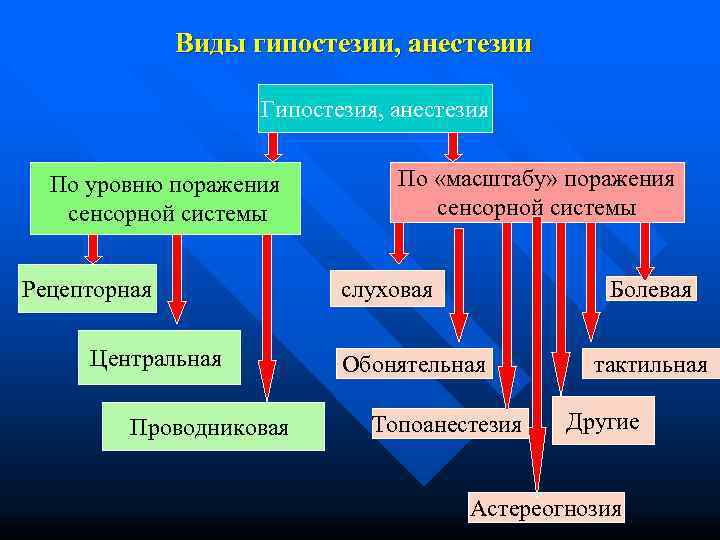
 Виды гипостезии, анестезии Гипостезия, анестезия По уровню поражения По «масштабу» поражения сенсорной системы Рецепторная слуховая Болевая Центральная Обонятельная тактильная Проводниковая Топоанестезия Другие Астереогнозия
Виды гипостезии, анестезии Гипостезия, анестезия По уровню поражения По «масштабу» поражения сенсорной системы Рецепторная слуховая Болевая Центральная Обонятельная тактильная Проводниковая Топоанестезия Другие Астереогнозия
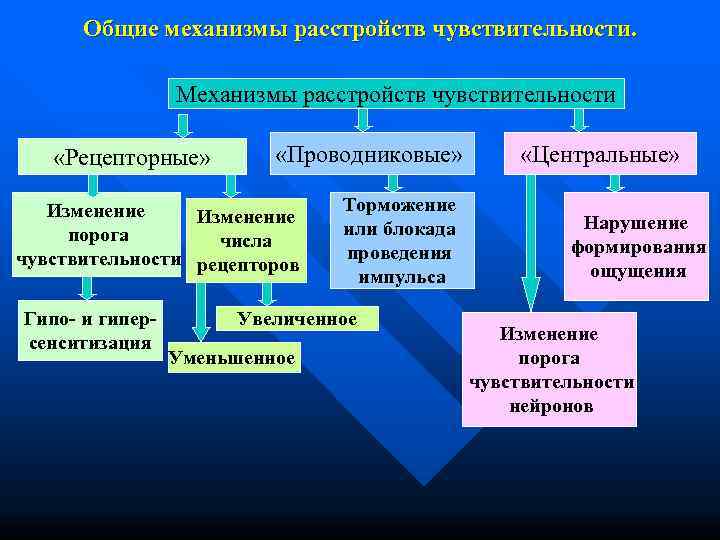
 Общие механизмы расстройств чувствительности. Механизмы расстройств чувствительности «Рецепторные» «Проводниковые» «Центральные» Изменение Торможение Изменение Нарушение порога или блокада числа формирования чувствительности рецепторов проведения импульса ощущения Гипо- и гипер- Увеличенное сенситизация Изменение Уменьшенное порога чувствительности нейронов
Общие механизмы расстройств чувствительности. Механизмы расстройств чувствительности «Рецепторные» «Проводниковые» «Центральные» Изменение Торможение Изменение Нарушение порога или блокада числа формирования чувствительности рецепторов проведения импульса ощущения Гипо- и гипер- Увеличенное сенситизация Изменение Уменьшенное порога чувствительности нейронов
 Лауряты Нобелевской премии 2012 года по химии, профессора – Роберт Лефковитц и Брайан Кобилка (США). Роберт Лефковитц Брайан Кобилка Исследование рецепторов, сопряженных с G-белками (GPCR – G – protein-coupled receptors).
Лауряты Нобелевской премии 2012 года по химии, профессора – Роберт Лефковитц и Брайан Кобилка (США). Роберт Лефковитц Брайан Кобилка Исследование рецепторов, сопряженных с G-белками (GPCR – G – protein-coupled receptors).
 Microglia Surveillance of Synapse : In vivo observation with Two Photon Microscope Seeing is believing !! Junichi Nabekura National Institute for Physiological Sciences Okazaki Japan
Microglia Surveillance of Synapse : In vivo observation with Two Photon Microscope Seeing is believing !! Junichi Nabekura National Institute for Physiological Sciences Okazaki Japan
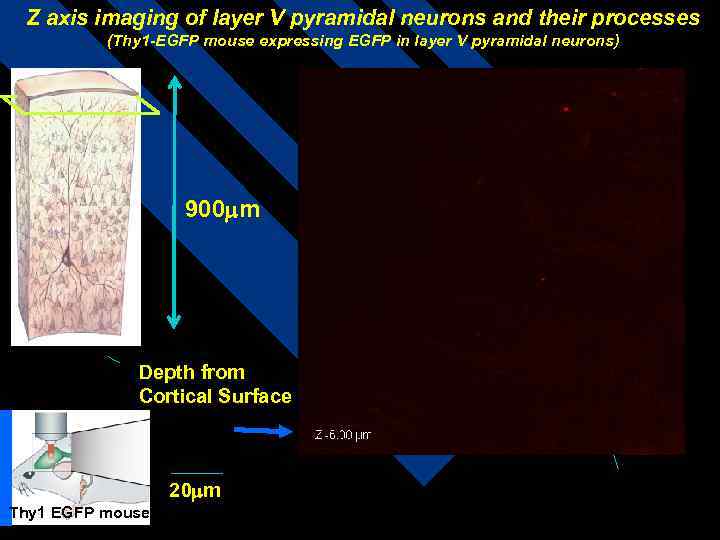
 Z axis imaging of layer V pyramidal neurons and their processes (Thy 1 -EGFP mouse expressing EGFP in layer V pyramidal neurons) 900 mm Depth from Cortical Surface 20 mm Thy 1 EGFP mouse
Z axis imaging of layer V pyramidal neurons and their processes (Thy 1 -EGFP mouse expressing EGFP in layer V pyramidal neurons) 900 mm Depth from Cortical Surface 20 mm Thy 1 EGFP mouse
 3 D View of Cortical Network of Layer 5 Pyramidal Neuron in vivo
3 D View of Cortical Network of Layer 5 Pyramidal Neuron in vivo
 Microglia processes touch other brain structure during 5 min pause?
Microglia processes touch other brain structure during 5 min pause?
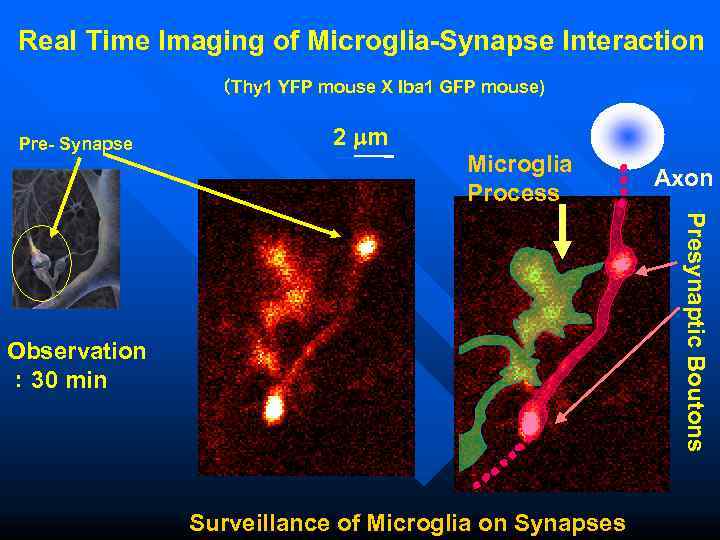
 Real Time Imaging of Microglia-Synapse Interaction (Thy 1 YFP mouse X Iba 1 GFP mouse) 神経細胞 Pre- Synapse 2 mm Microglia Axon Process Presynaptic Boutons Observation : 30 min Surveillance of Microglia on Synapses
Real Time Imaging of Microglia-Synapse Interaction (Thy 1 YFP mouse X Iba 1 GFP mouse) 神経細胞 Pre- Synapse 2 mm Microglia Axon Process Presynaptic Boutons Observation : 30 min Surveillance of Microglia on Synapses
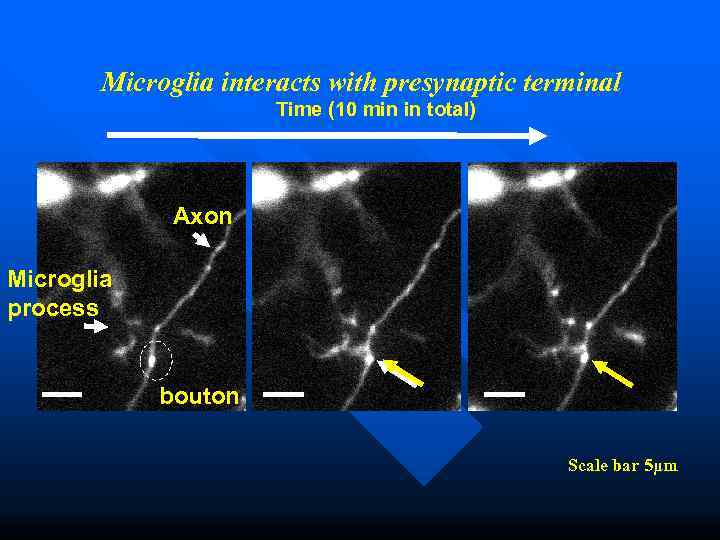
 Microglia interacts with presynaptic terminal Time (10 min in total) Axon Microglia process bouton Scale bar 5μm
Microglia interacts with presynaptic terminal Time (10 min in total) Axon Microglia process bouton Scale bar 5μm
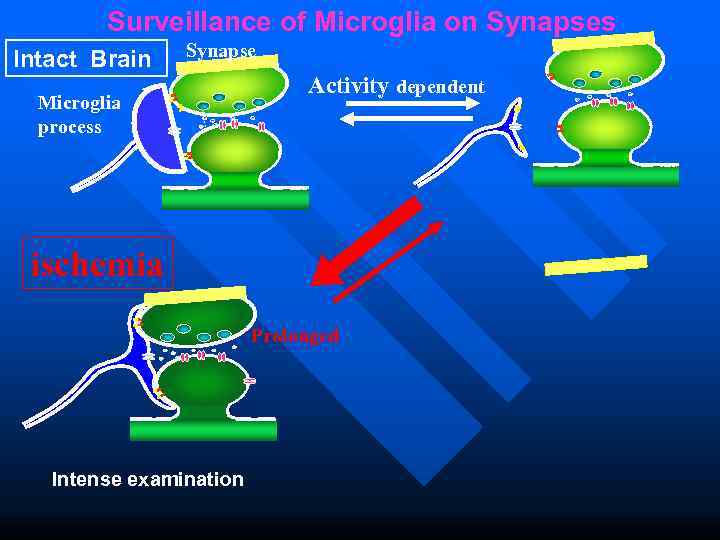
 Surveillance of Microglia on Synapses Synapse Intact Brain Activity dependent Microglia process ischemia Prolonged Intense examination
Surveillance of Microglia on Synapses Synapse Intact Brain Activity dependent Microglia process ischemia Prolonged Intense examination
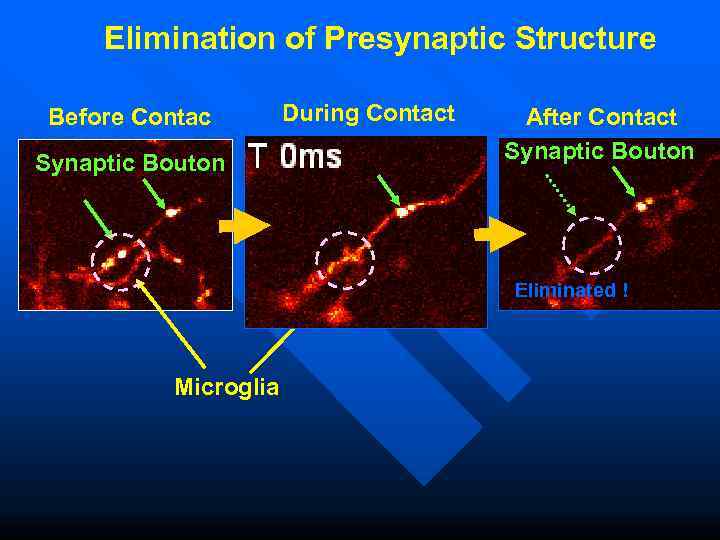
 --- Elimination of Presynaptic Structure Before Contact During Contact After Contact Synaptic Bouton Eliminated ! Microglia
--- Elimination of Presynaptic Structure Before Contact During Contact After Contact Synaptic Bouton Eliminated ! Microglia
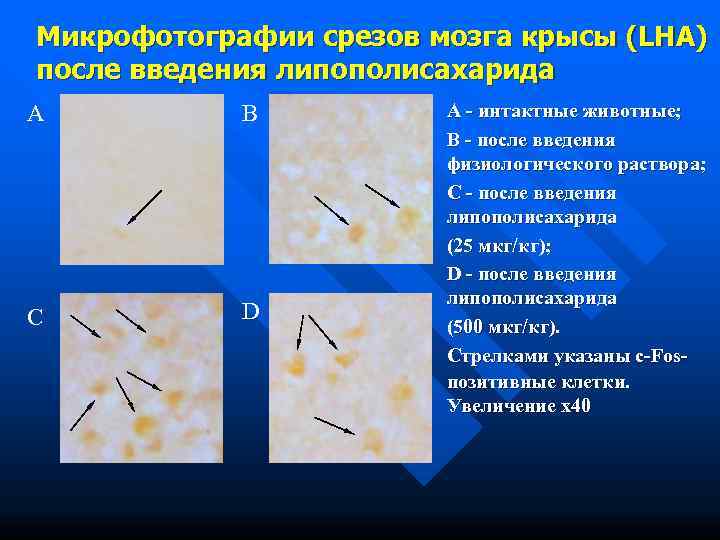
 Микрофотографии срезов мозга крысы (LHA) после введения липополисахарида A B A - интактные животные; B - после введения физиологического раствора; C - после введения липополисахарида (25 мкг/кг); D - после введения липополисахарида C D (500 мкг/кг). Стрелками указаны c-Fos- позитивные клетки. Увеличение х40
Микрофотографии срезов мозга крысы (LHA) после введения липополисахарида A B A - интактные животные; B - после введения физиологического раствора; C - после введения липополисахарида (25 мкг/кг); D - после введения липополисахарида C D (500 мкг/кг). Стрелками указаны c-Fos- позитивные клетки. Увеличение х40
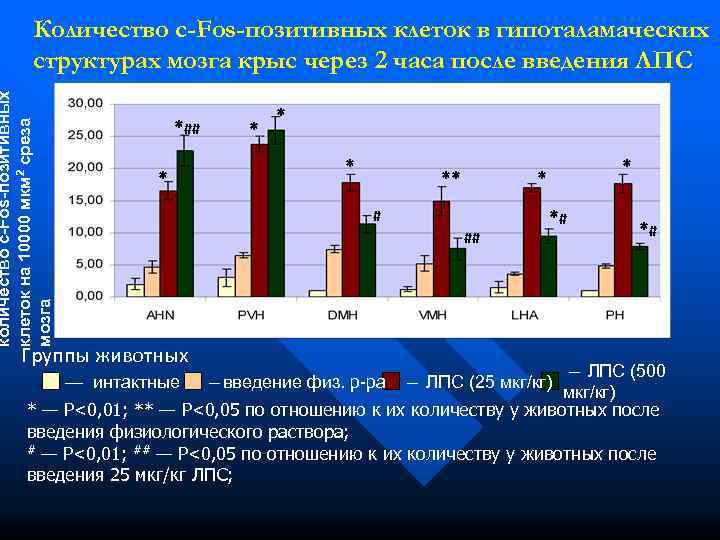
 Количество c-Fos-позитивных клеток в гипоталамаческих структурах мозга крыс через 2 часа после введения ЛПС количество c-Fos-позитивных *## * клеток на 10000 мкм 2 среза * ** # *# ## *# мозга Группы животных ЛПС (500 — — интактные — введение физ. р-ра — ЛПС (25 мкг/кг) мкг/кг) * — P<0, 01; ** — P<0, 05 по отношению к их количеству у животных после введения физиологического раствора; # — P<0, 01; ## — P<0, 05 по отношению к их количеству у животных после введения 25 мкг/кг ЛПС;
Количество c-Fos-позитивных клеток в гипоталамаческих структурах мозга крыс через 2 часа после введения ЛПС количество c-Fos-позитивных *## * клеток на 10000 мкм 2 среза * ** # *# ## *# мозга Группы животных ЛПС (500 — — интактные — введение физ. р-ра — ЛПС (25 мкг/кг) мкг/кг) * — P<0, 01; ** — P<0, 05 по отношению к их количеству у животных после введения физиологического раствора; # — P<0, 01; ## — P<0, 05 по отношению к их количеству у животных после введения 25 мкг/кг ЛПС;
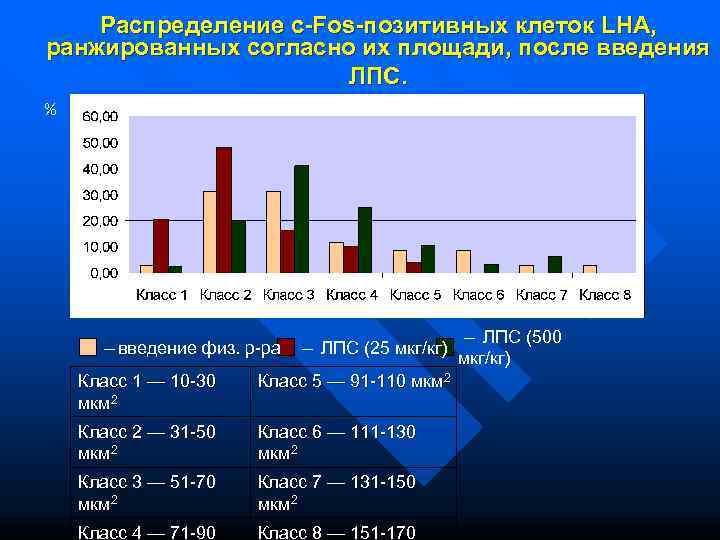
 Распределение c-Fos-позитивных клеток LHA, ранжированных согласно их площади, после введения ЛПС. % — ЛПС (500 — введение физ. р-ра — ЛПС (25 мкг/кг) мкг/кг) Класс 1 — 10 -30 Класс 5 — 91 -110 мкм 2 Класс 2 — 31 -50 Класс 6 — 111 -130 мкм 2 Класс 3 — 51 -70 Класс 7 — 131 -150 мкм 2 Класс 4 — 71 -90 Класс 8 — 151 -170
Распределение c-Fos-позитивных клеток LHA, ранжированных согласно их площади, после введения ЛПС. % — ЛПС (500 — введение физ. р-ра — ЛПС (25 мкг/кг) мкг/кг) Класс 1 — 10 -30 Класс 5 — 91 -110 мкм 2 Класс 2 — 31 -50 Класс 6 — 111 -130 мкм 2 Класс 3 — 51 -70 Класс 7 — 131 -150 мкм 2 Класс 4 — 71 -90 Класс 8 — 151 -170
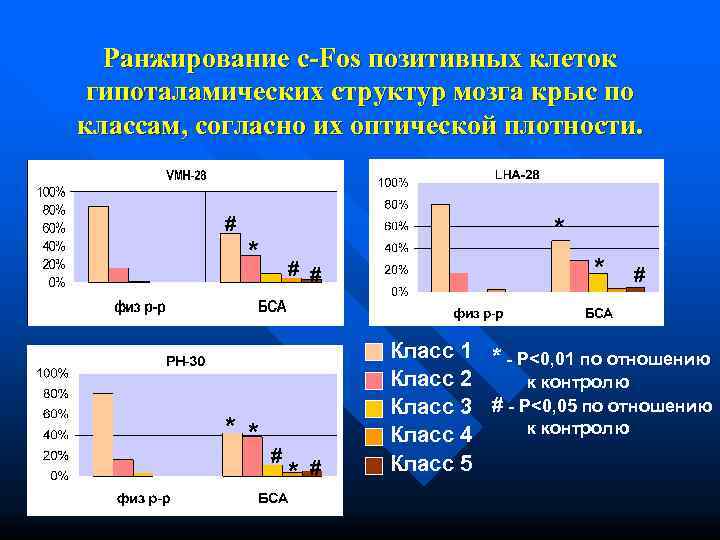
 Ранжирование c-Fos позитивных клеток гипоталамических структур мозга крыс по классам, согласно их оптической плотности. # * # # * # Класс 1 * - P<0, 01 по отношению Класс 2 к контролю Класс 3 # - P<0, 05 по отношению * * Класс 4 к контролю # Класс 5 * #
Ранжирование c-Fos позитивных клеток гипоталамических структур мозга крыс по классам, согласно их оптической плотности. # * # # * # Класс 1 * - P<0, 01 по отношению Класс 2 к контролю Класс 3 # - P<0, 05 по отношению * * Класс 4 к контролю # Класс 5 * #
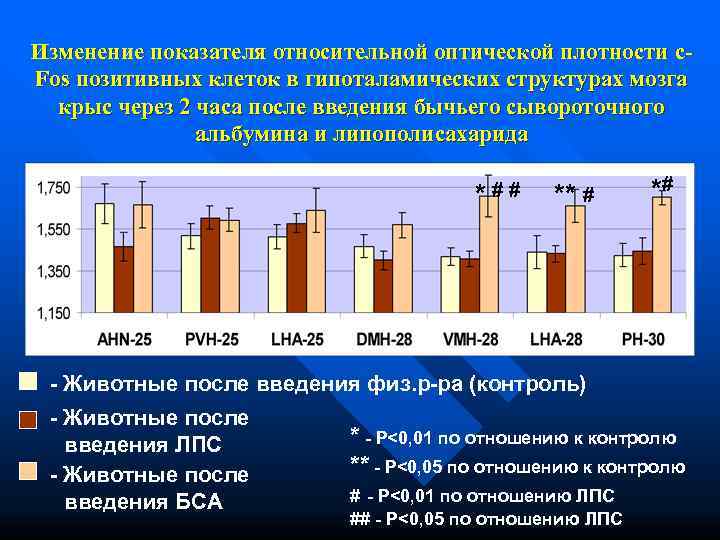
 Изменение показателя относительной оптической плотности c- Fos позитивных клеток в гипоталамических структурах мозга крыс через 2 часа после введения бычьего сывороточного альбумина и липополисахарида * ## ** # *# - Животные после введения физ. р-ра (контроль) - Животные после введения ЛПС * - P<0, 01 по отношению к контролю - Животные после ** - P<0, 05 по отношению к контролю введения БСА # - P<0, 01 по отношению ЛПС ## - P<0, 05 по отношению ЛПС
Изменение показателя относительной оптической плотности c- Fos позитивных клеток в гипоталамических структурах мозга крыс через 2 часа после введения бычьего сывороточного альбумина и липополисахарида * ## ** # *# - Животные после введения физ. р-ра (контроль) - Животные после введения ЛПС * - P<0, 01 по отношению к контролю - Животные после ** - P<0, 05 по отношению к контролю введения БСА # - P<0, 01 по отношению ЛПС ## - P<0, 05 по отношению ЛПС
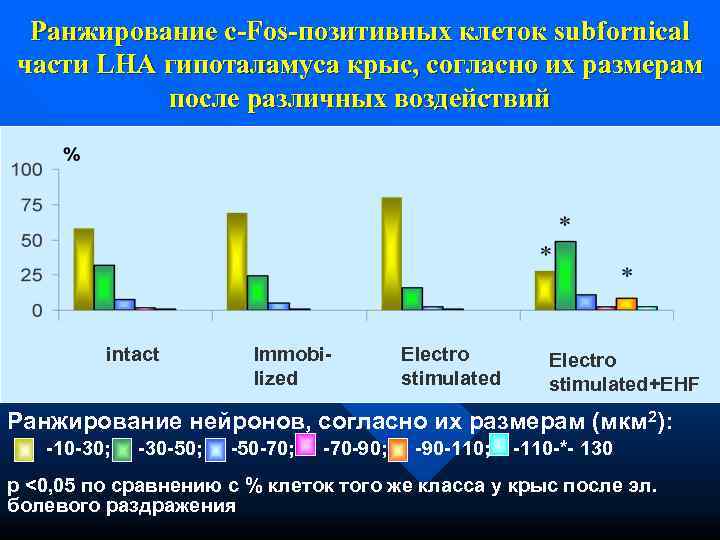
 Ранжирование c-Fos-позитивных клеток subfornical части LHA гипоталамуса крыс, согласно их размерам после различных воздействий intact Immobi- Electro lized stimulated+EHF Ранжирование нейронов, согласно их размерам (мкм 2): -10 -30; -30 -50; -50 -70; -70 -90; -90 -110; -110 -*- 130 p <0, 05 по сравнению с % клеток того же класса у крыс после эл. болевого раздражения
Ранжирование c-Fos-позитивных клеток subfornical части LHA гипоталамуса крыс, согласно их размерам после различных воздействий intact Immobi- Electro lized stimulated+EHF Ранжирование нейронов, согласно их размерам (мкм 2): -10 -30; -30 -50; -50 -70; -70 -90; -90 -110; -110 -*- 130 p <0, 05 по сравнению с % клеток того же класса у крыс после эл. болевого раздражения
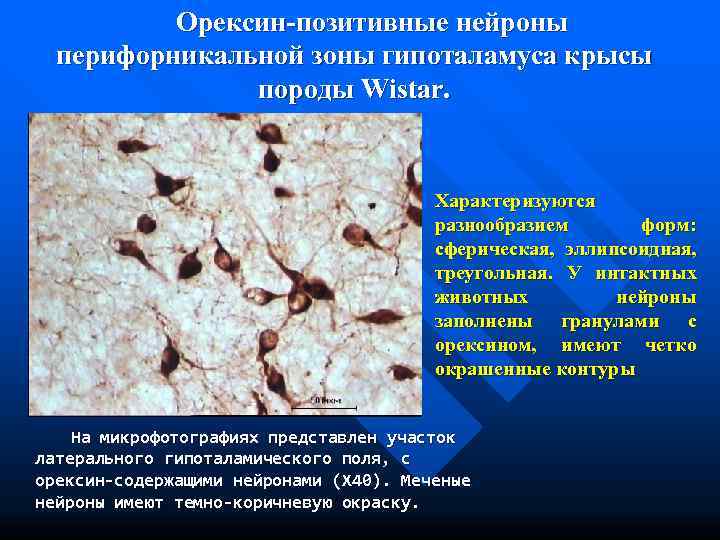
 Орексин-позитивные нейроны перифорникальной зоны гипоталамуса крысы породы Wistar. Характеризуются разнообразием форм: сферическая, эллипсоидная, треугольная. У интактных животных нейроны заполнены гранулами с орексином, имеют четко окрашенные контуры На микрофотографиях представлен участок латерального гипоталамического поля, с орексин-содержащими нейронами (X 40). Меченые нейроны имеют темно-коричневую окраску.
Орексин-позитивные нейроны перифорникальной зоны гипоталамуса крысы породы Wistar. Характеризуются разнообразием форм: сферическая, эллипсоидная, треугольная. У интактных животных нейроны заполнены гранулами с орексином, имеют четко окрашенные контуры На микрофотографиях представлен участок латерального гипоталамического поля, с орексин-содержащими нейронами (X 40). Меченые нейроны имеют темно-коричневую окраску.
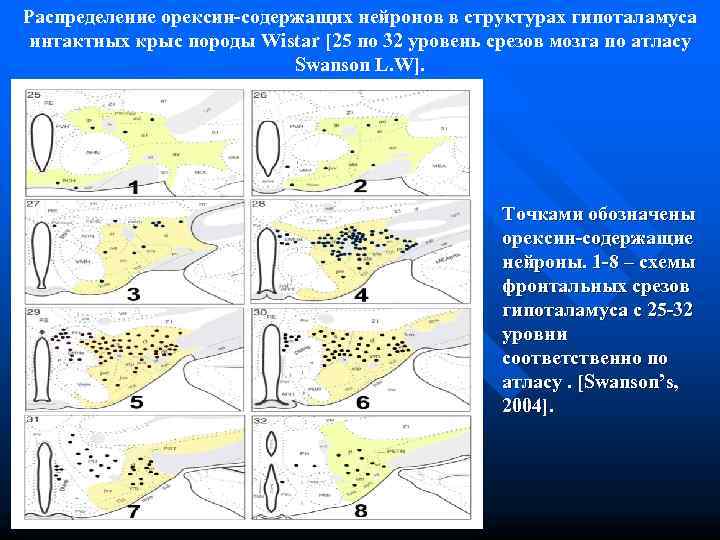
 Распределение орексин-содержащих нейронов в структурах гипоталамуса интактных крыс породы Wistar [25 по 32 уровень срезов мозга по атласу Swanson L. W]. Точками обозначены орексин-содержащие нейроны. 1 -8 – схемы фронтальных срезов гипоталамуса с 25 -32 уровни соответственно по атласу. [Swanson’s, 2004].
Распределение орексин-содержащих нейронов в структурах гипоталамуса интактных крыс породы Wistar [25 по 32 уровень срезов мозга по атласу Swanson L. W]. Точками обозначены орексин-содержащие нейроны. 1 -8 – схемы фронтальных срезов гипоталамуса с 25 -32 уровни соответственно по атласу. [Swanson’s, 2004].
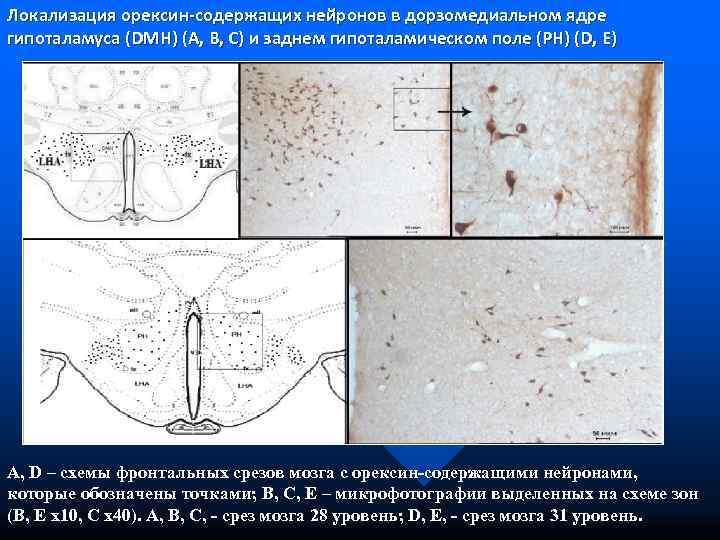
 Локализация орексин-содержащих нейронов в дорзомедиальном ядре гипоталамуса (DMH) (A, B, C) и заднем гипоталамическом поле (PH) (D, E) A, D – схемы фронтальных срезов мозга с орексин-содержащими нейронами, которые обозначены точками; B, C, E – микрофотографии выделенных на схеме зон (B, E х10, C х40). A, B, C, - срез мозга 28 уровень; D, E, - срез мозга 31 уровень.
Локализация орексин-содержащих нейронов в дорзомедиальном ядре гипоталамуса (DMH) (A, B, C) и заднем гипоталамическом поле (PH) (D, E) A, D – схемы фронтальных срезов мозга с орексин-содержащими нейронами, которые обозначены точками; B, C, E – микрофотографии выделенных на схеме зон (B, E х10, C х40). A, B, C, - срез мозга 28 уровень; D, E, - срез мозга 31 уровень.
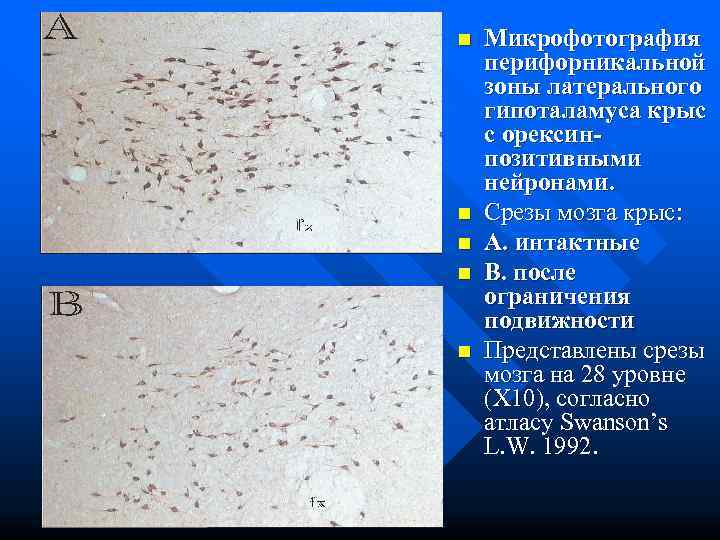
 n Микрофотография перифорникальной зоны латерального гипоталамуса крыс с орексин- позитивными нейронами. n Срезы мозга крыс: n А. интактные n B. после ограничения подвижности n Представлены срезы мозга на 28 уровне (X 10), согласно атласу Swanson’s L. W. 1992.
n Микрофотография перифорникальной зоны латерального гипоталамуса крыс с орексин- позитивными нейронами. n Срезы мозга крыс: n А. интактные n B. после ограничения подвижности n Представлены срезы мозга на 28 уровне (X 10), согласно атласу Swanson’s L. W. 1992.
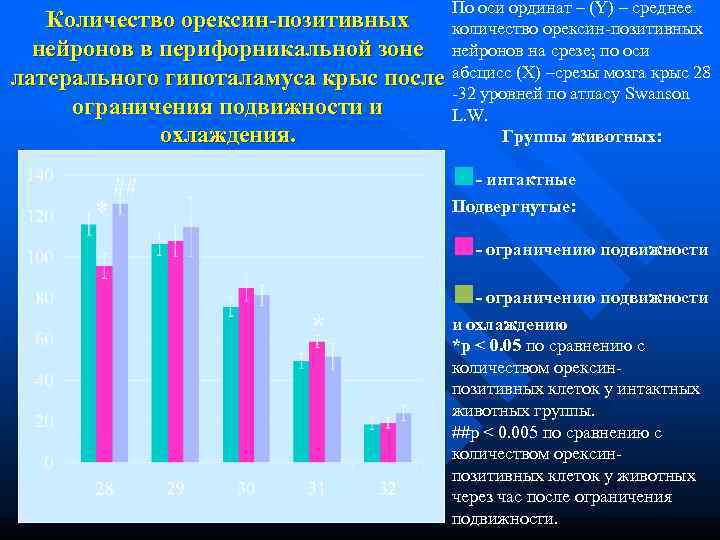
 По оси ординат – (Y) – среднее Количество орексин-позитивных количество орексин-позитивных нейронов в перифорникальной зоне нейронов на срезе; по оси латерального гипоталамуса крыс после абсцисс (X) –срезы мозга крыс 28 -32 уровней по атласу Swanson ограничения подвижности и L. W. охлаждения. Группы животных: ■- интактные Подвергнутые: ■- ограничению подвижности и охлаждению *p < 0. 05 по сравнению с количеством орексин- позитивных клеток у интактных животных группы. ##p < 0. 005 по сравнению с количеством орексин- позитивных клеток у животных через час после ограничения подвижности.
По оси ординат – (Y) – среднее Количество орексин-позитивных количество орексин-позитивных нейронов в перифорникальной зоне нейронов на срезе; по оси латерального гипоталамуса крыс после абсцисс (X) –срезы мозга крыс 28 -32 уровней по атласу Swanson ограничения подвижности и L. W. охлаждения. Группы животных: ■- интактные Подвергнутые: ■- ограничению подвижности и охлаждению *p < 0. 05 по сравнению с количеством орексин- позитивных клеток у интактных животных группы. ##p < 0. 005 по сравнению с количеством орексин- позитивных клеток у животных через час после ограничения подвижности.
 По оси ординат – (Y) - количество Изменение иммунореактивности орексин-позитивных нейронов в структурах и структуре на определенном уровне зонах гипоталамуса крыс, расположенных среза мозга; по оси абсцисс (X) – структуры на срезе мозга крыс по на срезах мозга 28 уровня. атласу Swanson L. W. Группы животных: ■- интактные Подвергнутые: ■- ограничению подвижности ■- ограничению подвижности и охлаждению **p < 0. 005 по сравнению с количеством орексин-позитивных клеток у интактных животных. ##p < 0. 005 по сравнению с количеством орексин-позитивных клеток у животных через час после ограничения подвижности.
По оси ординат – (Y) - количество Изменение иммунореактивности орексин-позитивных нейронов в структурах и структуре на определенном уровне зонах гипоталамуса крыс, расположенных среза мозга; по оси абсцисс (X) – структуры на срезе мозга крыс по на срезах мозга 28 уровня. атласу Swanson L. W. Группы животных: ■- интактные Подвергнутые: ■- ограничению подвижности ■- ограничению подвижности и охлаждению **p < 0. 005 по сравнению с количеством орексин-позитивных клеток у интактных животных. ##p < 0. 005 по сравнению с количеством орексин-позитивных клеток у животных через час после ограничения подвижности.
 По оси ординат – (Y) - количество Изменение иммунореактивности орексин-позитивных нейронов в структуре на определенном уровне орексин-позитивных нейронов в среза мозга; по оси абсцисс (X) – структурах и зонах гипоталамуса крыс, структуры на срезе мозга крыс по атласу Swanson L. W. расположенных на срезах мозга 29 уровня. Группы животных: ■- интактные Подвергнутые: ■- ограничению подвижности и охлаждению *p < 0. 05; **p < 0. 005 по сравнению с количеством орексин-позитивных клеток у интактных животных. #p < 0. 05 по сравнению с количеством орексин-позитивных клеток у животных через час после ограничения подвижности.
По оси ординат – (Y) - количество Изменение иммунореактивности орексин-позитивных нейронов в структуре на определенном уровне орексин-позитивных нейронов в среза мозга; по оси абсцисс (X) – структурах и зонах гипоталамуса крыс, структуры на срезе мозга крыс по атласу Swanson L. W. расположенных на срезах мозга 29 уровня. Группы животных: ■- интактные Подвергнутые: ■- ограничению подвижности и охлаждению *p < 0. 05; **p < 0. 005 по сравнению с количеством орексин-позитивных клеток у интактных животных. #p < 0. 05 по сравнению с количеством орексин-позитивных клеток у животных через час после ограничения подвижности.
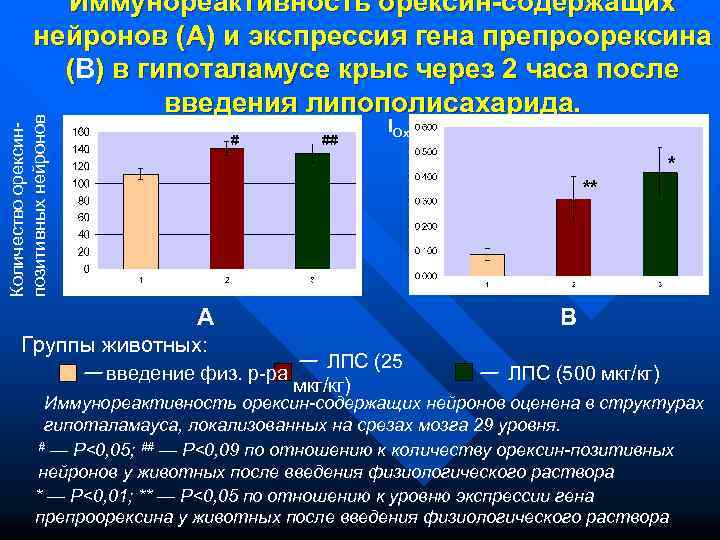
 Иммунореактивность орексин-содержащих нейронов (A) и экспрессия гена препроорексина (B) в гипоталамусе крыс через 2 часа после введения липополисахарида. позитивных нейронов IOx Количество орексин- # ## ** A B Группы животных: — ЛПС (25 — введение физ. р-ра — ЛПС (500 мкг/кг) Иммунореактивность орексин-содержащих нейронов оценена в структурах гипоталамауса, локализованных на срезах мозга 29 уровня. # — P<0, 05; ## — P<0, 09 по отношению к количеству орексин-позитивных нейронов у животных после введения физиологического раствора * — P<0, 01; ** — P<0, 05 по отношению к уровню экспрессии гена препроорексина у животных после введения физиологического раствора
Иммунореактивность орексин-содержащих нейронов (A) и экспрессия гена препроорексина (B) в гипоталамусе крыс через 2 часа после введения липополисахарида. позитивных нейронов IOx Количество орексин- # ## ** A B Группы животных: — ЛПС (25 — введение физ. р-ра — ЛПС (500 мкг/кг) Иммунореактивность орексин-содержащих нейронов оценена в структурах гипоталамауса, локализованных на срезах мозга 29 уровня. # — P<0, 05; ## — P<0, 09 по отношению к количеству орексин-позитивных нейронов у животных после введения физиологического раствора * — P<0, 01; ** — P<0, 05 по отношению к уровню экспрессии гена препроорексина у животных после введения физиологического раствора
 Изменение иммунореактивности орексин-позитивных нейронов в структурах и зонах гипоталамуса крыс, после ограничения подвижности и охлаждения 1 2 3 4 5 6 7 8 1 -4 –после ограничения подвижности; 5 -8 – после ограничения подвижности и охлаждения. Красным цветом обозначены структуры и зоны гипоталамуса крыс (по атласу Swanson L. W. ), в которых наблюдается увеличение иммунореактивности орексин- позитивных нейронов, зеленым – ее уменьшение.
Изменение иммунореактивности орексин-позитивных нейронов в структурах и зонах гипоталамуса крыс, после ограничения подвижности и охлаждения 1 2 3 4 5 6 7 8 1 -4 –после ограничения подвижности; 5 -8 – после ограничения подвижности и охлаждения. Красным цветом обозначены структуры и зоны гипоталамуса крыс (по атласу Swanson L. W. ), в которых наблюдается увеличение иммунореактивности орексин- позитивных нейронов, зеленым – ее уменьшение.
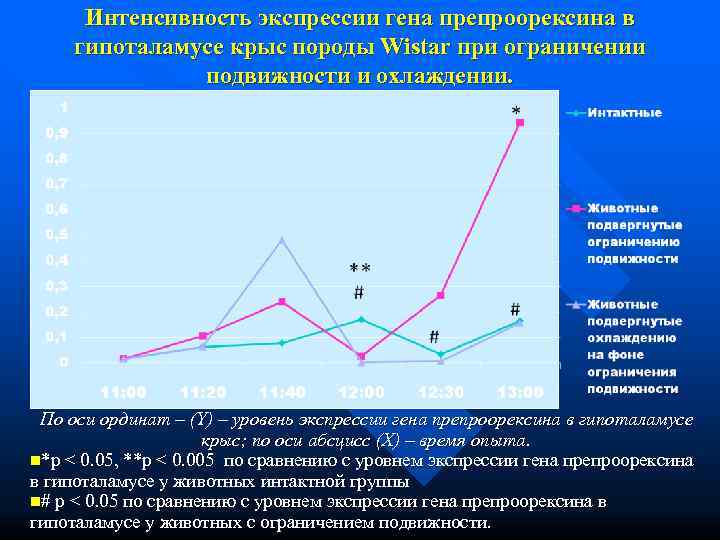
 Интенсивность экспрессии гена препроорексина в гипоталамусе крыс породы Wistar при ограничении подвижности и охлаждении. По оси ординат – (Y) – уровень экспрессии гена препроорексина в гипоталамусе крыс; по оси абсцисс (X) – время опыта. n*p < 0. 05, **p < 0. 005 по сравнению с уровнем экспрессии гена препроорексина в гипоталамусе у животных интактной группы n# p < 0. 05 по сравнению с уровнем экспрессии гена препроорексина в гипоталамусе у животных с ограничением подвижности.
Интенсивность экспрессии гена препроорексина в гипоталамусе крыс породы Wistar при ограничении подвижности и охлаждении. По оси ординат – (Y) – уровень экспрессии гена препроорексина в гипоталамусе крыс; по оси абсцисс (X) – время опыта. n*p < 0. 05, **p < 0. 005 по сравнению с уровнем экспрессии гена препроорексина в гипоталамусе у животных интактной группы n# p < 0. 05 по сравнению с уровнем экспрессии гена препроорексина в гипоталамусе у животных с ограничением подвижности.
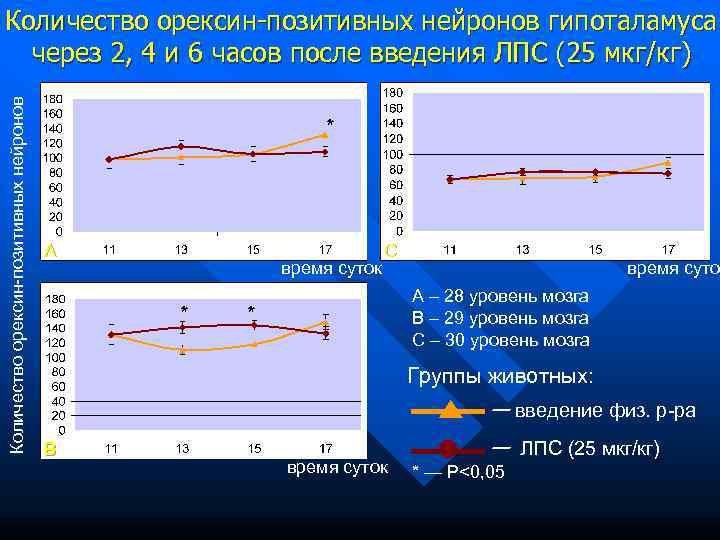
 Количество орексин-позитивных нейронов гипоталамуса через 2, 4 и 6 часов после введения ЛПС (25 мкг/кг) Количество орексин-позитивных нейронов * A C время суток А – 28 уровень мозга * * В – 29 уровень мозга С – 30 уровень мозга Группы животных: — введение физ. р-ра B — ЛПС (25 мкг/кг) время суток * — P<0, 05
Количество орексин-позитивных нейронов гипоталамуса через 2, 4 и 6 часов после введения ЛПС (25 мкг/кг) Количество орексин-позитивных нейронов * A C время суток А – 28 уровень мозга * * В – 29 уровень мозга С – 30 уровень мозга Группы животных: — введение физ. р-ра B — ЛПС (25 мкг/кг) время суток * — P<0, 05
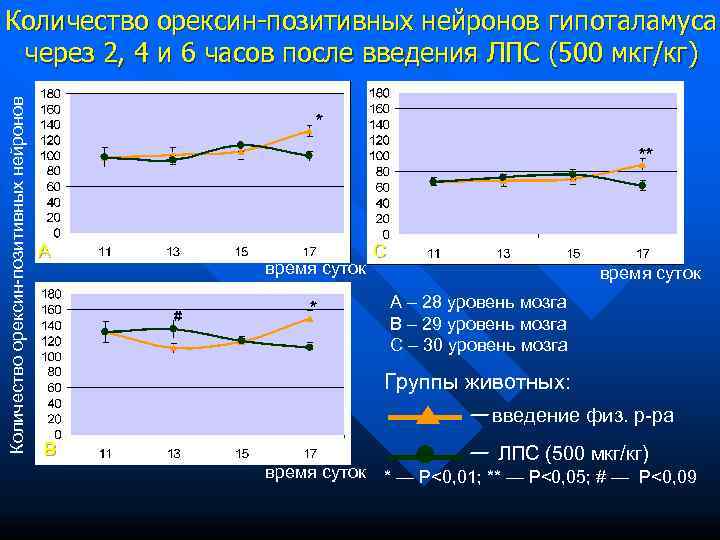
 Количество орексин-позитивных нейронов гипоталамуса через 2, 4 и 6 часов после введения ЛПС (500 мкг/кг) Количество орексин-позитивных нейронов * ** A C время суток * А – 28 уровень мозга # В – 29 уровень мозга С – 30 уровень мозга Группы животных: — введение физ. р-ра B — ЛПС (500 мкг/кг) время суток * — P<0, 01; ** — P<0, 05; # — P<0, 09
Количество орексин-позитивных нейронов гипоталамуса через 2, 4 и 6 часов после введения ЛПС (500 мкг/кг) Количество орексин-позитивных нейронов * ** A C время суток * А – 28 уровень мозга # В – 29 уровень мозга С – 30 уровень мозга Группы животных: — введение физ. р-ра B — ЛПС (500 мкг/кг) время суток * — P<0, 01; ** — P<0, 05; # — P<0, 09
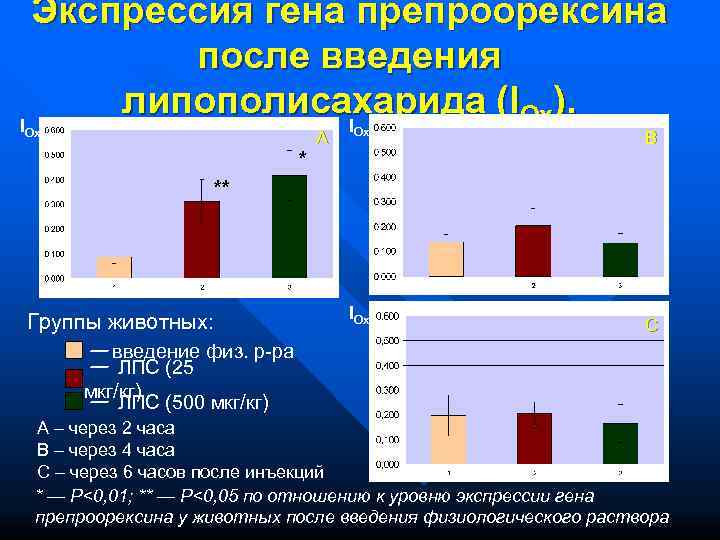
 Экспрессия гена препроорексина после введения I липополисахарида (IOx). I Ox A B ** IOx Группы животных: C — введение физ. р-ра — ЛПС (25 мкг/кг) — ЛПС (500 мкг/кг) А – через 2 часа В – через 4 часа С – через 6 часов после инъекций * — P<0, 01; ** — P<0, 05 по отношению к уровню экспрессии гена препроорексина у животных после введения физиологического раствора
Экспрессия гена препроорексина после введения I липополисахарида (IOx). I Ox A B ** IOx Группы животных: C — введение физ. р-ра — ЛПС (25 мкг/кг) — ЛПС (500 мкг/кг) А – через 2 часа В – через 4 часа С – через 6 часов после инъекций * — P<0, 01; ** — P<0, 05 по отношению к уровню экспрессии гена препроорексина у животных после введения физиологического раствора

