патофизиология клетки.ppt
- Количество слайдов: 67

ПАТОФИЗИОЛОГИЯ КЛЕТКИ

Повреждение клетки – разнообразные по этиологии, патогенезу и проявлениям нарушения ее структуры, метаболизма и функции, приводящие к многоликим расстройствам гомеостаза (постоянства р. Н, электролитов, воды, белков, углеводов, липидов, гормонов, витаминов и других ФАВ), а также снижению ее приспособляемости (к постоянно меняющимся условиям внешней и внутренней среды организма), резистентности (к действию разных повреждающих факторов) и продолжительности жизни. В учении о повреждении клетки можно условно выделить четыре раздела: патология клетки в целом; патология субклеточных структур; патология межклеточного взаимодействия; патология взаимодействия клеток с межклеточными структурами.

Этиология повреждения клетки В зависимости от свойств (природы) выделяют следующие три основных вида патогенных факторов: физические, химические и биологические. • К физическим факторам относятся: механические, температурные, космические воздействия, ионизирующая радиация, изменения осмотического давления, содержания воды и электролитов внутри и вне клеток и др. • К химическим факторам относятся: соли тяжелых металлов, различного (как простого, так и сложного) строения токсические вещества, в том числе пестициды, лекарственные средства, недостаток или избыток многообразных и необходимых для нормальной жизнедеятельности клетки веществ (кислорода, субстратов, медиаторов, комедиаторов, витаминов, гормонов, пептидов, трофогенов), а также патотрофогенов, антигенов, аутоантител и др. • К биологическим факторам относятся: вирусы, микоплазмы, риккетсии, бактерии, грибы, простейшие, паразиты (насекомые, гельминты и др. ) и продукты их жизнедеятельности (токсины и др. ).

Особенности повреждений при действии различных факторов

Этиология повреждения клетки • В зависимости от интенсивности действия патогенные факторы могут быть абсолютными и относительными. Первые независимо от условий (даже благоприятных) всегда способны вызвать то или иное повреждение клеток. Вторые могут оказаться патогенными только при неблагоприятных внешних и/или внутренних условиях. • В зависимости от происхождения выделяют следующие виды патогенных факторов: 1) экзогенные (первичные) и эндогенные (как первичные в результате прямого повреждения клеток; так и вторичные в результате опосредованного повреждения клеток); 2) инфекционными и неинфекционными.

Пути действия повреждающих агентов на клетки и межклеточные структуры. • прямое (непосредственное) действие патогенных факторов на клетки (клеточную мембрану, различные субклеточные структуры, ядро, цитоплазму) и межклеточные структуры; • опосредованное действие повреждающих факторов на клетки и/или межклеточные образования через нарушение межсистемной, вне- и внутриклеточной регуляторных систем (нервной, гуморальной, эндокринной, иммунной, генетической).

Виды повреждений клетки : • • • структурные и функциональные; острые и хронические; парциальные, субтотальные и тотальные; обратимые и необратимые; специфические и неспецифические; дисплазия; дистрофия; паранекроз; некробиоз; некроз.

Структурные (морфологические) повреждения клетки • набухание (увеличение) и вакуолизацию клетки и ее органелл (особенно митохондрий, цитоплазма, ядро); • изменения мембран клетки и органелл (лизосом, митохондрий, эндоплазматического ретикулюма, рибосом, полисом, аппарата Гольджи, ядра и др. ); • деструктивные изменения ядра (его размеров, формы, структуры); • уменьшение числа функционирующих органелл (рибосом, митохондрий и др. ); • снижение числа рецепторов мембран клеток; • нарушения межклеточных контактов; • расстройства контактов клеток с межклеточными структурами; • повреждение генетических структур клетки (генов, хромосом, генома).

Функциональные повреждения клетки • • • изменения физико-химических и биоэлектрических свойств мембран (например, увеличение электропроводности ткани, снижение электрического (омического) сопротивления клеточных мембран; повышение проницаемости мембран клеток и органелл для микро- и макромолекул (ионов, моно-, ди- и полимеров белков, липидов, углеводов; появление и увеличение в крови цитоплазматических ферментов (аспартат- и аланинаминотрансфераз, лактатдегидрогеназы, креатинкиназы, кислой фосфатазы и др. ) в результате повреждения клеток, особенно их мембран; изменение тинкториальных свойств клеток (увеличение способности клеток окрашиваться витальными красителями в результате повышения сорбционных свойств поврежденной клетки и возрастания проницаемости их мембран; уменьшение подвижности клеток; снижение активности рецепторов клеток; нарушение процесса деления клеток (снижение и извращение функции ядра, митохондрий и других внутриклеточных и внеклеточных структур); нарушение биохимических процессов в клетках и межклеточных структурах, главным образом, снижение потребления кислорода, содержания кальция в митохондриях и процесса окислительного фосфорилирования, приводящих к расстройствам как энергетического, так и пластического обменов); появление новых функций клеток и др.

• Острые и хронические повреждения. Острое повреждение клетки возникает быстро (секунды, минуты, часы, дни), хроническое – медленно (недели, месяцы, годы). Парциальные и тотальные повреждения. При парциальных повреждениях выходит из строя та или иная часть клетки. Тотальные повреждения распространяются на всю клетку. Обратимые и необратимые повреждения. Обратимые повреждения не сопровождаются гибелью клетки после действия патогенного агента. Они устраняются активированными клеточными защитно-приспособительными механизмами. Необратимые повреждения характеризуются выраженными и стойкими нарушениями внутриклеточного гомеостаза. Обычно заканчиваются гибелью клетки.

Неспецифические и специфические повреждения. Неспецифические повреждения одинаковы для различных патогенных воздействий. К ним относятся: - набухание клеток; - нарушение энергетики клетки; - клеточный ацидоз; - ионный дисбаланс; - увеличение сорбирования красителей. Специфические повреждения вызваны конкретным патогенным агентом. Примерами таких повреждений являются: - гемолиз эритроцитов антиэритроцитарными антителами; - блокирование холинэстеразы фосфорорганическими соединениями; - ингибирование цитохромоксидазы цианидами.

• Дисплазии (от греч. dys – нарушение, расстройство, plaseo – образую) – нарушения процесса развития клеток, которое проявляется выраженным и длительным изменением их структуры, функций и в целом жизнедеятельности, в том числе продолжительности жизни. • Дистрофии (от греч. dys – нарушение, расстройство, trophe – питаю) – это такие изменения состава клеточно-тканевых структур, которые обусловлены нарушениями в них процессов метаболизма (обмена веществ) и ведущие к накоплению или уменьшению тех или иных веществ (соединений), либо к появлению веществ, которые в норме не встречаются. • Паранекроз – состояние клеток и тканей, приближающееся к некробиозу, развивающееся вследствие дистрофических изменений и являющееся обратимым. Характеризуется помутнением цитоплазмы, возникновением грубодисперсных осадков, повышением вязкости коллоидов, уменьшением дисперсности, усилением сорбционных свойств и изменением электролитного состава цитоплазмы и ядра, а также вакуолизацией клетки, повышением проницаемости цитоплазматической мембраны для различных веществ, в том числе, для красителей.

• Некробиоз – состояние тканей (клеток), находящееся между жизнью и смертью и предшествующее некрозу и развивающееся вследствие необратимых дистрофических процессов. Длительность некробиоза разная в зависимости от характера повреждающих факторов, вида и состояния повреждаемых тканей. • Некроз – омертвение клеточно-тканевых структур части тела, наступающее при жизни целостного организма, и обусловленное действием различных повреждающих факторов. Некроз необходимо отличать от физиологического отмирания (умирания) клеток, наступающего вследствие их естественного, наследственно обусловленного, запрограммированного старения и изнашивания (апоптоза). Процесс апоптоза в условиях действия на организм повреждающих факторов, как правило, ускоряется, а восстановительные процессы в погибающих клетках – замедляются.

Основные механизмы повреждения клетки Нарушения энергетического обмена Нарушения пластического обмена. . Повреждение клеточных и субклеточных мембран. Нарушение ферментных систем Расстройства электролитного и водного баланса. Нарушения генетической программы. Нарушение пролиферативной активности. Расстройства функции рецепторного аппарата
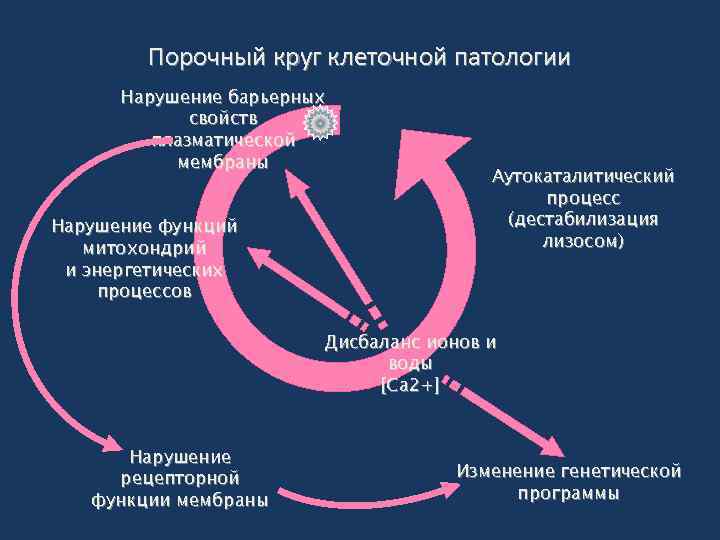
Порочный круг клеточной патологии Нарушение барьерных свойств плазматической мембраны Нарушение функций митохондрий и энергетических процессов Аутокаталитический процесс (дестабилизация лизосом) Дисбаланс ионов и воды [Ca 2+] Нарушение рецепторной функции мембраны Изменение генетической программы
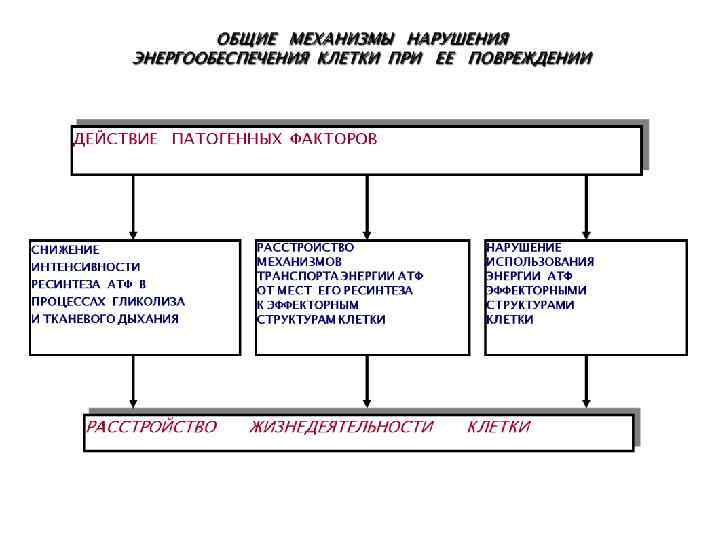
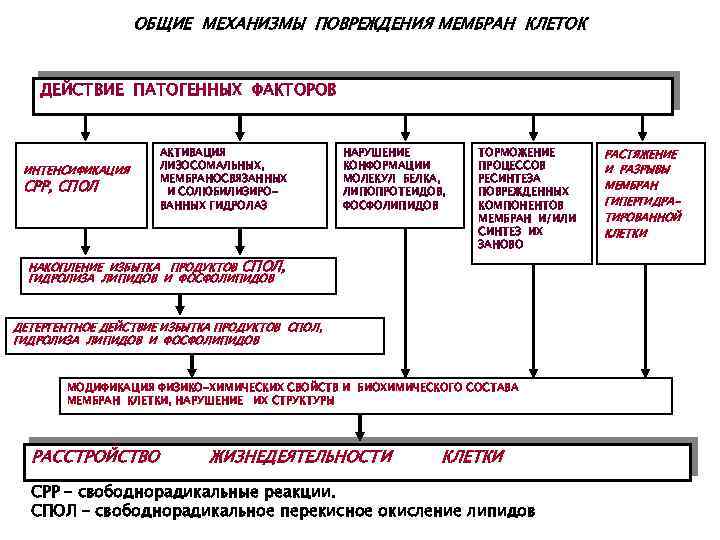
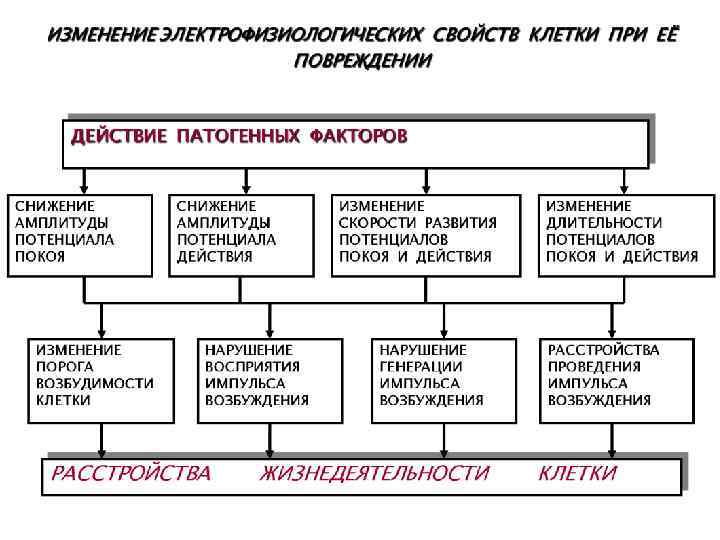
ОБЩИЕ МЕХАНИЗМЫ ПОВРЕЖДЕНИЯ МЕМБРАН КЛЕТОК ДЕЙСТВИЕ ПАТОГЕННЫХ ФАКТОРОВ ИНТЕНСИФИКАЦИЯ СРР, СПОЛ АКТИВАЦИЯ ЛИЗОСОМАЛЬНЫХ, МЕМБРАНОСВЯЗАННЫХ И СОЛЮБИЛИЗИРОВАННЫХ ГИДРОЛАЗ НАРУШЕНИЕ КОНФОРМАЦИИ МОЛЕКУЛ БЕЛКА, ЛИПОПРОТЕИДОВ, ФОСФОЛИПИДОВ ТОРМОЖЕНИЕ ПРОЦЕССОВ РЕСИНТЕЗА ПОВРЕЖДЕННЫХ КОМПОНЕНТОВ МЕМБРАН И/ИЛИ СИНТЕЗ ИХ ЗАНОВО НАКОПЛЕНИЕ ИЗБЫТКА ПРОДУКТОВ СПОЛ, ГИДРОЛИЗА ЛИПИДОВ И ФОСФОЛИПИДОВ ДЕТЕРГЕНТНОЕ ДЕЙСТВИЕ ИЗБЫТКА ПРОДУКТОВ СПОЛ, ГИДРОЛИЗА ЛИПИДОВ И ФОСФОЛИПИДОВ МОДИФИКАЦИЯ ФИЗИКО-ХИМИЧЕСКИХ СВОЙСТВ И БИОХИМИЧЕСКОГО СОСТАВА МЕМБРАН КЛЕТКИ, НАРУШЕНИЕ ИХ СТРУКТУРЫ РАССТРОЙСТВО ЖИЗНЕДЕЯТЕЛЬНОСТИ КЛЕТКИ СРР – свободнорадикальные реакции. СПОЛ – свободнорадикальное перекисное окисление липидов РАСТЯЖЕНИЕ И РАЗРЫВЫ МЕМБРАН ГИПЕРГИДРАТИРОВАННОЙ КЛЕТКИ
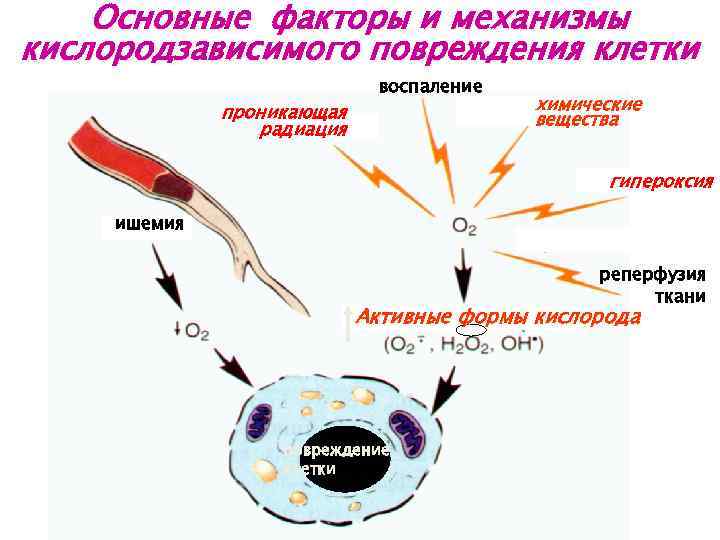
Основные факторы и механизмы кислородзависимого повреждения клетки проникающая радиация воспаление химические вещества гипероксия ишемия реперфузия ткани Активные формы кислорода повреждение клетки
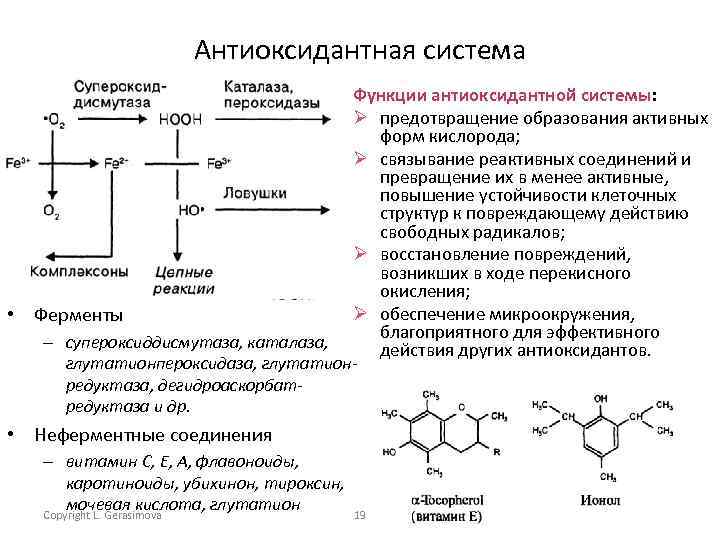
Антиоксидантная система • Ферменты Функции антиоксидантной системы: Ø предотвращение образования активных форм кислорода; Ø связывание реактивных соединений и превращение их в менее активные, повышение устойчивости клеточных структур к повреждающему действию свободных радикалов; Ø восстановление повреждений, возникших в ходе перекисного окисления; Ø обеспечение микроокружения, благоприятного для эффективного действия других антиоксидантов. – супероксиддисмутаза, каталаза, глутатионпероксидаза, глутатионредуктаза, дегидроаскорбатредуктаза и др. • Неферментные соединения – витамин С, Е, А, флавоноиды, каротиноиды, убихинон, тироксин, мочевая кислота, глутатион Copyright L. Gerasimova 19 2007
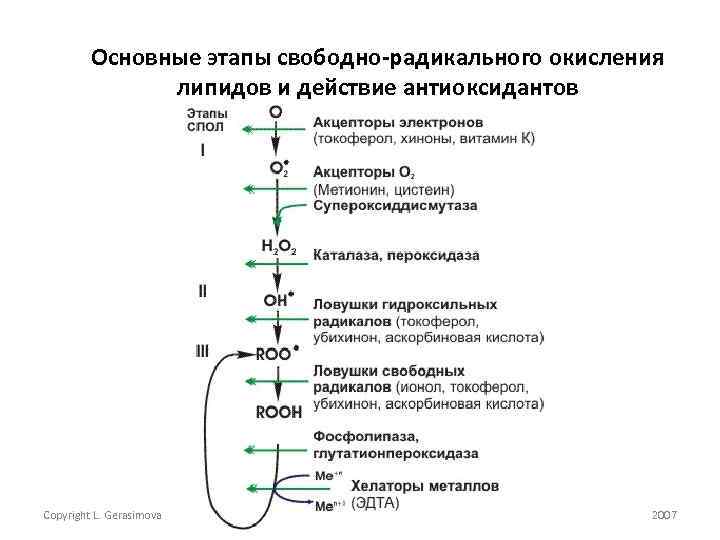
Основные этапы свободно-радикального окисления липидов и действие антиоксидантов Copyright L. Gerasimova 20 2007
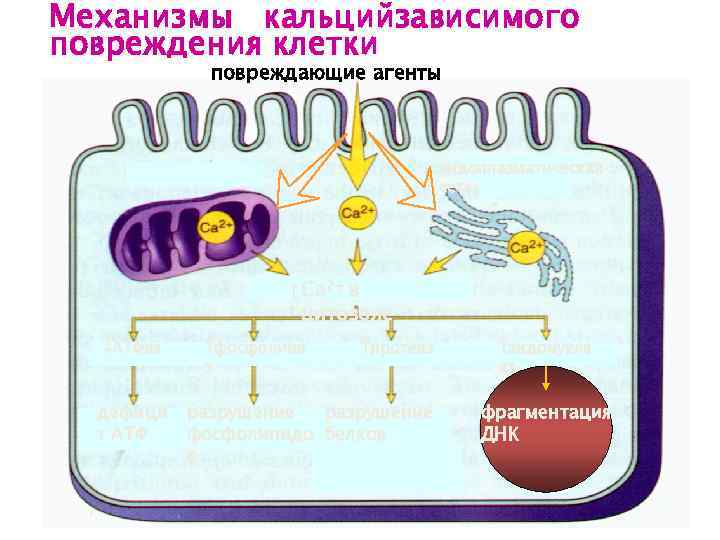
Механизмы кальцийзависимого повреждения клетки повреждающие агенты эндоплазматическая сеть Са 2+ в цитозоле АТФаз дефици т АТФ фосфолипа з протеаз разрушение фосфолипидо белков в эндонукле аз фрагментация ДНК
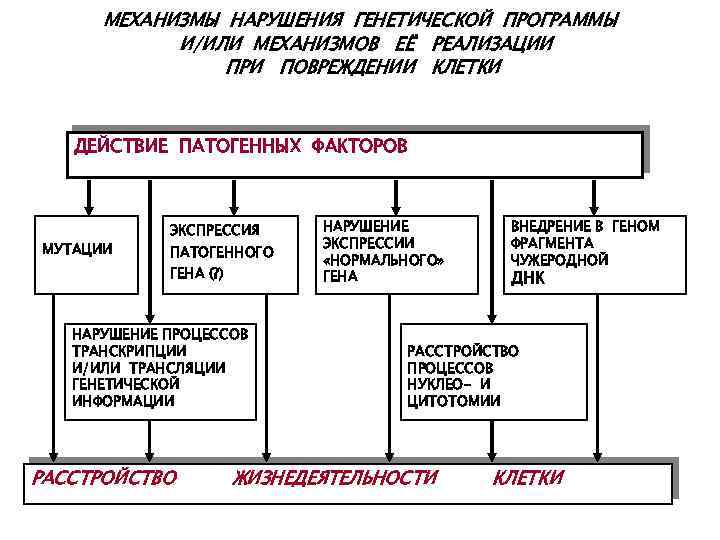
МЕХАНИЗМЫ НАРУШЕНИЯ ГЕНЕТИЧЕСКОЙ ПРОГРАММЫ И/ИЛИ МЕХАНИЗМОВ ЕЁ РЕАЛИЗАЦИИ ПРИ ПОВРЕЖДЕНИИ КЛЕТКИ ДЕЙСТВИЕ ПАТОГЕННЫХ ФАКТОРОВ МУТАЦИИ ЭКСПРЕССИЯ ПАТОГЕННОГО ГЕНА (? ) НАРУШЕНИЕ ПРОЦЕССОВ ТРАНСКРИПЦИИ И/ИЛИ ТРАНСЛЯЦИИ ГЕНЕТИЧЕСКОЙ ИНФОРМАЦИИ РАССТРОЙСТВО НАРУШЕНИЕ ЭКСПРЕССИИ «НОРМАЛЬНОГО» ГЕНА ВНЕДРЕНИЕ В ГЕНОМ ФРАГМЕНТА ЧУЖЕРОДНОЙ ДНК РАССТРОЙСТВО ПРОЦЕССОВ НУКЛЕО- И ЦИТОТОМИИ ЖИЗНЕДЕЯТЕЛЬНОСТИ КЛЕТКИ
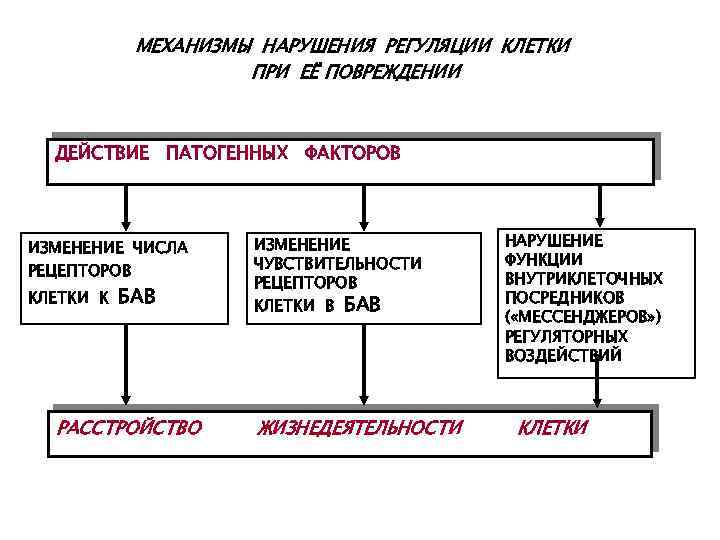
МЕХАНИЗМЫ НАРУШЕНИЯ РЕГУЛЯЦИИ КЛЕТКИ ПРИ ЕЁ ПОВРЕЖДЕНИИ ДЕЙСТВИЕ ПАТОГЕННЫХ ФАКТОРОВ ИЗМЕНЕНИЕ ЧИСЛА РЕЦЕПТОРОВ КЛЕТКИ К БАВ РАССТРОЙСТВО ИЗМЕНЕНИЕ ЧУВСТВИТЕЛЬНОСТИ РЕЦЕПТОРОВ КЛЕТКИ В БАВ ЖИЗНЕДЕЯТЕЛЬНОСТИ НАРУШЕНИЕ ФУНКЦИИ ВНУТРИКЛЕТОЧНЫХ ПОСРЕДНИКОВ ( «МЕССЕНДЖЕРОВ» ) РЕГУЛЯТОРНЫХ ВОЗДЕЙСТВИЙ КЛЕТКИ
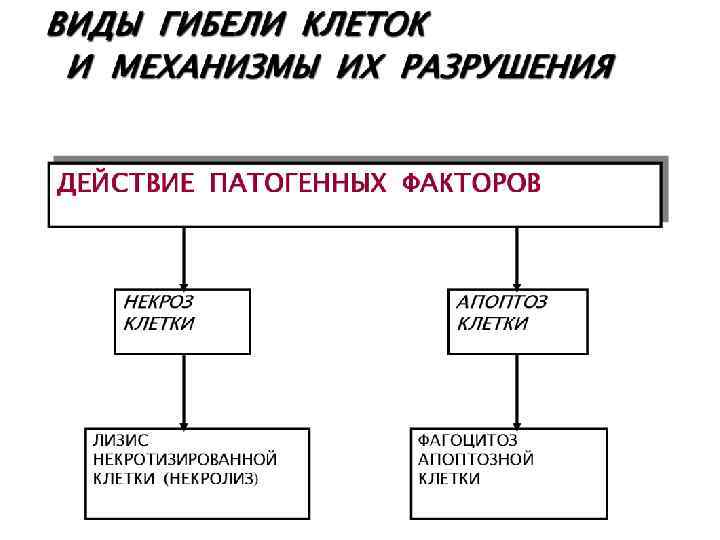

АПОПТОЗ (греч. apoptosis – опадание листьев) * Форма гибели отдельных клеток. * Возникает под действием внеили внутриклеточных факторов. * Осуществляется путём активации специализированных внутриклеточных процессов. * Регулируется определёнными генами.
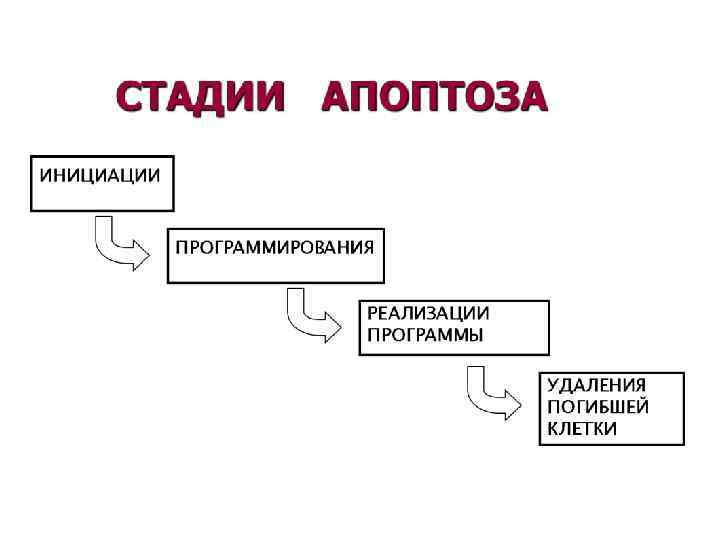
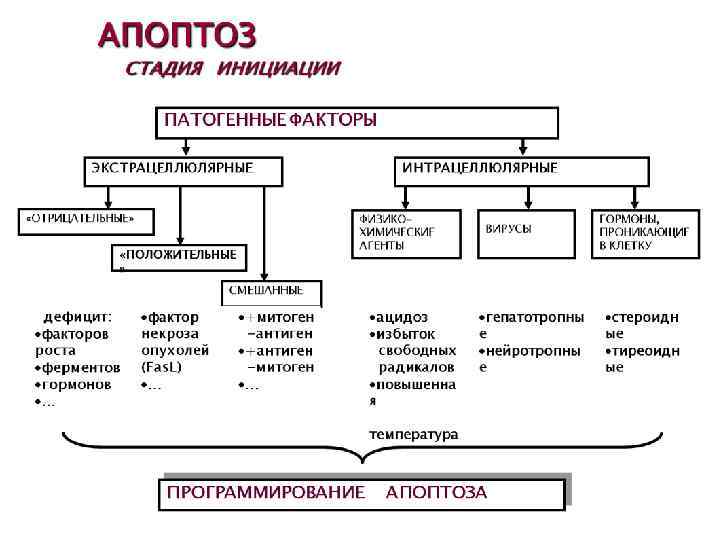
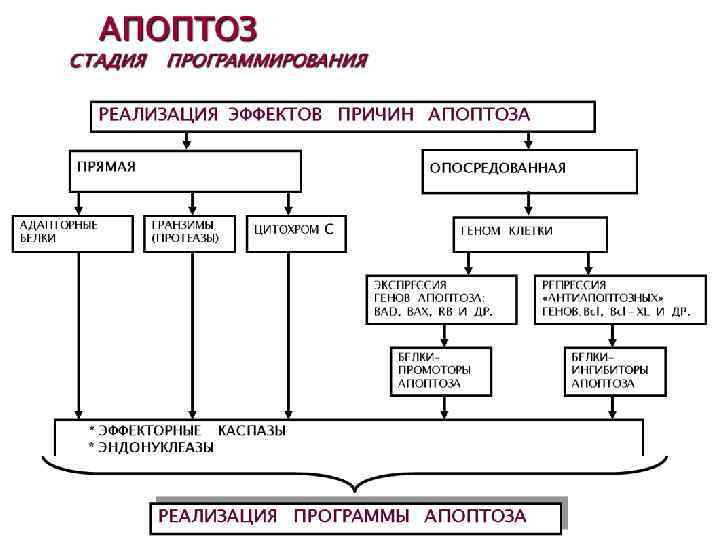
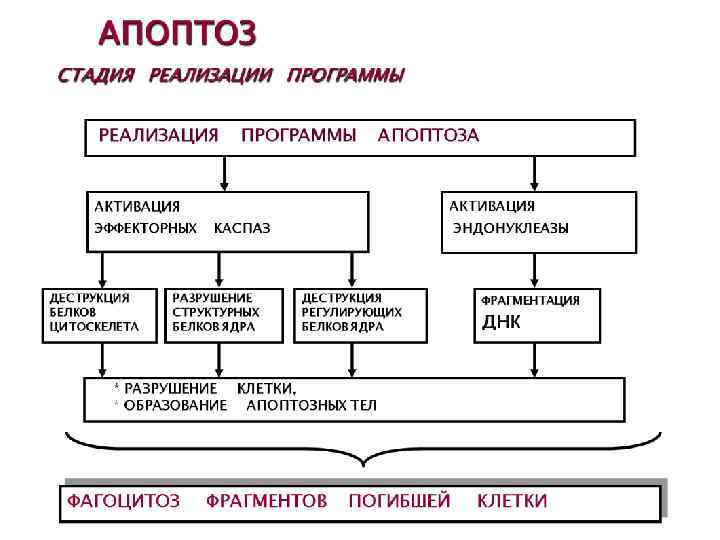
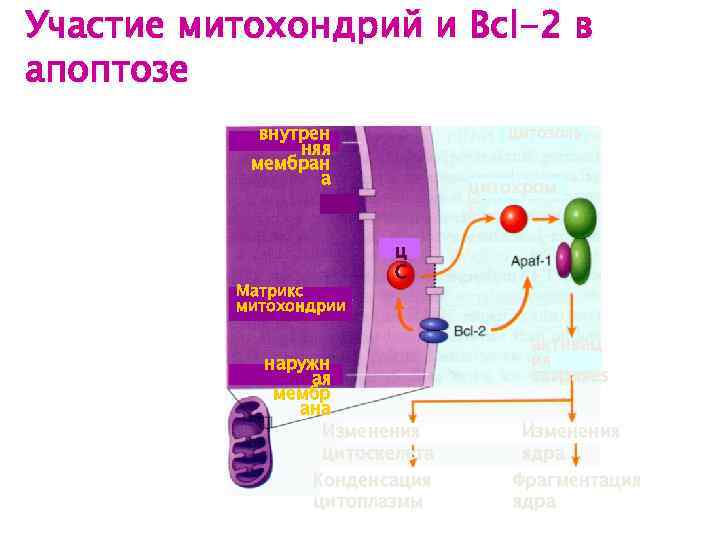
Участие митохондрий и Bcl-2 в апоптозе внутрен няя мембран а Матрикс митохондрии цитозоль цитохром С ц С наружн ая мембр ана Изменения цитоскелета Конденсация цитоплазмы активац ия caspases Изменения ядра Фрагментация ядра
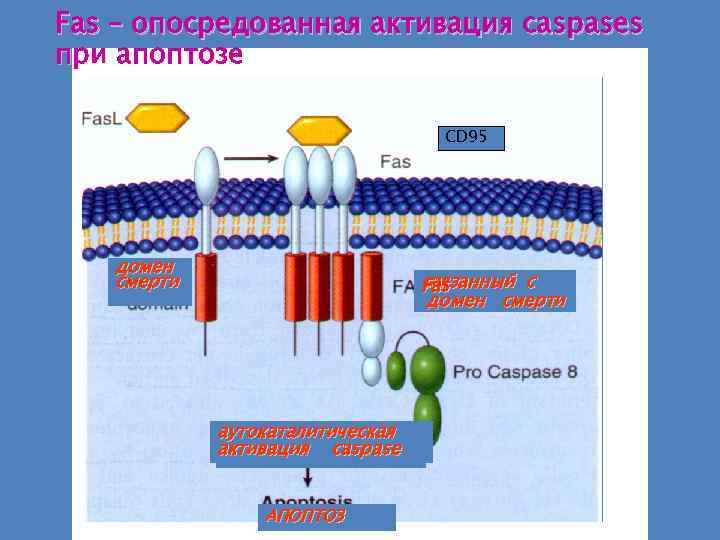
Fas – опосредованная активация caspases при апоптозе CD 95 домен смерти связанный с Fas домен смерти аутокаталитическая активация caspase АПОПТОЗ
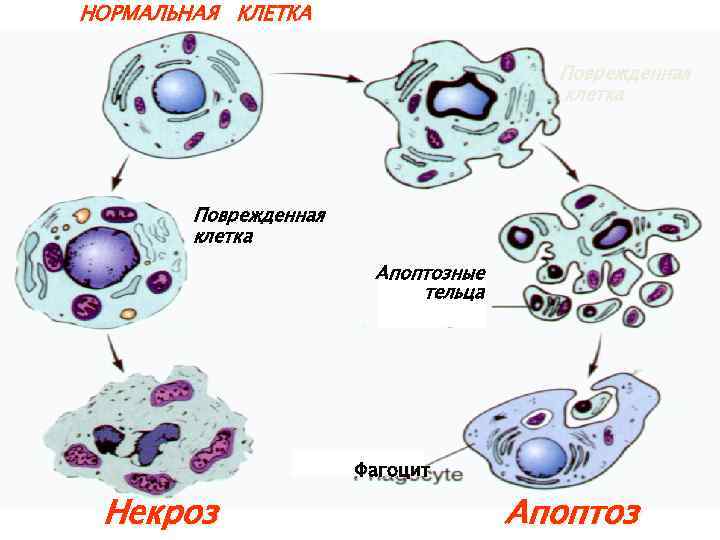
НОРМАЛЬНАЯ КЛЕТКА Поврежденная клетка Апоптозные тельца Фагоцит Некроз Апоптоз

Механизмы защиты клетки от повреждений • Активные (Активизация деятельности клетки и ее генетического аппарата, активизация антимутационных систем, активизация анаэробных процессов, активизация буферных систем крови и тканей, повышение экскреции метаболитов, гипертрофия и гиперплазия клеточных и субклеточных структур, регенерация). • Пассивные (Снижение функциональной активности поврежденной клетки, развитие гипотрофии, гипоплазии, атрофии клеточных структур, замещение поврежденных паренхиматозных структур соединительной тканью).

Принципы фармакологической коррекции нарушений функции клеток Принцип Обеспечить транспорт О 2 и субстратов метаболизма, увеличить ресинтез АТФ Copyright L. Gerasimova Цели Увеличить доставку О 2, глюкозы, жирных кислот и др. субстратов. Улучшить трансмембранный перенос О 2 и субстратов в клетки и митохондрии. Стимулировать ресинтез АТФ 37 Примеры групп препаратов О 2 Гюкозо-инсулиновая смесь Гиалуронидаза Карнитин Антигипоксанты: каротин, рибофлавины 2007

Принципы фармакологической коррекции нарушений функции клеток Принцип Уменьшить расход энергии в клетках Copyright L. Gerasimova Примеры групп препаратов Цели Снизить уровень функции 38 Адреноблокаторы Блокаторы фосфодиэстеразы Блокаторы протеинкиназ «Антагонисты» кальция Гипотермия 2007
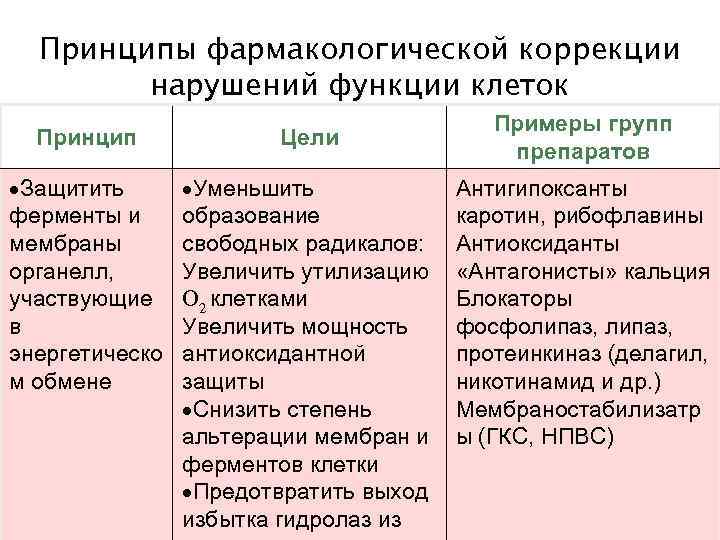
Принципы фармакологической коррекции нарушений функции клеток Принцип Цели Защитить ферменты и мембраны органелл, участвующие в энергетическо м обмене Уменьшить образование свободных радикалов: Увеличить утилизацию О 2 клетками Увеличить мощность антиоксидантной защиты Снизить степень альтерации мембран и ферментов клетки Предотвратить выход 39 избытка гидролаз из Copyright L. Gerasimova Примеры групп препаратов Антигипоксанты каротин, рибофлавины Антиоксиданты «Антагонисты» кальция Блокаторы фосфолипаз, протеинкиназ (делагил, никотинамид и др. ) Мембраностабилизатр ы (ГКС, НПВС) 2007

ДИСТРОФИИ

Дистрофии (от греч. dys – нарушение, расстройство, trophe – питаю) – это такие изменения состава клеточно-тканевых структур, которые обусловлены нарушениями в них процессов метаболизма (обмена веществ) и ведущие к накоплению или уменьшению тех или иных веществ (соединений), либо к появлению веществ, которые в норме не встречаются.

Классификация дистрофий 1. По времени развития различают: • наследственные, • приобретенные в пренатальный период (врожденные), • приобретенные в различные сроки постнатального периода. 2. По распространенности дистрофические процессы бывают местными и общими, которые могут быть в объеме: • отдельных клеток, • клеточных групп (в рамках структурно-функциональных единиц органа), • ткани, • органа, • многих тканей, органов, одной или нескольких физиологических и функциональных систем организма. 3. По структурному уровню дистрофии могут быть: • молекулярными (биохимический уровень), • субклеточными (электронно-микроскопический уровень), • клеточный (светооптический уровень), • сочетанный.

Классификация дистрофий 4. По преобладанию морфологических изменений в паренхиме или мезенхиме : • паренхиматозные, • мезенхимальные, • смешанные. 5. По преобладанию нарушений того или иного обмена веществ в паренхиме или мезенхиме различают дистрофии: • паренхиматозные: а) протеинозы или белковые – зернистая, вакуольная (гидропическая), гиалиново-капельная, роговая и др. ; б) липидозы или жировые; в) глюцидозы или углеводные; г) минералозы или минеральные; д) калькулезы, литиазы – образование камней; • мезенхимальные: а) протеинозы – гиалиноз (гомогенные белковые массы, содержащие особые гликопротеиды), амилоидоз – белковые массы, содержащие специфические гликопротеиды: комплекс глобулинов и полисахаридов), б) липидозы, в) глюцидозы. смешанные, к которым относятся: а) хромопротеидозы, б) нуклеопротеидозы, в) минералозы и др.
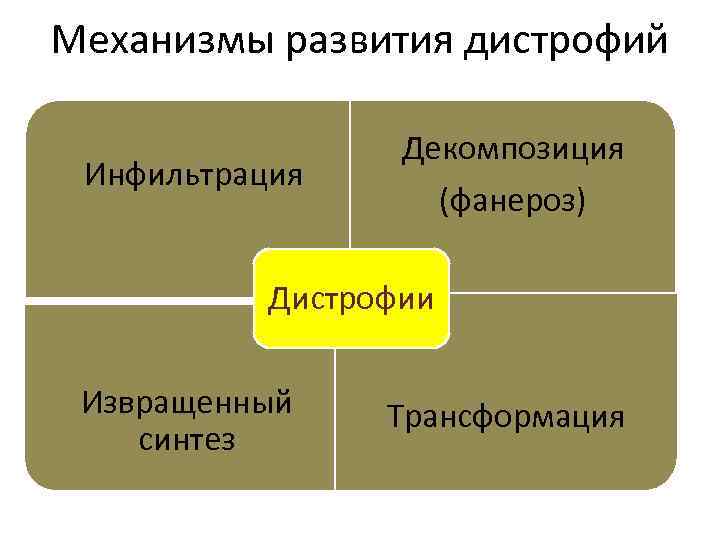
Механизмы развития дистрофий Инфильтрация Декомпозиция (фанероз) Дистрофии Извращенный синтез Трансформация

Приобретенные паренхиматозные белковые дистрофии. • • Зернистая Гиалиново-капельная Гидропическая Роговая
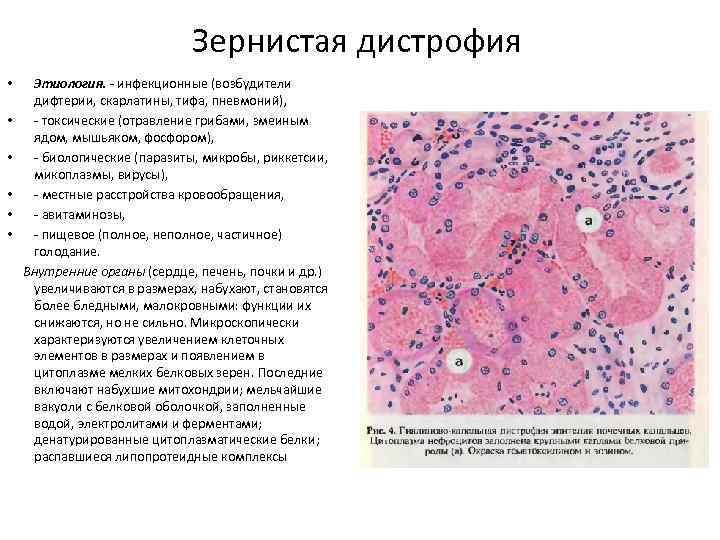
Зернистая дистрофия Этиология. - инфекционные (возбудители дифтерии, скарлатины, тифа, пневмоний), • - токсические (отравление грибами, змеиным ядом, мышьяком, фосфором), • - биологические (паразиты, микробы, риккетсии, микоплазмы, вирусы), • - местные расстройства кровообращения, • - авитаминозы, • - пищевое (полное, неполное, частичное) голодание. Внутренние органы (сердце, печень, почки и др. ) увеличиваются в размерах, набухают, становятся более бледными, малокровными: функции их снижаются, но не сильно. Микроскопически характеризуются увеличением клеточных элементов в размерах и появлением в цитоплазме мелких белковых зерен. Последние включают набухшие митохондрии; мельчайшие вакуоли с белковой оболочкой, заполненные водой, электролитами и ферментами; денатурированные цитоплазматические белки; распавшиеся липопротеидные комплексы •

Гиалиново-капельная дистрофия Этиология. Чаще всего этот вид дистрофии возникает под влиянием биологических (бактерий, вирусов), токсических и разнообразных длительно действующих флогогенных и других патогенных факторов. Патогенез. В механизмах развития данной дистрофии важное значение имеют: - глубокая денатурация белков цитоплазмы, - инфильтрация тела клетки грубодисперсными белками, - разрушение ультраструктур клеток и др. , - функция органа резко нарушена. Процесс необратим. Внешний вид органов (почек, печени, миокарда) изменен мало. Микроскопически характеризуется наличием в цитоплазме крупных гиалиново-подобных белковых капель, сливающихся между собой, и развитием деструкции ультраструктуры клеток
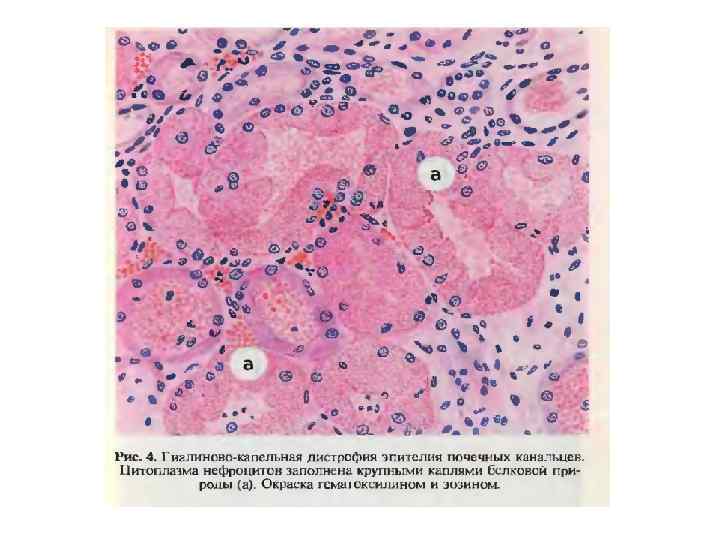

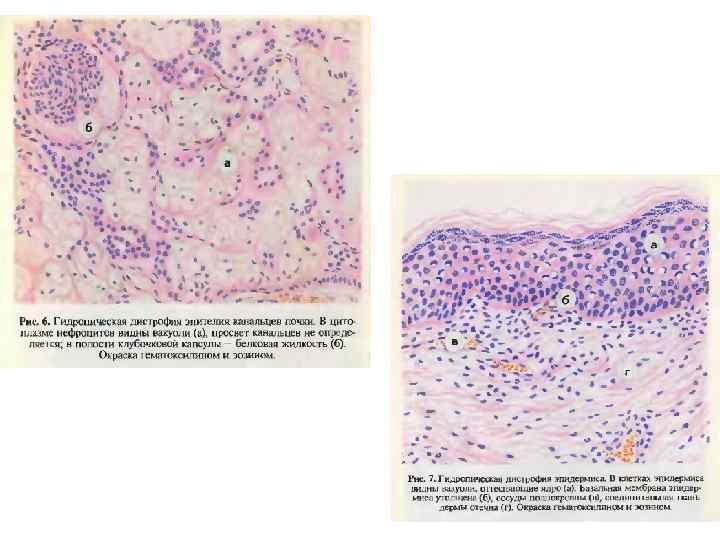
Гидропическая дистрофия Этиология. Среди этиологических факторов особое место в повреждениях клеток (кожи и слизистых) занимают термические факторы, возбудители натуральной оспы (эпидермис кожи), бешенства (нервные клетки) и других инфекций, а также голодание, особенно белковое, приводящее к кахексии, различные виды интоксикаций, авитаминозов и др. • Патогенез. Основными патогенетическими факторами являются: - нарушение белково-водно-электролитного обмена, - повышение проницаемости клеточных и субклеточных мембран, - распад липопротеидных комплексов, - активация гидролитических ферментов и др. • Внешний вид органа. Микроскопически характеризуется набуханием клеток и появлением в их цитоплазме (реже в ядре) сначала мелких, потом более крупных вакуолей, наполненных цитоплазматической жидкостью (вода, белки, ферменты). По мере увеличения воды вакуоли сливаются друг с другом, образуя пузырьки с оттесненным на периферию ядром, либо его лизисом или рексисом. Чаще наблюдается в эпителии кожи, почечных канальцах, клетках печени, мышц, коры надпочечников, нервных структур. •
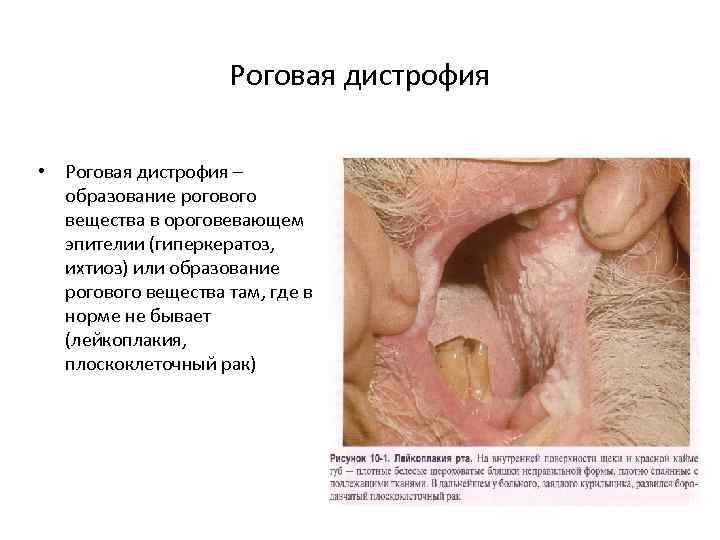
Роговая дистрофия • Роговая дистрофия – образование рогового вещества в ороговевающем эпителии (гиперкератоз, ихтиоз) или образование рогового вещества там, где в норме не бывает (лейкоплакия, плоскоклеточный рак)
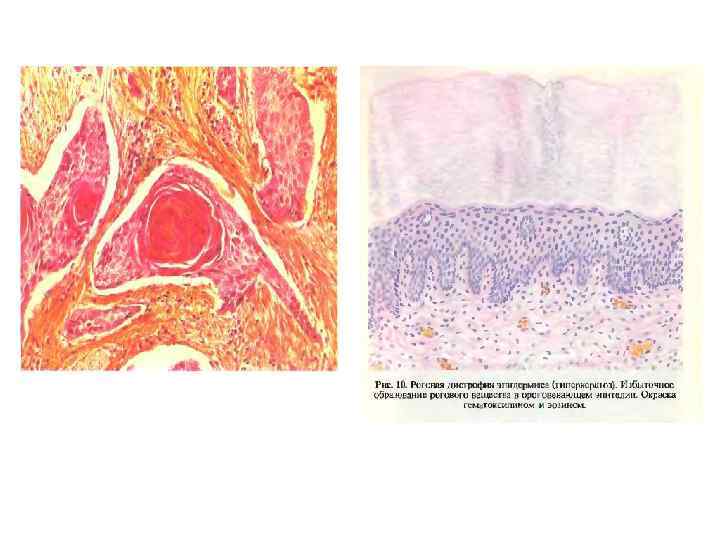
Плоскоклеточный рак с ороговением

Паренхиматозные липидозы • Паренхиматозные липидозы – накопление липидов в клетке разного состава. Чаще накапливается триглицерин. Общая причина – нарушение липидного обмена, деструкция внутриклеточных структур. Проявляется наличием мелких капель, крупных вакуолей, которые смещают на периферию ядро, и часто такая клетка имеет перстневидную форму. Причины жировой дистрофии • Отравление различными ядами (As, P, хлороформ), • Частный случай: токсины вирусов, микроорганизмов, • Гипоксия – приводит к сдвигу метаболизма, • Авитаминозы, • Белковое голодание. • Практическое значение имеет относительно трех органов. - печень, сердце, почки.

Жировая паренхиматозная дистрофия миокарда – «тигровое сердце» • При микроскопическом исследовании обнаруживается пылевидное или мелкокапельное ожирение • Исчерченность ( «тигровость» ) обусловлена преимущественным поражением кардиомиоцитов, расположенных у венозного отдела микроциркуляторного русла и/или кардиомиоцитов, находящихся в состоянии повышенной функциональной активности
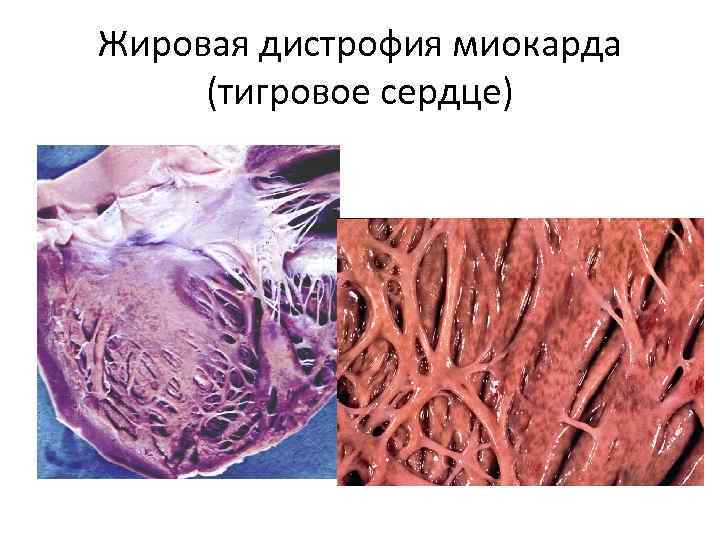
Жировая дистрофия миокарда (тигровое сердце)
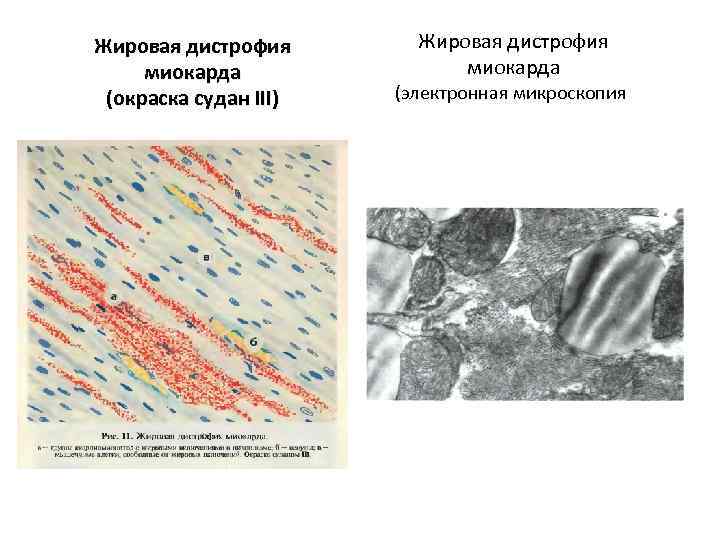
Жировая дистрофия миокарда (окраска судан III) Жировая дистрофия миокарда (электронная микроскопия)
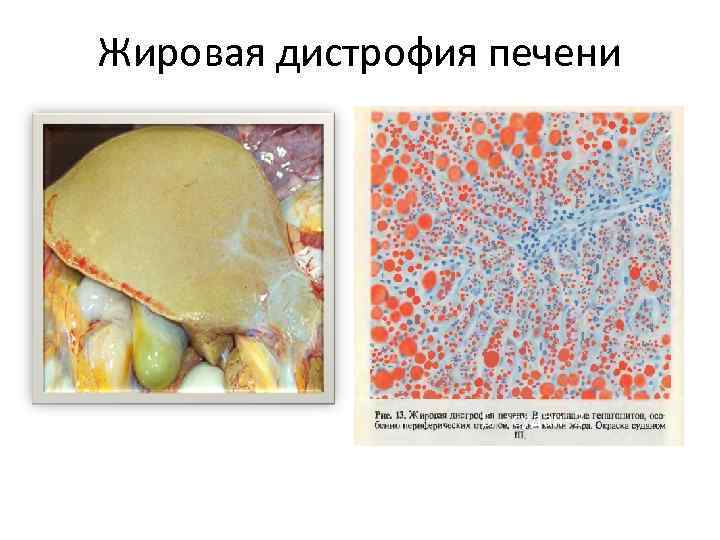
Жировая дистрофия печени Б – судан-3
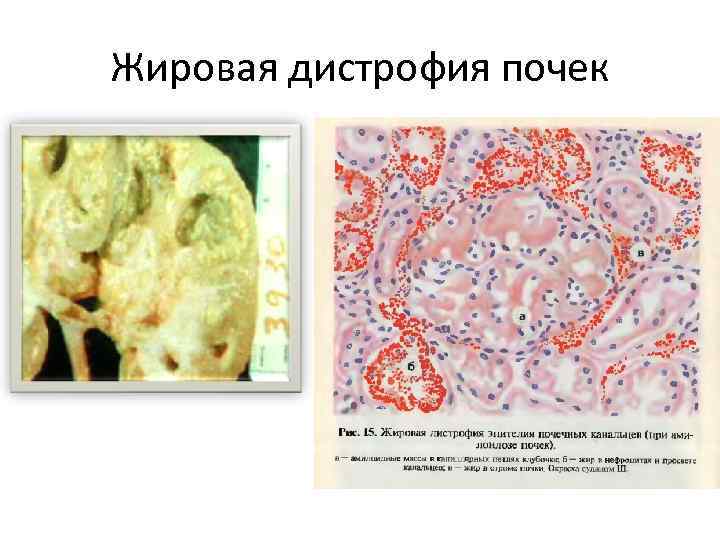
Жировая дистрофия почек

Паренхиматозные углеводные дистрофии • Связаны с нарушением обмена гликогена. Чаще встречается при сахарном диабете Характеризуется: 1. Гликогенной инфильтрацией эпителия канальцев 2. Жировой дистрофией в печени 3. Диабетической микро- и макроангиопатией • Связаны с нарушением обмена гликопротеидов (слизистая дистрофия при катаральном воспалении)
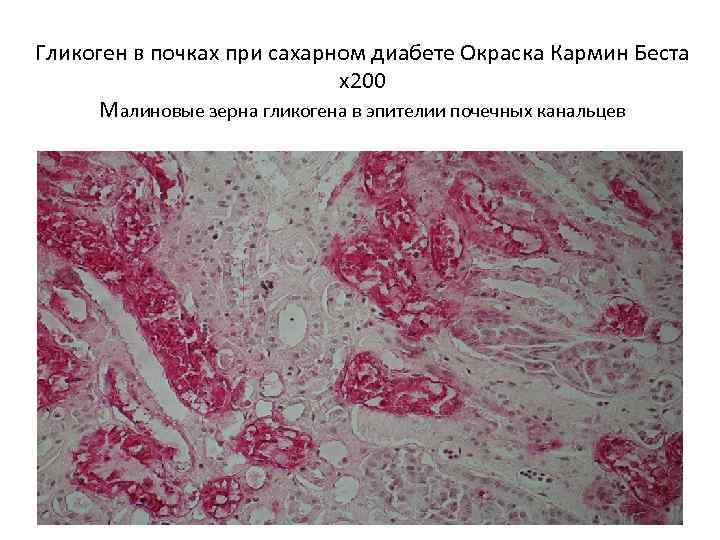
Гликоген в почках при сахарном диабете Окраска Кармин Беста х200 Малиновые зерна гликогена в эпителии почечных канальцев
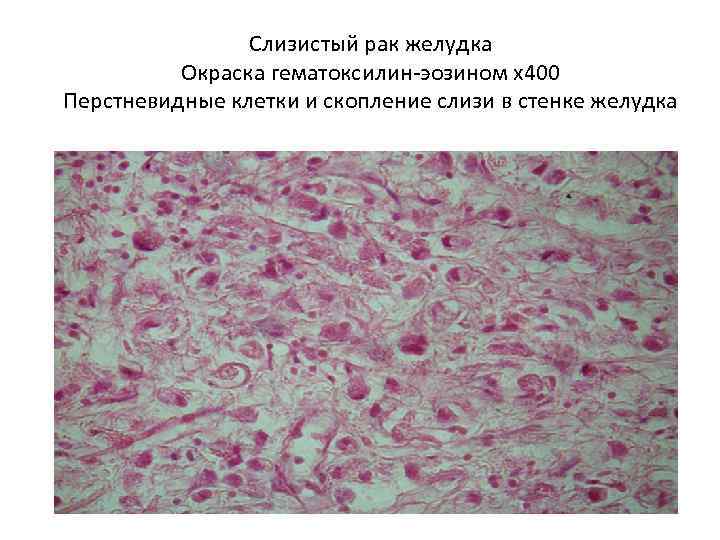
Слизистый рак желудка Окраска гематоксилин-эозином х400 Перстневидные клетки и скопление слизи в стенке желудка
Наследственные углеводные дистрофии • Болезнь Гирке – накопление гликогена в печени, в почках • Болезнь Помпе – гликоген в гладких и скелетных мышцах, миокарде
Минеральные дистрофии Известковые дистрофии (нарушение обмена кальция) I. II. III. Кальциноз Деминерализация Образование костей камней Известковые дистрофии
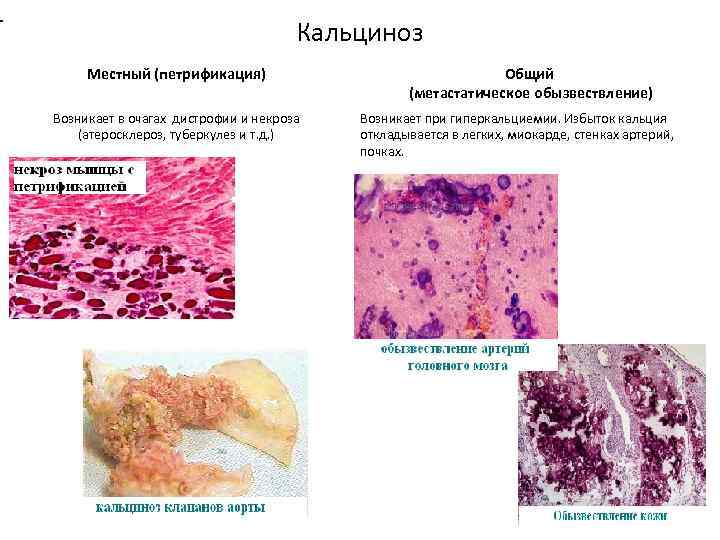
Кальциноз Местный (петрификация) Возникает в очагах дистрофии и некроза (атеросклероз, туберкулез и т. д. ) Общий (метастатическое обызвествление) Возникает при гиперкальциемии. Избыток кальция откладывается в легких, миокарде, стенках артерий, почках.
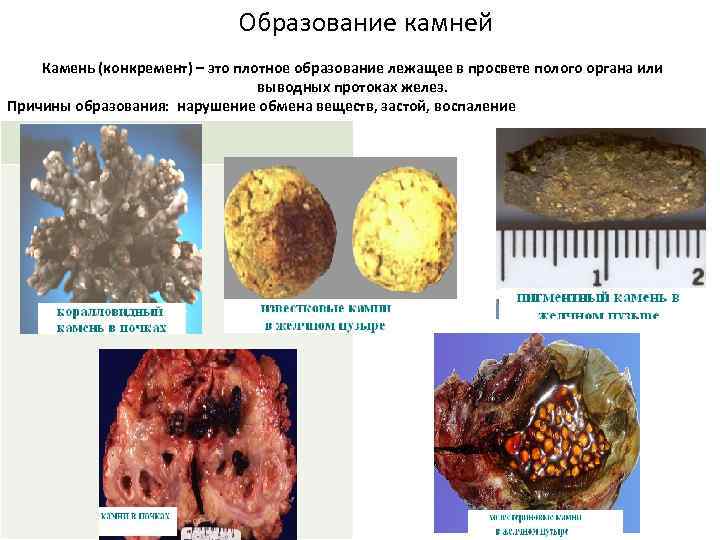
Образование камней Камень (конкремент) – это плотное образование лежащее в просвете полого органа или выводных протоках желез. Причины образования: нарушение обмена веществ, застой, воспаление
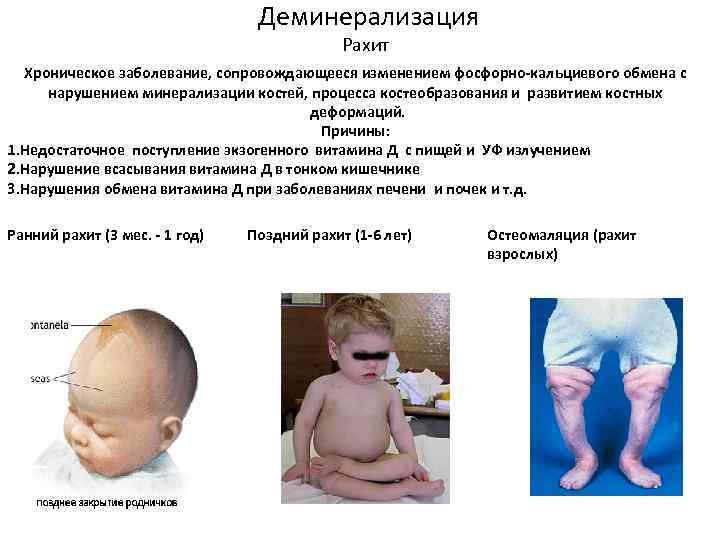
Деминерализация Рахит Хроническое заболевание, сопровождающееся изменением фосфорно-кальциевого обмена с нарушением минерализации костей, процесса костеобразования и развитием костных деформаций. Причины: 1. Недостаточное поступление экзогенного витамина Д с пищей и УФ излучением 2. Нарушение всасывания витамина Д в тонком кишечнике 3. Нарушения обмена витамина Д при заболеваниях печени и почек и т. д. Ранний рахит (3 мес. - 1 год) Поздний рахит (1 -6 лет) Остеомаляция (рахит взрослых)

Спасибо за внимание
патофизиология клетки.ppt