0.Совцов сергей александрович.ppt
- Количество слайдов: 67

Панкреатогенный сепсис Профессор С. А. Совцов Челябинск
«… Как нежащаяся пантера, уложила она голову в изгиб двенадцатиперстной кишки, распластала тонкое тело на аорте, убаюкивающей её мерными движениями, а чуть изогнутый хвост беспечно отклонила в ворота селезёнки затаившийся прекрасный хищник, который неожиданно при болезни может нанести непоправимый вред. » (А. А. Голубев, 1976)

Панкреатогенный сепсис • Это инфекционно-токсическое заболевание как системная воспалительная реакция организма, которое возникает при первичном очаге, локализующимся в поджелудочной железе и близ лежащей забрюшинной клетчатки при постоянном или периодическом поступлении микроорганизмов и их токсинов в кровоток из очага инфекции, что приводит к выбросу медиаторов в кровь (ФНО, ИЛ 1, ИЛ-6, ИЛ-8, ТАФ), несостоятельности факторов иммунной защиты, а отсюда к развитию генерализации инфекции, к дисфункции органов и систем.

Эпидемиология • В начале XXІ века в США регистрировалось более 700 000 случаев сепсиса, частота сепсиса в Европе составляет от 0, 6% до 12% в отделениях различного профиля. Септический шок развивается в 58% случаев тяжелого сепсиса и является одной из наиболее частых причин смерти реанимационных больных (по данным 2010 года стал 10 основной причиной смерти в США).

Эпидемиология • По результатам эпидемиологических исследований в Европе (EPISEPSIS) и Австралии (ANZICS) в 2013 году частота сепсиса в индустриальных странах составила 50 -100 случаев на 100 тыс. населения. Точных эпидемиологических данных о сепсисе в Российской Федерации нет, что отчасти объясняется невозможностью его качественной регистрации в большинстве лечебных учреждений.

Статистика • За 10 лет количество госпитализированных больных о. панкреатитом увеличилось в 2 раза, из них с панкреонекрозом в 2, 5 раза - с 24% до 40%. • Среди больных с острым панкреатитом пациенты с панкреонекрозом составляют 30, 5%. (С. А. Совцов и соавт, 2008 ).

Статистика • Около 20 – 25% пациентов с о. панкреатитом имеют тяжелую форму болезни, часто приводящие к полиорганной недостаточности и смерти. (Н. Веger c соавт. 2013). • Количество субтотальных и тотальных поражений pancreas при некротических формах острого панкреатита за последние 10 лет увеличилось с 43% до 65%.

основные пути инфицирования очагов панкреонекроза • Экзогенный путь –это инфицирование представителями госпитальной микрофлоры (Pseudomonas spp. , Klebsiella, Enterobakter и т. д. ) происходит при несвоевременном хирургическом вмешате льстве, когда микроорганизмы проникают в зону стерильного некроза "из вне" - через открытые дренажные системы и тампоны.

основные пути инфицирования очагов панкреонекроза • Эндогенный путь- это инфицирование аутоинфекцией в очаги стерильного некроза. Наиболее вероятны два пути инфицирования: транслокация кишечной микрофлоры в мезентеральные лимфатические узлы с последующей с гематогенной диссеминацией и трансдуктальная инвазия из билиарного тракта с инфицированной желчью

Причины развития панкреатогенного сепсиса • неадекватная санация; • несвоевременное хирургическое и интенсивное лечение; • неправильно выбранная тактика ведения больного; • нерациональная антибактериальная терапия

Предрапологающие факторы • Многофокусностью очагов некротического процесса, невозможностью их одномоментного удаления или санации в оптимальные для больного сроки; • Вовлечение в процесс в очагах гнойной секвестрации стенок сосудов с развитием тромбозов и тромбоваскулитов; • Близкое соседство резервуаров условно – патогенной инфекции (желчевыделительная система, толстая кишка);

Предрапологающие факторы • Благоприятные условия экзогенного инфицирования в связи с применением дренажей и тампонов; • Дополнительное инфицирование очагов секвестрации при возникновении дигестивных свищей; • Высокая протеолитическая активность в очагах гнойной секвестрации, спрсобствующая прорыву в кровь и генерализации инфекта; • Многократность санирующих вмешательств, каждое из которых сопровождается разрушением защитных барьеров и генерализацией инфекции (бактериемией).

Сепсис • у 30% сепсис как правило развивается на фоне выраженного SIRS; • у 70% пациентов клиниколабораторные его проявления укладываются в CARS (анергия) или • сочетание проявлений SIRS и. CARS.

Острый панкреатит • Нами в последние 5 лет наблюдались 647 больных острым панкреатитом, из них у 79% была интерстициальная форма заболевания. У остальных больных отмечено развитие панкреонекроза. В 102 наблюдениях развились различные формы гнойных осложнений панкреатита в виде абсцессов поджелудочной железы и окружающей клетчатки, гнойного бурсооментита, диффузных флегмон забрюшинных клетчаточных пространств.

Панкреатогенный сепсис • У 34 больного диагностировано септическое состояние, которое устанавливали на основании имеющихся нарушений функций органов, гипоперфузии и гипотензии. Нарушение перфузии сопровождалось, как правило, выраженным лактацидозом, олигоурией и острыми нарушениями психического статуса.
Септический шок • При развитии септического шока развивалась выраженная гипотензия( снижение среднего артериального давления более чем на 40 мм. рт. ст. от исходного), не смотря на адекватную инфузионную терапию.

Для диагностики сепсиса • нет ни одного достоверного критерия, только по совокупности клинической картины и всех методов исследования может быть поставлен этот диагноз

диагностические критерии панкреатогенного сепсиса • Наличие очага инфекции: инфицированный панкреонекроз, панкреатогенный абсцесс, фибринозно-гнойный перитонит, флегмона забрюшинной клетчатки. • Наличие 3 -4 признаков SIRS. • Лабораторные: белок менее 60 г/л, гемоглобин менее 90 г/л, эритроциты менее 3 х 1012/л, СОЭ более 40 мм/час.

диагностические критерии панкреатогенного сепсиса • Иммунологические: лимфопения, значительное снижение Т-лимфоцитов, высокий уровень ЦИК, значительное повышение С-реактивного белка, повышение Jg. А. • Положительные бактериологические посевы крови. • Наличие вторичных метастатических очагов. • Увеличение селезенки, доказанное по УЗИ или КТ. • Развитие ДВС — синдрома.

Определение лабораторных маркеров системного воспаления • К ним относятся повышение сывороточного уровня: • прокальцитонина, • С-реактивного белка, • фактора некроза опухоли (TNF), • интерлейкинов (IL -1, IL -6, IL -8, IL -10).

Метаболическая дисфункция • • p. H<7, 3 • • Дефицит оснований <5, 0 мк/л • • Лактат плазмы в 1, 5 раза выше нормы

Лабораторная диагностика • • • Целесообразно: Иммунный статус; Прокальцитонин С-реактивный белок (численная методика) Почасовой диурез

Диагностика Аппаратные методы – УЗИ органов брюшной полости – УЗИ сердца (патология клапанов) – R-графия груди
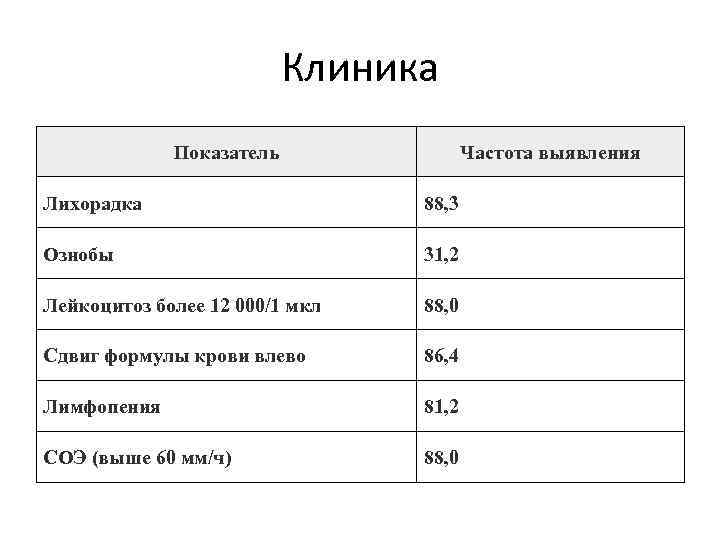
Клиника Показатель Частота выявления Лихорадка 88, 3 Ознобы 31, 2 Лейкоцитоз более 12 000/1 мкл 88, 0 Сдвиг формулы крови влево 86, 4 Лимфопения 81, 2 СОЭ (выше 60 мм/ч) 88, 0
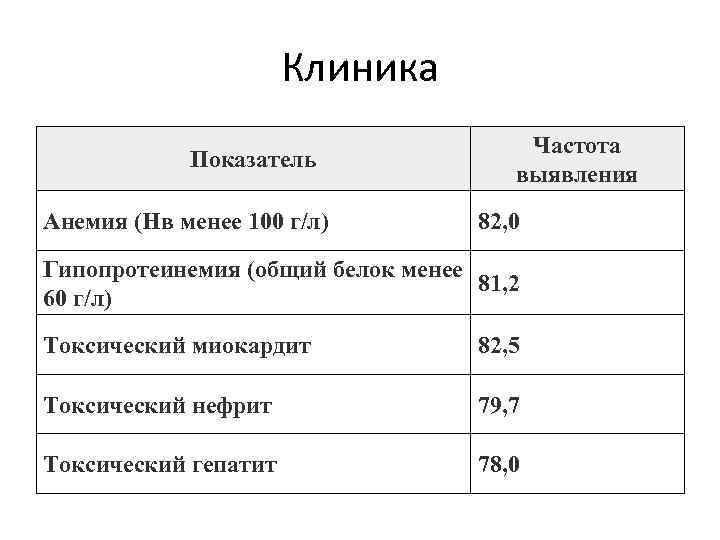
Клиника Показатель Анемия (Нв менее 100 г/л) Частота выявления 82, 0 Гипопротеинемия (общий белок менее 81, 2 60 г/л) Токсический миокардит 82, 5 Токсический нефрит 79, 7 Токсический гепатит 78, 0

Диагноз панкреатогенного сепсиса устанавливается при: • 1. При упорно сохраняющемся синдроме системного воспалительного ответа (SIRS) у больных с санированными гнойнонекротическими очагами; • 2. При наличии множественных гнойновоспалительных процессов в различных анатомических областях (гнойнонекротический парапанкреатит плюс пиемические очаги в брюшинной полости, печени, легких, мягких тканях и пр. );

Диагноз панкреатогенного сепсиса устанавливается при: • 3. При выраженной реакции селезенки (спленомегалия) и персистенции анемии (несмотря на адекватную заместительную терапию) у длительно лихорадящих больных при наличии гнойно-некротического парапанкреатита; • 4. При прогрессирующей анергии (CARS), имеющей как клиническое (субфебрильная лихорадка, резкое замедление или отсутствие заживления ран, патология грануляционной ткани, интеркуррентная инфекция и пр. ), так и иммунологическое проявление (снижение абсолютного числа лимфоцитов и субпопуляций CD 3, CD 4, CD 8, CD 20);

Диагноз • Иммунологическое исследование у таких больных выявляет лимфопению со значительным снижением доли «активных» Т – лимфоцитов, высокий уровень ЦИК со снижением активности комплемента, факторов неспецифической защиты и эффективности фагоцитоза, а также признаки присоединившейся вирусной инфекции. Окончательным доказательством наличия сепсиса является выявление бактериемии при повторных посевах крови.

Диагноз • основывается на некоторых клинических критериях: лихорадочной реакции с профузными потами, сохраняющейся после казалось бы адекватной хирургической санации гнойных очагов; появлении вторичных метастатических очагов инфекции вне брюшной полости; вялом течении раневого процесса; увеличении селезенки; присоединением множественных органных поражений.
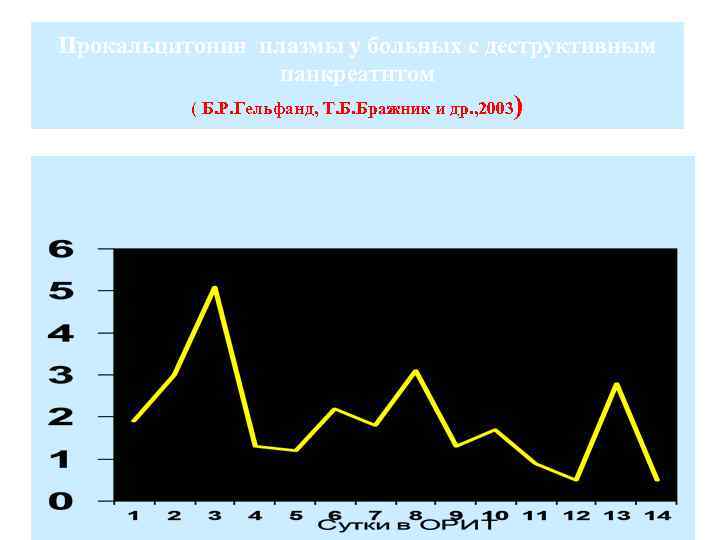
Прокальцитонин плазмы у больных с деструктивным панкреатитом ( Б. Р. Гельфанд, Т. Б. Бражник и др. , 2003)

Панкреатогенный сепсис • Является наглядым примером эндогенной назокомиальной инфекции у хирургических больных
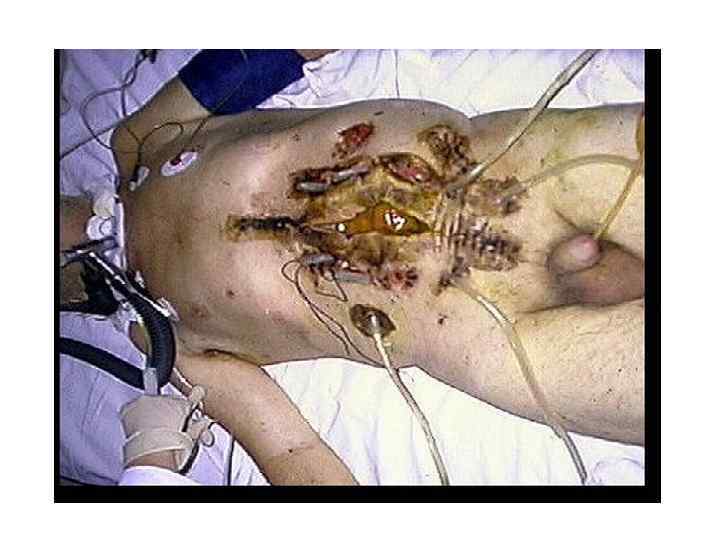

Бактериальная мозаика панкреатогенного сепсиса • нозокомиальные штаммы возбудителей, отличающиеся высокой и поливалентной резистентностью к антибиотикам: коагулазонегативные стафилококки, гемолитические стрептококки, псевдомонады, а также неспорообразующие анаэробы и дрожжеподобные грибы.

Особенности гнойно-септических осложнений при деструктивном панкреатите Спектр возбудителей расширяется. Постоянно изменяется уровень лекарственной устойчивости микроорганизмов. С одной стороны, всё чаще встречаются штаммы, образующие ферменты, разрушающие антибиотики • с другой -нередко развивается иммунологическая резистентность организма, которая способствует развитию гнойно-септических осложнений и усугубляет их течение. • •

Панкреатогенный сепсис • При деструктивном панкреатите первично процесс всегда носит абактериальный характер. При отказе от проведения полномасштабного комплекса консервативной терапии, включая раннее назначение антибактериальных препаратов - при отечной среднетяжелой форме заболевания и в фазе стерильного панкреонекроза происходит неконтролируемый эффект транслокации кишечной флоры в систему воротной вены с массивным эндогенным инфицированием пораженной ткани поджелудочной железы и забрюшинных клетчаточных пространств. На фоне тяжелой ферментемии и возникает классическое септическое состояние.

Антибактериальная терапия • Необходимо использовать максимальные и субмаксимальные дозы препаратов, проводить достаточно длительные курсы лечения, при смене препарата учитывать клинический эффект его применения, для оценки ее эффективности использовать повторный бактериологический контроль, включать в лечение препараты интерферона для подавления вирусной инфекции. Необходима направленная иммунотерапия, на первом этапе пассивная, затем разнонаправленная для воздействия на разные звенья иммунитета.

Лечение панкреатогенного сепсиса: • Подавление инфекции в септическом очаге и за его пределами; • Иммунокоррекция и иммуномодуляция; • Управляемая гипокоагуляция и подавление избыточной протеолитической активности крови; • Активная детоксикация; • Нормализация энергетического и пластического обеспечения организма больного.

Абсолютно показанные компоненты интенсивной терапии сепсиса Антибактериальные препараты иммунные препараты крови плазмозамещающие и кристаллоидные растворы • метаболическая коррекция • • • Препараты для общей анестезии (операции, перевязки) • 6 -10 недель • 1 -2 недели • 6 -8 недель • 4 -6 недель(2 -3 литра/сутки) • 6 -8 недель( 3 -4 тыс. ккалл/сутки) • 10 -15 раз и более

Относительно показанные препараты при лечении сепсиса • Гормональные • Гемо-энеросорбция • кардиальная и сосудистая терапия • коррекция гемокоагуляции, диуретики, витамины и др. • 7 -10 дней • 3 -4 сеанса • 3 -4 недели
Современные принципы лечения панкреатогенного сепсиса • 1. Своевременная и полноценная хирургическая санация септических очагов (прежде всего, забрюшинных гнойников) и устранение источников генерализации инфекции.

Современные принципы лечения панкреатогенного сепсиса • 2. Рационально спланированная и длительная (многоступенчатая) антибактериальная терапия, направленная на эрадикацию возбудителя из очагов инфекции. При проведении антибактериальной терапии наиболее часто используется комбинация аминогликозида III поколения с беталактамным антибиотиком или фторхинолонами с присоединением антианаэробного препарата имидазолового ряда. В ряде клинических ситуаций целесообразно проведение монотерапии с использованием новых высокоэффективных антибиотиков широкого спектра действия – карбапенемов, цефалоспоринов III-IV поколения, защищенных пенициллинов, гликопептидов (ванкомицин) либо в комбинации одного из этих препаратов с антианаэробным средством.

Современные принципы лечения панкреатогенного сепсиса • назоинтестинальная интубация и дренирование тонкой кишки, кишечный лаваж корригирующими растворами, энтеросорбция, внутрикишечная терапия (нутрицевтики, цитопротекторы, антиоксиданты, пребиотики) и селективная деконтаминация кишечника. • Ликвидация синдрома эндогенной интоксикации и коррекция нарушений гомеостаза (стимуляция и реабилитация естественных детоксицирующих систем и биологических барьеров, устранение тканевой гипоксии, коррекция системного и тканевого метаболизма, активная элиминация токсических продуктов из внутренних сред организма, в том числе с использованием методов вне органной детоксикации).

Плазмоферез • Показанияк плазмообмену: • Выраженные явления эндотоксикоза • Тяжелая форма острой печеночной недостаточности • Проводили в режиме плазмообмена, реоиммунокоррекции в программном режиме с интервалом 1 сутки от 3 до 6 сеансов с объемом эксфузии 50% объема циркулирующей плазмы за 1 сеанс.

Панкреатогенный сепсис • Больным с проявлением сердечной недостаточности выполняли плазмофильтрацию на аппарате «Гемос» и плазмофильтрах ПФМ-800 как наиболее щадящую процедуру.

Недостатки плазмофереза • Он агрессивно воздействует на внутренние среды организма, активируя гуморальные и клеточные реакции, способствуют возникновению коагулопатии. • При сепсисе, на фоне явлений гиповолемии, всегда страдает гемодинамика, что резко ограничивает их использование
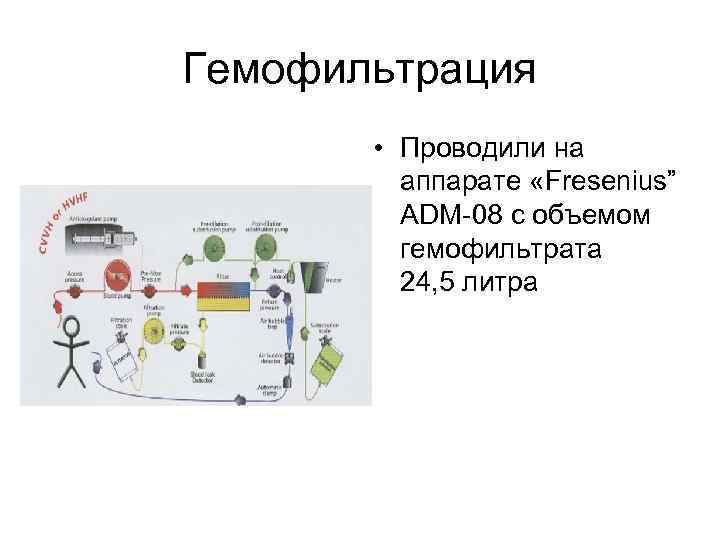
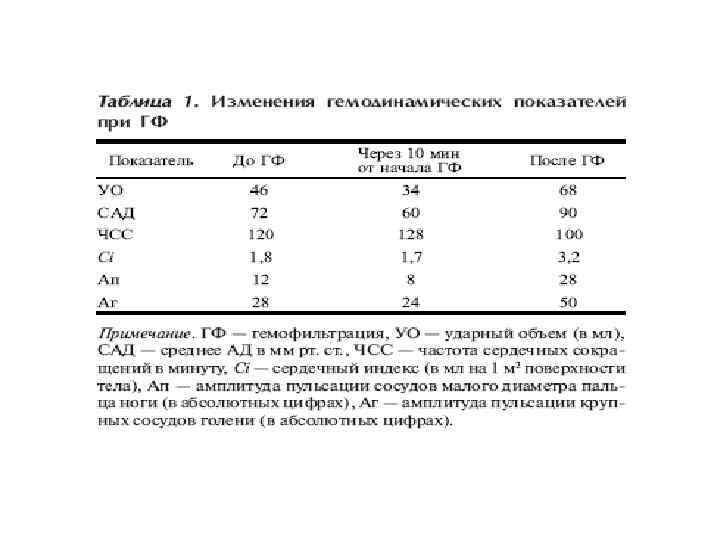
Гемофильтрация • Проводили на аппарате «Fresenius” ADM-08 c объемом гемофильтрата 24, 5 литра

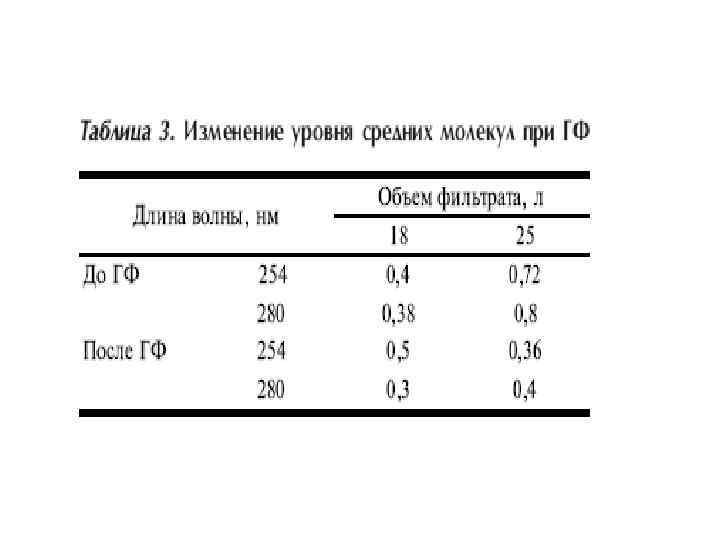
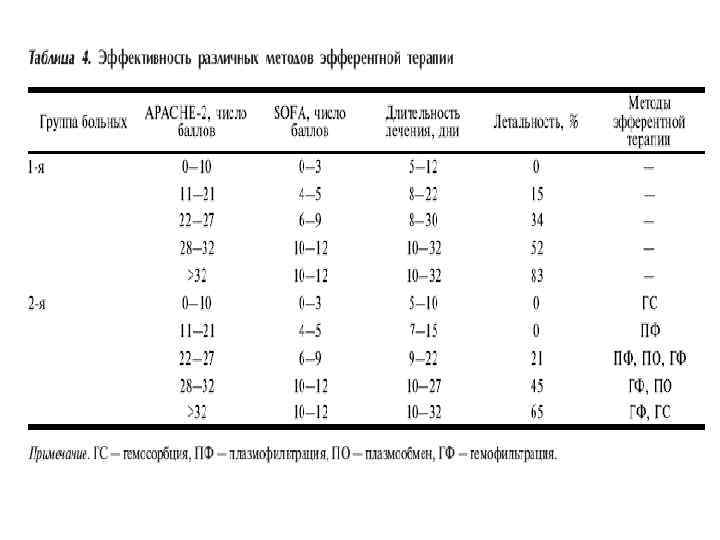

Эффективность гемофильтрации • Анализ биохимических показателей крови при гемофильтрации в режиме ультрафильтрации показал снижение концентрации мочевины на 32%, креатинина на 22% исходного уровня. • Скорость их фильтрации зависит от скорости кровотока через фильтр-чем выше скорость, тем больше концентрация мочевины в ультрафильтрате. • Скорость кровотока через фильтр не меняет концентрацию билирубина в крови.

Клиническая эффективность гемофильтрации • При исходной гипергидратации при полиорганной недостаточности(отек мозга, легких, тканевые отеки) надежно корригируется волемические растройства • Уменьшаются явления энцефалопатии, быстро восстанавливается сознание, функция кишечника(возможность проведения зондового и энтерального питания), купировались явления респираторного дистресс-синдрома

Недостаточная концентрация препаратов в очаге инфекции может быть обусловлена • применения экстракорпоральной детоксикации; • дефицитом транспортных белков (альбумина); • нарушением системного и регионарного кровотока, особенно в очаге инфекции; • формированием защитных "ловушек" для микробов (микротромбы, белковые отложения, микроагрегаты клеток)

Лечение панкреатогенного сепсиса • Полноценное обеспечение энергетических и пластических потребностей организма (метаболическая терапия) достигается путем проведения сбалансированного по основным нутритивным компонентам парентерального и раннего энтерального зондового питания с добавлением анаболических стероидов или их аналогов. • Иммуноориентированная терапия, направленная на реставрацию иммунореактивности организма и устранение дисбаланса цитокинов

Метаболические растройства при остром панкреатите. • • Выраженная азотурия Гипо – диспротеинемия Умеренная азотемия Дегидратация с последующей задержкой натрия и воды, гиперкалиурия.

МЕТАБОЛИЧЕСКИЕ ИЗМЕНЕНИЯ ПРИ ОСТРОМ ПАНКРЕАТИТЕ • Под влиянием воспалительного стресса и боли основной обмен повышается. • Если о. панкреатит осложняется сепсисом, то 80% пациентов находятся в гиперметаболическом состоянии. • Основной обмен при этом повышается в 1, 4 1, 5 раза.

Нельзя противопоставлять ПП и ЭП у больных с панкреатитом. ПП и ЭП являются единым целым в комплексной НП.
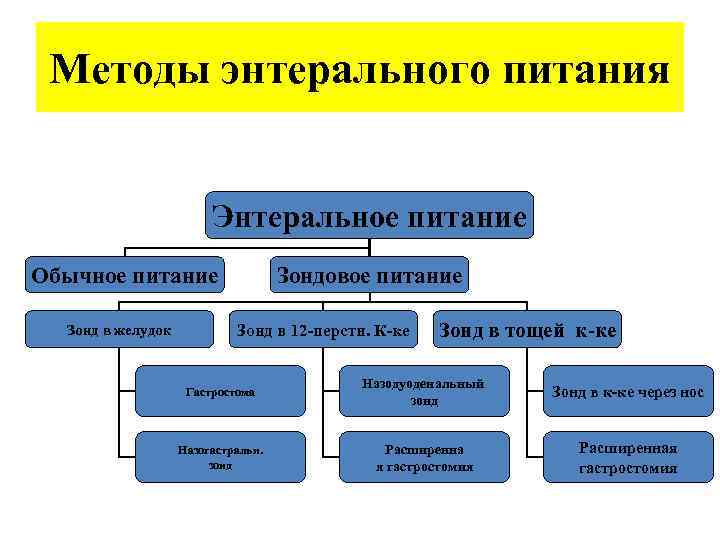
Методы энтерального питания Энтеральное питание Обычное питание Зонд в желудок Зондовое питание Зонд в 12 -перстн. К-ке Зонд в тощей к-ке Гастростома Назодуоденальный зонд Зонд в к-ке через нос Назогастральн. зонд Расширенна я гастростомия Расширенная гастростомия

МОНОМЕРНЫЕ ПС • Глюкозо-электролитные растворы, приближающиеся по составу к тонкокишечному химусу; • Позволяют восстановить гомеостазирующую функцию тонкой кишки, играющую центральную роль в патогенезе развития ПОН при критических состояниях; • Скорость введения мономерных смесей должна составлять 50 -100 мл/ч.

Энтерально-зондовое питание при остром панкреатите • Следует использовать диеты с минимальным стимулирующим эффектом панкреатической секреции. • Темп и концентрацию вводимых в кишку смесей следует увеличивать постепенно. • Первоначально вводятся электролитные и электролитноуглеводные растворы, далее углеводно-аминокислотные препараты, затем полноценные эмульсионные смеси для ЭЗП с добавлением панкреатических ферментов.

Профилактика абдоминального дискомфорта при ЭП • Кончик питательного зонда устанавливается в активной зоне кишки ( 30 -45 см за связкой Трейца); • Введение ЭПС должно быть равномерным в течение суток; • Скорость введения ЭПС в кишку при полном восстановлении ее моторно-пропульсивной функции – должна составлять 170 мл/ч

Результаты лечения • При отечной форме панкреатита никто не умер • при панкреонекрозе послеоперационная летальность составила 22, 6%, достигая при развитии септических осложнений показателя в 56, 1%. • Таким образом, видно, что высокие цифры послеоперационной летальности обусловлены развитием панкреатогенного сепсиса.

Летальность при сепсисе • составляет от 30 до 80%, в среднем колеблясь около 40%. Отмечается тенденция лишь к незначительному снижению летальности в последние десятилетия, несмотря на разработку новых методов диагностики и лечения этой патологии.

• Неутешительными являются и отдаленные результаты лечения сепсиса: прогнозируемая продолжительность жизни после перенесенного сепсиса в среднем составляет 5 лет, а 8 - летняя выживаемость после успешного лечения составляет всего 18%.

Инфицированный панкреонекроз • Это диктует необходимость подхода к инфицированному панкреонекрозу как к тяжелому септическому состоянию с ранним применением комплекса противосептического лечения, включая адекватную антибактериальную терапию для профилактики и лечения эндогенной инфекции на фоне раннего дренирования гнойных очагов.

0.Совцов сергей александрович.ppt