42a9c7d15be4e987d2344b5b0df9461e.ppt
- Количество слайдов: 44
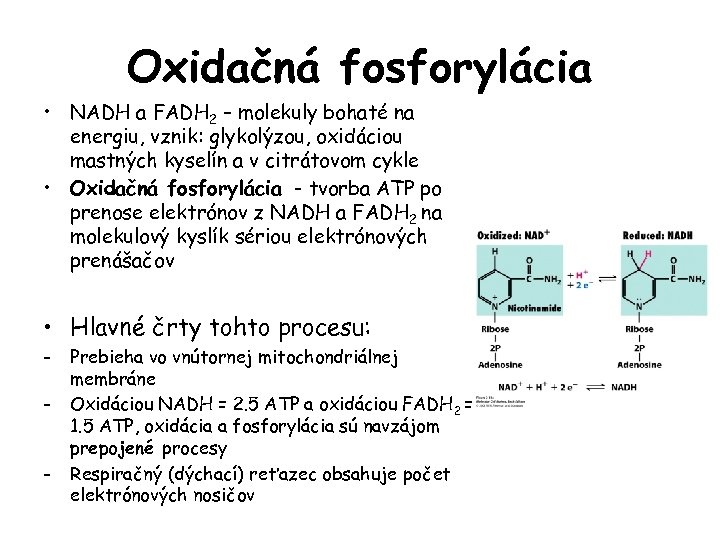 Oxidačná fosforylácia • NADH a FADH 2 – molekuly bohaté na energiu, vznik: glykolýzou, oxidáciou mastných kyselín a v citrátovom cykle • Oxidačná fosforylácia - tvorba ATP po prenose elektrónov z NADH a FADH 2 na molekulový kyslík sériou elektrónových prenášačov • Hlavné črty tohto procesu: - Prebieha vo vnútornej mitochondriálnej membráne Oxidáciou NADH = 2. 5 ATP a oxidáciou FADH 2 = 1. 5 ATP, oxidácia a fosforylácia sú navzájom prepojené procesy Respiračný (dýchací) reťazec obsahuje počet elektrónových nosičov
Oxidačná fosforylácia • NADH a FADH 2 – molekuly bohaté na energiu, vznik: glykolýzou, oxidáciou mastných kyselín a v citrátovom cykle • Oxidačná fosforylácia - tvorba ATP po prenose elektrónov z NADH a FADH 2 na molekulový kyslík sériou elektrónových prenášačov • Hlavné črty tohto procesu: - Prebieha vo vnútornej mitochondriálnej membráne Oxidáciou NADH = 2. 5 ATP a oxidáciou FADH 2 = 1. 5 ATP, oxidácia a fosforylácia sú navzájom prepojené procesy Respiračný (dýchací) reťazec obsahuje počet elektrónových nosičov
 • Protónmotívna sila (proton – motive force) je výsledok pôsobenia p. H gradientu a transmembránového elektrického potenciálu Oxidácia a fosforylácia sú spojené protónovým gradientom cez vnútornú mitochondriálnu membránu
• Protónmotívna sila (proton – motive force) je výsledok pôsobenia p. H gradientu a transmembránového elektrického potenciálu Oxidácia a fosforylácia sú spojené protónovým gradientom cez vnútornú mitochondriálnu membránu
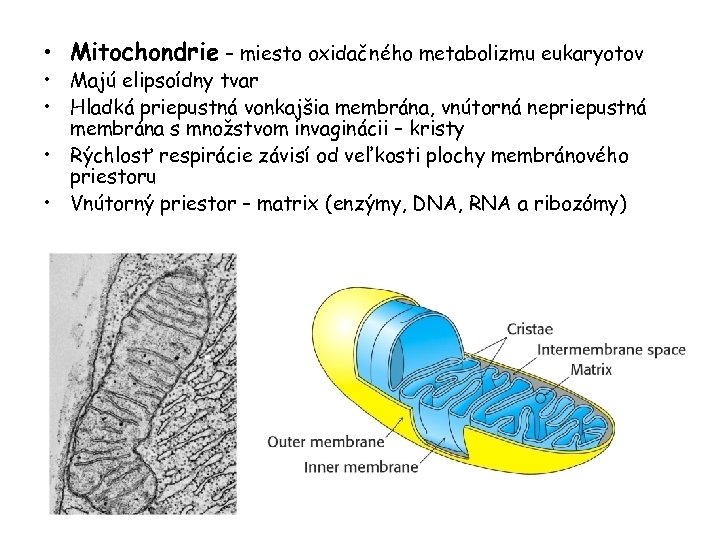 • Mitochondrie – miesto oxidačného metabolizmu eukaryotov • Majú elipsoídny tvar • Hladká priepustná vonkajšia membrána, vnútorná nepriepustná membrána s množstvom invaginácii – kristy • Rýchlosť respirácie závisí od veľkosti plochy membránového priestoru • Vnútorný priestor – matrix (enzýmy, DNA, RNA a ribozómy)
• Mitochondrie – miesto oxidačného metabolizmu eukaryotov • Majú elipsoídny tvar • Hladká priepustná vonkajšia membrána, vnútorná nepriepustná membrána s množstvom invaginácii – kristy • Rýchlosť respirácie závisí od veľkosti plochy membránového priestoru • Vnútorný priestor – matrix (enzýmy, DNA, RNA a ribozómy)
 Termodynamika transportu elektrónov • Termodynamickú účinnosť môžeme odhadnúť zo znalosti štandardných redoxných potenciálov • Oxidačno-redukčný potenciál Eo – zmena štandardnej voľnej Gibbsovej energie, ktorá je úmerná tendencii prijímať alebo odovzdávať elektróny v oxidačnoredukčných reakciách ΔGo'=-n. FΔEo‚ Eo'=Eo' (akceptor) - Eo' (donor) F – Faradajová konštanta = 96, 48 k. J/mol. V n=počet elektrónov
Termodynamika transportu elektrónov • Termodynamickú účinnosť môžeme odhadnúť zo znalosti štandardných redoxných potenciálov • Oxidačno-redukčný potenciál Eo – zmena štandardnej voľnej Gibbsovej energie, ktorá je úmerná tendencii prijímať alebo odovzdávať elektróny v oxidačnoredukčných reakciách ΔGo'=-n. FΔEo‚ Eo'=Eo' (akceptor) - Eo' (donor) F – Faradajová konštanta = 96, 48 k. J/mol. V n=počet elektrónov
 Electron transfer potential of NADH and FADH 2 -> Phosphoryl transfer potential of ATP A 1. 14 –Volt potential difference between NADH and O 2 drives electron transport and favors formation of a proton gradient NADH 1. 14 Volt O 2
Electron transfer potential of NADH and FADH 2 -> Phosphoryl transfer potential of ATP A 1. 14 –Volt potential difference between NADH and O 2 drives electron transport and favors formation of a proton gradient NADH 1. 14 Volt O 2

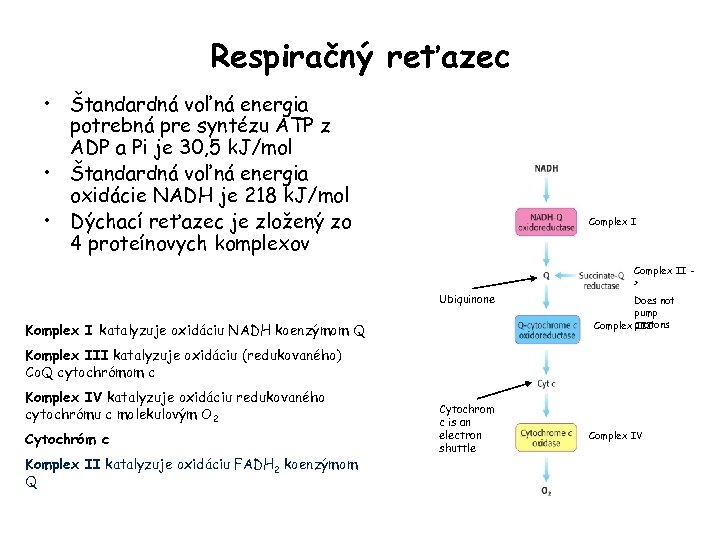 Respiračný reťazec • Štandardná voľná energia potrebná pre syntézu ATP z ADP a Pi je 30, 5 k. J/mol • Štandardná voľná energia oxidácie NADH je 218 k. J/mol • Dýchací reťazec je zložený zo 4 proteínovych komplexov Complex II > Ubiquinone Komplex I katalyzuje oxidáciu NADH koenzýmom Q Does not pump Complex protons III Komplex III katalyzuje oxidáciu (redukovaného) Co. Q cytochrómom c Komplex IV katalyzuje oxidáciu redukovaného cytochrómu c molekulovým O 2 Cytochróm c Komplex II katalyzuje oxidáciu FADH 2 koenzýmom Q Cytochrom c is an electron shuttle Complex IV
Respiračný reťazec • Štandardná voľná energia potrebná pre syntézu ATP z ADP a Pi je 30, 5 k. J/mol • Štandardná voľná energia oxidácie NADH je 218 k. J/mol • Dýchací reťazec je zložený zo 4 proteínovych komplexov Complex II > Ubiquinone Komplex I katalyzuje oxidáciu NADH koenzýmom Q Does not pump Complex protons III Komplex III katalyzuje oxidáciu (redukovaného) Co. Q cytochrómom c Komplex IV katalyzuje oxidáciu redukovaného cytochrómu c molekulovým O 2 Cytochróm c Komplex II katalyzuje oxidáciu FADH 2 koenzýmom Q Cytochrom c is an electron shuttle Complex IV
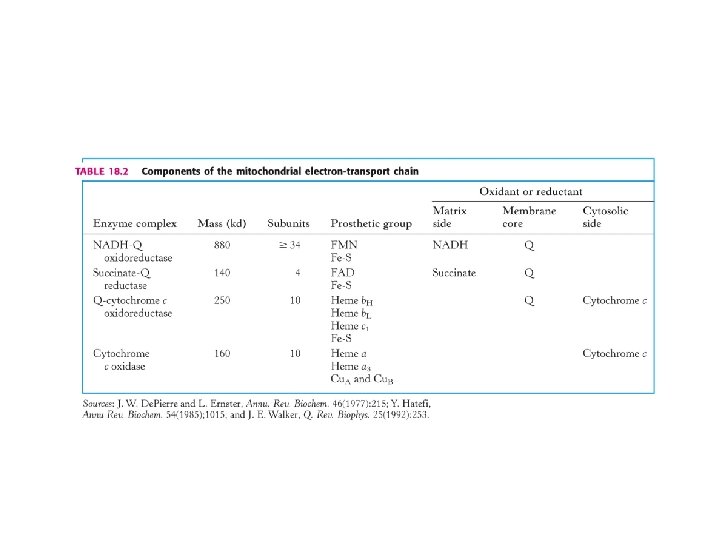
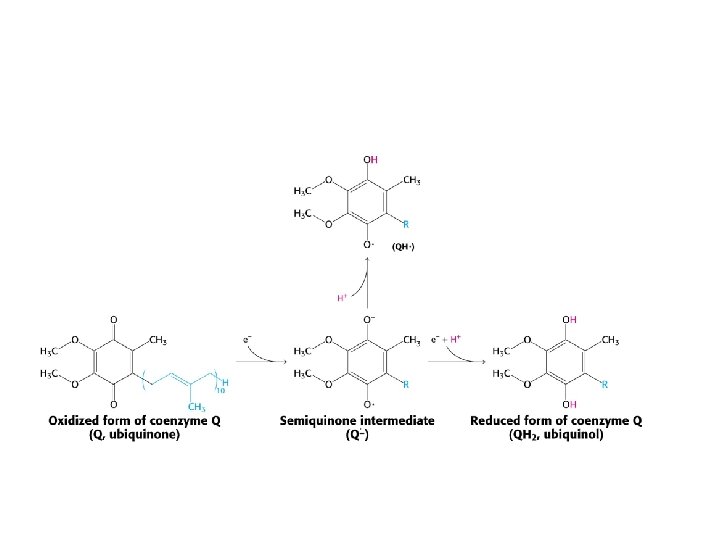
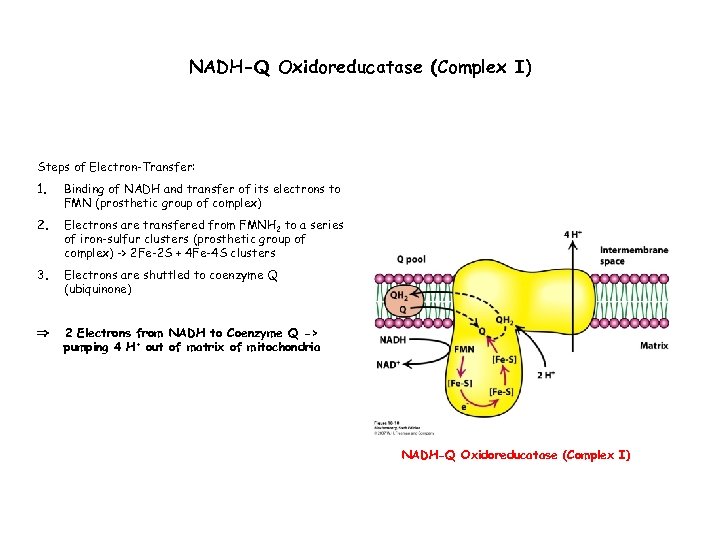 NADH-Q Oxidoreducatase (Complex I) Steps of Electron-Transfer: 1. Binding of NADH and transfer of its electrons to FMN (prosthetic group of complex) 2. Electrons are transfered from FMNH 2 to a series of iron-sulfur clusters (prosthetic group of complex) -> 2 Fe-2 S + 4 Fe-4 S clusters 3. Electrons are shuttled to coenzyme Q (ubiquinone) 2 Electrons from NADH to Coenzyme Q -> pumping 4 H+ out of matrix of mitochondria NADH-Q Oxidoreducatase (Complex I)
NADH-Q Oxidoreducatase (Complex I) Steps of Electron-Transfer: 1. Binding of NADH and transfer of its electrons to FMN (prosthetic group of complex) 2. Electrons are transfered from FMNH 2 to a series of iron-sulfur clusters (prosthetic group of complex) -> 2 Fe-2 S + 4 Fe-4 S clusters 3. Electrons are shuttled to coenzyme Q (ubiquinone) 2 Electrons from NADH to Coenzyme Q -> pumping 4 H+ out of matrix of mitochondria NADH-Q Oxidoreducatase (Complex I)
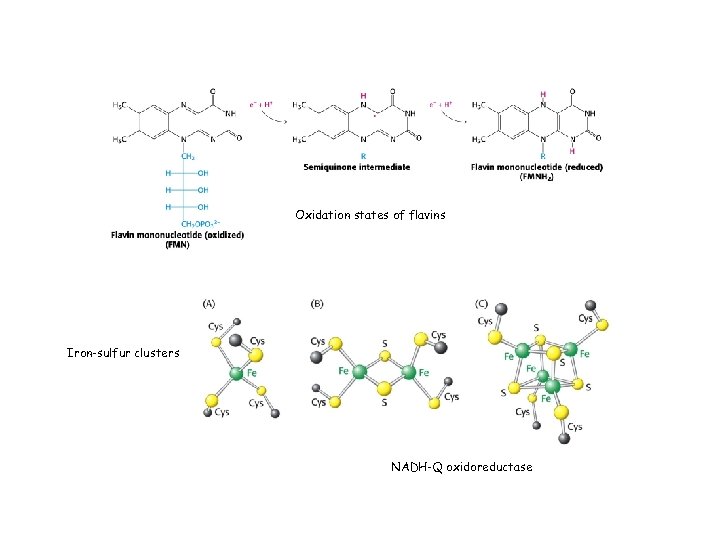 Oxidation states of flavins Iron-sulfur clusters NADH-Q oxidoreductase
Oxidation states of flavins Iron-sulfur clusters NADH-Q oxidoreductase
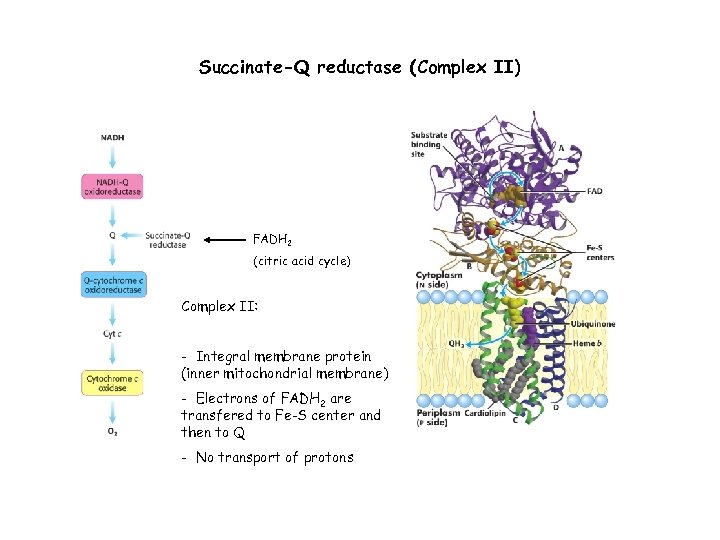 Succinate-Q reductase (Complex II) FADH 2 (citric acid cycle) Complex II: - Integral membrane protein (inner mitochondrial membrane) - Electrons of FADH 2 are transfered to Fe-S center and then to Q - No transport of protons
Succinate-Q reductase (Complex II) FADH 2 (citric acid cycle) Complex II: - Integral membrane protein (inner mitochondrial membrane) - Electrons of FADH 2 are transfered to Fe-S center and then to Q - No transport of protons
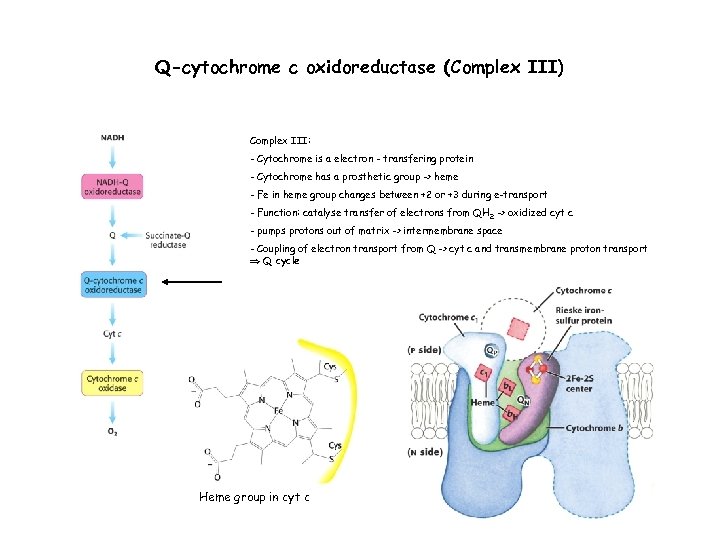 Q-cytochrome c oxidoreductase (Complex III) Complex III: - Cytochrome is a electron - transfering protein - Cytochrome has a prosthetic group -> heme - Fe in heme group changes between +2 or +3 during e-transport - Function: catalyse transfer of electrons from QH 2 -> oxidized cyt c - pumps protons out of matrix -> intermembrane space - Coupling of electron transport from Q -> cyt c and transmembrane proton transport Q cycle Heme group in cyt c
Q-cytochrome c oxidoreductase (Complex III) Complex III: - Cytochrome is a electron - transfering protein - Cytochrome has a prosthetic group -> heme - Fe in heme group changes between +2 or +3 during e-transport - Function: catalyse transfer of electrons from QH 2 -> oxidized cyt c - pumps protons out of matrix -> intermembrane space - Coupling of electron transport from Q -> cyt c and transmembrane proton transport Q cycle Heme group in cyt c
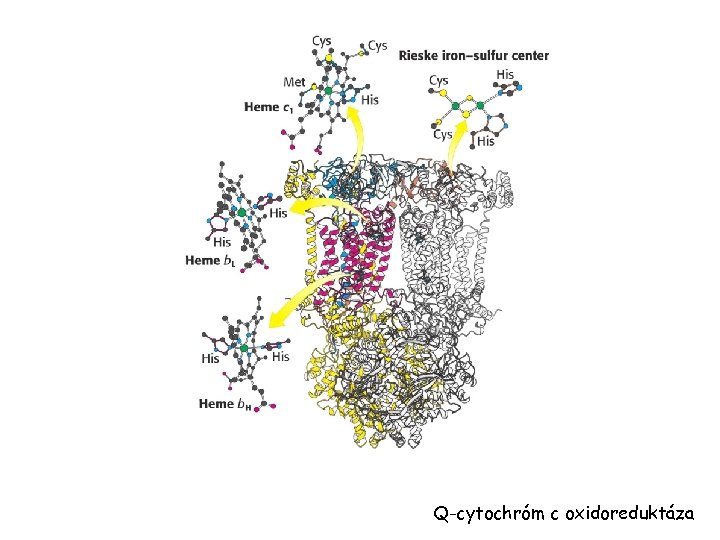 Q-cytochróm c oxidoreduktáza
Q-cytochróm c oxidoreduktáza
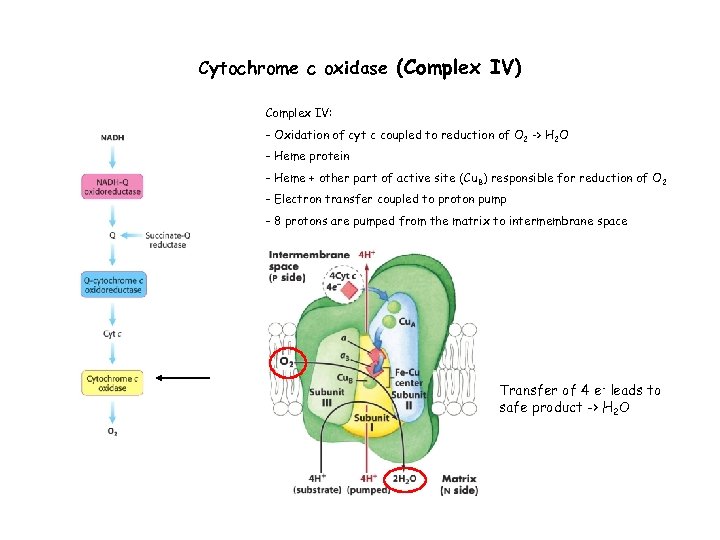 Cytochrome c oxidase (Complex IV) Complex IV: - Oxidation of cyt c coupled to reduction of O 2 -> H 2 O - Heme protein - Heme + other part of active site (Cu B) responsible for reduction of O 2 - Electron transfer coupled to proton pump - 8 protons are pumped from the matrix to intermembrane space Transfer of 4 e- leads to safe product -> H 2 O
Cytochrome c oxidase (Complex IV) Complex IV: - Oxidation of cyt c coupled to reduction of O 2 -> H 2 O - Heme protein - Heme + other part of active site (Cu B) responsible for reduction of O 2 - Electron transfer coupled to proton pump - 8 protons are pumped from the matrix to intermembrane space Transfer of 4 e- leads to safe product -> H 2 O
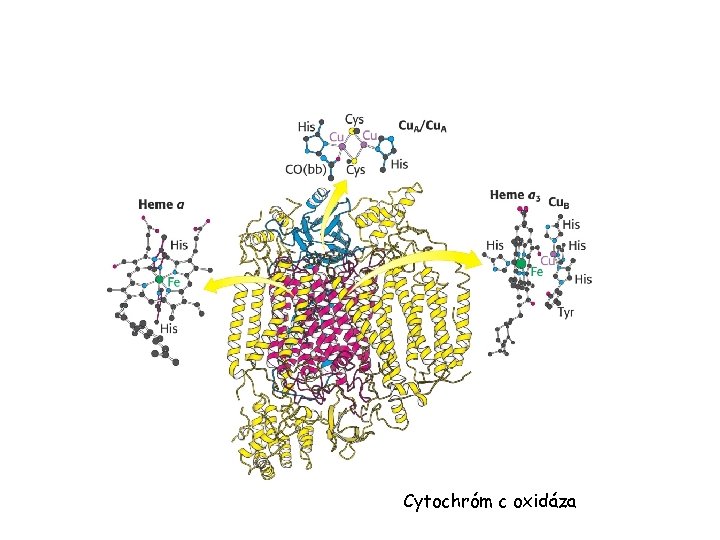 Cytochróm c oxidáza
Cytochróm c oxidáza
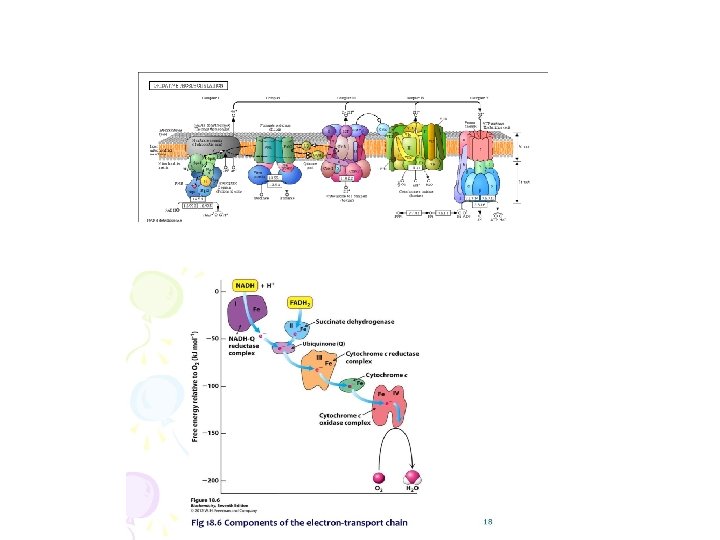
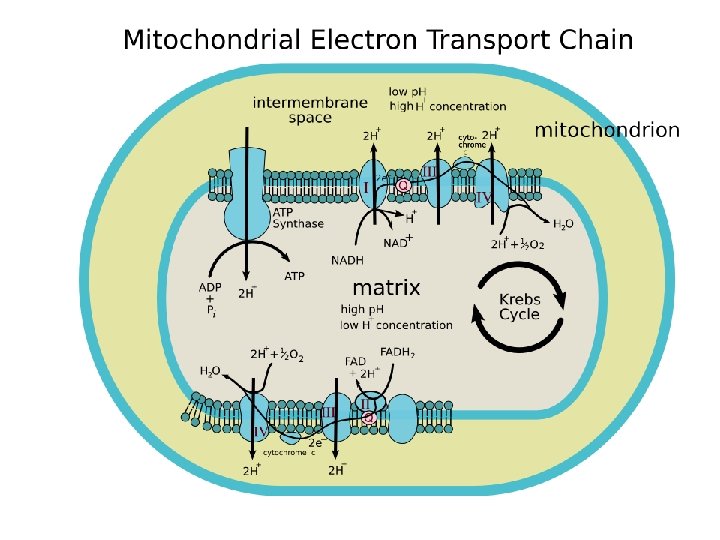
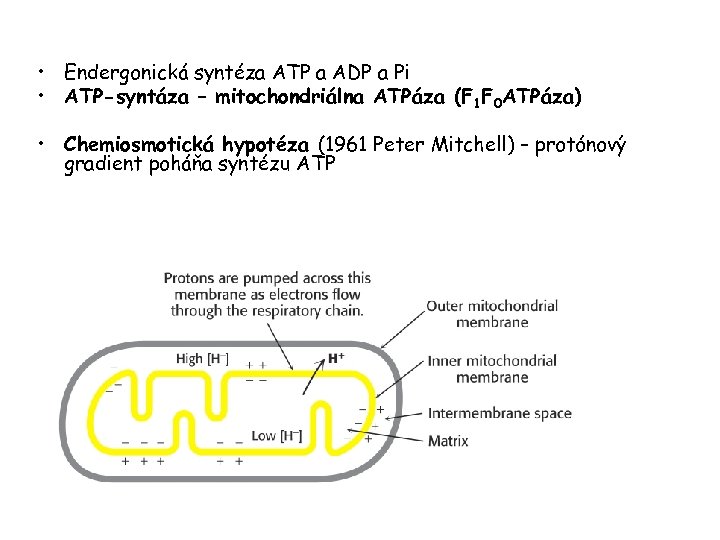 • Endergonická syntéza ATP a ADP a Pi • ATP-syntáza – mitochondriálna ATPáza (F 1 F 0 ATPáza) • Chemiosmotická hypotéza (1961 Peter Mitchell) – protónový gradient poháňa syntézu ATP
• Endergonická syntéza ATP a ADP a Pi • ATP-syntáza – mitochondriálna ATPáza (F 1 F 0 ATPáza) • Chemiosmotická hypotéza (1961 Peter Mitchell) – protónový gradient poháňa syntézu ATP
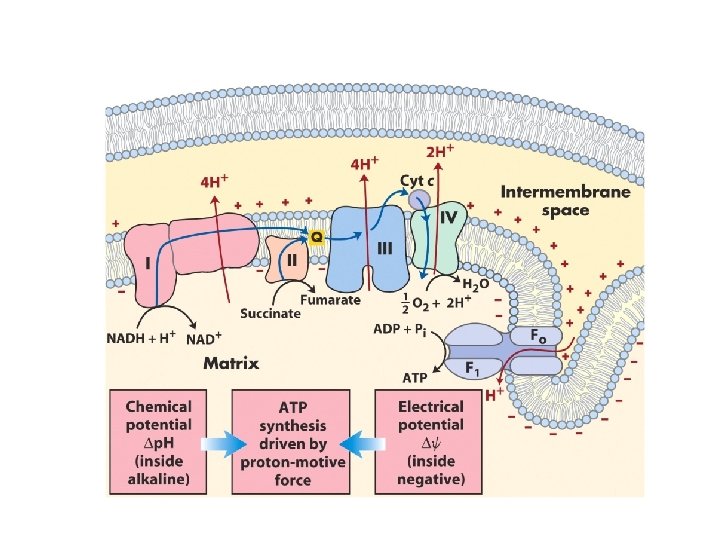
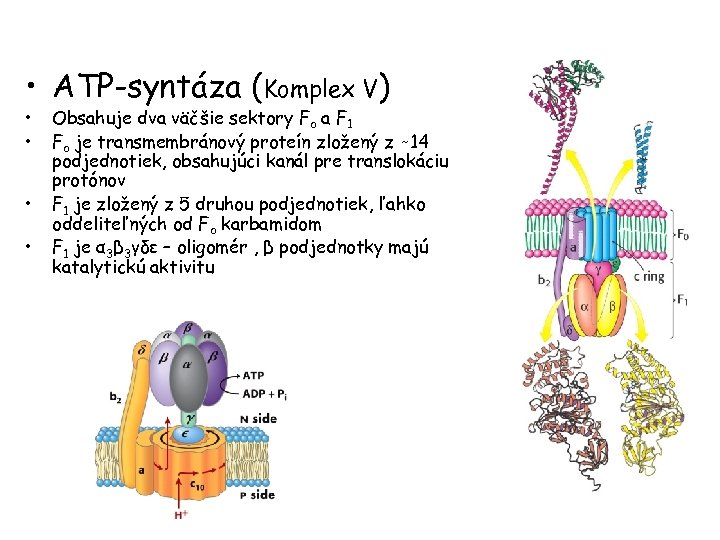 • ATP-syntáza (Komplex V) • • Obsahuje dva väčšie sektory Fo a F 1 Fo je transmembránový proteín zložený z 14 podjednotiek, obsahujúci kanál pre translokáciu protónov F 1 je zložený z 5 druhou podjednotiek, ľahko oddeliteľných od Fo karbamidom F 1 je α 3β 3γδε – oligomér , β podjednotky majú katalytickú aktivitu
• ATP-syntáza (Komplex V) • • Obsahuje dva väčšie sektory Fo a F 1 Fo je transmembránový proteín zložený z 14 podjednotiek, obsahujúci kanál pre translokáciu protónov F 1 je zložený z 5 druhou podjednotiek, ľahko oddeliteľných od Fo karbamidom F 1 je α 3β 3γδε – oligomér , β podjednotky majú katalytickú aktivitu
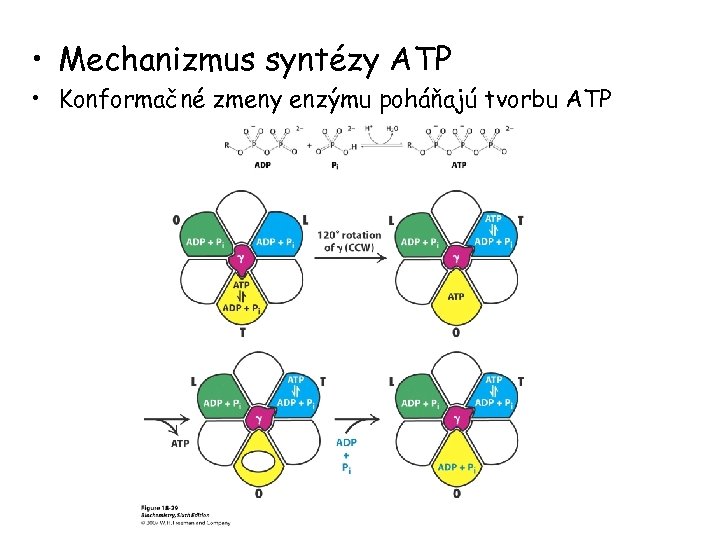 • Mechanizmus syntézy ATP • Konformačné zmeny enzýmu poháňajú tvorbu ATP
• Mechanizmus syntézy ATP • Konformačné zmeny enzýmu poháňajú tvorbu ATP
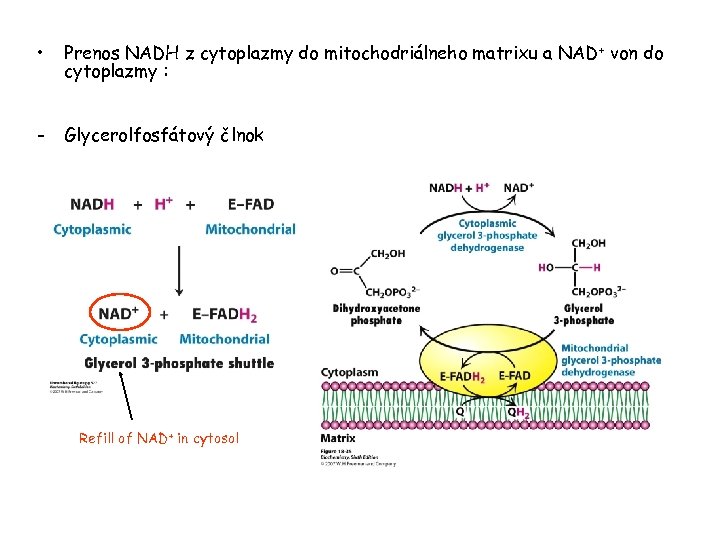 • Prenos NADH z cytoplazmy do mitochodriálneho matrixu a NAD + von do cytoplazmy : - Glycerolfosfátový člnok Refill of NAD+ in cytosol
• Prenos NADH z cytoplazmy do mitochodriálneho matrixu a NAD + von do cytoplazmy : - Glycerolfosfátový člnok Refill of NAD+ in cytosol
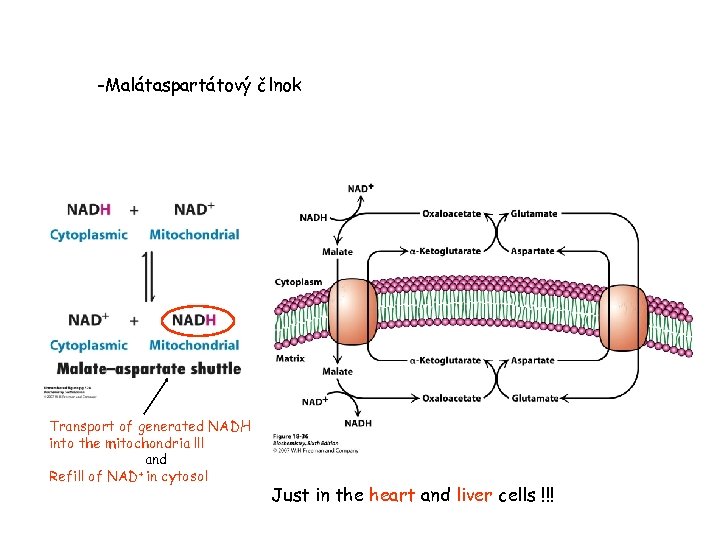 -Malátaspartátový člnok Transport of generated NADH into the mitochondria !!! and + in cytosol Refill of NAD Just in the heart and liver cells !!!
-Malátaspartátový člnok Transport of generated NADH into the mitochondria !!! and + in cytosol Refill of NAD Just in the heart and liver cells !!!
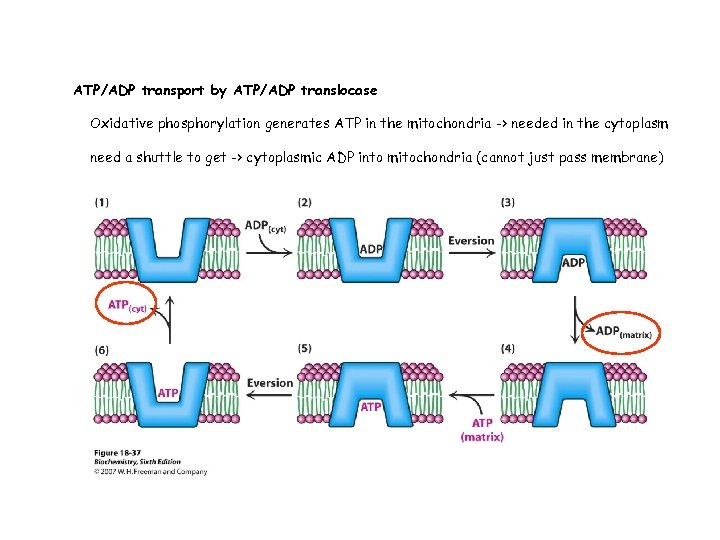 ATP/ADP transport by ATP/ADP translocase Oxidative phosphorylation generates ATP in the mitochondria -> needed in the cytoplasm need a shuttle to get -> cytoplasmic ADP into mitochondria (cannot just pass membrane)
ATP/ADP transport by ATP/ADP translocase Oxidative phosphorylation generates ATP in the mitochondria -> needed in the cytoplasm need a shuttle to get -> cytoplasmic ADP into mitochondria (cannot just pass membrane)
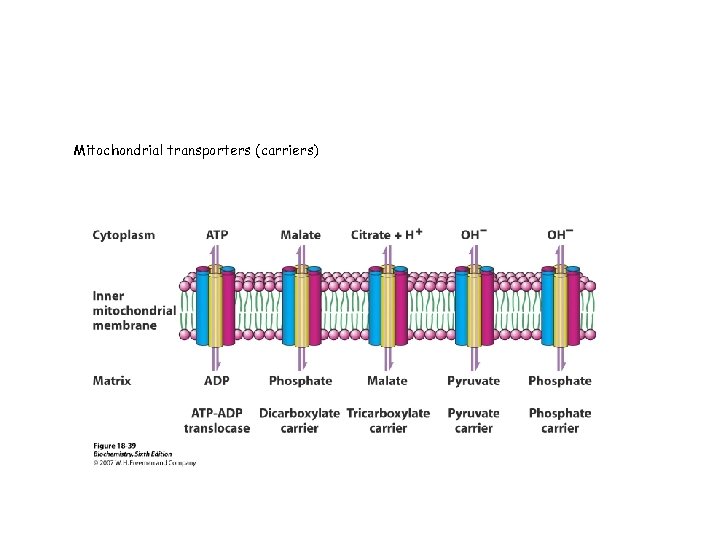 Mitochondrial transporters (carriers)
Mitochondrial transporters (carriers)
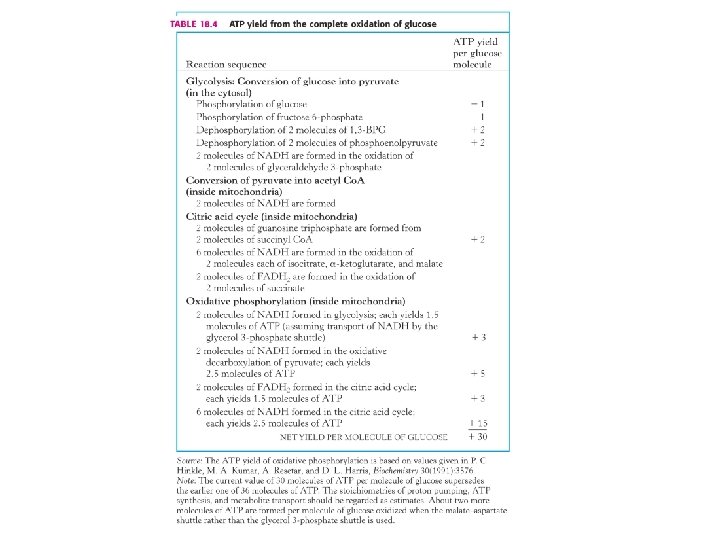
 Fotosyntéza • Fotosyntéza je dráha poháňaná svetlom, pritom sa viaže CO 2 tak, že vznikajú sacharidy (CH 2 O) svetlo CO 2 + H 2 O (CH 2 O) + O 2 • Fotosyntéza umožňuje kolobeh uhlíka v prírode • Je to zložitý súbor reakcií, ktoré sú rozdelené na svetelnú fázu a fázu prebiehajúcu počas tmy (Calvinov cyklus)
Fotosyntéza • Fotosyntéza je dráha poháňaná svetlom, pritom sa viaže CO 2 tak, že vznikajú sacharidy (CH 2 O) svetlo CO 2 + H 2 O (CH 2 O) + O 2 • Fotosyntéza umožňuje kolobeh uhlíka v prírode • Je to zložitý súbor reakcií, ktoré sú rozdelené na svetelnú fázu a fázu prebiehajúcu počas tmy (Calvinov cyklus)
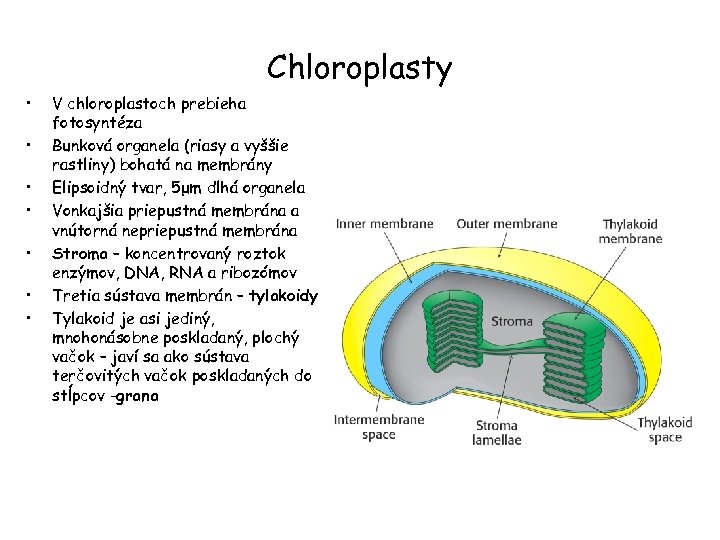 Chloroplasty • • V chloroplastoch prebieha fotosyntéza Bunková organela (riasy a vyššie rastliny) bohatá na membrány Elipsoidný tvar, 5μm dlhá organela Vonkajšia priepustná membrána a vnútorná nepriepustná membrána Stroma – koncentrovaný roztok enzýmov, DNA, RNA a ribozómov Tretia sústava membrán – tylakoidy Tylakoid je asi jediný, mnohonásobne poskladaný, plochý vačok – javí sa ako sústava terčovitých vačok poskladaných do stĺpcov -grana
Chloroplasty • • V chloroplastoch prebieha fotosyntéza Bunková organela (riasy a vyššie rastliny) bohatá na membrány Elipsoidný tvar, 5μm dlhá organela Vonkajšia priepustná membrána a vnútorná nepriepustná membrána Stroma – koncentrovaný roztok enzýmov, DNA, RNA a ribozómov Tretia sústava membrán – tylakoidy Tylakoid je asi jediný, mnohonásobne poskladaný, plochý vačok – javí sa ako sústava terčovitých vačok poskladaných do stĺpcov -grana
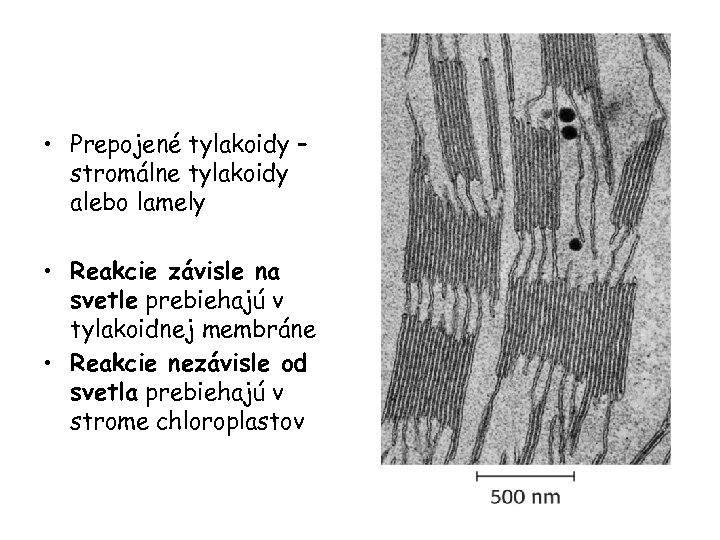 • Prepojené tylakoidy – stromálne tylakoidy alebo lamely • Reakcie závisle na svetle prebiehajú v tylakoidnej membráne • Reakcie nezávisle od svetla prebiehajú v strome chloroplastov
• Prepojené tylakoidy – stromálne tylakoidy alebo lamely • Reakcie závisle na svetle prebiehajú v tylakoidnej membráne • Reakcie nezávisle od svetla prebiehajú v strome chloroplastov
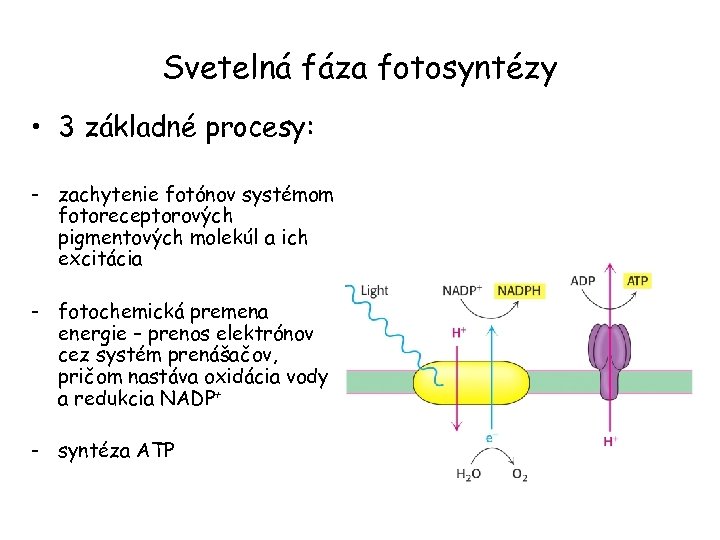 Svetelná fáza fotosyntézy • 3 základné procesy: - zachytenie fotónov systémom fotoreceptorových pigmentových molekúl a ich excitácia - fotochemická premena energie – prenos elektrónov cez systém prenášačov, pričom nastáva oxidácia vody a redukcia NADP+ - syntéza ATP
Svetelná fáza fotosyntézy • 3 základné procesy: - zachytenie fotónov systémom fotoreceptorových pigmentových molekúl a ich excitácia - fotochemická premena energie – prenos elektrónov cez systém prenášačov, pričom nastáva oxidácia vody a redukcia NADP+ - syntéza ATP
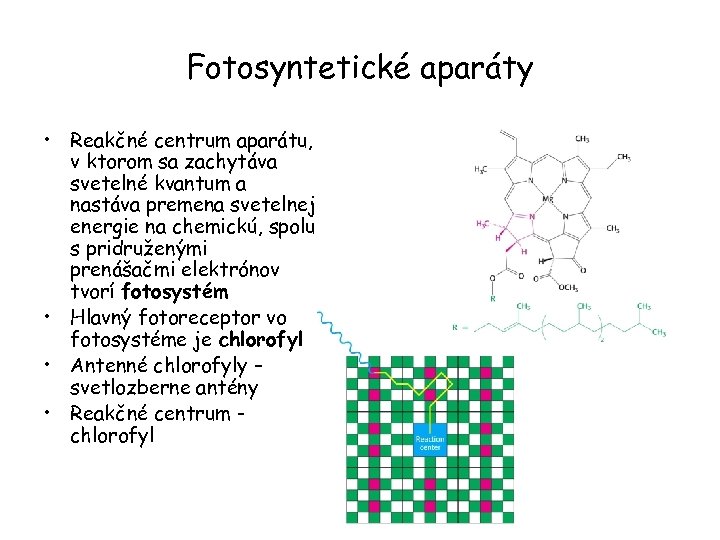 Fotosyntetické aparáty • Reakčné centrum aparátu, v ktorom sa zachytáva svetelné kvantum a nastáva premena svetelnej energie na chemickú, spolu s pridruženými prenášačmi elektrónov tvorí fotosystém • Hlavný fotoreceptor vo fotosystéme je chlorofyl • Antenné chlorofyly – svetlozberne antény • Reakčné centrum chlorofyl
Fotosyntetické aparáty • Reakčné centrum aparátu, v ktorom sa zachytáva svetelné kvantum a nastáva premena svetelnej energie na chemickú, spolu s pridruženými prenášačmi elektrónov tvorí fotosystém • Hlavný fotoreceptor vo fotosystéme je chlorofyl • Antenné chlorofyly – svetlozberne antény • Reakčné centrum chlorofyl
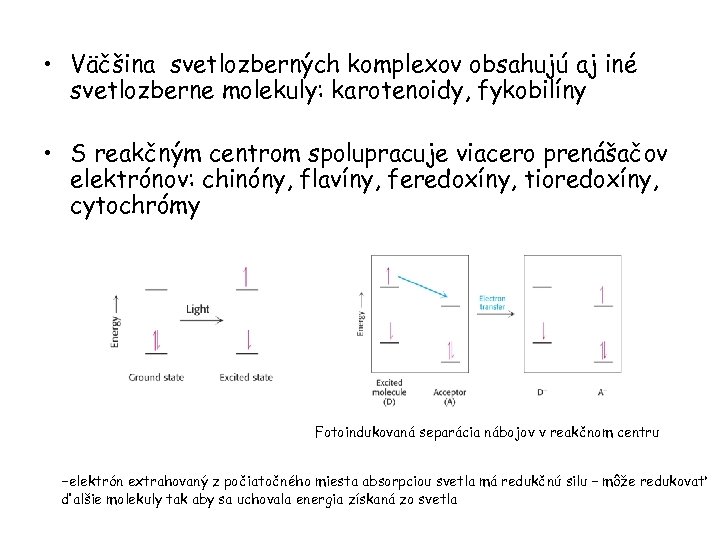 • Väčšina svetlozberných komplexov obsahujú aj iné svetlozberne molekuly: karotenoidy, fykobilíny • S reakčným centrom spolupracuje viacero prenášačov elektrónov: chinóny, flavíny, feredoxíny, tioredoxíny, cytochrómy Fotoindukovaná separácia nábojov v reakčnom centru -elektrón extrahovaný z počiatočného miesta absorpciou svetla má redukčnú silu – môže redukovať ďalšie molekuly tak aby sa uchovala energia získaná zo svetla
• Väčšina svetlozberných komplexov obsahujú aj iné svetlozberne molekuly: karotenoidy, fykobilíny • S reakčným centrom spolupracuje viacero prenášačov elektrónov: chinóny, flavíny, feredoxíny, tioredoxíny, cytochrómy Fotoindukovaná separácia nábojov v reakčnom centru -elektrón extrahovaný z počiatočného miesta absorpciou svetla má redukčnú silu – môže redukovať ďalšie molekuly tak aby sa uchovala energia získaná zo svetla
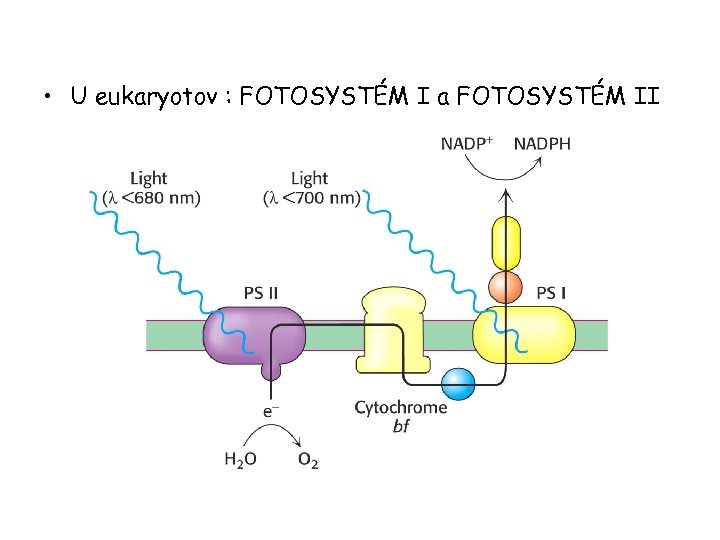 • U eukaryotov : FOTOSYSTÉM I a FOTOSYSTÉM II
• U eukaryotov : FOTOSYSTÉM I a FOTOSYSTÉM II
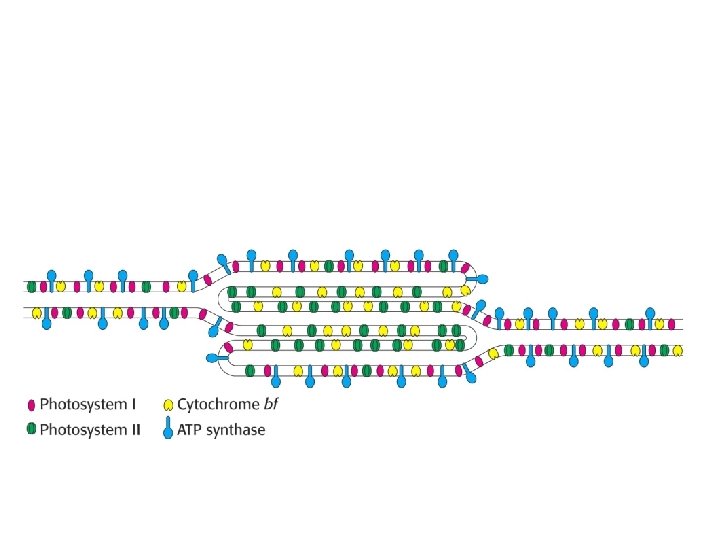
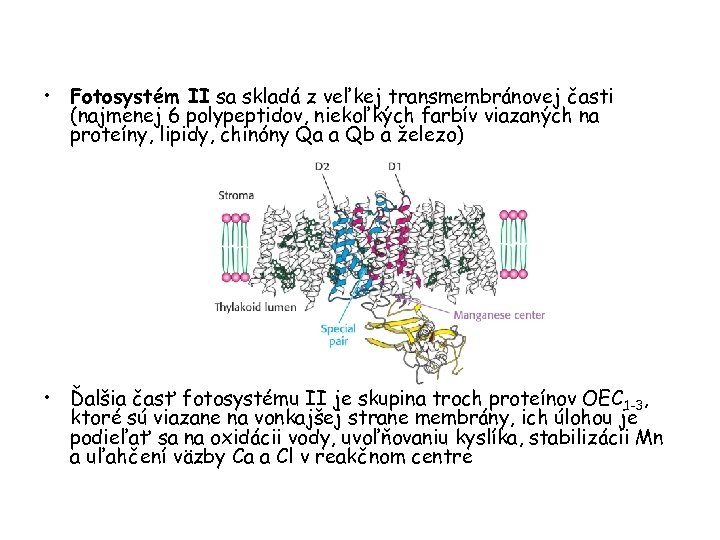 • Fotosystém II sa skladá z veľkej transmembránovej časti (najmenej 6 polypeptidov, niekoľkých farbív viazaných na proteíny, lipidy, chinóny Qa a Qb a železo) • Ďalšia časť fotosystému II je skupina troch proteínov OEC 1 -3, ktoré sú viazane na vonkajšej strane membrány, ich úlohou je podieľať sa na oxidácii vody, uvoľňovaniu kyslíka, stabilizácii Mn a uľahčení väzby Ca a Cl v reakčnom centre
• Fotosystém II sa skladá z veľkej transmembránovej časti (najmenej 6 polypeptidov, niekoľkých farbív viazaných na proteíny, lipidy, chinóny Qa a Qb a železo) • Ďalšia časť fotosystému II je skupina troch proteínov OEC 1 -3, ktoré sú viazane na vonkajšej strane membrány, ich úlohou je podieľať sa na oxidácii vody, uvoľňovaniu kyslíka, stabilizácii Mn a uľahčení väzby Ca a Cl v reakčnom centre
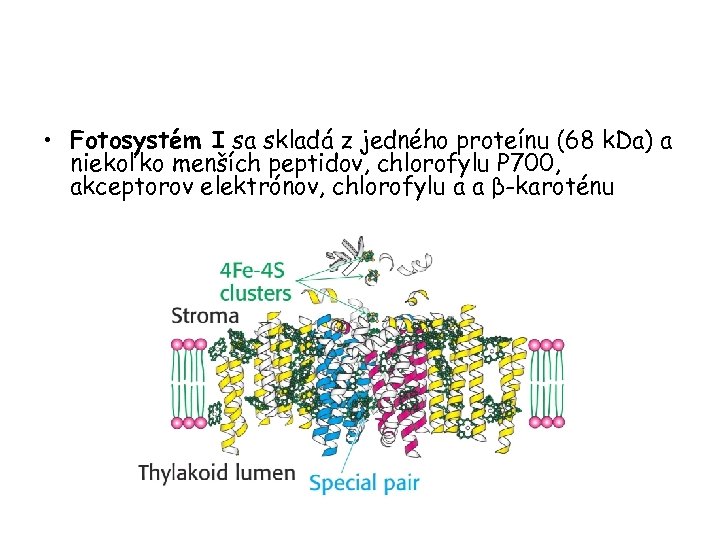 • Fotosystém I sa skladá z jedného proteínu (68 k. Da) a niekoľko menších peptidov, chlorofylu P 700, akceptorov elektrónov, chlorofylu a a β-karoténu
• Fotosystém I sa skladá z jedného proteínu (68 k. Da) a niekoľko menších peptidov, chlorofylu P 700, akceptorov elektrónov, chlorofylu a a β-karoténu
 • Tretí komplex je cytochróm bf s dvoma molekulami cytochrómu b 563, jedným Fe-S centrom a proteínom (17 k. Da) – tvorí protónový gradient • ATP-syntetáza (štvrtý komplex) – zložená z membránového sektora CFo a periférneho spájacieho faktora CF 1 • Piaty komplex nemá katalytickú aktivitu, jeho primárna funkcia je zachytávanie slnečnej energie (LHC), obsahuje dva peptidy, ktoré viažu viac ako polovicu z celého množstva chlorofylu a skoro celý chlorofyl b
• Tretí komplex je cytochróm bf s dvoma molekulami cytochrómu b 563, jedným Fe-S centrom a proteínom (17 k. Da) – tvorí protónový gradient • ATP-syntetáza (štvrtý komplex) – zložená z membránového sektora CFo a periférneho spájacieho faktora CF 1 • Piaty komplex nemá katalytickú aktivitu, jeho primárna funkcia je zachytávanie slnečnej energie (LHC), obsahuje dva peptidy, ktoré viažu viac ako polovicu z celého množstva chlorofylu a skoro celý chlorofyl b
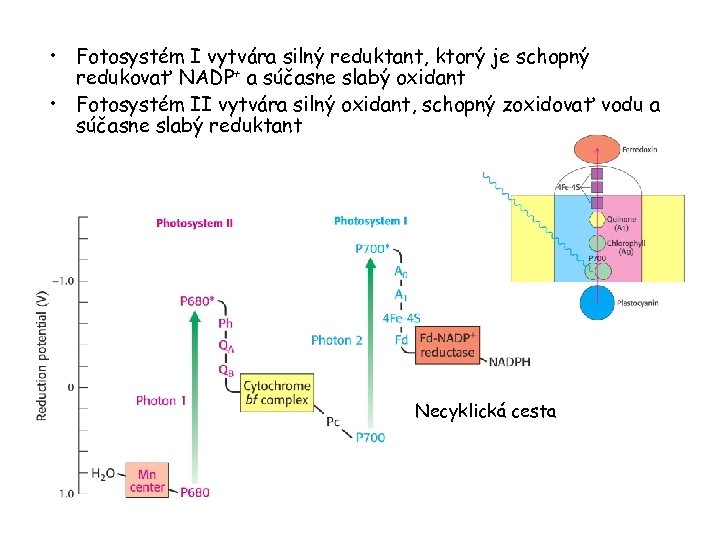 • Fotosystém I vytvára silný reduktant, ktorý je schopný redukovať NADP+ a súčasne slabý oxidant • Fotosystém II vytvára silný oxidant, schopný zoxidovať vodu a súčasne slabý reduktant Necyklická cesta
• Fotosystém I vytvára silný reduktant, ktorý je schopný redukovať NADP+ a súčasne slabý oxidant • Fotosystém II vytvára silný oxidant, schopný zoxidovať vodu a súčasne slabý reduktant Necyklická cesta
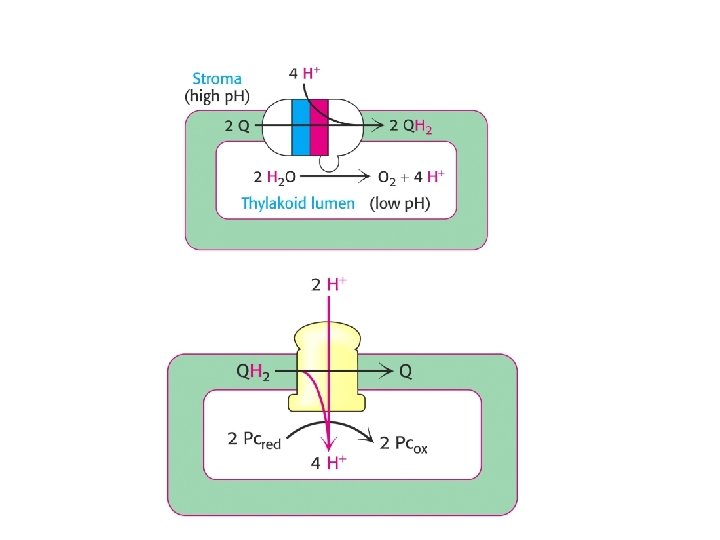
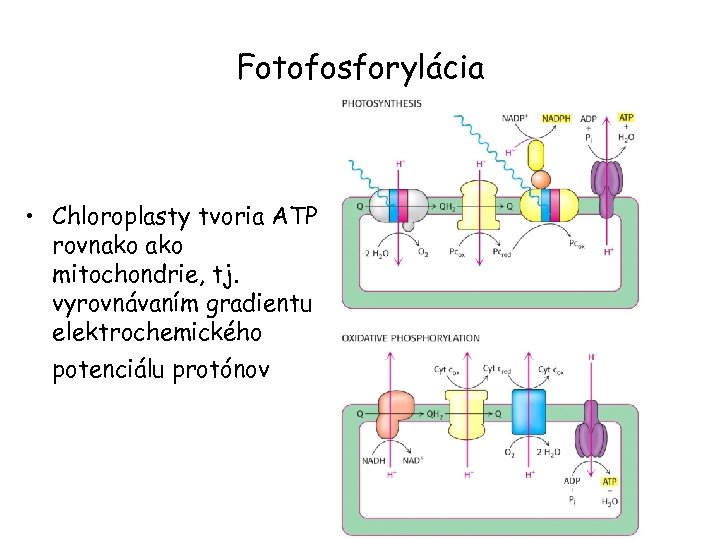 Fotofosforylácia • Chloroplasty tvoria ATP rovnako mitochondrie, tj. vyrovnávaním gradientu elektrochemického potenciálu protónov
Fotofosforylácia • Chloroplasty tvoria ATP rovnako mitochondrie, tj. vyrovnávaním gradientu elektrochemického potenciálu protónov
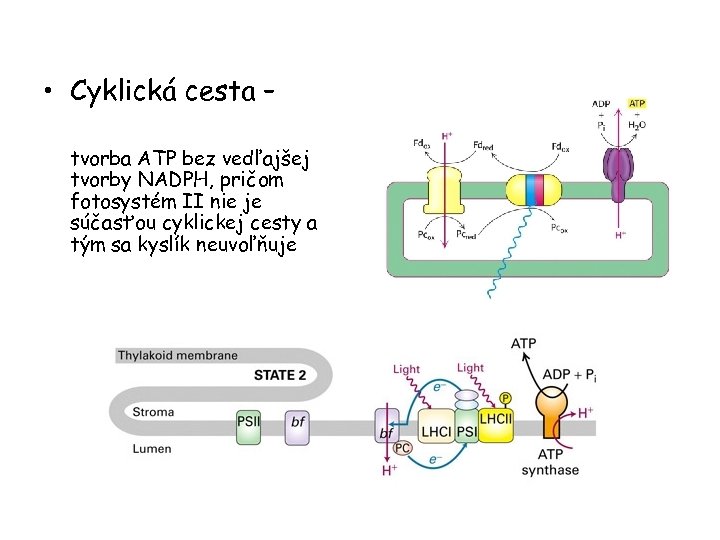 • Cyklická cesta – tvorba ATP bez vedľajšej tvorby NADPH, pričom fotosystém II nie je súčasťou cyklickej cesty a tým sa kyslík neuvoľňuje
• Cyklická cesta – tvorba ATP bez vedľajšej tvorby NADPH, pričom fotosystém II nie je súčasťou cyklickej cesty a tým sa kyslík neuvoľňuje