ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЫЕ РЕАКЦИИ [Автосохраненный].ppt
- Количество слайдов: 21
 ОВР в органической химии
ОВР в органической химии
 Окисление алкенов (кислая среда) В результате разрыва двойной связи образуются кетоны, карбоновые кислоты или диоксид углерода. CH 3–CH=CH–CH 3+KMn. O 4+H 2 SO 4 →СН 3 СООН+Mn. SO 4 + +K 2 SO 4+H 2 O C 4 H 8 +4 H 2 O – 8 е → 2 С 2 Н 4 О 2 + 8 Н+ 5 Mn. O 4 - +8 Н+ + 5 е → Mn 2+ +4 H 2 O 8 5 C 4 H 8+20 H 2 O+8 Mn. O 4 - +64 Н+→ 10 С 2 Н 4 О 2 +40 Н+ +8 Mn 2++32 H 2 O 5 CH 3–CH=CH–CH 3+8 KMn. O 4+12 H 2 SO 4 → 10 СН 3 СООН+8 Mn. SO 4 + 4 K 2 SO 4+12 H 2 O
Окисление алкенов (кислая среда) В результате разрыва двойной связи образуются кетоны, карбоновые кислоты или диоксид углерода. CH 3–CH=CH–CH 3+KMn. O 4+H 2 SO 4 →СН 3 СООН+Mn. SO 4 + +K 2 SO 4+H 2 O C 4 H 8 +4 H 2 O – 8 е → 2 С 2 Н 4 О 2 + 8 Н+ 5 Mn. O 4 - +8 Н+ + 5 е → Mn 2+ +4 H 2 O 8 5 C 4 H 8+20 H 2 O+8 Mn. O 4 - +64 Н+→ 10 С 2 Н 4 О 2 +40 Н+ +8 Mn 2++32 H 2 O 5 CH 3–CH=CH–CH 3+8 KMn. O 4+12 H 2 SO 4 → 10 СН 3 СООН+8 Mn. SO 4 + 4 K 2 SO 4+12 H 2 O
 Окисление алкенов (кислая среда) В результате разрыва двойной связи образуются кетоны, карбоновые кислоты или диоксид углерода. CH 3–CH=CH 2+K 2 Cr 2 O 7+H 2 SO 4 →СН 3 СООН+CO 2+Cr 2(SO 4)3 + +K 2 SO 4+H 2 O C 3 H 6 +4 H 2 O – 10 е → С 2 Н 4 О 2 +CO 2+10 Н+ Cr 2 O 72 - +14 Н+ + 6 е → 2 Cr 3+ +7 H 2 O 3 5 3 C 3 H 6+12 H 2 O+5 Cr 2 O 72 - +70 Н+ → 3 С 2 Н 4 О+3 CO 2 +30 Н+ + +10 Cr 3++35 H 2 O 3 CH 3–CH=CH 2+5 K 2 Cr 2 O 7+20 H 2 SO 4→ 3 СН 3 СООН+3 CO 2+ +5 Cr 2(SO 4)3 +5 K 2 SO 4+23 H 2 O
Окисление алкенов (кислая среда) В результате разрыва двойной связи образуются кетоны, карбоновые кислоты или диоксид углерода. CH 3–CH=CH 2+K 2 Cr 2 O 7+H 2 SO 4 →СН 3 СООН+CO 2+Cr 2(SO 4)3 + +K 2 SO 4+H 2 O C 3 H 6 +4 H 2 O – 10 е → С 2 Н 4 О 2 +CO 2+10 Н+ Cr 2 O 72 - +14 Н+ + 6 е → 2 Cr 3+ +7 H 2 O 3 5 3 C 3 H 6+12 H 2 O+5 Cr 2 O 72 - +70 Н+ → 3 С 2 Н 4 О+3 CO 2 +30 Н+ + +10 Cr 3++35 H 2 O 3 CH 3–CH=CH 2+5 K 2 Cr 2 O 7+20 H 2 SO 4→ 3 СН 3 СООН+3 CO 2+ +5 Cr 2(SO 4)3 +5 K 2 SO 4+23 H 2 O
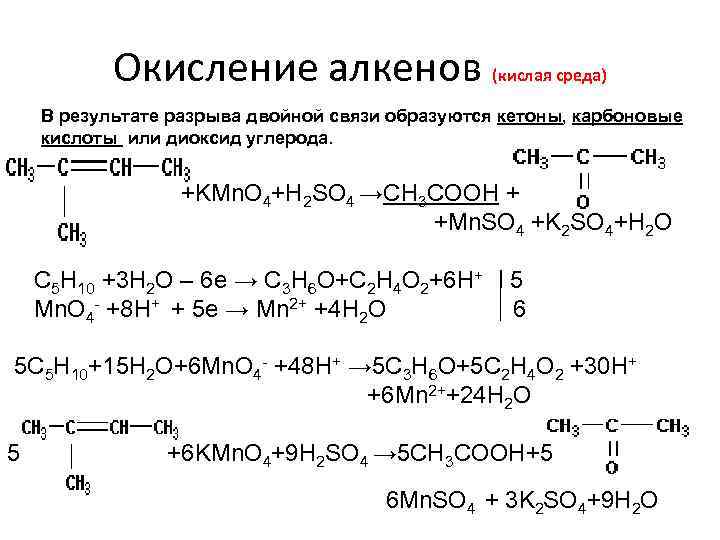 Окисление алкенов (кислая среда) В результате разрыва двойной связи образуются кетоны, карбоновые кислоты или диоксид углерода. +KMn. O 4+H 2 SO 4 →CH 3 COOH + +Mn. SO 4 +K 2 SO 4+H 2 O C 5 H 10 +3 H 2 O – 6 е → С 3 Н 6 О+С 2 Н 4 О 2+6 Н+ Mn. O 4 - +8 Н+ + 5 е → Mn 2+ +4 H 2 O 5 6 5 C 5 H 10+15 H 2 O+6 Mn. O 4 - +48 Н+ → 5 С 3 Н 6 О+5 C 2 H 4 O 2 +30 Н+ +6 Mn 2++24 H 2 O 5 +6 KMn. O 4+9 H 2 SO 4 → 5 СН 3 СООН+5 6 Mn. SO 4 + 3 K 2 SO 4+9 H 2 O
Окисление алкенов (кислая среда) В результате разрыва двойной связи образуются кетоны, карбоновые кислоты или диоксид углерода. +KMn. O 4+H 2 SO 4 →CH 3 COOH + +Mn. SO 4 +K 2 SO 4+H 2 O C 5 H 10 +3 H 2 O – 6 е → С 3 Н 6 О+С 2 Н 4 О 2+6 Н+ Mn. O 4 - +8 Н+ + 5 е → Mn 2+ +4 H 2 O 5 6 5 C 5 H 10+15 H 2 O+6 Mn. O 4 - +48 Н+ → 5 С 3 Н 6 О+5 C 2 H 4 O 2 +30 Н+ +6 Mn 2++24 H 2 O 5 +6 KMn. O 4+9 H 2 SO 4 → 5 СН 3 СООН+5 6 Mn. SO 4 + 3 K 2 SO 4+9 H 2 O
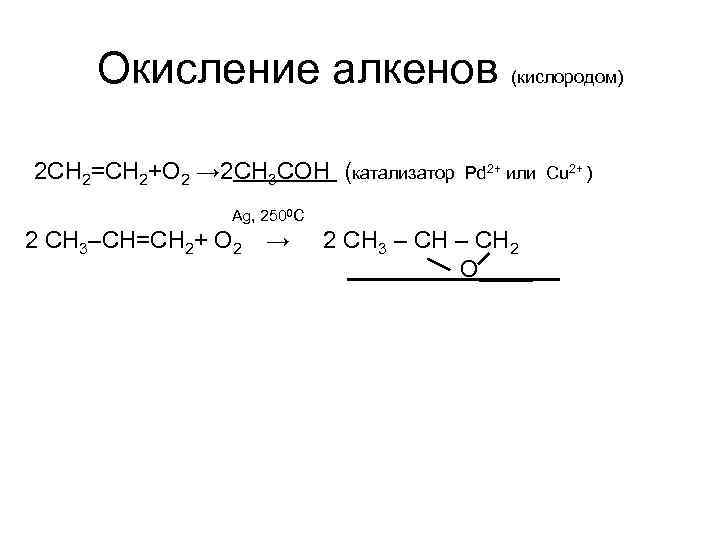 Окисление алкенов (кислородом) 2 CH 2=CH 2+O 2 → 2 СН 3 СОН (катализатор Pd 2+ или Cu 2+ ) Ag, 2500 C 2 CH 3–CH=CH 2+ O 2 → 2 CH 3 – CH 2 O____
Окисление алкенов (кислородом) 2 CH 2=CH 2+O 2 → 2 СН 3 СОН (катализатор Pd 2+ или Cu 2+ ) Ag, 2500 C 2 CH 3–CH=CH 2+ O 2 → 2 CH 3 – CH 2 O____
 Окисление алкинов (кислая среда) CH 3–C≡C–СН 2 –CH 3+KMn. O 4+H 2 SO 4→СН 3 СООН+С 2 Н 5 СООН +Mn. SO 4 +K 2 SO 4+H 2 O C 5 H 8 +4 H 2 O – 6 е → С 2 Н 4 О 2+С 3 Н 6 О 2 +6 Н+ 5 Mn. O 4 - +8 Н+ + 5 е → Mn 2+ +4 H 2 O 6 5 C 5 H 8+20 H 2 O+6 Mn. O 4 - +48 Н+ → 5 С 2 Н 4 О 2 +5 С 3 Н 6 О 2 + 30 Н+ + + 6 Mn 2++24 H 2 O 5 CH 3–C≡C–СН 2 –CH 3+6 KMn. O 4+9 H 2 SO 4→ 5 СН 3 СООН+ +5 С 2 Н 5 СООН+6 Mn. SO 4 +3 K 2 SO 4+4 H 2 O
Окисление алкинов (кислая среда) CH 3–C≡C–СН 2 –CH 3+KMn. O 4+H 2 SO 4→СН 3 СООН+С 2 Н 5 СООН +Mn. SO 4 +K 2 SO 4+H 2 O C 5 H 8 +4 H 2 O – 6 е → С 2 Н 4 О 2+С 3 Н 6 О 2 +6 Н+ 5 Mn. O 4 - +8 Н+ + 5 е → Mn 2+ +4 H 2 O 6 5 C 5 H 8+20 H 2 O+6 Mn. O 4 - +48 Н+ → 5 С 2 Н 4 О 2 +5 С 3 Н 6 О 2 + 30 Н+ + + 6 Mn 2++24 H 2 O 5 CH 3–C≡C–СН 2 –CH 3+6 KMn. O 4+9 H 2 SO 4→ 5 СН 3 СООН+ +5 С 2 Н 5 СООН+6 Mn. SO 4 +3 K 2 SO 4+4 H 2 O
 Окисление алкинов (нейтральная среда) CН≡CH+KMn. O 4→КООС – СООК+Mn. O 2+KOH + H 2 O C 2 H 2 +4 H 2 O – 8 е → 2 СОО- +10 Н+ Mn. O 4 - +2 H 2 O + 3 е → Mn. О 2 +4 OН- 3 8 3 C 2 H 2+12 H 2 O+8 Mn. O 4 - +16 H 2 O → 6 СОО-+30 Н+ +8 Mn. O 2 +32 OН 3 CН≡CH+8 KMn. O 4→ 3 КООС – СООК+8 Mn. O 2+2 KOH +2 H 2 O
Окисление алкинов (нейтральная среда) CН≡CH+KMn. O 4→КООС – СООК+Mn. O 2+KOH + H 2 O C 2 H 2 +4 H 2 O – 8 е → 2 СОО- +10 Н+ Mn. O 4 - +2 H 2 O + 3 е → Mn. О 2 +4 OН- 3 8 3 C 2 H 2+12 H 2 O+8 Mn. O 4 - +16 H 2 O → 6 СОО-+30 Н+ +8 Mn. O 2 +32 OН 3 CН≡CH+8 KMn. O 4→ 3 КООС – СООК+8 Mn. O 2+2 KOH +2 H 2 O
 Окисление алкинов (нейтральная среда) СН 3 – C≡CH+H 2 O+KMn. O 4→СН 3 СООK+КНСО 3 +Mn. O 2+KOH C 3 H 4 +5 H 2 O – 8 е → CH 3 СОО- + HCO 3 - +10 Н+ 3 Mn. O 4 - +2 H 2 O + 3 е → Mn. О 2 +4 OН 8 3 C 3 H 4+15 H 2 O+8 Mn. O 4 - +16 H 2 O → 3 CH 3 СОО- + 3 HCO 3 - + 30 Н+ +8 Mn. O 2 +32 OН 3 СН 3 – C≡CH + H 2 O + 8 KMn. O 4→ 3 СН 3 СООK + 3 КНСО 3 + + 8 Mn. O 2 + 2 KOH
Окисление алкинов (нейтральная среда) СН 3 – C≡CH+H 2 O+KMn. O 4→СН 3 СООK+КНСО 3 +Mn. O 2+KOH C 3 H 4 +5 H 2 O – 8 е → CH 3 СОО- + HCO 3 - +10 Н+ 3 Mn. O 4 - +2 H 2 O + 3 е → Mn. О 2 +4 OН 8 3 C 3 H 4+15 H 2 O+8 Mn. O 4 - +16 H 2 O → 3 CH 3 СОО- + 3 HCO 3 - + 30 Н+ +8 Mn. O 2 +32 OН 3 СН 3 – C≡CH + H 2 O + 8 KMn. O 4→ 3 СН 3 СООK + 3 КНСО 3 + + 8 Mn. O 2 + 2 KOH
 Окисление алкинов (щелочная среда) CH 3–C≡CH+KMn. O 4+KOH→СН 3 СООК+К 2 СО 3 +K 2 Mn. O 4+ H 2 O C 3 H 4 +11 OH- – 8 е → СН 3 СОО- + СО 32 - +6 H 2 O Mn. O 4 - + е → Mn. О 42 - 1 8 C 3 H 4+ 11 OH- +8 Mn. O 4 - → СН 3 СОО-+ СО 32 - + 6 H 2 O + 8 Mn. О 42 CH 3–C≡CH+8 KMn. O 4+11 KOH→СН 3 СООК+К 2 СО 3 +8 K 2 Mn. O 4+ + 6 H 2 O
Окисление алкинов (щелочная среда) CH 3–C≡CH+KMn. O 4+KOH→СН 3 СООК+К 2 СО 3 +K 2 Mn. O 4+ H 2 O C 3 H 4 +11 OH- – 8 е → СН 3 СОО- + СО 32 - +6 H 2 O Mn. O 4 - + е → Mn. О 42 - 1 8 C 3 H 4+ 11 OH- +8 Mn. O 4 - → СН 3 СОО-+ СО 32 - + 6 H 2 O + 8 Mn. О 42 CH 3–C≡CH+8 KMn. O 4+11 KOH→СН 3 СООК+К 2 СО 3 +8 K 2 Mn. O 4+ + 6 H 2 O
 Окисление аренов (кислая среда) С 6 H 5 – CH 3 +KMn. O 4+H 2 SO 4→С 6 Н 5 СООН+Mn. SO 4 +K 2 SO 4+H 2 O C 7 H 8 +2 H 2 O – 6 е → С 7 Н 6 О 2 +6 Н+ 5 Mn. O 4 - +8 Н+ + 5 е → Mn 2+ +4 H 2 O 6 5 C 7 H 8+10 H 2 O+6 Mn. O 4 - +48 Н+ → 5 С 7 Н 6 О 2 + 30 Н+ +6 Mn 2++24 H 2 O 5 С 6 H 5 – CH 3 +6 KMn. O 4+9 H 2 SO 4→ 5 С 6 Н 5 СООН+6 Mn. SO 4 + +3 K 2 SO 4+14 H 2 O
Окисление аренов (кислая среда) С 6 H 5 – CH 3 +KMn. O 4+H 2 SO 4→С 6 Н 5 СООН+Mn. SO 4 +K 2 SO 4+H 2 O C 7 H 8 +2 H 2 O – 6 е → С 7 Н 6 О 2 +6 Н+ 5 Mn. O 4 - +8 Н+ + 5 е → Mn 2+ +4 H 2 O 6 5 C 7 H 8+10 H 2 O+6 Mn. O 4 - +48 Н+ → 5 С 7 Н 6 О 2 + 30 Н+ +6 Mn 2++24 H 2 O 5 С 6 H 5 – CH 3 +6 KMn. O 4+9 H 2 SO 4→ 5 С 6 Н 5 СООН+6 Mn. SO 4 + +3 K 2 SO 4+14 H 2 O
 Окисление аренов (кислая среда) С 6 H 5 СН 2 – CH 3 +KMn. O 4+H 2 SO 4→С 6 Н 5 СООН +CO 2+ Mn. SO 4 +K 2 SO 4+H 2 O C 8 H 10 +4 H 2 O – 12 е → С 7 Н 6 О 2 + CO 2 +12 Н+ 5 Mn. O 4 - +8 Н+ + 5 е → Mn 2+ +4 H 2 O 12 5 C 8 H 10+20 H 2 O+12 Mn. O 4 - +96 Н+ → 5 С 7 Н 6 О 2 + 5 CO 2 + 60 Н+ + +12 Mn 2++48 H 2 O 5 С 6 H 5 СН 2 – CH 3 +12 KMn. O 4+18 H 2 SO 4→ 5 С 6 Н 5 СООН +5 CO 2+ 12 Mn. SO 4 +6 K 2 SO 4+28 H 2 O
Окисление аренов (кислая среда) С 6 H 5 СН 2 – CH 3 +KMn. O 4+H 2 SO 4→С 6 Н 5 СООН +CO 2+ Mn. SO 4 +K 2 SO 4+H 2 O C 8 H 10 +4 H 2 O – 12 е → С 7 Н 6 О 2 + CO 2 +12 Н+ 5 Mn. O 4 - +8 Н+ + 5 е → Mn 2+ +4 H 2 O 12 5 C 8 H 10+20 H 2 O+12 Mn. O 4 - +96 Н+ → 5 С 7 Н 6 О 2 + 5 CO 2 + 60 Н+ + +12 Mn 2++48 H 2 O 5 С 6 H 5 СН 2 – CH 3 +12 KMn. O 4+18 H 2 SO 4→ 5 С 6 Н 5 СООН +5 CO 2+ 12 Mn. SO 4 +6 K 2 SO 4+28 H 2 O
 Окисление аренов (щелочная среда) С 6 H 5 – CH 3 +KMn. O 4+KOH→С 6 Н 5 СООК + K 2 Mn. O 4+ H 2 O C 7 H 8 +7 OH- – 6 е → С 6 Н 5 СОО- +5 H 2 O Mn. O 4 - + е → Mn. О 42 - 1 6 C 7 H 8+ 7 OH- +6 Mn. O 4 - → С 6 Н 5 СОО-+ 5 H 2 O + 6 Mn. О 42 С 6 H 5 – CH 3 +6 KMn. O 4+7 KOH→ С 6 Н 5 СООК +6 K 2 Mn. O 4+ 5 H 2 O
Окисление аренов (щелочная среда) С 6 H 5 – CH 3 +KMn. O 4+KOH→С 6 Н 5 СООК + K 2 Mn. O 4+ H 2 O C 7 H 8 +7 OH- – 6 е → С 6 Н 5 СОО- +5 H 2 O Mn. O 4 - + е → Mn. О 42 - 1 6 C 7 H 8+ 7 OH- +6 Mn. O 4 - → С 6 Н 5 СОО-+ 5 H 2 O + 6 Mn. О 42 С 6 H 5 – CH 3 +6 KMn. O 4+7 KOH→ С 6 Н 5 СООК +6 K 2 Mn. O 4+ 5 H 2 O
 Окисление аренов (щелочная среда) С 6 H 5 СН 2–CH 3+KMn. O 4+KOH→С 6 Н 5 СООК +К 2 СО 3+K 2 Mn. O 4+H 2 O C 8 H 10 +15 OH- – 12 е → С 6 Н 5 СОО- + CO 32 - +10 H 2 O Mn. O 4 - + е → Mn. О 42 - 1 12 C 8 H 10+15 OH- +12 Mn. O 4 - →С 6 Н 5 СОО-+ СО 32 - +10 H 2 O + 12 Mn. О 42 С 6 H 5 СН 2–CH 3+12 KMn. O 4+15 KOH→С 6 Н 5 СООК +К 2 СО 3+ + 12 K 2 Mn. O 4+10 H 2 O
Окисление аренов (щелочная среда) С 6 H 5 СН 2–CH 3+KMn. O 4+KOH→С 6 Н 5 СООК +К 2 СО 3+K 2 Mn. O 4+H 2 O C 8 H 10 +15 OH- – 12 е → С 6 Н 5 СОО- + CO 32 - +10 H 2 O Mn. O 4 - + е → Mn. О 42 - 1 12 C 8 H 10+15 OH- +12 Mn. O 4 - →С 6 Н 5 СОО-+ СО 32 - +10 H 2 O + 12 Mn. О 42 С 6 H 5 СН 2–CH 3+12 KMn. O 4+15 KOH→С 6 Н 5 СООК +К 2 СО 3+ + 12 K 2 Mn. O 4+10 H 2 O
 Окисление аренов (нейтральная среда) С 6 H 5 – CH 3 +KMn. O 4→С 6 Н 5 СООK+Mn. O 2+KOH + H 2 O C 7 H 8 +2 H 2 O – 6 е → С 6 Н 5 СОО- +7 Н+ 1 Mn. O 4 - +2 H 2 O + 3 е → Mn. О 2 +4 OН 2 C 7 H 8+2 H 2 O+2 Mn. O 4 - +4 H 2 O →С 6 Н 5 СОО- + 7 Н++2 Mn. O 2 +8 OНС 6 H 5 – CH 3 +2 KMn. O 4→С 6 Н 5 СООK+2 Mn. O 2+KOH + H 2 O
Окисление аренов (нейтральная среда) С 6 H 5 – CH 3 +KMn. O 4→С 6 Н 5 СООK+Mn. O 2+KOH + H 2 O C 7 H 8 +2 H 2 O – 6 е → С 6 Н 5 СОО- +7 Н+ 1 Mn. O 4 - +2 H 2 O + 3 е → Mn. О 2 +4 OН 2 C 7 H 8+2 H 2 O+2 Mn. O 4 - +4 H 2 O →С 6 Н 5 СОО- + 7 Н++2 Mn. O 2 +8 OНС 6 H 5 – CH 3 +2 KMn. O 4→С 6 Н 5 СООK+2 Mn. O 2+KOH + H 2 O
 Окисление аренов (нейтральная среда) С 6 H 5 СН 2 – CH 3+KMn. O 4→С 6 Н 5 СООK+ К 2 СО 3+ Mn. O 2+KOH + H 2 O C 8 H 10 +5 H 2 O – 12 е → С 6 Н 5 СОО- +CO 32 - +15 Н+ 1 Mn. O 4 - +2 H 2 O + 3 е → Mn. О 2 +4 OН 4 C 8 H 10+5 H 2 O+4 Mn. O 4 - +8 H 2 O→С 6 Н 5 СОО- +CO 32 -+15 Н+ + +4 Mn. O 2 +16 OНС 6 H 5 – СН 2 – CH 3 +4 KMn. O 4→С 6 Н 5 СООK+ К 2 СО 3 +4 Mn. O 2 +KOH +2 H 2 O
Окисление аренов (нейтральная среда) С 6 H 5 СН 2 – CH 3+KMn. O 4→С 6 Н 5 СООK+ К 2 СО 3+ Mn. O 2+KOH + H 2 O C 8 H 10 +5 H 2 O – 12 е → С 6 Н 5 СОО- +CO 32 - +15 Н+ 1 Mn. O 4 - +2 H 2 O + 3 е → Mn. О 2 +4 OН 4 C 8 H 10+5 H 2 O+4 Mn. O 4 - +8 H 2 O→С 6 Н 5 СОО- +CO 32 -+15 Н+ + +4 Mn. O 2 +16 OНС 6 H 5 – СН 2 – CH 3 +4 KMn. O 4→С 6 Н 5 СООK+ К 2 СО 3 +4 Mn. O 2 +KOH +2 H 2 O
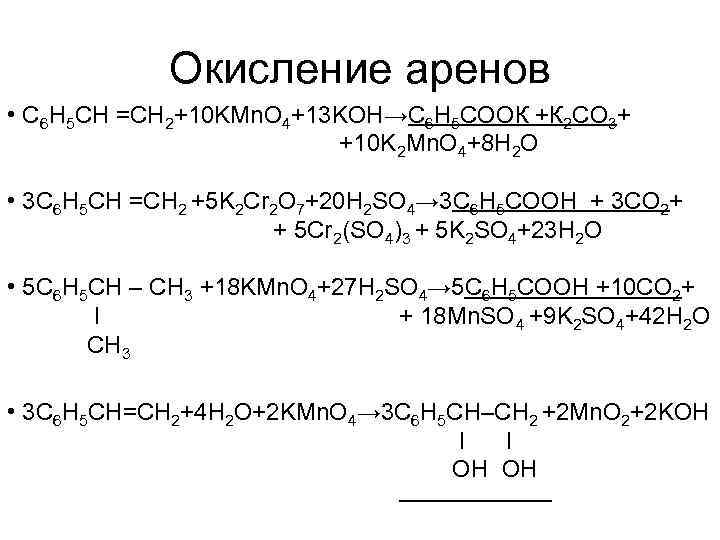 Окисление аренов • С 6 H 5 СН =CH 2+10 KMn. O 4+13 KOH→С 6 Н 5 СООК +К 2 СО 3+ +10 K 2 Mn. O 4+8 H 2 O • 3 С 6 H 5 СН =CH 2 +5 K 2 Cr 2 O 7+20 H 2 SO 4→ 3 С 6 Н 5 СООН + 3 CO 2+ + 5 Cr 2(SO 4)3 + 5 K 2 SO 4+23 H 2 O • 5 С 6 H 5 СН – CH 3 +18 KMn. O 4+27 H 2 SO 4→ 5 С 6 Н 5 СООН +10 CO 2+ I + 18 Mn. SO 4 +9 K 2 SO 4+42 H 2 O CH 3 • 3 С 6 H 5 СН=CH 2+4 H 2 O+2 KMn. O 4→ 3 С 6 H 5 СН–CH 2 +2 Mn. O 2+2 KOH I I OH OH
Окисление аренов • С 6 H 5 СН =CH 2+10 KMn. O 4+13 KOH→С 6 Н 5 СООК +К 2 СО 3+ +10 K 2 Mn. O 4+8 H 2 O • 3 С 6 H 5 СН =CH 2 +5 K 2 Cr 2 O 7+20 H 2 SO 4→ 3 С 6 Н 5 СООН + 3 CO 2+ + 5 Cr 2(SO 4)3 + 5 K 2 SO 4+23 H 2 O • 5 С 6 H 5 СН – CH 3 +18 KMn. O 4+27 H 2 SO 4→ 5 С 6 Н 5 СООН +10 CO 2+ I + 18 Mn. SO 4 +9 K 2 SO 4+42 H 2 O CH 3 • 3 С 6 H 5 СН=CH 2+4 H 2 O+2 KMn. O 4→ 3 С 6 H 5 СН–CH 2 +2 Mn. O 2+2 KOH I I OH OH
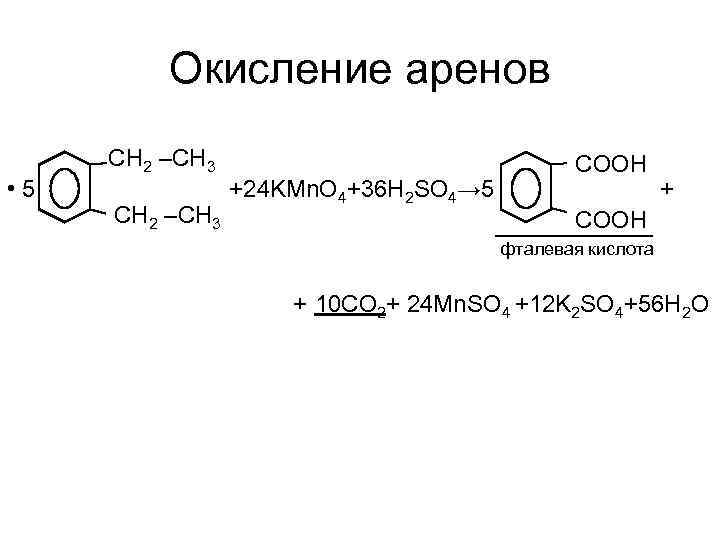 Окисление аренов • 5 CH 2 –CH 3 +24 KMn. O 4+36 H 2 SO 4→ 5 COOH + COOH фталевая кислота + 10 CO 2+ 24 Mn. SO 4 +12 K 2 SO 4+56 H 2 O
Окисление аренов • 5 CH 2 –CH 3 +24 KMn. O 4+36 H 2 SO 4→ 5 COOH + COOH фталевая кислота + 10 CO 2+ 24 Mn. SO 4 +12 K 2 SO 4+56 H 2 O
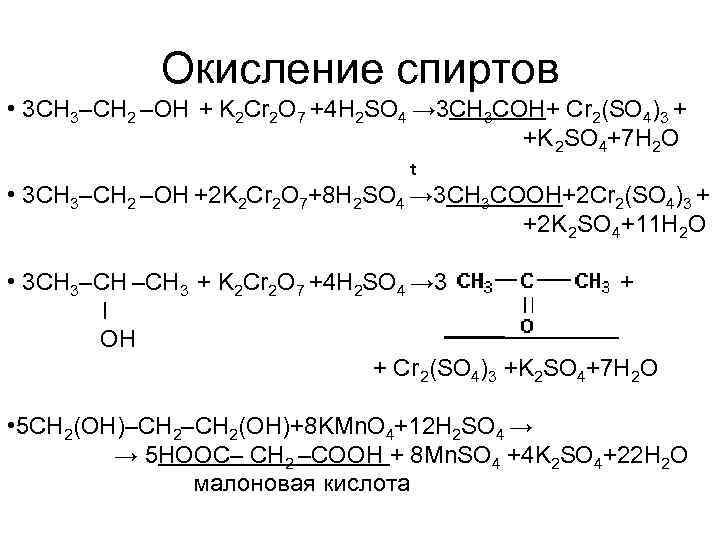 Окисление спиртов • 3 CH 3–CH 2 –ОН + K 2 Cr 2 O 7 +4 H 2 SO 4 → 3 СН 3 СОН+ Cr 2(SO 4)3 + +K 2 SO 4+7 H 2 O t • 3 CH 3–CH 2 –ОН +2 K 2 Cr 2 O 7+8 H 2 SO 4 → 3 СН 3 СОOН+2 Cr 2(SO 4)3 + +2 K 2 SO 4+11 H 2 O • 3 CH 3–CH 3 + K 2 Cr 2 O 7 +4 H 2 SO 4 → 3 + I OH + Cr 2(SO 4)3 +K 2 SO 4+7 H 2 O • 5 CH 2(OH)–CH 2(OH)+8 KMn. O 4+12 H 2 SO 4 → → 5 HOOС– CH 2 –СООН + 8 Mn. SO 4 +4 K 2 SO 4+22 H 2 O малоновая кислота
Окисление спиртов • 3 CH 3–CH 2 –ОН + K 2 Cr 2 O 7 +4 H 2 SO 4 → 3 СН 3 СОН+ Cr 2(SO 4)3 + +K 2 SO 4+7 H 2 O t • 3 CH 3–CH 2 –ОН +2 K 2 Cr 2 O 7+8 H 2 SO 4 → 3 СН 3 СОOН+2 Cr 2(SO 4)3 + +2 K 2 SO 4+11 H 2 O • 3 CH 3–CH 3 + K 2 Cr 2 O 7 +4 H 2 SO 4 → 3 + I OH + Cr 2(SO 4)3 +K 2 SO 4+7 H 2 O • 5 CH 2(OH)–CH 2(OH)+8 KMn. O 4+12 H 2 SO 4 → → 5 HOOС– CH 2 –СООН + 8 Mn. SO 4 +4 K 2 SO 4+22 H 2 O малоновая кислота
![Окисление альдегидов • 3 CH 3–CОН +2[Ag(NH 3)2]OH→ 3 СН 3 СОONH 4+2 Ag Окисление альдегидов • 3 CH 3–CОН +2[Ag(NH 3)2]OH→ 3 СН 3 СОONH 4+2 Ag](https://present5.com/presentation/3/56330743_437239568.pdf-img/56330743_437239568.pdf-19.jpg) Окисление альдегидов • 3 CH 3–CОН +2[Ag(NH 3)2]OH→ 3 СН 3 СОONH 4+2 Ag +3 NH 3+7 H 2 O • HCOOH +2[Ag(NH 3)2]OH→ (NH 4)2 CO 3 +H 2 O +2 Ag +2 NH 3 • CH 3–CОН + 2 KMn. O 4 +3 KOH →СН 3 СОOK+ 2 K 2 Mn. O 4 +2 H 2 O Окисление кетонов • 5 +8 KMn. O 4+12 H 2 SO 4 → 5 СН 3 СООН +5 СO 2 + +8 Mn. SO 4 +4 K 2 SO 4+17 H 2 O
Окисление альдегидов • 3 CH 3–CОН +2[Ag(NH 3)2]OH→ 3 СН 3 СОONH 4+2 Ag +3 NH 3+7 H 2 O • HCOOH +2[Ag(NH 3)2]OH→ (NH 4)2 CO 3 +H 2 O +2 Ag +2 NH 3 • CH 3–CОН + 2 KMn. O 4 +3 KOH →СН 3 СОOK+ 2 K 2 Mn. O 4 +2 H 2 O Окисление кетонов • 5 +8 KMn. O 4+12 H 2 SO 4 → 5 СН 3 СООН +5 СO 2 + +8 Mn. SO 4 +4 K 2 SO 4+17 H 2 O
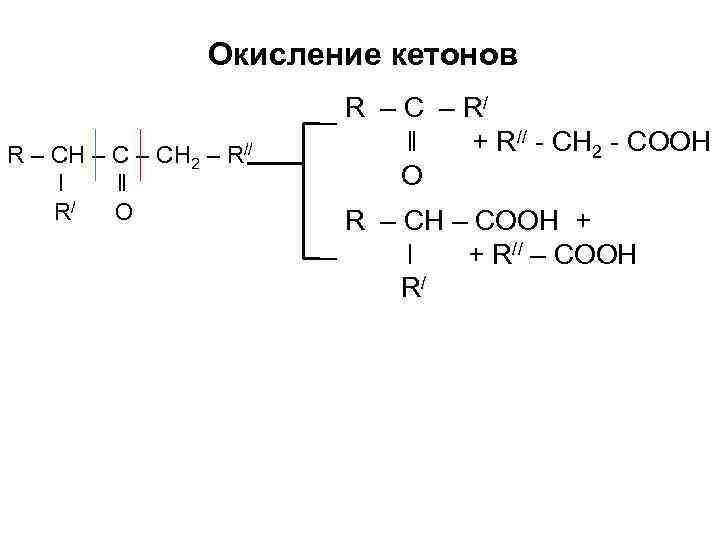 Окисление кетонов R – CH 2 – R// ǀ ǁ R/ O R – C – R/ ǁ + R// - CH 2 - COOH O R – CH – COOH + ǀ + R// – COOH R/
Окисление кетонов R – CH 2 – R// ǀ ǁ R/ O R – C – R/ ǁ + R// - CH 2 - COOH O R – CH – COOH + ǀ + R// – COOH R/
 Окисление • K 2 C 2 O 4 + 2 H 2 SO 4 → CO + CO 2 + H 2 O + 2 KHSO 4 • НСООН + Cl 2 → 2 HCl + CO 2↑ OH I адипиновая кислота • 5 +8 KMn. O 4+12 H 2 SO 4 → 5 HООС –(CH 2)4–СООH+ + 8 Mn. SO 4+4 K 2 SO 4+17 H 2 O • НСООН + PCl 5 → POCl 3+ CO↑ + 2 HCl
Окисление • K 2 C 2 O 4 + 2 H 2 SO 4 → CO + CO 2 + H 2 O + 2 KHSO 4 • НСООН + Cl 2 → 2 HCl + CO 2↑ OH I адипиновая кислота • 5 +8 KMn. O 4+12 H 2 SO 4 → 5 HООС –(CH 2)4–СООH+ + 8 Mn. SO 4+4 K 2 SO 4+17 H 2 O • НСООН + PCl 5 → POCl 3+ CO↑ + 2 HCl


