Kremny_i_ego_soedinenia.pptx
- Количество слайдов: 17


Открытие кремния Кремний был впервые открыт в 1811 году Гей-Люссаком и Тенаром. Он является одним из наиболее распространенных в земной коре элементов. В природе встречается в виде оксидов, силикатов и алюмосиликатов. Русское название элемента, данное ему Г. И. Гессом в 1831 году, произошло от старославянского слова „кремень“ — твёрдый камень. Таково же происхождение латинского silicium (и международного „силикат“): silex — камень, булыжник, а также утёс, скала.
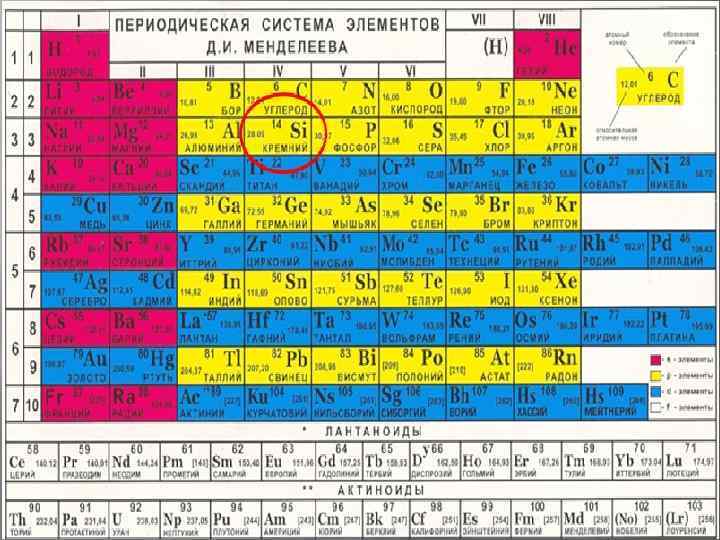

Кремний По распространению в земной коре занимает 2 -е место после кислорода его оксиды являются основной частью песка и глины в виде кристаллов входит в состав горных пород образует бесцветные кристаллы кварца и горного хрусталя на его основе создано промышленное производство керамики, стекла, цемента

Сверху вниз: Гранат. Лунный камень. Амазонит (полевой шпат, алюмосиликат калия КАl. Si 3 О 8) красивый поделочный камень из Ильменских гор (Урал).

Анализ образцов лунного грунта показал наличие Si. O 2 в количестве более 40%.

Строение и свойства атомов

Физические свойства кремния Кремний – кристаллическое вещество темно-серого цвета с металлическим блеском. Кристаллическая решетка кремния напоминает структуру алмаза. tплав(Si)=1415 ˚C

Получение кремния Лабораторный способ: Si. O 2+2 Mg=Si+2 Mg. O Промышленный способ: Si. O 2+2 C=2 CO+Si

Химические свойства кремния а) восстановительные 1) Si + O 2 =Si. O 2 2) Si + 2 CL 2 = Si. CL 4 3) Si + S = Si. S 2 4)Si + 2 H 2 O (пар) = Si. O 2 + H 2 5)Si + C = Si. C (карборунд) 6)Si +2 Na. OHконц) + H 2 O = Na 2 Si. O 3 + H 2 ( б) окислительные Si + 2 Ca = Ca Si 2

Соединения кремния Si. H 4 силан – бесцветный газ -получают косвенно, действуя на силициды металлов водой или кислотами: Mg 2 Si + 4 H 2 O = 2 Mg(OH)2 + Si. H 4 -менее стоек по сравнению с CH 4, самовоспламеняется при обычной температуре: Si. H 4 + 2 O 2 =Si. O 2 + 2 H 2 O

Кремниевая кислота и её соли Получить кремниевую кислоту можно только из её солей: Na 2 Si. O 3 + 2 HCl = 2 Na. CL +H 2 Si. O 32 - + 2 H+ = H 2 Si. O 3 Выделить в чистом виде нельзя, . т. к. при нагревании она разлагается: H 2 Si. O 3 = Si. O 2 + H 2 O соли кремниевой кислоты называют силикатами. Их можно получить сплавлением оксида кремния с оксидами металлов или карбонатами: Si. O 2 + Ca. O = Ca. Si. O 3 Si. O 2 + Ca. CO 3 = Ca. Si. O 3 + CO 2

Силикаты На силикаты приходится более 1/ массы всей земной коры. 4 К ним относится около 500 минералов, в т. ч. важнейшие породообразующие: полевые шпаты, слюды, пироксены и др. силикаты – это и песок, и глина, и кирпич, и стекло, и цемент, и эмаль, и тальк, и асбест, и изумруд, и топаз.

Применение соединений кремния Оконное стекло • Na 2 CO 3 + Ca. CO 3 + 6 Si. O 2 = Na 2 O. Ca. O. 6 Si. O 2 Хрусталь K 2 O. Pb. O. 6 Si. O 2

Керамика - общее название многочисленных материалов, полученных при спекании глин с различными минеральными добавками. Значит, и кирпич - керамика, и кафель, и осколки древнегреческой амфоры - тоже керамика.

Применение соединений кремния • Керамика Из керамики изготавливают изоляторы для высоковольтных ЛЭП и другие изделия, используемые в технике, строительстве, быту и т. п.

Спасибо за внимание!!!))))
Kremny_i_ego_soedinenia.pptx