ALL.ppt
- Количество слайдов: 76
Острый лимфобластный лейкоз: эпидемиология, клиника, диагностика и принципы лечения

Эпидемиология ОЛЛ Ежегодно в России диагностируется около 2 тыс. новых случаев ОЛЛ составляет 20% острых лейкозов взрослых: – 60% пациентов с ОЛЛ моложе 20 лет – ОЛЛ самая частая опухоль детского возраста: 30% всех злокачественных новообразований детей – Чаще возникает у лиц мужского пола: 62% Давыдов М. И. , Аксель Е. М. Вестник РОНЦ 2006; 17: 45 -47 Jemal A, et al. CA Cancer. 2004; 54: 8 -29.
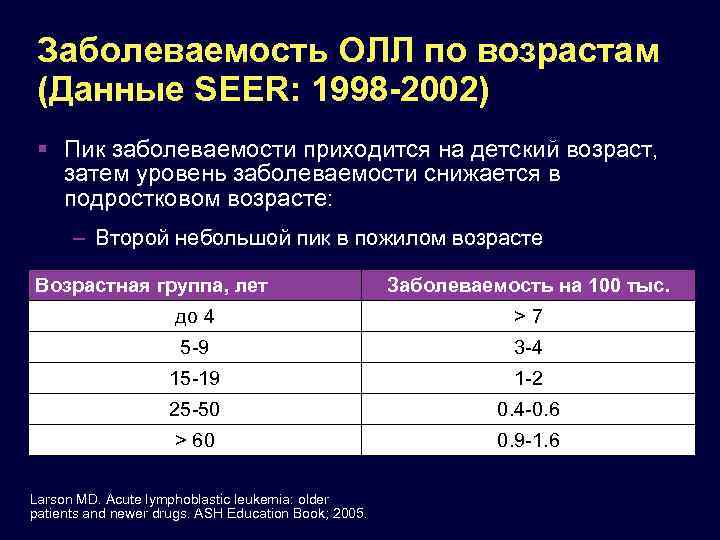
Заболеваемость ОЛЛ по возрастам (Данные SEER: 1998 -2002) Пик заболеваемости приходится на детский возраст, затем уровень заболеваемости снижается в подростковом возрасте: – Второй небольшой пик в пожилом возрасте Возрастная группа, лет Заболеваемость на 100 тыс. до 4 > 7 5 -9 3 -4 15 -19 1 -2 25 -50 0. 4 -0. 6 > 60 0. 9 -1. 6 Larson MD. Acute lymphoblastic leukemia: older patients and newer drugs. ASH Education Book; 2005.

Клиническая картина ОЛЛ Лихорадка Анемический синдром Геморрагический синдром Оссалгический синдром Пролиферативный синдром Дыхательная недостаточность Нарушения зрения Нейролейкемия Поражение кожи (лейкемиды)

Диагностика ОЛЛ Гемограмма Костномозговая пункция Люмбальная пункция МРТ головного мозга (по показаниям) УЗИ брюшная полость/забрюшинное пространство Рентгенография грудной клетки Биохимический анализ крови ЭКГ, Эхо-КГ Консультации специалистов
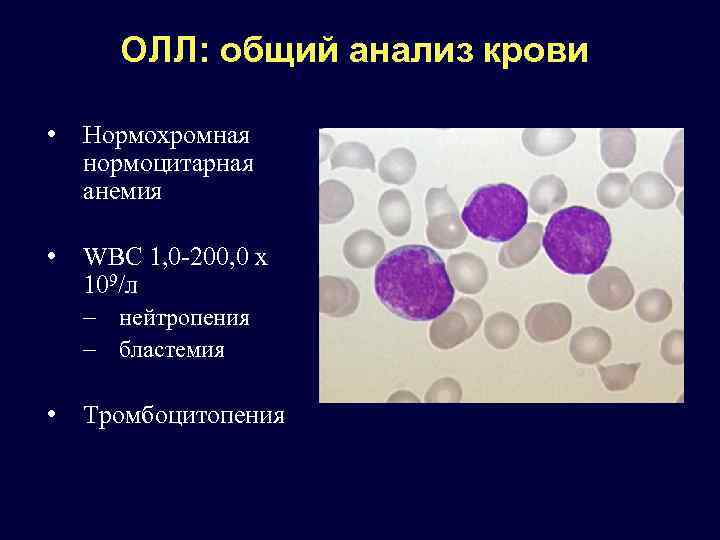
ОЛЛ: общий анализ крови • Нормохромная нормоцитарная анемия • WBC 1, 0 -200, 0 x 109/л - нейтропения - бластемия • Тромбоцитопения
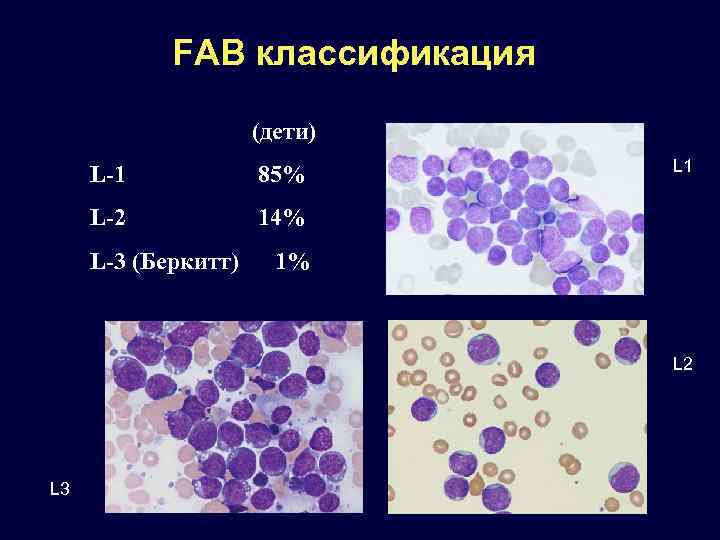
FAB классификация (дети) L-1 85% L-2 L 1 14% L-3 (Беркитт) 1% L 2 L 3

Цитохимические реакции: Реакция: Миелопероксидаза: PAS (гликоген) Судан черный Кислая фосфатаза Результат: (-) (+) в гранулярной форме (-) (+) Т-ОЛЛ
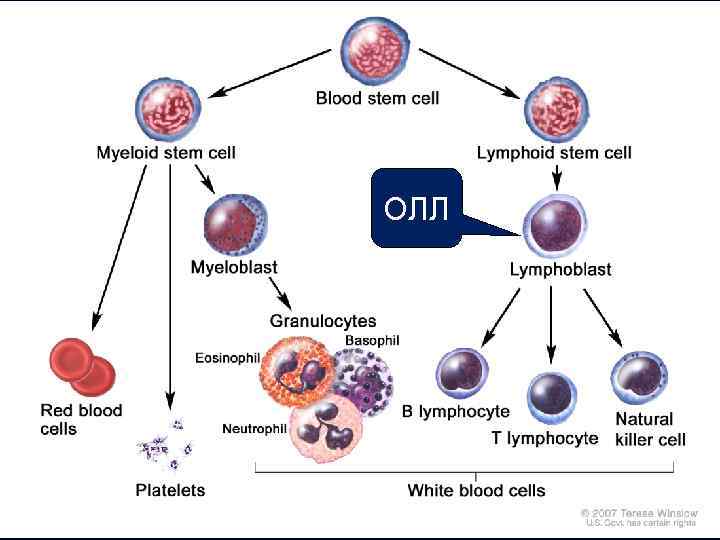
ОЛЛ
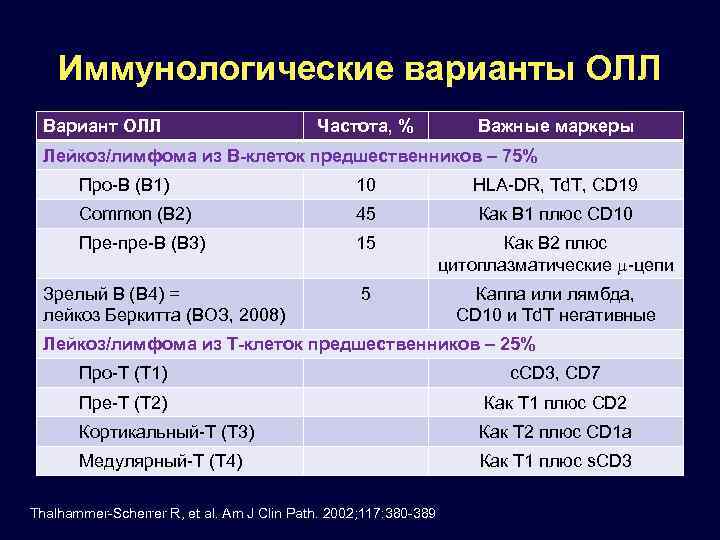
Иммунологические варианты ОЛЛ Вариант ОЛЛ Частота, % Важные маркеры Лейкоз/лимфома из В-клеток предшественников – 75% Про-В (B 1) 10 HLA-DR, Td. T, CD 19 Common (B 2) 45 Как B 1 плюс CD 10 Пре-пре-В (В 3) 15 Как B 2 плюс цитоплазматические -цепи 5 Каппа или лямбда, CD 10 и Td. T негативные Зрелый В (B 4) = лейкоз Беркитта (ВОЗ, 2008) Лейкоз/лимфома из Т-клеток предшественников – 25% Про-Т (Т 1) c. CD 3, CD 7 Пре-Т (Т 2) Как Т 1 плюс CD 2 Кортикальный-Т (Т 3) Как Т 2 плюс CD 1 a Медулярный-Т (Т 4) Как T 1 плюс s. CD 3 Thalhammer-Scherrer R, et al. Am J Clin Path. 2002; 117: 380 -389
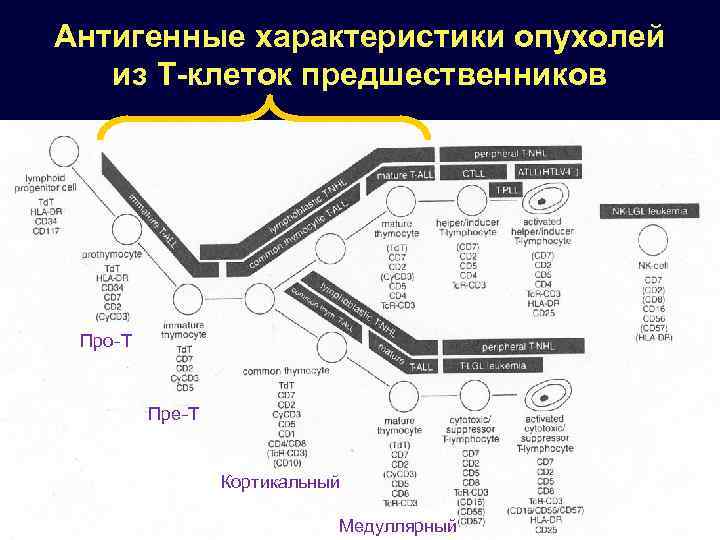
Антигенные характеристики опухолей из Т-клеток предшественников Про-Т Пре-Т Кортикальный Медуллярный
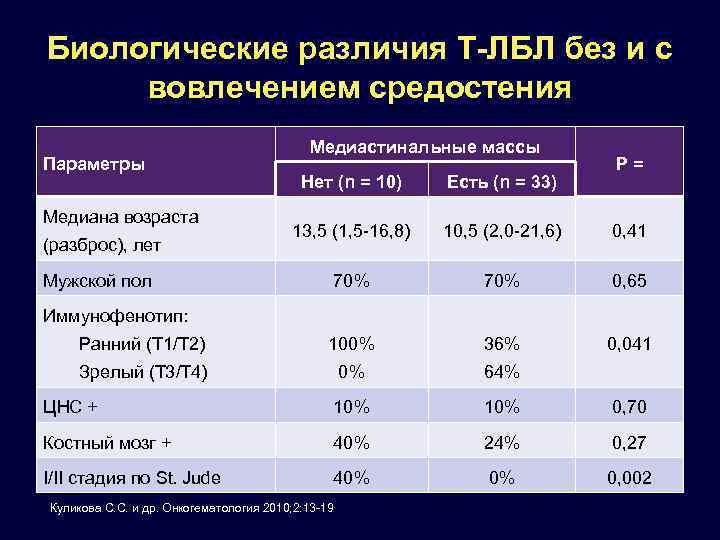
Биологические различия Т-ЛБЛ без и с вовлечением средостения Параметры Медиастинальные массы P= Нет (n = 10) Есть (n = 33) 13, 5 (1, 5 -16, 8) 10, 5 (2, 0 -21, 6) 0, 41 70% 0, 65 Ранний (Т 1/Т 2) 100% 36% 0, 041 Зрелый (Т 3/Т 4) 0% 64% ЦНС + 10% 0, 70 Костный мозг + 40% 24% 0, 27 I/II стадия по St. Jude 40% 0% 0, 002 Медиана возраста (разброс), лет Мужской пол Иммунофенотип: Куликова С. С. и др. Онкогематология 2010; 2: 13 -19
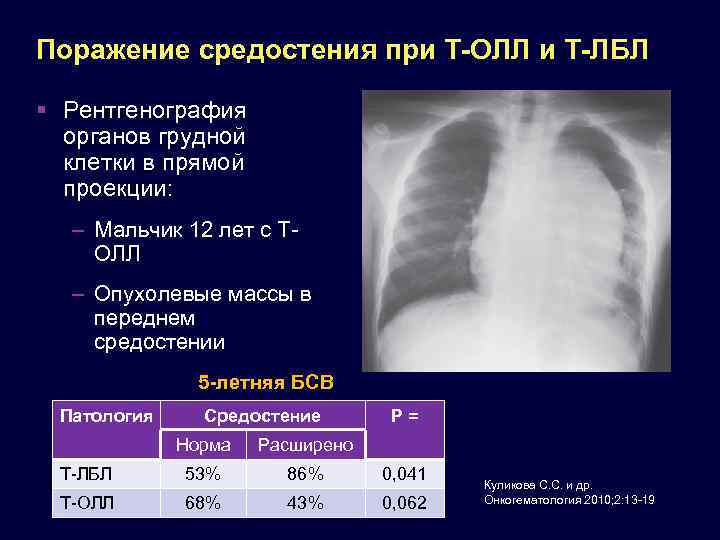
Поражение средостения при Т-ОЛЛ и Т-ЛБЛ Рентгенография органов грудной клетки в прямой проекции: – Мальчик 12 лет с ТОЛЛ – Опухолевые массы в переднем средостении 5 -летняя БСВ Патология Средостение Р= Норма Расширено Т-ЛБЛ 53% 86% 0, 041 Т-ОЛЛ 68% 43% 0, 062 Куликова С. С. и др. Онкогематология 2010; 2: 13 -19

Цитогенетические исследования Классическое цитогенетическое исследование (G-banding): - количественные нарушения - структурные нарушения хромосом FISH ПЦР
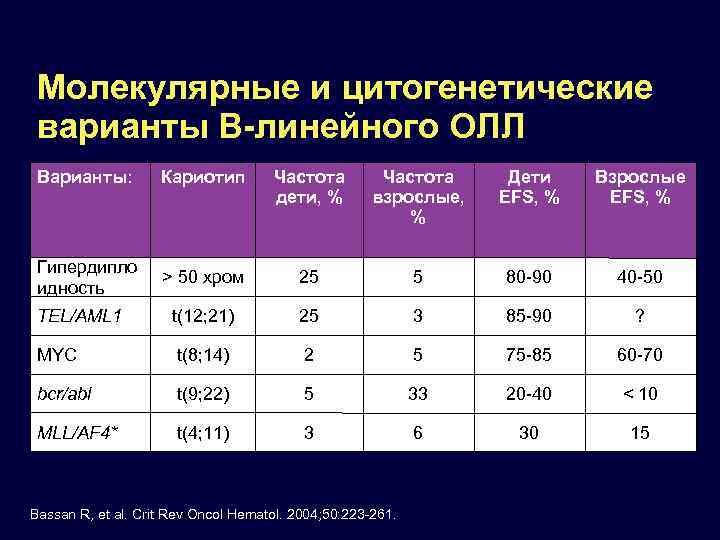
Молекулярные и цитогенетические варианты В-линейного ОЛЛ Варианты: Кариотип Частота дети, % Частота взрослые, % Дети EFS, % Взрослые EFS, % Гипердипло идность > 50 хром 25 5 80 -90 40 -50 TEL/AML 1 t(12; 21) 25 3 85 -90 ? MYC t(8; 14) 2 5 75 -85 60 -70 bcr/abl t(9; 22) 5 33 20 -40 < 10 MLL/AF 4* t(4; 11) 3 6 30 15 Bassan R, et al. Crit Rev Oncol Hematol. 2004; 50: 223 -261.
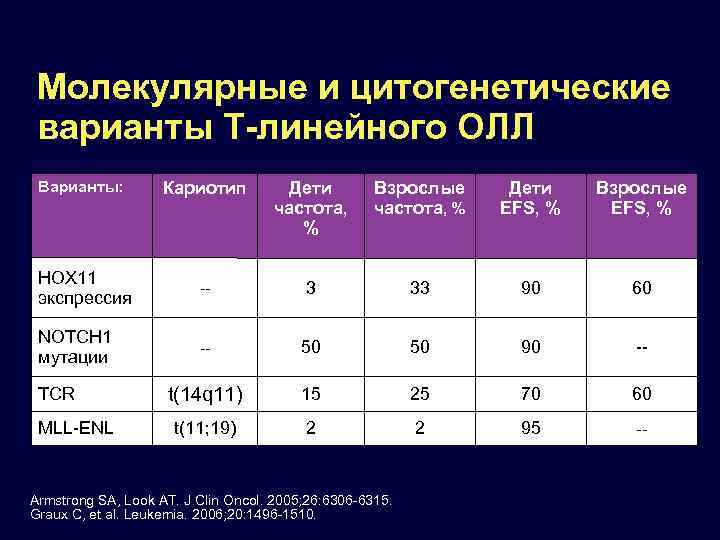
Молекулярные и цитогенетические варианты Т-линейного ОЛЛ Варианты: Кариотип Дети частота, % Взрослые частота, % Дети EFS, % Взрослые EFS, % HOX 11 экспрессия -- 3 33 90 60 NOTCH 1 мутации -- 50 50 90 -- t(14 q 11) 15 25 70 60 t(11; 19) 2 2 95 -- TCR MLL-ENL Armstrong SA, Look AT. J Clin Oncol. 2005; 26: 6306 -6315. Graux C, et al. Leukemia. 2006; 20: 1496 -1510.
В-ОЛЛ (FAB L 3): лейкоз Беркитта Чрезвычайно высокий пролиферативный потенциал и очень высокий уровень ЛДГ t(8; 14), t(2; 8), t(8; 22) – Транслокация между протоонкогеном myc на 8 -й хромосоме и локусом генов тяжелых цепей (хр. 14) или легких цепей (хромосомы 2 или 22)

Принципы лечения лейкоза Беркитта (В 4 ОЛЛ) Короткая интенсивная терапия, как при лимфоме Беркитта – Высокодозный MTX и циклофосфамид Интенсивная профилактика нейтролейкемии Нет пользы от поддерживающей терапии Излечиваются: 60%; рецидивы лишь в первые 6 мес
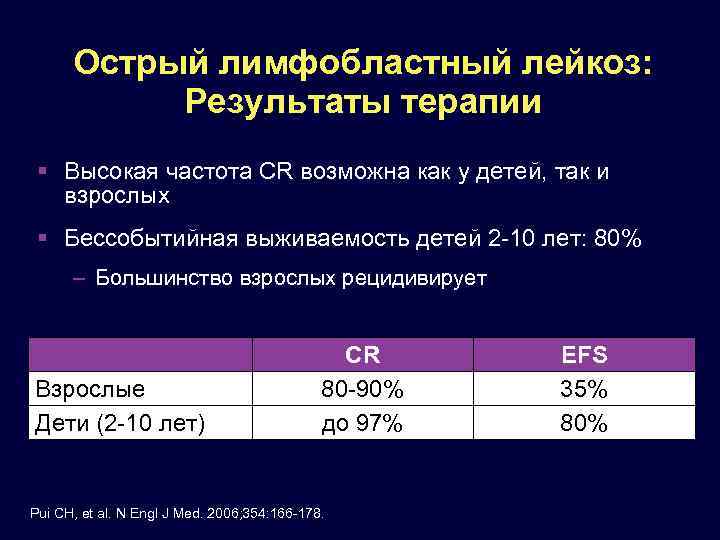
Острый лимфобластный лейкоз: Результаты терапии Высокая частота CR возможна как у детей, так и взрослых Бессобытийная выживаемость детей 2 -10 лет: 80% – Большинство взрослых рецидивирует Взрослые Дети (2 -10 лет) СR 80 -90% до 97% Pui CH, et al. N Engl J Med. 2006; 354: 166 -178. EFS 35% 80%

История методов лечения ОЛЛ 1948 - Sidney Farber et al. (New Engl J Med) – получил ремиссию ОЛЛ у ребенка с помощью Аминоптерина (антиметаболит) 1950 - Pearson et al. (JAMA) – описали противоопухолевый эффект АКТГ и кортизона при лимфомах и лейкозе 60 -е годы – комбинированная химиотерапия (Donald Pinkel) (Индукция VCR, PRED, L-Asp +консолидация 6 -MP, MTX) Начало 70 -х – ЦНС-направленная терапия (краниальное облучение + MTX i. th. ) Вторая половина 70 -х – „поздняя интенсификация“ (Hansjorg Riehm, BFM) 80 -е – стратегия стратификациии по группам риска Сейчас – стратификация лечения на основе достижений молекулярной генетики; ТАРГЕТНАЯ ТЕРАПИЯ
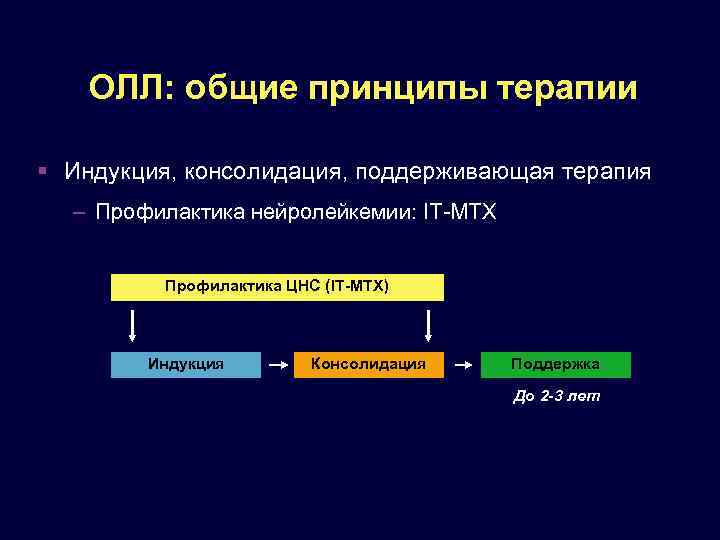
ОЛЛ: общие принципы терапии Индукция, консолидация, поддерживающая терапия – Профилактика нейролейкемии: IT-MTX Профилактика ЦНС (IT-MTX) Индукция Консолидация Поддержка До 2 -3 лет

Факторы риска у детей с ОЛЛ • • Стандартный риск - WBC < 50 тыс/мкл. - дети старше 1 года - ЦНС (-) • • • - нет Т-фенотипа - нет t(4; 11) и t(9; 22) - ремиссия на 36 день • • • Промежуточный риск - WBC > 50 тыс/мкл - дети < 1 года - ЦНС (+) - Т-иммунофенотип • Высокий риск • - t(4; 11) или t(9; 22) • - нет ремиссии на 36 день

Факторы прогноза у взрослых Стандартный риск – Возраст (непрерывная переменная; < 35 лет) – Число WBC (непрерывная переменная) – < 30, 000 для В-линейных – < 100, 000 для Т-линейных – T-клеточный ОЛЛ – ПР в первые 4 -е недели Коэкспрессия миелоидных маркеров: не влияет на БСВ – 20 -30% случаев ОЛЛ у взрослых Хромосомные и молекулярные изменения

Протоколы лечения на основе BFM Индукция фаза I (4 недели) – преднизолон, винкристин, рубомицин, L-аспарагиназа – не улучшает результаты добавление циклофосфана, высоких цитарабина и высоких доз антрациклинов Индукция фаза II (4 недели) – циклофосфан, цитарабин, 6 -МП Консолидация – 4 -7 циклов интенсивной ПХТ – Отсроченная реиндукция

Инициальные неотложные ситуации Гиперлейкоцитоз Опухоль средостения, компрессия В. П. В. /трахеи Олиго/анурия Гиперкалийемия Тяжелые инфекции

Профилактика нейролейкемии IT-MTX и системный HD-MTX Краниальное облучение – От него можно отказаться у пациентов получающих системную высокодозную терапию (MTX, ARA-C) и большой объем интратекальных введений MTX

L-аспарагиназа Используется только для лечения ОЛЛ и лимфобластных лимфом Фермент, вызывающий деплецию сывороточного L-аспарагина Нет миелосупрессии Не описаны отдаленные побочные эффекты Уникальный профиль токсичности

L-аспарагиназа: токсичность Гиперчувствительность – выработка нейтрализующих антител Печеночная токсичность – АЛТ/АСТ, билирубин, низкий альбумин Патология гемостаза – Кровотечения: снижение АТ III и протеина S Панкреатиты, сахарный диабет ЦНС-токсичность (сомноленция)

L-аспарагиназа у взрослых Нет рандомизированных исследований у взрослых Хорошо переносится взрослыми, но обычно суммарная доза дается меньше чем у детей В педиатрических исследованиях доказана целесообразность длительных режимов терапии L-аспарагиназой Исследований по образованию антител у взрослых нет

Пигелированная L-аспарагиназа (Онкоспар®) Пигелированная E. coli L-аспарагиназа Менее иммуногенная Длительный период полураспада У детей – Более быстрая редукция бластов в костном мозге – Низкая частота появления нейтрализующих антител – Профиль безопасности сходен с нативной L-асп. – Менее частые введения – Постоянная деплеция У взрослых аспарагина – Сходная токсичность с нативной формой после однократного и многократного введений Avramis VI, et al. Blood. 2002; 99: 1986 -1994. Panosyan EH, et al. J Pediatr Hematol Oncol. 2004; 26: 217 -226.

Лечение ОЛЛ у взрослых Большинство режимов взяты из педиатрических протоколов Мало рандомизированных клинических исследований по сравнению отдельных режимов или препаратов Менее интенсивные протоколы Во взрослых протоколах чаще происходят пропуски введений препаратов и/или нарушение тайминга
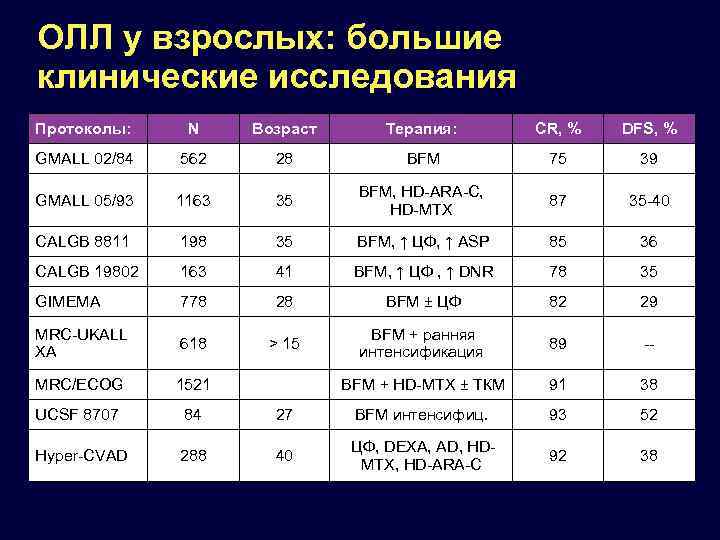
ОЛЛ у взрослых: большие клинические исследования Протоколы: N Возраст Терапия: CR, % DFS, % GMALL 02/84 562 28 BFM 75 39 GMALL 05/93 1163 35 BFM, HD-ARA-C, HD-MTX 87 35 -40 CALGB 8811 198 35 BFM, ↑ ЦФ, ↑ ASP 85 36 CALGB 19802 163 41 BFM, ↑ ЦФ , ↑ DNR 78 35 GIMEMA 778 28 BFM ± ЦФ 82 29 MRC-UKALL XA 618 > 15 BFM + ранняя интенсификация 89 -- MRC/ECOG 1521 BFM + HD-MTX ± ТКМ 91 38 UCSF 8707 84 27 BFM интенсифиц. 93 52 Hyper-CVAD 288 40 ЦФ, DEXA, AD, HDMTX, HD-ARA-C 92 38
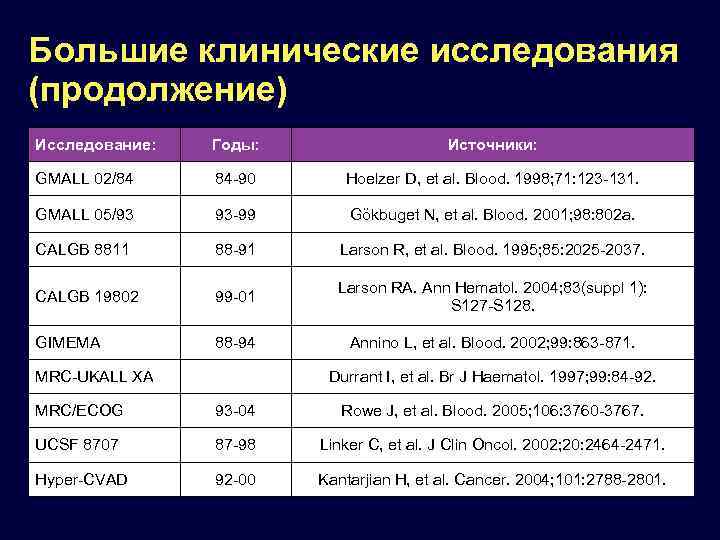
Большие клинические исследования (продолжение) Исследование: Годы: Источники: GMALL 02/84 84 -90 Hoelzer D, et al. Blood. 1998; 71: 123 -131. GMALL 05/93 93 -99 Gökbuget N, et al. Blood. 2001; 98: 802 a. CALGB 8811 88 -91 Larson R, et al. Blood. 1995; 85: 2025 -2037. CALGB 19802 99 -01 Larson RA. Ann Hematol. 2004; 83(suppl 1): S 127 -S 128. GIMEMA 88 -94 Annino L, et al. Blood. 2002; 99: 863 -871. MRC-UKALL XA Durrant I, et al. Br J Haematol. 1997; 99: 84 -92. MRC/ECOG 93 -04 Rowe J, et al. Blood. 2005; 106: 3760 -3767. UCSF 8707 87 -98 Linker C, et al. J Clin Oncol. 2002; 20: 2464 -2471. Hyper-CVAD 92 -00 Kantarjian H, et al. Cancer. 2004; 101: 2788 -2801.

Hyper-CVAD Цикл A – дексаметазон, винкристин, доксорубицин, циклофосфан Цикл B (после восстановления кроветворения) – Высокие дозы MTX и цитарабина – Без L-аспарагиназы Цикл A и B повторяют 4 раза (8 циклов) Kantarjian H, et al. J Clin Oncol. 2000; 18: 547 -561.

Hyper-CVAD для лечения ОЛЛ взрослых Сравнение режимов hyper-CVAD и VAD у первичных больных с ОЛЛ Результаты: Hyper-CVAD (N = 204) VAD (N = 222) CR, % 38 32 5 -летняя OS, % 39 21 Kantarjian et al. J Clin Oncol. 2000; 18: 547 -561.

ОЛЛ: поддерживающая терапия Еженедельно метотрексат + ежедневно 6 -МП – периодически пульсы VCR/стероиды Продолжительность: до 2 -3 лет Польза не доказана для B-ОЛЛ и Ph+ ОЛЛ Если не проводится — плохой прогноз !!! По взрослым рандомизированных исследований по поддерживающей терапии нет

6 -меркаптопурин 6 -доза подбирается по числу лейкоцитов крови еженедельно – Выше чувствительность у пациентов с дефицитом пуринметилтрансферазы Контроль печеночных ферментов – АЛТ/АСТ быстро восстанавливаются после отмены 6 -МП – Не следует снижать дозу 6 -МП или прерывать терапию при легкой токсичности (1 -2 степень)
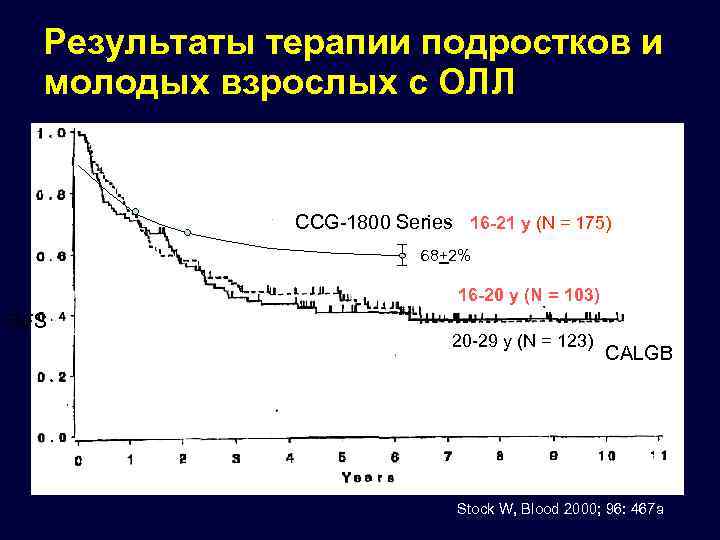
Результаты терапии подростков и молодых взрослых с ОЛЛ CCG-1800 Series 16 -21 y (N = 175) 68+2% 16 -20 y (N = 103) DFS 20 -29 y (N = 123) CALGB Stock W, Blood 2000; 96: 467 a
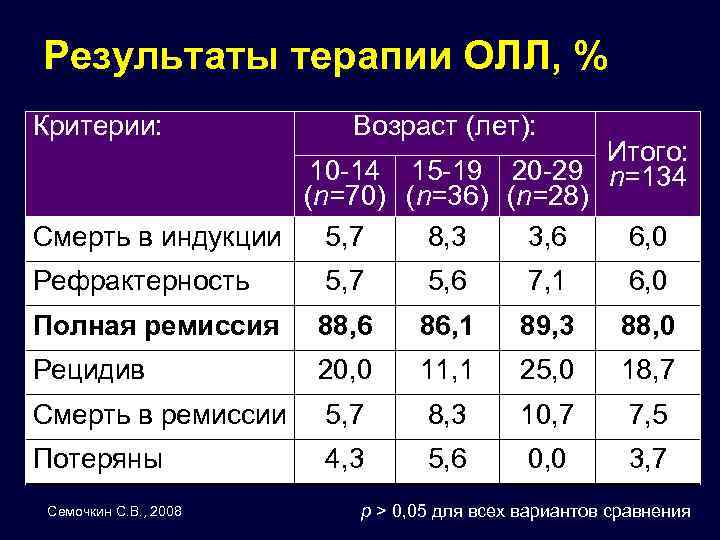
Результаты терапии ОЛЛ, % Критерии: Возраст (лет): Итого: 10 -14 15 -19 20 -29 n=134 (n=70) (n=36) (n=28) Смерть в индукции 5, 7 8, 3 3, 6 6, 0 Рефрактерность 5, 7 5, 6 7, 1 6, 0 Полная ремиссия 88, 6 86, 1 89, 3 88, 0 Рецидив 20, 0 11, 1 25, 0 18, 7 Смерть в ремиссии 5, 7 8, 3 10, 7 7, 5 Потеряны 4, 3 5, 6 0, 0 3, 7 Семочкин С. В. , 2008 p > 0, 05 для всех вариантов сравнения
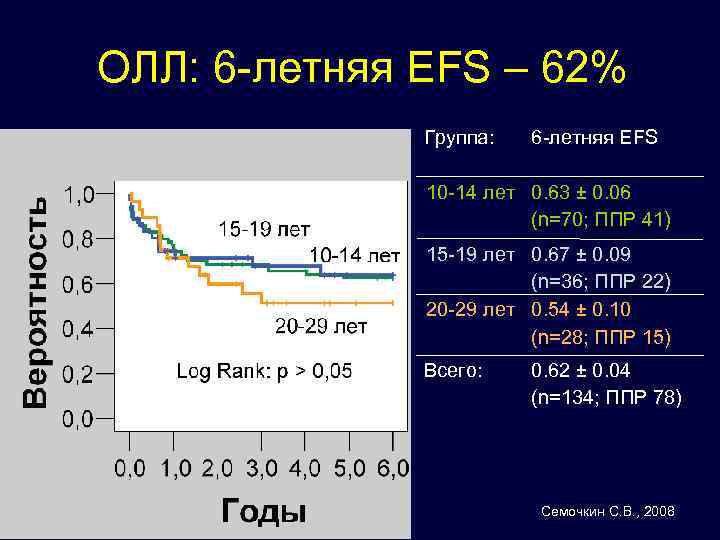
ОЛЛ: 6 -летняя EFS – 62% Группа: 6 -летняя EFS 10 -14 лет 0. 63 ± 0. 06 (n=70; ППР 41) 15 -19 лет 0. 67 ± 0. 09 (n=36; ППР 22) 20 -29 лет 0. 54 ± 0. 10 (n=28; ППР 15) Всего: 0. 62 ± 0. 04 (n=134; ППР 78) Семочкин С. В. , 2008
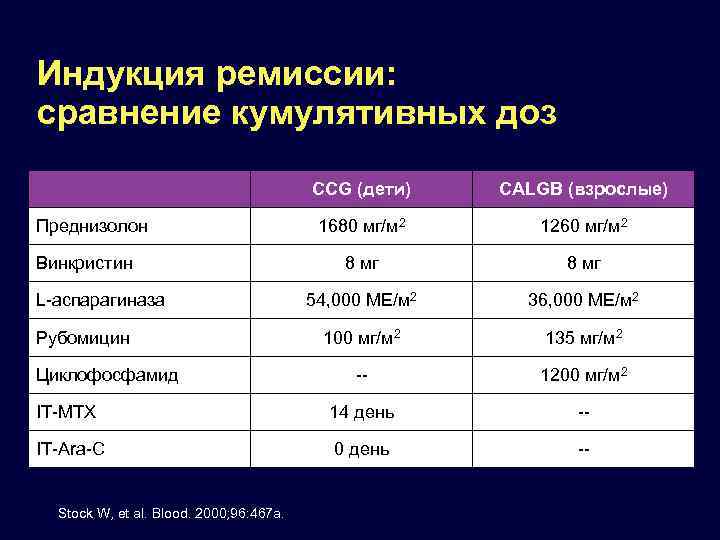
Индукция ремиссии: сравнение кумулятивных доз CCG (дети) CALGB (взрослые) 1680 мг/м 2 1260 мг/м 2 8 мг 54, 000 МЕ/м 2 36, 000 МЕ/м 2 100 мг/м 2 135 мг/м 2 -- 1200 мг/м 2 IT-MTX 14 день -- IT-Ara-C 0 день -- Преднизолон Винкристин L-аспарагиназа Рубомицин Циклофосфамид Stock W, et al. Blood. 2000; 96: 467 a.
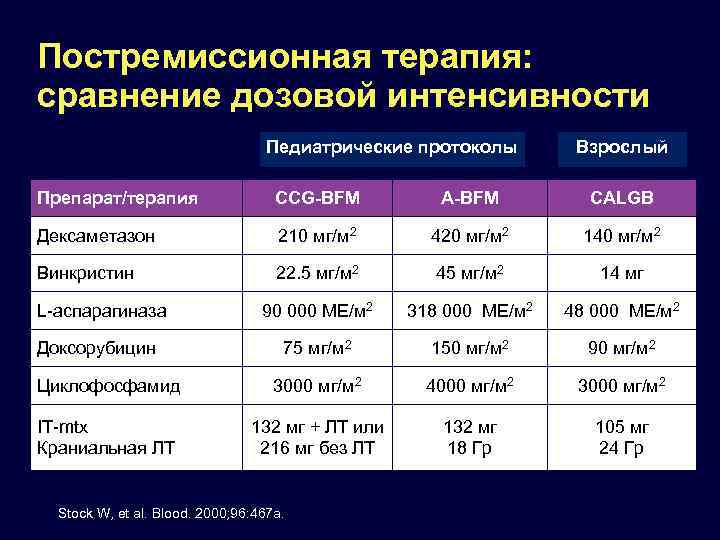
Постремиссионная терапия: сравнение дозовой интенсивности Педиатрические протоколы Взрослый Препарат/терапия CCG-BFM A-BFM CALGB Дексаметазон 210 мг/м 2 420 мг/м 2 140 мг/м 2 Винкристин 22. 5 мг/м 2 45 мг/м 2 14 мг 90 000 МЕ/м 2 318 000 МЕ/м 2 48 000 МЕ/м 2 75 мг/м 2 150 мг/м 2 90 мг/м 2 Циклофосфамид 3000 мг/м 2 4000 мг/м 2 3000 мг/м 2 IT-mtx Краниальная ЛТ 132 мг + ЛТ или 216 мг без ЛТ 132 мг 18 Гр 105 мг 24 Гр L-аспарагиназа Доксорубицин Stock W, et al. Blood. 2000; 96: 467 a.

Трансплантация костного мозга: рекомендации CIMBTR В первой ремиссии – Для пациентов группы высокого риска – Для пациентов стандартного риска не показана – Ауто-ТКМ: нет пользы по сравнению с ПХТ Во второй ремиссии – аллогенная ТКМ Hahn T, et al. Biol Blood Marrow Transplant. 2006; 12: 1 -30.
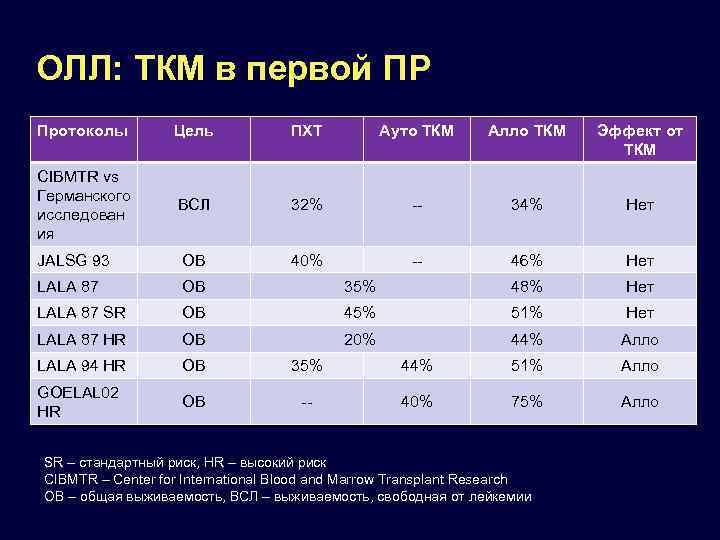
ОЛЛ: ТКМ в первой ПР Протоколы Цель ПХТ Ауто ТКМ Алло ТКМ Эффект от ТКМ CIBMTR vs Германского исследован ия ВСЛ 32% -- 34% Нет JALSG 93 ОВ 40% -- 46% Нет LALA 87 ОВ 35% 48% Нет LALA 87 SR ОВ 45% 51% Нет LALA 87 HR ОВ 20% 44% Алло LALA 94 HR ОВ 35% 44% 51% Алло GOELAL 02 HR ОВ -- 40% 75% Алло SR – стандартный риск, HR – высокий риск CIBMTR – Center for International Blood and Marrow Transplant Research ОВ – общая выживаемость, ВСЛ – выживаемость, свободная от лейкемии
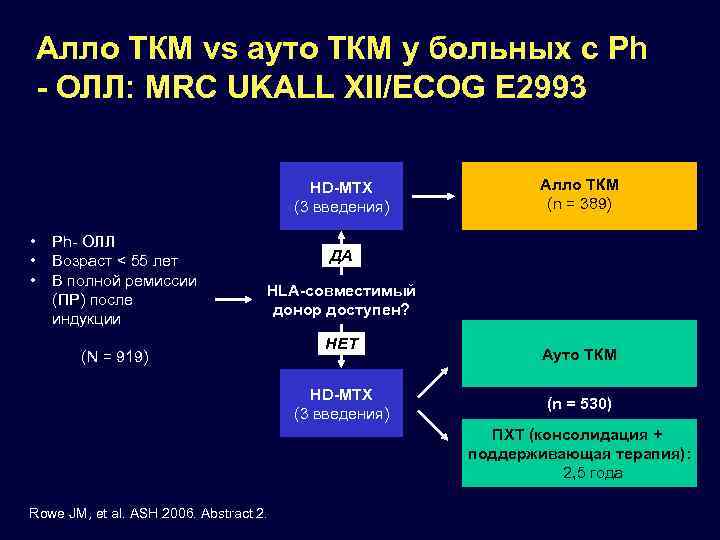
Алло ТКМ vs ауто ТКМ у больных с Ph - ОЛЛ: MRC UKALL XII/ECOG E 2993 HD-MTX (3 введения) • • • Ph- ОЛЛ Возраст < 55 лет В полной ремиссии (ПР) после индукции Алло ТКМ (n = 389) ДА HLA-совместимый донор доступен? (N = 919) НЕТ HD-MTX (3 введения) Ауто ТКМ (n = 530) ПХТ (консолидация + поддерживающая терапия): 2, 5 года Rowe JM, et al. ASH 2006. Abstract 2.
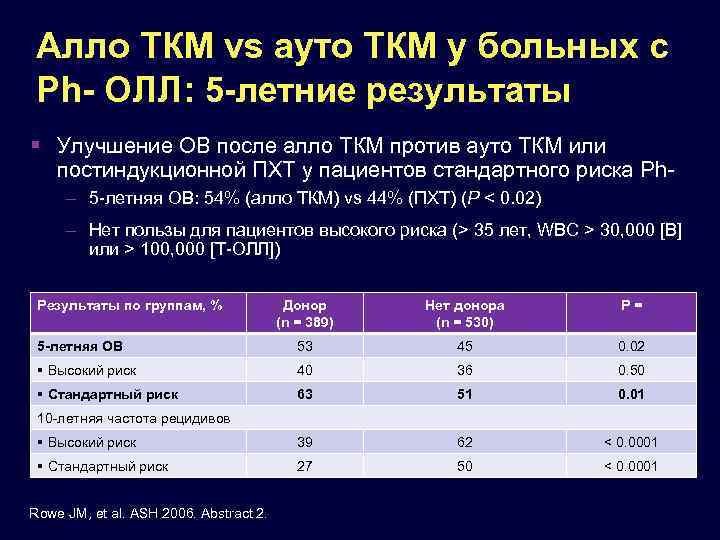
Алло ТКМ vs ауто ТКМ у больных с Ph- ОЛЛ: 5 -летние результаты Улучшение ОВ после алло ТКМ против ауто ТКМ или постиндукционной ПХТ у пациентов стандартного риска Ph– 5 -летняя ОВ: 54% (алло ТКМ) vs 44% (ПХТ) (P < 0. 02) – Нет пользы для пациентов высокого риска (> 35 лет, WBC > 30, 000 [B] или > 100, 000 [T-ОЛЛ]) Результаты по группам, % Донор (n = 389) Нет донора (n = 530) P= 5 -летняя ОВ 53 45 0. 02 Высокий риск 40 36 0. 50 Стандартный риск 63 51 0. 01 Высокий риск 39 62 < 0. 0001 Стандартный риск 27 50 < 0. 0001 10 -летняя частота рецидивов Rowe JM, et al. ASH 2006. Abstract 2.
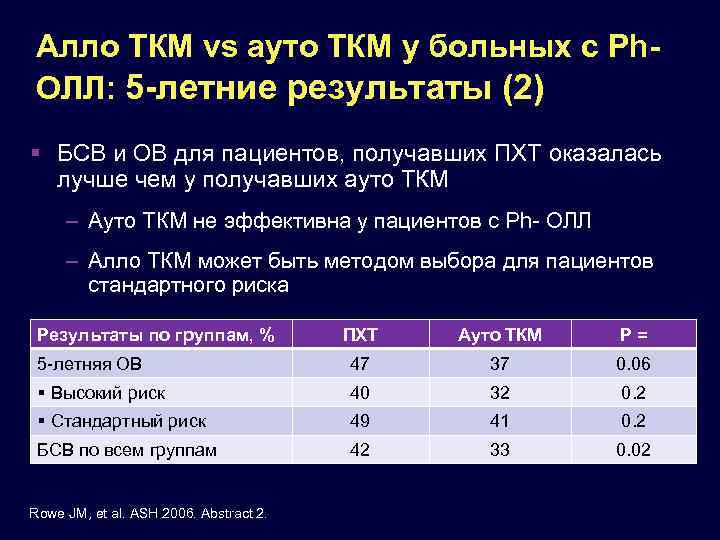
Алло ТКМ vs ауто ТКМ у больных с Ph. ОЛЛ: 5 -летние результаты (2) БСВ и ОВ для пациентов, получавших ПХТ оказалась лучше чем у получавших ауто ТКМ – Ауто ТКМ не эффективна у пациентов с Ph- ОЛЛ – Алло ТКМ может быть методом выбора для пациентов стандартного риска Результаты по группам, % ПХТ Ауто ТКМ P= 5 -летняя ОВ 47 37 0. 06 Высокий риск 40 32 0. 2 Стандартный риск 49 41 0. 2 БСВ по всем группам 42 33 0. 02 Rowe JM, et al. ASH 2006. Abstract 2.

ОЛЛ у пожилых больных Низкая частота CR и плохая EFS Снижается частота T-ОЛЛ Высокая частота Ph-позитивного ALL Исключаются из клинических исследований Часто проводится редуцированная терапия

Осложнения у пожилых с ОЛЛ Сопутствующие болезни Более тяжелые мукозиты Типичные проблемы – Винкристин: нейропатия, запоры – Стероиды: гипергликемия, инфекции – L-аспарагиназа: энцефалопатия Плохое восстановление гемопоэза – Добавление G-CSF повышает частоту CR
Лечение Ph-позитивного ОЛЛ: место ингибиторов тирозинкиназ

Ph-позитивный ОЛЛ t(9; 22) bcr/abl В-линейные ОЛЛ Частота растет с возрастом – Редко у детей; 50% у взрослых старше 55 лет Очень плохой прогноз – Практически невозможно излечение на ПХТ – Эффективна алло-ТКМ – Ниже частота ответов, чем при других вариантах ОЛЛ

Варианты белков, кодируемых генами BCR-ABL • р 210 BCR-ABL – ХМЛ • р 190 BCR-ABL – Ph+ ALL • р 230 BCR-ABL – «зрелый» ХМЛ • Ph+ ALL Взрослые р190 – 50 -70% р210 – 30 -50% Дети р190 – 85% р210 – 15% Иммунофенотип: В-линейный (CD 10+, CD 19+, Td. T+) Коэкспрессия СD 13, CD 33
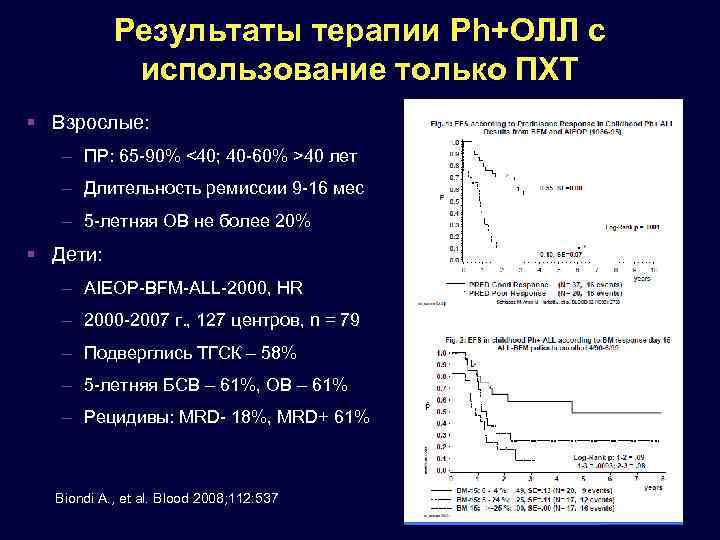
Результаты терапии Ph+ОЛЛ с использование только ПХТ Взрослые: – ПР: 65 -90% <40; 40 -60% >40 лет – Длительность ремиссии 9 -16 мес – 5 -летняя ОВ не более 20% Дети: – AIEOP-BFM-ALL-2000, HR – 2000 -2007 г. , 127 центров, n = 79 – Подверглись ТГСК – 58% – 5 -летняя БСВ – 61%, ОВ – 61% – Рецидивы: MRD- 18%, MRD+ 61% Biondi A. , et al. Blood 2008; 112: 537

Роль алло ТКМ (до иматиниба) 1986 -1996 г. 1995 -2005 г. 10 кооперированных групп 14 кооперированных групп – N = 326 (дети) – N = 640 (дети) – ПР – 82% – ПР – 89% – 7 -летняя БСВ – 25%, ОВ – 36% – 7 -летняя БСВ – 31%, ОВ – 44% Родственная ТКМ против ПХТ: – ОВ: 72% vs 42% (p = 0, 002) – БСВ: 65% vs 25% (р < 0, 001) – ОВ: 54% vs 48% (p > 0, 05) – БСВ: 48% vs 34% (p < 0, 05) Arico M. , et al. New Engl J Med 2000$342: 998 -1006 Arico M, et al. Blood 2008; 112: 213

Иматиниб в лечении Ph+ ОЛЛ Монотерапия — высокая частота CR – ответы не продолжительны: 1 -3 мес В качестве компонента протоколов ПХТ – Выше частота CR: 90 -97% и лучше результаты ПХТ[1, 2] – Больше пациентов доживают до ТКМ[3] – Лучше результаты ТКМ [3] – Одновременное назначение гливека и ПХТ лучше чем альтернирующий режим[4] 1. Thomas DA, et al. Blood. 2004; 103: 4396 -4407. 2. Yanada M, et al. J Clin Oncol. 2006; 24: 460 -464. 3. Lee S, et al. Blood. 2005; 105: 3449 -3457. 4. Wassmann B, et al. Blood. 2006; 108: 14691477.

Европейский педиатрический протокол Es. Ph. ALL для Ph+ОЛЛ (2004 г. ) «Плохой риск» «Хороший риск» – > 1000 бл. /мкл в крови на 8 день – < 1000 бл. /мкл в крови на 8 день – > 15% бластов в к. м. на 15 день – < 15% бластов в к. м. на 15 день – > 5% на 21 день – < 5% на 21 день – Нет ПР после индукции – ПР после индукции Иматиниб без рандомизации Показания для ТКМ: любой донор, включая гаплоидентичного Рандомизация с или без иматиниба Показания к ТКМ: наличие родственного донора 70% - подверглись ТКМ С 2010 г. внесены изменения: Camitta B. Hematology 2010: 731 – Иматиниб всем без рандомизации с 15 дня – Сокращены показания к ТГСК – После алло ТГСК – 1 год непрерывно иматиниб
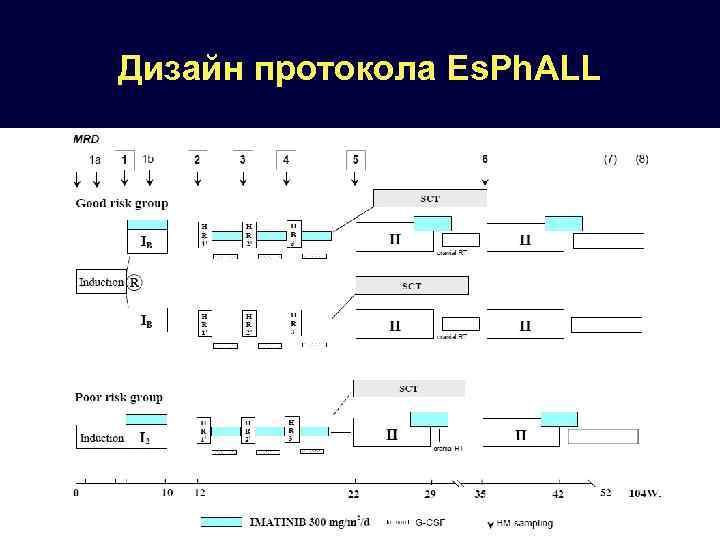
Дизайн протокола Es. Ph. ALL

COG stady AALL 0031 (2002 -2006 г. ) Старт иматиниба после индукции, на фоне высокоинтенсивной консолидирующей циклической терапии (Cph, VCR, ADR, Pred, HD-Mtx, Mtx+6 -MP) Ступенчатое увеличение продолжительности и дозы иматиниба (5 когорт) Наилучшие результаты (5 когорта)– 2, 3 года терапии: доза иматиниба 340 мг/м 2, непрерывный режим во время интенсивной терапии, поддерживающая терапия 3 -years EFS – 88% (историч. контроль – ПХТ - 35%, родственная ТГСК – 77% n-13, неродственная ТГСК – 83%, n-6) 40% пациентов подверглись алло-ТГСК Schultz KR, Bowman WP, Aledo A et al. J. Clin. Oncol. 27(31), 51755181 (2009).
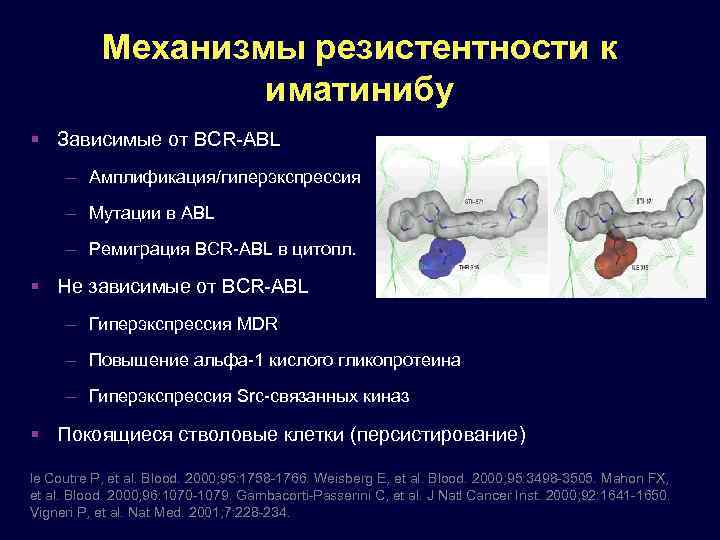
Механизмы резистентности к иматинибу Зависимые от BCR-ABL – Амплификация/гиперэкспрессия – Мутации в ABL – Ремиграция BCR-ABL в цитопл. Не зависимые от BCR-ABL – Гиперэкспрессия MDR – Повышение альфа-1 кислого гликопротеина – Гиперэкспрессия Src-связанных киназ Покоящиеся стволовые клетки (персистирование) le Coutre P, et al. Blood. 2000; 95: 1758 -1766. Weisberg E, et al. Blood. 2000; 95: 3498 -3505. Mahon FX, et al. Blood. 2000; 96: 1070 -1079. Gambacorti-Passerini C, et al. J Natl Cancer Inst. 2000; 92: 1641 -1650. Vigneri P, et al. Nat Med. 2001; 7: 228 -234.

Второе поколение ИТК Нилотиниб (Тасигна): Дазатиниб (Спрайсел) – – в 30 раз эффективнее иматиниба+ – в 325 раз эффективнее иматиниба+ – Незначительные структурные отличия от иматиниба – иная химическая структура, – лучшее связывание с ABL -тирозинкиназой – воздействие на множество киназных мишеней +Подавление жизнедеятельности клеток in vitro

Дазатиниб при ОЛЛ В патогенезе Ph+ ОЛЛ показана роль киназ семейства SRC Проникает через ГЭБ, создавая в ликворе терапевтические концентрации Побочные д-я: отеки, фотосенсибилизация, мукозит, цитопения, легочные инфильтраты, гидроторакс, гидроперикард, отек легких С 2008 г. одобрен для применения в РФ для терапии ХМЛ и Ph+ОЛЛ при резистентности и непереносимости предыдущей терапии у взрослых.

Использование дазатиниба при Ph+ОЛЛ у взрослых Взрослые, с 2006 г. – рефрактерные Ph+ОЛЛ – у 50% достигнута генетическая ремиссия (исключение – мутация Т 315 I) 2010 г. – 35 взрослых (средний возраст 53 г, 21 -79 лет) (Ravandi et all. ) - Hyper-CVAD + дазатиниб (14 дней между курсами) - 94% вышли в ремиссию, 1 -л EFS – 57% У 7 из 11 пациентов с нейролейкозом достигнута санация ликвора, причем у 4 – без интратекальных введений, монотерапия дазатинибом (Porkka K. )
Лечение рецидивов острого лимфобластного лейкоза Рецидивы Т-ОЛЛ
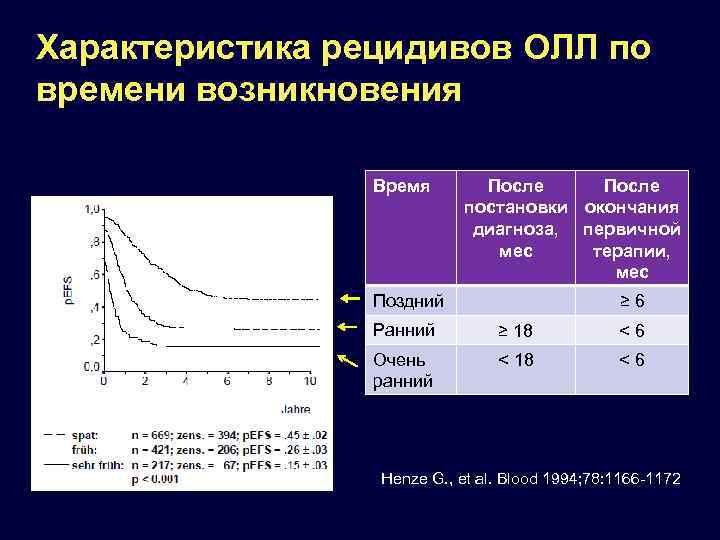
Характеристика рецидивов ОЛЛ по времени возникновения Время После постановки окончания диагноза, первичной мес терапии, мес Поздний ≥ 6 Ранний ≥ 18 < 6 Очень ранний < 18 < 6 Henze G. , et al. Blood 1994; 78: 1166 -1172
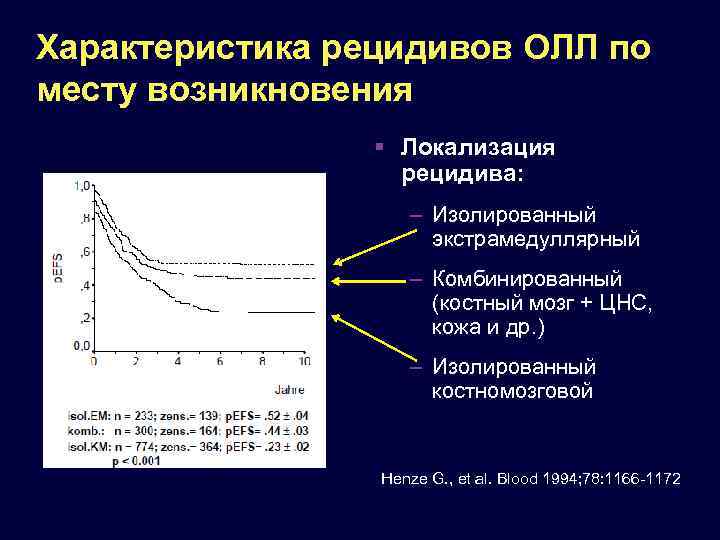
Характеристика рецидивов ОЛЛ по месту возникновения Локализация рецидива: – Изолированный экстрамедуллярный – Комбинированный (костный мозг + ЦНС, кожа и др. ) – Изолированный костномозговой Henze G. , et al. Blood 1994; 78: 1166 -1172
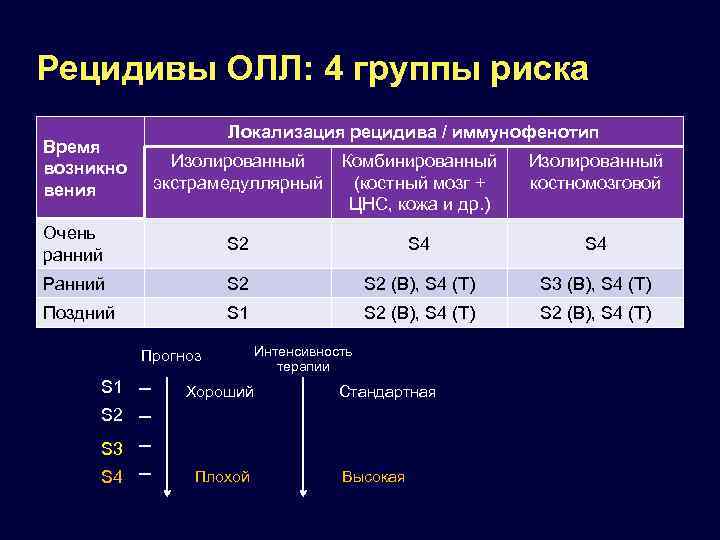
Рецидивы ОЛЛ: 4 группы риска Время возникно вения Локализация рецидива / иммунофенотип Изолированный экстрамедуллярный Комбинированный (костный мозг + ЦНС, кожа и др. ) Изолированный костномозговой Очень ранний S 2 S 4 Ранний S 2 (B), S 4 (T) S 3 (B), S 4 (T) Поздний S 1 S 2 (B), S 4 (T) Прогноз S 1 Хороший Интенсивность терапии Стандартная S 2 S 3 S 4 Плохой Высокая

ОЛЛ: новые химиопрепараты Винкаалкалоиды: – Винорельбин Антиметаболиты: – Неларабин (Атрианс®, рецидивы T-ОЛЛ и ЛБЛ) – Клофарабин (Эволтра®) – Триметрексат (ингибитор дегидрофолатредуктазы) Липосомальные и пигелированные препараты: – Пигелированная L-аспарагиназа (Онкоспар®) – Липосомальный даунорубицин (Даунозом®) – Липосомальный винкристин (VSLI®) – Липосомальный цитарабин (интратекально)

Винорельбин в терапии ОЛЛ Препарат из группы алкалоидов барвинка Механизм действия: – Подавляет полимеризацию тубулина, связываясь с митотическими микротрубочками, – Блокирует деление клеток в метафазе G 2 -M Дозирование: вводится в/в в средней дозе 25 -30 мг/м 2. Нет ограничения по дозе как у винкристина! Самые частые побочные эффекты: – нейтропения, – инфекционные осложнения Нейтротоксичность - ограниченна

Схемы на основе винорельбина Схема NND: – Винорельбин (навельбин) – 25 мг/м 2 в 1 и 8 -й день – Митоксантрон (новантрон) – 10 мг/м 2 в 1 -3 дни – Дексаметазон 10 мг/м 2 в 1 -7 дни в/в или р. о. Схема NNDF: – Винорельбин, митоксантрон и дексаметазон – как в схеме NND – Флударабин 25 мг/м 2 в 1 -3 дни Ритуксимаб 375 мг/м 2 в 1, 8, 15 и 22 дни: – для CD 20 -позитивных случаев Uckun FM, et al. BJH 2006; 135: 500 -508

Неларабин (Атрианс®) Показания к применению: – Рецидивирующие или рефрактерные к химиотерапии Тклеточный ОЛЛ и ЛБЛ – Показания основаны на индукции полной ремиссии в ряде клинических исследований – Рандомизированные клинические исследования, которые могли бы показать увеличение выживаемости или другую клиническую пользу, не проводились Неларабин – пролекарство аналога дезоксигуанозина - 9 -b-D-арабинофуранозилгуанина (ara-G)

Неларабин: клинические данные Два опорных исследования II фазы: CALGB 19801 - взрослые (≥ 16 лет) [1] – 1500 мг/м 2 в/в за 2 часа в 1, 3 и 5 дни, каждый 21 день COG P 9673 – дети (< 16 лет) [2] – 650 мг/м 2 в/в за 1 час с 1 по 5 день каждый 21 день 1. De. Angelo et al. Blood 2002, 2007 2. Berg et al. JCO 2005
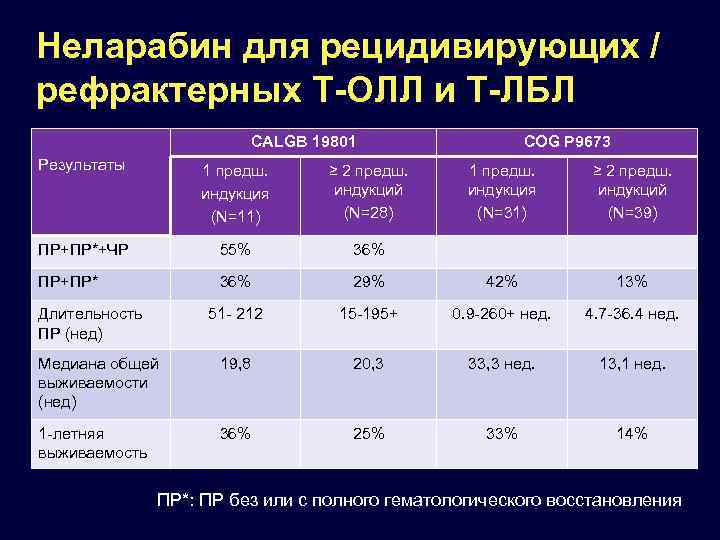
Неларабин для рецидивирующих / рефрактерных T-ОЛЛ и Т-ЛБЛ CALGB 19801 Результаты 1 предш. индукция (N=11) ≥ 2 предш. индукций (N=28) ПР+ПР*+ЧР 55% 36% ПР+ПР* 36% COG P 9673 1 предш. индукция (N=31) ≥ 2 предш. индукций (N=39) 29% 42% 13% 51 - 212 15 -195+ 0. 9 -260+ нед. 4. 7 -36. 4 нед. Медиана общей выживаемости (нед) 19, 8 20, 3 33, 3 нед. 13, 1 нед. 1 -летняя выживаемость 36% 25% 33% 14% Длительность ПР (нед) ПР*: ПР без или с полного гематологического восстановления
![Клофарабин (Эволтра®) для ОЛЛ Дети (N = 61)[1] Медиана – 3 линии предшествующей терапии Клофарабин (Эволтра®) для ОЛЛ Дети (N = 61)[1] Медиана – 3 линии предшествующей терапии](https://present5.com/presentation/175305606_278732067/image-73.jpg)
Клофарабин (Эволтра®) для ОЛЛ Дети (N = 61)[1] Медиана – 3 линии предшествующей терапии 52 мг/м 2 с 1 по 5 день – CR + CR* - 12 (20%) пациентов; PR - 6 (10%) – Медиана выживаемости: 13 недель – 9 ответивших получили ТКМ Взрослые (N = 12)[2] – 40 мг/м 2 1 -5 дни – ПР - 2 (17%) пациента 1. Jeha S, et al. J Clin Oncol. 2006; 24: 1917 -1923. 2. Kantarjian H, et al. Blood. 2003; 102: 2379 -2386.
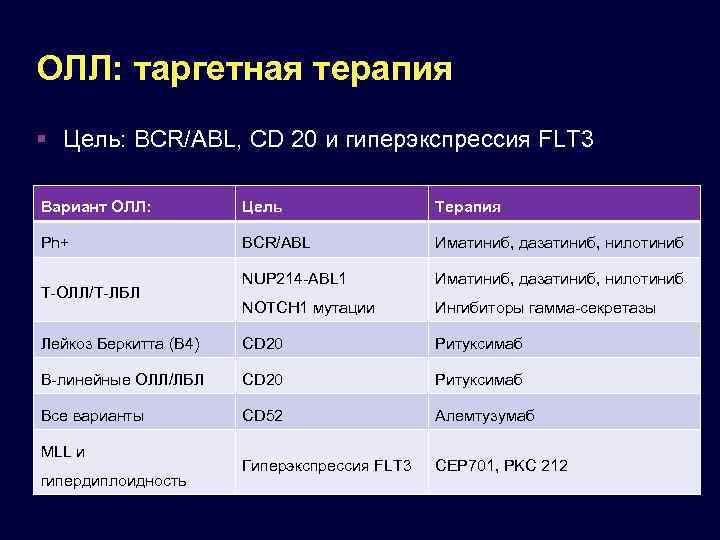
ОЛЛ: таргетная терапия Цель: BCR/ABL, CD 20 и гиперэкспрессия FLT 3 Вариант ОЛЛ: Цель Терапия Ph+ BCR/ABL Иматиниб, дазатиниб, нилотиниб NUP 214 -ABL 1 Иматиниб, дазатиниб, нилотиниб NOTCH 1 мутации Ингибиторы гамма-секретазы Лейкоз Беркитта (В 4) CD 20 Ритуксимаб В-линейные ОЛЛ/ЛБЛ CD 20 Ритуксимаб Все варианты CD 52 Алемтузумаб Гиперэкспрессия FLT 3 CEP 701, PKC 212 T-ОЛЛ/Т-ЛБЛ MLL и гипердиплоидность
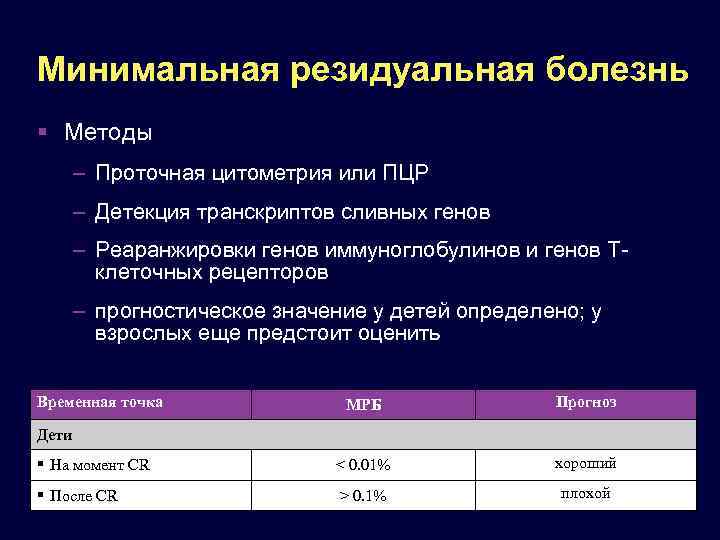
Минимальная резидуальная болезнь Методы – Проточная цитометрия или ПЦР – Детекция транскриптов сливных генов – Реаранжировки генов иммуноглобулинов и генов Tклеточных рецепторов – прогностическое значение у детей определено; у взрослых еще предстоит оценить Временная точка МРБ Прогноз На момент CR < 0. 01% хороший После CR > 0. 1% плохой Дети

Заключение Взрослые должны лечиться в рамках клинических исследований Необходимы протоколы для подростков и ЛМВ Для взрослых с Ph-ОЛЛ: иматиниб Алло-ТСК для пациентов высокого риска Режимы на основе контроля МРБ Селекция групп пациентов для таргетной терапии (Т-ОЛЛ и Т-ЛБЛ → неларабин) Появление новых молекулярных маркеров и новых мишеней для направленной терапии
ALL.ppt