Острый лейкоз .ppt
- Количество слайдов: 54
ОСТРЫЕ ЛЕЙКОЗЫ проф. Тенюков В. В Чебоксары – 2011 г.

ОСТРЫЕ ЛЕЙКОЗЫ Острый лейкоз – это заболевание из группы гемобластозов, злокачественная опухоль кроветворной ткани, исходящая из костного мозга, патоморфологическим субстратом которой являются лейкозные бластные клетки, соответствующие родоначальным элементам одного из ростков кроветворения.

ГЕМОБЛАСТОЗАМИ называют группу опухолей, возникших из кроветворных клеток. ОПУХОЛЬЮ называют плохо контролируемую организмом плюс-ткань, которая возникла из одной мутировавшей клетки. ЛЕЙКОЗЫ - это гемобластозы, при которых костный мозг повсеместно заселен опухолевыми клетками. ЛЕЙКОЗЫ - опухоль, исходящая из родоначальных (стволовых) кроветворных клеток с первичным поражением костного мозга.

Кроме лейкозов, в группу гемобластозов входят гематосаркомы, возникшие из кроветворных клеток, но представляющие собой внекостномозговые разрастания бластных клеток. Несколько реже других гемобластозов встречаются лимфоцитомы опухоли, состоящие из зрелых лимфоцитов или образованные разрастаниями, идентичными лимфатическому узлу, но мало или совсем не поражающие костный мозг.

• Выделяют лейкозы острые и хронические. Форма заболевания определяется не длительностью и остротой клинических проявлений, а строением опухолевых клеток. Так, к острым отнесены лейкозы, клеточный субстрат которых представлен бластами (незрелыми клетками), а к хроническим - лейкозы, при которых основная масса опухолевых клеток дифференцирована и состоит в основном из зрелых элементов.

• Согласно мировой статистике, 3, 3 -4, 7 детей из 100 тысяч заболевают лейкемией в возрасте до 15 лет. Около 40 -46 % случаев приходится на детей 2 -6 лет.

Схема гемопоэза Стволовая клетка крови Клетка предшественница миелопоэза Клетка предшественница лимфопоэза лейкопоэтин эритропоэтин тромбопоэтин миелобласт эритробласт мегакариобласты промиелоцит проэритроцит промегакариоцит Сегментояд. лейкоциты, моноциты ретикулоцит эритроцит Зрелые клетки мегакариоцит тромбоциты Созревающие клетки

Схема гемопоэза Клетка предшественница лимфопоэза Клетка предшественница Т-лимфоцитов Т-лимфобласт Т-иммунобласт В-лимфобласт В-иммунобласт В-пролимфоцит Т-лимфоцит Клетка предшественница В-лимфоцитов Активированный Т-лимфоцит В-лимфоцит Зрелые клетки проплазмоцит

ОСТРЫЕ ЛЕЙКОЗЫ Диагноз впервые поставлен немецким врачем Фредвейх в 1857 г. и русским врачем Славянским в 1867 г. , которые сообщили о быстро прогрессирующем лейкозном процессе. В 1889 г. Эпштейном острый лейкоз был признан самостоятельным процессом. В дальнейшем с развитием морфологических исследований термины “Острый” и “Хронический” стали отражать не временные, а цитоморфологические характеристики. Заболеваемость острым лейкозом на территории СНГ остается приблизительно 1 случай на 100. 000 населения в год.

Этиология • • Генетические факторы формируют предрасположенность к лейкозу и реализуются после физических, химических воздействий. Ионизирующее излучение (после атомного взрыва в Японии), после лучевой терапии; Воздействие лекаственных препаратов (бутадион, левомицетин, цитостатики); курение табака у пож. пациентов; Воздействие химических веществ (лаки, бензол, краски, пестициды); Обсуждается вирусная теория (в 1982 году был выделен ретро-вирус); В 1948 году впервые были применены цитостатики. Ранее жизнь больных острым лейкозом не превышала 2 месяцев.

Факторы риска • Ионизирующее излучение; • Воздействие химических (в том числе лекарственных) веществ (бензол, продукты перегонки нефти, цитостатики и др. ). После цитостатической терапии (вторичные лейкозы)через 2 года – через 6 -10 лет, после облучения через 5 - 10 лет. Частота острого лейкоза 13, 2: 100000 среди мужчин и 7, 7: 100000 среди женщин. Мужчины болеют чаще, чем женщины. При этом всеми исследователями отмечается 2 пика заболеваемости: в 3 -4 и 60 -69 лет.

Патогенез • Основная роль – хромосомные нарушения, определяющие прогноз болезни и тип специфического лечения; • Пролиферация клона опухолевых клеток; • Угнетение нормального кроветворения; • Выход бластных клеток в кровь; • Метастазирование в кроветворные (селезенка, печень, лимфоузлы) и некроветворные (кожа, ЦНС, яички, легкие) органы.

ПРИНЦИПЫ ДИАГНОСТИКИ ОСТРЫХ ЛЕЙКОЗОВ Методы исследований при острых лейкозах Группы методов исследования Методы Морфологические Световая микроскопия мазков крови и костного мозга; Гистологическое исследование костного мозга; Трансмиссионная электронная микроскопия. Цитохимические Световая микроскопия; Ультраструктурная цитохимия. Иммунологические (изучение клеточных маркеров) Проточная цитометрия; флюоресцентная микроскопия; Иммуноцитохимия с фиксацией клеток на стекле; Иммуногистохимическое исследование костного мозга. Цитогенетические Метод бондирования хромосом. Молекулярно-генетические ДНК-гибридизация (ДНК зондовая гибридизация по Southern blotting, флюоресцентная in situ гибридизация (FISH)); ПЦР; секвенирование (определение последовательности реаранжировки генов иммуноглобулина и рецептора Т-лимфоцитов, исследование точечных мутаций и микроделеций в генах). Дополнительные Определение лактатдегидрогеназы в сыворотке крови; Определение Ргликопротеина, экспрессии гена множественной лекарственной резистентности; MDR 1. Инструментальные Рентгенологический; Ультразвуковой; Ядерно-магнитнорезонансная томография.

КЛАССИФИКАЦИЯ ЛЕЙКОЗОВ Еще в конце прошлого века все лейкозы по морфологии клеток были разделены на две группы: острые и хронические. Группу острых лейкозов объединяет общий признак: субстрат опухоли составляют молодые, так называемые бластные клетки. Название форм острого лейкоза происходит от названий нормальных предшественников опухолевых клеток: миелобласты, эритробласты, лимфобласты и др. Острый лейкоз из морфологически неидентифицируемых бластных клеток получил название недифференцируемого. В группу хронических лейкозов входят дифференцирующиеся опухоли системы крови. Основной субстрат этих лейкозов составляют морфологически зрелые клетки.

Классификация острого лейкоза (в основу положены внешний вид, цитохимические, генетические особенности бластных клеток, их иммунофенотип) В 1975 г. гематологами Франции, США и Англии была создана ФАБ – классификация основанная на морфологии лейкемических клеток. 1. Нелимфобластные миелогенные (миелоидные) лейкозы, подразделяющиеся на 6 основных типов. 2. Лимфобластные – 3 типа. 3. Миэлопоэтические дисплазиимиэлодиспластический синдром (МДС) – 4 типа

1. Нелимфобластные миелогенные (миелоидные) лейкозы, подразделяющиеся на 6 основных типов • • • М 1 - острый миелобластный лейкоз без признаков созревания клеток (бластные клетки пероксидазопозитивные). М 2 - острый миелобластный лейкоз с признаками вызревания клеток (морфологические и цитохимические характеристики бластных клеток такие же, имеет место созревание до промиелоцитов и более зрелых форм, типичная цитогенетическая аномалия t (8, 21). М 3 - острый промиелоцитарный лейкоз (бластные клетки с обильной базофильной зернистостью, реакция на пероксидазу резко (+), типичная цитогенетическая аномалия t (15, 17). М 4 - острый миеломонобластный лейкоз (бластные клетки имеют морфоцитохимические характеристики как миело- так и монобластов, аберрация inv 16. М 5 - острый монобластый лейкоз (бластные клетки беззернисты, имеют моноцитоидные ядра, пероксидаза отсутствует, содержится фторидингибируемая неспецифическая эстераза, различные хромосомные аберрации в II паре). М 6 - острый эритролейкоз (эритромиелоз), бластные клетки представлены молодыми формами эритроидного ряда.

2. Лимфобластные – 3 типа. Острые лимфобластные лейкозы делятся на 3 типа в зависимости от цитологической характеристики бластов: • Л 1 - острый микролимфобластный лейкоз, преобладают малые лимфоидные клетки, иногда без ядрышка и без иммунологических маркеров. Эта форма выявляется у 65% детей и у 5 -10% взрослых больных. • Л 2 - острый лимфобластный лейкоз с типичный лимфобластами, чаще у взрослых. • Л 3 - острый макро- или пролимфобластный лейкоз, преобладают весьма крупные клетки.

В последние годы авторы ФАБ – классификации выделили еще два варианта ОЛ: М 0 - острый недифференцированный лейкоз М 7 - острый мегакариобластный лейкоз. Из всех упомянутых подвариантов ОЛ наиболее часто встречается М 2 и М 4. Кроме цитоморфологической, существует иммунологическая классификация острого лимфобластного лейкоза: Т • лимфобластный вариант, В лимфобластный вариант и нульлимфобластный, или ни Т- ни В- острый лимфобластный лейкоз.

• • • • Классификация (ВОЗ, 1999) Острые миелобластные лейкозы (ОМЛ) Острый малодифференцированный лейкоз ОМЛ без созревания ОМЛ с созреванием Острый промиелобластный лейкоз Острый миеломонобластный лейкоз Острый эритромиелоз Острый мегакариобластный лейкоз Острые лимфобластные лейкозы (ОЛЛ) Пре-пре-B-ОЛЛ Пре-B-ОЛЛ T-ОЛЛ

Специалистами ВОЗ в 1997 году разработана и утверждена новая классификация опухолей кроветворной и лимфоидной ткани (The Hematology Journal, 2000, V. 1, 53 -66). • • • • • • • • ☼ Острые миелоидные лейкемии (ОМЛ) I. Острые миелоидные лейкемии с цитогенетическими транслокациями ОМЛ с t (8; 21) (q 22; q 22), FVL 1 (CBFα)/ETO (q (CBFα)/ETO ОПЛ (ОМЛ с t(15; 17) (q 22; q 11 -21) и варианты, PML/RARα) q ( PML/ RARα) ОМЛ с аномальными эозинофилами в костном мозге (inv (16) (p 13; q 22) или t (16; 16) (p 13; q 11), СВFβ/MYH 11 X) (inv (p (p СВF β/MYH 11 X ОМЛ с 11 q 23 (MLL) аномалиями q (MLL) 11 II. Острая миелоидная лейкемия с мультилинейной дисплазией II. с предшествующим миелодиспластическим синдромом без предшествующего миелодиспластического синдрома III. ОМЛ и миелодиспластический синдром, связанные с терапией III. связанные с алкилирующими агентами связанные с эпиподофиллотоксином (могут быть лимфоидные) другие типы IV. Острые миелобластные лейкозы не относящие в другие категории: IV. ОМЛ минимально дифференцированная ОМЛ без созревания ОМЛ с созреванием Острая миеломоноцитарная лейкемия Острая эритроидная лейкемия Острая мегакариоцитарная лейкемия Острая базофильная лейкемия Острый панмиелоз с миелофиброзом ☼ Острые бифенотипические лейкемии ☼ Острая лимфоидная лейкемия (ОЛЛ) В-клеточная острая лимфобластная лейкемия (цитогенетические подгруппы) t (9; 22) (q 34; q 11); BCR/ABL t (v; 11 q 23); MLL реанранжированный (v 11 q t (1; 19) (q 23 p 13) E 2 A/PBX 1 t (12; 21)(p 12 q 22) ETV/CBFα Т-клеточная острая лимфобластная лейкемия Лейкемия из клеток типа Беркитта.

Клиника Острого лейкоза: • • • Клинические проявления ОЛ являются следствием пролиферации и накопления злокачественных лейкозных бластных клеток. количественно превышающих условный рубеж (более 1000 млрд) за которым истощаются компенсаторные возможности организма. Основной клинической симптоматикой ОЛ служат процессы гиперплазии опухолевой ткани (бластная трансформация костного мозга, увеличение лимфатических узлов, органов, появление опухолевых инфильтратов и т. д, ) и признаки подавления нормального кроветворения. Клиническая симптоматика развернутой стадии ОЛ складывается из 5 основных синдромов: 1. гиперпластического 2. геморрагического 3. анемического 4. интоксикационного 5. инфекционный осложнений

клиника • Гиперпластический синдром проявляется умеренным и безболезненным увеличением лимфоузлов, печени, селезенки (30 -50%), у 14 больных — увеличение миндалин, лимфоузлов средостения с симптомами сдавления. появляются кожные лейкозные инфильтраты (лейкемиды) в виде красновато-синеватых бляшек. • Лейкозная гиперплазия и инфильтрация костного мозга приводят к угнетению нормального кроветворения, в результате чего развивается анемия и тромбоцитопения. тяжелая анемия с гемоглобином ниже 60 гл, эритроциты менее 1 -1, 3 х1012 отмечается у 30%. Глубокая тромбоцитопения (ниже 50 х109л) служит основной причиной одного из самых коварных клинических синдромов — геморрагического, который наблюдается у 50 -60% больных. Геморрагические проявления весьма вариабельны: от мелкоточечных и мелкопятнистых единичных высыпаний на коже и слизистых оболочках до обширных кровоизлияний и профузных кровотечений — носовых, маточных, желудочно-кишечных и др. • Кровоизлияния очень часто сопровождаются неврологическими нарушениями, острыми расстройствами мозгового кровообращения.

клиника • Инфекционные процессы. , наблюдаемые у 80 -85% больных ОЛ, являются грозным, труднокупируемым осложнением. Наиболее многочисленная группа инфекционных осложнений бактериального происхождения 70 -80%, включающая пневмонии, сепсис, гнойные процессы. Тяжелые инфекционные осложнения вирусного и грибкового генеза наблюдаются реже у 4 -18 и 18 -30% больных. В последнее время уменьшилась роль стафилококковой инфекции и возросло значение грамотрицательной флоры. количество грибковых инфекций обнаруживает тенденцию к увеличению До 20%. Вирусные инфекции стали протекать тяжелее, участились случаи цитомегаловирусной инфекции, герпеса. • Клиническим проявлением локализации лейкозного процесса в оболочках и веществе головного мозга является синдром нейролейкоза. клиническая симптоматика нейролейкоза развивается постепенно и складывается из симптомов повышения внутричерепного давления и локальной симптоматики: менингоэнцефалический синдром, псевдотуморозный, расстройства функций черепно-мозговых нервов, поражение периферических нервов.

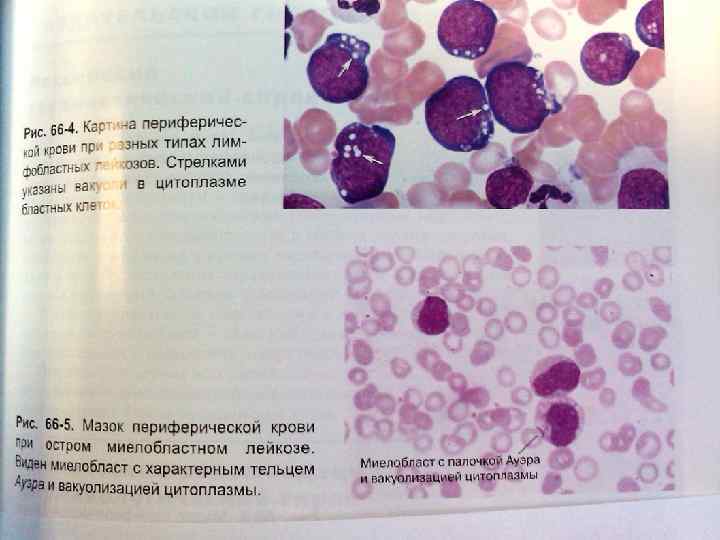
клиника Картина крови в развернутой стадии острого лейкоза весьма характерна. Помимо анемии и тромбоцитопении отмечается изменение числа лейкоцитов в довольно широких пределах: от 0, 1 х109л До 100 х109л с преобладанием форм с нормальным и сниженным лейкопеническим (38%) или сублейкимическим (44%) числом лейкоцитов. Лишь у 18% больных количество лейкоцитов превышает 50 х109л. У 30% больных бластные клетки в гемограмме отсутствуют. У большинства больных количество бластных форм составляет от нескольких процентов Дорошев 80 -90%. Клеточный состав гемограммы часто бывает мономорфным, представленный в основном бластными клетками. Зрелые гранулоциты выявляются в виде единичных палочкоядерных и сегментоядерных нейтрофилов. Между бластными клетками и зрелыми гранулоцитами почти нет промежуточных форм, что отражает провал в кроветворении — лейкемическое зияние (hiatus leukemicus). При нелимфобластных острых лейкозах в гемограмме могут обнаруживаться незрелые гранулоциты: промиелоциты, метамиелоциты, однако их количество невелико (Не более 10%).

Дифференциальная диагностика ОЛ проводится с: • • • Агранулоцитозами Апластической анемией Неспецифическими полиаденитами и заболеваниями соединительной ткани, аутоиммунным заболеваниями, аутоиммунными гепатитами, острым гемолизом, Вирусными инфекциями, вирусными гепатитами, СПИД, инфекционным мононуклеозом; Инфекциями, протекающими с панцитопенией – тяжелые бактериальные инфекции (сепсис), гистоплазмоз, гематогенно-диссеминированный туберкулез, сальмонеллез, бруцеллез, бореллиоз, сифилис и др. (клиническая картина, результаты посевов крови, отсутствие бластных клеток в периферической крови и костном мозге, туберкулиновые реакции, серологические реакции, RW); Тотальным некрозом костного мозга Метастазами опухолей в костный мозг – нейробластома, мелкоклеточный рак легкого, железистый рак и т. д. (необходима трепанобиопсия); Саркоидозом Гиперэозинофильным синдромом Другими гемобластозами: – миелодиспластическим синдромом (МДС) – ХМЛ – бластный криз Ph-хромосома может определяться в редких случаях при М 1 и М 2 вариантах ОНЛЛ; – ХЛЛ – картина лимфоидного бластного криза сходна с ОЛЛ, – НХЛ – в стадии лейкемизации;

Основу классификации стадий ОЛ можно представить следующим образом: первый острый период (развернутая стадия болезни); полная ремиссия; выздоровление; неполная ремиссия; рецидив, с указанием, первый он или повторный, его локализация, терминальная стадия

• Развернутый период характеризуется выраженным угнетением нормального кроветворения, высоким бластозом костного мозга (кроме малопроцентного лейкоза). Этот период неоднороден: первая атака лейкоза принципиальна отлична от рецидива, каждый последующий рецидив прогностически более тяжел, чем предыдущий и часто требует новой комбинации цитостатических средств. • К полной ремиссии относят состояния при которых в костном мозге не более 5% бластных клеток или общее количество лимфоидных клеток менее 30%, из них бластных клеток менее 5%; в крови лейкоцитов не менее 1, 5 1012/л, а тромбоцитов – не менее 1 1012/л, внекостномозговые лейкозные поражения отсутствуют.

• Выздоровлением от острого лейкоза считается полная ремиссия на протяжении 5 лет и более. • Неполная ремиссия (правильнее говорить об «улучшении» , а не о «ремиссии» ) представляет собой довольно разнородную группу состояний, которую характеризует или отчетливое гематологическое улучшение (уменьшение процента бластных клеток в костном мозге при увеличении процента нормальных клеток, сочетающееся с улучшением состава крови) или исчезновение бластных клеток из крови при сохранении бластоза костного мозга, или уменьшение количества бластных клеток в спинномозговой жидкости и т. п.

• Рецидив острого лейкоза может быть костномозговым (более 5% бластов в пунктате) или местным – внекостномозговым с любой локализацией лейкемической инфильтрации. • Терминальная стадия острого лейкоза на первый взгляд не имеет определенных черт, однако наблюдение показывает, что в развитии лейкоза неизбежно наступает момент, когда все цитостатические средства не только оказываются неэффективными, но процесс прогрессирует и на их фоне нарастают гранулоцитопения, тромбоцитопения, появляются некрозы на слизистых и спонтанные кровоизлияния. • К проявлениям терминальной стадии относится и возникновение очагов саркомного роста в коже, миокарде, почках. Однако решающая роль принадлежит полному угнетению нормальных ростков кроветворения, а не органным поражениям, которые не всегда означают бесперспективность терапии.

Лечение острого лейкоза Основные принципы: • -сочетание нескольких препаратов (полихимиотерапия) • -использование максимально больших доз химиопрепаратов • -циклический режим лечения • -длительное лечение (до полной эрадикации лейкозной опухоли)

Цели химиотерапии острых лейкозов • • • Эрадикация лейкемического клона; Восстановления кроветворения: аплазия костного мозга, «состояние клональной конкуренции, пролиферативное преимущество у клеток нормального кроветворного клона; Достижение длительной безрецидивной выживаемости больных

Принципы химиотерапии ОЛ: • • • принцип дозы интенсивности: снижение дозы препаратов на 20% приводит к снижению интенсивности лечения на 50%; увеличение дозы в два раза приводит к 10 -кратному увеличению количества погибающих опухолевых клеток; вероятность появления резистентности опухолевых клеток повышается при длительном применении лекарственных средств в низких концентрациях; прямая взаимосвязь между увеличением уровня спонтанных мутаций и объемом опухолевой массы; принцип использования комбинации цитостатических средств – суммация интенсивности дозы; принцип этапности терапии.

В соответствии с современными представлениями программа лечения острого лейкоза включает два этапа. 1) Индукция ремиссии. Индукционная терапия - химиотерапия, направленная на максимальное уничтожение лейкозных клеток, с целью достижения полной ремиссии. 2) Химиотерапия после достижения ремиссии. Химиотерапия поле достижения ремиссии обеспечивает предупреждение рецидива острого лейкоза. На этом этапе лечения могут быть использованы различные подходы: консолидация, интенсификация и поддерживающая терапия. • Консолидация используется после достижения полной ремиссии и проводится по тем же программам, которые применялись при индукции ремиссии. • Интенсификация предполагает применение более активной химиотерапии, чем при индукции ремиссии. • Поддерживающая терапия предполагает использование химиотерапевтических препаратов в дозах меньших по сравнению с этапом индукции, но в течение более длительного периода времени.

Этапы лечения ОЛ: • • индукция ремиссия (обычно 2 курса); консолидация (обычно 2 курса); поддерживающая (противорецидивная) терапия в течение 2 -3 лет; профилактика и лечение нейролейкемии (ОЛЛ, М 4, М 5, или если в дебюте ОМЛ гиперлейкоцитоз, М 3 на фоне терапии ATRA).

НОВЫЕ ПОДХОДЫ К ЛЕЧЕНИЮ ОСТРЫХ ЛЕЙКОЗОВ • • • Новые цитостатические средства 1. Нуклеозидные аналоги: флюдарабин 506 U (Ara-C)ОМЛ, ОЛЛ 2. Игибиторы топоизомеразы I: топотекан, камптоцетин. ОМЛ, МДС 3. Новые формы антрациклинов: липисомальный даунорубицин. ОМЛ 4. Платиновые производные: карбоплатин, CI-973 ОЛМ 5. Гипометилирующие средства: децитабин, 5 азацитидин. ОМЛ, МДС

ЛЕЧЕНИЕ ОСТРЫХ ЛЕЙКОЗОВ Новые нецитостатические средства и их сочетания 1. Дифференцирующие средства: полностью трансретиноевая кислота (весаноид) ОПЛ, МДС 2. Антипролиферативный, антиангиогенный эффекты: трансретиноевая кислота + INFa. ОМЛ, ОПЛ 3. Химиопротекторы: лизофиллин ОМЛ 4. Реверсия MDR 1 -фенотипа: циклоспорин, PSC 833 ОМЛ

ЛЕЧЕНИЕ ОСТРЫХ ЛЕЙКОЗОВ Биологические воздействия 1. Моноклональные антитела: Hu. M-195 (анти-CD 33) CMA-676 (анти-CD 33+calicheamicin) M 195+131 I (анти-CD 33+ 131 I) ОКТ-3 (анти-CD 3) В 43 -Генистеин (анти-CD-19) ОМЛ ОМЛ Т-ОЛЛ В-ОЛЛ 2. IL-2 сы» : OL(1)p 53, антисенсы к C-myb 3. «Антисен ОМЛ

ЛЕЧЕНИЕ ОСТРЫХ ЛЕЙКОЗОВ Новые терапевтические стратегии 1. Принцип интенсификации: трансплантация стволовых клеток периферической крови (ауто, алло) ОМЛ высокого риска, Ph+ ОЛЛ 2. «Траснплантат против лейкоза» : трансфузии лимфоцитов донора при рецидивах после аллогенной ТКМ, минитрансплантация ОМЛ, ОЛЛ
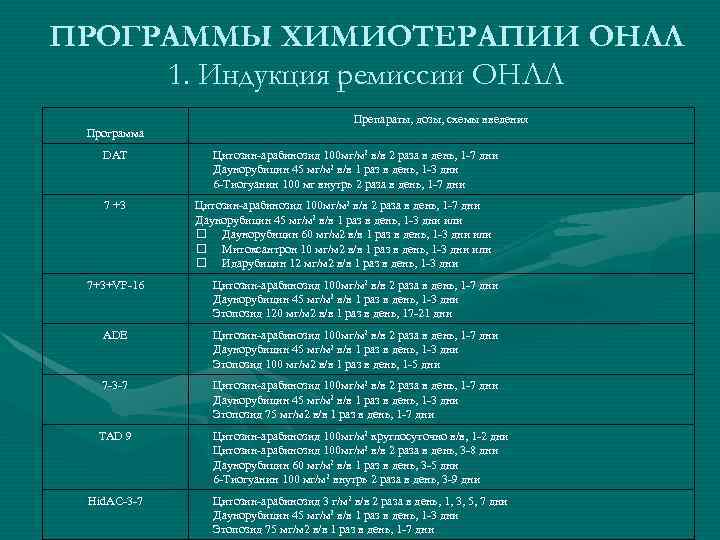
ПРОГРАММЫ ХИМИОТЕРАПИИ ОНЛЛ 1. Индукция ремиссии ОНЛЛ Препараты, дозы, схемы введения Программа DAT 7 +3 Цитозин-арабинозид 100 мг/м 2 в/в 2 раза в день, 1 -7 дни Даунорубицин 45 мг/м 2 в/в 1 раз в день, 1 -3 дни 6 -Тиогуанин 100 мг внутрь 2 раза в день, 1 -7 дни Цитозин-арабинозид 100 мг/м 2 в/в 2 раза в день, 1 -7 дни Даунорубицин 45 мг/м 2 в/в 1 раз в день, 1 -3 дни или Даунорубицин 60 мг/м 2 в/в 1 раз в день, 1 -3 дни или Митоксантрон 10 мг/м 2 в/в 1 раз в день, 1 -3 дни или Идарубицин 12 мг/м 2 в/в 1 раз в день, 1 -3 дни 7+3+VP-16 Цитозин-арабинозид 100 мг/м 2 в/в 2 раза в день, 1 -7 дни Даунорубицин 45 мг/м 2 в/в 1 раз в день, 1 -3 дни Этопозид 120 мг/м 2 в/в 1 раз в день, 17 -21 дни ADE Цитозин-арабинозид 100 мг/м 2 в/в 2 раза в день, 1 -7 дни Даунорубицин 45 мг/м 2 в/в 1 раз в день, 1 -3 дни Этопозид 100 мг/м 2 в/в 1 раз в день, 1 -5 дни 7 -3 -7 Цитозин-арабинозид 100 мг/м 2 в/в 2 раза в день, 1 -7 дни Даунорубицин 45 мг/м 2 в/в 1 раз в день, 1 -3 дни Этопозид 75 мг/м 2 в/в 1 раз в день, 1 -7 дни TAD 9 Цитозин-арабинозид 100 мг/м 2 круглосуточно в/в, 1 -2 дни Цитозин-арабинозид 100 мг/м 2 в/в 2 раза в день, 3 -8 дни Даунорубицин 60 мг/м 2 в/в 1 раз в день, 3 -5 дни 6 -Тиогуанин 100 мг/м 2 внутрь 2 раза в день, 3 -9 дни Hid. AC-3 -7 Цитозин-арабинозид 3 г/м 2 в/в 2 раза в день, 1, 3, 5, 7 дни Даунорубицин 45 мг/м 2 в/в 1 раз в день, 1 -3 дни Этопозид 75 мг/м 2 в/в 1 раз в день, 1 -7 дни

2. Консолидация ремиссии ОНЛЛ Препараты, дозы, схемы введения Программа MACE Амсакрин 100 мг/м 2 в/в 1 раз в день, 1 -5 дни Цитозин-арабинозид 200 мг/м 2 в/в круглосуточно, 1 -5 дни Этопозид 100 мг/м 2 в/в внутрь 2 раза в день, 3 -9 дни Mid. AC Цитозин-арабинозид 1 г/м 2 в/в 2 раза в день, 1 -3 дни Митоксантрон 10 мг/м 2 в/в 1 раз в день, 1 -5 дни HAM Цитозин-арабинозид 3 г/м 2 в/в 2 раза в день, 1 -3 дни Митоксантрон 10 мг/м 2 в/в 1 раз в день, 3 -5 дни S-HAM HD-ARA-C Did. AC Цитозин-арабинозид 1 г/м 2 в/в 2 раза в день, 1, 3, 8, 9 дни Митоксантрон 10 мг/м 2 в/в 1 раз в день, 3, 4, 10, 11 дни Цитарабин 3 г/м 2 2 раза в день, 1 -5 дни Цитозин-арабинозид 1 г/м 2 в/в 2 раза в день, 1 -5 дни Даунорубицин 45 мг/м 2 в/в 1 раз в день, 1 -3 дни 3. Поддерживающая терапия ОНЛЛ Препараты, дозы, схемы введения Программа 5+2 Цитозин-арабинозид 100 мг/м 2 в/в 2 раза в день, 1 -5 дни или 50 мг/м 2 подкожно 2 раза в день, 1 -5 дни Даунорубицин 45 мг/м 2 в/в 1 раз в день, 1 -2 дни 5+ЦФ Цитозин-арабинозид 100 мг/м 2 в/в 2 раза в день, 1 -5 дни или 50 мг/м 2 подкожно 2 раза в день, 1 -5 дни Циклофосфан 650 мг/м 2 в 1 день 5+6 -МП Цитозин-арабинозид 100 мг/м 2 в/в 2 раза в день, 1 -5 дни или 50 мг/м 2 подкожно 2 раза в день, 1 -5 дни 6 -Меркаптопурин 60 мг/м 2 2 раза в день внутрь, 1 -5 дни или 6 -Тиогуанин 50 мг/м 2 2 раза в день внутрь, 1 -5 дни

ПРОГНОСТИЧЕСКИЕ ФАКТОРЫ ПРИ ОСТРЫХ ЛЕЙКОЗАХ Положение о прогностических факторах при острых лейкозах разработано сравнительно недавно и включают: • возраст больного (при ОЛЛ у детей от 3 до 10 лет – благоприятный прогноз; при ОЛЛ у взрослых чем моложе пациент, тем лучше прогноз; наихудшие результаты у больных 60 лет и старше; аналогичные закономерности при ОМЛ); • клинико-лабораторные показатели (количество лейкоцитов, уровень ЛДГ, цитоморфологический вариант ОЛЛ, иммунофенотипические, цитогенетические характеристики каждого варианта ОЛ и т. д. , которые рассмотрены при описании каждой формы ОЛ); • адекватно проведенная химиотерапия

Неблагоприятные прогностические факторы ОЛ Факторы риска ОЛЛ ОМЛ Возраст Старше 35 лет Старше 60 лет Лейкоцитоз Выше 100 109/л Выше 30 109/л Уровень ЛДГ Выше 1000 ед/л Выше 700 ед/л Вариант ОЛ Пре-В, зрелый-В, пре-Т М 5, М 6, М 7 Костный мозг Трехростковая дисплазия кроветворения Отсутствие ремиссии На 28 день ХТ После 2 -х индукционных курсов ХТ Цитогенетические измененияt(9; 22), t(4; 11), t(8; 14), t(2; 8), t(8; 22)3 q 21, 3 q 26, t(6; 9), t(9; 22), 11 q 23, изменения 5 и 7 хромосом

ВСПОМОГАТЕЛЬНАЯ ТЕРАПИЯ. ПРИМЕНЕНИЕ РОСТКОВЫХ ГЕМОПОЭТИЧЕСКИХ ФАКТОРОВ РОСТА Основные профилактические меры: • Обеспечение адекватного сосудистого доступа • Профилактика синдрома массивного лизиса опухолевых клеток – водная нагрузка, форсированный диурез, аллопуринол. • Профилактика флебита, если не используется центральный венозный катетер. • Профилактика тошноты и рвоты. • Профилактика геморрагических осложнений с помощью заместительных трансфузий тромбоцитов (их уровень должен быть не менее 20 109/л, при лихорадке – 30 109/л). • Профилактика и лечение анемического синдрома – заместительные трансфузии эритроцитарной массы. Уровень гемоглобина 75 -80 г/л без признаков кислородной недостаточности (одышка при физической нагрузке, выраженная тахикардия, головные боли, головокружения, обморочные состояния) не требуют трансфузий эритроцитов. Должны быть исключены трансфузии цельной крови, которые помимо трансфузионных реакций часто способствуют запуску ДВС-синдрома. • Профилактика электролитных нарушений. • Профилактика коагуляционных нарушений (викасол – при использовании β-лактамных антибиотиков, свежезамороженная плазма и гепарин при гиперкоагуляционных состояниях). • Профилактика инфекционных осложнений – селективная деконтаминация кишечника, желательно направленного действия в соответствии с результатами посевов флоры кишечника и полости рта, обработка полости рта, санитарно-гигиенические мероприятия.

Лечение осложнений: Инфекционные осложнения. К наиболее грозным осложнениям относятся инфекции различной тяжести и локализации. Практически у 90% больных ОЛ в период индукции ремиссии возникают инфекционные осложнения. Главный принцип лечения инфекций – эмпирическая поэтапная антибиотикотерапия, с обязательными предварительными бактериологическими исследованиями для возможности последующей коррекции антибиотикотерапии. • Поводом к назначению антибиотикотерапии, особенно при агранулоцитозе, служит подъем температуры выше 380 С в течение не менее 4 часов, не связанное с введением пирогенных препаратов. Наиболее эффективно в/в введение нескольких антибиотиков широкого спектра действия в максимальных суточных дозах: • цефалоспорины I-II поколения цефалотин (2 г– 4 раза в день) и др. + аминогликозиды (гентамицин или брулламицин 240 мг 1 раз); • ампициллин (2 г 3 раза) + аминогликозиды; • цефтазидим (2 г 3 раза) + аминогликозиды; • цефоперазон (4 г 2 раза) + аминогликозиды; • цефтриаксон (4 г 1 раз) + аминогликозиды; • цефепим (2 г 3 раза) + аминогликозиды.

Инфекционные осложнения • • • На фоне терапии осуществляется постоянный мониторинг выделяемой от больного микрофлоры. При агранулоцитозе дополнительно обязательно проводится селективная деконтаминация кишечника с применением внутрь неабсорбируемых антибиотиков (1, 5 г ристомицина, 1, 5 г полимиксина М, 3 г нистатина растворенных в 200 мл воды; бисептол 960 2 таб по 2 раза в день). Сейчас используется комбинация таривида 200 мг (или ципробая 250 мг) в сочетании с низоралом 200 по 2 раза в день. При высокой вероятности выделения анаэробов включают метрагил 500 мг по 3 раза в стуки. Эффект терапии оценивают в основном по клиническим признакам. При отсутствии эффекта производят замену а/б через 4 суток. Неэффективные препараты заменяют на препараты резерва, такие как амикацин, (1, 5 г/ сут), нетилмицин (400 мг/сут), ингибиторозащищенные пенициллины, ванкомицин (2 г/сут), зивокс (линезолид при резистентности к ванкомицину) 600 по 2 раза в сутки в комбинации с цефалоспоринами III-IV поколения; «сульперазон» , + аминогликозиды (амикацин, нетилмицин), фторхинолоны (ципрофлоксацин) + ингибиторозащищенные пенициллины. В монотерапии используют: максипим (6 г/сут), тиенам (2 г/сут), меропенем (3 г/сут). При неэффективности антибактериальной терапии можно предположить наличие грибковой инфекции. В этой случае необходимо в/в введение амфотирецина В в/в 1 мг/кг в сутки или дифлюкан (400 мг первые сутки, затем 200 мг/сут).

Геморрагические осложнения. Геморрагический синдром представляет угрозу на первых этапах химиотерапии острых лейкозов. С проведением заместительной терапии он является причиной 10 -15% острых осложнений. Однако, именно геморрагический синдром является причиной 50% смертей больных в период индукции ремиссии больных острыми миелоидными лейкозами. Основу лечения составляет заместительная терапия тромбоцитарной массой и свежезамороженной плазмой. Показанием к трансфузии тромбоцитов служит снижение их менее 20 109/л или менее 50 109/л при наличии геморрагий верхней части туловища и лица, а также при кровоточивости различной локализации и повышении температуры тела свыше 380 С. Переливается не менее 4 доз тромбоцитарной массы (2 1011) или тромбоконцентрата (2 -4 1011 клеток), подобранных по системе АВО. Переливания осуществляют 2 -3 раза в неделю. При сохраняющемся геморрагическом синдроме и/или тяжелых инфекционных осложнениях дозу увеличивают или проводят ежедневные трансфузии до получения необходимого эффекта. Критерием эффективности считают прирост тромбоцитов через 1 час и 24 часа после трансфузии (не менее 20 109/л) или купирование кровоточивости. Кроме того, назначают этамзилат в дозе 750 -1500 мг/сут, сосудоукрепляющие средства (аскорутин), 5% раствор аминокапроновой кислоты и 1, 5% перекиси водорода, для обработки кровоточащих слизистых применяют гемостатическую губку. Тампоны постоянно орошают аминокапроновой кислотой и антибиотиками, чтобы избежать их высыхания и инфицирования. Удаление тампонов на 2 -3 сутки. Особого внимания требует геморрагический синдром, развивающийся при промиелоцитарном лейкозе (М 3). Этот вариант ОЛ характеризуется развитием ДВС-синдрома уже в начале заболевания и может усиливаться при проведении химиотерапии. Для диагностики ДВС-синдрома, наряду с клиническими данными проводят исследование гемостаза, обращая особое внимание на положительные паракоагуляционные тесты, снижение протромбинового комплекса, удлинение активированного частичного тромбопластинового времени и активированного времени рекальцификации. В лечении ДВС-синдрома используют трансфузии свежезамороженной плазмы до 1000 -2000 мл/сут. Первые 500 мл вводят струйно, повторные переливания делают через 6 -8 часов по контролем диуреза и центрального венозного давления.

Применение гемопоэтических факторов. Использование их продиктовано следующими положительными эффектами гемопоэтических факторов: • сокращение периода нейтропении (G-CSF, GM-CSF, IL-3, SCF); • выведение лейкемических клеток в S-фазу (прайминг) (G-CSF, GM-CSF, IL-3); • защита нормальных клеток-предшественниц кроветворения от воздействия ARA -C (G-CSF, GM-CSF, IL-3); • дифференцирующие эффекты на лейкемические клетки HL-60 линии (G-CSF, GM-CSF, IL-6); • прямое ингибирующее действие на лейкемические клетки ( IL-6); • усиление фагоцитарной активности (G-CSF, GM-CSF, M-CSF); • защита нелейкемических клеток от цитотоксических эффектов цитозинарабинозида (GM-CSF, IL-3). • По результатам применения G-CSF и GM-CSF продемонстрировано уменьшение периода нейтропении, но не выявлено увеличения продолжительности периода ремиссии и жизни пациентов. • Особое внимание заслуживает способ введения препаратов, который называется «прайминг» и используется лишь в терапии острых миелобластных лейкозов. Ростковый фактор вводится за несколько (не более 48 часов) дней до начала курса химиотерапиии. Стратегия «прайминга» базируется на способности G-CSF стимулировать пролиферацию лейкемических клеток in vitro, увеличивая процент этих клеток в фазе синтеза, что повышает цитотоксичность цитозинарабинозида и увеличивает гибель клеток лейкемического клона.

ЛЕЧЕНИЕ ОСТРОГО ЛЕЙКОЗА • Современный этап химиотерапии отличается применением программ, составленных в зависимости от патоморфологических форм, особенностей течения заболевания. Эти программы позволили добиться ремиссии у 8095% детей и 60 -80% взрослых. Основное в лечении – цитостатическая терапия, направленная на максимальное уничтожение опухолевых клеток. • Разработка программ цитостатической терапии согласуется с данными клеточной кинетики при ОЛ. Известно, что пролиферирующие клетки проходят фазы митотического цикла: фаза митоза М, самая короткая, характеризуется образованием 2 дочерних клеток, постмитотическая фаза G 1 - отражает период стабилизации, отдыха, фаза синтеза S характеризуется синтезом, удвоением ДНК, премитотическая фаза G 2, когда клетка готова к делению.

С позиций клеточной кинетики все химиопрепараты делятся на 2 группы. • Первая группа – это химические агенты, специфически действующие на клеточный цикл. • Вторая - вещества действию которых проявляется независимо от цикла (циклонеспецифические).

Основные группы противолейкозных препаратов. • 1. глюкокортикостероиды - нециклоспецифические, блок g 1, s • 2. антиметаболиты: 6 -меркаптопурин, 6 -тиогуанин, метотрексат циклоспецифические, вступают в конкурентные отношения с метаболитами, с предшествниками нуклеиновых кислот. Цитозин - арабинозид (цитозар) - антикистаболит, блокирует синтез ДНК - циклоспецифичен. • 3. растительные алкалоиды, антимитотические средства - винкристин, винбластин - нециклоспецифичены, в больших дозах блок g 2т. • 4. алкилирующие средства - циклофосфан - нециклоспецифичен, блок G фазы. • 5. производные нитромочевины – циклоспецифичны, лигибируют рост лейкозных клеток. • 6. противоопухолевые антибиотики (даунорубицин, рубиномицин, адренамицин) - ингибируют рост лейкозных клеток, подавляя синтез ДНК, РНК • 7. ферменты (L-аспирагиназа, этапозид), L-аспирагиназа нециклоспецифична, блок в G 1, S фазе (разлагает аспирин). Этапозид действует в G 2 фазе. • 8. анракиноины (митоксантрон, амсакрин) - фазовонеспецифичны.

Необходимо учитывать следующие принципиальные положения: • · сочетание цитостатических препаратов оказывает • • большее цитостатическое действие, причем комбинировать необходимо препараты различной фазово- и циклоспецифичности с нециклоспецифическими препаратами, чтобы охватить большее количество лейкозных клеток. · соблюдение цикличности и прерывистости в применении препаратов · длительность , упорность , достаточная активность терапии

ЛЕЧЕНИЕ ОСТРОГО ЛЕЙКОЗА • Лечение больных острым лейкозом необходимо начинать сразу же после подтверждения диагноза, поскольку при отсутствии терапии заболевание развивается очень быстро. Терапия должна проводиться в специализированном гематологическом стационаре, имеющем необходимый опыт работы и соответствующее оснащение. Размещение должно проводиться в палатах не более чем на 2 -х человек, с туалетом и душем. Важную роль играет вентиляция, обеспечивающая быстрое удаление из воздуха микробных тел, представляющих опасность для больных лейкозами, получающих химиотерапию. • Основное содержание лечения острого лейкоза - это химиотерапия, направленная на уничтожение лейкозных (бластных) клеток в организме больного. Кроме химиотерапии используют ряд вспомогательных методов в зависимости от состояния больного: переливание компонентов крови (эритроцитов, тромбоцитов), профилактику инфекционных осложнений, уменьшение проявлений интоксикации и др.

Спасибо за внимание!
Острый лейкоз .ppt