острые лейкозы Адаменко 8.ppt
- Количество слайдов: 72
 Острые лейкозы, агранулоцитоз Е. И. Адаменко 3 -я кафедра внутренних болезней БГМУ
Острые лейкозы, агранулоцитоз Е. И. Адаменко 3 -я кафедра внутренних болезней БГМУ
 § Впервые идея об опухолевой природе лейкозов была высказана в 1867 г. К. Славянским. § В конце XIX — начале XX века морфологические исследования позволили выделить острые и хронические лейкозы
§ Впервые идея об опухолевой природе лейкозов была высказана в 1867 г. К. Славянским. § В конце XIX — начале XX века морфологические исследования позволили выделить острые и хронические лейкозы
 Лейкозы (лейкемии) § Злокачественные опухоли кроветворной ткани с первичной локализацией в костном мозге и последующей диссеминацией в периферической крови, селезенке, лимфатических узлах и других тканях § Заболеваемость – 13 случаев на 100000 тыс. населения
Лейкозы (лейкемии) § Злокачественные опухоли кроветворной ткани с первичной локализацией в костном мозге и последующей диссеминацией в периферической крови, селезенке, лимфатических узлах и других тканях § Заболеваемость – 13 случаев на 100000 тыс. населения
 Классификация острые Субстрат опухоли – недифференцирован ные клетки- бласты Болеют чаще дети и подростки хронические Субстрат опухоли – более зрелые клетки, достигшие определенного уровня дифференциации Болеют лица старшего возраста
Классификация острые Субстрат опухоли – недифференцирован ные клетки- бласты Болеют чаще дети и подростки хронические Субстрат опухоли – более зрелые клетки, достигшие определенного уровня дифференциации Болеют лица старшего возраста
 острый лейкоз никогда не переходит в хронический, а хронический никогда не обостряется § термины «острый» и «хронический» используются только из-за удобства; § исключением является лишь хронический миелолейкоз, острая или терминальная фаза которого характеризуется развитием бластного криза — появлением в крови и костном мозге 30 -90 % бластных клеток, то есть развитием острого миелобластного (или лимфобластного) лейкоза.
острый лейкоз никогда не переходит в хронический, а хронический никогда не обостряется § термины «острый» и «хронический» используются только из-за удобства; § исключением является лишь хронический миелолейкоз, острая или терминальная фаза которого характеризуется развитием бластного криза — появлением в крови и костном мозге 30 -90 % бластных клеток, то есть развитием острого миелобластного (или лимфобластного) лейкоза.
 Острые лейкозы § группа клональных (онкологических) заболеваний, первично возникающих в костном мозге в результате мутации стволовой клетки крови § Следствием мутации является потеря потомками мутировавшей клетки способности к дифференцировке до зрелых клеток крови. § Морфологический субстрат оcтpыx лейкозов — бластные клетки
Острые лейкозы § группа клональных (онкологических) заболеваний, первично возникающих в костном мозге в результате мутации стволовой клетки крови § Следствием мутации является потеря потомками мутировавшей клетки способности к дифференцировке до зрелых клеток крови. § Морфологический субстрат оcтpыx лейкозов — бластные клетки
 Этиология § Курение является доказанным фактором риска при § § § остром миелоидном лейкозе (ОМЛ). Ионизирующая радиация (рост заболеваемости острыми лейкозами через 5 лет среди жителей Херосимы и Нагасаки) Химические вещества (длительный контакт с бензином, бензолом и др. ароматическими углеводородами) Длительный прием противоопухолевых лекарственных средств по поволу раковой опухоли другой локализации Вирусы (Эпштейна-Барра в развитии лимфомы Беркитта, ретровируса HTLV в развитии Т-клеточного лимфолейкоза Генетические и наследственные факторы, хромосомные аномалии (при болезни Дауна острый миелоидный лейкоз в 20 раз чаще, синдром Клайнфельтера 47 XXY, анемия Фанкони)
Этиология § Курение является доказанным фактором риска при § § § остром миелоидном лейкозе (ОМЛ). Ионизирующая радиация (рост заболеваемости острыми лейкозами через 5 лет среди жителей Херосимы и Нагасаки) Химические вещества (длительный контакт с бензином, бензолом и др. ароматическими углеводородами) Длительный прием противоопухолевых лекарственных средств по поволу раковой опухоли другой локализации Вирусы (Эпштейна-Барра в развитии лимфомы Беркитта, ретровируса HTLV в развитии Т-клеточного лимфолейкоза Генетические и наследственные факторы, хромосомные аномалии (при болезни Дауна острый миелоидный лейкоз в 20 раз чаще, синдром Клайнфельтера 47 XXY, анемия Фанкони)
 В генетической основе развития острого лейкоза § лежат изменения в структуре хромосом, т. е. хромосомные аберрации. § выделяют специфические или первичные и неспецифические хромосомные аберрации. § К первичным принято относить транслокации, делеции, инверсии, амплификации участков хромосом, содержащих онкогены, гены клеточных рецепторов, гены ростовых факторов. Подобные изменения способны образовывать новые последовательности ДНК и появление новых свойств у клетки, образование специфического клона. §
В генетической основе развития острого лейкоза § лежат изменения в структуре хромосом, т. е. хромосомные аберрации. § выделяют специфические или первичные и неспецифические хромосомные аберрации. § К первичным принято относить транслокации, делеции, инверсии, амплификации участков хромосом, содержащих онкогены, гены клеточных рецепторов, гены ростовых факторов. Подобные изменения способны образовывать новые последовательности ДНК и появление новых свойств у клетки, образование специфического клона. §
 • Вторичные хромосомные аберрации появляются на стадии опухолевой прогрессии в результате изменений сформировавшегося клона • нарушения специфичны для каждого лейкоза, нпр. При нелимфобластном лейкозах аномалии кариотипа наблюдаются чаще в 8, 21 паре, при ОЛЛ чаще в 4, 11 или 1, 19 парах хромосом
• Вторичные хромосомные аберрации появляются на стадии опухолевой прогрессии в результате изменений сформировавшегося клона • нарушения специфичны для каждого лейкоза, нпр. При нелимфобластном лейкозах аномалии кариотипа наблюдаются чаще в 8, 21 паре, при ОЛЛ чаще в 4, 11 или 1, 19 парах хромосом
 Патогенез § Клоновая теория § Лейкозные клетки являются потомством одной мутировавшей гемопоэтической клетки -предшественницы § Доказательство- обнаружение в опухолевых клетках одних и тех же хромосомных аббераций и одного и того же вида изофермента глюкозо-6 фосфатдегидрогеназы § Основные свойства лейкозных клеток: неспособность к дифференциации и способность к чрезмерной пролиферации и накоплению в костном мозге
Патогенез § Клоновая теория § Лейкозные клетки являются потомством одной мутировавшей гемопоэтической клетки -предшественницы § Доказательство- обнаружение в опухолевых клетках одних и тех же хромосомных аббераций и одного и того же вида изофермента глюкозо-6 фосфатдегидрогеназы § Основные свойства лейкозных клеток: неспособность к дифференциации и способность к чрезмерной пролиферации и накоплению в костном мозге
 Патогенез клетка Этиологический фактор Повреждение генетического аппарата клетки Гиперпролиферация, но сохраниется способность к дифференциации клон
Патогенез клетка Этиологический фактор Повреждение генетического аппарата клетки Гиперпролиферация, но сохраниется способность к дифференциации клон
 Патогенез Повторные мутации Интенсивная пролиферация, утрата способности к дифференциации, активация онкогенов, мутация генов, контролирующих апоптоз Опухолевый клон
Патогенез Повторные мутации Интенсивная пролиферация, утрата способности к дифференциации, активация онкогенов, мутация генов, контролирующих апоптоз Опухолевый клон
 Патогенез § Угнетение нормальных ростков кроветворения в костном мозге § Замена дифференцированных клеток бластами - неопластический клон вытесняет нормальные гемопоэтические клетки, что приводит к развитию дефицита зрелых клеток в периферической крови. Снижение количества или полное отсутствие зрелых клеток периферической крови обусловливает выпадение соответствующих функций периферической крови, что влечет за собой развитие клинических симптомов заболевания. § Появление способности лейкозных клеток расти и размножаться вне органов кроветворения § Уход лейкозных клеток из-под контроля цитостатической терапии Закон опухолевой прогрессии (по Фулдсу)
Патогенез § Угнетение нормальных ростков кроветворения в костном мозге § Замена дифференцированных клеток бластами - неопластический клон вытесняет нормальные гемопоэтические клетки, что приводит к развитию дефицита зрелых клеток в периферической крови. Снижение количества или полное отсутствие зрелых клеток периферической крови обусловливает выпадение соответствующих функций периферической крови, что влечет за собой развитие клинических симптомов заболевания. § Появление способности лейкозных клеток расти и размножаться вне органов кроветворения § Уход лейкозных клеток из-под контроля цитостатической терапии Закон опухолевой прогрессии (по Фулдсу)
 Морфология § лейкозная инфильтрация костного мозга в виде очаговых и диффузных инфильтратов из клеток с крупными светлыми ядрами, содержащими по нескольку ядрышек § Размеры и очертания ядер, а также ширина ободка плазмы могут варьировать. Бласты составляют 10 -20 % мозговых клеток § Цитогенетическую принадлежность бластов выявляют только с помощью специальных методов исследования — Ш цитохимических - реакции на пероксидазу, окраска на липиды суданом черным, ШИК-реакция, гистоферментохимические акции на выявление неспецифической эстеразы, хлорацетатэстеразы, кислой фосфатазы. Ш Иммуногистохимических - определение маркеров B-, Tлимфоцитов, клеток миелоидного и моноцитарного рядов. .
Морфология § лейкозная инфильтрация костного мозга в виде очаговых и диффузных инфильтратов из клеток с крупными светлыми ядрами, содержащими по нескольку ядрышек § Размеры и очертания ядер, а также ширина ободка плазмы могут варьировать. Бласты составляют 10 -20 % мозговых клеток § Цитогенетическую принадлежность бластов выявляют только с помощью специальных методов исследования — Ш цитохимических - реакции на пероксидазу, окраска на липиды суданом черным, ШИК-реакция, гистоферментохимические акции на выявление неспецифической эстеразы, хлорацетатэстеразы, кислой фосфатазы. Ш Иммуногистохимических - определение маркеров B-, Tлимфоцитов, клеток миелоидного и моноцитарного рядов. .
 Морфология § В костномозговой ткани происходят вытеснение нормальных клеток гемопоэза опухолевыми, истончение и резорбция ретикулярных волокон, нередко развивается миелофиброз. § При цитостатической терапии происходит опустошение костного мозга с гибелью бластных форм, увеличивается число жировых клеток и разрастается соединительная ткань. § Лейкозные инфильтраты в виде диффузных или очаговых скоплений обнаруживаются в лимфатических узлах, селезенке и печени. Это приводит к увеличению размеров этих органов. В печени характерно развитие жировой дистрофии. Возможна лейкозная инфильтрация слизистых оболочек полости рта и ткани миндалин.
Морфология § В костномозговой ткани происходят вытеснение нормальных клеток гемопоэза опухолевыми, истончение и резорбция ретикулярных волокон, нередко развивается миелофиброз. § При цитостатической терапии происходит опустошение костного мозга с гибелью бластных форм, увеличивается число жировых клеток и разрастается соединительная ткань. § Лейкозные инфильтраты в виде диффузных или очаговых скоплений обнаруживаются в лимфатических узлах, селезенке и печени. Это приводит к увеличению размеров этих органов. В печени характерно развитие жировой дистрофии. Возможна лейкозная инфильтрация слизистых оболочек полости рта и ткани миндалин.
 Морфология § В периферической крови и в костном мозге описывается феномен «лейкемического провала» ( «hiatus leucemicus» ), развивающийся за счет наличия только бластных и дифференцированных клеток и отсутствия промежуточных форм
Морфология § В периферической крови и в костном мозге описывается феномен «лейкемического провала» ( «hiatus leucemicus» ), развивающийся за счет наличия только бластных и дифференцированных клеток и отсутствия промежуточных форм
 Современная классификация острых лейкозов § FAB (Франко-Американо-Британской, 1976 г. ) § основанна на клоновой теории их патогенеза и на § § представлении о том, что каждая опухолевая клетка имеет своего «нормального» предшественника положены в основу цитоморфологические и цитохимические методы исследования Особенно велика роль этих методов в верификации острых миелоидных лейкозов, где результатов морфологического и цитохимического исследований в большинстве случаев бывает достаточно для постановки окончательного диагноза.
Современная классификация острых лейкозов § FAB (Франко-Американо-Британской, 1976 г. ) § основанна на клоновой теории их патогенеза и на § § представлении о том, что каждая опухолевая клетка имеет своего «нормального» предшественника положены в основу цитоморфологические и цитохимические методы исследования Особенно велика роль этих методов в верификации острых миелоидных лейкозов, где результатов морфологического и цитохимического исследований в большинстве случаев бывает достаточно для постановки окончательного диагноза.
 FAB-классификация Острые лейкозы миелоидные (нелимфобластные – ОНЛЛ) лимфобластные (ОЛЛ)
FAB-классификация Острые лейкозы миелоидные (нелимфобластные – ОНЛЛ) лимфобластные (ОЛЛ)
 § Эти типы выделяют в зависимости от принадлежности популяции бластных (лейкемических) клеток к лимфоидному или миелоидному росткам кроветворения § Лимфоидный росток представлен клетками 2 линий дифференцировки (созревания) — B- и T-линейной направленности, а миелоидный росток — 6 клеточными линиями, к финальным этапам созревания которых относят моноциты, сегментоядерные нейтрофилы, базофилы, эозинофилы, эритроциты и тромбоциты. § В свою очередь опухолевые клетки по своей природе могут принадлежать каждой из перечисленных линий дифференцировки клеток лимфоидной или миелоидной природы.
§ Эти типы выделяют в зависимости от принадлежности популяции бластных (лейкемических) клеток к лимфоидному или миелоидному росткам кроветворения § Лимфоидный росток представлен клетками 2 линий дифференцировки (созревания) — B- и T-линейной направленности, а миелоидный росток — 6 клеточными линиями, к финальным этапам созревания которых относят моноциты, сегментоядерные нейтрофилы, базофилы, эозинофилы, эритроциты и тромбоциты. § В свою очередь опухолевые клетки по своей природе могут принадлежать каждой из перечисленных линий дифференцировки клеток лимфоидной или миелоидной природы.
 Острые миелобластные лейкозы § в зависимости от типа бластных клеток, особенности ядра и цитоплазмы • М 0 – о. миелобластный лейкоз с минимальной миелоидной дифференцировкой бластов • М 1 – о. миелобластный лейкоз без созревания • М 2 – о. миелобластный лейкоз с созреванием • М 3 – о. промиелоцитарный лейкоз • М 4 – о. миеломонобластный лейкоз • М 4 эоз. - о. миеломонобластный лейкоз с эозинофилией • М 5 а – о. монобластный лейкоз без созревания • М 5 б – о. монобластный лейкоз с созреванием • М 6 – о. эритромиелоз • М 7 – о. мегакариобластный лейкоз
Острые миелобластные лейкозы § в зависимости от типа бластных клеток, особенности ядра и цитоплазмы • М 0 – о. миелобластный лейкоз с минимальной миелоидной дифференцировкой бластов • М 1 – о. миелобластный лейкоз без созревания • М 2 – о. миелобластный лейкоз с созреванием • М 3 – о. промиелоцитарный лейкоз • М 4 – о. миеломонобластный лейкоз • М 4 эоз. - о. миеломонобластный лейкоз с эозинофилией • М 5 а – о. монобластный лейкоз без созревания • М 5 б – о. монобластный лейкоз с созреванием • М 6 – о. эритромиелоз • М 7 – о. мегакариобластный лейкоз
 Острые лимфобластные лейкозы § • L 1 – о. лимфобластный лейкоз с микроформой бластов • L 2 – о. лимфобластный лейкоз с гетерогенными формами бластов • L 3 – о. лимфобластный лейкоз с беркиттоподобными бластами
Острые лимфобластные лейкозы § • L 1 – о. лимфобластный лейкоз с микроформой бластов • L 2 – о. лимфобластный лейкоз с гетерогенными формами бластов • L 3 – о. лимфобластный лейкоз с беркиттоподобными бластами
 Острые лимфобластные лейкозы определяют по сумме баллов, которые набирают видимые, морфологические характеристики клеток опухоли. для детей в 85% случаев характерен тип L 1. Иногда у пациентов могут одновременно выявляться бласты типов L 1 и L 2, причём иммунологически среди этих групп могут выявляться разные клетки, относящиеся к разным пролиферативным росткам. L 3. тип - это лимфобласты, всегда относящиеся к B-клеточному пролиферативному ростку.
Острые лимфобластные лейкозы определяют по сумме баллов, которые набирают видимые, морфологические характеристики клеток опухоли. для детей в 85% случаев характерен тип L 1. Иногда у пациентов могут одновременно выявляться бласты типов L 1 и L 2, причём иммунологически среди этих групп могут выявляться разные клетки, относящиеся к разным пролиферативным росткам. L 3. тип - это лимфобласты, всегда относящиеся к B-клеточному пролиферативному ростку.
 Острые лимфобластные лейкозы (ВОЗ, 1999) § Пре-пре-B-ОЛЛ § Пре-B-ОЛЛ § T-ОЛЛ
Острые лимфобластные лейкозы (ВОЗ, 1999) § Пре-пре-B-ОЛЛ § Пре-B-ОЛЛ § T-ОЛЛ
 Эпидемиология § Ежегодно регистрируется 35 новых § § § случаев острых лейкозов на 1 млн населения Структура заболеваемости в значительной степени зависит от возраста. ОЛЛ чаще развивается в детском возрасте и после 40 лет. Частота ОМЛ одинакова во всех возрастных rpуппах Мужчины и женщины болеют с одинаковой частотой Афроамериканцы в 2 раза реже болеют ОЛЛ, чем белое население Америки. Риск заболеть ОМЛ у них также несколько ниже, чем у белого населения
Эпидемиология § Ежегодно регистрируется 35 новых § § § случаев острых лейкозов на 1 млн населения Структура заболеваемости в значительной степени зависит от возраста. ОЛЛ чаще развивается в детском возрасте и после 40 лет. Частота ОМЛ одинакова во всех возрастных rpуппах Мужчины и женщины болеют с одинаковой частотой Афроамериканцы в 2 раза реже болеют ОЛЛ, чем белое население Америки. Риск заболеть ОМЛ у них также несколько ниже, чем у белого населения
 клинические стадии заболевания: § первая атака (начальная стадия) § Развернутая стадия § ремиссия (полная или неполная) § рецидив (первый, повторный) § терминальная
клинические стадии заболевания: § первая атака (начальная стадия) § Развернутая стадия § ремиссия (полная или неполная) § рецидив (первый, повторный) § терминальная
 Клиника варианты начала § Острое – лихорадка, слабость, выраженная интоксикация, боли в суставах, при глотании, в животе. Часто трактуют как ОРВИ § С выраженными геморрагическими явлениями – у 10%, развиваются профузные кровотечения различной локализации
Клиника варианты начала § Острое – лихорадка, слабость, выраженная интоксикация, боли в суставах, при глотании, в животе. Часто трактуют как ОРВИ § С выраженными геморрагическими явлениями – у 10%, развиваются профузные кровотечения различной локализации
 Клиника варианты начала § Медленное – нарастающая слабость, снижение трудоспособности, боли в костях, мышцах, суставах, небольшое увеличение лимфатических узлов, геморрагии на коже § Бессимптомное – обнаруживается случайно
Клиника варианты начала § Медленное – нарастающая слабость, снижение трудоспособности, боли в костях, мышцах, суставах, небольшое увеличение лимфатических узлов, геморрагии на коже § Бессимптомное – обнаруживается случайно
 Стадия развернутой клинической картины § Развивается вследствие интенсивной пролиферации, накопления лейкозных клеток и выраженных внекостномозговых проявлений § Слабость, утомляемость, боли в костях, суставах, в животе. Повышение температуры § 5 основных синдромов
Стадия развернутой клинической картины § Развивается вследствие интенсивной пролиферации, накопления лейкозных клеток и выраженных внекостномозговых проявлений § Слабость, утомляемость, боли в костях, суставах, в животе. Повышение температуры § 5 основных синдромов
 Гиперпластический синдром § Обусловлен лейкозной инфильтрацией тканей § Безболезненное увеличение лимфотических узлов, печени, селезенки, миндалин, из-за сдавления верхней полой вены увеличенными лимфотическими узлами средостения - одышка, цианоз, отечность шеи, набухание шейных вен
Гиперпластический синдром § Обусловлен лейкозной инфильтрацией тканей § Безболезненное увеличение лимфотических узлов, печени, селезенки, миндалин, из-за сдавления верхней полой вены увеличенными лимфотическими узлами средостения - одышка, цианоз, отечность шеи, набухание шейных вен
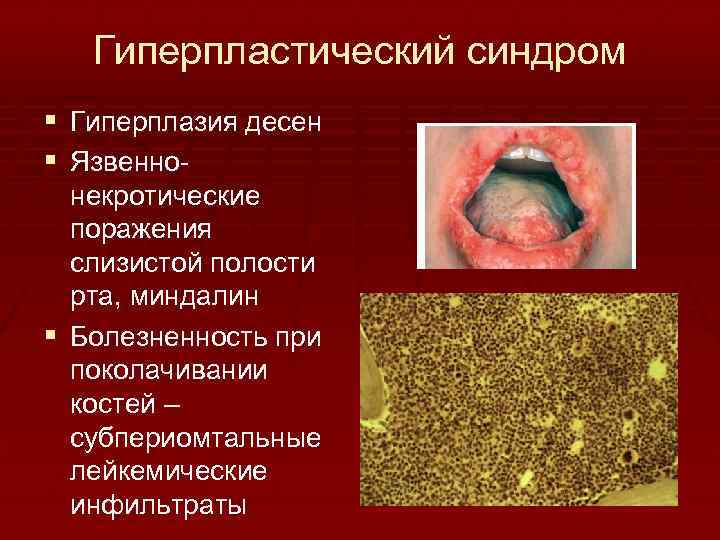 Гиперпластический синдром § Гиперплазия десен § Язвеннонекротические поражения слизистой полости рта, миндалин § Болезненность при поколачивании костей – субпериомтальные лейкемические инфильтраты
Гиперпластический синдром § Гиперплазия десен § Язвеннонекротические поражения слизистой полости рта, миндалин § Болезненность при поколачивании костей – субпериомтальные лейкемические инфильтраты
 Геморрагический синдром § У 50 -60% больных § обусловлен тромбоцитопенией, повреждением ь ь ь печени и стенок сосудов. Проявляется: геморрагическим диатезом петехиальнопятнистого типа, на коже и слизистых оболочках появляются «синячки» и петехии небольшого размера, легко провоцируется незначительными воздействиями — трением одежды, легкими ушибами. носовые кровотечения, кровотечения из десен, метроррагии, кровотечения из мочевыводящих путей. Ведет опасным осложнениям — кровоизлияниям в головной мозг и желудочно-кишечных кровотечениям
Геморрагический синдром § У 50 -60% больных § обусловлен тромбоцитопенией, повреждением ь ь ь печени и стенок сосудов. Проявляется: геморрагическим диатезом петехиальнопятнистого типа, на коже и слизистых оболочках появляются «синячки» и петехии небольшого размера, легко провоцируется незначительными воздействиями — трением одежды, легкими ушибами. носовые кровотечения, кровотечения из десен, метроррагии, кровотечения из мочевыводящих путей. Ведет опасным осложнениям — кровоизлияниям в головной мозг и желудочно-кишечных кровотечениям
 Другие синдромы § Анемический синдром § Интоксикационный синдром снижение массы тела, лихорадка, слабость, потливость, снижение аппетита § Иммунодефицитный синдром: нарушается клеточный и гуморальный иммунитет, фагоцитарная функция лейкоцитов, снижением активности комплемента – развиваются тяжелые инфекционно-воспалительные процессы, септическое состояние (чаще бактериальное происхождение) § ДВС-синдром § на коже появляются лейкемиды — приподнимающиеся над поверхностью кожи образования мягкой или плотной консистенции. Цвет их может соответствовать цвету кожи или быть светло-коричневым, желтым, розовым
Другие синдромы § Анемический синдром § Интоксикационный синдром снижение массы тела, лихорадка, слабость, потливость, снижение аппетита § Иммунодефицитный синдром: нарушается клеточный и гуморальный иммунитет, фагоцитарная функция лейкоцитов, снижением активности комплемента – развиваются тяжелые инфекционно-воспалительные процессы, септическое состояние (чаще бактериальное происхождение) § ДВС-синдром § на коже появляются лейкемиды — приподнимающиеся над поверхностью кожи образования мягкой или плотной консистенции. Цвет их может соответствовать цвету кожи или быть светло-коричневым, желтым, розовым
 Внекостномозговые проявления § Нейролейкемия (метастазирование лейкозных клеток в оболочки или вещество головного и спинного мозга: ШМЕНИНГИАЛЬНАЯ ФОРМА – головная боль, тошнота, рвота, светобоязнь ШЭНЦЕФАЛИТИЧЕСКАЯ – нарушение сна. Бред. Галлюцинации, головная боль ШДИЭНЦЕФАЛЬНАЯ – патологическая сонливость, нарушение терморегуляции ШМЕНИНГОМИЕЛИТИЧЕСКАЯ – парезы, параличи ШПОЛИРАДИКУЛОНЕВРИТИЧЕСКАЯ – нарушение чувствительности, выпадение рефлексов
Внекостномозговые проявления § Нейролейкемия (метастазирование лейкозных клеток в оболочки или вещество головного и спинного мозга: ШМЕНИНГИАЛЬНАЯ ФОРМА – головная боль, тошнота, рвота, светобоязнь ШЭНЦЕФАЛИТИЧЕСКАЯ – нарушение сна. Бред. Галлюцинации, головная боль ШДИЭНЦЕФАЛЬНАЯ – патологическая сонливость, нарушение терморегуляции ШМЕНИНГОМИЕЛИТИЧЕСКАЯ – парезы, параличи ШПОЛИРАДИКУЛОНЕВРИТИЧЕСКАЯ – нарушение чувствительности, выпадение рефлексов
 Поражение мочеполовой системы § Лейкозная инфильтрация яичек, яичников – безболезненное увеличение § Поражение полового члена – длительная болезненная эрекция § Лейкозная инфильтрация предстательной железы, уретры, мочевого пузыря
Поражение мочеполовой системы § Лейкозная инфильтрация яичек, яичников – безболезненное увеличение § Поражение полового члена – длительная болезненная эрекция § Лейкозная инфильтрация предстательной железы, уретры, мочевого пузыря
 Внекостномозговые проявления § Поражение органов пищеварения (пищевод, желудок, кишечник, печень, селезенка) § Поражение почек § Поражение легких § Поражение сердца § Поражение эндокринной системы, костно-мышечной системы, глаз
Внекостномозговые проявления § Поражение органов пищеварения (пищевод, желудок, кишечник, печень, селезенка) § Поражение почек § Поражение легких § Поражение сердца § Поражение эндокринной системы, костно-мышечной системы, глаз
 Диагностика § Жалобы § Анамнез § Объективный осмотр § ОБЩИЙ АНАЛИЗ КРОВИ: ШАнемия – нормохромная, нормоцитарная ШРетикулоцитопения ШТромбоцитопения ШИзменение общего количества лейкоцитов
Диагностика § Жалобы § Анамнез § Объективный осмотр § ОБЩИЙ АНАЛИЗ КРОВИ: ШАнемия – нормохромная, нормоцитарная ШРетикулоцитопения ШТромбоцитопения ШИзменение общего количества лейкоцитов
 ОБЩИЙ АНАЛИЗ КРОВИ: ь ь ь § Лейкемическая форма (100 X 109) Сублейкемическая (15 X 109) Алейкемическая (2, 5 X 109) Бластемия. Выход в периферическую кровь бластных клеток является основным морфологическим признаком острого лейкоза § Уменьшение зрелых нейтрофилов § Феномен ''провала'‘ – отсутствие юных, палочкоядерных и небольшое количество сегментоядерных лейкоцитов § Исчезновение эозинофилов, базофилов, увеличение СОЭ
ОБЩИЙ АНАЛИЗ КРОВИ: ь ь ь § Лейкемическая форма (100 X 109) Сублейкемическая (15 X 109) Алейкемическая (2, 5 X 109) Бластемия. Выход в периферическую кровь бластных клеток является основным морфологическим признаком острого лейкоза § Уменьшение зрелых нейтрофилов § Феномен ''провала'‘ – отсутствие юных, палочкоядерных и небольшое количество сегментоядерных лейкоцитов § Исчезновение эозинофилов, базофилов, увеличение СОЭ
 Миелограмма § Количество бластов – более 20% от числа всех клеток § Выраженная редукция эритроидного, гранулоцитарного и мегакариоцитарного ростков, что проявляется резким уменьшением количества соответствующих клеток § Стернальная пункция грудины § Трепатобиопсия крыла подвздошной кости
Миелограмма § Количество бластов – более 20% от числа всех клеток § Выраженная редукция эритроидного, гранулоцитарного и мегакариоцитарного ростков, что проявляется резким уменьшением количества соответствующих клеток § Стернальная пункция грудины § Трепатобиопсия крыла подвздошной кости
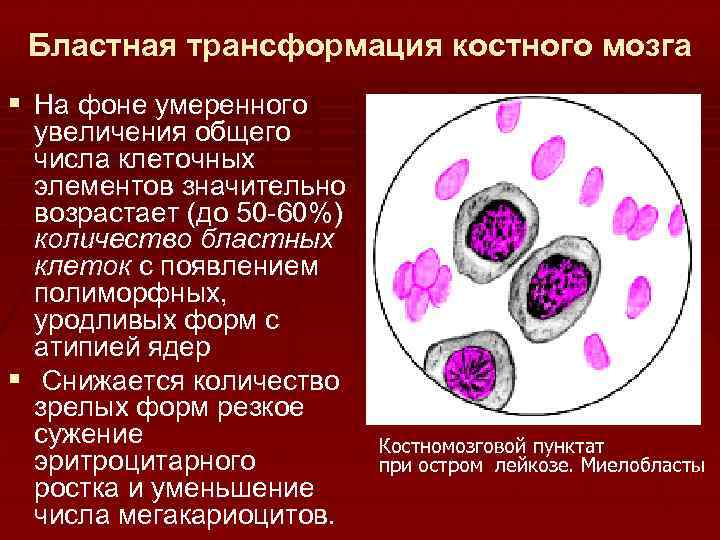 Бластная трансформация костного мозга § На фоне умеренного увеличения общего числа клеточных элементов значительно возрастает (до 50 -60%) количество бластных клеток с появлением полиморфных, уродливых форм с атипией ядер § Снижается количество зрелых форм резкое сужение эритроцитарного ростка и уменьшение числа мегакариоцитов. Костномозговой пунктат при остром лейкозе. Миелобласты
Бластная трансформация костного мозга § На фоне умеренного увеличения общего числа клеточных элементов значительно возрастает (до 50 -60%) количество бластных клеток с появлением полиморфных, уродливых форм с атипией ядер § Снижается количество зрелых форм резкое сужение эритроцитарного ростка и уменьшение числа мегакариоцитов. Костномозговой пунктат при остром лейкозе. Миелобласты
 Диагностика § цитохимическое исследование для определения вариантов острого лейкоза обязательно и крайне необходимо для более точной верификации острого лимфобластного лейкоза и миелолейкоза § (мазки периферической крови, пунктаты костного мозга, лейкоконцентрат венозной крови, спинномозговой жидкости, аспираты лимфатических узлов, селезенки, лейкозных инфильтратов различной локализации)
Диагностика § цитохимическое исследование для определения вариантов острого лейкоза обязательно и крайне необходимо для более точной верификации острого лимфобластного лейкоза и миелолейкоза § (мазки периферической крови, пунктаты костного мозга, лейкоконцентрат венозной крови, спинномозговой жидкости, аспираты лимфатических узлов, селезенки, лейкозных инфильтратов различной локализации)
 Диагностика § Биопсия лимфатического узла § Иммунологические и цитогенетические методы § § § (характеристика гемопоэтических клеток на основании набора антител к антигенам кластеров дифференцировки (CD) позволяет определять их линейную принадлежность и этап дифференцировки) – для определения вариантов лейкоза, что важно для подбора терапии Рентгенография и томография органов грудной клетки ЭКГ Ультразвуковое исследование Компьютерная томография Спинномозговая пункция
Диагностика § Биопсия лимфатического узла § Иммунологические и цитогенетические методы § § § (характеристика гемопоэтических клеток на основании набора антител к антигенам кластеров дифференцировки (CD) позволяет определять их линейную принадлежность и этап дифференцировки) – для определения вариантов лейкоза, что важно для подбора терапии Рентгенография и томография органов грудной клетки ЭКГ Ультразвуковое исследование Компьютерная томография Спинномозговая пункция
 Клинико-гематологические стадии § Первый острый период – от начала заболевания до до получения эффекта от цитостатической терапии § Ремиссия: Полная – нормализация клинической картины, периферической крови и миелограммы количество бластных клеток в костном мозге не превышает 5 % при отсутствии их в крови. Состав периферической крови близок к норме Неполная – нормализация клинического состояния, гемограммы, но в миелограмме бластов не более 20%
Клинико-гематологические стадии § Первый острый период – от начала заболевания до до получения эффекта от цитостатической терапии § Ремиссия: Полная – нормализация клинической картины, периферической крови и миелограммы количество бластных клеток в костном мозге не превышает 5 % при отсутствии их в крови. Состав периферической крови близок к норме Неполная – нормализация клинического состояния, гемограммы, но в миелограмме бластов не более 20%
 Клинико-гематологические стадии § Рецидив – возврат активной стадии после полной клинико-гематологической ремиссии в результате выхода остаточной лейкозной клеточной популяции из-под контроля проводимой поддерживающей терапии Рецидив острого лейкоза может возникать в костном мозге или вне костного мозга (кожа и т. д. ). Каждый последующий рецидив прогностически более опасен, чем предыдущий (клиника, бласты в периферической крови, более 5 % бластов в миелограмме)
Клинико-гематологические стадии § Рецидив – возврат активной стадии после полной клинико-гематологической ремиссии в результате выхода остаточной лейкозной клеточной популяции из-под контроля проводимой поддерживающей терапии Рецидив острого лейкоза может возникать в костном мозге или вне костного мозга (кожа и т. д. ). Каждый последующий рецидив прогностически более опасен, чем предыдущий (клиника, бласты в периферической крови, более 5 % бластов в миелограмме)
 Клинико-гематологические стадии § Выздоровление – ремиссия более 5 лет § Терминальная стадия - характеризуется резистентностью к цитостатической терапии, выраженным угнетением нормального кроветворения, развитием язвенно-некротических процессов
Клинико-гематологические стадии § Выздоровление – ремиссия более 5 лет § Терминальная стадия - характеризуется резистентностью к цитостатической терапии, выраженным угнетением нормального кроветворения, развитием язвенно-некротических процессов
 Задача § Известно: в мае 1937 года после гастролей в Японии и Америке всегда энергичный и неутомимый Шаляпин вернулся в Париж обессиленным, очень бледным и со странным «украшением» на лбу - шишкой зеленоватого цвета, по поводу которой он невесело шутил: «Еще вторая, и я буду настоящим рогоносцем!» Домашний врач месье Жандрон объяснил его состояние обычной усталостью и посоветовал певцу отдохнуть на популярном в то время курорте в Райхенхалле, под Веной. Однако курортная жизнь не заладилась. Превозмогая нарастающую слабость, осенью Шаляпин все же дал несколько концертов в Лондоне, а когда приехал домой, доктор Жандрон встревожился не на шутку и пригласил на консилиум лучших французских врачей.
Задача § Известно: в мае 1937 года после гастролей в Японии и Америке всегда энергичный и неутомимый Шаляпин вернулся в Париж обессиленным, очень бледным и со странным «украшением» на лбу - шишкой зеленоватого цвета, по поводу которой он невесело шутил: «Еще вторая, и я буду настоящим рогоносцем!» Домашний врач месье Жандрон объяснил его состояние обычной усталостью и посоветовал певцу отдохнуть на популярном в то время курорте в Райхенхалле, под Веной. Однако курортная жизнь не заладилась. Превозмогая нарастающую слабость, осенью Шаляпин все же дал несколько концертов в Лондоне, а когда приехал домой, доктор Жандрон встревожился не на шутку и пригласил на консилиум лучших французских врачей.
 § У пациента взяли кровь на исследование. На другой день ответ был готов. Жене певца Марии Викентьевне сообщили: у мужа белокровие - лейкемия - и жить ему осталось месяца четыре, от силы пять. Пересадку костного мозга тогда еще не делали, лекарств, подавляющих выработку «злокачественных» лейкоцитов, тоже не существовало. Чтобы хоть как-то притормозить развитие болезни, медики рекомендовали единственно возможное средство - переливание крови. Донором оказался француз по фамилии Шьен, а по-русски - Шариков. Не подозревавшего о страшном диагнозе Шаляпина это обстоятельство крайне забавляло. Он утверждал, что после курса процедур при первом же выступлении залает на сцене, как собака. Но о возвращении в театр не могло быть и речи. Пациенту становилось все хуже: в марте он уже не поднимался с постели.
§ У пациента взяли кровь на исследование. На другой день ответ был готов. Жене певца Марии Викентьевне сообщили: у мужа белокровие - лейкемия - и жить ему осталось месяца четыре, от силы пять. Пересадку костного мозга тогда еще не делали, лекарств, подавляющих выработку «злокачественных» лейкоцитов, тоже не существовало. Чтобы хоть как-то притормозить развитие болезни, медики рекомендовали единственно возможное средство - переливание крови. Донором оказался француз по фамилии Шьен, а по-русски - Шариков. Не подозревавшего о страшном диагнозе Шаляпина это обстоятельство крайне забавляло. Он утверждал, что после курса процедур при первом же выступлении залает на сцене, как собака. Но о возвращении в театр не могло быть и речи. Пациенту становилось все хуже: в марте он уже не поднимался с постели.
 § История болезни Шаляпина вошла в зарубежные учебники гематологии как весьма редкий случай. «Этого просто не может быть! - разводили руками доктора. - Богатырское телосложение и - лейкемия, да еще в таком возрасте!» Ведь острый миелобластный лейкоз, которым страдал Федор Иванович, практически не встречается на седьмом десятке. § Необычная шишка на лбу тоже получила объяснение. За зеленоватый цвет, вызванный повышенной активностью лейкоцитарного фермента - миелопероксидазы, специалисты назвали эту опухоль хлоромой (от греческого chloros - «зеленый» ). Она образуется при скоплении под кожей патологически измененных клеток крови (гранулоцитов). Хлорома - визитная карточка миелобластного лейкоза: как правило, она служит первым признаком заболевания.
§ История болезни Шаляпина вошла в зарубежные учебники гематологии как весьма редкий случай. «Этого просто не может быть! - разводили руками доктора. - Богатырское телосложение и - лейкемия, да еще в таком возрасте!» Ведь острый миелобластный лейкоз, которым страдал Федор Иванович, практически не встречается на седьмом десятке. § Необычная шишка на лбу тоже получила объяснение. За зеленоватый цвет, вызванный повышенной активностью лейкоцитарного фермента - миелопероксидазы, специалисты назвали эту опухоль хлоромой (от греческого chloros - «зеленый» ). Она образуется при скоплении под кожей патологически измененных клеток крови (гранулоцитов). Хлорома - визитная карточка миелобластного лейкоза: как правило, она служит первым признаком заболевания.
 ЛЕЧЕНИЕ § Первые препараты для лечения острых лейкозов (антагонисты фолиевой кислоты- метотрексат) были разработаны в 1948 г. В дальнейшем (1951— 1954) был создан 6 -меркаптопурин, а во второй половине 50 -х годов XIX века — препараты из группы антагонистов пиримидина. В 60 -х годах XX века было показано, что препарат с алкилирующим действием (циклофосфан) может быть использован для лечения острого лейкоза § Уже в это время начинала воплощаться в клиническую практику идея трансплантации костного мозга от здоровых лиц. Однако несовершенство методов исследования иммунной совместимости между донором и больным приводило к тому, что после трансплантации костного мозга продолжительность жизни пациентов была ниже, чем при лечении острого лейкоза кортикостероидами и 6 меркаптопурином
ЛЕЧЕНИЕ § Первые препараты для лечения острых лейкозов (антагонисты фолиевой кислоты- метотрексат) были разработаны в 1948 г. В дальнейшем (1951— 1954) был создан 6 -меркаптопурин, а во второй половине 50 -х годов XIX века — препараты из группы антагонистов пиримидина. В 60 -х годах XX века было показано, что препарат с алкилирующим действием (циклофосфан) может быть использован для лечения острого лейкоза § Уже в это время начинала воплощаться в клиническую практику идея трансплантации костного мозга от здоровых лиц. Однако несовершенство методов исследования иммунной совместимости между донором и больным приводило к тому, что после трансплантации костного мозга продолжительность жизни пациентов была ниже, чем при лечении острого лейкоза кортикостероидами и 6 меркаптопурином
 ЛЕЧЕНИЕ § В 60 -х — начале 70 -х годов появились и стали с успехом внедряться в клиническую практику новые цитостатические препараты. Был синтезирован цитозин-арабинозид, который в дальнейшем стал базисным препаратом в терапии ОМЛ. При использовании L-аспарагиназы были получены первые обнадеживающие результаты у больных ОЛЛ. В это же время началось изучение противоопухолевой активности антрациклиновых цитостатиков (даунорубицин, адриабластин), которые стали применять для лечения как ОМЛ, так и ОЛЛ. Была продемонстрирована более высокая эффективность комбинаций химиопрепаратов (полихимиотерапия) по сравнению с монотерапией
ЛЕЧЕНИЕ § В 60 -х — начале 70 -х годов появились и стали с успехом внедряться в клиническую практику новые цитостатические препараты. Был синтезирован цитозин-арабинозид, который в дальнейшем стал базисным препаратом в терапии ОМЛ. При использовании L-аспарагиназы были получены первые обнадеживающие результаты у больных ОЛЛ. В это же время началось изучение противоопухолевой активности антрациклиновых цитостатиков (даунорубицин, адриабластин), которые стали применять для лечения как ОМЛ, так и ОЛЛ. Была продемонстрирована более высокая эффективность комбинаций химиопрепаратов (полихимиотерапия) по сравнению с монотерапией
 ЛЕЧЕНИЕ § Были предложены комбинации винкристина с метотрексатом, 6 -меркаптопурином и преднизолоном (схема ВАМП), аналогичная схема с заменой винкристина циклофосфаном (ЦАМП), цитозинарабинозида (цитарабина) с преднизолоном и винкристином. К этому времени к терапии острого лейкоза начал постепенно применяться дифференцированный подход в зависимости от принадлежности опухолевых клеток к миелоидному или лимфоидному ростку кроветворения
ЛЕЧЕНИЕ § Были предложены комбинации винкристина с метотрексатом, 6 -меркаптопурином и преднизолоном (схема ВАМП), аналогичная схема с заменой винкристина циклофосфаном (ЦАМП), цитозинарабинозида (цитарабина) с преднизолоном и винкристином. К этому времени к терапии острого лейкоза начал постепенно применяться дифференцированный подход в зависимости от принадлежности опухолевых клеток к миелоидному или лимфоидному ростку кроветворения
 § В начале 70 -х годов появились сообщения о полихимиотерапии ОЛЛ с использованием Lаспарагиназы, винкристина и преднизолона. При лечении детей по этой схеме удалось получить 93% ремиссий. Достижения в лечении ОЛЛ у детей были положены в основу создания программ терапии взрослых пациентов. Указанные препараты у взрослых больных ОЛЛ относят к наиболее активным агентам и в настоящее время. Комбинирование цитарабина с даунорубицином (рубомицином) позволило значительно увеличить эффективность лечения ОМЛ. К концу 70 -х годов прогноз при острых лейкозах принципиально изменился, базисной терапией ОМЛ стала схема « 7+3» (цитарабин по 100 мг/м 2 2 раза в сутки в течение 7 дней, рубомицин 45 мг/м 2 1 раз в сутки в течение 3 дней), которая позволила значительно улучшить непосредственные и отдаленные результаты лечения этого заболевания. Частота полных ремиссий увеличилась до 58— 64%, а 5 -летняя безрецидивная выживаемость составила 10— 21%
§ В начале 70 -х годов появились сообщения о полихимиотерапии ОЛЛ с использованием Lаспарагиназы, винкристина и преднизолона. При лечении детей по этой схеме удалось получить 93% ремиссий. Достижения в лечении ОЛЛ у детей были положены в основу создания программ терапии взрослых пациентов. Указанные препараты у взрослых больных ОЛЛ относят к наиболее активным агентам и в настоящее время. Комбинирование цитарабина с даунорубицином (рубомицином) позволило значительно увеличить эффективность лечения ОМЛ. К концу 70 -х годов прогноз при острых лейкозах принципиально изменился, базисной терапией ОМЛ стала схема « 7+3» (цитарабин по 100 мг/м 2 2 раза в сутки в течение 7 дней, рубомицин 45 мг/м 2 1 раз в сутки в течение 3 дней), которая позволила значительно улучшить непосредственные и отдаленные результаты лечения этого заболевания. Частота полных ремиссий увеличилась до 58— 64%, а 5 -летняя безрецидивная выживаемость составила 10— 21%
 § Разработка программ цитостатической терапии согласуется с данными клеточной кинетики при ОЛ. Известно, что пролиферирующие клетки проходят фазы митотического цикла: фаза митоза М, самая короткая, характеризуется образованием 2 дочерних клеток, постмитотическая фаза G 1 - отражает период стабилизации, отдыха, фаза синтеза S - характеризуется синтезом, удвоением ДНК, премитотическая фаза G 2, когда клетка готова к делению. § С позиций клеточной кинетики все химиопрепараты делятся на 2 группы.
§ Разработка программ цитостатической терапии согласуется с данными клеточной кинетики при ОЛ. Известно, что пролиферирующие клетки проходят фазы митотического цикла: фаза митоза М, самая короткая, характеризуется образованием 2 дочерних клеток, постмитотическая фаза G 1 - отражает период стабилизации, отдыха, фаза синтеза S - характеризуется синтезом, удвоением ДНК, премитотическая фаза G 2, когда клетка готова к делению. § С позиций клеточной кинетики все химиопрепараты делятся на 2 группы.
 § Первая группа – химические агенты, § § § специфически действующие на клеточный цикл. Вторая - вещества действие которых проявляется независимо от цикла (циклонеспецифические) Основные группы противолейкозных препаратов: глюкокортикостероиды - циклоснепецифические, блок g 1, s антиметаболиты: 6 -меркаптопурин, 6 -тиогуанин, метотрексат -циклоспецифические, вступают в конкурентные отношения с метаболитами, с предшествниками нуклеиновых кислот. Цитозин - арабинозид (цитозар) - антикистаболит, блокирует синтез ДНК циклоспецифичен.
§ Первая группа – химические агенты, § § § специфически действующие на клеточный цикл. Вторая - вещества действие которых проявляется независимо от цикла (циклонеспецифические) Основные группы противолейкозных препаратов: глюкокортикостероиды - циклоснепецифические, блок g 1, s антиметаболиты: 6 -меркаптопурин, 6 -тиогуанин, метотрексат -циклоспецифические, вступают в конкурентные отношения с метаболитами, с предшествниками нуклеиновых кислот. Цитозин - арабинозид (цитозар) - антикистаболит, блокирует синтез ДНК циклоспецифичен.
 § растительные алкалоиды, атимитотические § § средства - винкристин, винбластин нециклоспецифичены, в больших дозах блок g 2 алкилирующие средства - циклофосфан - нециклоспецифичен, блок G фазы. производные нитромочевины – циклоспецифичны, игибируют рост лейкозных клеток. противоопухолевые антибиотики (даунорубицин, рубиномицин, адренамицин) ингибируют рост лейкозных клеток, подавляя синтез ДНК, РНК ферменты (L-аспирагиназа, этапозид), Lаспирагиназа нециклоспецифична, блок в G 1, S фазе
§ растительные алкалоиды, атимитотические § § средства - винкристин, винбластин нециклоспецифичены, в больших дозах блок g 2 алкилирующие средства - циклофосфан - нециклоспецифичен, блок G фазы. производные нитромочевины – циклоспецифичны, игибируют рост лейкозных клеток. противоопухолевые антибиотики (даунорубицин, рубиномицин, адренамицин) ингибируют рост лейкозных клеток, подавляя синтез ДНК, РНК ферменты (L-аспирагиназа, этапозид), Lаспирагиназа нециклоспецифична, блок в G 1, S фазе
 § Этапозид действует в G 2 фазе. § анракиноины (митоксантрон, амсакрин) - циклонеспецифичны. § Необходимо учитывать следующие принципиальные положения: сочетание цитостатических препаратов оказывает большее цитостатическое действие, причем комбинировать необходимо препараты различной фазово- и циклоспецифичности с нециклоспецифическими препаратами, чтобы охватить большее количество лейкозных клеток; соблюдение цикличности и прерывистости в применении препаратов длительность , упорность , достаточная активность терапии
§ Этапозид действует в G 2 фазе. § анракиноины (митоксантрон, амсакрин) - циклонеспецифичны. § Необходимо учитывать следующие принципиальные положения: сочетание цитостатических препаратов оказывает большее цитостатическое действие, причем комбинировать необходимо препараты различной фазово- и циклоспецифичности с нециклоспецифическими препаратами, чтобы охватить большее количество лейкозных клеток; соблюдение цикличности и прерывистости в применении препаратов длительность , упорность , достаточная активность терапии
 основной метод лечения - полихимиотерапия, которая включает несколько этапов § I — индукция (достижение) ремиссии, направленная на уничтожение или значительное уменьшение объема опухолевого клона и нормализацию кроветворения § II — консолидация ремиссии, целью которой является уничтожение оставшихся (резидуальных) лейкемических клеток § III этапом является поддерживающая терапия, преследующая те же цели, что и консолидация, однако потенциально воздействующая на опухолевые клетки, пережившие предыдущие этапы лечения § На сегодняшний день в целом ряде исследований в качестве альтернативы поддерживающей терапии используется трансплантация гемопоэтических стволовых клеток (ГСК).
основной метод лечения - полихимиотерапия, которая включает несколько этапов § I — индукция (достижение) ремиссии, направленная на уничтожение или значительное уменьшение объема опухолевого клона и нормализацию кроветворения § II — консолидация ремиссии, целью которой является уничтожение оставшихся (резидуальных) лейкемических клеток § III этапом является поддерживающая терапия, преследующая те же цели, что и консолидация, однако потенциально воздействующая на опухолевые клетки, пережившие предыдущие этапы лечения § На сегодняшний день в целом ряде исследований в качестве альтернативы поддерживающей терапии используется трансплантация гемопоэтических стволовых клеток (ГСК).
 § Современные программы лечения ОМЛ включают в себя на этапе индукции ремиссии базисную антрациклин-цитарабиновую комбинацию (схема « 7+3» ). В ряде протоколов этот лечебный этап модифицируют за счет добавления других химиопрепаратов (этопозид, тиогуанин), замены рубомицина другими антрациклиновыми препаратами и их аналогами (идарубицин или митоксантрон), использования комбинации цитарабина с другими химиопрепаратами (флударабин, топотекан).
§ Современные программы лечения ОМЛ включают в себя на этапе индукции ремиссии базисную антрациклин-цитарабиновую комбинацию (схема « 7+3» ). В ряде протоколов этот лечебный этап модифицируют за счет добавления других химиопрепаратов (этопозид, тиогуанин), замены рубомицина другими антрациклиновыми препаратами и их аналогами (идарубицин или митоксантрон), использования комбинации цитарабина с другими химиопрепаратами (флударабин, топотекан).
 § В течение последних 20 лет характер постремиссионной терапии претерпел значительные изменения. В настоящее время в большинстве лечебных протоколов преимущественно у больных моложе 60— 65 лет проводится интенсификация лечения путем эскалации доз цитарабина, что позволяет увеличить безрецидивную выживаемость, уменьшить общую продолжительность химиотерапии, а также отказаться от проведения длительной (на протяжении 2 лет) поддерживающей терапии низкими или стандартными дозами цитостатиков. Перечисленные лечебные подходы в целом позволяют получить ремиссии более чем у 70% больных, а также увеличить 5 -летнюю безрецидивную выживаемость до 45— 50%
§ В течение последних 20 лет характер постремиссионной терапии претерпел значительные изменения. В настоящее время в большинстве лечебных протоколов преимущественно у больных моложе 60— 65 лет проводится интенсификация лечения путем эскалации доз цитарабина, что позволяет увеличить безрецидивную выживаемость, уменьшить общую продолжительность химиотерапии, а также отказаться от проведения длительной (на протяжении 2 лет) поддерживающей терапии низкими или стандартными дозами цитостатиков. Перечисленные лечебные подходы в целом позволяют получить ремиссии более чем у 70% больных, а также увеличить 5 -летнюю безрецидивную выживаемость до 45— 50%
 § Важной составляющей современной терапии ОМЛ является трансплантация ГСК. Источником ГСК служит костный мозг или периферическая кровь. При ОМЛ, как и при других гемобластозах, применяют аллогенную трансплантацию ГСК от родственного или неродственного донора и аутологичную трансплантацию (трансплантация собственных ГСК при отсутствии поражения костного мозга, т. е. в периоде ремиссии). § Кроме того, проводятся аллогенная трансплантация ГСК пуповинной крови и трансплантация костного мозга или ГСК из периферической крови от гомозиготного близнеца (сингенная трансплантация), однако два последних метода используются крайне редко
§ Важной составляющей современной терапии ОМЛ является трансплантация ГСК. Источником ГСК служит костный мозг или периферическая кровь. При ОМЛ, как и при других гемобластозах, применяют аллогенную трансплантацию ГСК от родственного или неродственного донора и аутологичную трансплантацию (трансплантация собственных ГСК при отсутствии поражения костного мозга, т. е. в периоде ремиссии). § Кроме того, проводятся аллогенная трансплантация ГСК пуповинной крови и трансплантация костного мозга или ГСК из периферической крови от гомозиготного близнеца (сингенная трансплантация), однако два последних метода используются крайне редко
 Острый лимфобластный лейкоз § при ОЛЛ проводится дифференцированная терапия в зависимости от определенного варианта заболевания. Основные принципы терапии: многокомпонентность с использованием цитостатиков с различными механизмами действия, глюкокортикостероидов, трансплантации ГСК, использование новых молекулярно-направленных препаратов (ингибитор ABL-тирозинкиназы – иматиниб), обычно включает винкристин и преднизон вместе с L-аспарагиназой либо даунорубицином § индукция ремиссии построена по единому принципу и включает 2 фазы продолжительностью по 4 нед с использованием таких противоопухолевых препаратов, как винкристин, преднизолон, аспарагиназа, рубомицин, цитарабин, 6 меркаптопурин в зависимости от принадлежности больного к группе высокого или низкого риска
Острый лимфобластный лейкоз § при ОЛЛ проводится дифференцированная терапия в зависимости от определенного варианта заболевания. Основные принципы терапии: многокомпонентность с использованием цитостатиков с различными механизмами действия, глюкокортикостероидов, трансплантации ГСК, использование новых молекулярно-направленных препаратов (ингибитор ABL-тирозинкиназы – иматиниб), обычно включает винкристин и преднизон вместе с L-аспарагиназой либо даунорубицином § индукция ремиссии построена по единому принципу и включает 2 фазы продолжительностью по 4 нед с использованием таких противоопухолевых препаратов, как винкристин, преднизолон, аспарагиназа, рубомицин, цитарабин, 6 меркаптопурин в зависимости от принадлежности больного к группе высокого или низкого риска
 факторы неблагоприятного прогноза § § § возраст старше 35 лет лейкоцитоз длительное время достижения постоянной ремиссии § неблагоприятный иммунофенотип ОЛЛ § шанс пережить 5 -летний рубеж без рецидива имеют около 61% больных, при выявлении 2 факторов — лишь 25%. В то же время никто из пациентов не дожил до указанного срока при выявлении 3 и более прогностически неблагоприятных факторов
факторы неблагоприятного прогноза § § § возраст старше 35 лет лейкоцитоз длительное время достижения постоянной ремиссии § неблагоприятный иммунофенотип ОЛЛ § шанс пережить 5 -летний рубеж без рецидива имеют около 61% больных, при выявлении 2 факторов — лишь 25%. В то же время никто из пациентов не дожил до указанного срока при выявлении 3 и более прогностически неблагоприятных факторов
 Трансплантация стволовых клеток § как и химиотерапия, преследует цель уничтожения опухолевых § § клеток указанный метод лечения является этапом терапии и не может рассматриваться как замена химиотерапии Трансплантация схематично осуществляется следующим образом: Сначала больному проводится так называемая миелоаблативная (уничтожающая как нормальное, так и опухолевое кроветворение) химио- и/или лучевая терапия, которая иначе называется режимом кондиционирования. Затем больному осуществляется инфузия ГСК. Противоопухолевый эффект трансплантации получают за счет не только миелоаблативной химиотерапии, но и развития реакции «трансплантат против лейкоза» , при котором донорские иммунокомпетентные клетки действуют на лейкемические клетки реципиента, пережившие терапию высокими дозами цитостатиков.
Трансплантация стволовых клеток § как и химиотерапия, преследует цель уничтожения опухолевых § § клеток указанный метод лечения является этапом терапии и не может рассматриваться как замена химиотерапии Трансплантация схематично осуществляется следующим образом: Сначала больному проводится так называемая миелоаблативная (уничтожающая как нормальное, так и опухолевое кроветворение) химио- и/или лучевая терапия, которая иначе называется режимом кондиционирования. Затем больному осуществляется инфузия ГСК. Противоопухолевый эффект трансплантации получают за счет не только миелоаблативной химиотерапии, но и развития реакции «трансплантат против лейкоза» , при котором донорские иммунокомпетентные клетки действуют на лейкемические клетки реципиента, пережившие терапию высокими дозами цитостатиков.
 Методом выбора при § нейролейкемии является внутрилюмбальное введение метотрексата и облучение головы в дозе 2400 рад. § При наличии внекостномозговых лейкемических очагов (носоглотка, яичко, лимфатические узлы средостения и др. ), вызывающих сдавление органов и болевой синдром, показана локальная лучевая терапия в общей дозе 500 -2500 рад
Методом выбора при § нейролейкемии является внутрилюмбальное введение метотрексата и облучение головы в дозе 2400 рад. § При наличии внекостномозговых лейкемических очагов (носоглотка, яичко, лимфатические узлы средостения и др. ), вызывающих сдавление органов и болевой синдром, показана локальная лучевая терапия в общей дозе 500 -2500 рад
 Лечение инфекционных осложнений § антибиотики широкого спектра действия, направленные против наиболее частых возбудителей - синегнойной палочки, кишечной палочки, золотистого стафилококка. Курс не менее 5 дней, вводят внутривенно § Для профилактики инфекционных осложнений, особенно у больных с гранулоцитопенией, необходим тщательный уход за кожей и слизистой оболочкой полости рта, помещение больных в специальные асептические палаты, стерилизация кишечника с помощью неадсорбируемых антибиотиков (канамицин, ровамицин, неолепцин). § лечение геморрагии - переливание тромбоцитарной массы. Одномоментно больному переливают 200 -10000 г/л тромбоцитов 1 -2 раза в неделю. В некоторых случаях (ДВС – синдром) для купирования кровоточивости показано применение гепарина (при наличии внутрисосудистой коагуляции), эпсилонаминокапроновой кислоты (при повышенном фибронолизе).
Лечение инфекционных осложнений § антибиотики широкого спектра действия, направленные против наиболее частых возбудителей - синегнойной палочки, кишечной палочки, золотистого стафилококка. Курс не менее 5 дней, вводят внутривенно § Для профилактики инфекционных осложнений, особенно у больных с гранулоцитопенией, необходим тщательный уход за кожей и слизистой оболочкой полости рта, помещение больных в специальные асептические палаты, стерилизация кишечника с помощью неадсорбируемых антибиотиков (канамицин, ровамицин, неолепцин). § лечение геморрагии - переливание тромбоцитарной массы. Одномоментно больному переливают 200 -10000 г/л тромбоцитов 1 -2 раза в неделю. В некоторых случаях (ДВС – синдром) для купирования кровоточивости показано применение гепарина (при наличии внутрисосудистой коагуляции), эпсилонаминокапроновой кислоты (при повышенном фибронолизе).
 Агранулоцитоз – клинико-гематологичесий синдром, характеризующийся лейкопенией и значительным уменьшением, иногда вплоть до полного исчезновения, гранулоцитов из периферической крови
Агранулоцитоз – клинико-гематологичесий синдром, характеризующийся лейкопенией и значительным уменьшением, иногда вплоть до полного исчезновения, гранулоцитов из периферической крови
 Агранулоцитоз: § синдром общего заболевания § у детей встречается редко, чаще как симптом гипопластической анемии § бывает врожденный и приобретенный миелотоксический иммунный при воздействии ионизирующей радиации или цитотоксических лекарственных средств обусловленный либо появлением аутоантител (например, при красной волчанке), либо антител к гранулоцитам после приёма лекарственных средств, приобретающих при попадании в организм после соединения с белком свойства антигена
Агранулоцитоз: § синдром общего заболевания § у детей встречается редко, чаще как симптом гипопластической анемии § бывает врожденный и приобретенный миелотоксический иммунный при воздействии ионизирующей радиации или цитотоксических лекарственных средств обусловленный либо появлением аутоантител (например, при красной волчанке), либо антител к гранулоцитам после приёма лекарственных средств, приобретающих при попадании в организм после соединения с белком свойства антигена
 ЭТИОПАТОГЕНЕЗ: q. Ионизирующая радиация, лучевая терапия, химические вещества (бензол), инсектициды q. Лекарственные средства в результате прямого угнетения кроветворения (цитостатики, вальпроевая кислота, карбамазепин, беталактамные антибиотики), либо действуя как гаптены (препараты золота, антитиреоидные препараты и пр. ) q. Аутоиммунные заболевания (например, красная волчанка, аутоиммунный тиреоидит) q. Вирусные инфекции (вызванные вирусом Эпстайна —Барр, цитомегаловирус, жёлтая лихорадка, вирусные гепатиты) q. Тяжёлые генерализованные инфекции (как бактериальные, так и вирусные) q. Исхудание q. Генетические нарушения
ЭТИОПАТОГЕНЕЗ: q. Ионизирующая радиация, лучевая терапия, химические вещества (бензол), инсектициды q. Лекарственные средства в результате прямого угнетения кроветворения (цитостатики, вальпроевая кислота, карбамазепин, беталактамные антибиотики), либо действуя как гаптены (препараты золота, антитиреоидные препараты и пр. ) q. Аутоиммунные заболевания (например, красная волчанка, аутоиммунный тиреоидит) q. Вирусные инфекции (вызванные вирусом Эпстайна —Барр, цитомегаловирус, жёлтая лихорадка, вирусные гепатиты) q. Тяжёлые генерализованные инфекции (как бактериальные, так и вирусные) q. Исхудание q. Генетические нарушения
 Диагноз: 1. Клинические - общая слабость, гингивит, стоматит - язвенно-некротическое поражение слизистых оболочек рта, глотки, желудочно-кишечного тракта - высокая температура тела - иногда умеренное увеличение печени, селезенки и регионарных лимфоузлов - бактериальные и грибковые инфекции
Диагноз: 1. Клинические - общая слабость, гингивит, стоматит - язвенно-некротическое поражение слизистых оболочек рта, глотки, желудочно-кишечного тракта - высокая температура тела - иногда умеренное увеличение печени, селезенки и регионарных лимфоузлов - бактериальные и грибковые инфекции
 2. Лабораторные В периферической крови: лейкопения (1 -2) • 10*9/л и ниже, относительный лимфоцитоз, гранулоцитопения (от 20 % до 0 гранулоцитов, с грубой токсической зернистостью), умеренная анемия, анизоцитоз, полихромазия. В тяжелых случаях - тромбоцитопения, сопровождающаяся гемморрагическим синдромом Картина костного мозга непостоянна - от незначительного функционального угнетения гранулоцитопоэза до выраженной гипоплазии гранулоцитарного ростка. Система красной крови и мегакариоцитарный аппарат поражаются редко
2. Лабораторные В периферической крови: лейкопения (1 -2) • 10*9/л и ниже, относительный лимфоцитоз, гранулоцитопения (от 20 % до 0 гранулоцитов, с грубой токсической зернистостью), умеренная анемия, анизоцитоз, полихромазия. В тяжелых случаях - тромбоцитопения, сопровождающаяся гемморрагическим синдромом Картина костного мозга непостоянна - от незначительного функционального угнетения гранулоцитопоэза до выраженной гипоплазии гранулоцитарного ростка. Система красной крови и мегакариоцитарный аппарат поражаются редко
 Диагноз: основывается на клиническом симптомокомплексе и характерных изменениях периферической крови Картина костного мозга весьма динамична и имеет до некоторой степени относительное значение
Диагноз: основывается на клиническом симптомокомплексе и характерных изменениях периферической крови Картина костного мозга весьма динамична и имеет до некоторой степени относительное значение
 Лечение агранулоцитоза 1. Устранение причинных факторов 2. Создание стерильных условий для больного 3. Профилактика и лечение инфекционных осложнений В комплексной терапии инфекционных осложнений при агранулоцитозе рекомендуются также применение внутривенно иммуноглобулина в дозе 400 мг/кг однократно, внутривенное введение антистафилококковой плазмы 100 -150 мл 1 раз в день в течение 4 -5 дней. 4. Переливание лейкоцитарной массы - при резко выраженном снижении лейкоцитов
Лечение агранулоцитоза 1. Устранение причинных факторов 2. Создание стерильных условий для больного 3. Профилактика и лечение инфекционных осложнений В комплексной терапии инфекционных осложнений при агранулоцитозе рекомендуются также применение внутривенно иммуноглобулина в дозе 400 мг/кг однократно, внутривенное введение антистафилококковой плазмы 100 -150 мл 1 раз в день в течение 4 -5 дней. 4. Переливание лейкоцитарной массы - при резко выраженном снижении лейкоцитов
 Лечение агранулоцитоза: 5. Глюкокортикоидные препараты преимущественно при иммунном агранулоцитозе в связи со стимуляцией гранулоцитопоэза и торможением продукции антилейкоцитарных антител (преднизолон 40 - 100 мг/сут) 6. Стимуляторы лейкопоэза: натрия нуклеинат 5 мл 5% раствора 2 раза в день в/м или внутрь по 0. 2 -0. 4 г 3 -5 раз в день; лейкоген 0. 02 г 3 раза в день, пентоксил по 0. 1 -0. 15 г 3 -4 раза в день после еды. Курс лечения - 2 -4 недели. Применяют колониестимулирующие факторы молграмостим, лейкомакс 3 -10 мкг/кг подкожно в течение 7 -10 дней. 7. Дезинтоксикационная терапия При выраженной интоксикации проводится дезинтоксикационная терапия: внутривенно капельно вводят гемодез 400 мл 1 раз в день, 5% раствор глюкозы 500 мл, изотонический раствор натрия хлорида или раствор Рингера 0. 5 -1 л.
Лечение агранулоцитоза: 5. Глюкокортикоидные препараты преимущественно при иммунном агранулоцитозе в связи со стимуляцией гранулоцитопоэза и торможением продукции антилейкоцитарных антител (преднизолон 40 - 100 мг/сут) 6. Стимуляторы лейкопоэза: натрия нуклеинат 5 мл 5% раствора 2 раза в день в/м или внутрь по 0. 2 -0. 4 г 3 -5 раз в день; лейкоген 0. 02 г 3 раза в день, пентоксил по 0. 1 -0. 15 г 3 -4 раза в день после еды. Курс лечения - 2 -4 недели. Применяют колониестимулирующие факторы молграмостим, лейкомакс 3 -10 мкг/кг подкожно в течение 7 -10 дней. 7. Дезинтоксикационная терапия При выраженной интоксикации проводится дезинтоксикационная терапия: внутривенно капельно вводят гемодез 400 мл 1 раз в день, 5% раствор глюкозы 500 мл, изотонический раствор натрия хлорида или раствор Рингера 0. 5 -1 л.


