Лекция_03.04.ppt
- Количество слайдов: 57

Особые свойства дисперсных систем. Методы дисперсионного анализа Одной из важных характеристик дисперсных систем является дисперсность, т. е степень раздробленности вещества дисперсной фазы и ее размер. Коллоидная химия рассматривает дисперсные системы, размер частиц которых может меняться в достаточно широком интервале – от 10 -9 до 10 -4 м. Именно размер частиц определяет основные свойства таких систем. Например, в системах с размером частиц большим 1 мкм, наблюдается явление седиментации, приводящее к разделению дисперсной фазы и дисперсионной среды. Кроме того, дисперсную фазу, находящуюся в твердом состоянии, в таких системах можно отделить и фильтрацией, поскольку частицы такого размера не проходят через обычные фильтры.
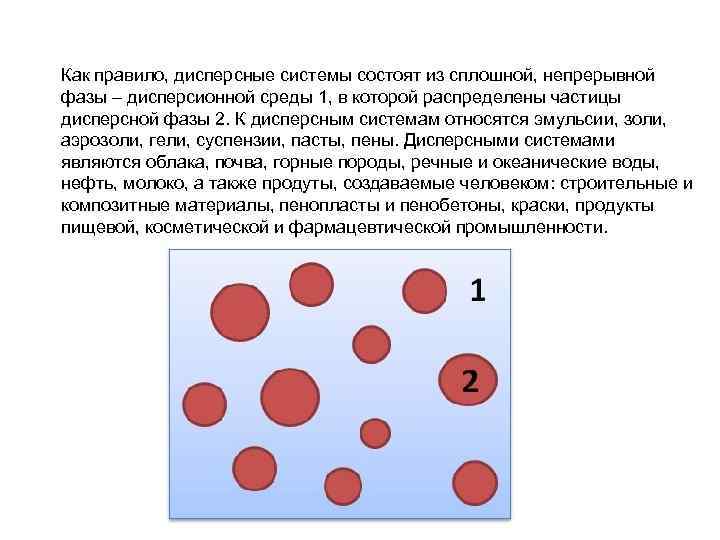
Как правило, дисперсные системы состоят из сплошной, непрерывной фазы – дисперсионной среды 1, в которой распределены частицы дисперсной фазы 2. К дисперсным системам относятся эмульсии, золи, аэрозоли, гели, суспензии, пасты, пены. Дисперсными системами являются облака, почва, горные породы, речные и океанические воды, нефть, молоко, а также продуты, создаваемые человеком: строительные и композитные материалы, пенопласты и пенобетоны, краски, продукты пищевой, косметической и фармацевтической промышленности.
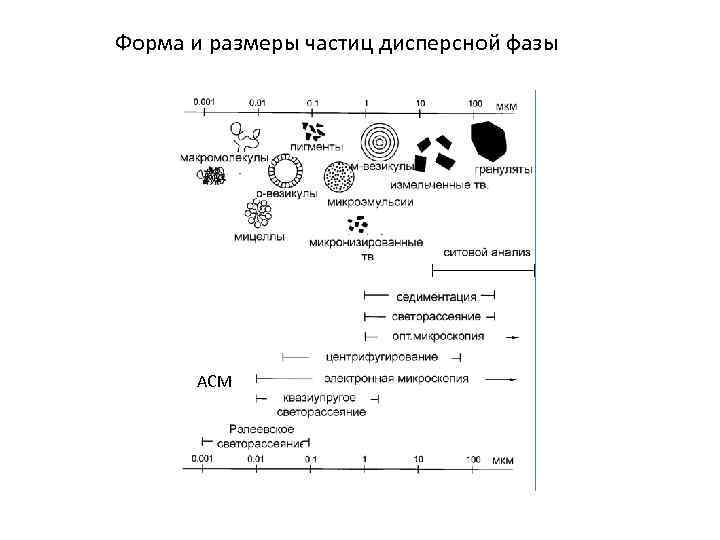
Форма и размеры частиц дисперсной фазы АСМ

Высокодисперсными являются системы с размером частиц менее 1 мкм, системы с частицами большего размера называют грубодисперсными. Системы с размером частиц до 100 нм относят к ультрамикрогетерогенным коллоидным системам или наносистемам. Классификация дисперсных систем по размерам частиц вызвана тем, что физические и химические свойства малых частиц значительно отличаются от свойств более крупных объектов. К числу таких свойств относятся прочность, теплоемкость, температура плавления, магнитные и электрические характеристики, реакционная способность. Количественными характеристиками дисперсности также служат удельная поверхность (отношение поверхности частиц к их массе) и дисперсность (отношение поверхности частиц к их объему).
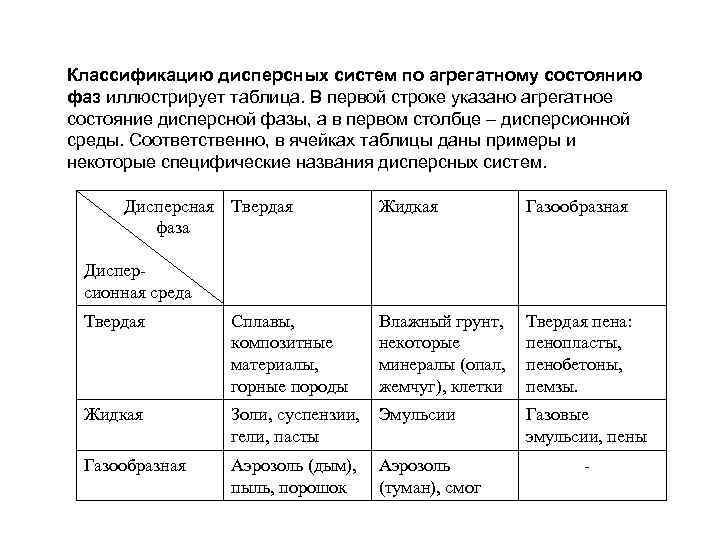
Классификацию дисперсных систем по агрегатному состоянию фаз иллюстрирует таблица. В первой строке указано агрегатное состояние дисперсной фазы, а в первом столбце – дисперсионной среды. Соответственно, в ячейках таблицы даны примеры и некоторые специфические названия дисперсных систем. Дисперсная Твердая Жидкая Газообразная фаза Дисперсионная среда Твердая Сплавы, композитные материалы, горные породы Влажный грунт, некоторые минералы (опал, жемчуг), клетки Твердая пена: пенопласты, пенобетоны, пемзы. Жидкая Золи, суспензии, Эмульсии гели, пасты Газовые эмульсии, пены Газообразная Аэрозоль (дым), Аэрозоль пыль, порошок (туман), смог -
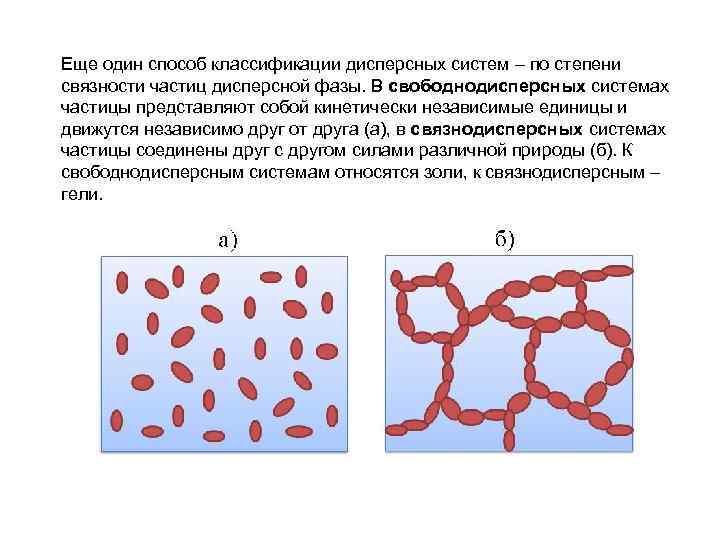
Еще один способ классификации дисперсных систем – по степени связности частиц дисперсной фазы. В свободнодисперсных системах частицы представляют собой кинетически независимые единицы и движутся независимо друг от друга (а), в связнодисперсных системах частицы соединены друг с другом силами различной природы (б). К свободнодисперсным системам относятся золи, к связнодисперсным – гели.
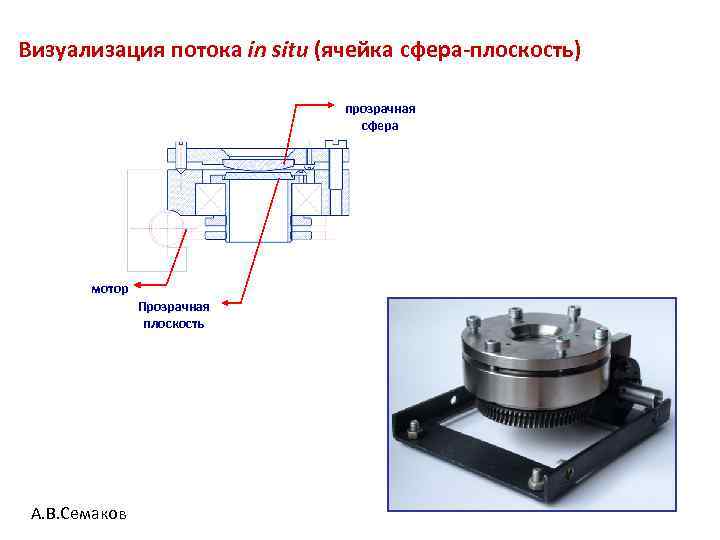
Визуализация потока in situ (ячейка сфера-плоскость) прозрачная сфера мотор Прозрачная плоскость А. В. Семаков

Даже для крупных частиц ПММА (d~60 мкм) локализация и упорядочение могут наблюдаться в реальном времени
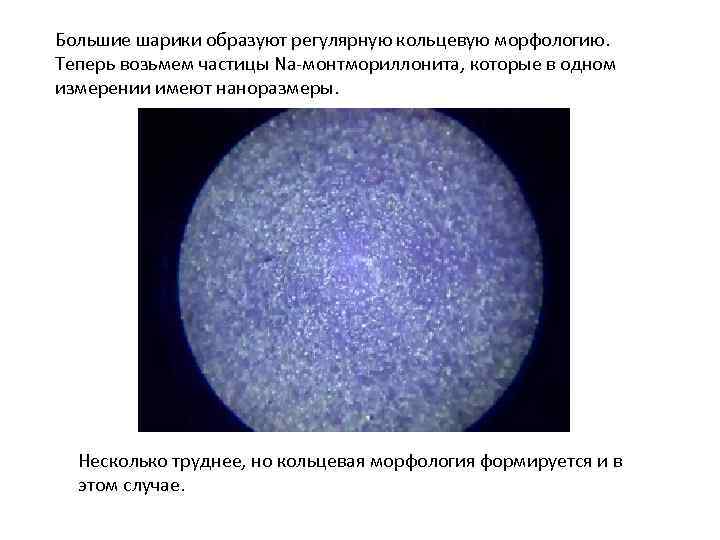
Большие шарики образуют регулярную кольцевую морфологию. Теперь возьмем частицы Na-монтмориллонита, которые в одном измерении имеют наноразмеры. Несколько труднее, но кольцевая морфология формируется и в этом случае.
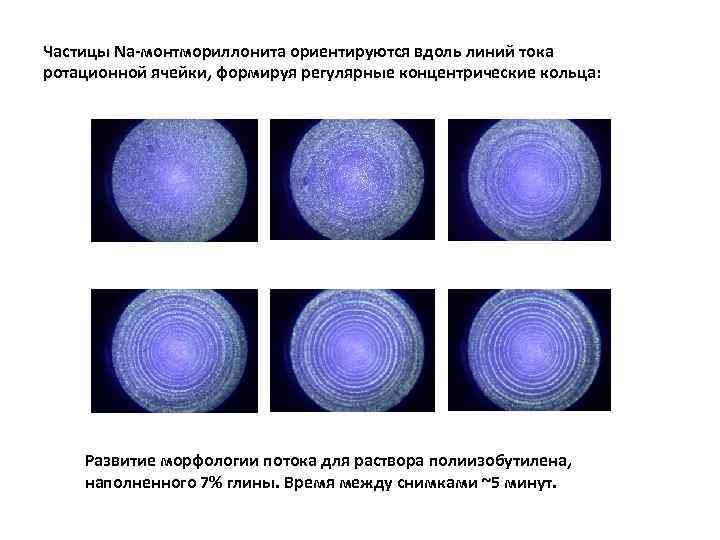
Частицы Na-монтмориллонита ориентируются вдоль линий тока ротационной ячейки, формируя регулярные концентрические кольца: Развитие морфологии потока для раствора полиизобутилена, наполненного 7% глины. Время между снимками ~5 минут.

По устойчивости дисперсных систем различают термодинамически устойчивые (лиофильные) системы и термодинамически неустойчивые (лиофобные). Лиофильные системы отличаются малым значением межфазного натяжения (ниже 10 -2 м. Дж/м 2), сходной химической природой дисперсной фазы и дисперсионной среды; системы образуются самопроизвольно. К термодинамически устойчивым системам относятся микроэмульсии, мицеллярные растворы. Термодинамически неустойчивые системы состоят из неродственных фаз, имеют высокое значение натяжения на границе частиц со средой и для их образования надо затратить работу. Наиболее характерными представителями таких систем являются пены, аэрозоли.

Для частиц малого размера характерно участие в броуновском движении, а сами дисперсные системы характеризуются необычными оптическим свойствами, связанными с рассеянием света на частицах дисперсной фазы. Рассеянием света обусловлена опалесценция или эффект Тиндаля (Тьендаля). Обычно этот эффект наблюдается при прохождении светового луча через оптически неоднородную среду в виде светящегося конуса, выделяющегося на темном фоне. Таким образом можно легко отличить молекулярные растворы от коллоидных систем. Для проводящих частиц (золей металлов, оксидов, сульфидов) характерно избирательное поглощение света, которое зависит от размера частиц. Например, высокодисперсные золи золота с радиусом частиц r = 20 нм имеют интенсивно красную окраску (область поглощения этих золей лежит в зеленой части спектра), а золи с r = 50 нм окрашены в синий цвет.

Широкое разнообразие дисперсных систем предопределяет самые различные методы оценки размеров частиц дисперсной фазы и распределения их по размерам. Совокупность методов определения размеров частиц, формы, распределения частиц по размерам носит название дисперсионного анализа. Все методы дисперсионного анализа основаны на том или ином свойстве дисперсной системы и ограничены определенным интервалом размеров частиц, в котором может быть использован тот или иной метод.

Кинетические свойства дисперсных систем Броуновское движение ‑ беспорядочное движение малых (размером 10 -9 – 10 -6 м) частиц, взвешенных в жидкости или газе. Это явление было открыто Р. Броуном в 1827, который наблюдал под микроскопом беспорядочное движение мельчайших частиц различной природы. Интенсивность броуновского движения увеличивается с ростом температуры среды, с уменьшением вязкости жидкости и размеров частиц. Объяснение броуновского движения было дано А. Эйнштейном и М. Смолуховским в 1905 -06 гг на основе молекулярно-кинетической теории. Согласно этой теории, молекулы жидкости находятся в постоянном тепловом движении, причём импульсы различных молекул неодинаковы по величине и направлению. Если поверхность частицы достаточно велика по сравнению с размерами молекул среды, то удары, испытываемые частицей со стороны окружающих её молекул, не будут точно компенсироваться.

Сила, действующая на единицу поверхности частицы также флуктуирует и в любой момент возникает несбалансированная сила. Поэтому в результате «бомбардировки» молекулами броуновская частица приходит в беспорядочное движение, изменяя величину и направление своей скорости примерно до 1020 раз в секунду. Результирующее движение частицы определяемое случайными изменением мгновенных сил зависит от противодействующих сил вязкого сопротивления, также зависящих от скорости частицы. При наблюдении броуновского движения регистрируется положение частицы через равные промежутки времени.

Мерой хаотического движения частицы может служить величина

Броуновское движение является непосредственной причиной диффузии коллоидных частиц. Диффузией называется процесс самопроизвольного выравнивания концентраций, приводящий к установлению одинакового химического потенциала каждого компонента во всех элементах объема данной системы. Если дисперсную систему, содержащую с молей частиц дисперсной фазы, привести в контакт с дисперсионной средой, то градиент химического потенциала при переносе частиц из области с высоким химическим потенциалом в область с более низким химическим потенциалом может быть представлен в виде: (2) где ‑ число молей частиц дисперсной фазы в единице объема (предполагая, что в 1 моле 6. 1023 частиц), - градиент концентрации.

В этом случае сила, действующая на одну частицу дисперсной фазы, будет равна , Движению частицы препятствует сила вязкого сопротивления, в определенный момент эти силы становятся равными, что позволяет определить скорость движения частицы , и поток частиц, который будет равен произведению скорости на концентрацию частиц: (3)

Вместе с тем, в соответствии с первым законом Фика поток диффузии jd – количество вещества, проходящего за 1 сек. через единицу поверхности S, перпендикулярной данному потоку, будет равен: , (4) где D – коэффициент диффузии (м 2 с-1), (величина постоянная для стационарной диффузии), Из сопоставления уравнений (3) и (4) следует, что: (5) Полученное выражение для коэффициента диффузии позволяет найти простую связь между этой величиной и средним сдвигом частицы: (6) Таким образом, измеряя скорость движения фронта диффундирующих частиц, можно определить коэффициент диффузии и радиус частиц дисперсной фазы.

Оптические свойства дисперсных систем Оптические свойства свободнодисперсных систем определяются свойствами частиц дисперсной фазы, и их изучение позволяет определить не только размер частиц, но и их форму и концентрацию. При падении луча света на дисперсную систему могут наблюдаться следующие явления: преломление света частицами дисперсной фазы; отражение света от поверхности частиц; рассеяние света; поглощение света частицами дисперсной фазы. Преломление и отражение света наблюдается в дисперсных системах, размер частиц которых превышает длину волны падающего света (микрогетерогенные системы с размерами частиц больше 10 -6 м). Визуально это явление выражается в мутности таких систем, наблюдаемой как в проходящем, так и в отраженном свете. Рассеяние света наблюдается, если размер частиц в дисперсной системе меньше длины волны падающего света.

Теория статического светорассеяния для непроводящих частиц была развита Релеем. Исходя из следующих допущений, ‑ частицы имеют сферическую форму, ‑ радиус частиц меньше длины волны падающего света ( ); ‑ частицы не поглощают свет, т. е. золи являются бесцветными; ‑ частицы оптически изотропны, ‑ расстояние между частицами в системе больше длины волны падающего света, т. е. концентрация частиц мала; ‑ объем дисперсной системы также мал, и можно не учитывать вторичное рассеяние света, Релей получил уравнение, связывающее интенсивность падающего света с интенсивностью света, рассеянного единицей объема системы : (9), где и ‑ показатели преломления частиц и среды, n ‑ число частиц дисперсной фазы в единице объема, ‑ объем одной частицы; ‑ длина волны падающего света. Величина t характеризует способность системы рассевать свет и называется мутностью дисперсной системы.

Нефелометрический метод основан на измерении интенсивности света, рассеянного дисперсной системой. Уравнение (9) можно представить в виде: (10),

Турбодиметрический метод основан на измерении интенсивности света, прошедшего через дисперсную систему. Свет при прохождении через дисперсную систему может поглощаться как дисперсионной средой, так и дисперсной фазой. Если дисперсионная среда и дисперсная фаза для света данной длины волны являются прозрачными, т. е. не происходит поглощения, то уменьшение интенсивности прошедшего света будет связано только с его рассеянием, т. е. рассеянный свет можно считать условно поглощенным. В этом случае уменьшение интенсивности света будет пропорционально интенсивности падающего света и приращению толщины слоя, через который проходит свет: Интегрирование этого выражения приводит к уравнению: (11)

Ультрамикроскопический метод определения размера частиц основан на наблюдении светорассеяния единичной частицей дисперсной фазы в обычном оптическом микроскопе. При боковом освещении дисперсной системы под микроскопом коллоидные частицы идентифицируются в виде отдельных светлых точек. Подсчитывая среднее частиц и число их в единице объема, можно найти объем, а, следовательно, и радиус одной частицы. В современных ультрамикроскопах источниками света служат лазеры, а счет частиц производится электронными фотоумножителями, соединенными с компьютером. Такие приборы позволяют с большой точностью определить как размер, так и распределение частиц по размерам.

Метод динамического (квазиупругого) рассеяния света используется для частиц, размер которых лежит в интервале от нескольких нм до сотен нм. В этом методе измеряется зависимость интенсивности рассеяния света в дисперсной системе от времени при данной длине волны. Броуновское движение частиц дисперсной фазы приводит к флуктуациям их локальной концентрации. Результатом этого являются локальные неоднородности показателя преломления и соответственно - флуктуации интенсивности рассеянного света при прохождении лазерного луча через такую среду. Коэффициент диффузии обратно пропорционален характерному времени релаксации флуктуаций интенсивности рассеянного света. Рассеянный свет аккумулируется фотодетектором и преобразуется коррелятором для получения автокорреляционной функции. Компьютерный расчет этой функции дает значение среднего гидродинамического радиуса частиц, определенного из уравнения Стокса-Эйнштейна:

Устойчивость дисперсных систем Под устойчивостью дисперсных систем понимают их способность сохранять неизменным исходный размер частиц и равномерное распределение частиц по объему системы. Различают седиментационную и агрегативную устойчивость.

Седиментационная устойчивость При рассмотрении броуновского движения и диффузии влиянием гравитационного поля можно было пренебречь вследствие малого размера частиц. С увеличением размера влияние сил гравитации возрастает и в интервале радиусов частиц от 10 -6 до 10 -4 м в свободнодисперсных системах наблюдается оседание (или всплывание в зависимости от соотношения плотностей дисперсной фазы и дисперсионной среды) частиц. Это явление называется седиментацией. Седиментационная устойчивость – это устойчивость системы против снижения потенциальной энергии частиц дисперсной фазы при их оседании под действием силы тяжести. Условием седиментационной устойчивости свободнодисперсных систем является достаточно малый размер частиц.

В поле силы тяжести на каждую сферическую частицу с радиусом r действует сила Fg, равная Fg= (4/3)πr 3(ρ – ρ0) g, где g – ускорение силы тяжести, ρ и ρ0 – плотности вещества частицы и дисперсионной среды соответственно. Под действием этой силы происходит равноускоренное движение частиц. По мере увеличения скорости нарастает сила, препятствующая движению, обусловленная вязкостью дисперсионной среды η. По закону Стокса сила вязкого сопротивления равна: Fη= B v = 6π η r v , где B = 6πηr – коэффициент вязкого сопротивления, v – скорость движения частицы.

Ускоренное движение частиц под действием силы тяжести Fg происходит до тех пор, пока сила Fg не уравновесится силой вязкого сопротивления Fη; после этого движение становится равномерным и осуществляется с постоянной скоростью. Из условия Fg= Fη следует, что v = 2 r 2 (ρ – ρ0) g/9 η или v ~ r 2Δρ/ η Соответственно, время разрушения дисперсной системы t при оседании частиц из столба высотой H (t =H/ v) будет зависеть от r, η и Δρ как t ~ H η /(r 2Δρ) т. е. система тем устойчивей, чем меньше размер частиц, выше вязкость среды и меньше разность плотностей частицы и среды.

Вместе с тем, седиментация частиц, приводящая к расслоению дисперсной системы и увеличению разности концентрации между верхними и нижними слоями, сопровождается уменьшением энтропии системы. Этому будет препятствовать броуновское движение частиц, вызывающее их диффузию в направлении обратном седиментации. Для выявления приоритетного процесса (седиментации или диффузии) сравнивают потоки, т. е. число частиц n , проходящих за 1 с через единицу площади, нормальной к направлению движения. Соответственно, седиментационный поток равен: jc = v n, а диффузионный поток по закону Фика равен jд = – D dn /dz где D – коэффициент диффузии, равный по закону Эйнштейна D = k. T/6πηr dn/ dz – градиент концентрации по высоте z.

При jc > jд – преобладает седиментация, что обычно и имеет место в грубодисперсных системах; при jc < jд – диффузия, и система оказывается седиментационно устойчивой, что характерно для коллоидных систем. В системах с некоторым средним размером частиц седиментационные и диффузионные потоки могут уравновешивать друга, т. е. jc = jд. Это приводит к возникновению седиментационно-диффузионного равновесия: v n = – D d n/ d z или dn/dz=-(n/D)dz Интегрирование этого выражения дает равновесное распределение концентрации частиц n по высоте z: n(z) = n 0 exp(–v z / D) = n 0 exp[– (4/3)πr 3Δρg z/k. T] = n 0 exp[– meg z/k. T], где n 0 – концентрация частиц на уровне, принятом за нулевой, me =(4/3) πr 3(ρ – ρ0) – эффективная масса частиц (с учетом архимедовой поправки).

Это уравнение позволяет определить высоту z, на которой концентрация дисперсной фазы уменьшается в определенное число раз, например, в е раз, по сравнению с высотой z = 0. z 1/e =D/v Для дисперсных систем с размером частиц r < 0, 1 мкм непосредственное наблюдение установления седиментационнодиффузионного равновесия в поле силы тяжести Земли существенно затруднено или оказывается практически невозможным, так как равновесие достигается чрезвычайно медленно. Поскольку tсед ~ z 1/e /v и z 1/e ~ D /v , следует, что tсед~ D /v 2. Подставляя в это выражение D = k. T/6π η r и v =2 r 2(ρ – ρ0) g /9 η, находим, что время установления равновесия обратно пропорционально пятой степени размера частиц, т. е. t ~ 1/r 5.

Соответственно, для частиц с радиусом заметно меньшим 0, 1 мкм, это время достигает нескольких лет. Равновесие может быть сдвинуто в сторону преобладания седиментации при замене гравитационного поля центробежным со значительно бόльшим ускорением. Это возможно достигнуть в центрифугах и ультрацентрифугах, позволяющих создавать ускорения до 105 -106 g и благодаря этому проводить не только седиментацию коллоидных частиц, но даже и седиментационное разделение молекул разной массы.

Итак, в земных условиях седиментационно устойчивыми являются тонкие (особенно коллоидные) взвеси. Многие из таких взвесей вызывают у человека такие тяжелые заболевания, как антракоз (угольная пыль) и силикоз (силикатная пыль, которой много на цементных заводах). Кроме того, тонкие устойчивые взвеси органических веществ (уголь, лаки, сахар и т. п. ) являются еще и взрывоопасными, т. к. возгорание быстро распространяется по громадной поверхности, сопровождаясь одновременным выделением большого количества энергии. Поэтому разрушение таких дисперсий представляет важную экологическую и технологическую задачу. Путь нарушения седиментационной устойчивости – укрупнение частиц. С этой целью проводится искусственное дождевание с использованием добавок ПАВ для улучшения смачивания водой органических частиц. Капли воды захватывают частицы пыли и падая обеспечивают их оседание. Всем хорошо известны факты освежения воздуха после дождя и вблизи фонтанов.

Простая связь между размером частиц r и скоростью их седиментации: r=K v, где K= 9 η/2(ρ-ρ0 )g – постоянная для данной системы и условий опыта, лежит в основе седиментационного анализа, позволяющего по изучению седиментации определять дисперсный состав системы – размер частиц и их распределение по размерам.

Агрегативная устойчивость – это устойчивость системы к укрупнению частиц. Для лиофобных дисперсных систем характерен большой избыток свободной поверхностной энергии Fs=σ12 S. Чем выше дисперсность (выше S), тем больше энергия системы и тем в большей степени она удалена от состояния равновесия. Поэтому в дисперсных системах самопроизвольно протекают процессы, приводящие к уменьшению свободной поверхностной энергии, т. е. ΔFs < 0. К таким процессам относятся коагуляция (сцепление частиц с образованием агрегатов), коалесценция (слияние капель), изотермическая перегонка (перенос вещества при постоянной температуре от мелких частиц к более крупным).

Так как ΔFs = σ12 ΔS+Δσ12 S, уменьшение поверхностной энергии ΔFs < 0 может быть обусловлено как уменьшением поверхности раздела фаз Δs < 0 при неизменном поверхностном натяжении (σ12=const), так и снижением σ (Δσ12< 0) при неизменной поверхности раздела фаз (s =const). Первый случай ΔFs = σ12ΔS < 0 реализуется при коалесценции капель и при изотермической перегонке вещества. При срастании кристаллических частиц также происходит частичное исчезновение поверхности раздела в месте срастания.

При коагуляции поверхность раздела фаз не меняется, т. к. в месте контакта частиц, как правило, остается тонкая пленка жидкой дисперсионной среды. Уменьшение Fs в этом случае достигается в результате частичного взаимного насыщения поверхностных сил – нескомпенсированных молекулярных сил на границе раздела фаз, что эквивалентно локальному снижению поверхностного натяжения σ12 в зоне соприкосновения (контакта) частиц, т. е. ΔFs = Δσ12 S < 0. В отличие от процессов коалесценции и изотермической перегонки, являющихся необратимыми процессами, коагуляция – процесс обратимый. Обратным коагуляции является процесс пептизации, не требующий для его протекания приложения энергии извне.

Будучи термодинамически неустойчивыми, лиофобные дисперсные системы могут достаточно долго сохранять без изменения исходную дисперсность, т. е. оставаться агрегативно устойчивыми. Это обеспечивается действием различных факторов стабилизации, которые затрудняют протекание процессов, приводящих к разрушению систем. К основным факторам стабилизации относятся: - электростатическое отталкивание диффузных частей двойных электрических слоев (ионно-электростатическая составляющая расклинивающего давления); - «лиофилизация» поверхности за счет адсорбции ПАВ; - образование на поверхности гидрофильных частиц структурированных слоев воды с измененными свойствами по сравнению с объемной жидкостью – повышенной вязкостью (структурная составляющая расклинивающего давления); - структурно-механический барьер (по Ребиндеру).

Агрегативная устойчивость непосредственно влияет и на седиментационную устойчивость: нарушение агрегативной устойчивости, приводящее к укрупнению частиц, вызывает снижение и нарушение седиментационной устойчивости.

Расклинивающее давление в тонких пленках В процессе теплового движения коллоидные частицы сталкиваются друг с другом. Их дальнейшая «судьба» – останутся ли они в сцепленном состоянии, т. е. произойдет ли коагуляция, или они разойдутся, и система сохранит агрегативную устойчивость – будет в основном зависеть от свойств тонких пленок в зазоре между частицами.
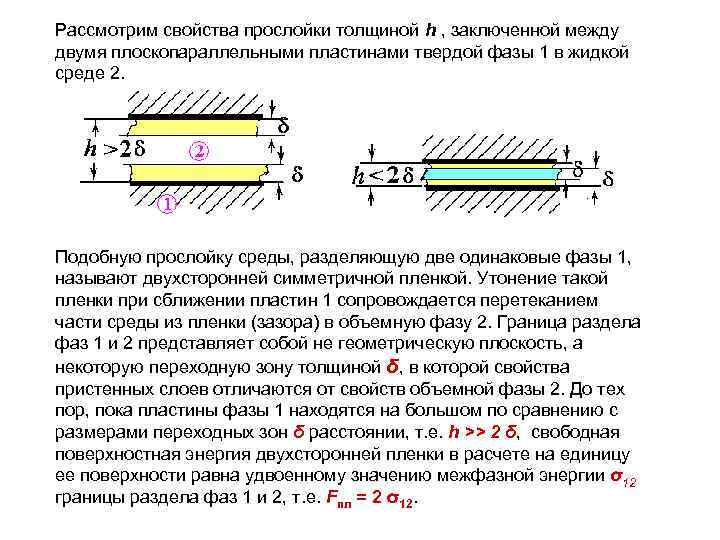
Рассмотрим свойства прослойки толщиной h , заключенной между двумя плоскопараллельными пластинами твердой фазы 1 в жидкой среде 2. Подобную прослойку среды, разделяющую две одинаковые фазы 1, называют двухсторонней симметричной пленкой. Утонение такой пленки при сближении пластин 1 сопровождается перетеканием части среды из пленки (зазора) в объемную фазу 2. Граница раздела фаз 1 и 2 представляет собой не геометрическую плоскость, а некоторую переходную зону толщиной δ, в которой свойства пристенных слоев отличаются от свойств объемной фазы 2. До тех пор, пока пластины фазы 1 находятся на большом по сравнению с размерами переходных зон δ расстоянии, т. е. h >> 2 δ, свободная поверхностная энергия двухсторонней пленки в расчете на единицу ее поверхности равна удвоенному значению межфазной энергии σ12 границы раздела фаз 1 и 2, т. е. Fпл = 2 σ12.
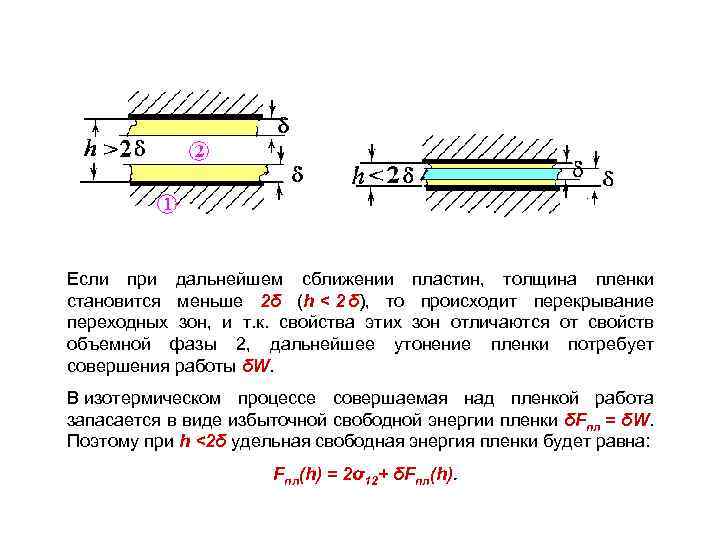
Если при дальнейшем сближении пластин, толщина пленки становится меньше 2δ (h < 2 δ), то происходит перекрывание переходных зон, и т. к. свойства этих зон отличаются от свойств объемной фазы 2, дальнейшее утонение пленки потребует совершения работы δW. В изотермическом процессе совершаемая над пленкой работа запасается в виде избыточной свободной энергии пленки δFпл = δW. Поэтому при h <2δ удельная свободная энергия пленки будет равна: Fпл(h) = 2σ12+ δFпл(h).

Изменение энергии системы при уменьшении толщины пленки можно рассматривать как результат преодоления некоторого избыточного давления, названного Дерягиным расклинивающим давлением. Расклинивающее давление Π = Π(h) – это то избыточное давление, которое необходимо приложить к ограничивающим пленку поверхностям, чтобы толщина пленки h оставалась постоянной. Расклинивающее давление можно рассматривать как избыточное (по сравнению с объемами фаз) давление, которое действует со стороны прослойки на поверхности пластин и стремится их раздвинуть (расклинить).

Чтобы в равновесном процессе уменьшить толщину прослойки на величину dh, необходимо совершить работу, равную d. W = – Π(h)dh. Соответственно, связь между расклинивающим давлением Π, энергией пленки Fпл и ее толщиной h можно записать в виде: Π = – d Fпл(h)/ dh = –dδFпл(h)/ d h Это выражение аналогично по смыслу выражению p = –d. F/d. V, описывающему связь объемного давления, свободной энергии и объема фазы. Следовательно, δFпл(h) = – Π(h) d h.

Расклинивающее давление может быть как положительным, т. е. препятствовать утонению пленки и сближению пластин, так и отрицательным – способствовать утонению пленки и сближению пластин. Расклинивающее давление может иметь различную физикохимическую природу. Соответственно, Дерягиным было предложено рассматривать различные составляющие этой термодинамической величины.

Молекулярная составляющая расклинивающего давления обусловлена молекулярным притяжением. Между сближаемыми пластинами действуют силы притяжения, связанные с проявлением дальнодействующих дисперсионных взаимодействий. Так как дисперсионные взаимодействия суммируются по объемам взаимодействующих фаз, результат суммирования дает зависимость энергии взаимодействия (притяжения) в вакууме 2 -х объемов (пластин) в расчете на единицу поверхности от ширины зазора h в виде Umol = - A 11 /12 π h 2 [Дж/м 2], где A 11 – константа Гамакера.

При взаимодействии пластин в конденсированной среде 2, вместо константы A 11 используется сложная константа Гамакера A*, учитывающая взаимодействие молекул фазы 1 и фазы 2: A* = (√A 11 – √A 22)2, Соответственно, энергия притяжения двух объемов фазы 1 в среде 2, выразится как Umol = – A*/12 π h 2 [Дж/м 2], Поскольку имеет место притяжение, Umol < 0.

Umol – это работа, которую необходимо приложить к единице площади пластин, чтобы удалить их с расстояния h на бесконечно большое расстояние в обратимом равновесном процессе. Она равна энергии, которая выделяется при сближении пластин с h = ∞ до данного расстояния h под действием сил молекулярного притяжения. Соответственно, энергия взаимодействия U равна ∆Fпл(h) и, в случае действия только молекулярных сил, Umol < 0 и Π = – d ∆Fпл(h)/ d h = – А*/6 π h 3< 0.

Таким образом, при действии только молекулярных сил, происходит самопроизвольное сближение поверхностей пластин и утонение пленки. Для двух сферических частиц радиусом r их полная энергия и сила молекулярного притяжения могут быть записаны как Uсф = – А* r/ 12 h [Дж] и F = – А* r/12 h 2 [H] и характеризуют энергию и силу сцепления частиц в контакте Uк и Fк.

Электростатическая составляющая расклинивающего давления связана с электростатическим отталкиванием диффузных слоев ионов, окружающих частицы дисперсной фазы. При контакте твердых частиц с водной фазой и особенно с раствором электролитов на границе раздела возникает двойной электрический слой (ДЭС). Толщина диффузного слоя δ зависит от концентрации электролита с0, зарядности ионов z и температуры Т: δ ~ √(Т/z 2 с0). При сближении двух поверхностей, на которых имеется ДЭС, при расстоянии h < 2 δ происходит перекрывание диффузных слоев противоионов, сопровождающееся возникновением отталкивания одноименных зарядов (рисунок).
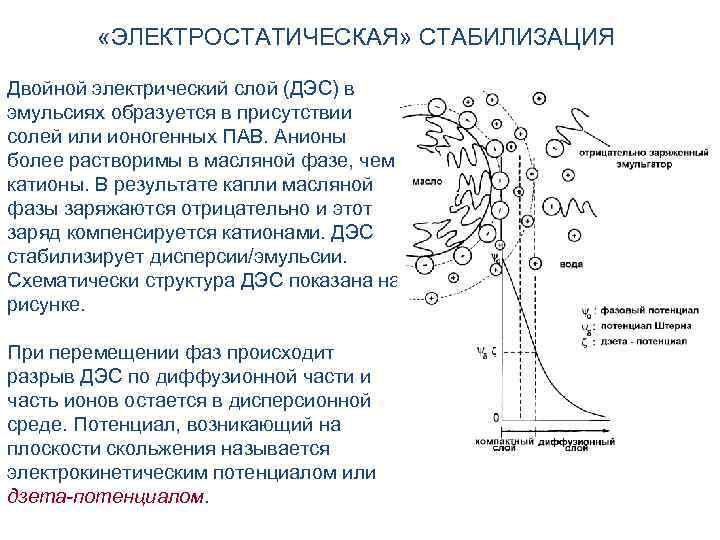
«ЭЛЕКТРОСТАТИЧЕСКАЯ» СТАБИЛИЗАЦИЯ Двойной электрический слой (ДЭС) в эмульсиях образуется в присутствии солей или ионогенных ПАВ. Анионы более растворимы в масляной фазе, чем катионы. В результате капли масляной фазы заряжаются отрицательно и этот заряд компенсируется катионами. ДЭС стабилизирует дисперсии/эмульсии. Схематически структура ДЭС показана на рисунке. При перемещении фаз происходит разрыв ДЭС по диффузионной части и часть ионов остается в дисперсионной среде. Потенциал, возникающий на плоскости скольжения называется электрокинетическим потенциалом или дзета-потенциалом.

В центре зазора h/2 увеличивается плотность зарядов ρ(h/2) и потенциал φ(h/2), который равен удвоенному потенциалу одиночного диффузного слоя φ(h/2) = 2 φ1(h/2). Произведение ρ(h/2)·φ(h/2) характеризует плотность электростатической энергии в центре зазора, т. е. работу концентрирования зарядов при сближении поверхностей. Плотность энергии в пленке (Дж/м 3) представляет электростатическую составляющую расклинивающего давления: Πel ~ ρ(h/2)·φ(h/2) [Дж/м 3≡ H/м 2]. собой

Так как φ(x) в диффузном слое меняется с расстоянием x по экспоненте φ(x) ~ exp(–x/δ), Πel также проявляет экспоненциальную зависимость от ширины зазора h: Πel ~ exp(–h/δ). Поскольку электростатическое отталкивание препятствует утонению пленки в зазоре, то Πel > 0. Энергия электростатического взаимодействия Uel соответствует энергии отталкивания (Uel > 0) и также экспоненциально зависит от ширины зазора h: Uel ~ exp(–h/δ). Повышение концентрации с0 приводит к снижению Πel и Uel. Таким образом, электростатическая составляющая Πel и Uel является фактором стабилизации дисперсных систем, т. к. создает препятствие для сближения частиц и их коагуляции.

Структурная составляющая расклинивающего давления связана с образованием на гидрофильных поверхностях структурированных слоев воды. Структура воды в таких тонких пристенных слоях отличается от структуры воды в объеме фазы. Структурированность пристенных слоев воды создает дополнительное сопротивление для сближения частиц и препятствует коагуляции. С ней в значительной степени связаны и иные свойства таких водных пленок – повышенная вязкость и пониженная температура замерзания, играющие большую роль в физических свойствах почв.

Наиболее сильным фактором стабилизации, согласно Ребиндеру, является структурно-механический барьер. Он создается при адсорбции молекул ПАВ, как правило высокомолекулярных, которые способны к образованию структурированного слоя на межфазной границе. К таким веществам относятся глюкозиды, белки, производные целлюлозы (карбоксиметилцеллюлоза) и другие так называемые защитные коллоиды – высокомолекулярные вещества со сложным строением молекул, которые имеют функциональные группы разной гидрофильности в пределах одной молекулы. По отношению к дисперсиям гидрофильных порошков в неполярных жидкостях высокой стабилизирующей способностью обладают многие маслорастворимые ПАВ, способные прочно (химически) адсорбироваться на поверхности гидрофильных частиц. Стабилизированные таким путем лиофобные системы приобретают свойства дисперсий данного стабилизатора, т. е. становятся лиофилизованными. По Ребиндеру, высокую эффективность структурно-механического барьера определяют следующие условия:

1. Наличие повышенной вязкости и механической прочности адсорбционных и межфазных слоев стабилизатора – их способность сопротивляться деформации и разрушению – в сочетании с достаточной подвижностью, обеспечивающей залечивание случайно возникающих дефектов слоя. Для систем с твердыми частицами условием эффективной стабилизации может быть также достаточно высокая прочность закрепления молекул стабилизатора на поверхности частиц, т. е. большая энергия взаимодействия этих молекул с твердой поверхностью (в этих условиях менее существенным становится требование к собственной прочности слоя, обусловливаемой взаимодействием его молекул между собой). 2. Лиофильность наружной части межфазного или адсорбционного слоя, т. е. его родственность дисперсионной среде, обеспечивающая «плавность» перехода от дисперсной фазы к дисперсионной среде.
Лекция_03.04.ppt