Л.2. Химич. состав.ppt
- Количество слайдов: 32

ОСОБЕННОСТИ ХИМИЧЕСКОГО СОСТАВА ЖИВЫХ ОРГАНИЗМОВ
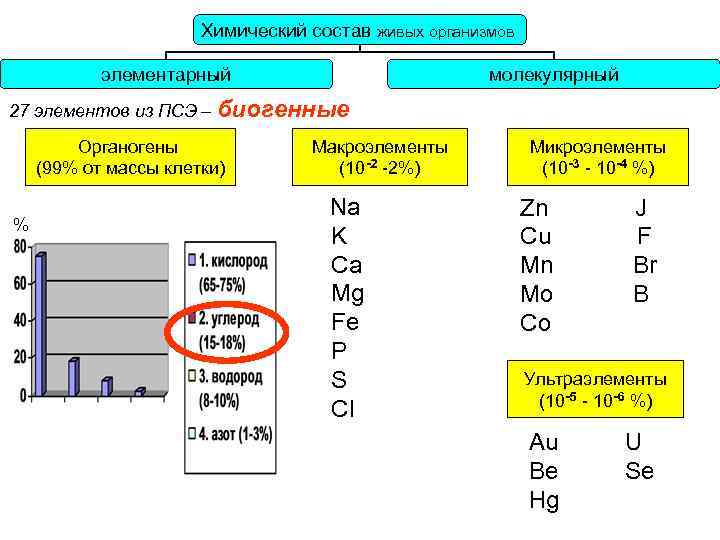
Химический состав живых организмов элементарный молекулярный 27 элементов из ПСЭ – биогенные Органогены (99% от массы клетки) % Макроэлементы (10 -2 -2%) Na K Ca Mg Fe P S Cl Микроэлементы (10 -3 - 10 -4 %) Zn Cu Mn Mo Co J F Br B Ультраэлементы (10 -5 - 10 -6 %) Au Be Hg U Se
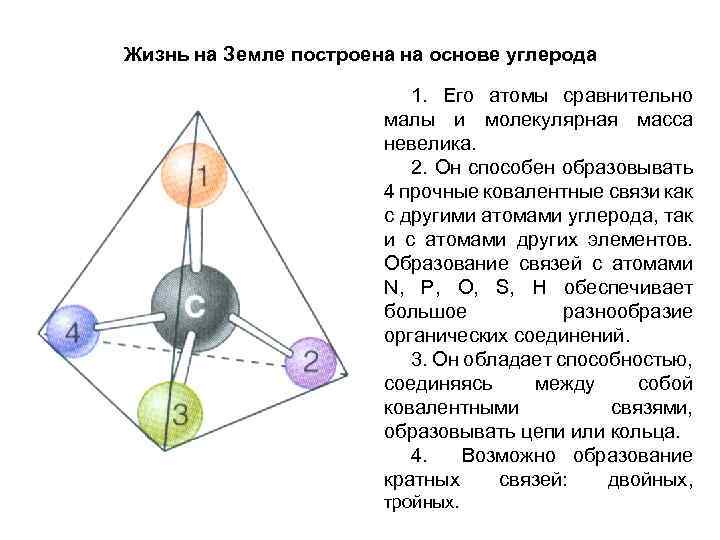
Жизнь на Земле построена на основе углерода 1. Его атомы сравнительно малы и молекулярная масса невелика. 2. Он способен образовывать 4 прочные ковалентные связи как с другими атомами углерода, так и с атомами других элементов. Образование связей с атомами N, P, O, S, H обеспечивает большое разнообразие органических соединений. 3. Он обладает способностью, соединяясь между собой ковалентными связями, образовывать цепи или кольца. 4. Возможно образование кратных связей: двойных, тройных.
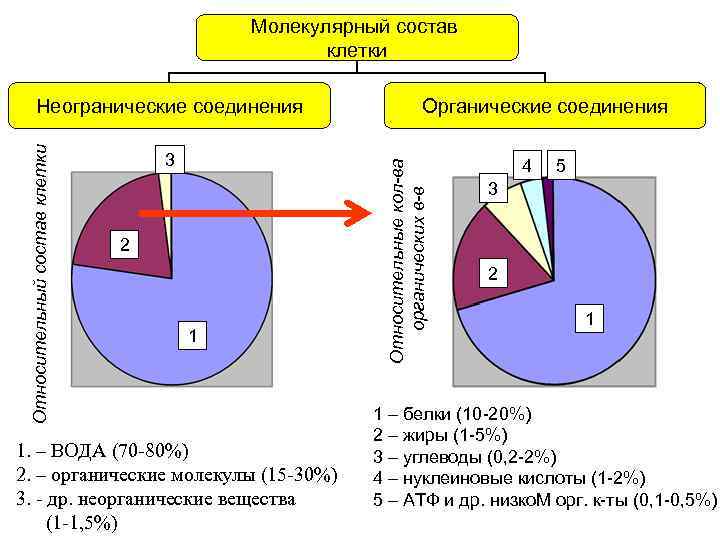
Молекулярный состав клетки 3 2 1 1. – ВОДА (70 -80%) 2. – органические молекулы (15 -30%) 3. - др. неорганические вещества (1 -1, 5%) Органические соединения Относительные кол-ва органических в-в Относительный состав клетки Неогранические соединения 4 5 3 2 1 1 – белки (10 -20%) 2 – жиры (1 -5%) 3 – углеводы (0, 2 -2%) 4 – нуклеиновые кислоты (1 -2%) 5 – АТФ и др. низко. М орг. к-ты (0, 1 -0, 5%)

Процент воды в тканях ВОДА – главный компонент клеток. Мозг………………. . 70 - 85 У человека – 60% массы тела (40% - внутричклеточная) Мышцы……………. . 75 Физико-химические свойства • малый размер молекулы • полярность • способность образовывать водородные связи • высокая теплоемкость и теплопроводность • высокое поверхностное натяжение Функции воды Кожа………………. . 70 Соединительная…. 60 Кости………………. . . 25 Жировая……………. 20 1. Универсальный растворитель 2. Среда биологических (оплодотворение, транспирация, прорастание семян) и биохимических реакций 3. Среда для транспорта веществ 4. Участие в водно-солевом и др. обменах в-в. 5. Определяет физические свойства клеток (объем, упругость, осмотическое довление, тургор, структуру коллоидов) и несет опорную функцию (гидростатический скелет) 6. Распределяет тепло по организму 7. В процессе фотосинтеза – исходное, в процессе дыхания – конечное вещество 8. Среда обитания организмов, распространения семян.
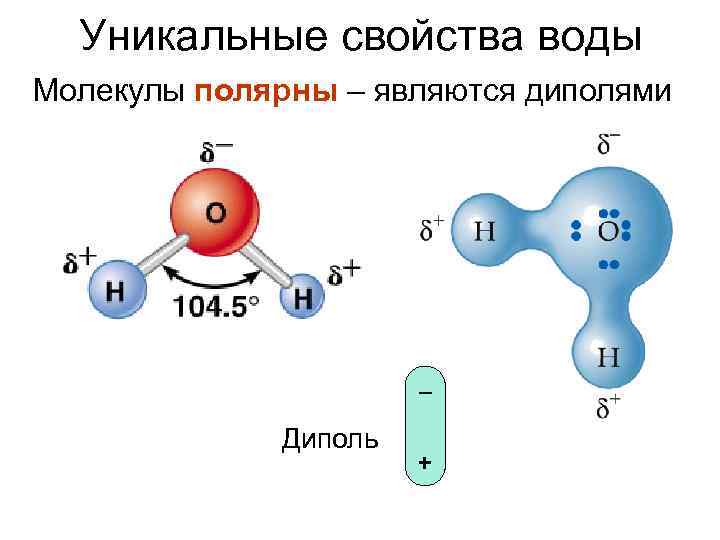
Уникальные свойства воды Молекулы полярны – являются диполями – Диполь +
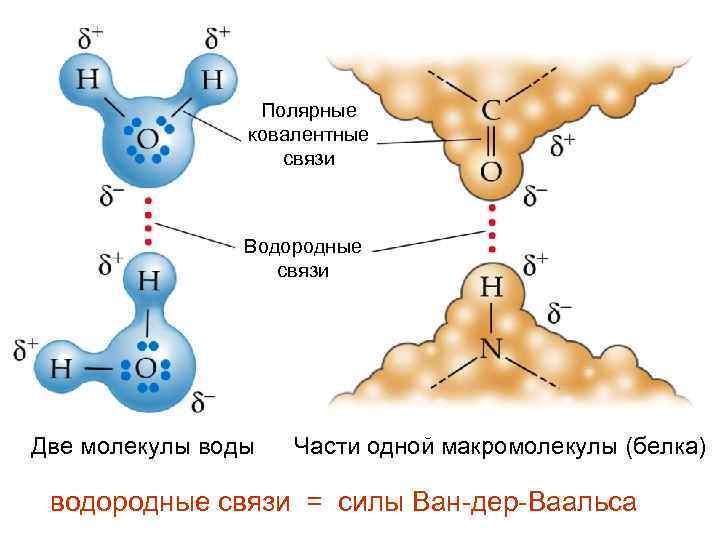
Полярные ковалентные связи Водородные связи Две молекулы воды Части одной макромолекулы (белка) водородные связи = силы Ван-дер-Ваальса
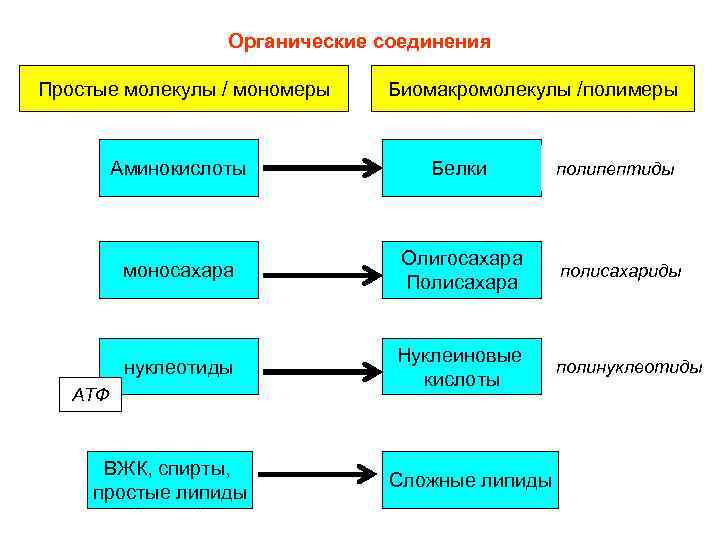
Органические соединения Простые молекулы / мономеры Биомакромолекулы /полимеры Аминокислоты Белки моносахара Олигосахара Полисахара полисахариды нуклеотиды Нуклеиновые кислоты полинуклеотиды АТФ ВЖК, спирты, простые липиды Сложные липиды полипептиды
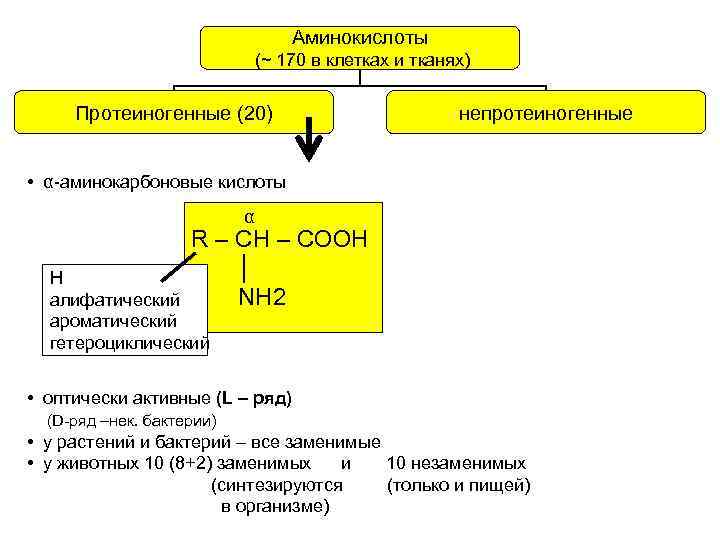
Аминокислоты (~ 170 в клетках и тканях) Протеиногенные (20) непротеиногенные • α-аминокарбоновые кислоты α R – CH – COOH │ NH 2 Н алифатический ароматический гетероциклический • оптически активные (L – ряд) (D-ряд –нек. бактерии) • у растений и бактерий – все заменимые • у животных 10 (8+2) заменимых и 10 незаменимых (синтезируются (только и пищей) в организме)

БЕЛКИ = ПРОТЕИНЫ (от греч. protos – первый, главный)
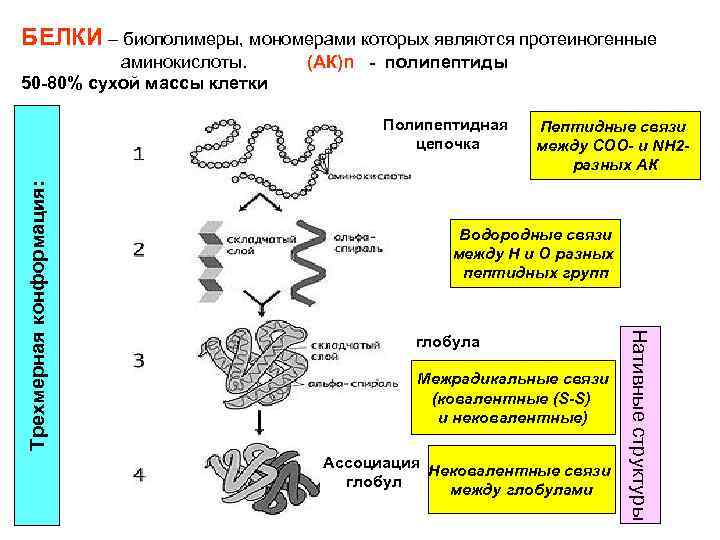
БЕЛКИ – биополимеры, мономерами которых являются протеиногенные аминокислоты. 50 -80% сухой массы клетки (АК)n - полипептиды Пептидные связи между СОО- и NH 2 разных АК Водородные связи между Н и О разных пептидных групп глобула Межрадикальные связи (ковалентные (S-S) и нековалентные) Ассоциация Нековалентные связи глобул между глобулами Нативные структуры Трехмерная конформация: Полипептидная цепочка
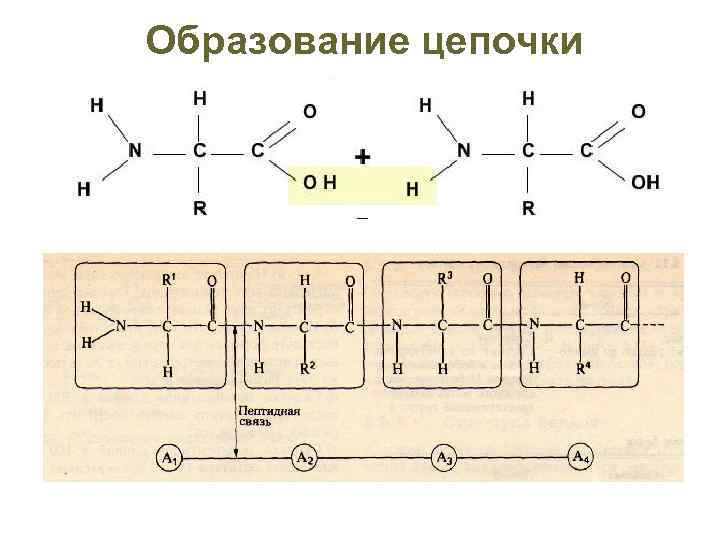
Образование цепочки Энергия N-конец Пептидная связь С-конец

I Первичная структура белка – это последовательность аминокислот в полипептидной цепочке, записанная в порядке N……. . C. (соответствует направлению роста цепочки при ее синтезе в клетке). N Мет 1 Глу Гис Ала Трп 2 3 4 5 6 Цис 7 Вал 8 Иле 9 C
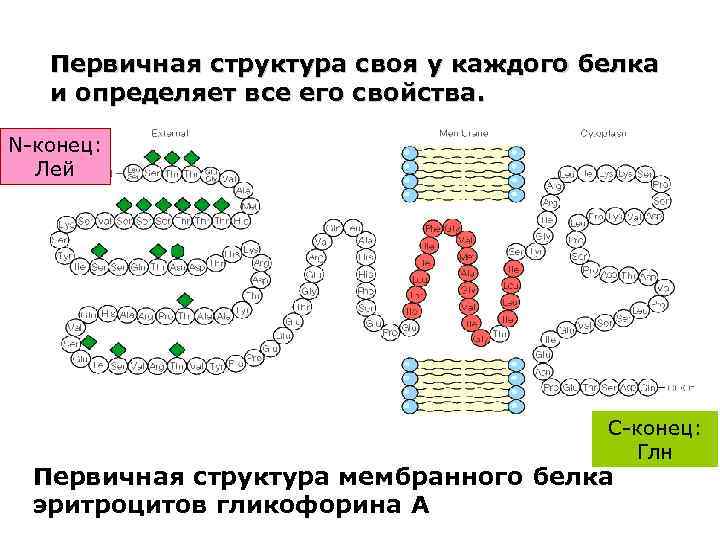
Первичная структура своя у каждого белка и определяет все его свойства. N-конец: Лей C-конец: Глн Первичная структура мембранного белка эритроцитов гликофорина А
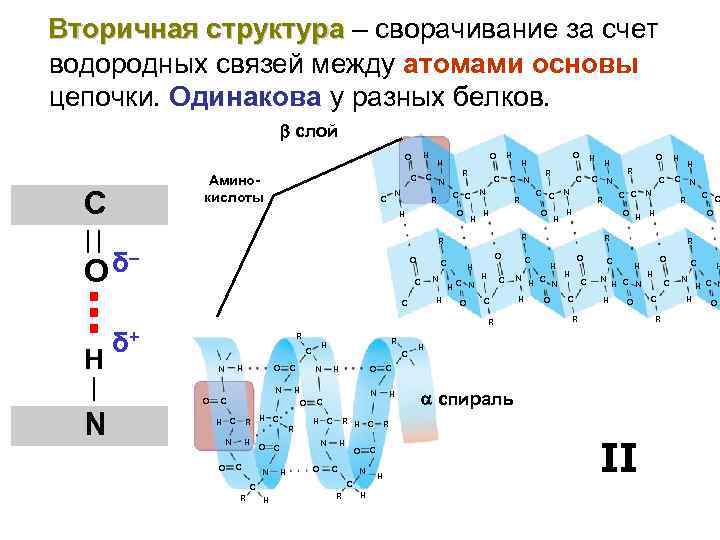
Вторичная структура – сворачивание за счет водородных связей между атомами основы цепочки. Одинакова у разных белков. слой H O Аминокислоты С N C R C C H O H C N C C R O H H C N О O C H R O H N N O N C R H N O C H O C N C O C R H N C O H C N O H C C N H R H N H C N C C R H H N H H C N O H C N C R O H H O H C C R C N H C O R C H C R H H C N O R O H C C R H спираль R C C C R C O H N O H C O H H C H R H C C H R δ+ R H R C N N R R δ– O H II C N H H H C N O

Лайнус Полинг Открыл α-спираль в 1951
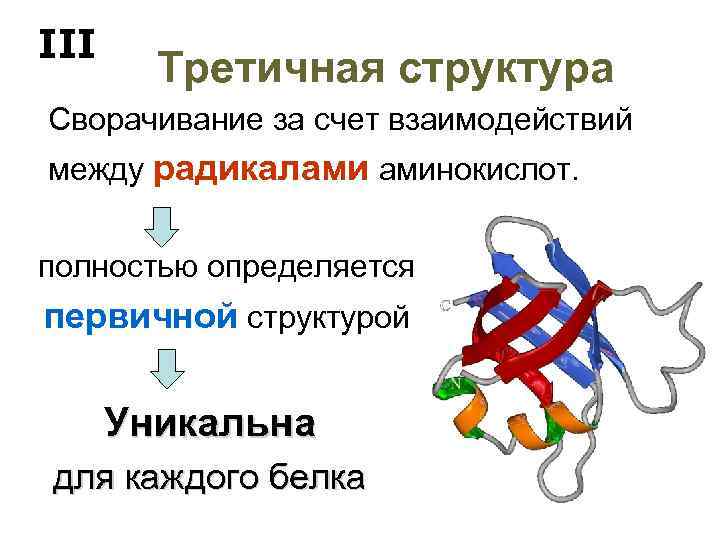
III Третичная структура Сворачивание за счет взаимодействий между радикалами аминокислот. полностью определяется первичной структурой Уникальна для каждого белка

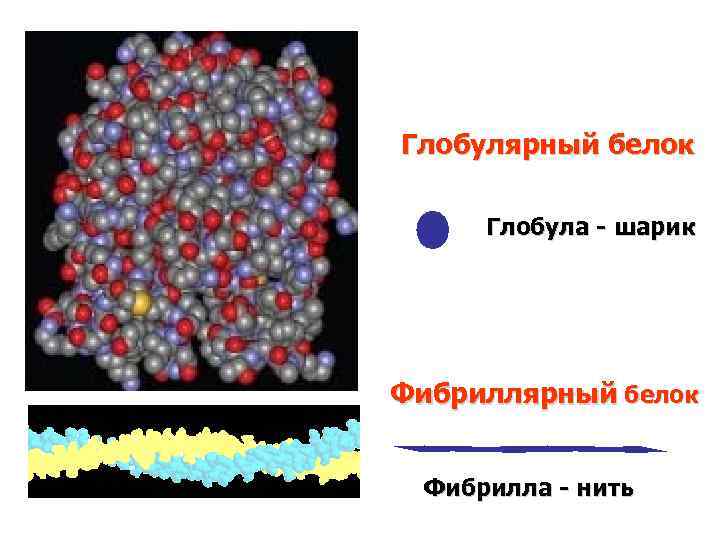
Глобулярный белок Глобула - шарик Фибриллярный белок Фибрилла - нить

IV Четвертичная структура • Объединение двух и более (до 20) полипептидных цепочек в один белок. Одна цепочка = субъединица Ø Связи – не ковалентные, между субъединицами. Четвертичную структуру имеют не все белки (меньше половины) Ø +
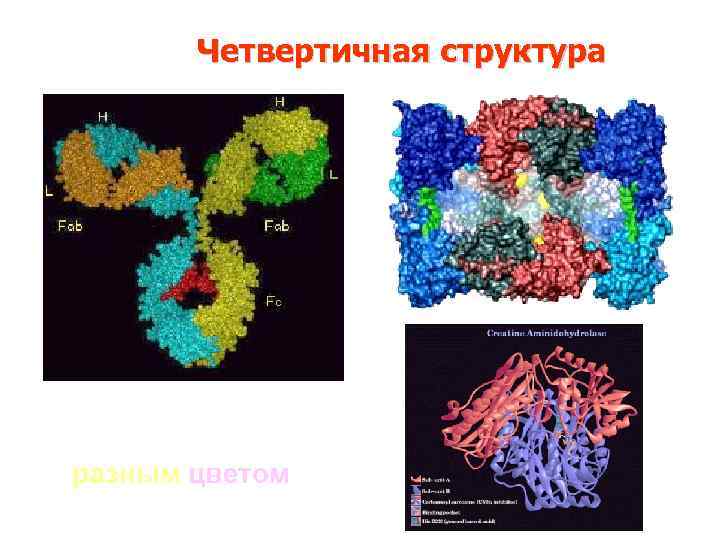
Четвертичная структура Разные цепочки – разным цветом
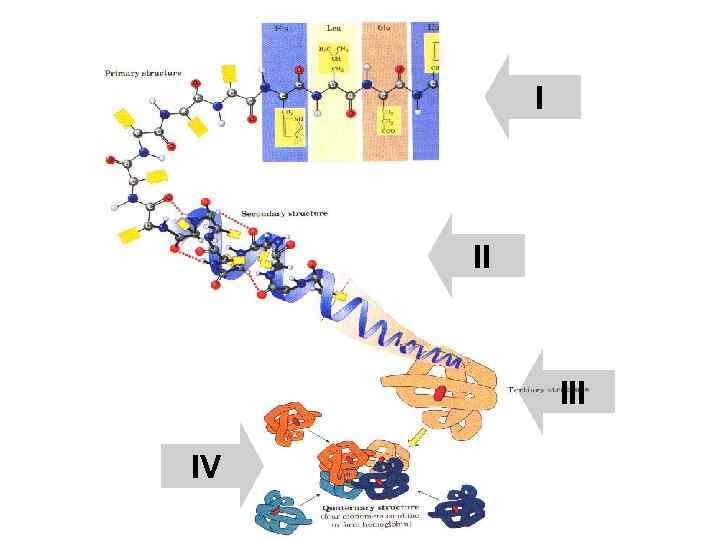
I II IV

Денатурация – разрушение нативной структуры (первичная сохраняется) - обратимая (с ренатурацией) - необратимая Денатурирующие агенты: t, р. Н, УФ, давление, механическое воздействие, органические растворители, дезинфицирующие вещества… При денатурации: • потеря биологической активности • изменение физико-химических свойств (понижение растворимости, изм. оптической акт. )
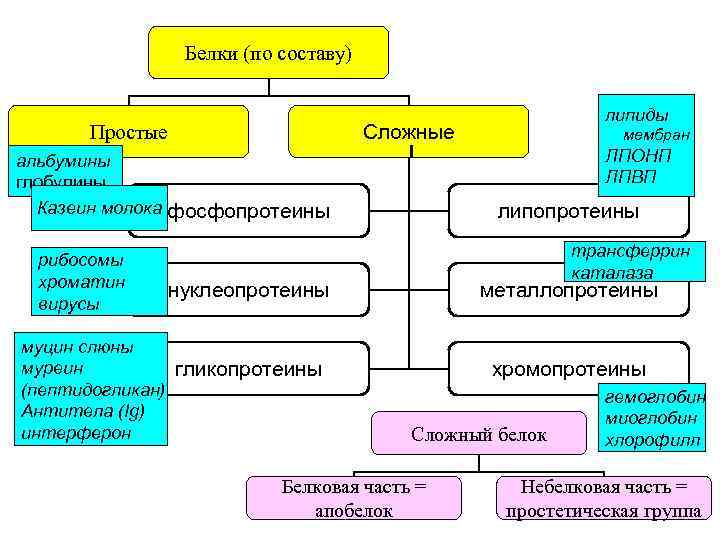
Белки (по составу) Сложные Простые липопротеины трансферрин каталаза нуклеопротеины муцин слюны муреин гликопротеины (пептидогликан) Антитела (Ig) интерферон мембран ЛПОНП ЛПВП альбумины глобулины Казеин молока фосфопротеины рибосомы хроматин вирусы липиды металлопротеины хромопротеины Сложный белок Белковая часть = апобелок гемоглобин миоглобин хлорофилл Небелковая часть = простетическая группа
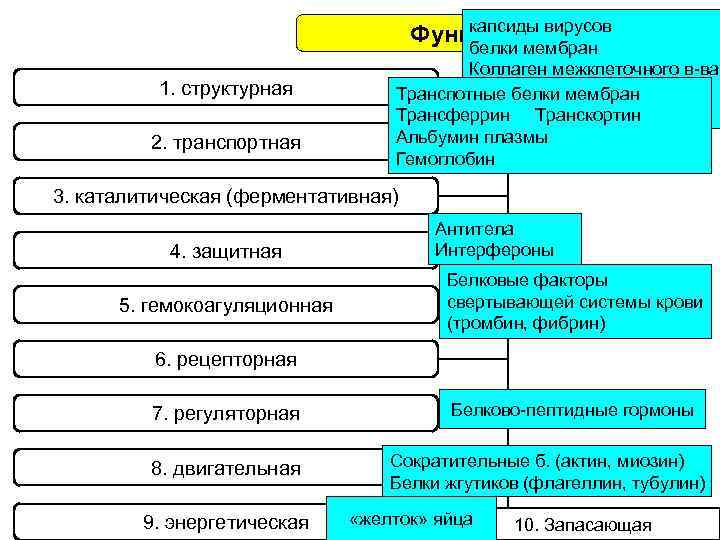
капсиды вирусов Функции белков белки мембран 1. структурная 2. транспортная Коллаген межклеточного в-ва белки цитоскелета Транспотные белки мембран белки Транскортин Трансферрин ламины ядра Альбумин плазмы Гемоглобин 3. каталитическая (ферментативная) 4. защитная 5. гемокоагуляционная Антитела Интерфероны Белковые факторы свертывающей системы крови (тромбин, фибрин) 6. рецепторная 7. регуляторная 8. двигательная 9. энергетическая Белково-пептидные гормоны Сократительные б. (актин, миозин) Белки жгутиков (флагеллин, тубулин) «желток» яйца 10. Запасающая
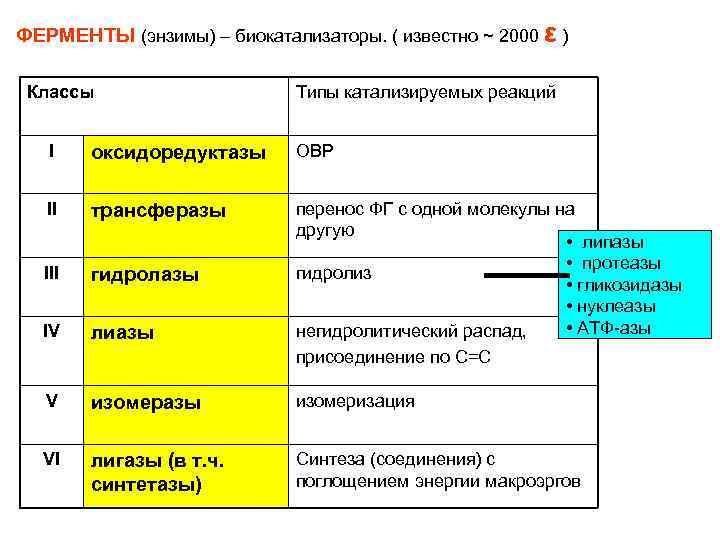
ФЕРМЕНТЫ (энзимы) – биокатализаторы. ( известно ~ 2000 ε ) Классы Типы катализируемых реакций I оксидоредуктазы ОВР II трансферазы III гидролазы IV лиазы перенос ФГ с одной молекулы на другую • липазы • протеазы гидролиз • гликозидазы • нуклеазы • АТФ-азы негидролитический распад, присоединение по С=С V изомеразы изомеризация VI лигазы (в т. ч. синтетазы) Синтеза (соединения) с поглощением энергии макроэргов
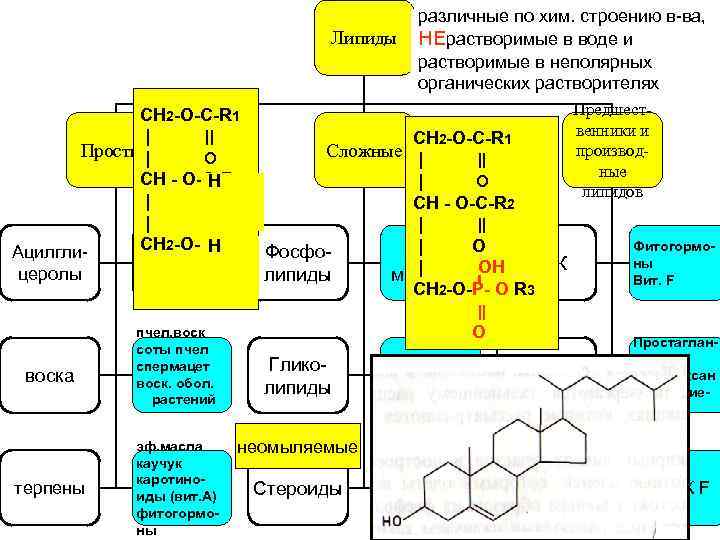
Липиды СН 2 -О-С-R 1 | || Простые | O СН - О-С-R 2 H | || | O МАГ, ДАГ, СН 2 -О-С-R 3 H Ацилгли. ТАГ= церолы || нейтральные жиры O различные по хим. строению в-ва, НЕрастворимые в воде и растворимые в неполярных органических растворителях СН 2 -О-С-R 1 Сложные | || | O СН - О-С-R 2 | || | O Фосфо. ФЛ ВЖК | липиды мембран OH СН 2 -О-P- O R 3 Предшественники и производные липидов Фитогормоны Вит. F || воска терпены пчел. воск соты пчел спермацет воск. обол. растений эф. масла каучук каротиноиды (вит. А) фитогормоны O Гликолипиды ГЛ мембран Эйкозаноиды Простагландины тромбоксан лейкотриены неомыляемые холестерин желчные кислоты стероидные гормоны Вит. Д Жирораст воримые вит. АДЕКF Стероиды
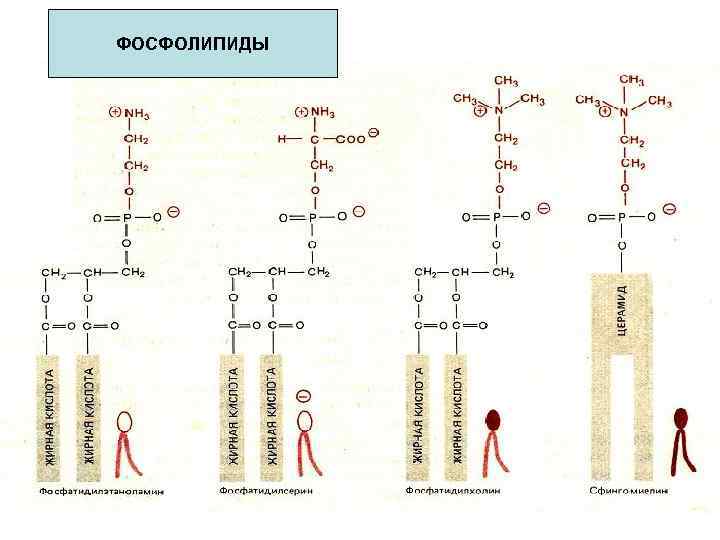
ФОСФОЛИПИДЫ
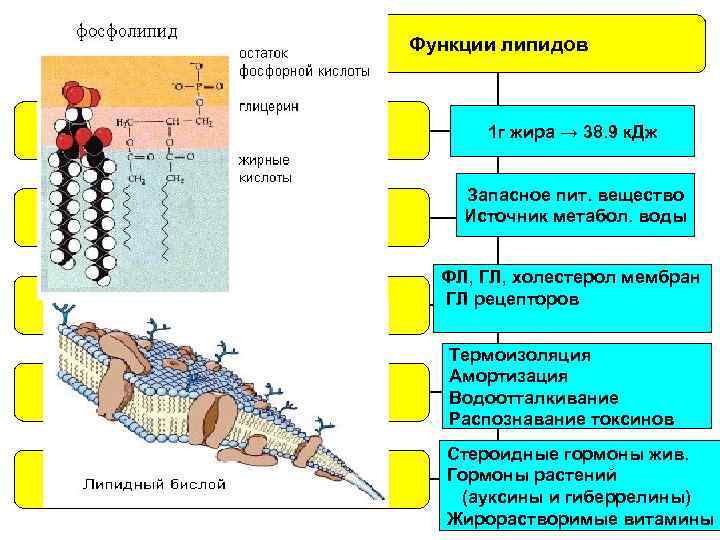
Функции липидов 1. энергетическая 1 г жира → 38. 9 к. Дж 2. резервная Запасное пит. вещество Источник метабол. воды 3. структурная ФЛ, ГЛ, холестерол мембран ГЛ рецепторов 4. защитная 5. регуляторная Термоизоляция Амортизация Водоотталкивание Распознавание токсинов Стероидные гормоны жив. Гормоны растений (ауксины и гиберрелины) Жирорастворимые витамины
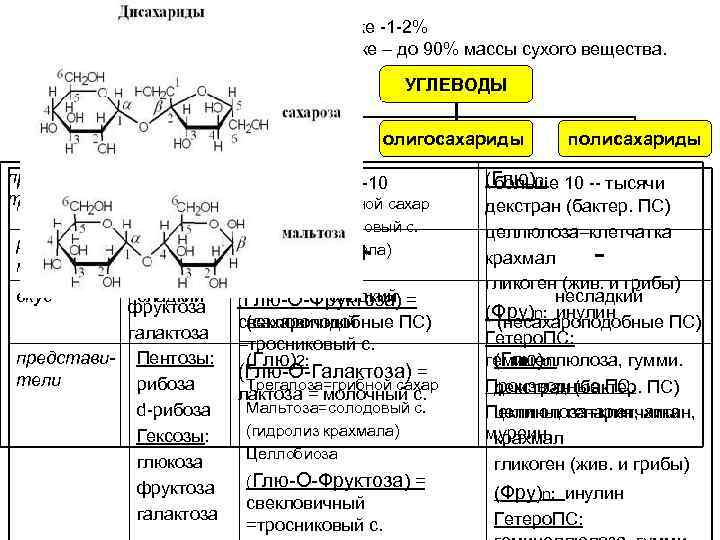
УГЛЕВОДЫ (сахариды) в жив. клетке -1 -2% в раст. клетке – до 90% массы сухого вещества. УГЛЕВОДЫ моносохариды представи- Пентозы: количество 1 тели мономеров рибоза O)m Сn(H 2 d-рибоза раствори. Гексозы: мость глюкоза вкус сладкий фруктоза галактоза представи- Пентозы: тели рибоза d-рибоза Гексозы: глюкоза фруктоза галактоза + (Глю)2: олигосахариды 2 -10 Трегалоза=грибной сахар Мальтоза=солодовый с. (гидролиз крахмала) Целлобиоза + сладкий (Глю-О-Фруктоза) = (сахароподобные ПС) свекловичный =тросниковый с. (Глю)2: (Глю-О-Галактоза) = Трегалоза=грибной сахар лактоза = молочный с. Мальтоза=солодовый с. (гидролиз крахмала) Целлобиоза (Глю-О-Фруктоза) = свекловичный =тросниковый с. полисахариды (Глю)n: 10 -- тысячи больше декстран (бактер. ПС) целлюлоза=клетчатка крахмал гликоген (жив. и грибы) несладкий (Фру)n: инулин (несахароподобные ПС) Гетеро. ПС: гемицеллюлоза, гумми. (Глю)n: Производные ПС: ПС) декстран (бактер. Пектины, гепарин, хитин, целлюлоза=клетчатка муреин крахмал гликоген (жив. и грибы) - (Фру)n: инулин Гетеро. ПС:
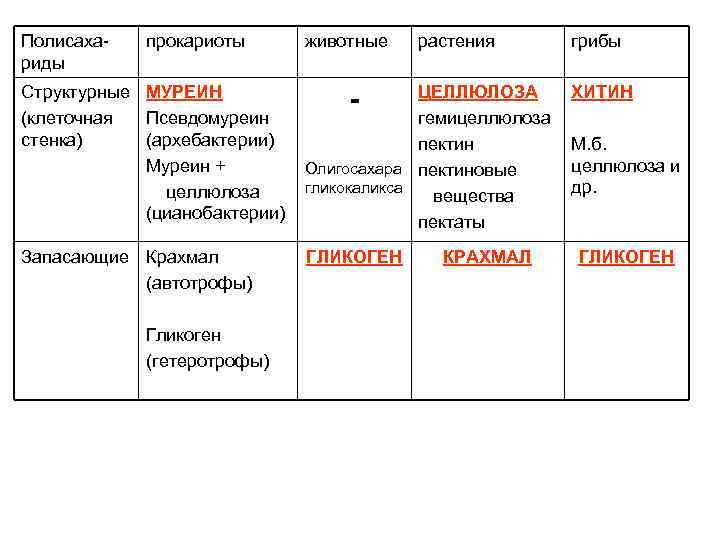
Полисахариды прокариоты животные растения Структурные МУРЕИН (клеточная Псевдомуреин стенка) (архебактерии) Муреин + целлюлоза (цианобактерии) ЦЕЛЛЮЛОЗА гемицеллюлоза пектин Олигосахара пектиновые гликокаликса вещества пектаты Запасающие Крахмал (автотрофы) ГЛИКОГЕН Гликоген (гетеротрофы) - КРАХМАЛ грибы ХИТИН М. б. целлюлоза и др. ГЛИКОГЕН
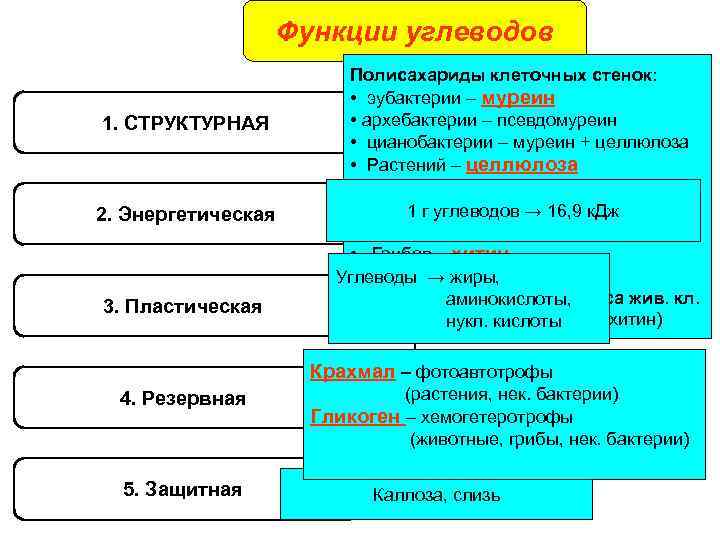
Функции углеводов 1. СТРУКТУРНАЯ 2. Энергетическая 3. Пластическая Полисахариды клеточных стенок: • эубактерии – муреин • архебактерии – псевдомуреин • цианобактерии – муреин + целлюлоза • Растений – целлюлоза гемицеллюлоза пектины, пектиновые 1 г углеводов → 16, 9 к. Дж в-ва, пектаты • Грибов – хитин Углеводы м. б. жиры, → целлюлоза и др. Олигосахариды гликокаликса жив. кл. аминокислоты, Нар. скелет членистоногих (хитин) нукл. кислоты Крахмал – фотоавтотрофы 4. Резервная 5. Защитная (растения, нек. бактерии) Гликоген – хемогетеротрофы (животные, грибы, нек. бактерии) Каллоза, слизь
Л.2. Химич. состав.ppt