4_алкены.ppt
- Количество слайдов: 56

ОСОБЕННОСТИ СТРОЕНИЯ, РЕАКЦИОННОЙ СПОСОБНОСТИ И МЕТОДЫ СИНТЕЗА АЛКЕНОВ 1

Алкены Алкенами называются ненасыщенные углеводороды, молекулы которых содержат одну двойную связь. Сn. Н 2 n олефины 2
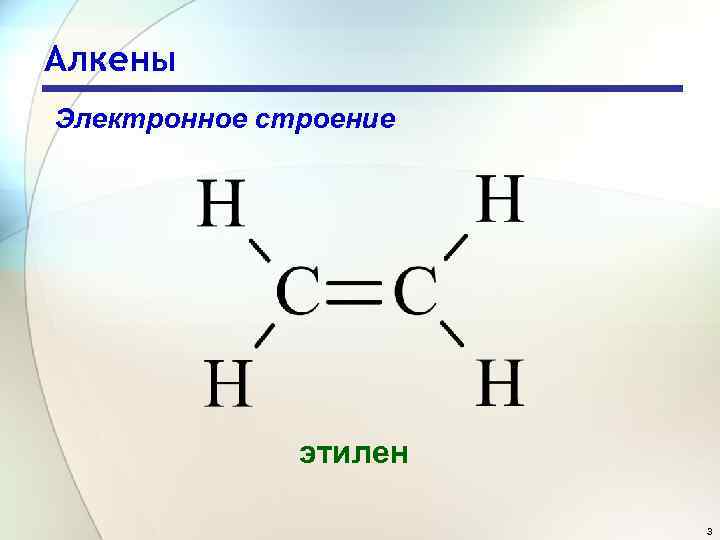
Алкены Электронное строение этилен 3
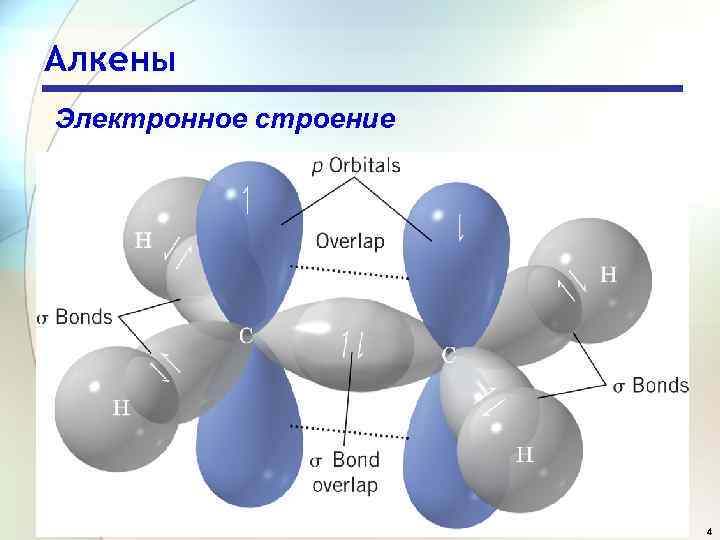
Алкены Электронное строение 4

Алкены Номенклатура 1) в алкенах с неразветвленной цепью нумерацию производят с того конца, ближе к которому находится двойная связь. В названии алкана, соответствующего этой родоначальной структуре, суффикс -ан заменяется на –ен. пропилен этилен гексен-2 5
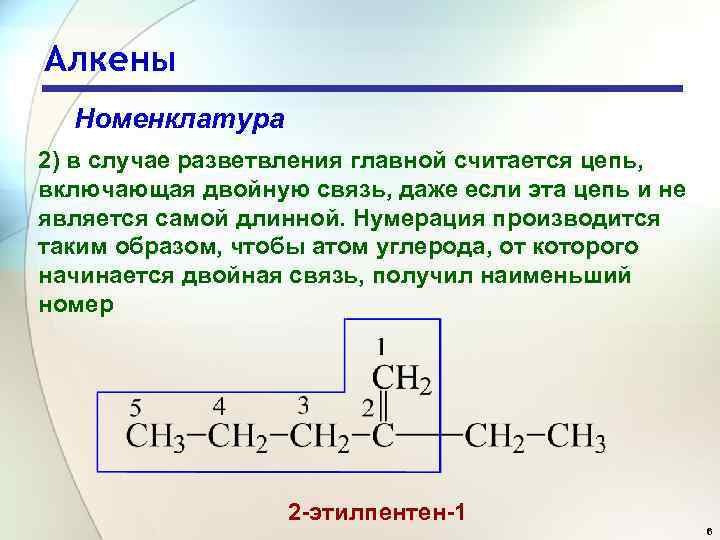
Алкены Номенклатура 2) в случае разветвления главной считается цепь, включающая двойную связь, даже если эта цепь и не является самой длинной. Нумерация производится таким образом, чтобы атом углерода, от которого начинается двойная связь, получил наименьший номер 2 -этилпентен-1 6

Алкены Номенклатура 3) Углеводородные заместители обозначаются префиксом. Положение их указывается цифрой, соответствующей номеру того атома углерода, у которого находится заместитель. Заместители перечисляются в алфавитном порядке. В случае нескольких одинаковых углеводородных заместителей перед их названием ставится умножительная приставка ди-, три- и т. д. 7
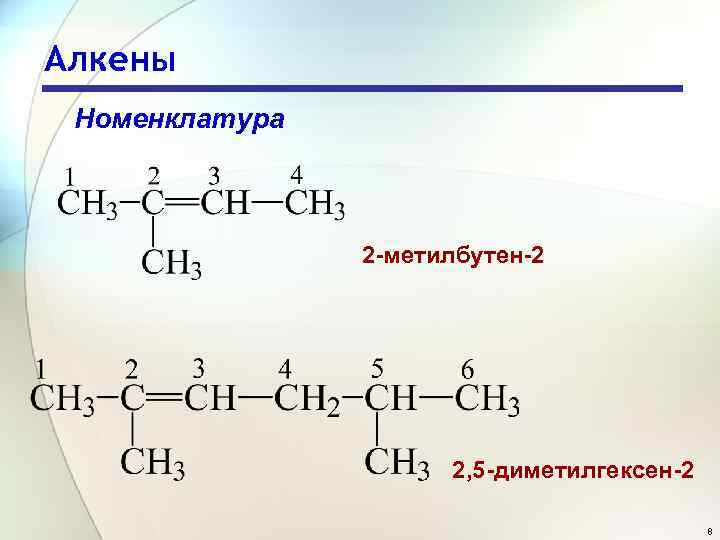
Алкены Номенклатура 2 -метилбутен-2 2, 5 -диметилгексен-2 8
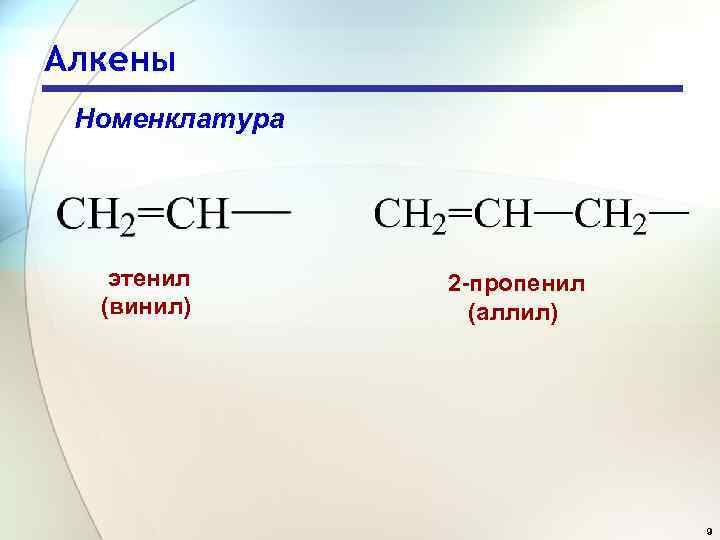
Алкены Номенклатура этенил (винил) 2 -пропенил (аллил) 9
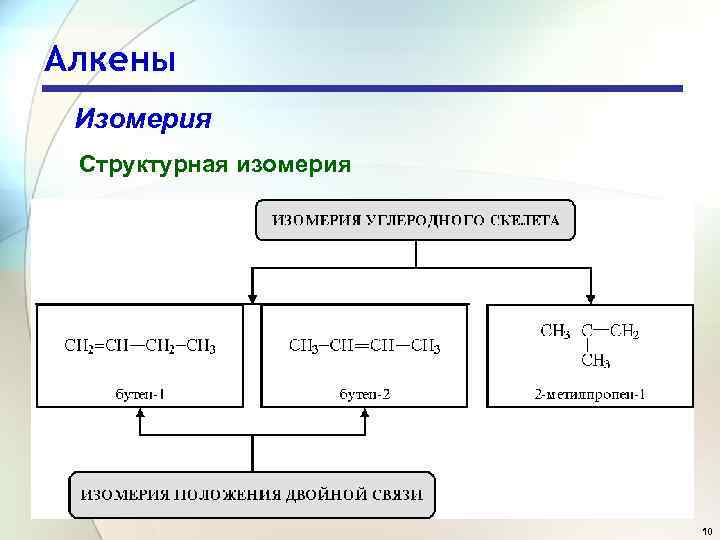
Алкены Изомерия Структурная изомерия 10

Алкены Изомерия Пространственная изомерия Цис- и транс-изомеры бутена-2 11
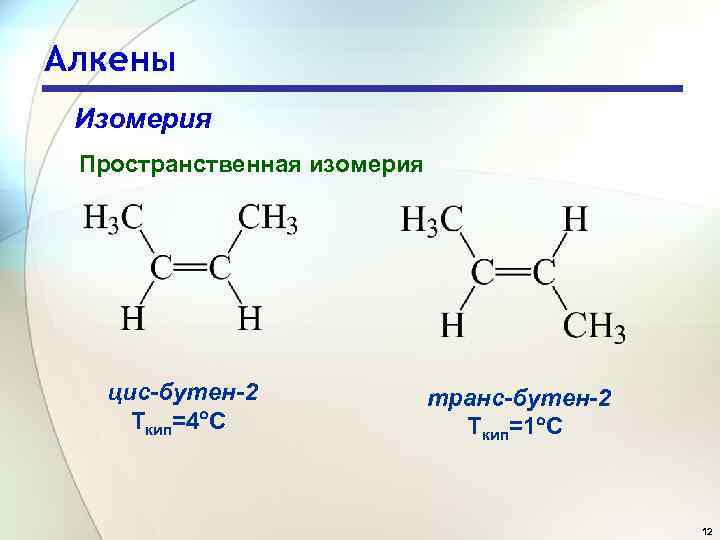
Алкены Изомерия Пространственная изомерия цис-бутен-2 Ткип=4 С транс-бутен-2 Ткип=1 С 12
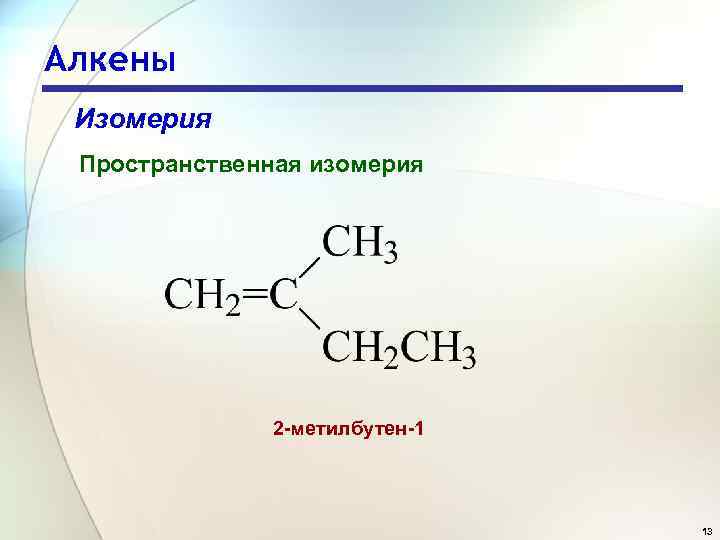
Алкены Изомерия Пространственная изомерия 2 -метилбутен-1 13
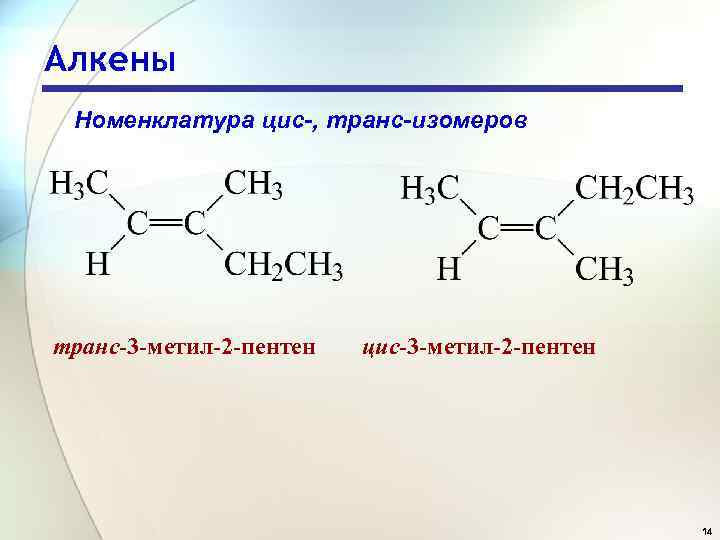
Алкены Номенклатура цис-, транс-изомеров транс-3 -метил-2 -пентен цис-3 -метил-2 -пентен 14
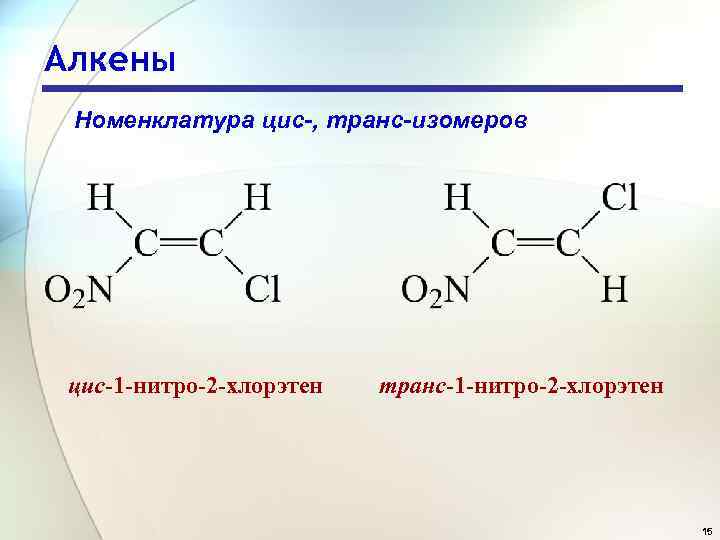
Алкены Номенклатура цис-, транс-изомеров цис-1 -нитро-2 -хлорэтен транс-1 -нитро-2 -хлорэтен 15
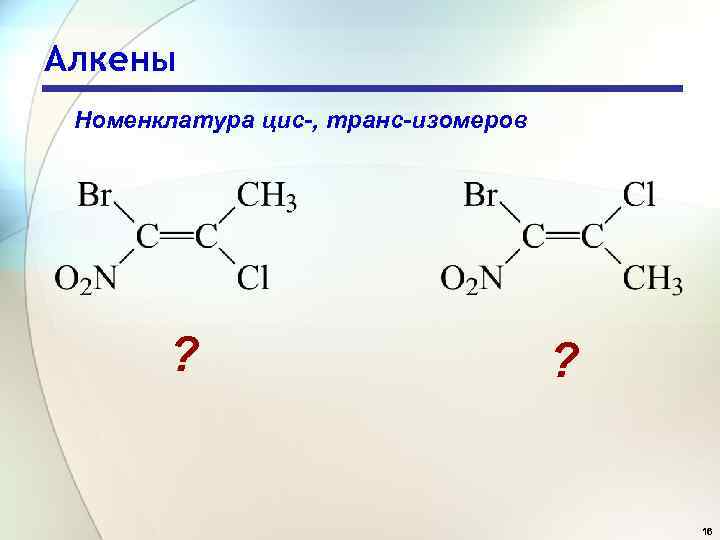
Алкены Номенклатура цис-, транс-изомеров ? ? 16

Алкены Номенклатура цис-, транс-изомеров Система Кана–Ингольда–Прелога ? Роберт Сидни Кан (9. 06. 1899 -15. 09. 1981) (Великобритания) Ингольд Кристофер Прелог Владимир (28. 10. 1893– 8. 10. 1970) (23. 07. 1906– 07. 01. 1998) (Великобритания) (Швейцария) 17

Алкены Номенклатура цис-, транс-изомеров 1. Используя систему Кана–Ингольда–Прелога, определяют сначала относительное старшинство заместителей, связанных с двойной связью, и дают им номера по старшинству 1 или 2. 2. Если две наиболее старшие группы расположены по одну сторону от плоскости -связи, то конфигурация заместителей обозначается символом Z, если же эти группы находятся по разные стороны от плоскости -связи, то конфигурация обозначается символом Е. 18
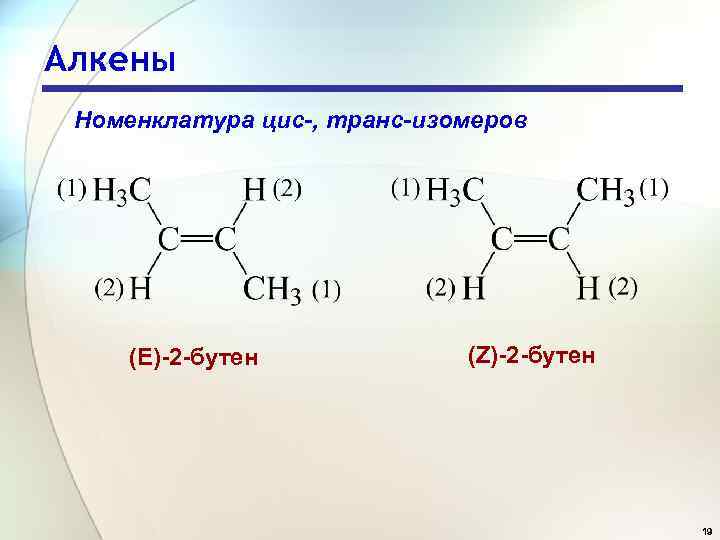
Алкены Номенклатура цис-, транс-изомеров (Е)-2 -бутен (Z)-2 -бутен 19
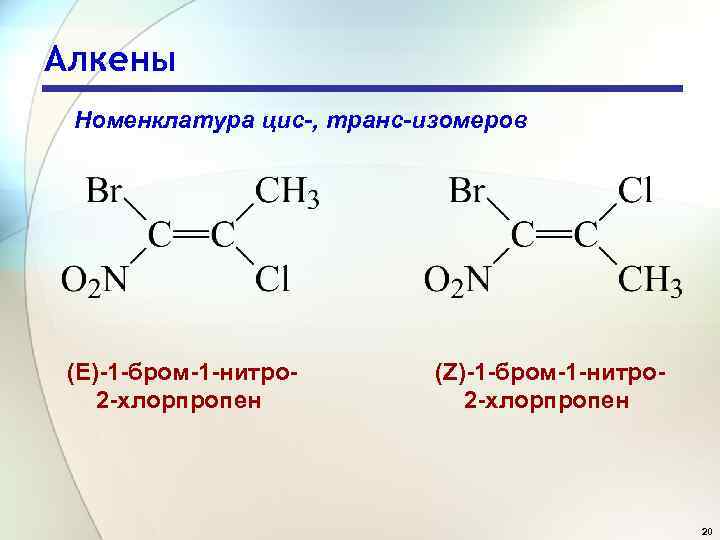
Алкены Номенклатура цис-, транс-изомеров (Е)-1 -бром-1 -нитро 2 -хлорпропен (Z)-1 -бром-1 -нитро 2 -хлорпропен 20

Алкены Физические свойства 21
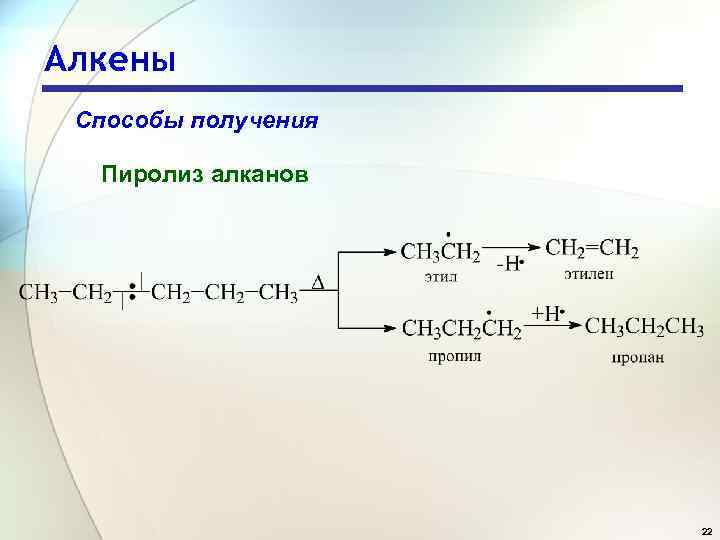
Алкены Способы получения Пиролиз алканов 22
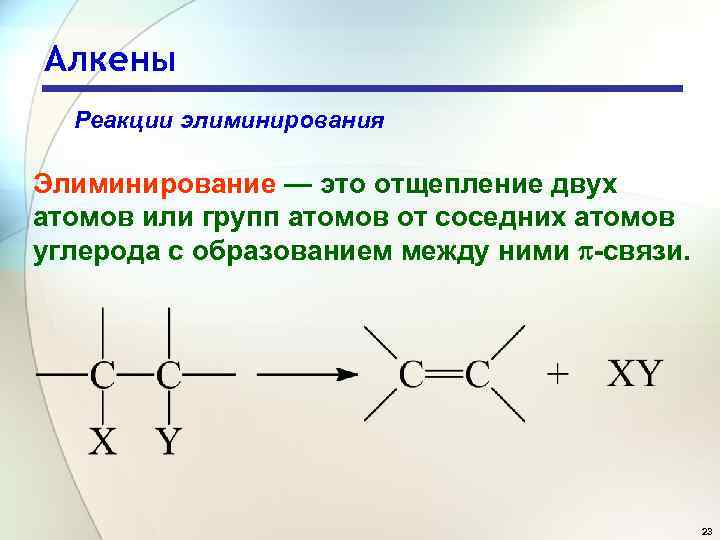
Алкены Реакции элиминирования Элиминирование — это отщепление двух атомов или групп атомов от соседних атомов углерода с образованием между ними -связи. 23
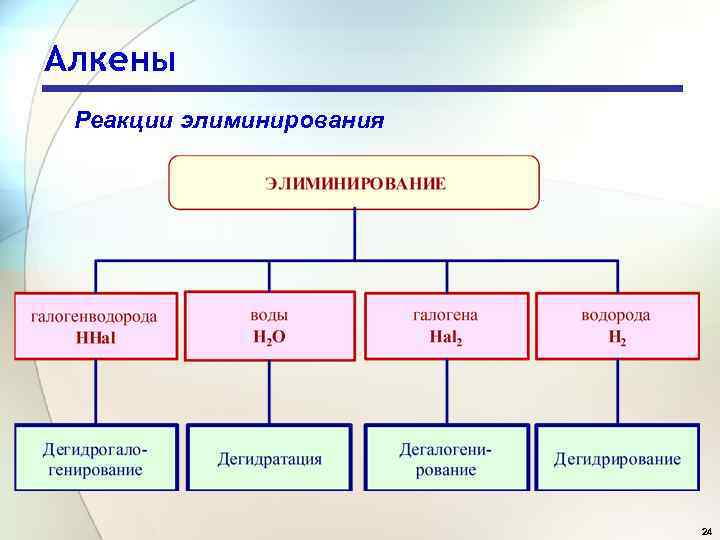
Алкены Реакции элиминирования 24

Алкены Реакции элиминирования Дегидрогалогенирование 25

Алкены Реакции элиминирования Дегидрогалогенирование Правило Зайцева В случае нессиметричных алкилгалогенидов отщепление атома водорода происходит от наименее гидрогенизированного атома углерода. 26

Алкены Реакции элиминирования Дегидрогалогенирование ЗАЙЦЕВ Александр Михайлович (Россия) (2. VII. 1841 - 1. IX. 1910) 27
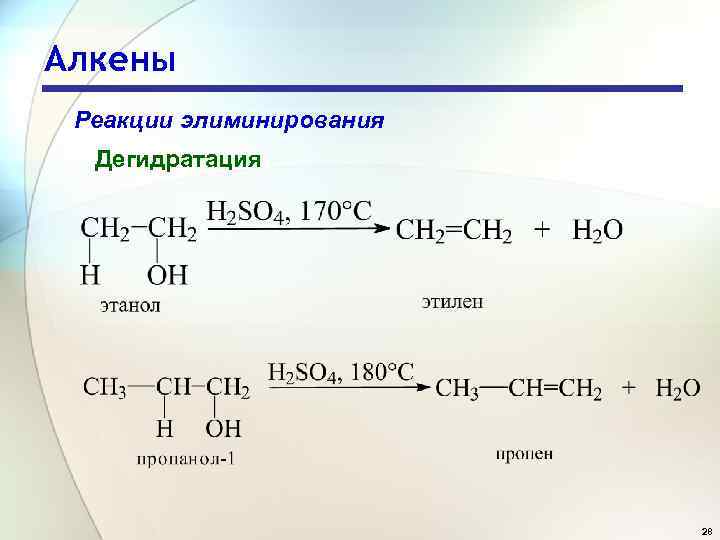
Алкены Реакции элиминирования Дегидратация 28

Алкены Реакции элиминирования Дегалогенирование 29

Алкены Реакции элиминирования Дегидрирование 30
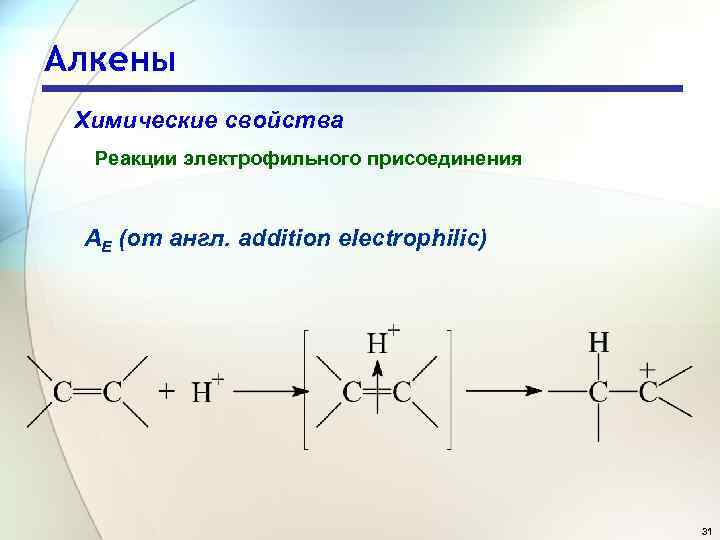
Алкены Химические свойства Реакции электрофильного присоединения АE (от англ. addition electrophilic) 31
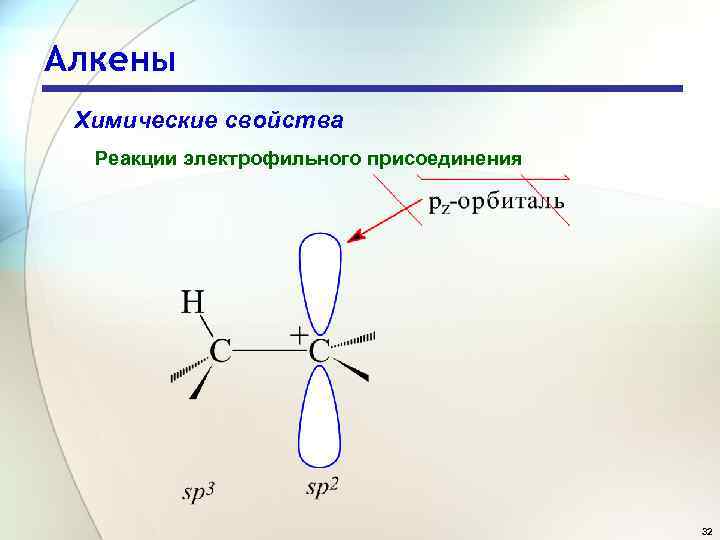
Алкены Химические свойства Реакции электрофильного присоединения 32
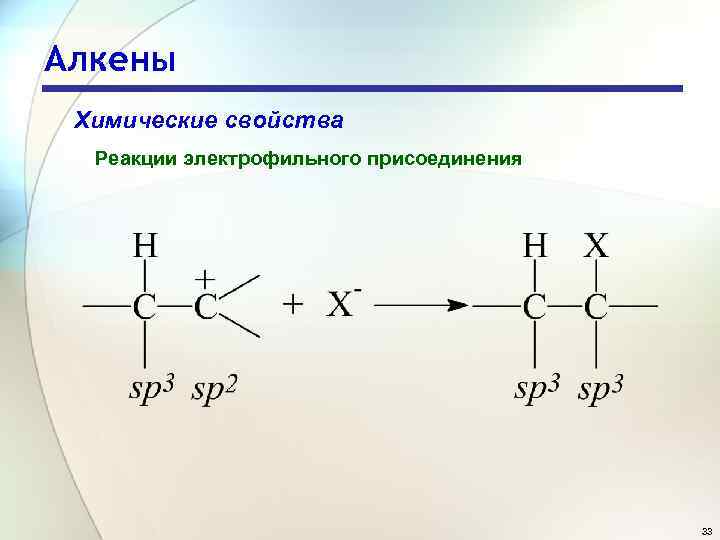
Алкены Химические свойства Реакции электрофильного присоединения 33

Алкены Химические свойства Реакции электрофильного присоединения +I–эффект –I–эффект 34

Алкены Химические свойства Реакции электрофильного присоединения Гидрогалогенирование 35
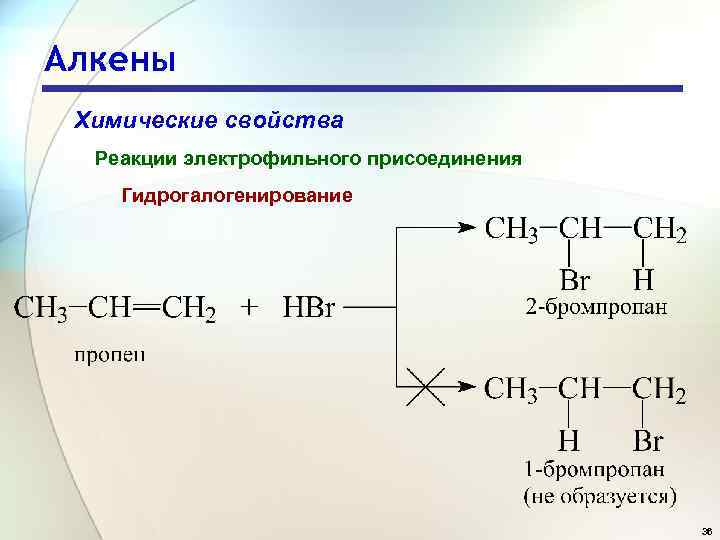
Алкены Химические свойства Реакции электрофильного присоединения Гидрогалогенирование 36

Алкены Химические свойства Реакции электрофильного присоединения Гидрогалогенирование Правило Марковникова: присоединении молекул типа НХ к несимметричным алкенам атом водорода присоединяется к более гидрогенизированному атому углерода двойной связи. 37

Алкены МАРКОВНИКОВ Владимир Васильевич 13. 12. 1837 – 29. 01. 1904 38
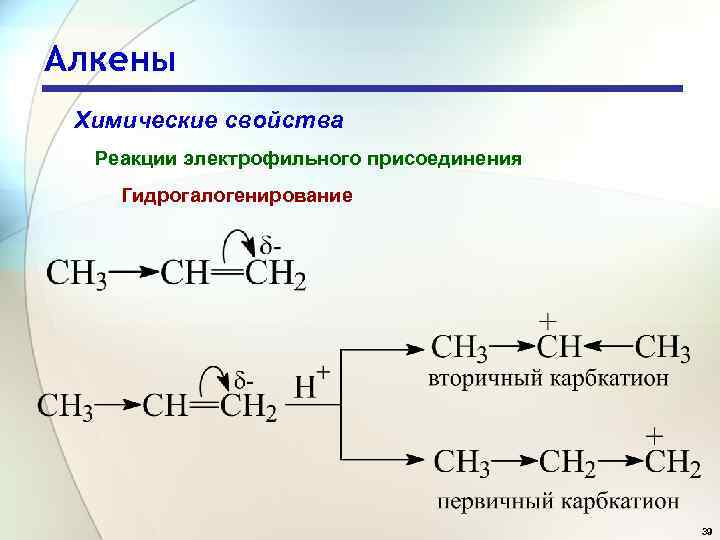
Алкены Химические свойства Реакции электрофильного присоединения Гидрогалогенирование 39
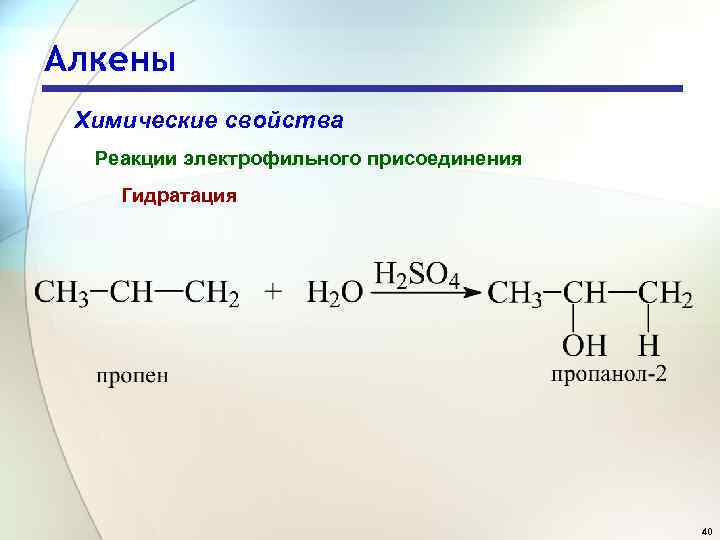
Алкены Химические свойства Реакции электрофильного присоединения Гидратация 40
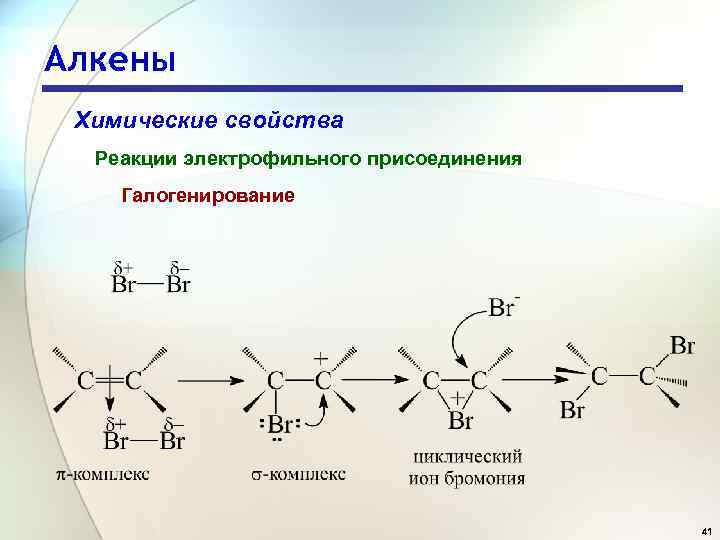
Алкены Химические свойства Реакции электрофильного присоединения Галогенирование 41
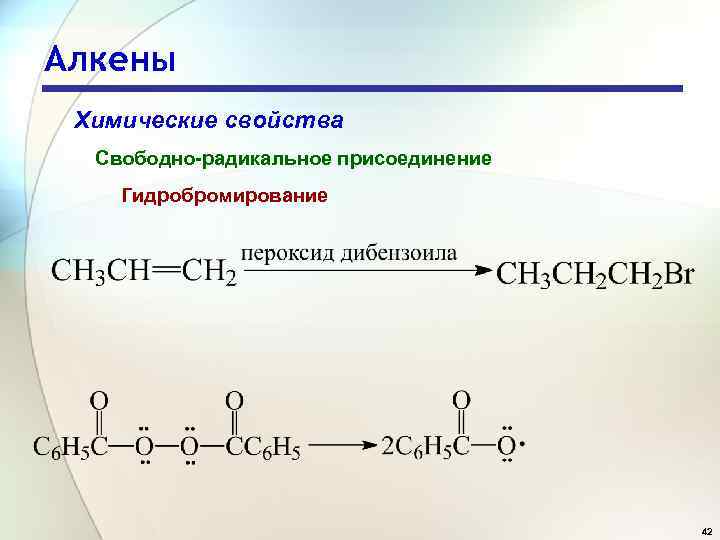
Алкены Химические свойства Свободно-радикальное присоединение Гидробромирование 42

Алкены Химические свойства Свободно-радикальное присоединение Гидробромирование Присоединение HBr против правила Марковникова происходит следующим образом: Br (а не Н ) реагирует в первую очередь с -системой и быстрее всего образуется наиболее стабильный радикал. «Перекисный эффект» или эффект Хараша. 43

Алкены Химические свойства Свободно-радикальное присоединение Аллильное замещение галогенами 44

Алкены Химические свойства Окисление по Вагнеру ВАГНЕР Егорович (9. XII. 1849 – 27. XI. 1903) 45
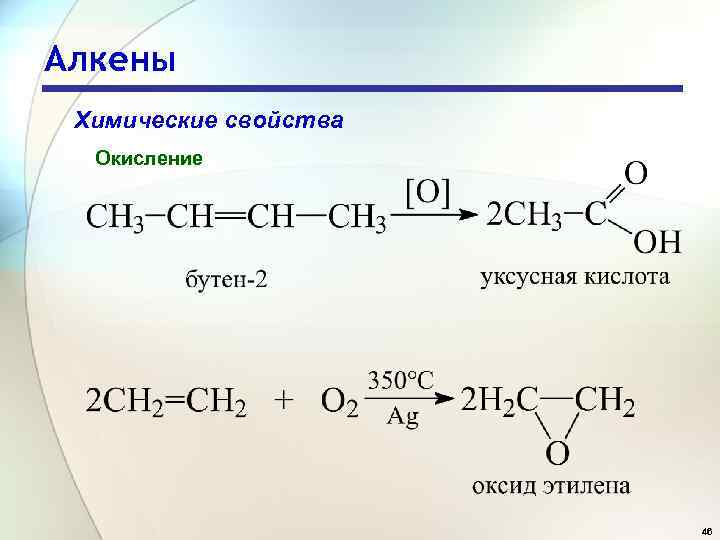
Алкены Химические свойства Окисление 46
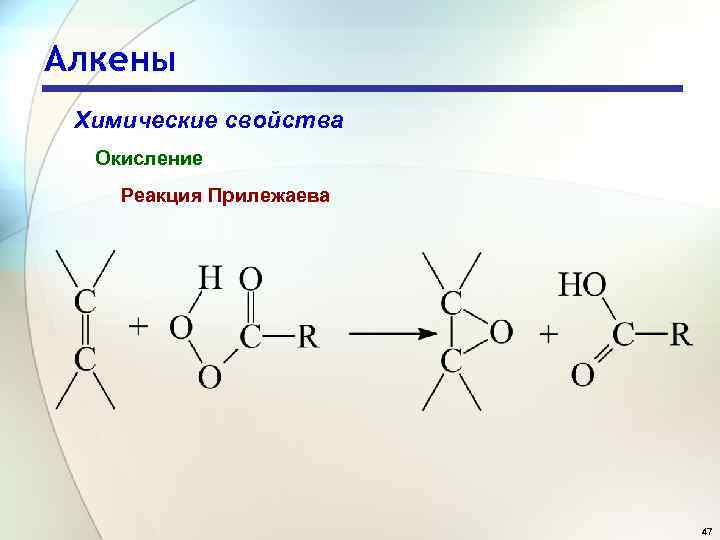
Алкены Химические свойства Окисление Реакция Прилежаева 47

Алкены Химические свойства Окисление Горение C 2 H 4 + 3 O 2 2 CO 2 + 2 H 2 O 48
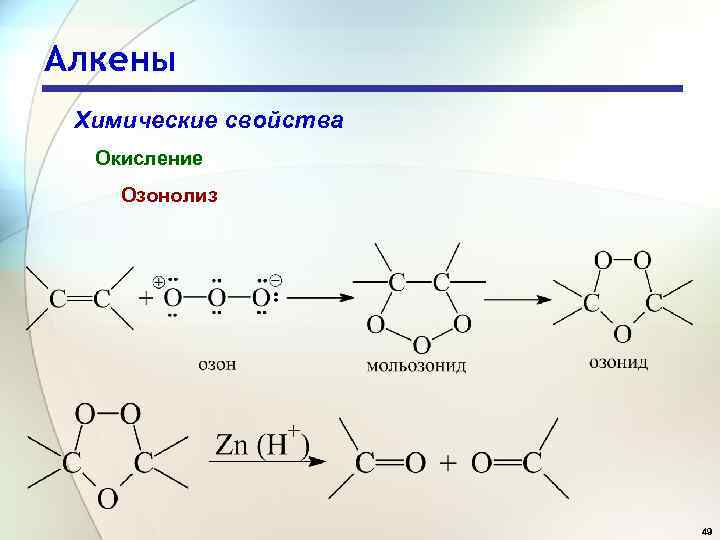
Алкены Химические свойства Окисление Озонолиз 49
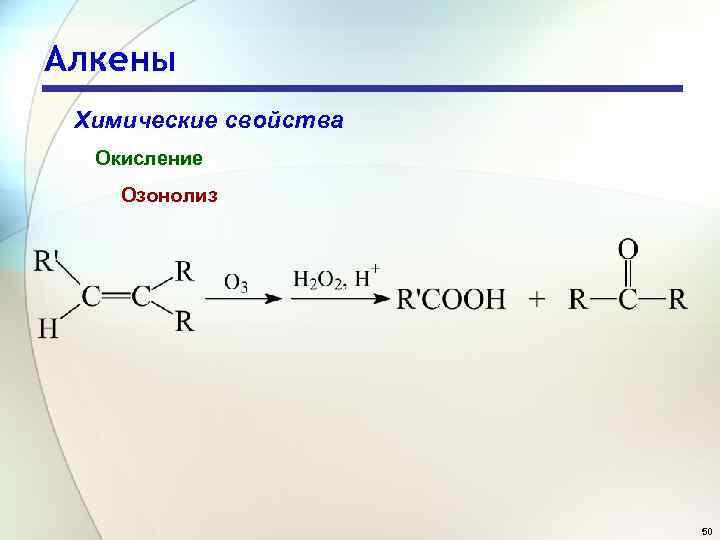
Алкены Химические свойства Окисление Озонолиз 50
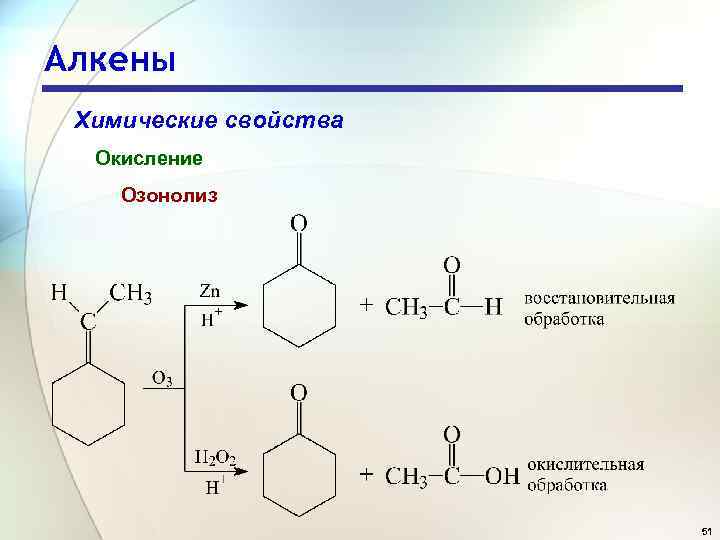
Алкены Химические свойства Окисление Озонолиз 51

Алкены Химические свойства Восстановление (гидрирование) 52
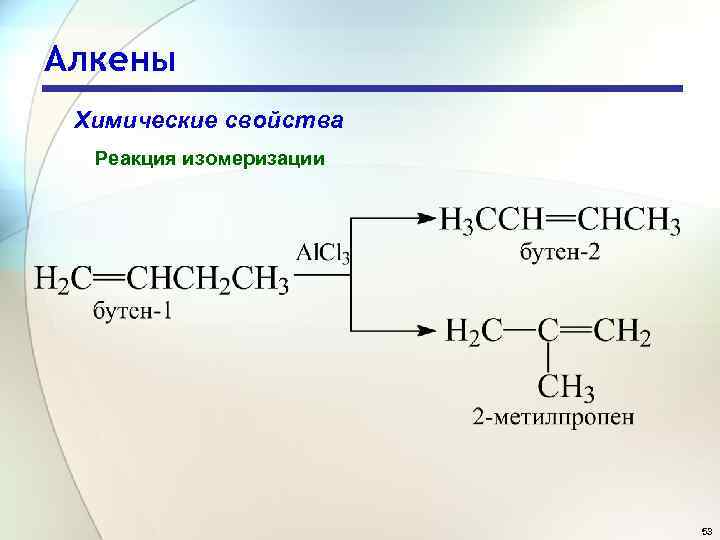
Алкены Химические свойства Реакция изомеризации 53

Алкены Химические свойства Реакция полимеризации — это последовательное присоединение молекул ненасыщенных соединений друг к другу с образованием высокомолекулярного продукта — полимера. 54
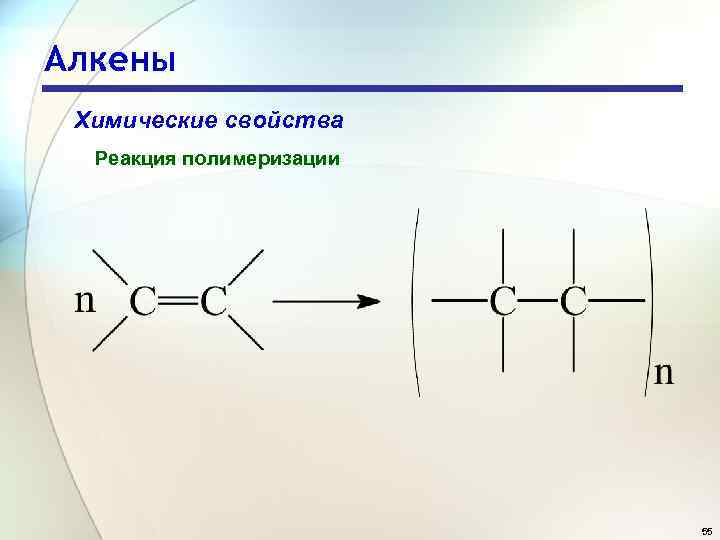
Алкены Химические свойства Реакция полимеризации 55
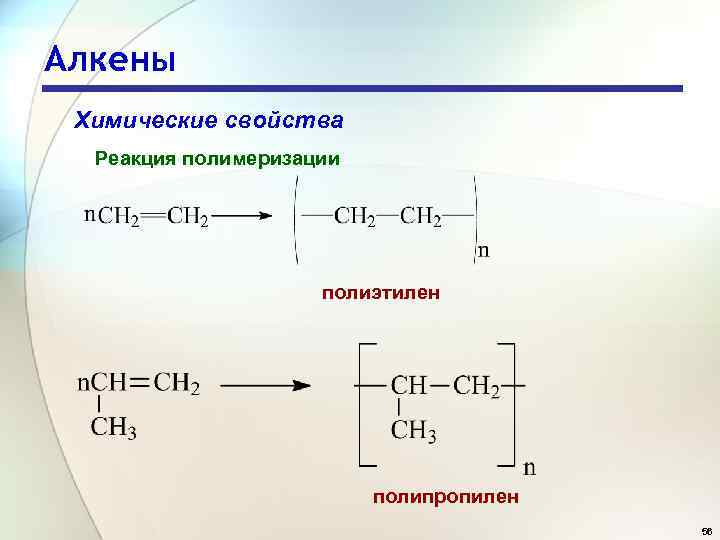
Алкены Химические свойства Реакция полимеризации полиэтилен полипропилен 56
4_алкены.ppt