онкология лекция1.ppt
- Количество слайдов: 119
 Основы хирургической онкологии кафедра хирургии с курсом урологии, онкологии, травматологии и ортопедии канд. мед. наук, доцент Л. В. Никитина
Основы хирургической онкологии кафедра хирургии с курсом урологии, онкологии, травматологии и ортопедии канд. мед. наук, доцент Л. В. Никитина
 Принцип онкологической настороженности «Судьба больного раком зависит от того врача, к которому он впервые обратился» (Н. И. Пирогов) Николай Иванович Пирогов (1810 -1881 гг. )
Принцип онкологической настороженности «Судьба больного раком зависит от того врача, к которому он впервые обратился» (Н. И. Пирогов) Николай Иванович Пирогов (1810 -1881 гг. )
 Актуальность проблемы В мире ежегодно злокачественным заболеваниями заболевает более 10 млн. человек, В мире ежегодно от злокачественных заболеваний умирает 5 млн. человек. В России каждый пятый житель заболевает в течение жизни одной из форм злокачественных заболеваний.
Актуальность проблемы В мире ежегодно злокачественным заболеваниями заболевает более 10 млн. человек, В мире ежегодно от злокачественных заболеваний умирает 5 млн. человек. В России каждый пятый житель заболевает в течение жизни одной из форм злокачественных заболеваний.
 Основные статистические показатели в онкологии v Заболеваемость — число зарегистрированных первичных больных ЗН в течение года на 100 000 населения (в России в 2005 г. — 330, 5). v Смертность — число умерших в течение определённого периода v времени на 100 000 населения (в России в 2005 г. — 200, 6). v Распространённость — доля населения, страдающего ЗН в определённый период времени на 100 000 населения (в России в 2005 г. — 1672). v Кумулятивный показатель — риск развития ЗН в течение жизни (до 75 лет) при условии отсутствия всех причин смерти (в России в 2005 г. — 22, 7%, у мужчин — 27. 5%, у женщин — 19, 8%). В возрасте до 60 лет этот показатель для обоих полов составляет 8, 2%. Заболеваемость ЗН зависит от демографической структуры населения: чем выше доля старших возрастных групп, тем выше показатель заболеваемости. Стандартизованные показатели (обычно рассчитывают на 100 000 населения. Стандартизованная заболеваемость в России в 2005 г. составила 192, 7 у женщин и 265. 6 у мужчин.
Основные статистические показатели в онкологии v Заболеваемость — число зарегистрированных первичных больных ЗН в течение года на 100 000 населения (в России в 2005 г. — 330, 5). v Смертность — число умерших в течение определённого периода v времени на 100 000 населения (в России в 2005 г. — 200, 6). v Распространённость — доля населения, страдающего ЗН в определённый период времени на 100 000 населения (в России в 2005 г. — 1672). v Кумулятивный показатель — риск развития ЗН в течение жизни (до 75 лет) при условии отсутствия всех причин смерти (в России в 2005 г. — 22, 7%, у мужчин — 27. 5%, у женщин — 19, 8%). В возрасте до 60 лет этот показатель для обоих полов составляет 8, 2%. Заболеваемость ЗН зависит от демографической структуры населения: чем выше доля старших возрастных групп, тем выше показатель заболеваемости. Стандартизованные показатели (обычно рассчитывают на 100 000 населения. Стандартизованная заболеваемость в России в 2005 г. составила 192, 7 у женщин и 265. 6 у мужчин.
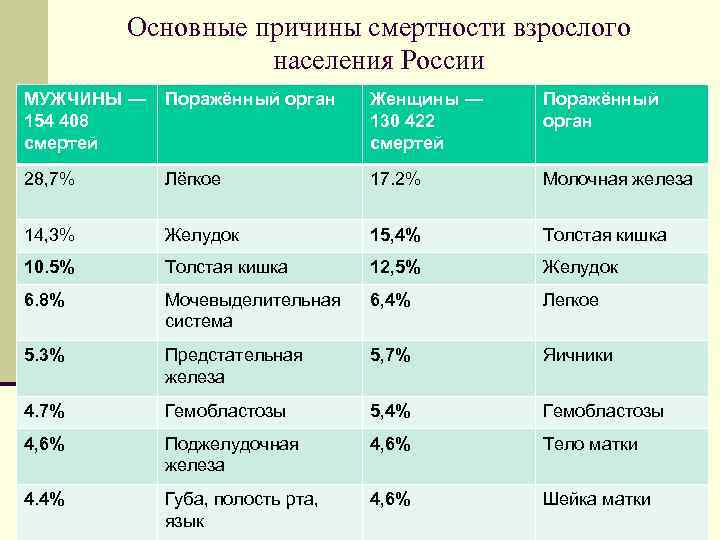 Основные причины смертности взрослого населения России МУЖЧИНЫ — 154 408 смертей Поражённый орган Женщины — 130 422 смертей Поражённый орган 28, 7% Лёгкое 17. 2% Молочная железа 14, 3% Желудок 15, 4% Толстая кишка 10. 5% Толстая кишка 12, 5% Желудок 6. 8% Мочевыделительная система 6, 4% Легкое 5. 3% Предстательная железа 5, 7% Яичники 4. 7% Гемобластозы 5, 4% Гемобластозы 4, 6% Поджелудочная железа 4, 6% Тело матки 4. 4% Губа, полость рта, язык 4, 6% Шейка матки
Основные причины смертности взрослого населения России МУЖЧИНЫ — 154 408 смертей Поражённый орган Женщины — 130 422 смертей Поражённый орган 28, 7% Лёгкое 17. 2% Молочная железа 14, 3% Желудок 15, 4% Толстая кишка 10. 5% Толстая кишка 12, 5% Желудок 6. 8% Мочевыделительная система 6, 4% Легкое 5. 3% Предстательная железа 5, 7% Яичники 4. 7% Гемобластозы 5, 4% Гемобластозы 4, 6% Поджелудочная железа 4, 6% Тело матки 4. 4% Губа, полость рта, язык 4, 6% Шейка матки
 Канцерогенез Автор теории Год Основные принципы П. Потт 1775 Теория химического канцерогенеза Дж. Конгейм 1870 -е Нарушение эмбриогенеза (из эмбриональных зачатков, отшнурованных в процессе эмбрионального развития) М. Рибберт 1890 -е Нарушение формирования органов: из зачатков, образующихся постоянно в процессе роста организма при снижении давления окружающих тканей Р. Вирхов 18801890 Травмы и хроническое раздражение тканей Г. Шпеман XIX век В. М. Зыков, Д. В. Ненкжов 1902 Теория ≪организаторов≫. Воздействие стеринов на эмбриогенез и формообразование Окислительно-восстановительная теория (за 11 лет до О. Варбурга)
Канцерогенез Автор теории Год Основные принципы П. Потт 1775 Теория химического канцерогенеза Дж. Конгейм 1870 -е Нарушение эмбриогенеза (из эмбриональных зачатков, отшнурованных в процессе эмбрионального развития) М. Рибберт 1890 -е Нарушение формирования органов: из зачатков, образующихся постоянно в процессе роста организма при снижении давления окружающих тканей Р. Вирхов 18801890 Травмы и хроническое раздражение тканей Г. Шпеман XIX век В. М. Зыков, Д. В. Ненкжов 1902 Теория ≪организаторов≫. Воздействие стеринов на эмбриогенез и формообразование Окислительно-восстановительная теория (за 11 лет до О. Варбурга)
 Канцерогенез Автор теории Год Основные принципы В. Эллерман и И О. Берг 1908 Вирусная теория: воздействие специфических вирусов И. И. Мечников 1909 Нарушение иммунной защиты П. Раус 1911 Вирусная теория: экспериментальная перевиваемая саркома 0. Варбург 1913 Теория нарушения гликолиза, дыхания клеток Б. Фишер. Вазельс 1920 -е Влияние внешних и внутренних факторов на предуготованные изменения в регенерирующей ткани Г. А. Надсон и Г. С. Филиппов 1925 Воздействие ионизирующего излучения Гетани 1957 Нарушение функциональной активности гипоталамуса Л. А. Зильбер 1966 Вирусогенетическая теория: эндогенные вирусы, онкогены Конец XX века Полиэтиологическая теория: генетическое и средовое (модифицирующее) влияния, молекулярные механизмы
Канцерогенез Автор теории Год Основные принципы В. Эллерман и И О. Берг 1908 Вирусная теория: воздействие специфических вирусов И. И. Мечников 1909 Нарушение иммунной защиты П. Раус 1911 Вирусная теория: экспериментальная перевиваемая саркома 0. Варбург 1913 Теория нарушения гликолиза, дыхания клеток Б. Фишер. Вазельс 1920 -е Влияние внешних и внутренних факторов на предуготованные изменения в регенерирующей ткани Г. А. Надсон и Г. С. Филиппов 1925 Воздействие ионизирующего излучения Гетани 1957 Нарушение функциональной активности гипоталамуса Л. А. Зильбер 1966 Вирусогенетическая теория: эндогенные вирусы, онкогены Конец XX века Полиэтиологическая теория: генетическое и средовое (модифицирующее) влияния, молекулярные механизмы
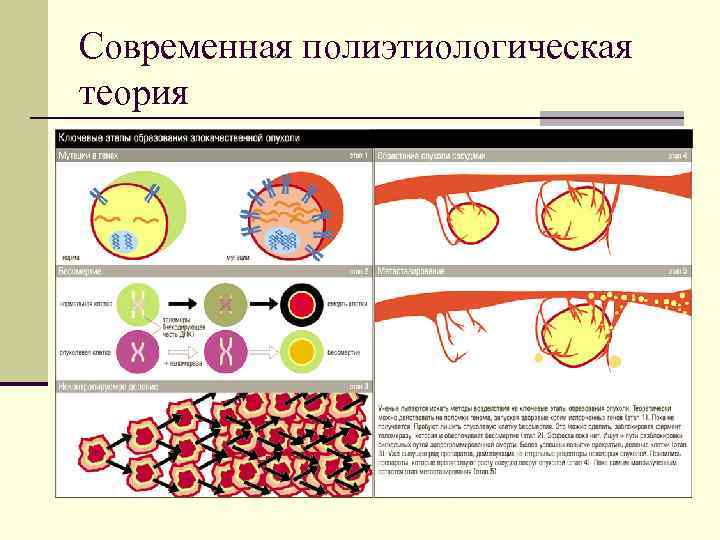 Современная полиэтиологическая теория
Современная полиэтиологическая теория
 Этиологические факторы. Питание. Европейская противораковая программа под эгидой ВОЗ приводит рекомендации по питанию. • Вероятность ЗН в значительной мере определена генетически, но уровень знаний не позволяет уверенно идентифицировать лиц, подверженных высокому риску. Рекомендации должны быть приложены ко всей популяции для лиц старше 2 лет. • Специфические рекомендации по питанию. - Жиры не должны превышать 30% обшей энергетической ценности пищи (не более 10% должны приходиться на насыщенные жиры, 6~8% — на полиненасыщенные, оставшаяся часть — на мононенасыщенные). - Желательно употребление разнообразных свежих овощей и фруктов несколько раз в день. - Необходимо сбалансировать физическую нагрузку и рацион для сохранения нормальной массы тела. - Пищевые добавки можно принимать только после обсуждения с врачом. - Необходимо ограничить потребление соли и пиши, консервированной при помощи нитритов, нитратов. Норма потребления соли — не более 6 г/сут. - Необходимо резкое ограничение потребления алкогольных напитков. • Соблюдение всех пунктов позволит снизить риск приблизительно на 35%.
Этиологические факторы. Питание. Европейская противораковая программа под эгидой ВОЗ приводит рекомендации по питанию. • Вероятность ЗН в значительной мере определена генетически, но уровень знаний не позволяет уверенно идентифицировать лиц, подверженных высокому риску. Рекомендации должны быть приложены ко всей популяции для лиц старше 2 лет. • Специфические рекомендации по питанию. - Жиры не должны превышать 30% обшей энергетической ценности пищи (не более 10% должны приходиться на насыщенные жиры, 6~8% — на полиненасыщенные, оставшаяся часть — на мононенасыщенные). - Желательно употребление разнообразных свежих овощей и фруктов несколько раз в день. - Необходимо сбалансировать физическую нагрузку и рацион для сохранения нормальной массы тела. - Пищевые добавки можно принимать только после обсуждения с врачом. - Необходимо ограничить потребление соли и пиши, консервированной при помощи нитритов, нитратов. Норма потребления соли — не более 6 г/сут. - Необходимо резкое ограничение потребления алкогольных напитков. • Соблюдение всех пунктов позволит снизить риск приблизительно на 35%.
 Этиологические факторы. Избыточная масса тела. v Старайтесь не допускать избыточной массы тела. • Каждый день выполняйте физические упражнения. • Увеличьте объём и разнообразие овощей и фруктов: их нужно употреблять не меньше 5 раз в день. Ограничьте потребление пищи, содержащей животные жиры. Если Вы употребляете алкоголь, будь то пиво, вино или крепкие напитки, ограничьте его количество до двух (мужчины) или одной (женщины) условных доз (1 условная доза алкоголя — 15 мл чистого этилового спирта).
Этиологические факторы. Избыточная масса тела. v Старайтесь не допускать избыточной массы тела. • Каждый день выполняйте физические упражнения. • Увеличьте объём и разнообразие овощей и фруктов: их нужно употреблять не меньше 5 раз в день. Ограничьте потребление пищи, содержащей животные жиры. Если Вы употребляете алкоголь, будь то пиво, вино или крепкие напитки, ограничьте его количество до двух (мужчины) или одной (женщины) условных доз (1 условная доза алкоголя — 15 мл чистого этилового спирта).
 Этиологические факторы. Курение. v Не начинайте курить, если курите — откажитесь от этой привычки. v Если вам не удаётся бросить курить, хотя бы не курите в присутствии некурящих.
Этиологические факторы. Курение. v Не начинайте курить, если курите — откажитесь от этой привычки. v Если вам не удаётся бросить курить, хотя бы не курите в присутствии некурящих.
 Этиологические факторы. Повышенная инсоляция. v Избегайте чрезмерного пребывания на солнце. Особенно важно защитить детей и подростков. v Тем, у кого есть склонность к солнечным ожогам, необходимо принимать активные меры защиты на протяжении всей жизни.
Этиологические факторы. Повышенная инсоляция. v Избегайте чрезмерного пребывания на солнце. Особенно важно защитить детей и подростков. v Тем, у кого есть склонность к солнечным ожогам, необходимо принимать активные меры защиты на протяжении всей жизни.
 Этиологические факторы. Канцерогенные вещества v Строго следите за тем, чтобы не подвергнуться воздействию канцерогенных веществ. v Соблюдайте все инструкции по мерам безопасности в отношении канцерогенных веществ. v Следуйте национальным рекомендациям по защите от радиации.
Этиологические факторы. Канцерогенные вещества v Строго следите за тем, чтобы не подвергнуться воздействию канцерогенных веществ. v Соблюдайте все инструкции по мерам безопасности в отношении канцерогенных веществ. v Следуйте национальным рекомендациям по защите от радиации.
 Этиологические факторы. Вирусы v Вирус папилломы человека 74% в миндалине! v Вирус иммунодефицита человека 5% больных с ОГШ – молодой контингент больных размеры опухоли и распространенность! v Вирус простого герпеса Белок вируса у 42% больных с раком полости рта и 0% среди контрольной группы v Вирус Эпштейна-Барра 81% больных Гренландии, 90% людей земного шара – серологически положительны
Этиологические факторы. Вирусы v Вирус папилломы человека 74% в миндалине! v Вирус иммунодефицита человека 5% больных с ОГШ – молодой контингент больных размеры опухоли и распространенность! v Вирус простого герпеса Белок вируса у 42% больных с раком полости рта и 0% среди контрольной группы v Вирус Эпштейна-Барра 81% больных Гренландии, 90% людей земного шара – серологически положительны
 Предраковые заболевания Все изменения клеток и формирующихся из них структур связаны с нарушением дифференцировки клеток-предшественниц. Существует 3 основных варианта нарушений тканевой дифференцировки. Врождённые пороки развития (врождённые уродства, гетеротопии, гетероплазии, гамартомы). Метаплазия — замещение одного типа дифференцированных клеточных элементов другим вследствие хронического воспаления, эндокринного воздействия и нарушений питания. Например, переходный эпителий мочевого пузыря при хроническом воспалении может превращаться в многослойный плоский или железистый призматический; при длительном дефиците витамина А развивается плоскоэпителиальная метаплазия эпителия дыхательных путей; островки многослойного плоского ороговевающего эпителия обнаруживают в молочной, щитовидной и предстательной железах при хронических воспалительных процессах и гормональных нарушениях. изменения в соединительной ткани (например, появление кости и хряща в посттравматических рубцах). Дисплазия характеризуется появлением клеток с внешними характеристиками злокачественных новообразований. Диспластические изменения нередко возникают на фоне метаплазии. В широком смысле понятие «дисплазия» должно включать в себя не только весь спектр предраковых изменений, но и инвазивный рак.
Предраковые заболевания Все изменения клеток и формирующихся из них структур связаны с нарушением дифференцировки клеток-предшественниц. Существует 3 основных варианта нарушений тканевой дифференцировки. Врождённые пороки развития (врождённые уродства, гетеротопии, гетероплазии, гамартомы). Метаплазия — замещение одного типа дифференцированных клеточных элементов другим вследствие хронического воспаления, эндокринного воздействия и нарушений питания. Например, переходный эпителий мочевого пузыря при хроническом воспалении может превращаться в многослойный плоский или железистый призматический; при длительном дефиците витамина А развивается плоскоэпителиальная метаплазия эпителия дыхательных путей; островки многослойного плоского ороговевающего эпителия обнаруживают в молочной, щитовидной и предстательной железах при хронических воспалительных процессах и гормональных нарушениях. изменения в соединительной ткани (например, появление кости и хряща в посттравматических рубцах). Дисплазия характеризуется появлением клеток с внешними характеристиками злокачественных новообразований. Диспластические изменения нередко возникают на фоне метаплазии. В широком смысле понятие «дисплазия» должно включать в себя не только весь спектр предраковых изменений, но и инвазивный рак.
 Предраковые состояния Предопухолевым заболеванием (состоянием), или предраком, принято считать врождённые или приобретённые изменения тканей, способствующие возникновению злокачественных новообразований. С клинической точки зрения различают облигатные и факультативные предопухолевые состояния. Для многих опухолей такие состояния не определены, что создаёт определённые трудности в организации профилактических мероприятий. Облигатный предрак, как правило, обусловлен генетическими или врождёнными факторами и рано или поздно перерождается в рак. К таким заболеваниям относят семейный полипоз толстой кишки, аденоматозный полип желудка. Факультативный предрак трансформируется в злокачественное новообразование относительно редко. Факультативный рак не связан с наследственными и врождёнными изменениями тканей. Чем дольше существует факультативное предраковое состояние, тем выше вероятность развития злокачественной опухоли, хотя у большинства больных в течение жизни она не развивается. К факультативному предраку относят дисгормональную гиперплазию с пролиферацией эпителия протоков молочной железы, атрофический гастрит с глубокой перестройкой слизистой оболочки, неспецифический язвенный колит, эрозию шейки матки, кожный рог и др.
Предраковые состояния Предопухолевым заболеванием (состоянием), или предраком, принято считать врождённые или приобретённые изменения тканей, способствующие возникновению злокачественных новообразований. С клинической точки зрения различают облигатные и факультативные предопухолевые состояния. Для многих опухолей такие состояния не определены, что создаёт определённые трудности в организации профилактических мероприятий. Облигатный предрак, как правило, обусловлен генетическими или врождёнными факторами и рано или поздно перерождается в рак. К таким заболеваниям относят семейный полипоз толстой кишки, аденоматозный полип желудка. Факультативный предрак трансформируется в злокачественное новообразование относительно редко. Факультативный рак не связан с наследственными и врождёнными изменениями тканей. Чем дольше существует факультативное предраковое состояние, тем выше вероятность развития злокачественной опухоли, хотя у большинства больных в течение жизни она не развивается. К факультативному предраку относят дисгормональную гиперплазию с пролиферацией эпителия протоков молочной железы, атрофический гастрит с глубокой перестройкой слизистой оболочки, неспецифический язвенный колит, эрозию шейки матки, кожный рог и др.
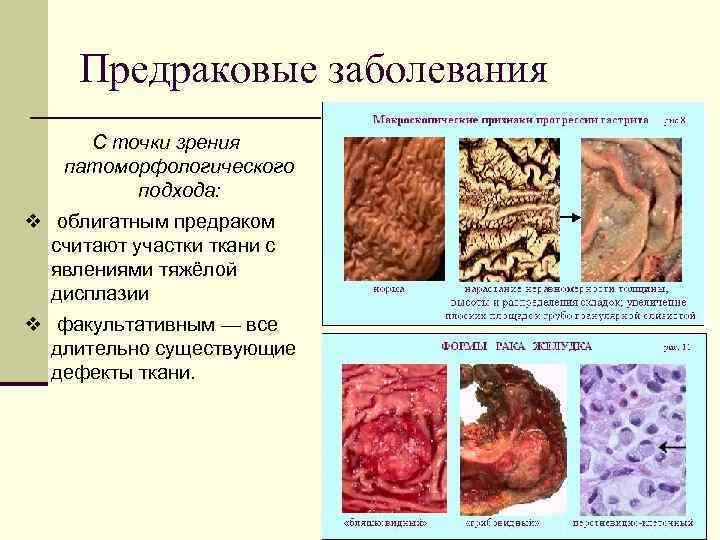 Предраковые заболевания С точки зрения патоморфологического подхода: v облигатным предраком считают участки ткани с явлениями тяжёлой дисплазии v факультативным — все длительно существующие дефекты ткани.
Предраковые заболевания С точки зрения патоморфологического подхода: v облигатным предраком считают участки ткани с явлениями тяжёлой дисплазии v факультативным — все длительно существующие дефекты ткани.
 Молекулярные механизмы канцерогенеза и опухолевой прогрессии v При избыточном действии одного или нескольких мутагенов в результате срыва адаптивных механизмов в клетке может происходить нарушение нормальных процессов, протекающих в её генетическом аппарате. v При повышенном содержании химических канцерогенов и облучении при неполноценной антиоксидантной защите происходят прямые поломки в геноме, т. е. точечные мутации, генные делеции и хромосомные перестройки, нарушающие нормальную функцию генов и кодируемых ими белков. v Описанные нарушения приводят к ещё большей изоляции клетки, искажению её сигнального и генетического аппаратов и, как следствие, к появлению трансформированных клеток. v Опухолевая клетка характеризуется комплексом нарушений на генном, хромосомном и геномном уровнях, которые выражаются в разнообразных типах точечных мутаций, хромосомных аберрациях и изменении количества хромосом.
Молекулярные механизмы канцерогенеза и опухолевой прогрессии v При избыточном действии одного или нескольких мутагенов в результате срыва адаптивных механизмов в клетке может происходить нарушение нормальных процессов, протекающих в её генетическом аппарате. v При повышенном содержании химических канцерогенов и облучении при неполноценной антиоксидантной защите происходят прямые поломки в геноме, т. е. точечные мутации, генные делеции и хромосомные перестройки, нарушающие нормальную функцию генов и кодируемых ими белков. v Описанные нарушения приводят к ещё большей изоляции клетки, искажению её сигнального и генетического аппаратов и, как следствие, к появлению трансформированных клеток. v Опухолевая клетка характеризуется комплексом нарушений на генном, хромосомном и геномном уровнях, которые выражаются в разнообразных типах точечных мутаций, хромосомных аберрациях и изменении количества хромосом.
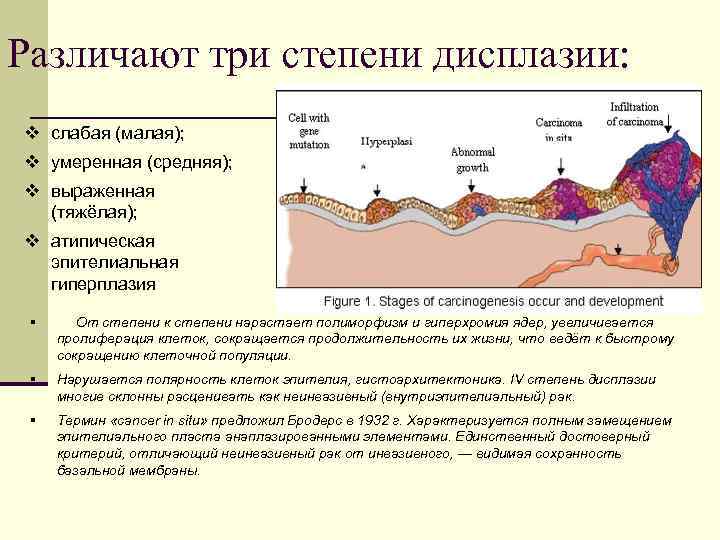 Различают три степени дисплазии: v слабая (малая); v умеренная (средняя); v выраженная (тяжёлая); v атипическая эпителиальная гиперплазия § От степени к степени нарастает полиморфизм и гиперхромия ядер, увеличивается пролиферация клеток, сокращается продолжительность их жизни, что ведёт к быстрому сокращению клеточной популяции. § Нарушается полярность клеток эпителия, гистоархитектоника. IV степень дисплазии многие склонны расценивать как неинвазивный (внутриэпителиальный) рак. § Термин «cancer in situ» предложил Бродерс в 1932 г. Характеризуется полным замещением эпителиального пласта анаплазированными элементами. Единственный достоверный критерий, отличающий неинвазивный рак от инвазивного, — видимая сохранность базальной мембраны.
Различают три степени дисплазии: v слабая (малая); v умеренная (средняя); v выраженная (тяжёлая); v атипическая эпителиальная гиперплазия § От степени к степени нарастает полиморфизм и гиперхромия ядер, увеличивается пролиферация клеток, сокращается продолжительность их жизни, что ведёт к быстрому сокращению клеточной популяции. § Нарушается полярность клеток эпителия, гистоархитектоника. IV степень дисплазии многие склонны расценивать как неинвазивный (внутриэпителиальный) рак. § Термин «cancer in situ» предложил Бродерс в 1932 г. Характеризуется полным замещением эпителиального пласта анаплазированными элементами. Единственный достоверный критерий, отличающий неинвазивный рак от инвазивного, — видимая сохранность базальной мембраны.
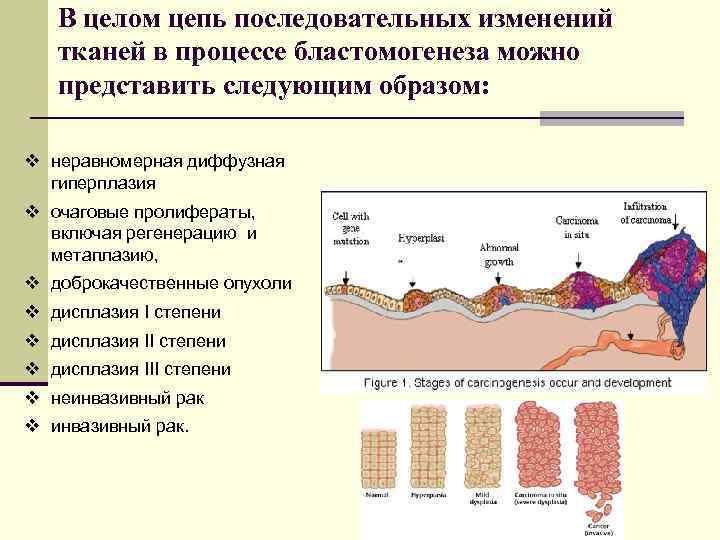 В целом цепь последовательных изменений тканей в процессе бластомогенеза можно представить следующим образом: v неравномерная диффузная гиперплазия v очаговые пролифераты, включая регенерацию и метаплазию, v доброкачественные опухоли v дисплазия I степени v дисплазия III степени v неинвазивный рак v инвазивный рак.
В целом цепь последовательных изменений тканей в процессе бластомогенеза можно представить следующим образом: v неравномерная диффузная гиперплазия v очаговые пролифераты, включая регенерацию и метаплазию, v доброкачественные опухоли v дисплазия I степени v дисплазия III степени v неинвазивный рак v инвазивный рак.
 Классификация опухолей Доброкачественные опухоли Злокачественные опухоли 1. клетки повторяют клетки 1. атипия и полиморфизм ткани, из которой развивалась клеток опухоль. 2. рост экспансивный 2. рост инфильтрирующий 3. не даёт метастазов 3. склонны к метастазированию (гематогенным, лимфогенным путем, контактно- инвазия в окружающие ткани) 4. практически не дают 4. склонны к рецидивов рецидивированию. 5. не оказывают влияния на 5. вызывают интоксикацию, общее состояние (за кахексию. исключением редких форм) 6. клетки повторяют клетки 6. атипия и полиморфизм ткани, из которой развивалась клеток опухоль.
Классификация опухолей Доброкачественные опухоли Злокачественные опухоли 1. клетки повторяют клетки 1. атипия и полиморфизм ткани, из которой развивалась клеток опухоль. 2. рост экспансивный 2. рост инфильтрирующий 3. не даёт метастазов 3. склонны к метастазированию (гематогенным, лимфогенным путем, контактно- инвазия в окружающие ткани) 4. практически не дают 4. склонны к рецидивов рецидивированию. 5. не оказывают влияния на 5. вызывают интоксикацию, общее состояние (за кахексию. исключением редких форм) 6. клетки повторяют клетки 6. атипия и полиморфизм ткани, из которой развивалась клеток опухоль.
 Доброкачественные опухоли Название формируется : вид ткани+ ОМА v Липома v Фиброма v Миома v Остеома v Невринома
Доброкачественные опухоли Название формируется : вид ткани+ ОМА v Липома v Фиброма v Миома v Остеома v Невринома
 Виды злокачественных опухолей Рак - опухоли из эпителиальной ткани Саркома - опухоли из производных мезенхимы Эпителий - ткань, покрывающая поверхность кожи, роговицу глаза и выстилающая все полости организма, внутреннюю поверхность полых органов пищеварительной, дыхательной и мочеполовой систем. Мезенхима - зародышевая соединительная ткань. Мезенхима возникает за счет клеток, которые выселяются из разных зародышевых листков: эктодермы, энтодермы и мезодермы. Из мезенхимы образуются: собственно соединительная ткань, кровеносные сосуды (их эндотелий), клетки крови, мышцы, висцеральный скелет, пигментные клетки и нижний слой соединительнотканной части кожи.
Виды злокачественных опухолей Рак - опухоли из эпителиальной ткани Саркома - опухоли из производных мезенхимы Эпителий - ткань, покрывающая поверхность кожи, роговицу глаза и выстилающая все полости организма, внутреннюю поверхность полых органов пищеварительной, дыхательной и мочеполовой систем. Мезенхима - зародышевая соединительная ткань. Мезенхима возникает за счет клеток, которые выселяются из разных зародышевых листков: эктодермы, энтодермы и мезодермы. Из мезенхимы образуются: собственно соединительная ткань, кровеносные сосуды (их эндотелий), клетки крови, мышцы, висцеральный скелет, пигментные клетки и нижний слой соединительнотканной части кожи.
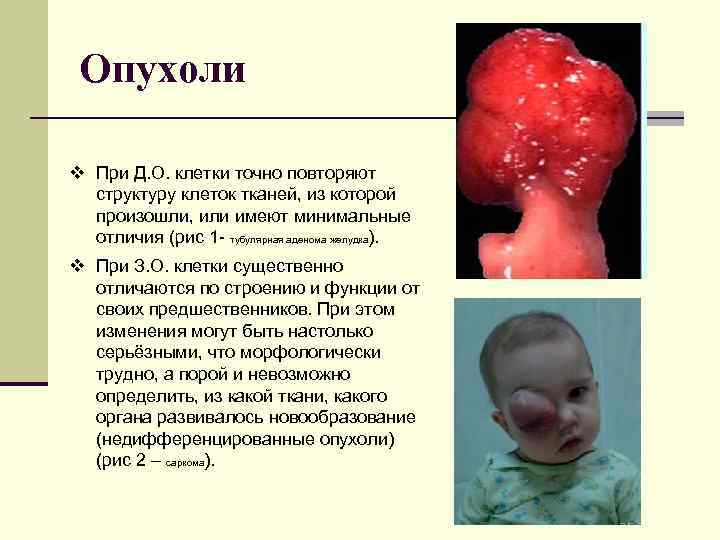 Опухоли v При Д. О. клетки точно повторяют структуру клеток тканей, из которой произошли, или имеют минимальные отличия (рис 1 - тубулярная аденома желудка). v При З. О. клетки существенно отличаются по строению и функции от своих предшественников. При этом изменения могут быть настолько серьёзными, что морфологически трудно, а порой и невозможно определить, из какой ткани, какого органа развивалось новообразование (недифференцированные опухоли) (рис 2 – саркома).
Опухоли v При Д. О. клетки точно повторяют структуру клеток тканей, из которой произошли, или имеют минимальные отличия (рис 1 - тубулярная аденома желудка). v При З. О. клетки существенно отличаются по строению и функции от своих предшественников. При этом изменения могут быть настолько серьёзными, что морфологически трудно, а порой и невозможно определить, из какой ткани, какого органа развивалось новообразование (недифференцированные опухоли) (рис 2 – саркома).
 ОПУХОЛИ Из ткани хорды: ● Доброкачественные: ● Злокачественные: Хордома злокачественная доброкачественная Из соединительной ткани: Миксосаркома Миксома Фибросаркома Фиброма Липома Из жировой ткани: Липосаркома Из сосудистых элементов: Ангиосаркома Гемангиоэндотелиома Ангиома Гемангиоэндотелиома (телеангиэктатическая, злокачественная кавернозная)
ОПУХОЛИ Из ткани хорды: ● Доброкачественные: ● Злокачественные: Хордома злокачественная доброкачественная Из соединительной ткани: Миксосаркома Миксома Фибросаркома Фиброма Липома Из жировой ткани: Липосаркома Из сосудистых элементов: Ангиосаркома Гемангиоэндотелиома Ангиома Гемангиоэндотелиома (телеангиэктатическая, злокачественная кавернозная)
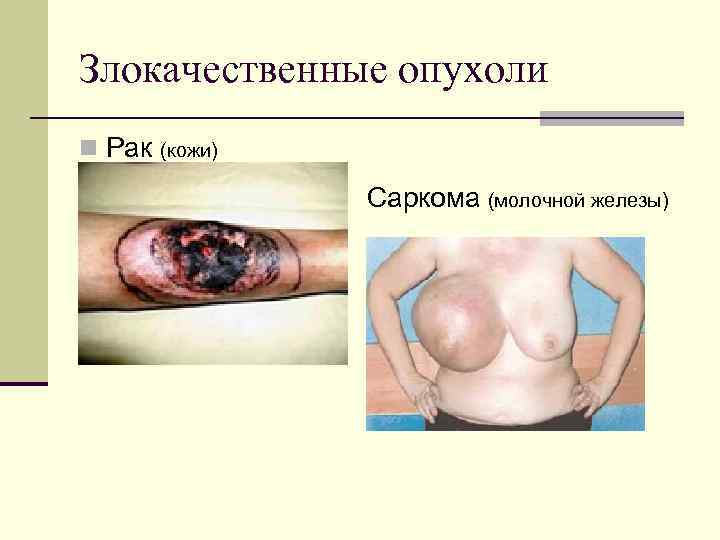 Злокачественные опухоли Рак (кожи) Саркома (молочной железы)
Злокачественные опухоли Рак (кожи) Саркома (молочной железы)
 Саркома (С), виды сарком (от греч. sárx, родительный падеж sarkós — мясо и -oma — окончание в названиях опухолей; название обусловлено тем, что С. на разрезе напоминает сырое рыбье мясо) v С. составляют до 10% всех злокачественных опухолей v мезенхимома — С. из эмбриональной соединительной ткани v С. из зрелых тканей мезенхимального происхождения — костной (остеосаркома), хрящевой (хондросаркома), сосудистой (ангиосаркома), кроветворной (ретикулосаркома), мышечной (лейомиосаркома, рабдомиосаркома), опорных элементов нервной ткани (глиосаркома). v Название формируется: вид ткани+САРКОМА
Саркома (С), виды сарком (от греч. sárx, родительный падеж sarkós — мясо и -oma — окончание в названиях опухолей; название обусловлено тем, что С. на разрезе напоминает сырое рыбье мясо) v С. составляют до 10% всех злокачественных опухолей v мезенхимома — С. из эмбриональной соединительной ткани v С. из зрелых тканей мезенхимального происхождения — костной (остеосаркома), хрящевой (хондросаркома), сосудистой (ангиосаркома), кроветворной (ретикулосаркома), мышечной (лейомиосаркома, рабдомиосаркома), опорных элементов нервной ткани (глиосаркома). v Название формируется: вид ткани+САРКОМА
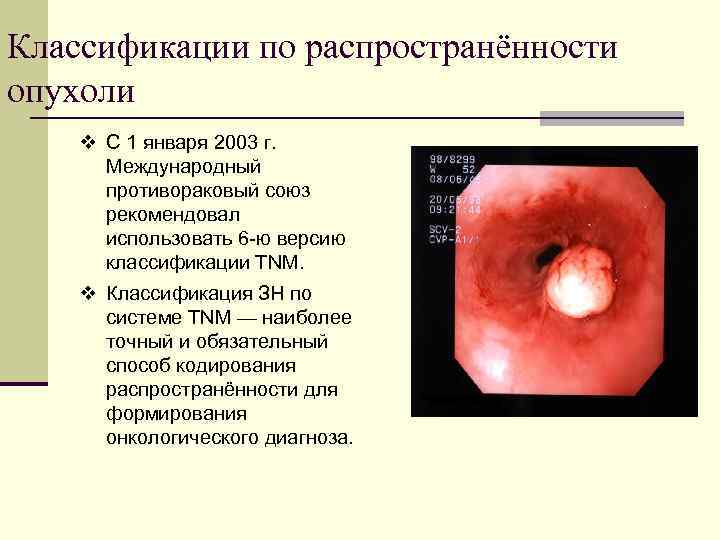 Классификации по распространённости опухоли v С 1 января 2003 г. Международный противораковый союз рекомендовал использовать 6 -ю версию классификации TNM. v Классификация ЗН по системе TNM — наиболее точный и обязательный способ кодирования распространённости для формирования онкологического диагноза.
Классификации по распространённости опухоли v С 1 января 2003 г. Международный противораковый союз рекомендовал использовать 6 -ю версию классификации TNM. v Классификация ЗН по системе TNM — наиболее точный и обязательный способ кодирования распространённости для формирования онкологического диагноза.
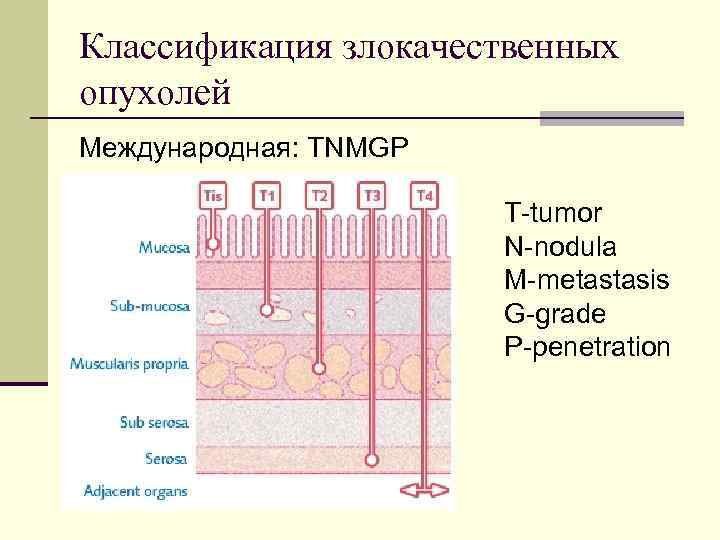 Классификация злокачественных опухолей Международная: TNMGP T-tumor N-nodula M-metastasis G-grade P-penetration
Классификация злокачественных опухолей Международная: TNMGP T-tumor N-nodula M-metastasis G-grade P-penetration
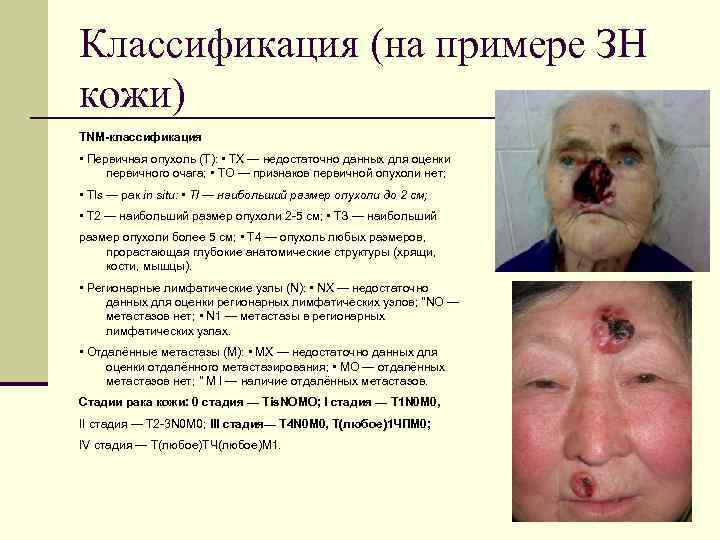 Классификация (на примере ЗН кожи) TNM-классификация • Первичная опухоль (Т): • ТХ — недостаточно данных для оценки первичного очага; • ТО — признаков первичной опухоли нет; • Tls — рак in situ: • Tl — наибольший размер опухоли до 2 см; • Т 2 — наибольший размер опухоли 2 -5 см; • ТЗ — наибольший размер опухоли более 5 см; • Т 4 — опухоль любых размеров, прорастающая глубокие анатомические структуры (хрящи, кости, мышцы). • Регионарные лимфатические узлы (N): • NX — недостаточно данных для оценки регионарных лимфатических узлов; "NO — метастазов нет; • N 1 — метастазы в регионарных лимфатических узлах. • Отдалённые метастазы (М): • MX — недостаточно данных для оценки отдалённого метастазирования; • МО — отдалённых метастазов нет; " M l — наличие отдалённых метастазов. Стадии рака кожи: 0 стадия — Tis. NOMO; I стадия — T 1 N 0 M 0, II стадия — T 2 -3 N 0 M 0; III стадия— T 4 N 0 M 0, Т(любое)1 ЧПМ 0; IV стадия — Т(любое)ТЧ(любое)М 1.
Классификация (на примере ЗН кожи) TNM-классификация • Первичная опухоль (Т): • ТХ — недостаточно данных для оценки первичного очага; • ТО — признаков первичной опухоли нет; • Tls — рак in situ: • Tl — наибольший размер опухоли до 2 см; • Т 2 — наибольший размер опухоли 2 -5 см; • ТЗ — наибольший размер опухоли более 5 см; • Т 4 — опухоль любых размеров, прорастающая глубокие анатомические структуры (хрящи, кости, мышцы). • Регионарные лимфатические узлы (N): • NX — недостаточно данных для оценки регионарных лимфатических узлов; "NO — метастазов нет; • N 1 — метастазы в регионарных лимфатических узлах. • Отдалённые метастазы (М): • MX — недостаточно данных для оценки отдалённого метастазирования; • МО — отдалённых метастазов нет; " M l — наличие отдалённых метастазов. Стадии рака кожи: 0 стадия — Tis. NOMO; I стадия — T 1 N 0 M 0, II стадия — T 2 -3 N 0 M 0; III стадия— T 4 N 0 M 0, Т(любое)1 ЧПМ 0; IV стадия — Т(любое)ТЧ(любое)М 1.
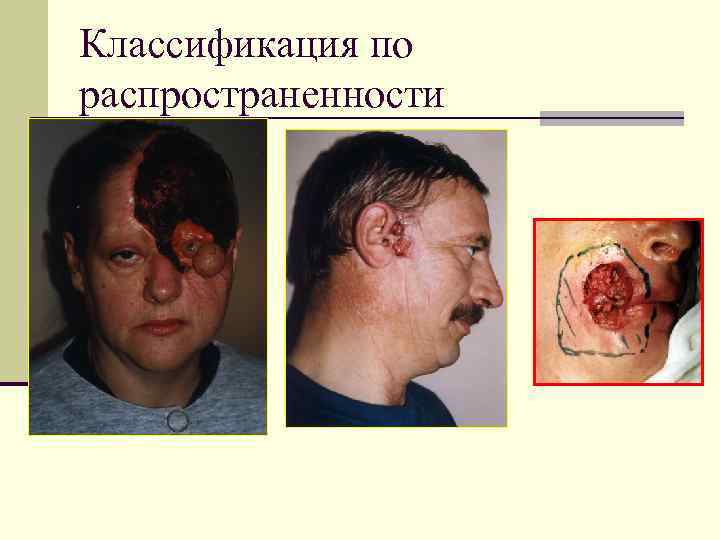 Классификация по распространенности
Классификация по распространенности
 МЕЖДУНАРОДНАЯ КЛАССИФИКАЦИЯ ПО СИСТЕМЕ TNM (на примере опухоли МЖ) Т - первичная опухоль ТХ - недостаточно данных для оценки первичной опухоли ТО - первичная опухоль не определяется Tis – преинвазивная карцинома: интрадуктальная или лобулярная карцинома in situ, или болезнь Педжета соска без наличия опухолевого узла Т 1 – опухоль до 2 см в наибольшем измерении Т 2 – опухоль до 5 см в наибольшем измерении Т 3 – опухоль более 5 см в наибольшем измерении Т 4 – опухоль любого размера с прямым распространением на грудную стенку или кожу N - регионарные лимфатические узлы NX - недостаточно данных для оценки регионарных лимфатических узлов NO - нет признаков метастатического поражения регионарных лимфатических узлов N 1 – имеются метастазы в смещаемых подмышечных лимфатических узлах на стороне поражения N 2 - имеются метастазы в подмышечных лимфатических узлах, фиксированных друг с другом или с другими структурами, на стороне поражения N 3 - имеются метастазы во внутренних лимфатических узлах молочной железы на стороне поражения М - отдаленные метастазы МХ - недостаточно данных для определения отдаленных метастазов МО - нет признаков отдаленных метастазов М 1 - имеются отдаленные метастазы
МЕЖДУНАРОДНАЯ КЛАССИФИКАЦИЯ ПО СИСТЕМЕ TNM (на примере опухоли МЖ) Т - первичная опухоль ТХ - недостаточно данных для оценки первичной опухоли ТО - первичная опухоль не определяется Tis – преинвазивная карцинома: интрадуктальная или лобулярная карцинома in situ, или болезнь Педжета соска без наличия опухолевого узла Т 1 – опухоль до 2 см в наибольшем измерении Т 2 – опухоль до 5 см в наибольшем измерении Т 3 – опухоль более 5 см в наибольшем измерении Т 4 – опухоль любого размера с прямым распространением на грудную стенку или кожу N - регионарные лимфатические узлы NX - недостаточно данных для оценки регионарных лимфатических узлов NO - нет признаков метастатического поражения регионарных лимфатических узлов N 1 – имеются метастазы в смещаемых подмышечных лимфатических узлах на стороне поражения N 2 - имеются метастазы в подмышечных лимфатических узлах, фиксированных друг с другом или с другими структурами, на стороне поражения N 3 - имеются метастазы во внутренних лимфатических узлах молочной железы на стороне поражения М - отдаленные метастазы МХ - недостаточно данных для определения отдаленных метастазов МО - нет признаков отдаленных метастазов М 1 - имеются отдаленные метастазы
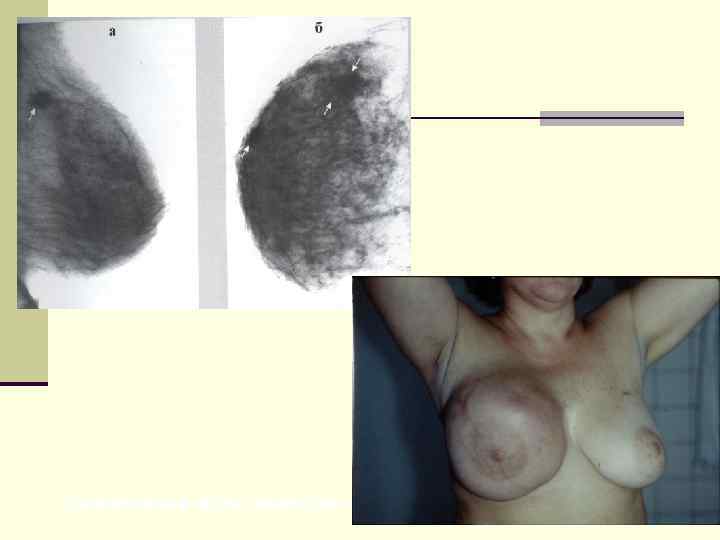 Синхронный мультицентрический рак молочных желез
Синхронный мультицентрический рак молочных желез
 Диагноз онкологического больного v Основное заболевание v Конкурирующие заболевания — обнаруженные у больного заболевания, которые каждое в отдельности само по себе и через осложнения могут привести к смерти. Сочетаясь по времени и поэтому, утяжеляя состояние больного, они значительно драматизируют течение болезни и ускоряют наступление смерти больного. v Сочетающиеся заболевания — каждое из них не является смертельным, однако, развиваясь одновременно, они в совокупности вызывают смертельный исход. Главный признак — совпадение во времени и усложнение патогенеза, что дает новое качественное состояние патологических процессов и выражается в определенных осложнениях. v Фоновое заболевание — нозологическая единица, которая сыграла существенную роль в возникновении и неблагоприятном течении процесса, поставленного во главу диагноза, и способствовала возникновению различных, в том числе и смертельных, осложнений. К числу фоновых заболеваний можно отнести нозологические единицы как имеющие, так и не имеющие прямой патогенетической связи с основным заболеванием. v Ятрогения (от греческого iatros — врач) или ятрогенное заболевание — понятие, объединяющее психогенные реакции пациента, вызванные неосторожным высказыванием или поведением медицинского персонала.
Диагноз онкологического больного v Основное заболевание v Конкурирующие заболевания — обнаруженные у больного заболевания, которые каждое в отдельности само по себе и через осложнения могут привести к смерти. Сочетаясь по времени и поэтому, утяжеляя состояние больного, они значительно драматизируют течение болезни и ускоряют наступление смерти больного. v Сочетающиеся заболевания — каждое из них не является смертельным, однако, развиваясь одновременно, они в совокупности вызывают смертельный исход. Главный признак — совпадение во времени и усложнение патогенеза, что дает новое качественное состояние патологических процессов и выражается в определенных осложнениях. v Фоновое заболевание — нозологическая единица, которая сыграла существенную роль в возникновении и неблагоприятном течении процесса, поставленного во главу диагноза, и способствовала возникновению различных, в том числе и смертельных, осложнений. К числу фоновых заболеваний можно отнести нозологические единицы как имеющие, так и не имеющие прямой патогенетической связи с основным заболеванием. v Ятрогения (от греческого iatros — врач) или ятрогенное заболевание — понятие, объединяющее психогенные реакции пациента, вызванные неосторожным высказыванием или поведением медицинского персонала.
 Диагноз онкологического больного Ещё одной особенностью онкологического диагноза считают отражение этапов лечения ЗН. Все методы воздействия на опухоль должны указываться в окончательной формулировке диагноза. Для этого используют шаблон ≪состояние после . . . ≫. Примеры типичного построения диагноза у выписанных больных: 1. Основное заболевание. Перстневидноклеточный рак нижней трети желудка I стадии (T 2 N 0 M 0); состояние после резекции по Бильрот 1 в мае 2003 г. Рецидив опухоли с диссеминапией по брюшине: состояние после двух курсов химиотерапии в 2004 г. ; частичная ремиссия. Осложнения. Рецидивирующее желудочное кровотечение. Двусторонняя пневмония. Сопутствующие заболевания. Атеросклеротический коронарокардиосклероз, пневмосклероз, эмфизема лёгких. 2. Основное заболевание. Первично-множественный метахронный рак: 1. Рак сигмовидной кишки III стадии, T 2 N 1 M 0; состояние после левосторонней гемиколэктомии в 2004 г. и двух курсов химиотерапии в 2005 г. 2. Периферический рак верхней доли правого лёгкого II стадии, T 3 N 0 M 0; состояние после верхней лобэктомии в 2001 г. Осложнение. Тромбоцитопения. Сопутствующие заболевания. Атеросклеротический коронарокардиосклероз. Хронический обструктивный бронхит.
Диагноз онкологического больного Ещё одной особенностью онкологического диагноза считают отражение этапов лечения ЗН. Все методы воздействия на опухоль должны указываться в окончательной формулировке диагноза. Для этого используют шаблон ≪состояние после . . . ≫. Примеры типичного построения диагноза у выписанных больных: 1. Основное заболевание. Перстневидноклеточный рак нижней трети желудка I стадии (T 2 N 0 M 0); состояние после резекции по Бильрот 1 в мае 2003 г. Рецидив опухоли с диссеминапией по брюшине: состояние после двух курсов химиотерапии в 2004 г. ; частичная ремиссия. Осложнения. Рецидивирующее желудочное кровотечение. Двусторонняя пневмония. Сопутствующие заболевания. Атеросклеротический коронарокардиосклероз, пневмосклероз, эмфизема лёгких. 2. Основное заболевание. Первично-множественный метахронный рак: 1. Рак сигмовидной кишки III стадии, T 2 N 1 M 0; состояние после левосторонней гемиколэктомии в 2004 г. и двух курсов химиотерапии в 2005 г. 2. Периферический рак верхней доли правого лёгкого II стадии, T 3 N 0 M 0; состояние после верхней лобэктомии в 2001 г. Осложнение. Тромбоцитопения. Сопутствующие заболевания. Атеросклеротический коронарокардиосклероз. Хронический обструктивный бронхит.
 Часть больных поздно обращается к врачу! Причины различны: v при наличии хронических заболеваний больному трудно уловить момент возникновения новых жалоб; v боязнь узнать правду; v низкий социальный и культурный статус пациента; v обращение к целителям, экстрасенсам и другим нетрадиционалистам, которые быстро, безболезненно «поставят диагноз» и «вылечат» больного.
Часть больных поздно обращается к врачу! Причины различны: v при наличии хронических заболеваний больному трудно уловить момент возникновения новых жалоб; v боязнь узнать правду; v низкий социальный и культурный статус пациента; v обращение к целителям, экстрасенсам и другим нетрадиционалистам, которые быстро, безболезненно «поставят диагноз» и «вылечат» больного.
 Этапы диагностики опухолей v Первый этап осуществляется врачом поликлиники v Заподозрив опухоль или диагностировав её, врач общей лечебной сети обязан направить больного в онкологическое учреждение (районное онкологическое отделение, онкологический диспансер, больницу, институт) для проведения второго этапа диагностики (уточнённой)
Этапы диагностики опухолей v Первый этап осуществляется врачом поликлиники v Заподозрив опухоль или диагностировав её, врач общей лечебной сети обязан направить больного в онкологическое учреждение (районное онкологическое отделение, онкологический диспансер, больницу, институт) для проведения второго этапа диагностики (уточнённой)
 «Успехи в противораковой борьбе зависят в основном от работы первичных поликлинических лечебных учреждений. Важно, чтобы на самом первом этапе обращения больного в поликлинику были предприняты все меры для исключения или подтверждения злокачественной опухоли» . Б. Е. Петерсон, 1977 г.
«Успехи в противораковой борьбе зависят в основном от работы первичных поликлинических лечебных учреждений. Важно, чтобы на самом первом этапе обращения больного в поликлинику были предприняты все меры для исключения или подтверждения злокачественной опухоли» . Б. Е. Петерсон, 1977 г.
 v Основные показатели состояния и качества онкологической помощи: процент поздней диагностики, летальность на первом году с момента установления диагноза и процент морфологического подтверждения диагноза — к сожалению, в России пока не имеют тенденции к улучшению. v Основные причины запущенности онкологических заболеваний обусловлены в половине случаев скрытым течением болезни и несвоевременным обращением больного к врачу, а в половине — врачебными ошибками и неоправданно длительным обследованием, тем, что принято называть отсутствием профессиональной онкологической настороженности. v При детальном анализе причин запущенности, оказывается, что методичный сбор анамнеза и полноценное физикальное и инструментальное обследование позволяют заподозрить у значительной части пациентов онкологическое заболевание и при «скрытом течении»
v Основные показатели состояния и качества онкологической помощи: процент поздней диагностики, летальность на первом году с момента установления диагноза и процент морфологического подтверждения диагноза — к сожалению, в России пока не имеют тенденции к улучшению. v Основные причины запущенности онкологических заболеваний обусловлены в половине случаев скрытым течением болезни и несвоевременным обращением больного к врачу, а в половине — врачебными ошибками и неоправданно длительным обследованием, тем, что принято называть отсутствием профессиональной онкологической настороженности. v При детальном анализе причин запущенности, оказывается, что методичный сбор анамнеза и полноценное физикальное и инструментальное обследование позволяют заподозрить у значительной части пациентов онкологическое заболевание и при «скрытом течении»
 Особенности сбора жалоб и анамнеза
Особенности сбора жалоб и анамнеза
 Программа сбора анамнестических данных должна включать: v вопросы о факторах, модифицирующих опухолевый рост, наследственности, хронических заболеваниях; v вопросы, направленные на выявление жалоб общего характера, а также — симптомов, характерных для различных локализаций опухолей. Врач должен оценить основные характеристики признаков заболевания: выраженность, давность, динамику.
Программа сбора анамнестических данных должна включать: v вопросы о факторах, модифицирующих опухолевый рост, наследственности, хронических заболеваниях; v вопросы, направленные на выявление жалоб общего характера, а также — симптомов, характерных для различных локализаций опухолей. Врач должен оценить основные характеристики признаков заболевания: выраженность, давность, динамику.
 Заставить врача подумать о возможном онкологическом заболевании должны следующие признаки: v изменение привычек, появление отвращения к какому-нибудь виду пищи, запахам и т. д. ; v немотивированные изменения самочувствия при неизменном режиме труда и быта; v появление патологических выделений из носа, соска молочной железы, прямой кишки и т. д. ; v нарушение проходимости полых органов; v появление ранее не существовавших видимых или пальпируемых образований на коже или слизистых оболочках полости рта, носа и др. Врач общей лечебной сети должен помнить, что слово «опухоль» является условным термином, так как злокачественный процесс может выражаться не только в избытке ткани, но и в ее дефиците (язвы, незаживающие раны).
Заставить врача подумать о возможном онкологическом заболевании должны следующие признаки: v изменение привычек, появление отвращения к какому-нибудь виду пищи, запахам и т. д. ; v немотивированные изменения самочувствия при неизменном режиме труда и быта; v появление патологических выделений из носа, соска молочной железы, прямой кишки и т. д. ; v нарушение проходимости полых органов; v появление ранее не существовавших видимых или пальпируемых образований на коже или слизистых оболочках полости рта, носа и др. Врач общей лечебной сети должен помнить, что слово «опухоль» является условным термином, так как злокачественный процесс может выражаться не только в избытке ткани, но и в ее дефиците (язвы, незаживающие раны).
 v Классический синдром дискомфорта ( «синдром малых признаков» ), описанного А. И. Савицким v Проявляется возможным проявлением паранеопластических синдромов (кожных, неврологических, эндокринных и т. д. ) той или иной степени выраженности. v Как правило, для анамнеза онкологического больного характерно непрерывное нарастание симптомов.
v Классический синдром дискомфорта ( «синдром малых признаков» ), описанного А. И. Савицким v Проявляется возможным проявлением паранеопластических синдромов (кожных, неврологических, эндокринных и т. д. ) той или иной степени выраженности. v Как правило, для анамнеза онкологического больного характерно непрерывное нарастание симптомов.
 Общие симптомы злокачественных образований Синдром нарушения функции (желтуха)
Общие симптомы злокачественных образований Синдром нарушения функции (желтуха)
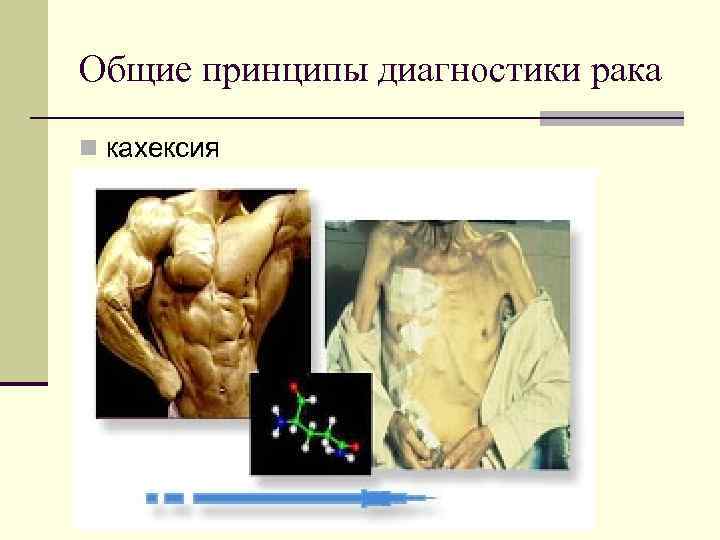 Общие принципы диагностики рака кахексия
Общие принципы диагностики рака кахексия
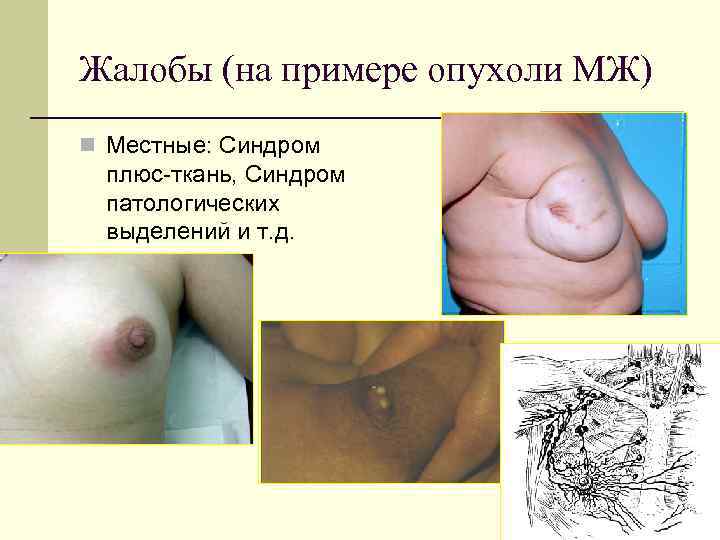 Жалобы (на примере опухоли МЖ) Местные: Синдром плюс-ткань, Синдром патологических выделений и т. д.
Жалобы (на примере опухоли МЖ) Местные: Синдром плюс-ткань, Синдром патологических выделений и т. д.
 v Главным правилом для врача при обследовании больного с подозрением на наличие онкологической патологии должен стать полный осмотр, а не только осмотр пораженной области и зоны возможного регионарного метастазирования. v Эта установка объясняется тем, что местное поражение может оказаться отдаленным метастазом опухоли, локализирующейся совсем в другом месте. v Кроме того, возможно синхронное возникновение множественных опухолей в органе (толстая кишка, кожа и др. ).
v Главным правилом для врача при обследовании больного с подозрением на наличие онкологической патологии должен стать полный осмотр, а не только осмотр пораженной области и зоны возможного регионарного метастазирования. v Эта установка объясняется тем, что местное поражение может оказаться отдаленным метастазом опухоли, локализирующейся совсем в другом месте. v Кроме того, возможно синхронное возникновение множественных опухолей в органе (толстая кишка, кожа и др. ).
 Трудности диагностики ЗН в первичном звене v клиническая картина может быть неполной или атипичной; v подходящая болезнь не сразу «приходит в голову» ; v больной скрывает или отрицает симптомы v плохое планирование медосмотров — без учета особенностей обследуемой группы, без целенаправленного поиска заболеваний, характерных именно для этого контингента, отсутствие согласованности (дублирование обследования одной группы наряду с невключением в исследование другой); v охват чрезмерно больших слоев населения, что неизбежно ведет к снижению качества осмотров; v низкая оснащенность (отсутствие возможности широко использовать рутинные, не говоря уже о современнейших, лабораторные, рентгенологические, ультразвуковые и эндоскопические методы обследования).
Трудности диагностики ЗН в первичном звене v клиническая картина может быть неполной или атипичной; v подходящая болезнь не сразу «приходит в голову» ; v больной скрывает или отрицает симптомы v плохое планирование медосмотров — без учета особенностей обследуемой группы, без целенаправленного поиска заболеваний, характерных именно для этого контингента, отсутствие согласованности (дублирование обследования одной группы наряду с невключением в исследование другой); v охват чрезмерно больших слоев населения, что неизбежно ведет к снижению качества осмотров; v низкая оснащенность (отсутствие возможности широко использовать рутинные, не говоря уже о современнейших, лабораторные, рентгенологические, ультразвуковые и эндоскопические методы обследования).
 Задачи второго этапа диагностики v Определение локализации опухоли, v распространённости её в органе, v морфологическое подтверждение диагноза, v оценка состояния регионарных лимфатических узлов, v поиск возможных отдалённых метастазов. для этой цели применяются инструментальные, лабораторные и морфологические методы исследования.
Задачи второго этапа диагностики v Определение локализации опухоли, v распространённости её в органе, v морфологическое подтверждение диагноза, v оценка состояния регионарных лимфатических узлов, v поиск возможных отдалённых метастазов. для этой цели применяются инструментальные, лабораторные и морфологические методы исследования.
 К компетенции онкологов относится: v знание предраковых заболеваний; v знание симптомов ранних стадий злокачественных опухолей; v тщательное обследование каждого больного врачом любой специальности для выявления возможного заболевания злокачественной опухолью; v в диагностически трудных случаях должна существовать профессиональная установка на подозрение атипичного или осложненного течения онкологического заболевания; v знание принципов онкологической помощи, организации лечения в сети онкологических лечебных учреждений и быстрое направление по назначению больного с подозрением на опухоль.
К компетенции онкологов относится: v знание предраковых заболеваний; v знание симптомов ранних стадий злокачественных опухолей; v тщательное обследование каждого больного врачом любой специальности для выявления возможного заболевания злокачественной опухолью; v в диагностически трудных случаях должна существовать профессиональная установка на подозрение атипичного или осложненного течения онкологического заболевания; v знание принципов онкологической помощи, организации лечения в сети онкологических лечебных учреждений и быстрое направление по назначению больного с подозрением на опухоль.
 Морфологическое подтверждение злокачественного характера опухоли v Первая задача — всесторонняя характеристика первичной опухоли, то есть символа «Т» по международной классификации ВОЗ (TNM). v Для этого используются различные методы взятия материала для морфологического исследования.
Морфологическое подтверждение злокачественного характера опухоли v Первая задача — всесторонняя характеристика первичной опухоли, то есть символа «Т» по международной классификации ВОЗ (TNM). v Для этого используются различные методы взятия материала для морфологического исследования.
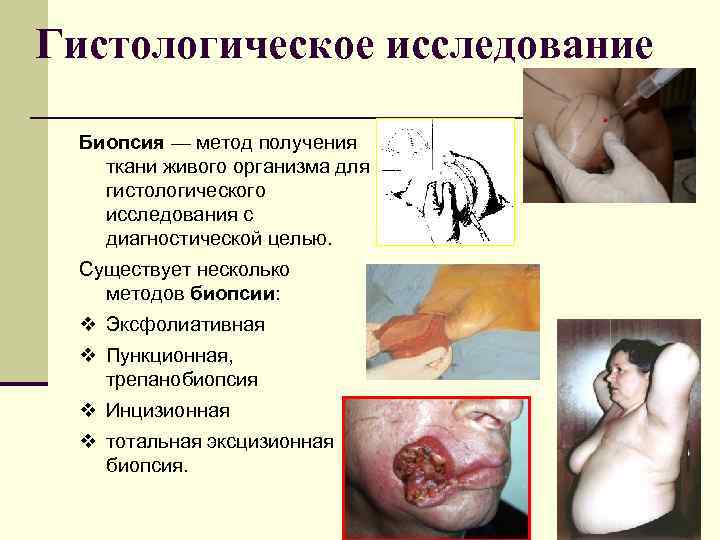 Гистологическое исследование Биопсия — метод получения ткани живого организма для гистологического исследования с диагностической целью. Существует несколько методов биопсии: v Эксфолиативная v Пункционная, трепанобиопсия v Инцизионная v тотальная эксцизионная биопсия.
Гистологическое исследование Биопсия — метод получения ткани живого организма для гистологического исследования с диагностической целью. Существует несколько методов биопсии: v Эксфолиативная v Пункционная, трепанобиопсия v Инцизионная v тотальная эксцизионная биопсия.
 Иммуногистохимические методы v В конце 1970 -х гг. в клиническую практику стали внедрять методы, сочетавшие в себе гистохимические и иммунологические основы. v В 1950— 1955 гг. группа исследователей под руководством Альберта Кунса впервые получила меченые флуоресцеином AT и применили их в диагностических целях. v Но только в 1975 г. Кохлер и Милштейн разработан и «гибридомную технологию» получения моноклональных AT и открыли широкие перспективы для использования ионоклональных AT в онкологии. v За открытие принципов синтеза моноклональных AT авторы получили Нобелевскую премию в 1984 г. В настоящее время моноклональные AT используют не только для диагностики, но и для направленной цитостатической терапии.
Иммуногистохимические методы v В конце 1970 -х гг. в клиническую практику стали внедрять методы, сочетавшие в себе гистохимические и иммунологические основы. v В 1950— 1955 гг. группа исследователей под руководством Альберта Кунса впервые получила меченые флуоресцеином AT и применили их в диагностических целях. v Но только в 1975 г. Кохлер и Милштейн разработан и «гибридомную технологию» получения моноклональных AT и открыли широкие перспективы для использования ионоклональных AT в онкологии. v За открытие принципов синтеза моноклональных AT авторы получили Нобелевскую премию в 1984 г. В настоящее время моноклональные AT используют не только для диагностики, но и для направленной цитостатической терапии.
 Показания для использования иммуногистохимических методов: v Диагностика опухолей неясного генеза. v Определение клональности у больных лейкозом. v Обнаружение небольшого количества злокачественных клеток (например, в лимфатическом узле). v Окрашивание компонентов стромы опухоли. v Иммунное фенотипирование опухоли, особенно гемобластозов.
Показания для использования иммуногистохимических методов: v Диагностика опухолей неясного генеза. v Определение клональности у больных лейкозом. v Обнаружение небольшого количества злокачественных клеток (например, в лимфатическом узле). v Окрашивание компонентов стромы опухоли. v Иммунное фенотипирование опухоли, особенно гемобластозов.
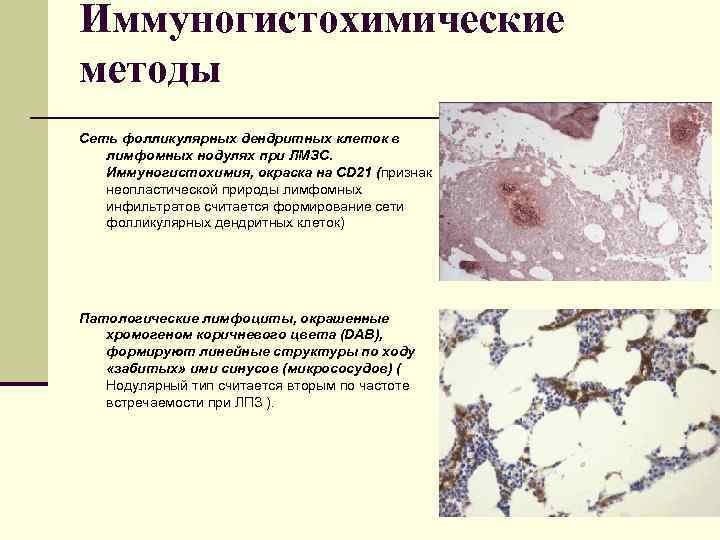 Иммуногистохимические методы Сеть фолликулярных дендритных клеток в лимфомных нодулях при ЛМЗС. Иммуногистохимия, окраска на CD 21 (признак неопластической природы лимфомных инфильтратов считается формирование сети фолликулярных дендритных клеток) Патологические лимфоциты, окрашенные хромогеном коричневого цвета (DAB), формируют линейные структуры по ходу «забитых» ими синусов (микрососудов) ( Нодулярный тип считается вторым по частоте встречаемости при ЛПЗ ).
Иммуногистохимические методы Сеть фолликулярных дендритных клеток в лимфомных нодулях при ЛМЗС. Иммуногистохимия, окраска на CD 21 (признак неопластической природы лимфомных инфильтратов считается формирование сети фолликулярных дендритных клеток) Патологические лимфоциты, окрашенные хромогеном коричневого цвета (DAB), формируют линейные структуры по ходу «забитых» ими синусов (микрососудов) ( Нодулярный тип считается вторым по частоте встречаемости при ЛПЗ ).
 Цитология ЦМ исследования технически прост, быстр, сравнительно дёшев, малотравматичен. Однако «лёгкость» метода обманчива, так как цитологическое исследование должно заканчиваться формулировкой ответственного заключения, на основе которого разрабатывается тактика лечения. Материал для цитологического исследования получают с помошью: v тонкоигольной аспирационной биопсии патологических очагов и регионарных лимфатических узлов; v эксфолиативной биопсии, мазков с поверхности ран и язв; v сбора мокроты, мочи, асцитической жидкости, плеврального экссудата (транссудата), содержимого кист, секрета; v отпечатков новообразований и лимфатических узлов во время операции.
Цитология ЦМ исследования технически прост, быстр, сравнительно дёшев, малотравматичен. Однако «лёгкость» метода обманчива, так как цитологическое исследование должно заканчиваться формулировкой ответственного заключения, на основе которого разрабатывается тактика лечения. Материал для цитологического исследования получают с помошью: v тонкоигольной аспирационной биопсии патологических очагов и регионарных лимфатических узлов; v эксфолиативной биопсии, мазков с поверхности ран и язв; v сбора мокроты, мочи, асцитической жидкости, плеврального экссудата (транссудата), содержимого кист, секрета; v отпечатков новообразований и лимфатических узлов во время операции.
 Основные принципы цитологической диагностики v Различие клеточного состава в норме и патологии. v Оценка не одной отдельно взятой клетки, а их совокупности; большое значение придают фону препарата. v Цитологу необходимо пройти традиционную патологоанатомическую подготовку. v Каждое исследование завершают формулировкой чёткого заключения.
Основные принципы цитологической диагностики v Различие клеточного состава в норме и патологии. v Оценка не одной отдельно взятой клетки, а их совокупности; большое значение придают фону препарата. v Цитологу необходимо пройти традиционную патологоанатомическую подготовку. v Каждое исследование завершают формулировкой чёткого заключения.
 Критерии цитологической диагностики злокачественных новообразований 1. Изменения клетки. v Увеличение размеров (могут быть гигантскими). Редко злокачественные клетки имеют нормальные размеры (например, при тубулярном раке, маститоподобном варианте долькового рака молочной железы, фолликулярном раке щитовидной железы, светлоклеточном раке почки), что затрудняет цитологическую диагностику. v Изменение формы и полиморфизм клеточных элементов. v Нарушение соотношения ядра и цитоплазмы в сторону увеличения ядра. v Противоречие в степенях зрелости ядра и цитоплазмы: например, молодое ядро в ороговевшей цитоплазме при высокодифференцированном плоскоклеточном раке. 2. Изменения ядер клеток: увеличение, полиморфизм, бугристость, неравномерный рисунок хроматина, неровность контуров (наиболее постоянный признак), гиперхромия; наличие фигуры клеточного деления (в цитологических препаратах сравнительно редки). 3. Изменения ядрышек: увеличение количества (больше, чем в нормальной клетке) и размеров, неправильная форма.
Критерии цитологической диагностики злокачественных новообразований 1. Изменения клетки. v Увеличение размеров (могут быть гигантскими). Редко злокачественные клетки имеют нормальные размеры (например, при тубулярном раке, маститоподобном варианте долькового рака молочной железы, фолликулярном раке щитовидной железы, светлоклеточном раке почки), что затрудняет цитологическую диагностику. v Изменение формы и полиморфизм клеточных элементов. v Нарушение соотношения ядра и цитоплазмы в сторону увеличения ядра. v Противоречие в степенях зрелости ядра и цитоплазмы: например, молодое ядро в ороговевшей цитоплазме при высокодифференцированном плоскоклеточном раке. 2. Изменения ядер клеток: увеличение, полиморфизм, бугристость, неравномерный рисунок хроматина, неровность контуров (наиболее постоянный признак), гиперхромия; наличие фигуры клеточного деления (в цитологических препаратах сравнительно редки). 3. Изменения ядрышек: увеличение количества (больше, чем в нормальной клетке) и размеров, неправильная форма.
 Иммуноцитохимия Иммуноцитохимический метод исследования основан на оценке реакции клеток на различные маркёры. Это расширяет возможности морфологической диагностики. Набор сывороток для установления природы патологического очага включает следующее: v Набор цитокератинов для диагностики эпителиальных опухолей. v Общий лейкоцитарный Аг для маркировки опухолей лимфоидной системы. v Виментин для диагностики опухолей мягких тканей. v НМВ-45 для диагностики меланомы.
Иммуноцитохимия Иммуноцитохимический метод исследования основан на оценке реакции клеток на различные маркёры. Это расширяет возможности морфологической диагностики. Набор сывороток для установления природы патологического очага включает следующее: v Набор цитокератинов для диагностики эпителиальных опухолей. v Общий лейкоцитарный Аг для маркировки опухолей лимфоидной системы. v Виментин для диагностики опухолей мягких тканей. v НМВ-45 для диагностики меланомы.
 Иммуноцитохимическое исследование v позволяет определить источник метастазирования при невыявленном первичном очаге. К сожалению, возможности этого метода весьма ограничены. v На практике патогномоничны только 3 маркёра: тиреоглобулин для выявления первичной опухоли и метастазов папиллярного и фолликулярного рака щитовидной железы, кальцитонин для диагностики новообразований из С-клеток, простатоспецифический Аг (ПСА) при раке предстательной железы.
Иммуноцитохимическое исследование v позволяет определить источник метастазирования при невыявленном первичном очаге. К сожалению, возможности этого метода весьма ограничены. v На практике патогномоничны только 3 маркёра: тиреоглобулин для выявления первичной опухоли и метастазов папиллярного и фолликулярного рака щитовидной железы, кальцитонин для диагностики новообразований из С-клеток, простатоспецифический Аг (ПСА) при раке предстательной железы.
 Выявление биологических онкомаркеров Большой интерес для современной онкологии представляет использование полимеразной цепной реакции (ПЦР) для определения изменений различных генов в плазме крови с целью раннего выявления злокачественных новообразований различной локализации, профилактики развития рака, а также формирования групп риска для динамического наблюдения. ООО «Центром молекулярно-генетической диагностики Сабирова А. Х. » был проведен профилактический осмотр с использованием полимеразной цепной реакции 837 работников газодобывающей компании. Были выявлены изменения генов у 358 (42, 8%) пациентов. У 18 (2, 2%) пациентов при дальнейшем наблюдении диагностированы и морфологически подтверждены в онкологических центрах России различные формы рака на 0 (in situ) и I стадиях опухолевого процесса. Временные интервалы от момента выявления изменений некоторых генов до момента диагностики значимых форм рака были различными и составили от 4 до 15 месяцев. Данные пациенты пролечены в онкологических центрах России. Остальной группе пациентов проведена соответствующая терапия. У 34 удалось добиться ингибирования мутаций. Оставшиеся 295 пациентов внесены в группу риска.
Выявление биологических онкомаркеров Большой интерес для современной онкологии представляет использование полимеразной цепной реакции (ПЦР) для определения изменений различных генов в плазме крови с целью раннего выявления злокачественных новообразований различной локализации, профилактики развития рака, а также формирования групп риска для динамического наблюдения. ООО «Центром молекулярно-генетической диагностики Сабирова А. Х. » был проведен профилактический осмотр с использованием полимеразной цепной реакции 837 работников газодобывающей компании. Были выявлены изменения генов у 358 (42, 8%) пациентов. У 18 (2, 2%) пациентов при дальнейшем наблюдении диагностированы и морфологически подтверждены в онкологических центрах России различные формы рака на 0 (in situ) и I стадиях опухолевого процесса. Временные интервалы от момента выявления изменений некоторых генов до момента диагностики значимых форм рака были различными и составили от 4 до 15 месяцев. Данные пациенты пролечены в онкологических центрах России. Остальной группе пациентов проведена соответствующая терапия. У 34 удалось добиться ингибирования мутаций. Оставшиеся 295 пациентов внесены в группу риска.
 Биологические онкомаркеры (ПЦР-реакция) v Общие представления о биологических маркерах. В отличие от классических опухолевых маркеров, выявляемых в сыворотке крови, биологические маркеры (называемые также клеточными, тканевыми или молекулярными) определяются непосредственно в опухолевой ткани. Большинство этих маркеров характеризуют биологические особенности опухоли – пролиферативную активность, гормональную чувствительность, выраженность метастазирования. v Биологические маркеры нашли реальное применение преимущественно при раке молочной железы (РМЖ); именно при этом заболевании накоплен наибольший клинический опыт. Определение биомаркера решает две практические задачи: 1) выявление среди больных ранними стадиями заболевания группы повышенного риска прогрессирования опухоли, требующей дополнительного обследования и/или лечения; 2) оценка индивидуальной чувствительности к проводимой или планируемой терапии.
Биологические онкомаркеры (ПЦР-реакция) v Общие представления о биологических маркерах. В отличие от классических опухолевых маркеров, выявляемых в сыворотке крови, биологические маркеры (называемые также клеточными, тканевыми или молекулярными) определяются непосредственно в опухолевой ткани. Большинство этих маркеров характеризуют биологические особенности опухоли – пролиферативную активность, гормональную чувствительность, выраженность метастазирования. v Биологические маркеры нашли реальное применение преимущественно при раке молочной железы (РМЖ); именно при этом заболевании накоплен наибольший клинический опыт. Определение биомаркера решает две практические задачи: 1) выявление среди больных ранними стадиями заболевания группы повышенного риска прогрессирования опухоли, требующей дополнительного обследования и/или лечения; 2) оценка индивидуальной чувствительности к проводимой или планируемой терапии.
 Биологические онкомаркеры v В регуляции пролиферации клеток рака молочной железы участвуют различные факторы роста. v К числу важнейших относятся пептиды группы эпидермального фактора роста (ЭФР, a-трасформирующий фактор роста, амфирегулин и др. ). v Показано, что наличие в опухоли молочной железы рецепторов эпидермального фактора роста (РЭФР), в особенности, в отсутствии рецепторов стероидных гормонов, свидетельствует о неблагоприятном прогнозе заболевания, даже на ранних стадиях, а также о резистентности к эндокринной терапии.
Биологические онкомаркеры v В регуляции пролиферации клеток рака молочной железы участвуют различные факторы роста. v К числу важнейших относятся пептиды группы эпидермального фактора роста (ЭФР, a-трасформирующий фактор роста, амфирегулин и др. ). v Показано, что наличие в опухоли молочной железы рецепторов эпидермального фактора роста (РЭФР), в особенности, в отсутствии рецепторов стероидных гормонов, свидетельствует о неблагоприятном прогнозе заболевания, даже на ранних стадиях, а также о резистентности к эндокринной терапии.
 Онкомаркёры Связанные с опухолью маркёры, или онкомаркёры, — вещества, повышение концентрации которых в биологических жидкостях (крови или моче) ассоциируется с наличием злокачественной опухоли и/или отражает степень её распространения и эффект проводимого лечения. В большинстве случаев онкомаркёры — сложные белки (гликопротеины или липопротеины), синтезируемые опухолевыми или окружающими опухоль нормальными клетками. В клинической практике широко применяют определение приблизительно 20 онкомаркёров (чаше радиоиммунологическим и иммуноферментным методами). v Рак МЖ – пролактин, эстрадиол v Опухоль яичек – хорионический гонадотропин
Онкомаркёры Связанные с опухолью маркёры, или онкомаркёры, — вещества, повышение концентрации которых в биологических жидкостях (крови или моче) ассоциируется с наличием злокачественной опухоли и/или отражает степень её распространения и эффект проводимого лечения. В большинстве случаев онкомаркёры — сложные белки (гликопротеины или липопротеины), синтезируемые опухолевыми или окружающими опухоль нормальными клетками. В клинической практике широко применяют определение приблизительно 20 онкомаркёров (чаше радиоиммунологическим и иммуноферментным методами). v Рак МЖ – пролактин, эстрадиол v Опухоль яичек – хорионический гонадотропин
 Лучевая диагностика 1) ранняя (доклиническая) диагностика новообразований или скрининг онкологических заболеваний; 2) оценка патологических изменений органов и тканей при использовании неинвазивных лучевых технологий; 2. 1. диагностика и дифференциальная диагностика выявленных патологических изменений, в частности онкологических и не онкологических заболеваний, определение анатомических и функциональных особенностей патологического процесса; 2. 2. стадирование злокачественных опухолей, включая традиционную оценку распространенности первичной опухоли, метастазов в регионарные лимфатические узлы и наличие отдаленных метастазов; 2. 3. оценка результатов хирургического, лекарственного и лучевого лечения, включая как изменение собственно опухолевой ткани, так и возникающие в ходе лечения осложнения или реакции; 2. 4. динамическое наблюдение за больными в отдаленные сроки после лечения; 3) интервенционные радиологические процедуры, т. е. малоинвазивные лечебные и диагностические мероприятия под контролем различных лучевых технологий.
Лучевая диагностика 1) ранняя (доклиническая) диагностика новообразований или скрининг онкологических заболеваний; 2) оценка патологических изменений органов и тканей при использовании неинвазивных лучевых технологий; 2. 1. диагностика и дифференциальная диагностика выявленных патологических изменений, в частности онкологических и не онкологических заболеваний, определение анатомических и функциональных особенностей патологического процесса; 2. 2. стадирование злокачественных опухолей, включая традиционную оценку распространенности первичной опухоли, метастазов в регионарные лимфатические узлы и наличие отдаленных метастазов; 2. 3. оценка результатов хирургического, лекарственного и лучевого лечения, включая как изменение собственно опухолевой ткани, так и возникающие в ходе лечения осложнения или реакции; 2. 4. динамическое наблюдение за больными в отдаленные сроки после лечения; 3) интервенционные радиологические процедуры, т. е. малоинвазивные лечебные и диагностические мероприятия под контролем различных лучевых технологий.
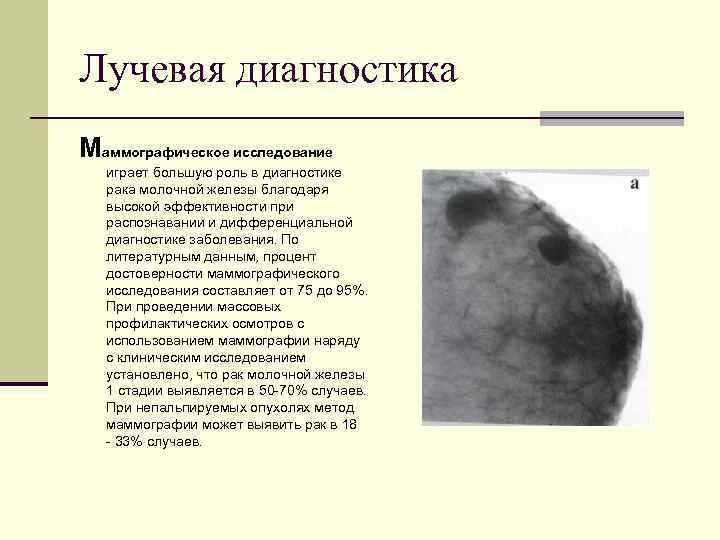 Лучевая диагностика Маммографическое исследование играет большую роль в диагностике рака молочной железы благодаря высокой эффективности при распознавании и дифференциальной диагностике заболевания. По литературным данным, процент достоверности маммографического исследования составляет от 75 до 95%. При проведении массовых профилактических осмотров с использованием маммографии наряду с клиническим исследованием установлено, что рак молочной железы 1 стадии выявляется в 50 -70% случаев. При непальпируемых опухолях метод маммографии может выявить рак в 18 - 33% случаев.
Лучевая диагностика Маммографическое исследование играет большую роль в диагностике рака молочной железы благодаря высокой эффективности при распознавании и дифференциальной диагностике заболевания. По литературным данным, процент достоверности маммографического исследования составляет от 75 до 95%. При проведении массовых профилактических осмотров с использованием маммографии наряду с клиническим исследованием установлено, что рак молочной железы 1 стадии выявляется в 50 -70% случаев. При непальпируемых опухолях метод маммографии может выявить рак в 18 - 33% случаев.
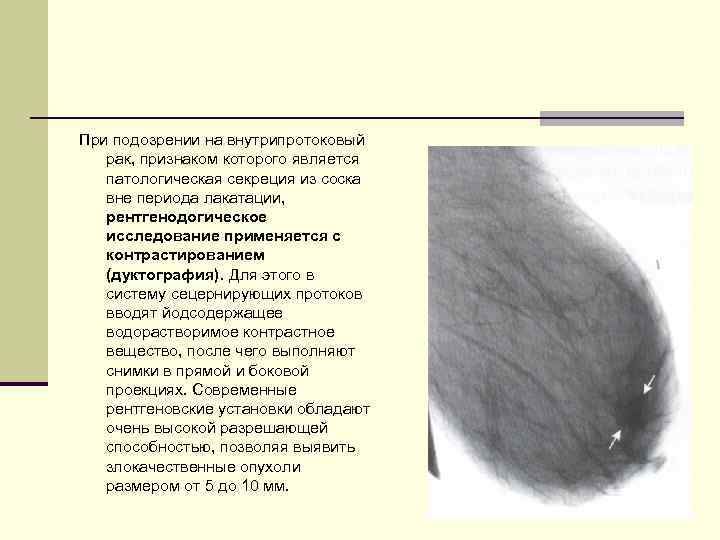 При подозрении на внутрипротоковый рак, признаком которого является патологическая секреция из соска вне периода лакатации, рентгенодогическое исследование применяется с контрастированием (дуктография). Для этого в систему сецернирующих протоков вводят йодсодержащее водорастворимое контрастное вещество, после чего выполняют снимки в прямой и боковой проекциях. Cовременные рентгеновские установки обладают очень высокой разрешающей способностью, позволяя выявить злокачественные опухоли размером от 5 до 10 мм.
При подозрении на внутрипротоковый рак, признаком которого является патологическая секреция из соска вне периода лакатации, рентгенодогическое исследование применяется с контрастированием (дуктография). Для этого в систему сецернирующих протоков вводят йодсодержащее водорастворимое контрастное вещество, после чего выполняют снимки в прямой и боковой проекциях. Cовременные рентгеновские установки обладают очень высокой разрешающей способностью, позволяя выявить злокачественные опухоли размером от 5 до 10 мм.
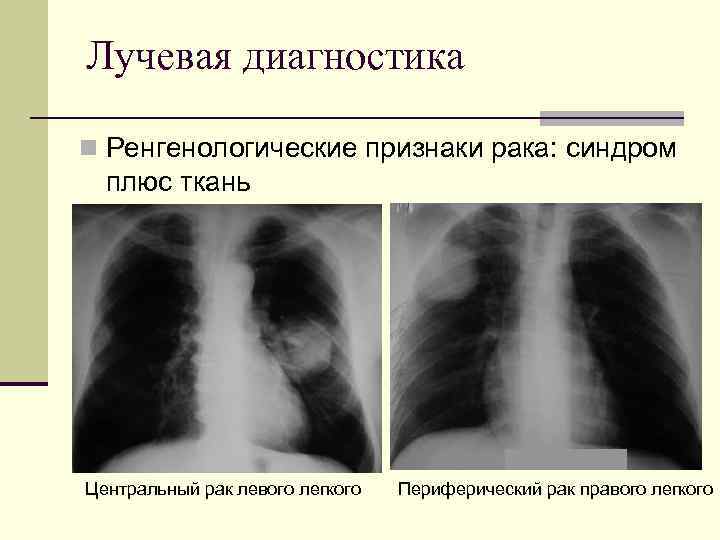 Лучевая диагностика Ренгенологические признаки рака: синдром плюс ткань Центральный рак левого легкого Периферический рак правого легкого
Лучевая диагностика Ренгенологические признаки рака: синдром плюс ткань Центральный рак левого легкого Периферический рак правого легкого
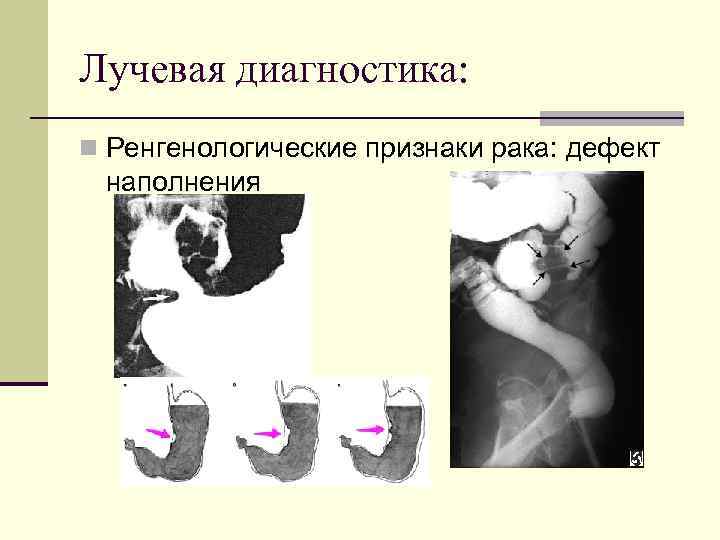 Лучевая диагностика: Ренгенологические признаки рака: дефект наполнения
Лучевая диагностика: Ренгенологические признаки рака: дефект наполнения
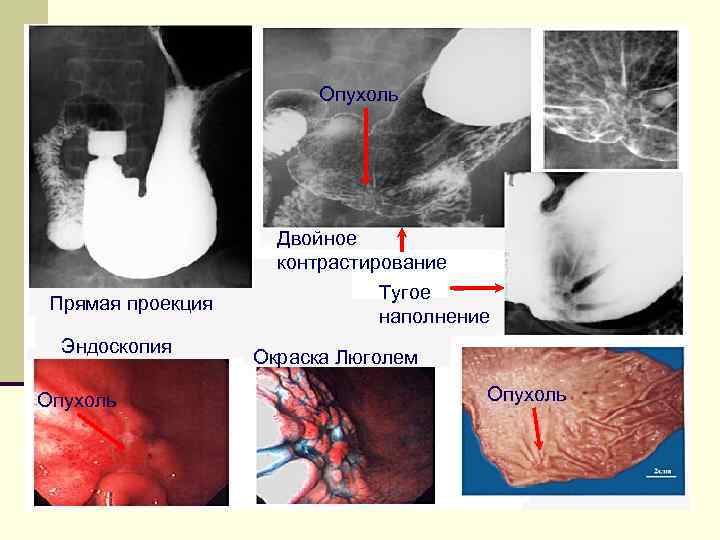 Опухоль Прямая проекция Эндоскопия Опухоль Двойное контрастирование Тугое наполнение Окраска Люголем Опухоль
Опухоль Прямая проекция Эндоскопия Опухоль Двойное контрастирование Тугое наполнение Окраска Люголем Опухоль
 ПЭТ v Позитро нно-эмиссио нная томогра фия (позитронная эмиссионная томография, сокращ. ПЭТ), двухфотонная эмиссионная томография — v Позитронно-эмиссионная томография — это развивающийся диагностический и исследовательский метод ядерной медицины. v В основе этого метода лежит возможность при помощи специального ПЭТсканера отслеживать распределение в организме биологически активных соединений, меченных позитрон-излучающими радиоизотопами. v Потенциал ПЭТ в значительной степени определяется арсеналом доступных меченых соединений — радиофармпрепаратов (РФП). v Именно выбор подходящего РФП позволяет изучать с помощью ПЭТ такие разные процессы, как метаболизм, транспорт веществ, лигандрецепторные взаимодействия, экспрессию генов и т. д. v чувствительность – 100%; специфичность – 69%; точность – 95%; прогностичность положительного результата – 90%; отрицательного результата – 100%.
ПЭТ v Позитро нно-эмиссио нная томогра фия (позитронная эмиссионная томография, сокращ. ПЭТ), двухфотонная эмиссионная томография — v Позитронно-эмиссионная томография — это развивающийся диагностический и исследовательский метод ядерной медицины. v В основе этого метода лежит возможность при помощи специального ПЭТсканера отслеживать распределение в организме биологически активных соединений, меченных позитрон-излучающими радиоизотопами. v Потенциал ПЭТ в значительной степени определяется арсеналом доступных меченых соединений — радиофармпрепаратов (РФП). v Именно выбор подходящего РФП позволяет изучать с помощью ПЭТ такие разные процессы, как метаболизм, транспорт веществ, лигандрецепторные взаимодействия, экспрессию генов и т. д. v чувствительность – 100%; специфичность – 69%; точность – 95%; прогностичность положительного результата – 90%; отрицательного результата – 100%.
 ПЭТ На сегодняшний день в ПЭТ в основном применяются позитрон-излучающие изотопы элементов второго периода периодической системы: Углерод -11(T½= 20, 4 мин. ) Азот-13 (T½=9, 96 мин. ) Кислород-15(T½=2, 03 мин. ) Фтор-18 (T½=109, 8 мин. )
ПЭТ На сегодняшний день в ПЭТ в основном применяются позитрон-излучающие изотопы элементов второго периода периодической системы: Углерод -11(T½= 20, 4 мин. ) Азот-13 (T½=9, 96 мин. ) Кислород-15(T½=2, 03 мин. ) Фтор-18 (T½=109, 8 мин. )
 Результат ПЭТ-исследования. 1. Выявление рецидивной опухоли верхушки левого легкого
Результат ПЭТ-исследования. 1. Выявление рецидивной опухоли верхушки левого легкого
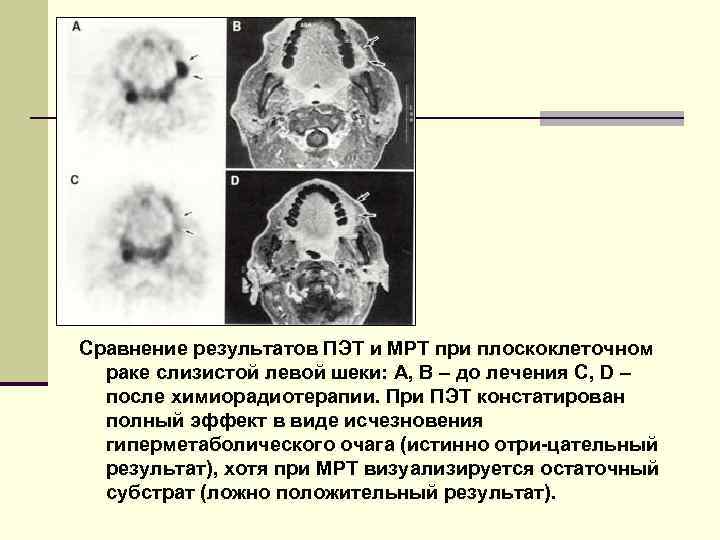 Сравнение результатов ПЭТ и МРТ при плоскоклеточном раке слизистой левой шеки: A, B – до лечения C, D – после химиорадиотерапии. При ПЭТ констатирован полный эффект в виде исчезновения гиперметаболического очага (истинно отри-цательный результат), хотя при МРТ визуализируется остаточный субстрат (ложно положительный результат).
Сравнение результатов ПЭТ и МРТ при плоскоклеточном раке слизистой левой шеки: A, B – до лечения C, D – после химиорадиотерапии. При ПЭТ констатирован полный эффект в виде исчезновения гиперметаболического очага (истинно отри-цательный результат), хотя при МРТ визуализируется остаточный субстрат (ложно положительный результат).
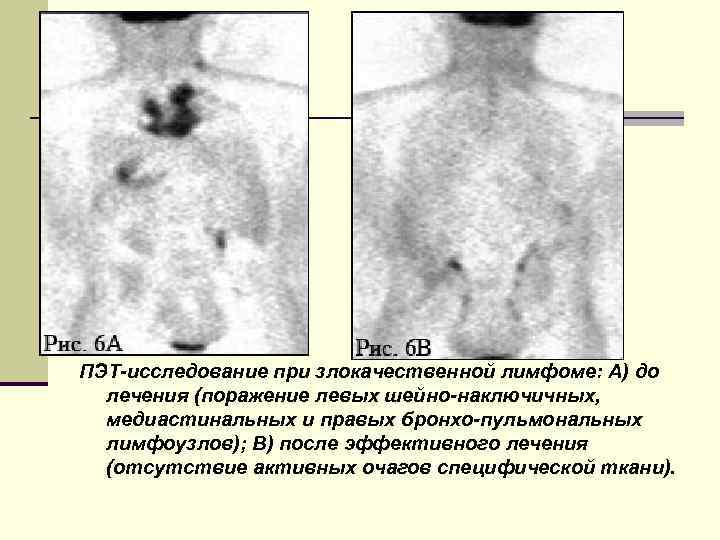 ПЭТ-исследование при злокачественной лимфоме: А) до лечения (поражение левых шейно-наключичных, медиастинальных и правых бронхо-пульмональных лимфоузлов); В) после эффективного лечения (отсутствие активных очагов специфической ткани).
ПЭТ-исследование при злокачественной лимфоме: А) до лечения (поражение левых шейно-наключичных, медиастинальных и правых бронхо-пульмональных лимфоузлов); В) после эффективного лечения (отсутствие активных очагов специфической ткани).
 КТ Томогра фия (греч. τομη — сечение) — метод неразрушающего послойного исследования внутренней структуры объекта посредством его многократного просвечивания в различных пересекающихся направлениях.
КТ Томогра фия (греч. τομη — сечение) — метод неразрушающего послойного исследования внутренней структуры объекта посредством его многократного просвечивания в различных пересекающихся направлениях.
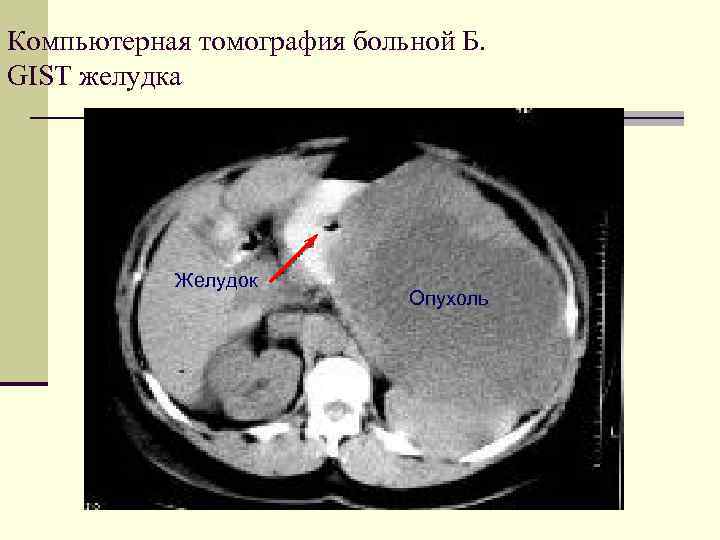 Компьютерная томография больной Б. GIST желудка Желудок Опухоль
Компьютерная томография больной Б. GIST желудка Желудок Опухоль
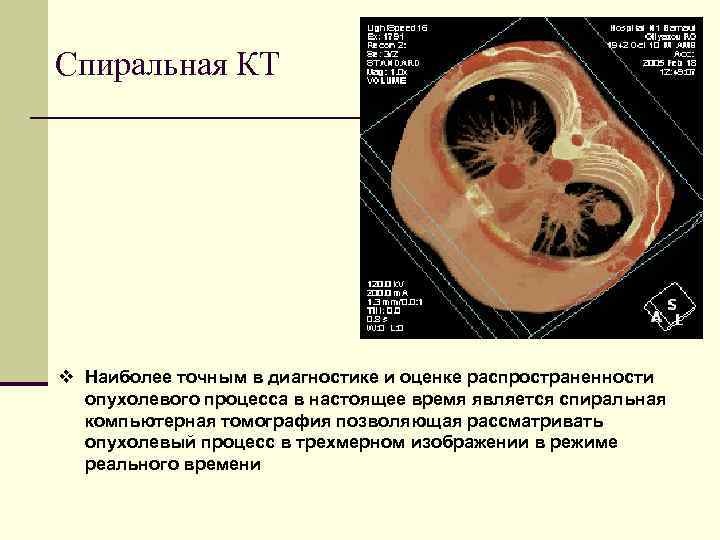 Спиральная КТ v Наиболее точным в диагностике и оценке распространенности опухолевого процесса в настоящее время является спиральная компьютерная томография позволяющая рассматривать опухолевый процесс в трехмерном изображении в режиме реального времени
Спиральная КТ v Наиболее точным в диагностике и оценке распространенности опухолевого процесса в настоящее время является спиральная компьютерная томография позволяющая рассматривать опухолевый процесс в трехмерном изображении в режиме реального времени
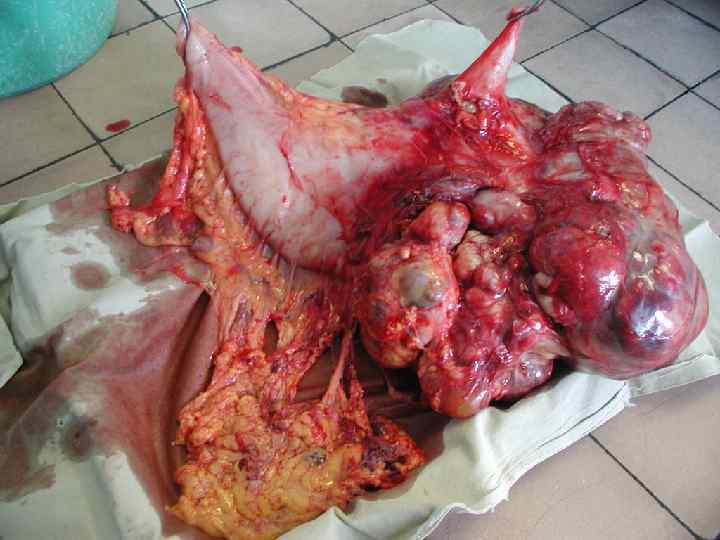
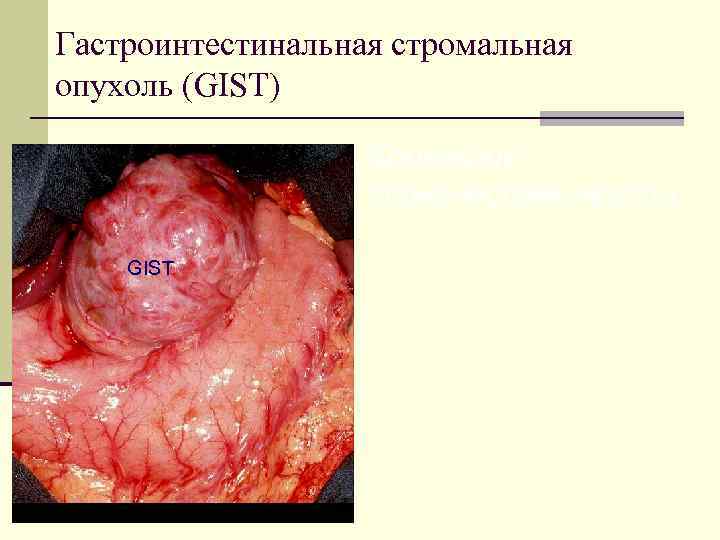 Гастроинтестинальная стромальная опухоль (GIST) Критерии злокачественности: GIST
Гастроинтестинальная стромальная опухоль (GIST) Критерии злокачественности: GIST
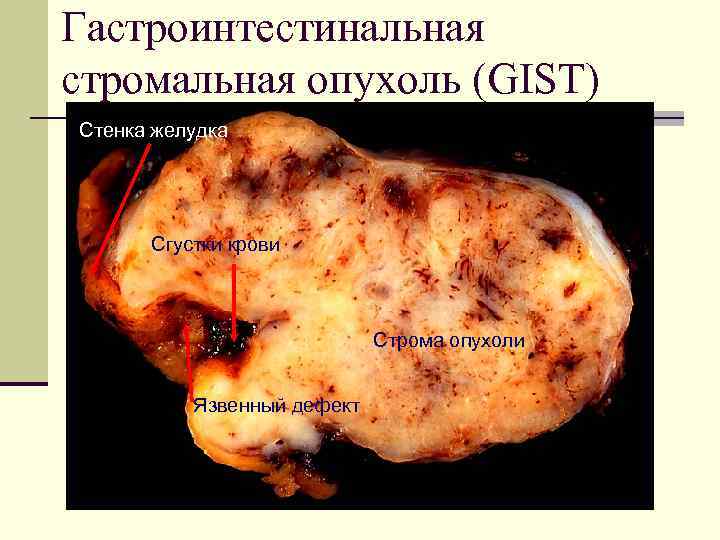 Гастроинтестинальная стромальная опухоль (GIST) Стенка желудка Сгустки крови Строма опухоли Язвенный дефект
Гастроинтестинальная стромальная опухоль (GIST) Стенка желудка Сгустки крови Строма опухоли Язвенный дефект
 Бронхографическая картина при раке легкого Эндоскопическое исследование Бронхографически при раке удается установить ампутацию бронха, его сужение с узурированным неровным контуром, дефект наполнения бронха, супра- и ретростеническое расширение его
Бронхографическая картина при раке легкого Эндоскопическое исследование Бронхографически при раке удается установить ампутацию бронха, его сужение с узурированным неровным контуром, дефект наполнения бронха, супра- и ретростеническое расширение его
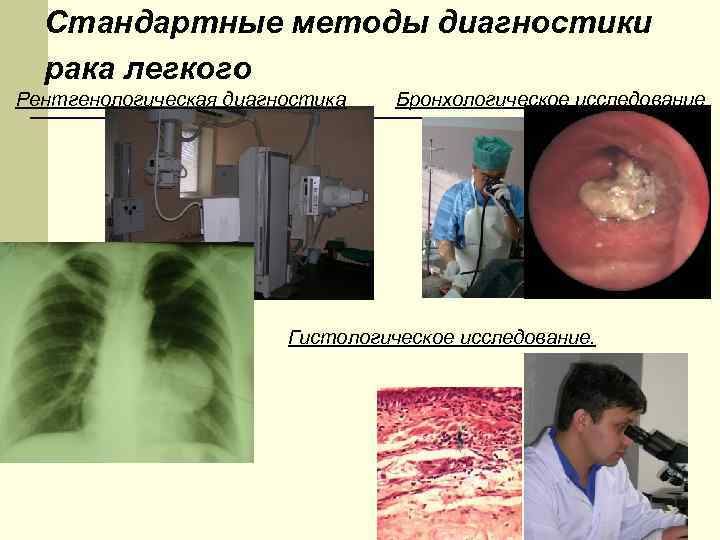 Стандартные методы диагностики рака легкого Рентгенологическая диагностика Бронхологическое исследование Гистологическое исследование.
Стандартные методы диагностики рака легкого Рентгенологическая диагностика Бронхологическое исследование Гистологическое исследование.
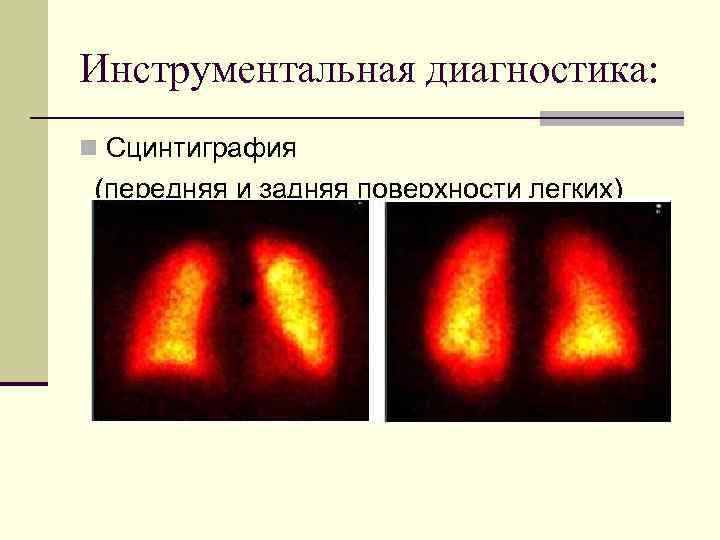 Инструментальная диагностика: Сцинтиграфия (передняя и задняя поверхности легких)
Инструментальная диагностика: Сцинтиграфия (передняя и задняя поверхности легких)
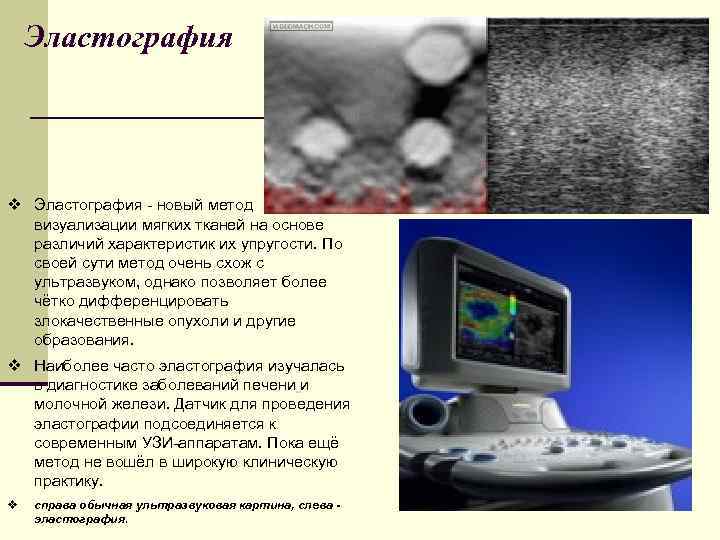 Эластография v Эластография - новый метод визуализации мягких тканей на основе различий характеристик их упругости. По своей сути метод очень схож с ультразвуком, однако позволяет более чётко дифференцировать злокачественные опухоли и другие образования. v Наиболее часто эластография изучалась в диагностике заболеваний печени и молочной желези. Датчик для проведения эластографии подсоединяется к современным УЗИ-аппаратам. Пока ещё метод не вошёл в широкую клиническую практику. v справа обычная ультразвуковая картина, слева эластография.
Эластография v Эластография - новый метод визуализации мягких тканей на основе различий характеристик их упругости. По своей сути метод очень схож с ультразвуком, однако позволяет более чётко дифференцировать злокачественные опухоли и другие образования. v Наиболее часто эластография изучалась в диагностике заболеваний печени и молочной желези. Датчик для проведения эластографии подсоединяется к современным УЗИ-аппаратам. Пока ещё метод не вошёл в широкую клиническую практику. v справа обычная ультразвуковая картина, слева эластография.
 Эндоскопические методы
Эндоскопические методы
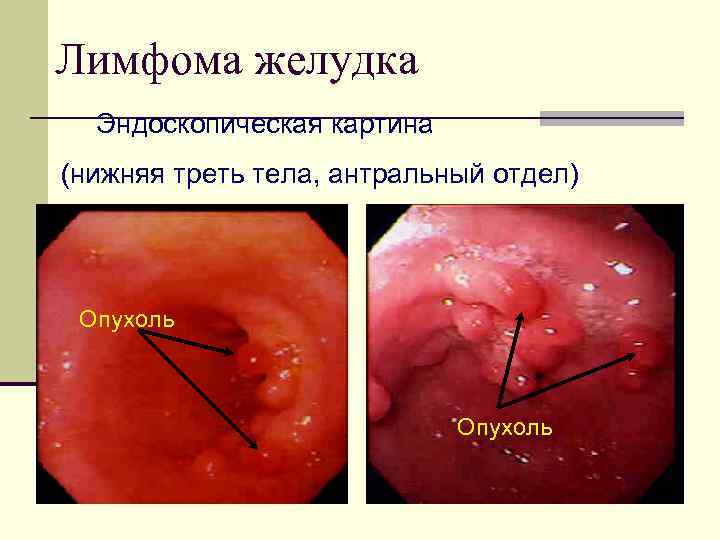 Лимфома желудка Эндоскопическая картина (нижняя треть тела, антральный отдел) Опухоль
Лимфома желудка Эндоскопическая картина (нижняя треть тела, антральный отдел) Опухоль
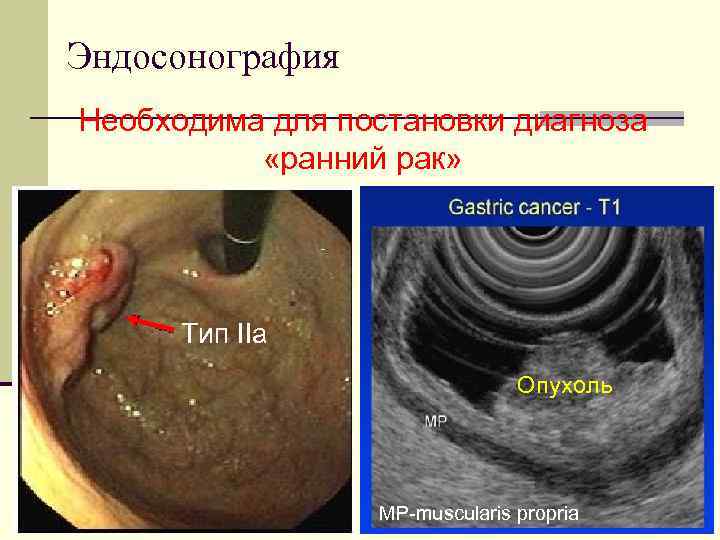 Эндосонография Необходима для постановки диагноза «ранний рак» Тип IIa Опухоль MP-muscularis propria
Эндосонография Необходима для постановки диагноза «ранний рак» Тип IIa Опухоль MP-muscularis propria
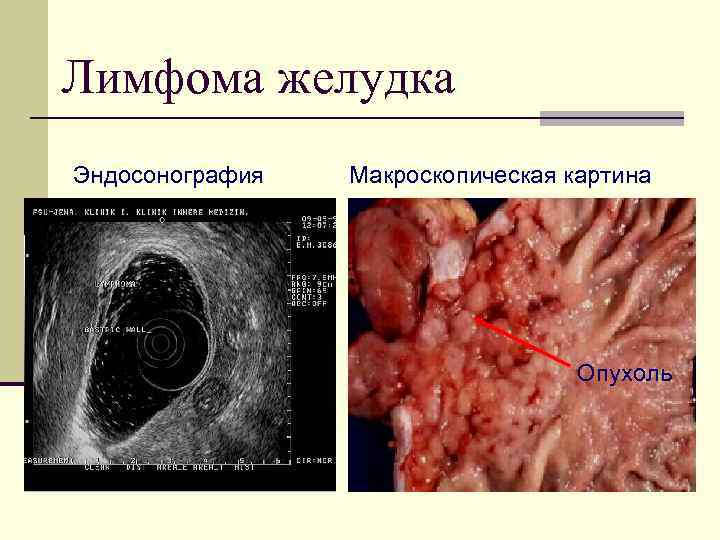 Лимфома желудка Эндосонография Макроскопическая картина Опухоль
Лимфома желудка Эндосонография Макроскопическая картина Опухоль
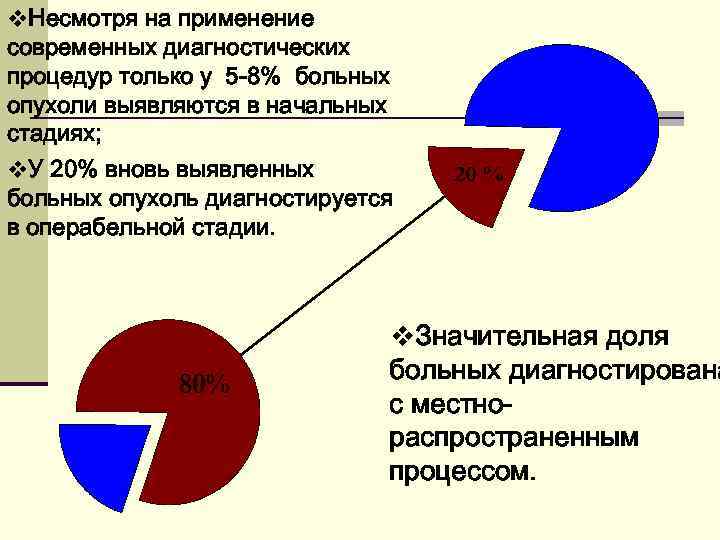 v. Несмотря на применение современных диагностических процедур только у 5 -8% больных опухоли выявляются в начальных стадиях; v. У 20% вновь выявленных больных опухоль диагностируется в операбельной стадии. v. Значительная доля больных диагностирована с местнораспространенным процессом.
v. Несмотря на применение современных диагностических процедур только у 5 -8% больных опухоли выявляются в начальных стадиях; v. У 20% вновь выявленных больных опухоль диагностируется в операбельной стадии. v. Значительная доля больных диагностирована с местнораспространенным процессом.
 Принципы лечения опухолей Хирургический Лучевой Химиотерапевтический
Принципы лечения опухолей Хирургический Лучевой Химиотерапевтический
 Комбинированное и комплексное лечение v Комбинированное лечение – когда сочетают два метода лечения. v Комплексное - при сочетании трёх и более методов лечения. Показания к тому или иному способу лечения или их комбинацию устанавливают в зависимости от стадии опухоли, её локализации и гистологической структуры.
Комбинированное и комплексное лечение v Комбинированное лечение – когда сочетают два метода лечения. v Комплексное - при сочетании трёх и более методов лечения. Показания к тому или иному способу лечения или их комбинацию устанавливают в зависимости от стадии опухоли, её локализации и гистологической структуры.
 Лечение доброкачественных опухолей При доброкачественных образованиях важным является вопрос о показаниях к операции, т. к. доброкачественные опухоли, не несущие в себе угрозы жизни пациента, не всегда должны быть обязательно удалены. При доброкачественных образованиях операция необходима при наличии: v Постояноой травматизации опухоли; v Нарушение функции органа; v До операции нет абсолютной уверенности в том, что опухоль не является злокачественной; v Косметические дефекты. Принципы хирургического лечения При хирургическом лечении опухоли понимают полное её удаление в пределах здоровых тканей. При этом образование должно быть удалено целиком в месте с капсулой, если такая имеется. Операция полностью излечивает пациента.
Лечение доброкачественных опухолей При доброкачественных образованиях важным является вопрос о показаниях к операции, т. к. доброкачественные опухоли, не несущие в себе угрозы жизни пациента, не всегда должны быть обязательно удалены. При доброкачественных образованиях операция необходима при наличии: v Постояноой травматизации опухоли; v Нарушение функции органа; v До операции нет абсолютной уверенности в том, что опухоль не является злокачественной; v Косметические дефекты. Принципы хирургического лечения При хирургическом лечении опухоли понимают полное её удаление в пределах здоровых тканей. При этом образование должно быть удалено целиком в месте с капсулой, если такая имеется. Операция полностью излечивает пациента.
 Принципы хирургического лечения злокачественных образований Радикальные операции 1 Абластика – комплекс мер по предупреждению распространения во время операции опухолевых клеток. 2 Антибластика – комплекс мер по уничтожению во время операции отдельных клеток опухоли, оторвавшихся от основной её массы. Выделяют: физическую – использование электроножа, лазера, облучение опухоли перед операцией и в раннем послеоперационном периоде; и химическую – обработка раневой поверхности после удаления опухоли 70 о спиртом, в/в введение противоопухолевых химиопрепаратов на операционном столе, регионарная перфузия противоопухолевыми химиотерапевтическими препаратами. 3. Зональность – при операции по поводу злокачественного образования необходимо не только удалить его, но и убрать всю зону, в которой могут находиться отдельные раковые клетки. 4. Футлярность – лимфатические сосуды и узлы, по которым возможно распространение опухолевых клеток, располагаются в клетчаточных пространствах, поэтому необходимо удаление клетчатки всего фасциального футляра вместе с фасцией.
Принципы хирургического лечения злокачественных образований Радикальные операции 1 Абластика – комплекс мер по предупреждению распространения во время операции опухолевых клеток. 2 Антибластика – комплекс мер по уничтожению во время операции отдельных клеток опухоли, оторвавшихся от основной её массы. Выделяют: физическую – использование электроножа, лазера, облучение опухоли перед операцией и в раннем послеоперационном периоде; и химическую – обработка раневой поверхности после удаления опухоли 70 о спиртом, в/в введение противоопухолевых химиопрепаратов на операционном столе, регионарная перфузия противоопухолевыми химиотерапевтическими препаратами. 3. Зональность – при операции по поводу злокачественного образования необходимо не только удалить его, но и убрать всю зону, в которой могут находиться отдельные раковые клетки. 4. Футлярность – лимфатические сосуды и узлы, по которым возможно распространение опухолевых клеток, располагаются в клетчаточных пространствах, поэтому необходимо удаление клетчатки всего фасциального футляра вместе с фасцией.
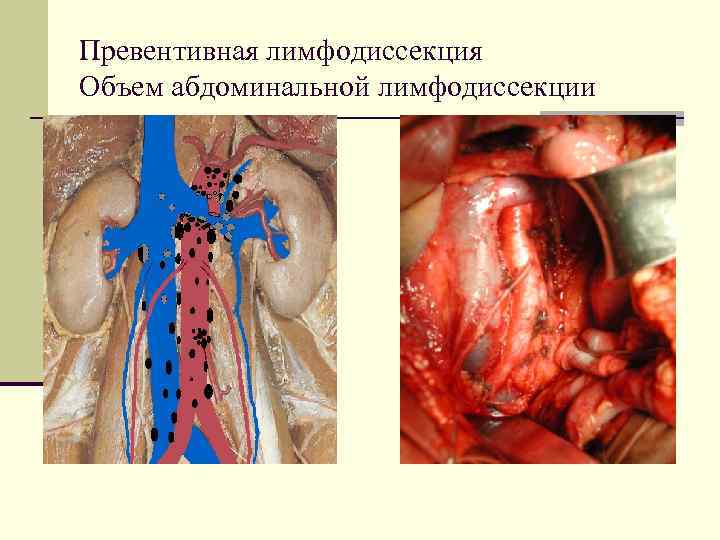 Превентивная лимфодиссекция Объем абдоминальной лимфодиссекции
Превентивная лимфодиссекция Объем абдоминальной лимфодиссекции
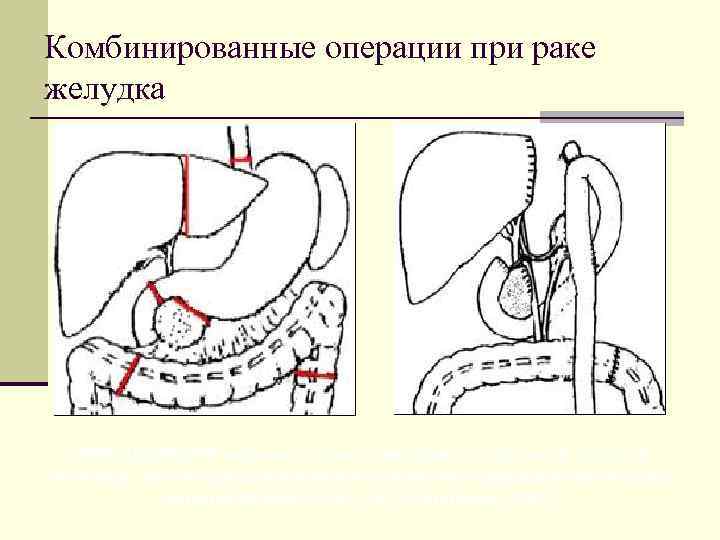 Комбинированные операции при раке желудка Эвисцерация верхнего левого квадранта брюшной полости по поводу местно-распространенного диффузно-инфильтративного рака желудка (Borrmann IV type). H. Furukawa, 2003.
Комбинированные операции при раке желудка Эвисцерация верхнего левого квадранта брюшной полости по поводу местно-распространенного диффузно-инфильтративного рака желудка (Borrmann IV type). H. Furukawa, 2003.
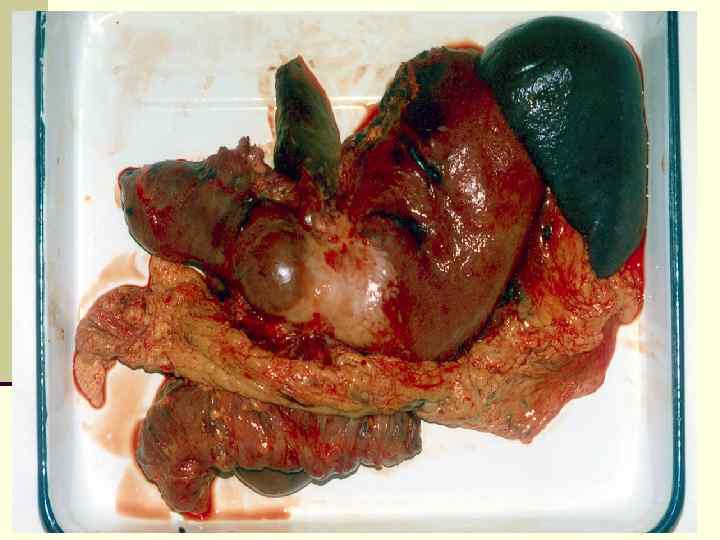
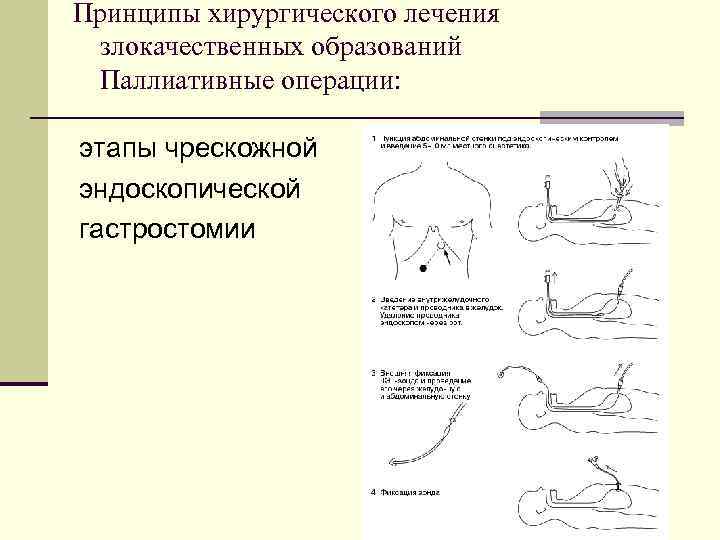 Принципы хирургического лечения злокачественных образований Паллиативные операции: этапы чрескожной эндоскопической гастростомии
Принципы хирургического лечения злокачественных образований Паллиативные операции: этапы чрескожной эндоскопической гастростомии
 ИСПОЛЬЗОВАНИЕ ДОПОЛНИТЕЛЬНЫХ ФИЗИЧЕСКИХ МЕТОДОВ электрохирургия, криохирургию, лазерохирургия. используют как на этапах стандартных операций, так и самостоятельно. Особенно широко эти методы применяют при наружном расположении злокачественных новообразований. • Электрохирургические операции проводят в двух режимах: электроэксцизия и электрокоагуляция. В первом случае специальным электроножом иссекают ткани в зоне патологического образования, во втором — сжигают ткань опухоли (обычно в виде паллиативной процедуры). • Криохирургия — метод глубокого замораживания ткани опухоли, что приводит к её некрозу и рассасыванию. • С помощью лазера получают концентрированные пучки света, энергию которых можно регулировать и точно рассчитывать глубину коагуляции ткани по линии разреза или в зоне очага опухоли. В онкологических клиниках чаще используют СО 2 -лазер (10, 6 мкм) и лазеры (1, 06 мкм) с непрерывным режимом излучения.
ИСПОЛЬЗОВАНИЕ ДОПОЛНИТЕЛЬНЫХ ФИЗИЧЕСКИХ МЕТОДОВ электрохирургия, криохирургию, лазерохирургия. используют как на этапах стандартных операций, так и самостоятельно. Особенно широко эти методы применяют при наружном расположении злокачественных новообразований. • Электрохирургические операции проводят в двух режимах: электроэксцизия и электрокоагуляция. В первом случае специальным электроножом иссекают ткани в зоне патологического образования, во втором — сжигают ткань опухоли (обычно в виде паллиативной процедуры). • Криохирургия — метод глубокого замораживания ткани опухоли, что приводит к её некрозу и рассасыванию. • С помощью лазера получают концентрированные пучки света, энергию которых можно регулировать и точно рассчитывать глубину коагуляции ткани по линии разреза или в зоне очага опухоли. В онкологических клиниках чаще используют СО 2 -лазер (10, 6 мкм) и лазеры (1, 06 мкм) с непрерывным режимом излучения.
 ОРГАНОСОХРАНЯЮЩЕЕ ЛЕЧЕНИЕ И РЕКОНСТРУКТИВНО-ПЛАСТИЧЕСКИЕ ОПЕРАЦИИ Реконструктивные операции в основном показаны больным с местнораспространённым раком, при рецидиве опухоли.
ОРГАНОСОХРАНЯЮЩЕЕ ЛЕЧЕНИЕ И РЕКОНСТРУКТИВНО-ПЛАСТИЧЕСКИЕ ОПЕРАЦИИ Реконструктивные операции в основном показаны больным с местнораспространённым раком, при рецидиве опухоли.
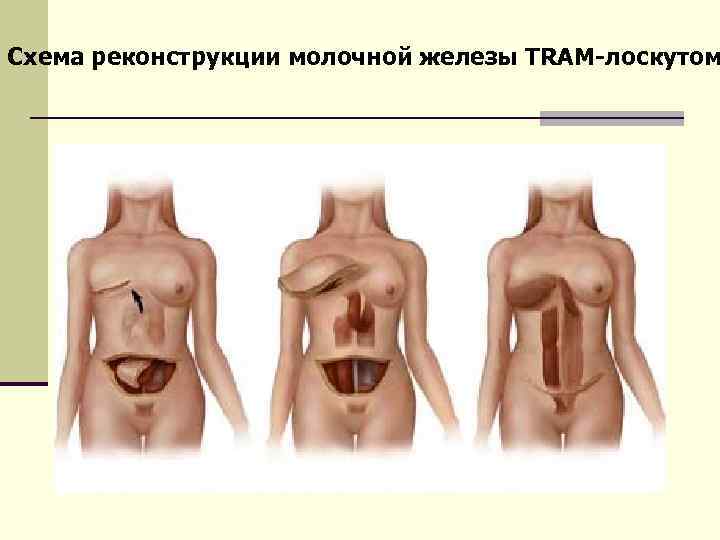 Схема реконструкции молочной железы TRAM-лоскутом
Схема реконструкции молочной железы TRAM-лоскутом
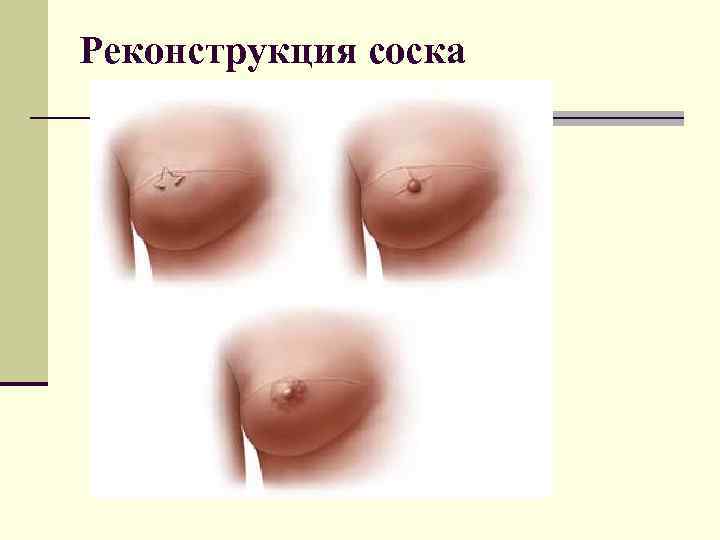 Реконструкция соска
Реконструкция соска
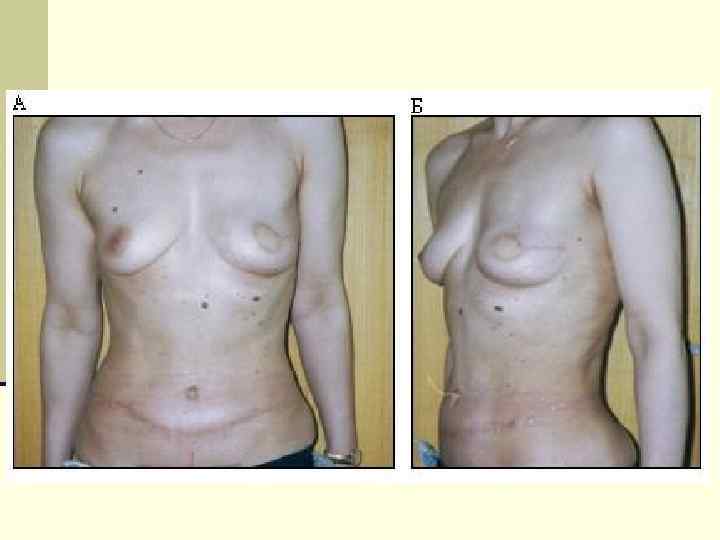
 ПРОФИЛАКТИЧЕСКАЯ ХИРУРГИЯ В последние годы хирургическая онкология оказалась в центре проблемы вторичной профилактики (профилактического лечения). Вопрос о проведении профилактических операций часто возникает при генетически обусловленных онкологических заболеваниях (например, семейном полипозе, синдромах множественной эндокринной неоплазии и др. ), причём он касается не только самого больного, но и его родственников. Важную роль профилактическая хирургия имеет и при ряде предопухолевых заболеваниях (лейкоплакии, крипторхизм, хронический язвенный колит и др. ).
ПРОФИЛАКТИЧЕСКАЯ ХИРУРГИЯ В последние годы хирургическая онкология оказалась в центре проблемы вторичной профилактики (профилактического лечения). Вопрос о проведении профилактических операций часто возникает при генетически обусловленных онкологических заболеваниях (например, семейном полипозе, синдромах множественной эндокринной неоплазии и др. ), причём он касается не только самого больного, но и его родственников. Важную роль профилактическая хирургия имеет и при ряде предопухолевых заболеваниях (лейкоплакии, крипторхизм, хронический язвенный колит и др. ).
 Принципы лучевой терапии основан на том, что быстро размножающиеся клетки опухоли с большей интенсивностью обменных процессов более чувствительны к воздействию ионизирующего изучения. Задача лучевой терапии: уничтожение опухолевого очага с восстановлением на его месте тканей, обладающих нормальными свойствами обмена и роста. Основные способы лучевой терапии: внешнее облучение – используют установки для рентгенотерапии и телегамматерапии; внутриполостное облучение – источник излучения приближен к месту расположения опухоли; внутритканевое облучение – применяют специальные иглы и трубочки с радиоизотопными препаратами, которые хирургическим путём устанавливают в ткани. Осложнения лучевой терапии: местные: реактивный эпидермит, лучевой дерматит, лучевой индуративный отёк, лучевые некротические язвы; общие – общие расстройства, являющиеся проявлением лучевой болезни (слабость, потеря аппетита, тошнота, рвота, нарушения сна и т. д. )
Принципы лучевой терапии основан на том, что быстро размножающиеся клетки опухоли с большей интенсивностью обменных процессов более чувствительны к воздействию ионизирующего изучения. Задача лучевой терапии: уничтожение опухолевого очага с восстановлением на его месте тканей, обладающих нормальными свойствами обмена и роста. Основные способы лучевой терапии: внешнее облучение – используют установки для рентгенотерапии и телегамматерапии; внутриполостное облучение – источник излучения приближен к месту расположения опухоли; внутритканевое облучение – применяют специальные иглы и трубочки с радиоизотопными препаратами, которые хирургическим путём устанавливают в ткани. Осложнения лучевой терапии: местные: реактивный эпидермит, лучевой дерматит, лучевой индуративный отёк, лучевые некротические язвы; общие – общие расстройства, являющиеся проявлением лучевой болезни (слабость, потеря аппетита, тошнота, рвота, нарушения сна и т. д. )
 Принципы химиотерапии Химиотерапия – воздействие на опухоль различными фармакологическими средствами. Наиболее эффективна при системных онкологических заболеваниях (лейкоз, лимфогрануломатоз) и опухоли гормонзависимых органов (рак молочной железы, яичника, предстательной железы и др. ). Группы химиотерапевтических препаратов: vцитостатики; vантиметаболиты; vпротивоопухолевые антибиотики; vиммуномодуляторы; vгормональные препараты
Принципы химиотерапии Химиотерапия – воздействие на опухоль различными фармакологическими средствами. Наиболее эффективна при системных онкологических заболеваниях (лейкоз, лимфогрануломатоз) и опухоли гормонзависимых органов (рак молочной железы, яичника, предстательной железы и др. ). Группы химиотерапевтических препаратов: vцитостатики; vантиметаболиты; vпротивоопухолевые антибиотики; vиммуномодуляторы; vгормональные препараты
 Химиотерапия v Адьювантная v Неадьювантная При планировании комплексного радикального лечения лекарственная терапия может использоваться до применения локального воздействия (неоадъювантная терапия), после применения локального воздействия (адъювантная терапия) или в обоих случаях.
Химиотерапия v Адьювантная v Неадьювантная При планировании комплексного радикального лечения лекарственная терапия может использоваться до применения локального воздействия (неоадъювантная терапия), после применения локального воздействия (адъювантная терапия) или в обоих случаях.
 Основные задачи неоадъювантной терапии: • раннее начато системного воздействия; • уменьшение размеров опухоли; • изучение лекарственного патоморфоза (важно для определения чувствительности опухоли к цитостатикам и оценки целесообразности продолжения терапии теми же препаратами).
Основные задачи неоадъювантной терапии: • раннее начато системного воздействия; • уменьшение размеров опухоли; • изучение лекарственного патоморфоза (важно для определения чувствительности опухоли к цитостатикам и оценки целесообразности продолжения терапии теми же препаратами).
 Показания для назначения адъювантной терапии: v чёткое определение стадии процесса и гистогенеза опухоли; v адъювантную терапию целесообразно проводить при опухолях, для лечения которых существуют высокоактивные препараты; только тогда можно реально улучшить прогноз и, самое главное, увеличить длительность безрецидивного периода и продолжительность жизни. v Адъювантная терапия не является профилактической и должна назначаться в лечебных дозах с применением повторных курсов и соблюдением общепринятых интервалов.
Показания для назначения адъювантной терапии: v чёткое определение стадии процесса и гистогенеза опухоли; v адъювантную терапию целесообразно проводить при опухолях, для лечения которых существуют высокоактивные препараты; только тогда можно реально улучшить прогноз и, самое главное, увеличить длительность безрецидивного периода и продолжительность жизни. v Адъювантная терапия не является профилактической и должна назначаться в лечебных дозах с применением повторных курсов и соблюдением общепринятых интервалов.
 Химиопрепараты v Цитостатики – тормозят размножение опухолевых клеток, угнетая их митотическую активность. К ним относятся 6 циклофосфан, тио. ТЭФ, винбластин, винкристин. v Антиметаболиты – вещества действующие на обменные процессы в опухолевых клетках. Основные препараты: 5 -фторурацил, фторафур (антогонист пиримидина), метотрексат (антогонист фолиевой кислоты), меркаптопурин (антогонист пурина). v Противоопухолевые антибиотики - вещества, вырабатываемые микроорганизмами, прежде всего актиномицетами, обладают противоопухолевым действием. К ним относят: актиномицин, дактиномицин, сарколизин, рубромицин, доксорубицин, карминомицин, митомицин. v Иммуномодуляторы – применяются наиболее широко последнее время, особенно при гипернефроидном раке почки. v Гормональные препараты – применяется при гормонозависимых опухолевидных новообразованиях. Такие препараты: синэстрол, фосфэстерол, диэтилстильбэстрол, метилтестостерон, тестостерона пропионат, тамоксифен торимефен).
Химиопрепараты v Цитостатики – тормозят размножение опухолевых клеток, угнетая их митотическую активность. К ним относятся 6 циклофосфан, тио. ТЭФ, винбластин, винкристин. v Антиметаболиты – вещества действующие на обменные процессы в опухолевых клетках. Основные препараты: 5 -фторурацил, фторафур (антогонист пиримидина), метотрексат (антогонист фолиевой кислоты), меркаптопурин (антогонист пурина). v Противоопухолевые антибиотики - вещества, вырабатываемые микроорганизмами, прежде всего актиномицетами, обладают противоопухолевым действием. К ним относят: актиномицин, дактиномицин, сарколизин, рубромицин, доксорубицин, карминомицин, митомицин. v Иммуномодуляторы – применяются наиболее широко последнее время, особенно при гипернефроидном раке почки. v Гормональные препараты – применяется при гормонозависимых опухолевидных новообразованиях. Такие препараты: синэстрол, фосфэстерол, диэтилстильбэстрол, метилтестостерон, тестостерона пропионат, тамоксифен торимефен).
 Лекарственная терапия — основной метод лечения злокачественных опухолей в стадии генерализации. В зависимости от чувствительности опухоли к тем или иным препаратам может использоваться химиотерапия, гормонотерапия, иммунотерапия или их сочетание.
Лекарственная терапия — основной метод лечения злокачественных опухолей в стадии генерализации. В зависимости от чувствительности опухоли к тем или иным препаратам может использоваться химиотерапия, гормонотерапия, иммунотерапия или их сочетание.
 Противопоказания к проведению ХТ • тяжёлое общее состояние больного; • угнетение кроветворения; • гнойные процессы и распад опухоли; • инфекционные заболевания; • кровохарканье; • инфаркт миокарда; • острое нарушение мозгового кровообращения; • выраженная сердечно-сосудистая недостаточность; • тяжёлое нарушение функции печени и почек; • тяжёлый сахарный диабет.
Противопоказания к проведению ХТ • тяжёлое общее состояние больного; • угнетение кроветворения; • гнойные процессы и распад опухоли; • инфекционные заболевания; • кровохарканье; • инфаркт миокарда; • острое нарушение мозгового кровообращения; • выраженная сердечно-сосудистая недостаточность; • тяжёлое нарушение функции печени и почек; • тяжёлый сахарный диабет.
 Гормонотерапия. Современные подходы к гормонотерапии опухолей включают несколько основных направлений: • снижение уровня гормонов, стимулирующих рост опухоли (непосредственное воздействие на эндокринные железы или через регулирующие их системы); • блокирование стимулирующего действия гормонов на клетки опухоли (воздействие на клетки-мишени); • повышение чувствительности клеток опухоли к цитостатикам и использование гормонов в качестве носителей химиотерапевтических препаратов. Гормонотерапия высокоэффективна при раке молочной железы, раке предстательной железы, раке эндометрия.
Гормонотерапия. Современные подходы к гормонотерапии опухолей включают несколько основных направлений: • снижение уровня гормонов, стимулирующих рост опухоли (непосредственное воздействие на эндокринные железы или через регулирующие их системы); • блокирование стимулирующего действия гормонов на клетки опухоли (воздействие на клетки-мишени); • повышение чувствительности клеток опухоли к цитостатикам и использование гормонов в качестве носителей химиотерапевтических препаратов. Гормонотерапия высокоэффективна при раке молочной железы, раке предстательной железы, раке эндометрия.
 Наиболее часто в клинической практике используются следующие группы гормональных препаратов и антигормонов: • антиэстрогены (тамоксифен. фулвестрант); • ингибиторы ароматазы (анастрозол, летрозол. эксеместан); • прогестины (медроксипрогестерон); • агонисты гонадотропин-рилизинг гормона (гозерелин. бусерелин): • антиандрогены (бикалутамил. флютамид): • глюкокортикоиды, андрогены. эстрогены.
Наиболее часто в клинической практике используются следующие группы гормональных препаратов и антигормонов: • антиэстрогены (тамоксифен. фулвестрант); • ингибиторы ароматазы (анастрозол, летрозол. эксеместан); • прогестины (медроксипрогестерон); • агонисты гонадотропин-рилизинг гормона (гозерелин. бусерелин): • антиандрогены (бикалутамил. флютамид): • глюкокортикоиды, андрогены. эстрогены.
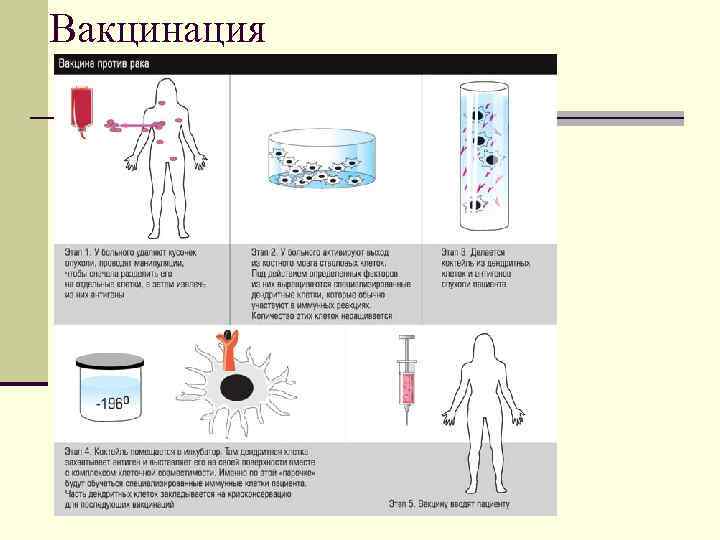 Вакцинация
Вакцинация
 Профилактика ЗН
Профилактика ЗН
 Скрининговые методы исследования Маммография. Достоверное снижение смертности от рака молочной железы среди женщин старше 50 лет в среднем на 30% получены при исследованиях проведенных в США, Канаде, Швеции и Шотландии. [1] Цитология мазка с шейки матки. Достоверное снижение смертности от рака шейки матки в среднем на 80% получены при исследованиях проведенных в Финляндии, Исландии, Швеции, Дании, и Норвегии. [1] Тест на скрытую кровь в кале. Достоверное снижение смертности от рака толстой/прямой кишки в среднем на 15% получены при исследованиях, проведенных в штате Миннесота (США), Англии, Финляндии. [1]
Скрининговые методы исследования Маммография. Достоверное снижение смертности от рака молочной железы среди женщин старше 50 лет в среднем на 30% получены при исследованиях проведенных в США, Канаде, Швеции и Шотландии. [1] Цитология мазка с шейки матки. Достоверное снижение смертности от рака шейки матки в среднем на 80% получены при исследованиях проведенных в Финляндии, Исландии, Швеции, Дании, и Норвегии. [1] Тест на скрытую кровь в кале. Достоверное снижение смертности от рака толстой/прямой кишки в среднем на 15% получены при исследованиях, проведенных в штате Миннесота (США), Англии, Финляндии. [1]
 Скрининговые методы исследования Тест на ПСА - простой, дешевый, приемлемый, легко доступный и весьма распространенный среди пациентов и врачей. В Милане (Италия), где отсутствует реклама или поощрение скрининга рака предстательной железы, было подсчитано, что 26, 9% мужчин в возрасте 40 и более лет без наличия в анамнезе рака и 34% мужчин в возрасте 50 лет и старше обследуются с помощью теста на ПСА в течение двух лет.
Скрининговые методы исследования Тест на ПСА - простой, дешевый, приемлемый, легко доступный и весьма распространенный среди пациентов и врачей. В Милане (Италия), где отсутствует реклама или поощрение скрининга рака предстательной железы, было подсчитано, что 26, 9% мужчин в возрасте 40 и более лет без наличия в анамнезе рака и 34% мужчин в возрасте 50 лет и старше обследуются с помощью теста на ПСА в течение двух лет.
 Благодарю за внимание! Рак излечим! На ранних стадиях
Благодарю за внимание! Рак излечим! На ранних стадиях


