Термодинамика лк 5-6.ppt
- Количество слайдов: 26
 Основы химической термодинамики Лекция 5 -6
Основы химической термодинамики Лекция 5 -6
 Термодинамика –это наука о превращениях различных видов энергии друг в друга. Все химические реакции сопровождаются энергетическими эффектами. Термодинамика позволяет определить: 1. Количество поглощенной или выделенной энергии в ходе химической реакции; 2. Возможность самопроизвольного протекания химической реакции без эксперимента.
Термодинамика –это наука о превращениях различных видов энергии друг в друга. Все химические реакции сопровождаются энергетическими эффектами. Термодинамика позволяет определить: 1. Количество поглощенной или выделенной энергии в ходе химической реакции; 2. Возможность самопроизвольного протекания химической реакции без эксперимента.
 1. Первый закон термодинамики. Основные понятия n Теплота Q, подводимая к термодинамической системе, расходуется на изменение внутренней энергии ∆U и на совершение работы А Q = ∆U + А
1. Первый закон термодинамики. Основные понятия n Теплота Q, подводимая к термодинамической системе, расходуется на изменение внутренней энергии ∆U и на совершение работы А Q = ∆U + А
 Внутренняя энергия U – это энергия частиц, составляющих данную систему. Внутренняя энергия идеального газа зависит только от его температуры, поэтому с ростом температуры внутренняя энергия растет. Абсолютное значение U определить невозможно, но можно рассчитать ∆U. Работа А – это работа против всех внешних сил, но обычно это работа изменения объема. Теплота Q и работа А – две формы передачи энергии.
Внутренняя энергия U – это энергия частиц, составляющих данную систему. Внутренняя энергия идеального газа зависит только от его температуры, поэтому с ростом температуры внутренняя энергия растет. Абсолютное значение U определить невозможно, но можно рассчитать ∆U. Работа А – это работа против всех внешних сил, но обычно это работа изменения объема. Теплота Q и работа А – две формы передачи энергии.
 В зависимости от условий протекания различают 4 типа процессов: 1. изохорный – протекает при постоянном объеме (V=const); 2. изобарный – протекает при постоянном давлении (p=const); 3. изотермический – протекает при постоянной температуре (T=const); 4. адиабатный – протекает без теплообмена с окружающей средой (∆Q=0).
В зависимости от условий протекания различают 4 типа процессов: 1. изохорный – протекает при постоянном объеме (V=const); 2. изобарный – протекает при постоянном давлении (p=const); 3. изотермический – протекает при постоянной температуре (T=const); 4. адиабатный – протекает без теплообмена с окружающей средой (∆Q=0).
 Химические процессы протекают либо при постоянном объеме (V=const), либо при постоянном давлении (p=const). а) V=const d. V=0, A=0 QV=∆U Вся теплота, подводимая в изохорных условиях, идет на изменение внутренней энергии. б) p=const
Химические процессы протекают либо при постоянном объеме (V=const), либо при постоянном давлении (p=const). а) V=const d. V=0, A=0 QV=∆U Вся теплота, подводимая в изохорных условиях, идет на изменение внутренней энергии. б) p=const
 QP =∆U + А = ( U 2 –U 1 ) + p ∙ ( V 2 – V 1 ) = = (U 2 + p. V 2 ) – (U 1 + p. V 1 ) H – энтальпия, теплосодержание. QP = H 2 – H 1 = ∆H Вся теплота, подводимая в изобарных условиях, идет на изменение энтальпии.
QP =∆U + А = ( U 2 –U 1 ) + p ∙ ( V 2 – V 1 ) = = (U 2 + p. V 2 ) – (U 1 + p. V 1 ) H – энтальпия, теплосодержание. QP = H 2 – H 1 = ∆H Вся теплота, подводимая в изобарных условиях, идет на изменение энтальпии.
 Тепловой эффект реакции – количество выделенной или поглощенной в ходе реакции теплоты. По знаку теплового эффекта все реакции делятся на 2 типа. 1) Экзотермические реакции –это реакции, сопровождающиеся выделением теплоты. При этом энтальпия уменьшается, т. к. энергия из системы уходит, выделяется. ∆ H < 0 – экзо 2) Эндотермические реакции – это реакции, сопровождающиеся поглощением теплоты. В результате этого теплосодержание системы возрастает. ∆ H > 0 – эндо.
Тепловой эффект реакции – количество выделенной или поглощенной в ходе реакции теплоты. По знаку теплового эффекта все реакции делятся на 2 типа. 1) Экзотермические реакции –это реакции, сопровождающиеся выделением теплоты. При этом энтальпия уменьшается, т. к. энергия из системы уходит, выделяется. ∆ H < 0 – экзо 2) Эндотермические реакции – это реакции, сопровождающиеся поглощением теплоты. В результате этого теплосодержание системы возрастает. ∆ H > 0 – эндо.
 Термохимические уравнения – это химические уравнения, в которых указывается тепловой эффект реакции ∆ H и состояние веществ: (к) – кристаллическое, (ж) – жидкое, (г) – газообразное, (р) – растворенное. Как правило, ∆ H приводится для стандартной температуры 250 С (298, 15 К) и стандартного давления 1 атм. Если температура не равна 298, 15 К, она должна быть указана в нижнем индексе.
Термохимические уравнения – это химические уравнения, в которых указывается тепловой эффект реакции ∆ H и состояние веществ: (к) – кристаллическое, (ж) – жидкое, (г) – газообразное, (р) – растворенное. Как правило, ∆ H приводится для стандартной температуры 250 С (298, 15 К) и стандартного давления 1 атм. Если температура не равна 298, 15 К, она должна быть указана в нижнем индексе.
 2 С + О 2 = 2 СО; ∆Н 0298 = - 221 к. Дж. (графит) (г) В термохимии приняты дробные коэффициенты, при этом число атомов должно быть целым. С + ½ О 2 = СО; (графит) (г) ∆Н 0298 = - 110, 5 к. Дж.
2 С + О 2 = 2 СО; ∆Н 0298 = - 221 к. Дж. (графит) (г) В термохимии приняты дробные коэффициенты, при этом число атомов должно быть целым. С + ½ О 2 = СО; (графит) (г) ∆Н 0298 = - 110, 5 к. Дж.
 2. Закон Гесса Это следствие I закона термодинамики применительно к химическим процессам. n Тепловой эффект процесса зависит только от вида и состояния исходных веществ и продуктов реакции и не зависит от пути перехода от исходных веществ к продуктам реакции. n
2. Закон Гесса Это следствие I закона термодинамики применительно к химическим процессам. n Тепловой эффект процесса зависит только от вида и состояния исходных веществ и продуктов реакции и не зависит от пути перехода от исходных веществ к продуктам реакции. n
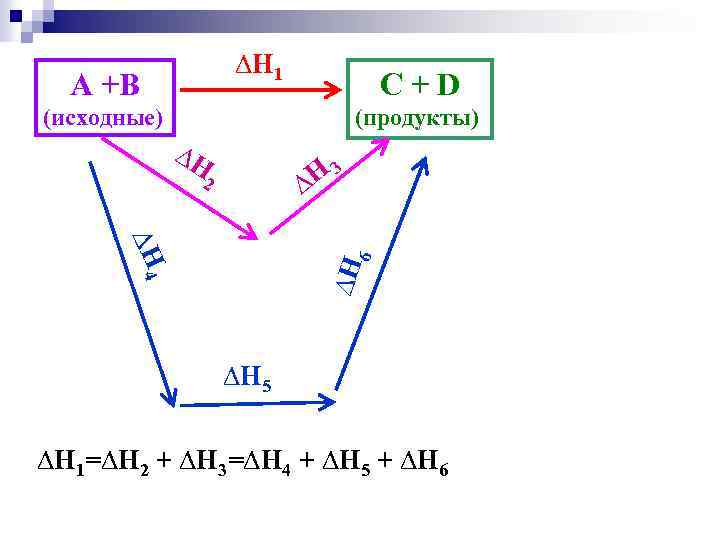 ∆Н 1 A +B C+D (исходные) (продукты) ∆Н Н 3 ∆ 2 ∆Н 6 ∆Н 4 ∆Н 5 ∆Н 1=∆Н 2 + ∆Н 3=∆Н 4 + ∆Н 5 + ∆Н 6
∆Н 1 A +B C+D (исходные) (продукты) ∆Н Н 3 ∆ 2 ∆Н 6 ∆Н 4 ∆Н 5 ∆Н 1=∆Н 2 + ∆Н 3=∆Н 4 + ∆Н 5 + ∆Н 6
 Следствие из закона Гесса Тепловой эффект реакции равен сумме теплот образования продуктов реакции минус сумма теплот образования исходных веществ. Теплота (энтальпия) образования ∆f. Н – тепловой эффект реакции образования 1 моля вещества из простых веществ, устойчивых при Т=298, 15 К (250 С) и р=1 атм, т. е. в стандартных условиях. Это справочная величина. Теплота образования простых веществ, устойчивых при стандартных условиях, равна 0. ∆f. Н 0(О 2)=0; ∆f. Н 0(О 3)≠ 0 ; ∆f. Н 0(Zn) ≠ 0. (г) [∆f. Н 0]=к. Дж/моль. (г)
Следствие из закона Гесса Тепловой эффект реакции равен сумме теплот образования продуктов реакции минус сумма теплот образования исходных веществ. Теплота (энтальпия) образования ∆f. Н – тепловой эффект реакции образования 1 моля вещества из простых веществ, устойчивых при Т=298, 15 К (250 С) и р=1 атм, т. е. в стандартных условиях. Это справочная величина. Теплота образования простых веществ, устойчивых при стандартных условиях, равна 0. ∆f. Н 0(О 2)=0; ∆f. Н 0(О 3)≠ 0 ; ∆f. Н 0(Zn) ≠ 0. (г) [∆f. Н 0]=к. Дж/моль. (г)
 Пример Для какой из приведенных ниже реакций изменение энтальпии соответствует стандартной энтальпии образования Ba. SO 3 (к) ? 1) Ba(NO 3)2 (ж) + H 2 SO 3 (ж) = Ba. SO 3 (к) + 2 HNO 3 (ж) 2) Ba. O (к) + SO 2 (г) = Ba. SO 3 (к) 3) Ba (к) + S (к) + O 3 (г) = Ba. SO 3 (к) 4) 2 Ba (к) + 2 S (к) + 3 O 2 (г) = 2 Ba. SO 3 (к) 5) Ba (к) + S (к) + 3/2 O 2 (г) = Ba. SO 3 (к)
Пример Для какой из приведенных ниже реакций изменение энтальпии соответствует стандартной энтальпии образования Ba. SO 3 (к) ? 1) Ba(NO 3)2 (ж) + H 2 SO 3 (ж) = Ba. SO 3 (к) + 2 HNO 3 (ж) 2) Ba. O (к) + SO 2 (г) = Ba. SO 3 (к) 3) Ba (к) + S (к) + O 3 (г) = Ba. SO 3 (к) 4) 2 Ba (к) + 2 S (к) + 3 O 2 (г) = 2 Ba. SO 3 (к) 5) Ba (к) + S (к) + 3/2 O 2 (г) = Ba. SO 3 (к)
 ∆Н 0=∑ ∆f. Н 0(прод) - ∑ ∆f. Н 0(исх) Суммирование ведется по каждому молю, т. е. с учетом коэффициентов: если в уравнении реакции есть коэффициенты, не равные 1, то ∆f. Н 0 такого вещества надо умножить на коэффициент. a. A + b. B = d. D + e. E ∆Н 0=∑ ∆f. Н 0(прод) - ∑ ∆f. Н 0(исх)= =(d ∆f. Н 0(D) +e ∆f. Н 0(E)) -(a ∆f. Н 0(A) +b ∆f. Н 0(B))
∆Н 0=∑ ∆f. Н 0(прод) - ∑ ∆f. Н 0(исх) Суммирование ведется по каждому молю, т. е. с учетом коэффициентов: если в уравнении реакции есть коэффициенты, не равные 1, то ∆f. Н 0 такого вещества надо умножить на коэффициент. a. A + b. B = d. D + e. E ∆Н 0=∑ ∆f. Н 0(прод) - ∑ ∆f. Н 0(исх)= =(d ∆f. Н 0(D) +e ∆f. Н 0(E)) -(a ∆f. Н 0(A) +b ∆f. Н 0(B))
 3. Второй закон термодинамики Самопроизвольно в изолированной системе могут протекать только те процессы, которые сопровождаются повышением энтропии. n Энтропия S – мера беспорядка системы, мера хаотичности. n
3. Второй закон термодинамики Самопроизвольно в изолированной системе могут протекать только те процессы, которые сопровождаются повышением энтропии. n Энтропия S – мера беспорядка системы, мера хаотичности. n
 Она растет при повышении температуры, плавлении, кипении, сублимации (возгонке), расширении и т. п. Процессы, связанные с повышением порядка, охлаждение, кристаллизация, конденсация, сжатие – сопровождаются уменьшением энтропии.
Она растет при повышении температуры, плавлении, кипении, сублимации (возгонке), расширении и т. п. Процессы, связанные с повышением порядка, охлаждение, кристаллизация, конденсация, сжатие – сопровождаются уменьшением энтропии.
![[S 0]=Дж/моль·К, это справочная величина. ∆S 0=∑ S 0(прод) - ∑ S 0(исх) Суммирование [S 0]=Дж/моль·К, это справочная величина. ∆S 0=∑ S 0(прод) - ∑ S 0(исх) Суммирование](https://present5.com/presentation/3/92561635_133575704.pdf-img/92561635_133575704.pdf-18.jpg) [S 0]=Дж/моль·К, это справочная величина. ∆S 0=∑ S 0(прод) - ∑ S 0(исх) Суммирование ведется по каждому молю, т. е. с учетом коэффициентов.
[S 0]=Дж/моль·К, это справочная величина. ∆S 0=∑ S 0(прод) - ∑ S 0(исх) Суммирование ведется по каждому молю, т. е. с учетом коэффициентов.
 4. Критерий направленности процесса n Существует потенциал, характеризующий химические процессы, протекающие при p, T=const, он называется изобарно-изотермический потенциал, или, ради краткости, изобарный потенциал. Чаще всего называют энергия Гиббса G.
4. Критерий направленности процесса n Существует потенциал, характеризующий химические процессы, протекающие при p, T=const, он называется изобарно-изотермический потенциал, или, ради краткости, изобарный потенциал. Чаще всего называют энергия Гиббса G.
 ∆G<0 Возможность самопроизвольного протекания реакции в прямом направлении. ∆Gпрямой= - ∆Gобратной ∆G>0 Невозможность самопроизвольного протекания реакции в прямом направлении. ∆G=0 Равновесие, протекает и прямая, и обратная реакции одновременно. Чем ∆G<0, тем дальше система от состояния равновесия и тем более она реакционноспособна.
∆G<0 Возможность самопроизвольного протекания реакции в прямом направлении. ∆Gпрямой= - ∆Gобратной ∆G>0 Невозможность самопроизвольного протекания реакции в прямом направлении. ∆G=0 Равновесие, протекает и прямая, и обратная реакции одновременно. Чем ∆G<0, тем дальше система от состояния равновесия и тем более она реакционноспособна.
 Существует 2 способа расчета Δ G. 1) Аналогично расчету Δ H и Δ S 2) a. A + b. B = d. D + e. E ∆G 0=∑ ∆f. G 0(прод) - ∑ ∆f. G 0(исх)= =(d ∆f. G 0(D) +e ∆f. G 0(E)) -(a ∆f. G 0(A) +b ∆f. G 0(B)). ∆f. G 0, как и ∆f. H 0, для простых веществ, устойчивых при стандартных условиях, равно 0. ∆f. G 0(О 2)=0; ∆f. G 0(О 3)≠ 0. (г) [∆f. G 0]=к. Дж/моль, ∆f. G 0 – это справочная величина.
Существует 2 способа расчета Δ G. 1) Аналогично расчету Δ H и Δ S 2) a. A + b. B = d. D + e. E ∆G 0=∑ ∆f. G 0(прод) - ∑ ∆f. G 0(исх)= =(d ∆f. G 0(D) +e ∆f. G 0(E)) -(a ∆f. G 0(A) +b ∆f. G 0(B)). ∆f. G 0, как и ∆f. H 0, для простых веществ, устойчивых при стандартных условиях, равно 0. ∆f. G 0(О 2)=0; ∆f. G 0(О 3)≠ 0. (г) [∆f. G 0]=к. Дж/моль, ∆f. G 0 – это справочная величина.
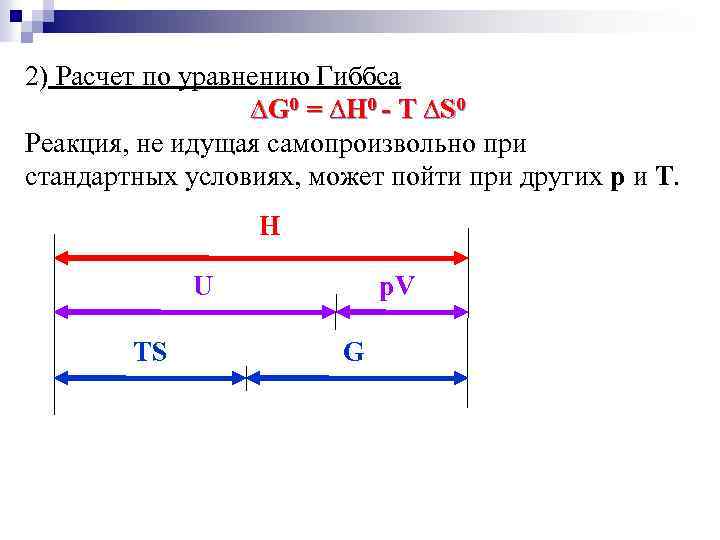 2) Расчет по уравнению Гиббса ∆G 0 = ∆Н 0 - T ∆S 0 Реакция, не идущая самопроизвольно при стандартных условиях, может пойти при других p и T. H U TS p. V G
2) Расчет по уравнению Гиббса ∆G 0 = ∆Н 0 - T ∆S 0 Реакция, не идущая самопроизвольно при стандартных условиях, может пойти при других p и T. H U TS p. V G
 Задача CH 4 + CO 2 = 2 CO + 2 H 2 (г) (г) 1)Определить тепловой эффект реакции ∆Н 0=∑ ∆f. Н 0(прод) - ∑ ∆f. Н 0(исх)= =(2 ∆f. Н 0(СO) +2 ∆f. Н 0(Н 2)) -(∆f. Н 0(CH 4) + ∆f. Н 0(CO 2)) = =(2·(-110, 52) + 2· 0) – -(-74, 85 + (-393, 51)) = = 247, 32 (к. Дж). ∆Н 0>0, - реакция эндотермическая.
Задача CH 4 + CO 2 = 2 CO + 2 H 2 (г) (г) 1)Определить тепловой эффект реакции ∆Н 0=∑ ∆f. Н 0(прод) - ∑ ∆f. Н 0(исх)= =(2 ∆f. Н 0(СO) +2 ∆f. Н 0(Н 2)) -(∆f. Н 0(CH 4) + ∆f. Н 0(CO 2)) = =(2·(-110, 52) + 2· 0) – -(-74, 85 + (-393, 51)) = = 247, 32 (к. Дж). ∆Н 0>0, - реакция эндотермическая.
 2) Определить изменение энтропии ∆S 0=∑ S 0(прод) - ∑ S 0(исх)= =(2 ·S 0(СO) +2 · S 0(Н 2)) -(S 0(CH 4) + S 0(CO 2)) = =(2 · 197, 91 + 2 · 130, 59) – - (186, 19 + 213, 65) = =257, 16 (Дж/К)
2) Определить изменение энтропии ∆S 0=∑ S 0(прод) - ∑ S 0(исх)= =(2 ·S 0(СO) +2 · S 0(Н 2)) -(S 0(CH 4) + S 0(CO 2)) = =(2 · 197, 91 + 2 · 130, 59) – - (186, 19 + 213, 65) = =257, 16 (Дж/К)
 3) Определить изменение энергии Гиббса ∆G 0 = ∆Н 0 - T ∆S 0 = =247, 32 к. Дж – - 298, 15 К· 257, 16 · 10 -3 к. Дж/K ≈ ≈ 170, 65 к. Дж. ∆G 0>0, - процесс самопроизвольно не идет при Т=298, 15 К и р=1 атм.
3) Определить изменение энергии Гиббса ∆G 0 = ∆Н 0 - T ∆S 0 = =247, 32 к. Дж – - 298, 15 К· 257, 16 · 10 -3 к. Дж/K ≈ ≈ 170, 65 к. Дж. ∆G 0>0, - процесс самопроизвольно не идет при Т=298, 15 К и р=1 атм.
 4) При какой температуре процесс пойдет самопроизвольно Любой процесс идет самопроизвольно при температуре равновесия. В этом случае ∆G 0 = 0, тогда правая часть уравнения Гиббса равна нулю: ∆Н 0 - T ∆S 0 =0, ∆Н 0 = Tравн· ∆S 0 , отсюда
4) При какой температуре процесс пойдет самопроизвольно Любой процесс идет самопроизвольно при температуре равновесия. В этом случае ∆G 0 = 0, тогда правая часть уравнения Гиббса равна нулю: ∆Н 0 - T ∆S 0 =0, ∆Н 0 = Tравн· ∆S 0 , отсюда


