 Основы термодинамики процессов коррозии металлов внутренняя энергия (U), энтальпия (Н), энтропия (S), Дж/(моль-град. ) изобарно-изотермический потенциал (G), химический потенциал (µ). ∆U = Q - A A = P∆V или ∆Н = ∆U + P∆V ∆НР = -Q
Основы термодинамики процессов коррозии металлов внутренняя энергия (U), энтальпия (Н), энтропия (S), Дж/(моль-град. ) изобарно-изотермический потенциал (G), химический потенциал (µ). ∆U = Q - A A = P∆V или ∆Н = ∆U + P∆V ∆НР = -Q
 ∆G = ∆Н - T∆S Дж/моль ∆G = -RT In К реакция окисления металла: Me + О 2 ↔ Ме. О 2 ∆G = -RT ln К -RT ln a 02
∆G = ∆Н - T∆S Дж/моль ∆G = -RT In К реакция окисления металла: Me + О 2 ↔ Ме. О 2 ∆G = -RT ln К -RT ln a 02
 Коррозия металлов в неэлектролитах Коррозия в неэлектролитах — это коррозия в жидкостях, не проводящих электрический ток. Примеры неэлектролитов: -бром; -расплавленная сера; -многие органические вещества (бензол, хлороформ, фенол и т. д. ); -жидкое топливо (нефть, керосин, бензин); -смазочные масла.
Коррозия металлов в неэлектролитах Коррозия в неэлектролитах — это коррозия в жидкостях, не проводящих электрический ток. Примеры неэлектролитов: -бром; -расплавленная сера; -многие органические вещества (бензол, хлороформ, фенол и т. д. ); -жидкое топливо (нефть, керосин, бензин); -смазочные масла.
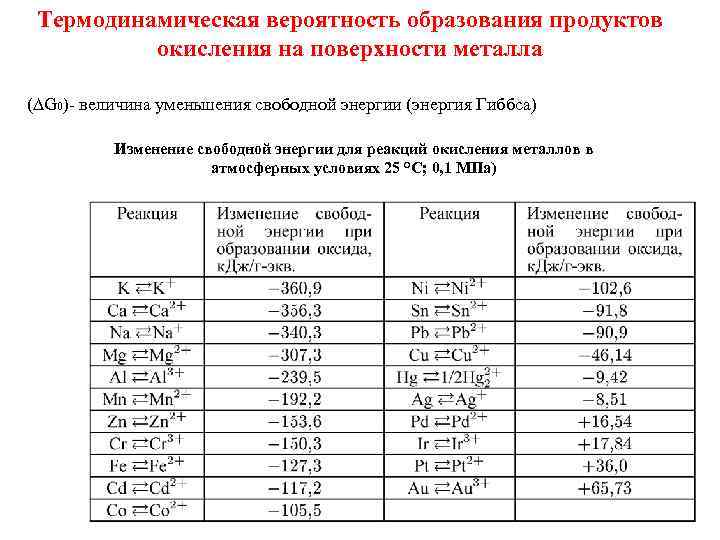 Термодинамическая вероятность образования продуктов окисления на поверхности металла (∆G 0)- величина уменьшения свободной энергии (энергия Гиббса) Изменение свободной энергии для реакций окисления металлов в атмосферных условиях 25 °С; 0, 1 МПа)
Термодинамическая вероятность образования продуктов окисления на поверхности металла (∆G 0)- величина уменьшения свободной энергии (энергия Гиббса) Изменение свободной энергии для реакций окисления металлов в атмосферных условиях 25 °С; 0, 1 МПа)
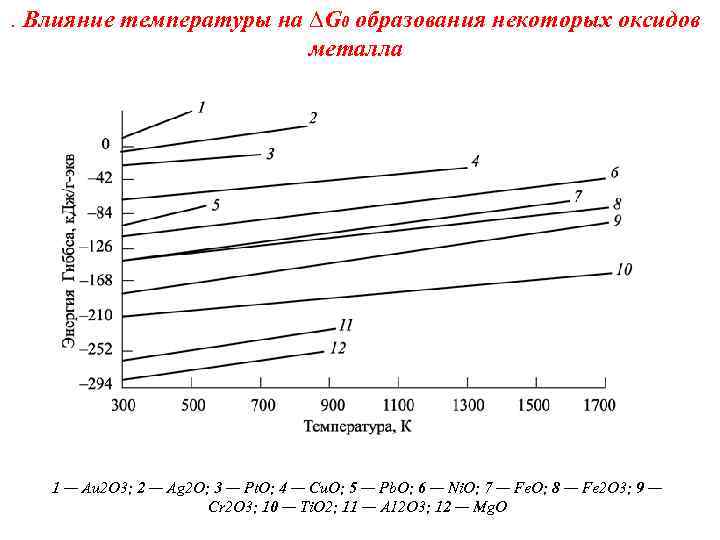 . Влияние температуры на ∆G 0 образования некоторых оксидов металла 1 — Au 2 O 3; 2 — Ag 2 O; 3 — Pt. O; 4 — Сu. О; 5 — Рb. О; 6 — Ni. О; 7 — Fe. O; 8 — Fe 2 O 3; 9 — Cr 2 O 3; 10 — Тi. O 2; 11 — А 12 О 3; 12 — Mg. O
. Влияние температуры на ∆G 0 образования некоторых оксидов металла 1 — Au 2 O 3; 2 — Ag 2 O; 3 — Pt. O; 4 — Сu. О; 5 — Рb. О; 6 — Ni. О; 7 — Fe. O; 8 — Fe 2 O 3; 9 — Cr 2 O 3; 10 — Тi. O 2; 11 — А 12 О 3; 12 — Mg. O
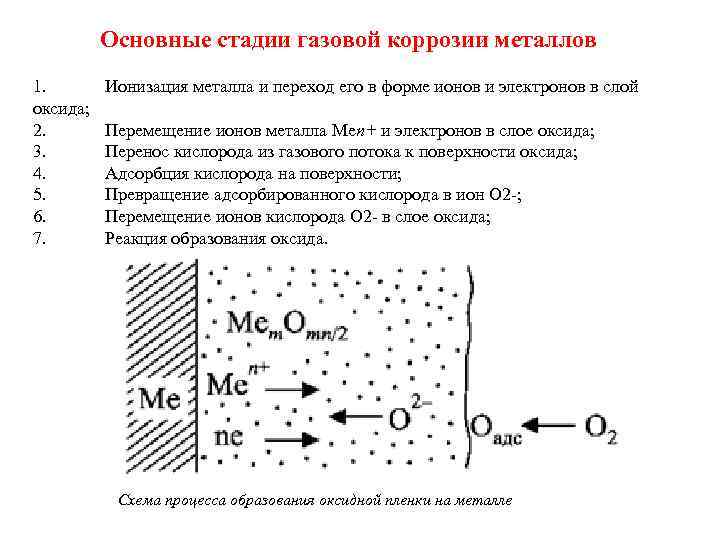 Основные стадии газовой коррозии металлов 1. оксида; 2. 3. 4. 5. 6. 7. Ионизация металла и переход его в форме ионов и электронов в слой Перемещение ионов металла Меп+ и электронов в слое оксида; Перенос кислорода из газового потока к поверхности оксида; Адсорбция кислорода на поверхности; Превращение адсорбированного кислорода в ион О 2 -; Перемещение ионов кислорода О 2 - в слое оксида; Реакция образования оксида. Схема процесса образования оксидной пленки на металле
Основные стадии газовой коррозии металлов 1. оксида; 2. 3. 4. 5. 6. 7. Ионизация металла и переход его в форме ионов и электронов в слой Перемещение ионов металла Меп+ и электронов в слое оксида; Перенос кислорода из газового потока к поверхности оксида; Адсорбция кислорода на поверхности; Превращение адсорбированного кислорода в ион О 2 -; Перемещение ионов кислорода О 2 - в слое оксида; Реакция образования оксида. Схема процесса образования оксидной пленки на металле
 Пленки на поверхности металлов -тонкие (невидимые) пленки толщиной от мономолекулярного слоя до 40 нм; -средние пленки (видимые благодаря интерференционному окрашиванию как цвета побежалости), имеющие толщину 40 - 500 нм; -толстые (видимые) пленки толщиной более 500 нм. Толщина образуемых пленок во многом определяется условиями окисления.
Пленки на поверхности металлов -тонкие (невидимые) пленки толщиной от мономолекулярного слоя до 40 нм; -средние пленки (видимые благодаря интерференционному окрашиванию как цвета побежалости), имеющие толщину 40 - 500 нм; -толстые (видимые) пленки толщиной более 500 нм. Толщина образуемых пленок во многом определяется условиями окисления.
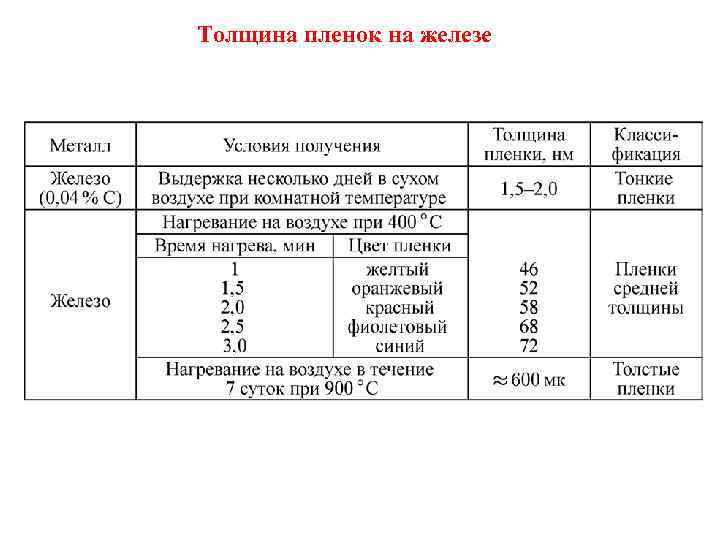 Толщина пленок на железе
Толщина пленок на железе
 Аме — атомная масса металла; ρме — плотность металла. где Мок — молекулярная масса оксида; n— число атомов металла в молекуле оксида; ρок — плотность оксида. при Vок/Vме > 1 образуется сплошная пленка, при Vok/Vме < 1 пленка не получается сплошной.
Аме — атомная масса металла; ρме — плотность металла. где Мок — молекулярная масса оксида; n— число атомов металла в молекуле оксида; ρок — плотность оксида. при Vок/Vме > 1 образуется сплошная пленка, при Vok/Vме < 1 пленка не получается сплошной.
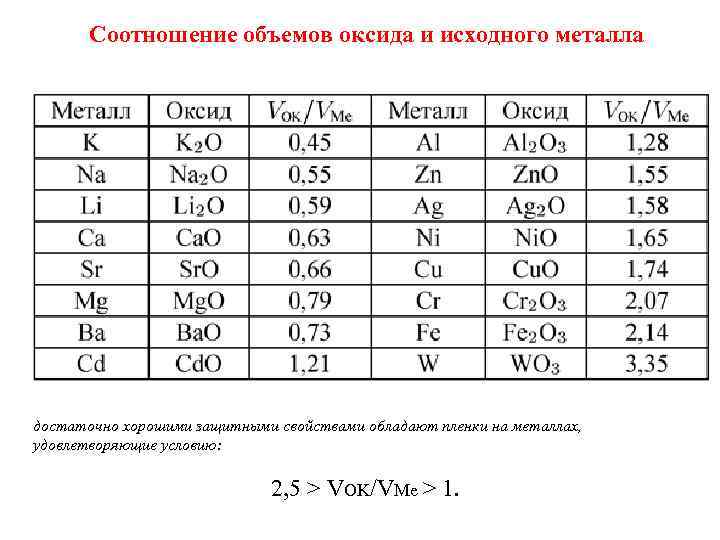 Соотношение объемов оксида и исходного металла достаточно хорошими защитными свойствами обладают пленки на металлах, удовлетворяющие условию: 2, 5 > VOK/VMe > 1.
Соотношение объемов оксида и исходного металла достаточно хорошими защитными свойствами обладают пленки на металлах, удовлетворяющие условию: 2, 5 > VOK/VMe > 1.
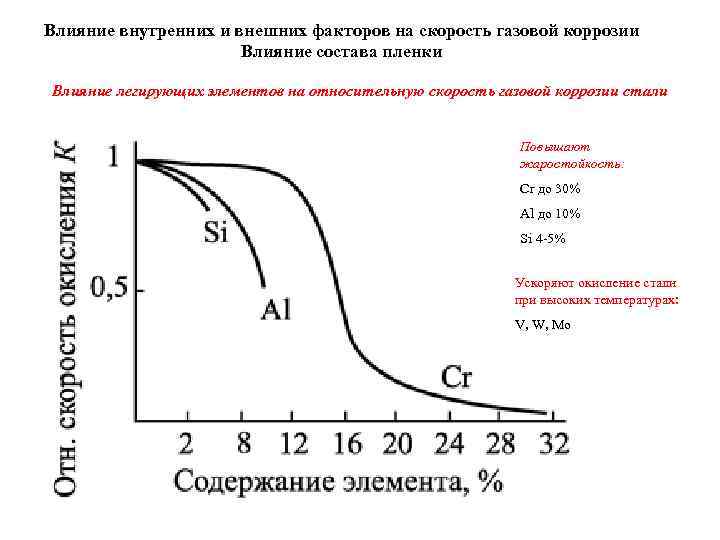 Влияние внутренних и внешних факторов на скорость газовой коррозии Влияние состава пленки Влияние легирующих элементов на относительную скорость газовой коррозии стали Повышают жаростойкость: Cr до 30% Al до 10% Si 4 -5% Ускоряют окисление стали при высоких температурах: V, W, Mo
Влияние внутренних и внешних факторов на скорость газовой коррозии Влияние состава пленки Влияние легирующих элементов на относительную скорость газовой коррозии стали Повышают жаростойкость: Cr до 30% Al до 10% Si 4 -5% Ускоряют окисление стали при высоких температурах: V, W, Mo
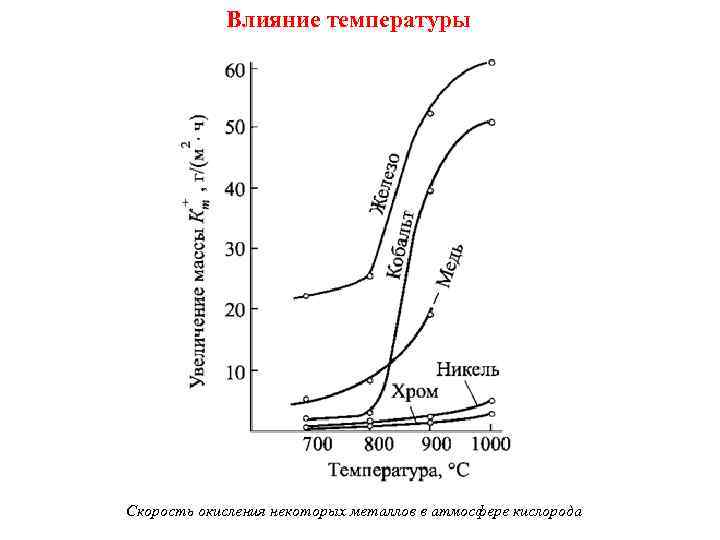 Влияние температуры Скорость окисления некоторых металлов в атмосфере кислорода
Влияние температуры Скорость окисления некоторых металлов в атмосфере кислорода