8 физика ТЕРМОДИНАМИКА.ppt
- Количество слайдов: 42
 ОСНОВЫ ТЕРМОДИНАМИКИ
ОСНОВЫ ТЕРМОДИНАМИКИ
 1. Внутренняя энергия U макроскопической системы – это ее полная энергия за исключением кинетической энергии системы как целого и потенциальной энергии во внешнем силовом поле. Внутренняя энергия включает в себя: ь кинетическую энергию хаотического движения молекул ь потенциальную энергию взаимодействия между молекулами ь внутримолекулярную энергию ь внутриатомную энергию ь внутриядерную энергию Внутренняя энергия идеального газа включает в себя: только кинетическую энергию хаотического движения молекул. Внутренняя энергия системы является функцией ее состояния.
1. Внутренняя энергия U макроскопической системы – это ее полная энергия за исключением кинетической энергии системы как целого и потенциальной энергии во внешнем силовом поле. Внутренняя энергия включает в себя: ь кинетическую энергию хаотического движения молекул ь потенциальную энергию взаимодействия между молекулами ь внутримолекулярную энергию ь внутриатомную энергию ь внутриядерную энергию Внутренняя энергия идеального газа включает в себя: только кинетическую энергию хаотического движения молекул. Внутренняя энергия системы является функцией ее состояния.
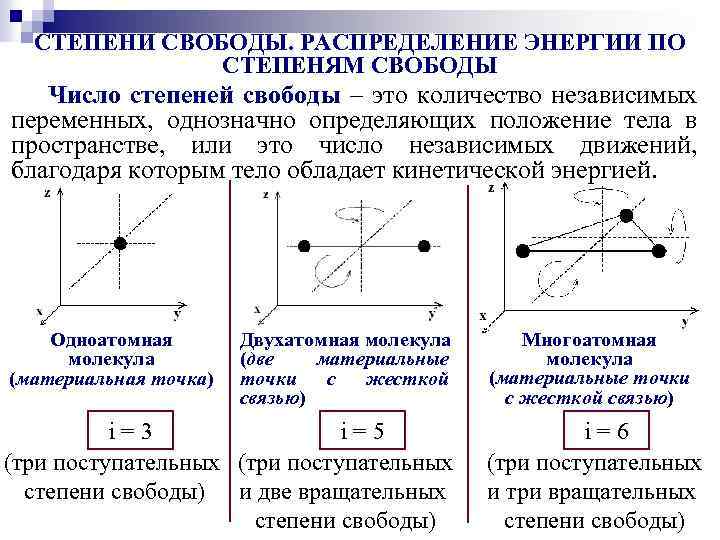 СТЕПЕНИ СВОБОДЫ. РАСПРЕДЕЛЕНИЕ ЭНЕРГИИ ПО СТЕПЕНЯМ СВОБОДЫ Число степеней свободы – это количество независимых переменных, однозначно определяющих положение тела в пространстве, или это число независимых движений, благодаря которым тело обладает кинетической энергией. Одноатомная молекула (материальная точка) Двухатомная молекула (две материальные точки с жесткой связью) i=3 i=5 (три поступательных степени свободы) и две вращательных степени свободы) Многоатомная молекула (материальные точки с жесткой связью) i=6 (три поступательных и три вращательных степени свободы)
СТЕПЕНИ СВОБОДЫ. РАСПРЕДЕЛЕНИЕ ЭНЕРГИИ ПО СТЕПЕНЯМ СВОБОДЫ Число степеней свободы – это количество независимых переменных, однозначно определяющих положение тела в пространстве, или это число независимых движений, благодаря которым тело обладает кинетической энергией. Одноатомная молекула (материальная точка) Двухатомная молекула (две материальные точки с жесткой связью) i=3 i=5 (три поступательных степени свободы) и две вращательных степени свободы) Многоатомная молекула (материальные точки с жесткой связью) i=6 (три поступательных и три вращательных степени свободы)
 Если молекула не жесткая (возможны относительные смещения атомов в молекуле), то дополнительно вводится колебательная степень свободы. iколеб=1 iколеб=3 Теорема о равномерном распределении энергии по степеням свободы (Больцман): На каждую поступательную и вращательную степень свободы приходится энергия, равная (k. T)/2, а на каждую колебательную степень свободы – энергия, равная k. Т. Средняя кинетическая энергия одной молекулы:
Если молекула не жесткая (возможны относительные смещения атомов в молекуле), то дополнительно вводится колебательная степень свободы. iколеб=1 iколеб=3 Теорема о равномерном распределении энергии по степеням свободы (Больцман): На каждую поступательную и вращательную степень свободы приходится энергия, равная (k. T)/2, а на каждую колебательную степень свободы – энергия, равная k. Т. Средняя кинетическая энергия одной молекулы:
 ВНУТРЕННЯЯ ЭНЕРГИЯ ИДЕАЛЬНОГО ГАЗА Внутренняя энергия идеального газа – это сумма кинетических энергий движения всех его молекул (молекулы идеального газа не взаимодействуют с другом на расстоянии). N – число молекул =R Внутренняя энергия – функция температуры
ВНУТРЕННЯЯ ЭНЕРГИЯ ИДЕАЛЬНОГО ГАЗА Внутренняя энергия идеального газа – это сумма кинетических энергий движения всех его молекул (молекулы идеального газа не взаимодействуют с другом на расстоянии). N – число молекул =R Внутренняя энергия – функция температуры
 Р Работа А, совершаемая газом при изменении его объема от V 1 до V 2 d. V=Sdr dr d. V = S∙dr – изменение объема газа – элементарная работа Графическое представление работы V 1 V 2
Р Работа А, совершаемая газом при изменении его объема от V 1 до V 2 d. V=Sdr dr d. V = S∙dr – изменение объема газа – элементарная работа Графическое представление работы V 1 V 2
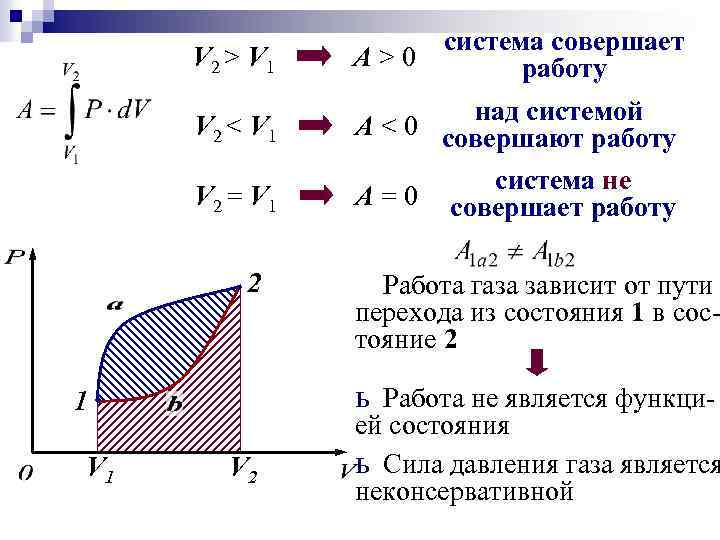 система совершает работу V 2 > V 1 A>0 V 2 < V 1 над системой A < 0 совершают работу V 2 = V 1 система не совершает работу 2 Работа газа зависит от пути перехода из состояния 1 в состояние 2 ь Работа не является функци- 1 V 1 A=0 V 2 ей состояния ь Сила давления газа является неконсервативной
система совершает работу V 2 > V 1 A>0 V 2 < V 1 над системой A < 0 совершают работу V 2 = V 1 система не совершает работу 2 Работа газа зависит от пути перехода из состояния 1 в состояние 2 ь Работа не является функци- 1 V 1 A=0 V 2 ей состояния ь Сила давления газа является неконсервативной
 Теплопередача – это процесс обмена энергией с окружающими телами, при котором изменяются только внутренние параметры термодинамической системы. Способы теплопередачи ь теплопроводность ь конвекция ь излучение теплопроводность конвекция излучение Мерой энергии, переданной при теплопередаче, является количество теплоты Q. Эта величина, как и работа, не является полным дифференциалом (зависит от процесса). Q > 0 – система получает тепло Q < 0 – система отдает тепло
Теплопередача – это процесс обмена энергией с окружающими телами, при котором изменяются только внутренние параметры термодинамической системы. Способы теплопередачи ь теплопроводность ь конвекция ь излучение теплопроводность конвекция излучение Мерой энергии, переданной при теплопередаче, является количество теплоты Q. Эта величина, как и работа, не является полным дифференциалом (зависит от процесса). Q > 0 – система получает тепло Q < 0 – система отдает тепло
 Закон сохранения энергии, в котором учитывается особая форма передачи энергии путем теплопередачи, является фундаментальным законом физики и называется первым началом термодинамики: Количество тепла, полученное системой, расходуется на приращение внутренней энергии системы и на совершение системой работы над внешними телами (системами). – дифференциальная форма первого начала термодинамики
Закон сохранения энергии, в котором учитывается особая форма передачи энергии путем теплопередачи, является фундаментальным законом физики и называется первым началом термодинамики: Количество тепла, полученное системой, расходуется на приращение внутренней энергии системы и на совершение системой работы над внешними телами (системами). – дифференциальная форма первого начала термодинамики
 3. ТЕПЛОЕМКОСТЬ и КОЛИЧЕСТВО ТЕПЛОТЫ Полная теплоемкость тела или системы – скалярная физическая величина, характеризующая процесс теплообмена и равная количеству тепла, полученному термодинамической системой для изменения его температуры на один Кельвин: Удельная теплоемкость – скалярная физическая величина, равная количеству тепла, необходимому для нагревания единицы массы газа на один Кельвин:
3. ТЕПЛОЕМКОСТЬ и КОЛИЧЕСТВО ТЕПЛОТЫ Полная теплоемкость тела или системы – скалярная физическая величина, характеризующая процесс теплообмена и равная количеству тепла, полученному термодинамической системой для изменения его температуры на один Кельвин: Удельная теплоемкость – скалярная физическая величина, равная количеству тепла, необходимому для нагревания единицы массы газа на один Кельвин:
 Удельная теплоемкость Молярная теплоемкость - скалярная физическая величина, равная количеству тепла, необходимому для нагревания одного моля газа на один Кельвин: =c – связь молярной и удельной теплоемкости
Удельная теплоемкость Молярная теплоемкость - скалярная физическая величина, равная количеству тепла, необходимому для нагревания одного моля газа на один Кельвин: =c – связь молярной и удельной теплоемкости
 Теплоемкость зависит от характера процесса, при котором система получает тепло. Теплоемкость при постоянном объеме V= const – первое начало термодинамики Молярная теплоемкость при постоянном объеме:
Теплоемкость зависит от характера процесса, при котором система получает тепло. Теплоемкость при постоянном объеме V= const – первое начало термодинамики Молярная теплоемкость при постоянном объеме:
 Молярная теплоемкость при постоянном давлении: Соотношения между теплоемкостями – уравнение Майера – коэффициент Пуассона
Молярная теплоемкость при постоянном давлении: Соотношения между теплоемкостями – уравнение Майера – коэффициент Пуассона
 Количество тепла при нагревании/охлаждении тел можно рассчитывать через удельную теплоемкость: Количество тепла при плавлении/кристаллизации тел можно рассчитывать через удельную теплоту плавления: λ – удельная теплота плавления, [Дж/кг] Количество тепла при парообразовании/ конденсации можно рассчитывать через удельную теплоту парообразования: L – удельная теплота парообразования, [Дж/кг]
Количество тепла при нагревании/охлаждении тел можно рассчитывать через удельную теплоемкость: Количество тепла при плавлении/кристаллизации тел можно рассчитывать через удельную теплоту плавления: λ – удельная теплота плавления, [Дж/кг] Количество тепла при парообразовании/ конденсации можно рассчитывать через удельную теплоту парообразования: L – удельная теплота парообразования, [Дж/кг]
 4. Адиабатный процесс Q=0 Адиабатный процесс – это процесс протекающий без теплообмена с окружающей средой. Работа совершается за счет убыли внутренней энергии Если А > 0, то ∆U < 0; А < 0, то ∆U > 0. При адиабатном расширении газ охлаждается.
4. Адиабатный процесс Q=0 Адиабатный процесс – это процесс протекающий без теплообмена с окружающей средой. Работа совершается за счет убыли внутренней энергии Если А > 0, то ∆U < 0; А < 0, то ∆U > 0. При адиабатном расширении газ охлаждается.

 Уравнение адиабатного процесса
Уравнение адиабатного процесса
 Из уравнения Майера: – коэффициент Пуассона – уравнение адиабаты
Из уравнения Майера: – коэффициент Пуассона – уравнение адиабаты
 Из уравнения состояния: – уравнение Пуассона
Из уравнения состояния: – уравнение Пуассона
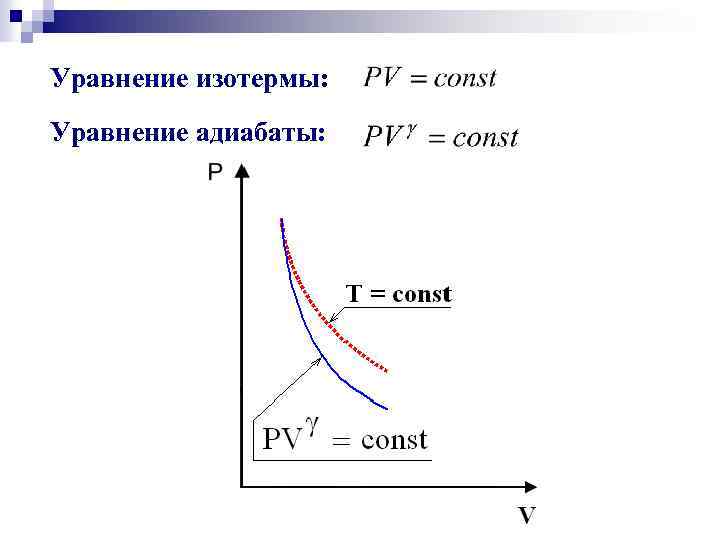 Уравнение изотермы: Уравнение адиабаты:
Уравнение изотермы: Уравнение адиабаты:
 5. Обратимые и необратимые процессы Обратимый процесс – равновесный процесс, который может протекать как в прямом, так и в обратном направлении. Свойства обратимого процесса: 1. Если система при прямом ходе на каком либо участке получает тепло ΔQ и совершает работу ΔА, то при обратном ходе на этом же участке система отдает тепло ΔQ' = ΔQ и над ней совершается работа ΔА' = ΔА 2. После протекания обратимого процесса в окружающей среде не должно оставаться никаких изменений Важнейшим признаком является его равновесность. обратимого процесса
5. Обратимые и необратимые процессы Обратимый процесс – равновесный процесс, который может протекать как в прямом, так и в обратном направлении. Свойства обратимого процесса: 1. Если система при прямом ходе на каком либо участке получает тепло ΔQ и совершает работу ΔА, то при обратном ходе на этом же участке система отдает тепло ΔQ' = ΔQ и над ней совершается работа ΔА' = ΔА 2. После протекания обратимого процесса в окружающей среде не должно оставаться никаких изменений Важнейшим признаком является его равновесность. обратимого процесса
 Всякий необратимый процесс - это такой процесс, обратный которому маловероятен. Все процессы в природе - необратимые. Приближением к обратимым термодинамическим процессам могут служить изопроцессы с идеальным газом. При обратимом процессе всегда совершается максимальная работа.
Всякий необратимый процесс - это такой процесс, обратный которому маловероятен. Все процессы в природе - необратимые. Приближением к обратимым термодинамическим процессам могут служить изопроцессы с идеальным газом. При обратимом процессе всегда совершается максимальная работа.
 6. Круговые термодинамические процессы Круговой процесс (цикл) - процесс, в результате которого термодинамическая система возвращается в исходное состояние. Круговые процессы лежат в основе работы всех тепловых машин: двигателей внутреннего сгорания, паровых и газовых турбин, паровых и холодильных машин и т. д. Работа расширения (1 a 2) положительна (d. V >0) Работа сжатия (2 b 1) отрицательна (d. V < 0). Работа, совершаемая за цикл, определяется площадью, охватываемой кривой.
6. Круговые термодинамические процессы Круговой процесс (цикл) - процесс, в результате которого термодинамическая система возвращается в исходное состояние. Круговые процессы лежат в основе работы всех тепловых машин: двигателей внутреннего сгорания, паровых и газовых турбин, паровых и холодильных машин и т. д. Работа расширения (1 a 2) положительна (d. V >0) Работа сжатия (2 b 1) отрицательна (d. V < 0). Работа, совершаемая за цикл, определяется площадью, охватываемой кривой.
 (система вернулась в 0 исходное состояние) – первое начало термодинамики для кругового процесса Работа, совершаемая за цикл, равна количеству теплоты полученной извне. Q 1 – количество теплоты, полученное системой; Q 2 – количество теплоты, отданное системой.
(система вернулась в 0 исходное состояние) – первое начало термодинамики для кругового процесса Работа, совершаемая за цикл, равна количеству теплоты полученной извне. Q 1 – количество теплоты, полученное системой; Q 2 – количество теплоты, отданное системой.
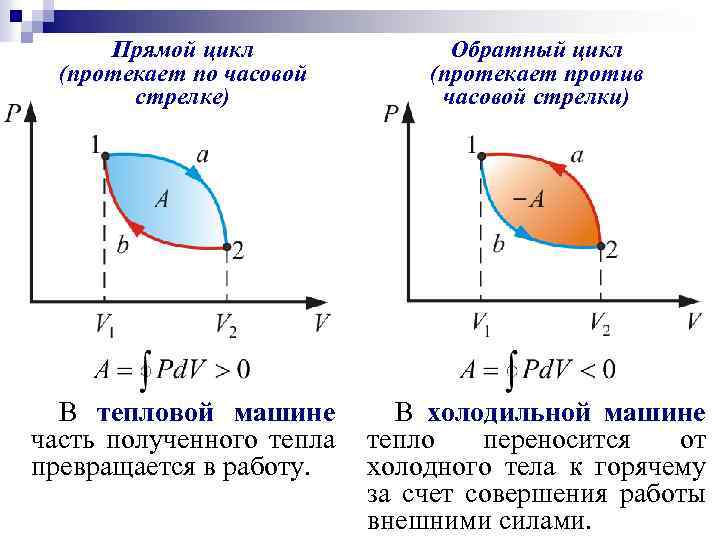 Прямой цикл (протекает по часовой стрелке) Обратный цикл (протекает против часовой стрелки) В тепловой машине часть полученного тепла превращается в работу. В холодильной машине тепло переносится от холодного тела к горячему за счет совершения работы внешними силами.
Прямой цикл (протекает по часовой стрелке) Обратный цикл (протекает против часовой стрелки) В тепловой машине часть полученного тепла превращается в работу. В холодильной машине тепло переносится от холодного тела к горячему за счет совершения работы внешними силами.
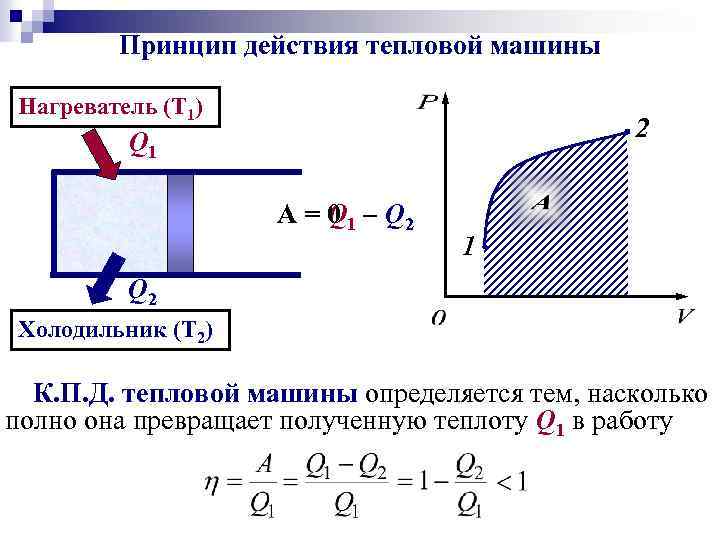 Принцип действия тепловой машины Нагреватель (Т 1) 2 Q 1 A = 0 1 – Q 2 Q 1 Q 2 Холодильник (Т 2) К. П. Д. тепловой машины определяется тем, насколько полно она превращает полученную теплоту Q 1 в работу
Принцип действия тепловой машины Нагреватель (Т 1) 2 Q 1 A = 0 1 – Q 2 Q 1 Q 2 Холодильник (Т 2) К. П. Д. тепловой машины определяется тем, насколько полно она превращает полученную теплоту Q 1 в работу


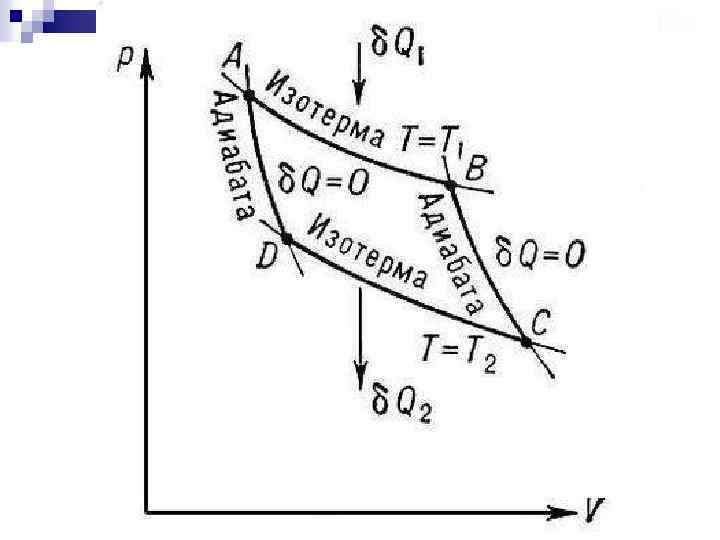
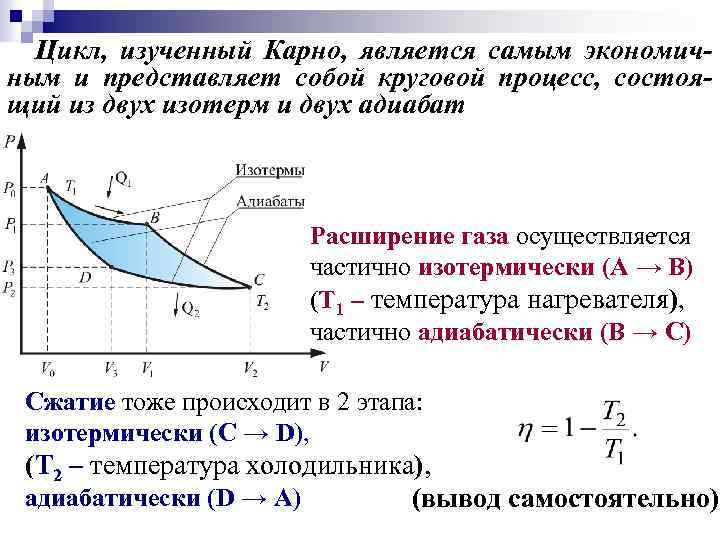 Цикл, изученный Карно, является самым экономичным и представляет собой круговой процесс, состоящий из двух изотерм и двух адиабат Расширение газа осуществляется частично изотермически (A → B) (T 1 – температура нагревателя), частично адиабатически (B → C) Сжатие тоже происходит в 2 этапа: изотермически (C → D), (T 2 – температура холодильника), адиабатически (D → A) (вывод самостоятельно)
Цикл, изученный Карно, является самым экономичным и представляет собой круговой процесс, состоящий из двух изотерм и двух адиабат Расширение газа осуществляется частично изотермически (A → B) (T 1 – температура нагревателя), частично адиабатически (B → C) Сжатие тоже происходит в 2 этапа: изотермически (C → D), (T 2 – температура холодильника), адиабатически (D → A) (вывод самостоятельно)
 7. Приведенное количество тепла. Неравенство Клаузиуса. Утверждение о том, что КПД всех обратимых машин одинаков, а КПД необратимой машины всегда меньше, чем обратимой можно записать в виде неравенства: Q 1 – количество тепла, полученное за цикл, Q 2 - количество тепла, отданное за цикл. Вместо отдаваемого телу с температурой Т 2 тепла Q 2 введем получаемое от этого тела тепло - Q 2: - неравенство Клаузиуса. - приведенное количество тепла - это отношение количества тепла, полученного термодинамической системой, к температуре, при которой оно получено.
7. Приведенное количество тепла. Неравенство Клаузиуса. Утверждение о том, что КПД всех обратимых машин одинаков, а КПД необратимой машины всегда меньше, чем обратимой можно записать в виде неравенства: Q 1 – количество тепла, полученное за цикл, Q 2 - количество тепла, отданное за цикл. Вместо отдаваемого телу с температурой Т 2 тепла Q 2 введем получаемое от этого тела тепло - Q 2: - неравенство Клаузиуса. - приведенное количество тепла - это отношение количества тепла, полученного термодинамической системой, к температуре, при которой оно получено.
 Сумма приведенных количеств тепла, сообщенных системе при обратимом переходе из произвольного начального состояния в произвольное конечное, не зависит от пути, по которому произошел переход, а зависит только от параметров начального и конечного состояний. Количество теплоты Q – зависит от процесса Приведенное количество теплоты – не зависит от процесса, а определяется только состоянием системы (является функцией состояния). Это позволяет ввести новую функцию состояния S энтропию : S = [Дж/К] Понятие энтропии ввёл Клаузиус в 1865 г.
Сумма приведенных количеств тепла, сообщенных системе при обратимом переходе из произвольного начального состояния в произвольное конечное, не зависит от пути, по которому произошел переход, а зависит только от параметров начального и конечного состояний. Количество теплоты Q – зависит от процесса Приведенное количество теплоты – не зависит от процесса, а определяется только состоянием системы (является функцией состояния). Это позволяет ввести новую функцию состояния S энтропию : S = [Дж/К] Понятие энтропии ввёл Клаузиус в 1865 г.
 8. Энтропия – это функция состояния термодинамичес -кой системы, изменение которой при переходе системы из некоторого состояния 1 в состояние 2 равно сумме приведенных количеств тепла, сообщенных системе при любом обратимом переходе из состояния 1 в 2. изменение энтропии в интегральной и дифференциальной формах Энтропия системы определяется с точностью до произвольной постоянной. Физический смысл имеет лишь разность энтропий. Энтропия – величина аддитивная, т. е. она равна сумме энтропий всех тел входящих в систему:
8. Энтропия – это функция состояния термодинамичес -кой системы, изменение которой при переходе системы из некоторого состояния 1 в состояние 2 равно сумме приведенных количеств тепла, сообщенных системе при любом обратимом переходе из состояния 1 в 2. изменение энтропии в интегральной и дифференциальной формах Энтропия системы определяется с точностью до произвольной постоянной. Физический смысл имеет лишь разность энтропий. Энтропия – величина аддитивная, т. е. она равна сумме энтропий всех тел входящих в систему:
 Изотермический процесс (Т 1 = Т 2) Изохорический процесс (V 1 = V 2) Изобарический процесс (Р 1 = Р 2) Адиабатический процесс Q = 0 Адиабатический процесс является изоэнтропийным
Изотермический процесс (Т 1 = Т 2) Изохорический процесс (V 1 = V 2) Изобарический процесс (Р 1 = Р 2) Адиабатический процесс Q = 0 Адиабатический процесс является изоэнтропийным
 – изменение энтропии произвольном процессе Если система замкнута δQ=0, то ΔS ≥ 0 – математическая запись II начала термодинамики: Энтропия замкнутой системы при любых происходивших в ней процессах не может убывать (она или увеличивается или остается неизменной). Если система обменивается теплом с внешней средой, то ее энтропия может вести себя любым образом. Реальные термодинамические процессы – необратимы => в них энтропия адиабатически изолированной системы неизбежно будет возрастать.
– изменение энтропии произвольном процессе Если система замкнута δQ=0, то ΔS ≥ 0 – математическая запись II начала термодинамики: Энтропия замкнутой системы при любых происходивших в ней процессах не может убывать (она или увеличивается или остается неизменной). Если система обменивается теплом с внешней средой, то ее энтропия может вести себя любым образом. Реальные термодинамические процессы – необратимы => в них энтропия адиабатически изолированной системы неизбежно будет возрастать.
 Статистический смысл энтропии Энтропия связана с микроскопическим строением системы и статистическим характером теплового движения частиц системы. Макросостояние – это состояние вещества, характеризуемое его термодинамическими параметрами. Микросостояние – это состояние системы, характеризуемое состоянием каждой входящей в нее молекулы. Термодинамической вероятностью макросостояния W называется число микросостояний, осуществляющих данное макросостояние (или число перестановок одноименных элементов, при которых сохраняется данное макросостояние).
Статистический смысл энтропии Энтропия связана с микроскопическим строением системы и статистическим характером теплового движения частиц системы. Макросостояние – это состояние вещества, характеризуемое его термодинамическими параметрами. Микросостояние – это состояние системы, характеризуемое состоянием каждой входящей в нее молекулы. Термодинамической вероятностью макросостояния W называется число микросостояний, осуществляющих данное макросостояние (или число перестановок одноименных элементов, при которых сохраняется данное макросостояние).
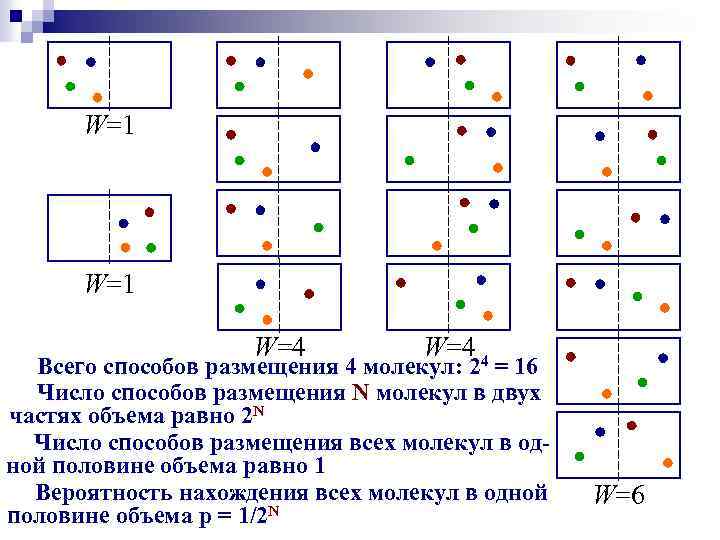 W=1 W=4 4 Всего способов размещения 4 молекул: 2 = 16 Число способов размещения N молекул в двух частях объема равно 2 N Число способов размещения всех молекул в одной половине объема равно 1 Вероятность нахождения всех молекул в одной половине объема p = 1/2 N W=6
W=1 W=4 4 Всего способов размещения 4 молекул: 2 = 16 Число способов размещения N молекул в двух частях объема равно 2 N Число способов размещения всех молекул в одной половине объема равно 1 Вероятность нахождения всех молекул в одной половине объема p = 1/2 N W=6
 Зависимость между энтропией S и термодинамической вероятностью W установил Больцман k – постоянная Больцмана Людвиг Больцман (1844– 1906) Энтропия пропорциональна логарифму термодинамической вероятности состояния Упорядоченная система имеет низкую энтропию, так как вероятность состояния наименьшая, неупорядоченная система – высокую энтропию, так как вероятность наибольшая. Энтропия (с точки зрения статистики) – мера беспорядочности теплового движения.
Зависимость между энтропией S и термодинамической вероятностью W установил Больцман k – постоянная Больцмана Людвиг Больцман (1844– 1906) Энтропия пропорциональна логарифму термодинамической вероятности состояния Упорядоченная система имеет низкую энтропию, так как вероятность состояния наименьшая, неупорядоченная система – высокую энтропию, так как вероятность наибольшая. Энтропия (с точки зрения статистики) – мера беспорядочности теплового движения.

 7. Обратимые и необратимые процессы Обратимый термодинамический процесс - это такой равновесный процесс, который допускает возможность возвращения системы в первоначальное состояние через ту же последовательность промежуточных состояний, что и в прямом процессе без каких-либо изменений в окружающих систему телах. Равновесность – важнейший признак обратимого процесса. Обратимый процесс обладает следующим свойством: если в прямом процессе система получает тепло Q и совершает работу А, то в обратном процессе она отдает тепло Q´ и над ней совершается работа А´, равные (по абсолютной величине) Q´ = Q и А´ = А в прямом процессе. При обратимом процессе всегда совершается максимальная работа.
7. Обратимые и необратимые процессы Обратимый термодинамический процесс - это такой равновесный процесс, который допускает возможность возвращения системы в первоначальное состояние через ту же последовательность промежуточных состояний, что и в прямом процессе без каких-либо изменений в окружающих систему телах. Равновесность – важнейший признак обратимого процесса. Обратимый процесс обладает следующим свойством: если в прямом процессе система получает тепло Q и совершает работу А, то в обратном процессе она отдает тепло Q´ и над ней совершается работа А´, равные (по абсолютной величине) Q´ = Q и А´ = А в прямом процессе. При обратимом процессе всегда совершается максимальная работа.
 Термодинамический процесс называется необратимым, если по его завершению систему нельзя вернуть в исходное состояние так, чтобы в окружающих телах не осталось какихлибо изменений. Все процессы в природе - необратимые. Приближением к обратимым термодинамическим процессам могут служить изопроцессы с идеальным газом.
Термодинамический процесс называется необратимым, если по его завершению систему нельзя вернуть в исходное состояние так, чтобы в окружающих телах не осталось какихлибо изменений. Все процессы в природе - необратимые. Приближением к обратимым термодинамическим процессам могут служить изопроцессы с идеальным газом.



