Презентация_тема 5.Океан.ppt
- Количество слайдов: 64
 Основы океанологии Тема 5 Строение и химический состав морской воды
Основы океанологии Тема 5 Строение и химический состав морской воды
 Две основные гипотезы, объясняющие происхождение воды на Земле. *Гипотеза «холодного» начала: гидросфера образовалась при нагреве и расплавлении первичного холодного пылевого облака. *Гипотеза «горячего» начала: первичное горячее вещество Земли, охлаждаясь, разделилось на жидкую и газообразную фазы, а дальнейшее понижение температуры привело к выделению из газообразной фазы гидросферы и атмосферы
Две основные гипотезы, объясняющие происхождение воды на Земле. *Гипотеза «холодного» начала: гидросфера образовалась при нагреве и расплавлении первичного холодного пылевого облака. *Гипотеза «горячего» начала: первичное горячее вещество Земли, охлаждаясь, разделилось на жидкую и газообразную фазы, а дальнейшее понижение температуры привело к выделению из газообразной фазы гидросферы и атмосферы
 В начальный докембрийский этап развития от 4, 5 млрд. (время начала формирования земной коры) и до 3, 6 млрд. лет назад на Земле происходила интенсивная вулканическая деятельность, в результате которой верхние слои проплавлялись, на поверхность Земли изливались базальтовые лавы. С постепенным охлаждением верхних слоев Земли (от 3, 6 до 1, 7 млрд. лет) и конденсацией водяных паров стали образовываться водные бассейны.
В начальный докембрийский этап развития от 4, 5 млрд. (время начала формирования земной коры) и до 3, 6 млрд. лет назад на Земле происходила интенсивная вулканическая деятельность, в результате которой верхние слои проплавлялись, на поверхность Земли изливались базальтовые лавы. С постепенным охлаждением верхних слоев Земли (от 3, 6 до 1, 7 млрд. лет) и конденсацией водяных паров стали образовываться водные бассейны.
 1. Земля первоначально была в расплавленном состоянии. Часть летучих компонентов после охлаждения осаждалась на поверхность Земли. Первичный океан - кислотный раствор, который растворял изверженные породы и приводил к осаждению карбонатов. Из первичных атмосферы и гидросферы начала извлекаться углекислота, что привело к возникновению условий, пригодных для существования жизни
1. Земля первоначально была в расплавленном состоянии. Часть летучих компонентов после охлаждения осаждалась на поверхность Земли. Первичный океан - кислотный раствор, который растворял изверженные породы и приводил к осаждению карбонатов. Из первичных атмосферы и гидросферы начала извлекаться углекислота, что привело к возникновению условий, пригодных для существования жизни
 2. Поступление воды за счет горячих источников. В течении 4, 5 млрд. лет они выбросили достаточное количество воды для существования океана. Вода современного океана скопилась за счет постепенного поступления из недр Земли.
2. Поступление воды за счет горячих источников. В течении 4, 5 млрд. лет они выбросили достаточное количество воды для существования океана. Вода современного океана скопилась за счет постепенного поступления из недр Земли.
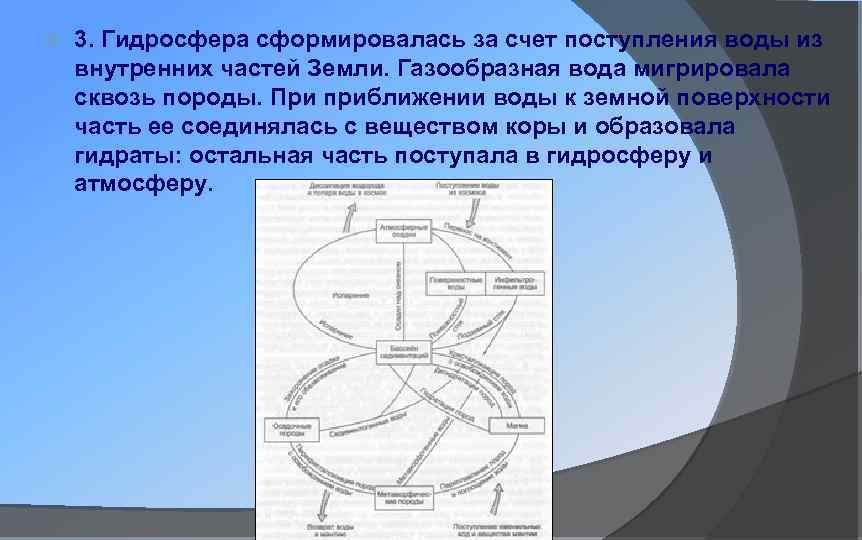 3. Гидросфера сформировалась за счет поступления воды из внутренних частей Земли. Газообразная вода мигрировала сквозь породы. При приближении воды к земной поверхности часть ее соединялась с веществом коры и образовала гидраты: остальная часть поступала в гидросферу и атмосферу.
3. Гидросфера сформировалась за счет поступления воды из внутренних частей Земли. Газообразная вода мигрировала сквозь породы. При приближении воды к земной поверхности часть ее соединялась с веществом коры и образовала гидраты: остальная часть поступала в гидросферу и атмосферу.
 5. 1. Молекулярное строение воды и ее аномалии *Вода состоит из молекул чистой воды H 2 О и составляет 99, 73% всего объема воды. *Остальной объем воды приходится на молекулярные соединения изотопов водорода Н 2 и изотопов кислорода О 17, О 18 в различных сочетаниях. *Вода, в состав которой входит изотоп водорода дейтерий, называется тяжёлой водой D 2 O.
5. 1. Молекулярное строение воды и ее аномалии *Вода состоит из молекул чистой воды H 2 О и составляет 99, 73% всего объема воды. *Остальной объем воды приходится на молекулярные соединения изотопов водорода Н 2 и изотопов кислорода О 17, О 18 в различных сочетаниях. *Вода, в состав которой входит изотоп водорода дейтерий, называется тяжёлой водой D 2 O.
 *Соединяясь, два атома водорода и один атом кислорода передают другу свои электроны, образуя устойчивую молекулу; *Молекула с общими электронами идеально удовлетворяет правилу заполнения электронных оболочек. *Водородные связи не химической природы. Они легко разрушаются и быстро восстанавливаются, что делает структуру воды исключительно изменчивой
*Соединяясь, два атома водорода и один атом кислорода передают другу свои электроны, образуя устойчивую молекулу; *Молекула с общими электронами идеально удовлетворяет правилу заполнения электронных оболочек. *Водородные связи не химической природы. Они легко разрушаются и быстро восстанавливаются, что делает структуру воды исключительно изменчивой
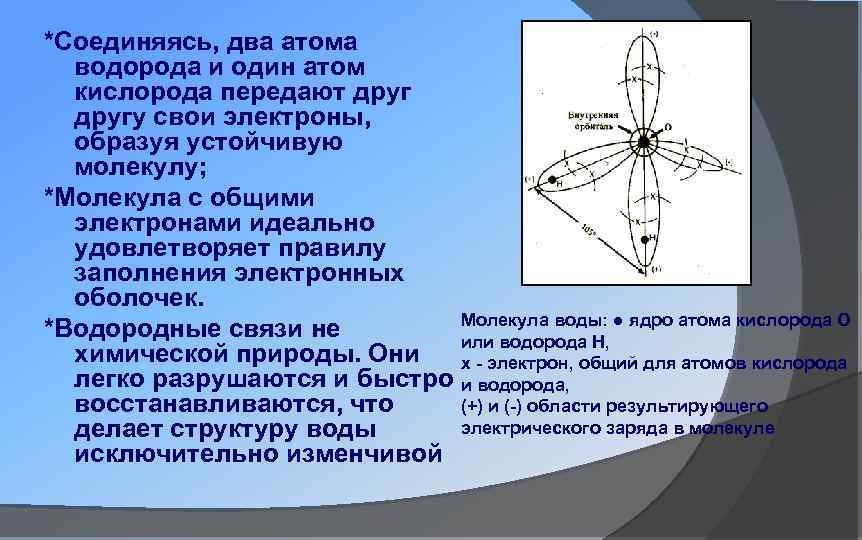 *Соединяясь, два атома водорода и один атом кислорода передают другу свои электроны, образуя устойчивую молекулу; *Молекула с общими электронами идеально удовлетворяет правилу заполнения электронных оболочек. Молекула воды: ● ядро атома кислорода О *Водородные связи не или водорода Н, химической природы. Они х - электрон, общий для атомов кислорода легко разрушаются и быстро и водорода, восстанавливаются, что (+) и (-) области результирующего электрического заряда в молекуле делает структуру воды исключительно изменчивой
*Соединяясь, два атома водорода и один атом кислорода передают другу свои электроны, образуя устойчивую молекулу; *Молекула с общими электронами идеально удовлетворяет правилу заполнения электронных оболочек. Молекула воды: ● ядро атома кислорода О *Водородные связи не или водорода Н, химической природы. Они х - электрон, общий для атомов кислорода легко разрушаются и быстро и водорода, восстанавливаются, что (+) и (-) области результирующего электрического заряда в молекуле делает структуру воды исключительно изменчивой
 1. Аномалия плотности. У воды максимальная плотность (1. 00 г·см-3) наблюдается при температуре 4 о. С, а не при температуре замерзания 0 о. С. 2. Аномалия изменения объема при замерзании. При замерзании вода увеличивает свой объем почти на 10%. 3. Аномалия удельной теплоемкости. Теплоемкость воды в 3100 раз больше, чем у воздуха, в 4 раза больше, чем у горных пород. 4. Аномалия теплоты плавления. Вода обладает высокой удельной теплотой плавления. Теплота плавления льда равна 79, 7 кал·г-1. 5. Аномалия скрытой теплоты парообразования. Огромное количество тепла принадлежит воде в парообразной фазе. 6. Аномалия диэлектрической постоянной. Диэлектрическая постоянная при 20°С равна 81 единице, а у большинства других веществ она находится в пределах от 2 до 3 единиц. Прямым следствием большая способность к растворению различных веществ. 7. Аномалия коэффициенат преломления света. Коэффициент преломления света в воде 1. 34. По волновой теории света он должен быть равным 9.
1. Аномалия плотности. У воды максимальная плотность (1. 00 г·см-3) наблюдается при температуре 4 о. С, а не при температуре замерзания 0 о. С. 2. Аномалия изменения объема при замерзании. При замерзании вода увеличивает свой объем почти на 10%. 3. Аномалия удельной теплоемкости. Теплоемкость воды в 3100 раз больше, чем у воздуха, в 4 раза больше, чем у горных пород. 4. Аномалия теплоты плавления. Вода обладает высокой удельной теплотой плавления. Теплота плавления льда равна 79, 7 кал·г-1. 5. Аномалия скрытой теплоты парообразования. Огромное количество тепла принадлежит воде в парообразной фазе. 6. Аномалия диэлектрической постоянной. Диэлектрическая постоянная при 20°С равна 81 единице, а у большинства других веществ она находится в пределах от 2 до 3 единиц. Прямым следствием большая способность к растворению различных веществ. 7. Аномалия коэффициенат преломления света. Коэффициент преломления света в воде 1. 34. По волновой теории света он должен быть равным 9.
 Химический состав морской воды *Из-за уникальной растворяющей способности воды до сих пор не удалось получить химически чистую воду - она всегда содержит растворенный материал сосуда. Поэтому в природе не встречается химически чистая вода. *Особенностью морской воды - она представляет слабый ионизированный молекулярный или коллоидный раствор, содержащий большое количество частиц. *Размеры растворенных в морской воде частиц весьма разнообразны в зависимости от близости берега.
Химический состав морской воды *Из-за уникальной растворяющей способности воды до сих пор не удалось получить химически чистую воду - она всегда содержит растворенный материал сосуда. Поэтому в природе не встречается химически чистая вода. *Особенностью морской воды - она представляет слабый ионизированный молекулярный или коллоидный раствор, содержащий большое количество частиц. *Размеры растворенных в морской воде частиц весьма разнообразны в зависимости от близости берега.
 Химический состав морской воды 1) главные ионы (хлор, натрий, сульфат, магний, кальций, калий, бикарбонат, бром, барит, стронций, фтор), которые составляют 99. 98% массы всех растворенных веществ; 2) растворенные газы (O 2, N 2, CO 2, H 2 S, Ar и другие инертные газы; 3) биогенные элементы (С, Н, N, P, Si, Fe, Mn) и их соединения, из которых состоят морские организмы; 4) группа микроэлементов с концентрацией меньше 1 × 10 -6; 5) органические вещества.
Химический состав морской воды 1) главные ионы (хлор, натрий, сульфат, магний, кальций, калий, бикарбонат, бром, барит, стронций, фтор), которые составляют 99. 98% массы всех растворенных веществ; 2) растворенные газы (O 2, N 2, CO 2, H 2 S, Ar и другие инертные газы; 3) биогенные элементы (С, Н, N, P, Si, Fe, Mn) и их соединения, из которых состоят морские организмы; 4) группа микроэлементов с концентрацией меньше 1 × 10 -6; 5) органические вещества.
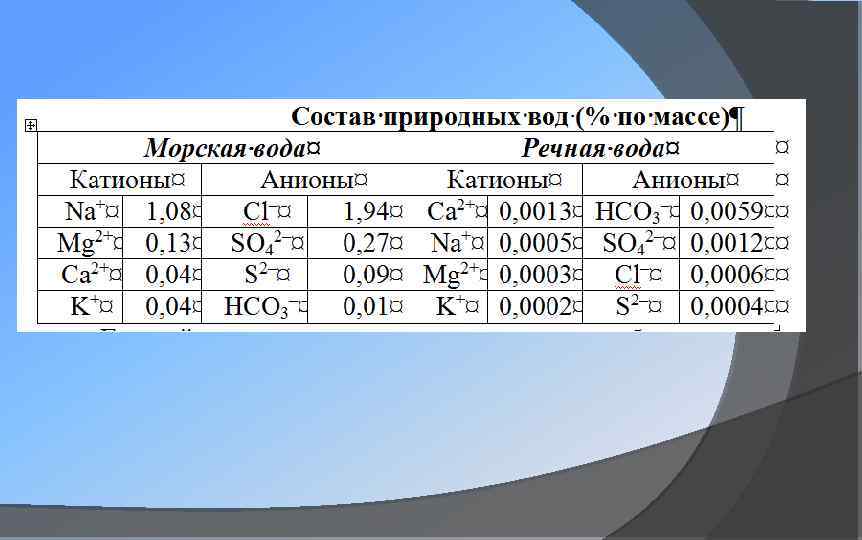
 Основные соединения: 1) хлориды (Na. Cl, Mg. Cl 2, KCl) - обусловливают горько-соленый вкус воды; 2) сульфаты (Mg. S 04, Ca. S 04, K 2 S 04). 3) карбонаты (Са. СОз). *В морской воде преобладают хлориды Na. Cl (около 78%), Mg. Cl 2 (>9%), KCl (около 2%) *сульфаты - Mg. SO 4 (свыше 6. 5%), Ca. SO 4 (около 3. 5%) *Гидрокарбонаты менее 1%.
Основные соединения: 1) хлориды (Na. Cl, Mg. Cl 2, KCl) - обусловливают горько-соленый вкус воды; 2) сульфаты (Mg. S 04, Ca. S 04, K 2 S 04). 3) карбонаты (Са. СОз). *В морской воде преобладают хлориды Na. Cl (около 78%), Mg. Cl 2 (>9%), KCl (около 2%) *сульфаты - Mg. SO 4 (свыше 6. 5%), Ca. SO 4 (около 3. 5%) *Гидрокарбонаты менее 1%.
 *Общее содержание твердых веществ, растворенных в морской воде, выражают в тысячных долях весовых единиц - промилле и обозначают знаком ‰. *Содержание растворенных твердых веществ, выраженное в промилле, численно равно их весу в граммах в одном килограмме морской воды.
*Общее содержание твердых веществ, растворенных в морской воде, выражают в тысячных долях весовых единиц - промилле и обозначают знаком ‰. *Содержание растворенных твердых веществ, выраженное в промилле, численно равно их весу в граммах в одном килограмме морской воды.
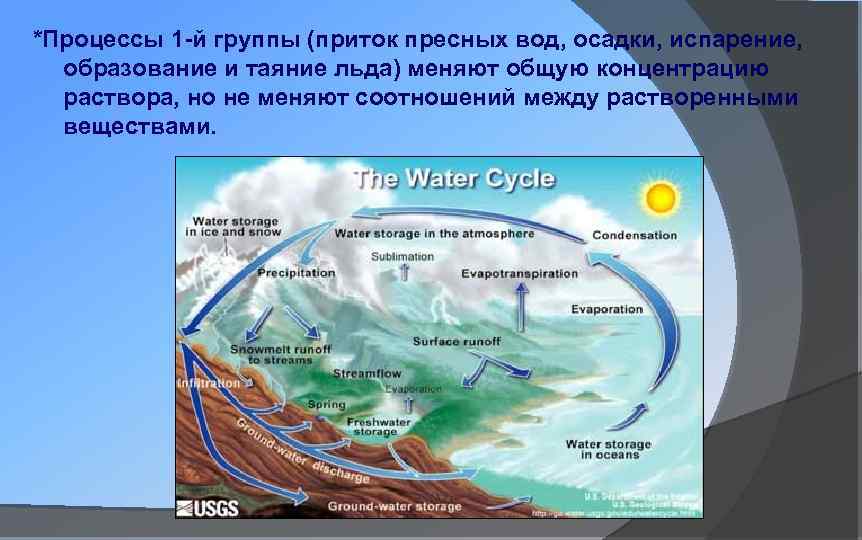 *Процессы 1 -й группы (приток пресных вод, осадки, испарение, образование и таяние льда) меняют общую концентрацию раствора, но не меняют соотношений между растворенными веществами.
*Процессы 1 -й группы (приток пресных вод, осадки, испарение, образование и таяние льда) меняют общую концентрацию раствора, но не меняют соотношений между растворенными веществами.
 *Процессы 2 -й группы: -фотосинтез растений и дыхание животных - деятельность бактерий и морских организмов, расходующих химические вещества на постройку своих скелетов и панцирей -растворение донных отложений - Эти процессы меняют соотношение между растворенными в воде веществами, которые в значительной мере определяют условия жизни в океане.
*Процессы 2 -й группы: -фотосинтез растений и дыхание животных - деятельность бактерий и морских организмов, расходующих химические вещества на постройку своих скелетов и панцирей -растворение донных отложений - Эти процессы меняют соотношение между растворенными в воде веществами, которые в значительной мере определяют условия жизни в океане.
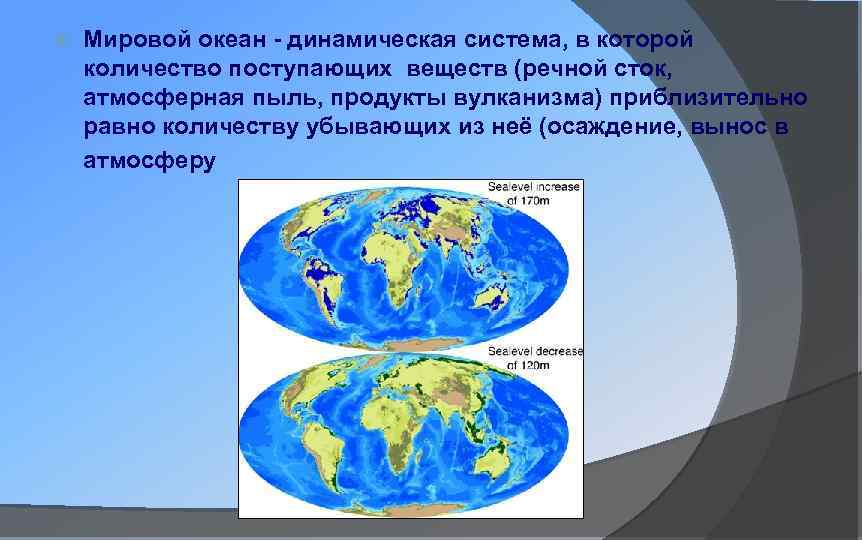 Мировой океан - динамическая система, в которой количество поступающих веществ (речной сток, атмосферная пыль, продукты вулканизма) приблизительно равно количеству убывающих из неё (осаждение, вынос в атмосферу
Мировой океан - динамическая система, в которой количество поступающих веществ (речной сток, атмосферная пыль, продукты вулканизма) приблизительно равно количеству убывающих из неё (осаждение, вынос в атмосферу
 *Соленость - общий вес в граммах всех твердых веществ, растворенных в 1000 граммах морской воды, при условии, что фтор, бром, иод замещены эквивалентным количеством хлора, все карбонаты превращены в окислы и все органические вещества сожжены *Средняя солёность вод Мирового океана близка к 35. 0‰. *Соотношение между соленостью S и содержанием хлора Сl – хлорный коэффициент - выражается формулой: S= 1. 80655 Сl ‰
*Соленость - общий вес в граммах всех твердых веществ, растворенных в 1000 граммах морской воды, при условии, что фтор, бром, иод замещены эквивалентным количеством хлора, все карбонаты превращены в окислы и все органические вещества сожжены *Средняя солёность вод Мирового океана близка к 35. 0‰. *Соотношение между соленостью S и содержанием хлора Сl – хлорный коэффициент - выражается формулой: S= 1. 80655 Сl ‰
 Образование газов в морской воде: *Обмен с атмосферой *Газовые эманации недр (вулканизм, в т. ч газово-грязевой) *Биологическая деятельность *Речной сток
Образование газов в морской воде: *Обмен с атмосферой *Газовые эманации недр (вулканизм, в т. ч газово-грязевой) *Биологическая деятельность *Речной сток
 Фонтан газа грязевого вулкана Двуреченского в 2003 г.
Фонтан газа грязевого вулкана Двуреченского в 2003 г.
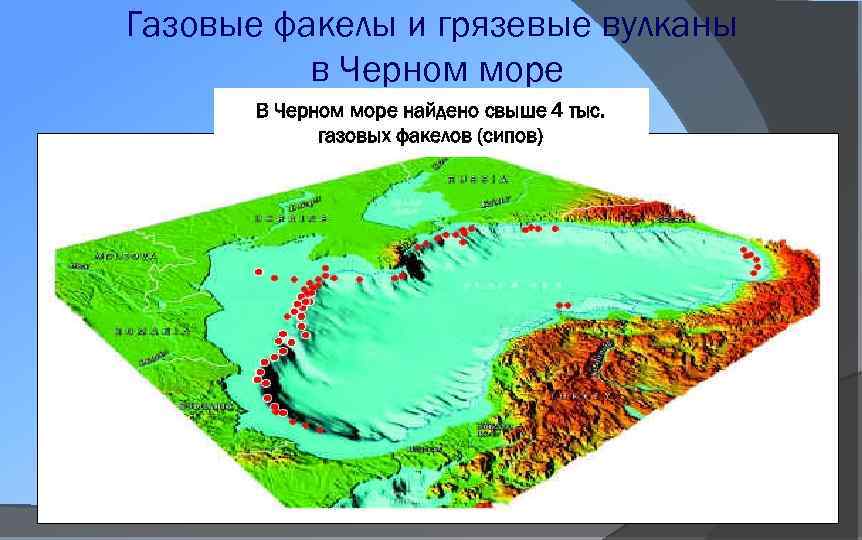 Газовые факелы и грязевые вулканы в Черном море В Черном море найдено свыше 4 тыс. газовых факелов (сипов)
Газовые факелы и грязевые вулканы в Черном море В Черном море найдено свыше 4 тыс. газовых факелов (сипов)
 Содержание газов обычно выражают в процентах от его насыщающего количества и называют относительным содержанием. За насыщающее принимают то количество газа, которое может раствориться в воде данной температуры и солености при нормальной сухой атмосфере и давлении 1013 мб.
Содержание газов обычно выражают в процентах от его насыщающего количества и называют относительным содержанием. За насыщающее принимают то количество газа, которое может раствориться в воде данной температуры и солености при нормальной сухой атмосфере и давлении 1013 мб.
 *Растворенный кислород O 2 *Важнейший биогидрохимический показатель состояния среды. Обеспечивает существование водных организмов и определяет интенсивность окислительных процессов в морях и океанах *На некоторых глубинах в верхнем слое образование и расход кислорода примерно одинаковы. *Эти глубины называют слоями компенсации. *Слои перемещаются по вертикали в зависимости от физикохимических, гидробиологических условий и подводной освещенности
*Растворенный кислород O 2 *Важнейший биогидрохимический показатель состояния среды. Обеспечивает существование водных организмов и определяет интенсивность окислительных процессов в морях и океанах *На некоторых глубинах в верхнем слое образование и расход кислорода примерно одинаковы. *Эти глубины называют слоями компенсации. *Слои перемещаются по вертикали в зависимости от физикохимических, гидробиологических условий и подводной освещенности
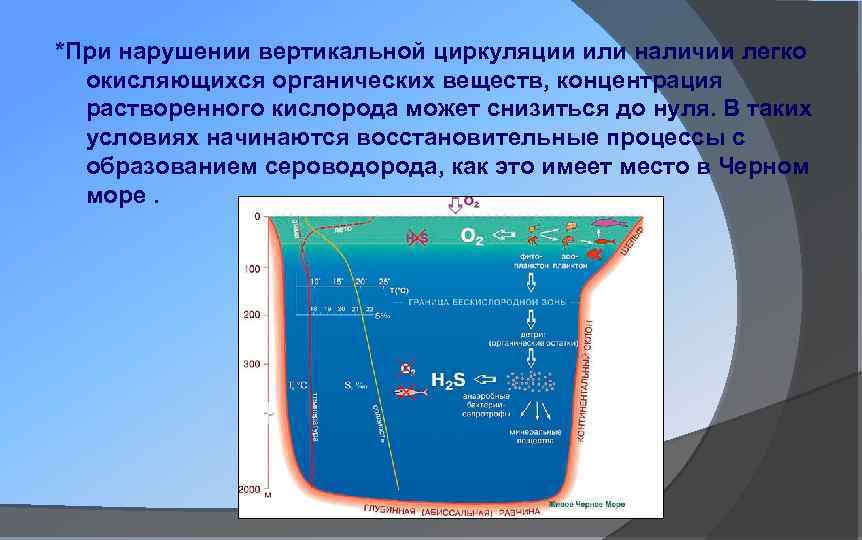 *При нарушении вертикальной циркуляции или наличии легко окисляющихся органических веществ, концентрация растворенного кислорода может снизиться до нуля. В таких условиях начинаются восстановительные процессы с образованием сероводорода, как это имеет место в Черном море.
*При нарушении вертикальной циркуляции или наличии легко окисляющихся органических веществ, концентрация растворенного кислорода может снизиться до нуля. В таких условиях начинаются восстановительные процессы с образованием сероводорода, как это имеет место в Черном море.
 *Гипоксия или дефицит кислорода вызывает «заморы» рыбы, обычно наблюдается в предустьевых районах и мелководных
*Гипоксия или дефицит кислорода вызывает «заморы» рыбы, обычно наблюдается в предустьевых районах и мелководных
 Растворенный азот N 2 *В поверхностных слоях относительное содержание всегда близко к 100% и обычно уменьшается с глубиной. *Избыток азота образуется за счет восстановления нитратов и распада органических веществ.
Растворенный азот N 2 *В поверхностных слоях относительное содержание всегда близко к 100% и обычно уменьшается с глубиной. *Избыток азота образуется за счет восстановления нитратов и распада органических веществ.
 *Азотфиксация-растворенный азот усваивается азотофикси-рующими бактериями и перерабатывается ими в азотистые соединения, которые затем поглощаются растениями *Жизнь на Земле существует за счет азота, связанного азотфиксирующими бактериями (цианобактерии) *Цианобактерии «подстраивают» связывание азота под имеющийся фосфор. При разрушении клеток планктона вода обогащается азотом и фосфором в соотношении N : P = 16 : 1.
*Азотфиксация-растворенный азот усваивается азотофикси-рующими бактериями и перерабатывается ими в азотистые соединения, которые затем поглощаются растениями *Жизнь на Земле существует за счет азота, связанного азотфиксирующими бактериями (цианобактерии) *Цианобактерии «подстраивают» связывание азота под имеющийся фосфор. При разрушении клеток планктона вода обогащается азотом и фосфором в соотношении N : P = 16 : 1.
 *За счет азотфиксации в океан из атмосферы попадает 140 миллионов т азота в год. * Примерно такое же количество азота возвращается в атмосферу в результате денитрификации — восстановления нитратов. * Азот связывается азотфиксаторами поблизости от тех мест, где он наиболее активно теряется в ходе денитрификации. Такие области выявлены, в частности, в Тихом океане и в Аравийском море.
*За счет азотфиксации в океан из атмосферы попадает 140 миллионов т азота в год. * Примерно такое же количество азота возвращается в атмосферу в результате денитрификации — восстановления нитратов. * Азот связывается азотфиксаторами поблизости от тех мест, где он наиболее активно теряется в ходе денитрификации. Такие области выявлены, в частности, в Тихом океане и в Аравийском море.
 Сероводород H 2 S *Появляется на глубине при дефиците кислорода и в результате слабого вертикального обмена. *Присутствует в некоторых глубоких фиордах Норвегии, в Балтийском, Каспийском, Черном и Аравийском морях. *Образование сероводорода в морской воде объясняется чаще всего деятельностью гнилостных бактерий, разлагающих органический белок и сероводородных (анаэробных) бактерий
Сероводород H 2 S *Появляется на глубине при дефиците кислорода и в результате слабого вертикального обмена. *Присутствует в некоторых глубоких фиордах Норвегии, в Балтийском, Каспийском, Черном и Аравийском морях. *Образование сероводорода в морской воде объясняется чаще всего деятельностью гнилостных бактерий, разлагающих органический белок и сероводородных (анаэробных) бактерий
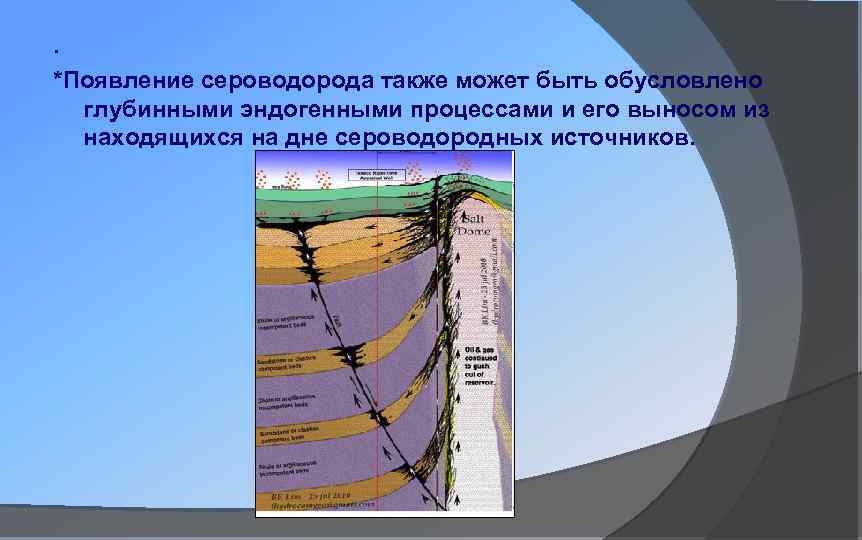 . *Появление сероводорода также может быть обусловлено глубинными эндогенными процессами и его выносом из находящихся на дне сероводородных источников.
. *Появление сероводорода также может быть обусловлено глубинными эндогенными процессами и его выносом из находящихся на дне сероводородных источников.
 *2 млрд лет назад в океанах содержался высокий уровень сероводорода и мало кислорода. *Лишь 580 млн лет назад океан насытился кислородом, началась эволюция высших форм жизни. Животные появились на Земле довольно внезапно и сравнительно поздно в геологической летописи.
*2 млрд лет назад в океанах содержался высокий уровень сероводорода и мало кислорода. *Лишь 580 млн лет назад океан насытился кислородом, началась эволюция высших форм жизни. Животные появились на Земле довольно внезапно и сравнительно поздно в геологической летописи.
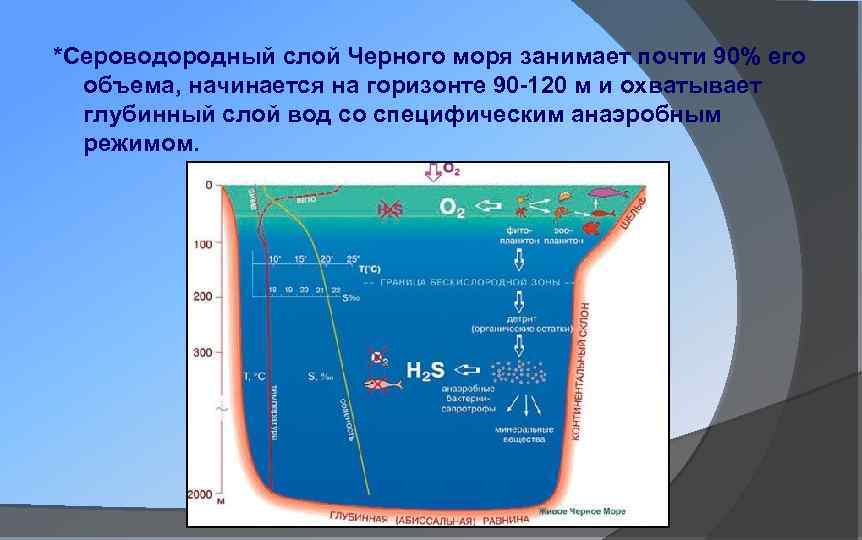 *Сероводородный слой Черного моря занимает почти 90% его объема, начинается на горизонте 90 -120 м и охватывает глубинный слой вод со специфическим анаэробным режимом.
*Сероводородный слой Черного моря занимает почти 90% его объема, начинается на горизонте 90 -120 м и охватывает глубинный слой вод со специфическим анаэробным режимом.
 *При отсутствии свободного кислорода отмершая органика поглощается сульфатредуцирующими бактериями. *Используя кислород, входящий в сульфатные соединения, они окисляют органику и продуцируют сероводород: 2 CHOH+SO 42 - бактериальное разложение S 2 - + 2 CO 2 +2 H 2 O, S 2 - + 2 H+ H 2 S *При наличии в морской воде нитратов окисление сероводорода осуществляется и денитрифицирующими бактериями.
*При отсутствии свободного кислорода отмершая органика поглощается сульфатредуцирующими бактериями. *Используя кислород, входящий в сульфатные соединения, они окисляют органику и продуцируют сероводород: 2 CHOH+SO 42 - бактериальное разложение S 2 - + 2 CO 2 +2 H 2 O, S 2 - + 2 H+ H 2 S *При наличии в морской воде нитратов окисление сероводорода осуществляется и денитрифицирующими бактериями.
 *В 1982 г. - резкий куполообразный подъем сероводородсодержащих масс до глубины 60 м и внедрение его в фотический слой. *Эти процессы - доказательство вихревых перемещений и трансформаций Черноморских вод. *Содержание сероводорода с глубиной 250 м - 300 м - 1. 10 -4 моль/л; 500 м – 2, 5. 10 -4 моль/л; 2000 м – 3. 10 -4 моль/л.
*В 1982 г. - резкий куполообразный подъем сероводородсодержащих масс до глубины 60 м и внедрение его в фотический слой. *Эти процессы - доказательство вихревых перемещений и трансформаций Черноморских вод. *Содержание сероводорода с глубиной 250 м - 300 м - 1. 10 -4 моль/л; 500 м – 2, 5. 10 -4 моль/л; 2000 м – 3. 10 -4 моль/л.
 *Сульфатредуцирующие бактерии, разлагающие органическое вещество и высвобождающие неорганические биогены, участвуют в круговороте веществ Черного моря. * В результате процессов перемешивания и апвеллинга морских вод биогены возвращаются в поверхностные, богатые кислородом горизонты и утилизируются фитопланктоном.
*Сульфатредуцирующие бактерии, разлагающие органическое вещество и высвобождающие неорганические биогены, участвуют в круговороте веществ Черного моря. * В результате процессов перемешивания и апвеллинга морских вод биогены возвращаются в поверхностные, богатые кислородом горизонты и утилизируются фитопланктоном.
 Углекислый газ или двуокись углерода CO 2 *Источники: атмосфера, дыхание растений, разложение органики, извержение вулканов, поствулканические процессы. *Расходуется на фотосинтез растений и образование морскими организмами скелетов и раковин.
Углекислый газ или двуокись углерода CO 2 *Источники: атмосфера, дыхание растений, разложение органики, извержение вулканов, поствулканические процессы. *Расходуется на фотосинтез растений и образование морскими организмами скелетов и раковин.
 *Углекислый газ растворяется в воде в значительно больших количествах, чем кислород и азот. Он находится в морской воде частью в растворенном, свободном состоянии, частью в химически связанной форме бикарбонатов Са(НСОз)2 или карбонатов (Са. СОз).
*Углекислый газ растворяется в воде в значительно больших количествах, чем кислород и азот. Он находится в морской воде частью в растворенном, свободном состоянии, частью в химически связанной форме бикарбонатов Са(НСОз)2 или карбонатов (Са. СОз).
 *Растворимость CO 2 в морской воде возрастает с понижением температуры. *Холодные воды Арктики и вообще высоких широт содержат больше углекислого газа, чем воды низких широт. *Значительное содержание CO 2 отмечается в придонных холодных водах на глубинах ниже 40005000 м, что сказывается на растворении известковых раковин.
*Растворимость CO 2 в морской воде возрастает с понижением температуры. *Холодные воды Арктики и вообще высоких широт содержат больше углекислого газа, чем воды низких широт. *Значительное содержание CO 2 отмечается в придонных холодных водах на глубинах ниже 40005000 м, что сказывается на растворении известковых раковин.
 Щелочной резерв. Активная реакция морской воды. *Морская вода обладает свойствами щелочи. *Щелочность морской воды определяется щелочным резервом - количеством кислоты, которое надо прибавить к определенному объему воды, чтобы в ней не оставалось карбонатных и бикарбонатных ионов и недиссоциированных молекул угольной кислоты.
Щелочной резерв. Активная реакция морской воды. *Морская вода обладает свойствами щелочи. *Щелочность морской воды определяется щелочным резервом - количеством кислоты, которое надо прибавить к определенному объему воды, чтобы в ней не оставалось карбонатных и бикарбонатных ионов и недиссоциированных молекул угольной кислоты.
 *Первая и вторая диссоциации угольной кислоты приводят к образованию водородных ионов. *Активную реакцию равновесие между бикарбонатами. морской угольной воды р. Н характеризует кислотой, карбонатами и *Бикарбонаты и карбонаты делают морскую воду щелочной, угольная кислота - кислой.
*Первая и вторая диссоциации угольной кислоты приводят к образованию водородных ионов. *Активную реакцию равновесие между бикарбонатами. морской угольной воды р. Н характеризует кислотой, карбонатами и *Бикарбонаты и карбонаты делают морскую воду щелочной, угольная кислота - кислой.
 *1 л нормальной воды содержится 1· 10 -7 водородных ионов. Эту концентрацию ионов обычно обозначают десятичным логарифмом с обратным знаком, т. е. p. H = - lg [Н+]. Если р. Н=7 вода является нейтральной; если р. Н >7 вода обладает щелочными свойствами, если р. Н <7 - кислотными. *Наибольших значений (8, 0 -8, 35) р. Н достигает в поверхностном слое океана благодаря интенсивному потреблению CO 2 при фотосинтезе. * С увеличением глубины р. Н уменьшается, что связано с увеличением концентрации CO 2.
*1 л нормальной воды содержится 1· 10 -7 водородных ионов. Эту концентрацию ионов обычно обозначают десятичным логарифмом с обратным знаком, т. е. p. H = - lg [Н+]. Если р. Н=7 вода является нейтральной; если р. Н >7 вода обладает щелочными свойствами, если р. Н <7 - кислотными. *Наибольших значений (8, 0 -8, 35) р. Н достигает в поверхностном слое океана благодаря интенсивному потреблению CO 2 при фотосинтезе. * С увеличением глубины р. Н уменьшается, что связано с увеличением концентрации CO 2.
 Биогенные элементы (С, Н, N, P, Si, Fe, Mn) и их соединения (bios – жизнь и gennein – производить) * Соединения фосфора, азота и кремния в океане – элементы биогенного цикла, это то же самое, что и азотные и фосфатные удобрения, необходимые для роста сельскохозяйственных культур на суше.
Биогенные элементы (С, Н, N, P, Si, Fe, Mn) и их соединения (bios – жизнь и gennein – производить) * Соединения фосфора, азота и кремния в океане – элементы биогенного цикла, это то же самое, что и азотные и фосфатные удобрения, необходимые для роста сельскохозяйственных культур на суше.
 *Соединения фосфора (фосфаты) *Физиологически важный компонент химического состава морских вод, определяющий их продуктивность. *Чрезмерная концентрация приводит к повышенному потреблению кислорода. В таких случаях соединения фосфора рассматривают как загрязняющие вещества.
*Соединения фосфора (фосфаты) *Физиологически важный компонент химического состава морских вод, определяющий их продуктивность. *Чрезмерная концентрация приводит к повышенному потреблению кислорода. В таких случаях соединения фосфора рассматривают как загрязняющие вещества.
 соли кремниевой кислоты *Используются многими водорослями, в частности, диатомовыми для построения клетки. *Изменения в содержании кремния позволяют судить об изменениях в режиме вод
соли кремниевой кислоты *Используются многими водорослями, в частности, диатомовыми для построения клетки. *Изменения в содержании кремния позволяют судить об изменениях в режиме вод
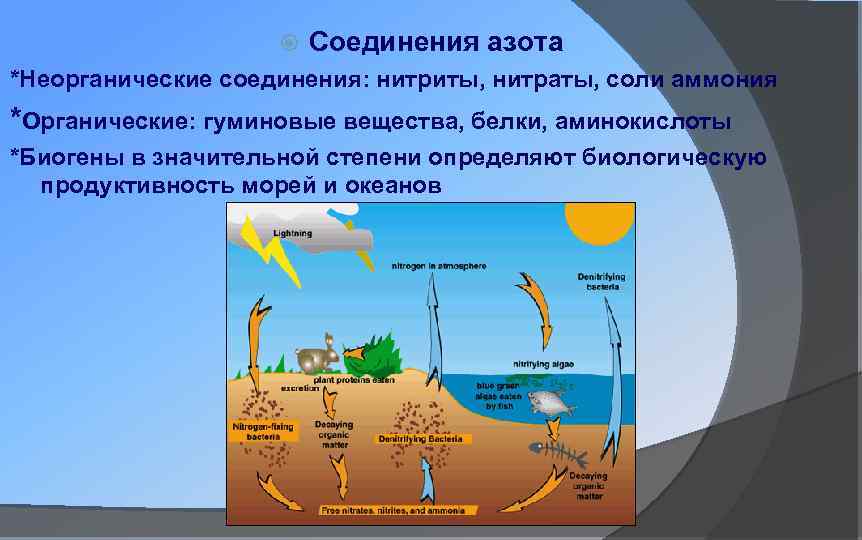 Соединения азота *Неорганические соединения: нитриты, нитраты, соли аммония *Органические: гуминовые вещества, белки, аминокислоты *Биогены в значительной степени определяют биологическую продуктивность морей и океанов
Соединения азота *Неорганические соединения: нитриты, нитраты, соли аммония *Органические: гуминовые вещества, белки, аминокислоты *Биогены в значительной степени определяют биологическую продуктивность морей и океанов
 Нитриты (NO 2)находятся в местах значительного скопления органического вещества отмерших организмов.
Нитриты (NO 2)находятся в местах значительного скопления органического вещества отмерших организмов.
 *Огромное количество биогенных элементов (нитратов, нитритов, фосфатов) поступает ежедневно в воды озера, вызывая бурный рост и размножение одноклеточных водорослей.
*Огромное количество биогенных элементов (нитратов, нитритов, фосфатов) поступает ежедневно в воды озера, вызывая бурный рост и размножение одноклеточных водорослей.
 *Нитраты (NO 3) *Необходимы для морского фитопланктона *Отсутствие приводит к угнетению водорослей, снижению интенсивности процесса фотосинтеза. * Воды, богатые нитратами, например антарктические, отличаются высокой продуктивностью.
*Нитраты (NO 3) *Необходимы для морского фитопланктона *Отсутствие приводит к угнетению водорослей, снижению интенсивности процесса фотосинтеза. * Воды, богатые нитратами, например антарктические, отличаются высокой продуктивностью.
 Человек нуждается в течение дня в 5 мг нитратов на кг тела. - Симптом отравления нитратами у человека возникает, когда он употребил около 10 грамм
Человек нуждается в течение дня в 5 мг нитратов на кг тела. - Симптом отравления нитратами у человека возникает, когда он употребил около 10 грамм
 Антарктида
Антарктида




 Криль
Криль
 Аммонийный азот NH 4 *Первичный продукт обмена веществ *Результат полной минерализации органических остатков. *Аммонийный азот, нитраты, нитриты и фосфор выполняют важнейшие биохимические функции. *Азот входит в состав белков, аминокислот и многих других органических соединений, без которых невозможно существование живых клеток.
Аммонийный азот NH 4 *Первичный продукт обмена веществ *Результат полной минерализации органических остатков. *Аммонийный азот, нитраты, нитриты и фосфор выполняют важнейшие биохимические функции. *Азот входит в состав белков, аминокислот и многих других органических соединений, без которых невозможно существование живых клеток.
 *Аммонийный азот потребляется фитопланктоном в процессе фотосинтеза *Знание концентрации аммонийного азота необходимо для оценки биологической продуктивности моря и интенсивности минерализации органических веществ.
*Аммонийный азот потребляется фитопланктоном в процессе фотосинтеза *Знание концентрации аммонийного азота необходимо для оценки биологической продуктивности моря и интенсивности минерализации органических веществ.
 *Биогены совершают непрерывный круговорот. Они потребляются водными растениями при фотосинтезе в верхнем, освещенном слое океана. *Восстановление биогенов происходит в поверхностной продуктивной зоне океана, либо в процессе разложения отмерших организмов в глубинных слоях. *Вынос их в продуктивную зону осуществляется турбулентным перемешиванием и вертикальной циркуляцией, особенно в областях подъема вод (зонах апвеллинга). *
*Биогены совершают непрерывный круговорот. Они потребляются водными растениями при фотосинтезе в верхнем, освещенном слое океана. *Восстановление биогенов происходит в поверхностной продуктивной зоне океана, либо в процессе разложения отмерших организмов в глубинных слоях. *Вынос их в продуктивную зону осуществляется турбулентным перемешиванием и вертикальной циркуляцией, особенно в областях подъема вод (зонах апвеллинга). *
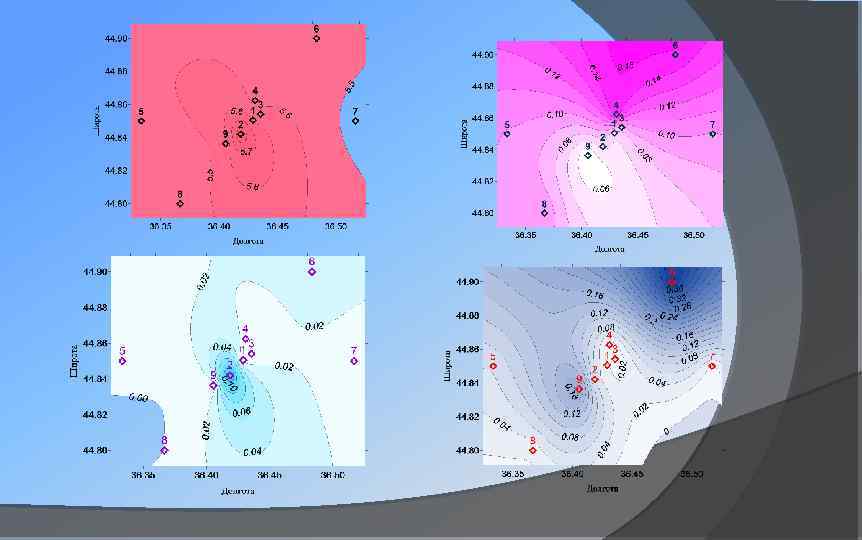
 Распределение содержания хлорофилла в мг/м 3 *Центральные части океанов (фиолетовые ) - «биологические пустыни» , развитие фитопланктона ограничено дефицитом биогенов— азота и фосфора. *Высоко-продуктивные районы (зеленые и желтые) - Северная Атлантика, северная часть Тихого океана, воды, примыкающие к Антарктиде, и прибрежные области
Распределение содержания хлорофилла в мг/м 3 *Центральные части океанов (фиолетовые ) - «биологические пустыни» , развитие фитопланктона ограничено дефицитом биогенов— азота и фосфора. *Высоко-продуктивные районы (зеленые и желтые) - Северная Атлантика, северная часть Тихого океана, воды, примыкающие к Антарктиде, и прибрежные области
 Микроэлементы *Суммарная концентрация микроэлементов меньше 0. 01% суммы главных ионов. *Максимум: Серебро 3· 10– 3 %, литий 1, 5· 10– 5 %, иод 6· 10– 6 %, цинк 1· 10– 6 %, железо 1· 10– 6 %. *Минимум: Золото 4· 10– 10 % и кадмий 1· 10– 8 %. *Моллюски, фильтруя воду в процессе дыхания и питания, концентрируют ванадий, медь, цинк, кобальт, свинец.
Микроэлементы *Суммарная концентрация микроэлементов меньше 0. 01% суммы главных ионов. *Максимум: Серебро 3· 10– 3 %, литий 1, 5· 10– 5 %, иод 6· 10– 6 %, цинк 1· 10– 6 %, железо 1· 10– 6 %. *Минимум: Золото 4· 10– 10 % и кадмий 1· 10– 8 %. *Моллюски, фильтруя воду в процессе дыхания и питания, концентрируют ванадий, медь, цинк, кобальт, свинец.
 *Органика в океане непрерывно появляется в виде первичной продукции - зеленой массы растений *Одновременно происходит потребление органического вещества, его отмирание и разложение. *Остатки отмерших организмов находятся в воде океана в виде взвеси. *Их биохимический распад источник растворенных органических веществ (молекулярные и коллоидные соединения)
*Органика в океане непрерывно появляется в виде первичной продукции - зеленой массы растений *Одновременно происходит потребление органического вещества, его отмирание и разложение. *Остатки отмерших организмов находятся в воде океана в виде взвеси. *Их биохимический распад источник растворенных органических веществ (молекулярные и коллоидные соединения)
 Интенсивная хозяйственная деятельность человека привела к нарушению природных процессов не только в пресных водоемах, но и во многих прибрежных областях морей и океанов. Месторождение Субботина Концентрация меди и нефтепродуктов
Интенсивная хозяйственная деятельность человека привела к нарушению природных процессов не только в пресных водоемах, но и во многих прибрежных областях морей и океанов. Месторождение Субботина Концентрация меди и нефтепродуктов


