Основы общей химии.pptx
- Количество слайдов: 14

ОСНОВЫ ОБЩЕЙ ХИМИИ. ОСНОВНЫЕ ПОНЯТИЯ И ЗАКОНЫ Презентацию предоставил Семеняченко Александр (РГК -13)

Предмет Химии Химические элементы и их соединения, а также закономерности, которым подчиняются различные химические реакции. Зачатки химии возникли со времен первых представителей вида «человек разумный» , то есть около 39000 лет назад. Как самостоятельная дисциплина определилась в XVI-XVII веках, после ряда научных открытий, обосновавших механистическую картину мира, создания фабрик, появления буржуазного общества.

Вещество и его свойства Вещество – это форма материи, состоящая из частиц, обладающих массой покоя. Каждое вещество имеет определенный состав. Оно состоит из молекул, атомов и ионов. Молекула – это наименьшая частица вещества, которая сохраняет химические свойства данного вещества. Атом – наименьшая, химически неделимая частица. Ион – атом или группа атомов, которые имеют электрический заряд. Свойство – это качественная и количественная характеристика физического тела или явления.

Химический элемент Это одинаковый вид атомов, характеризующийся определенным зарядом ядра и присущим только ему строением электронных оболочек. В настоящее время известно 110 химических элементов: 89 существует в природе, остальные получены искусственно. Атомный номер Z равен числу протонов в атомном ядре. В электронной оболочке электронейтрального атома содержится Z электронов. Массовое число A равно числу протонов Z и числу нейтронов N в атомном ядре: A=Z+N Нуклиды – атомы с определенным числом протонов и нейтронов.
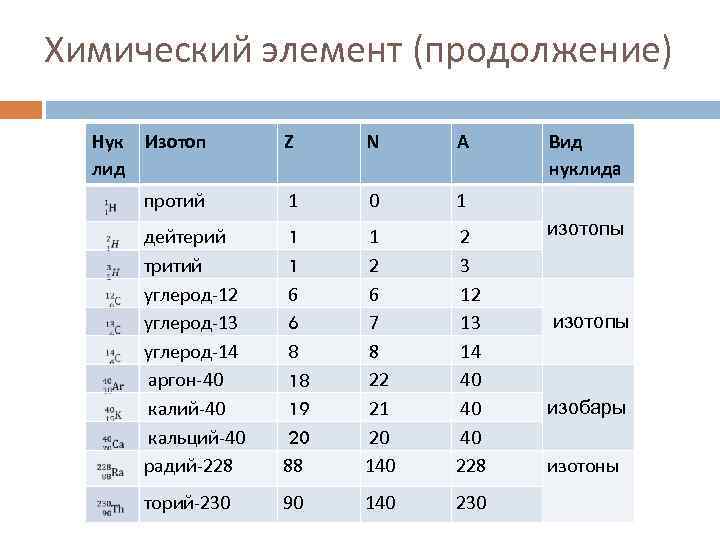
Химический элемент (продолжение) Нук лид Изотоп Z N A Вид нуклида протий 1 0 1 дейтерий тритий углерод-12 углерод-13 углерод-14 аргон-40 калий-40 кальций-40 радий-228 1 1 6 6 8 18 19 20 88 1 2 6 7 8 22 21 20 140 2 3 12 13 14 40 40 40 228 изотопы торий-230 90 140 230 изотопы изобары изотоны

Химическая формула вещества Химическая формула – это изображение состава вещества при помощи символов элементов и числовых индексов. Химическая формула показывает, атом каких элементов и в каких относительных количествах составляют данное вещество.
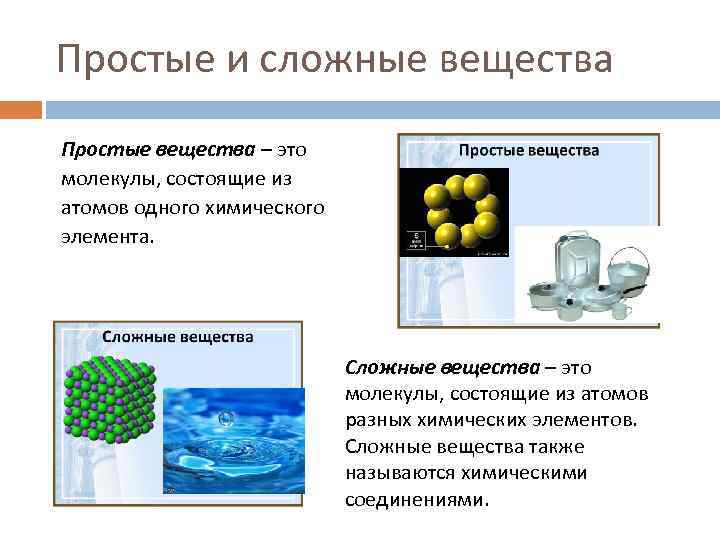
Простые и сложные вещества Простые вещества – это молекулы, состоящие из атомов одного химического элемента. Сложные вещества – это молекулы, состоящие из атомов разных химических элементов. Сложные вещества также называются химическими соединениями.

Аллотропия – это способность химических элементов существовать в виде нескольких простых веществ. Например, у кислорода два аллотропических видоизменения (модификации) – кислород и озон, у углерода – алмаз и графит, у фосфора три модификации – белый, красный и черный фосфор.

Степень окисления элемента Степень окисления – условный заряд атома в соединении. Степень окисления имеет положительные, отрицательные и нулевое значения. Степень окисления атомов в простых веществах равна нулю. Степень окисления атома в сложном веществе может быть постоянной и переменной. Атомы металлов в соединениях имеют только положительную степень окисления. Атомы неметаллов в соединениях могут иметь положительную и отрицательную степень окисления.

Атомно-молекулярное учение Основные положения учения об атомах и молекулах разработал М. В. Ломоносов. 1. Все вещества состоят из молекул, атомов и ионов. 2. Атомы и молекулы находятся в непрерывном движении, их скорость возрастает с увеличением температуры. 3. Молекулы состоят из атомов, которые имеют массу и размеры. 4. Между молекулами в веществе существуют силы взаимного притяжения и отталкивания. 5. Молекулы простых веществ состоят из одинаковых атомов, а молекулы сложных веществ – из разных атомов.

Атомно-молекулярное учение (продолжение) Атомы элементов и молекулы веществ характеризуются определенной физической массой m. В последствии, было введено понятие об атомной единице массы, т. к. абсолютные массы и молекул чрезвычайно малы, и пользоваться такими значениями неудобно. АТОМНАЯ ЕДИНИЦА МАССЫ (а. е. м. ) равная 1/12 части массы атома углерода.

Число Авогадро Амедео Авогадро, граф Куаренья и Черрето Lorenzo Romano Amedeo Carlo Avogadro di Quaregna e Cerreto

Молярная масса

Молярный объем газа
Основы общей химии.pptx