ЛЕКЦИЯ Геном 2008.ppt
- Количество слайдов: 39

Основы молекулярной генетики и биотехнологии l Программа «Геном человека» (Human Genome) l Клонирование l Тканевая инженерия l Генная инженерия: l l l Генная инженерия растений Генная инженерия животных Генная терапия

Проект «Геном человека»

Еще в 1988 году расшифровка генома человека казалась нереальной…

' ' В начале 90 -х проект был инициирован (J. Watson) В середине 90 -х планировалось его закончить к 2010 году… ' 3 млрд. долларов в год на проект тратилось ежегодно только США ' В проект вовлечены все ведущие страны мира ' … И уже в 2001 геном был расшифрован (окончание 1 -го этапа).


Ø Геном (Genome) – совокупность всех генов данного вида Ø Количество генов вида превосходит количество генов особи (генетический полиморфизм) Ø Геном человека (Homo sapiens) содержит 3 167, 7 миллионов нуклеотидов Ø Точное число структурных генов сегодня не способен назвать никто (по завершение 1 -го этапа проекта (2001) 30 000 тыс. , сегодня (2007) называется цифра 20 500 – 21 000). Это намного меньше предварительных расчетов, приводимых ранее (80 000 – 140 000). Ø Число генов Drosophila ~ 13 500, Caenorhabtidis Elegans (круглый червь) ~ 19 000.

Ø Последовательность нуклеотидов у разных людей имеет общность Ø Ø Ø в 99, 9% азотистых оснований. Функция около 50% генов до сих пор не выяснена. Менее 2% ДНК человека кодирует функциональные белки По оценкам, за последние 50 млн. лет драматически снизился темп накопления новых повторов ДНК в геноме человека. В эволюции других млекопитающих этого не произошло. . . По-видимому, 40 -50 млн. лет назад эволюция предков человека пошла по пути внутреннего усложнения генов. Число же генов у человека и, например, грызунов мало отличается. Раньше считалось, что генов и белков – равное количество. Число генов «урезали» втрое, но число белков осталось тем же, если не больше «протеом» (proteome), совокупный набор белков, человека превосходит протеом других видов и остается пока недоизучен. У человека образуется в три раза больше разных белков, чем у других видов. Основные причины – выраженность альтернативного сплайсинга у человека и более сложные конформационные преобразования структуры белка по завершении трансляции.

Ø Основная причина затруднений вычислить точное число генов: необычно большие размеры интронов в геноме человека и их количество. Ø Среднего размера ген состоит из 1, 350 нуклеотидов (с интронами – 3 тыс. ), максимальное число экзонов - 79 (белок дистрофин). Ø Среднее число экзонов в гене - 4. Ø Среднее размер белка – 450 аминокислот. Ø Однако, размеры генов широко варьируют: от нескольких сотен до 2. 4 миллиона нуклеотидов.

' Альтернативный сплайсинг – одна из особенностей геномики Homo sapiens
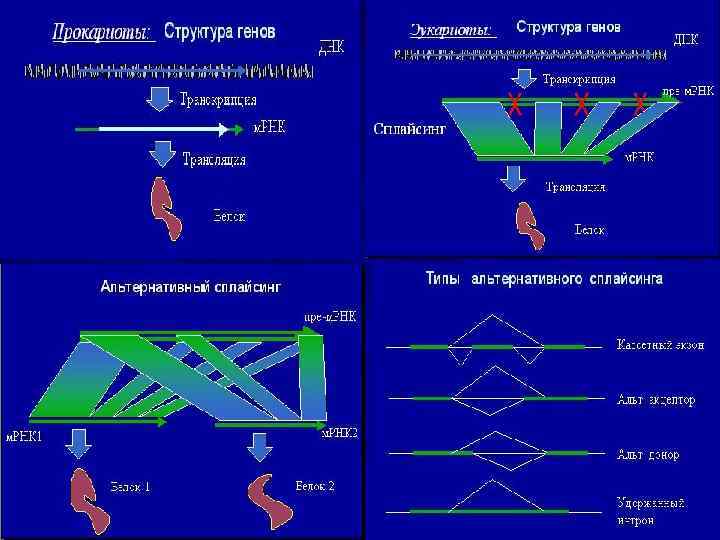

Примером альтернативно сплайсинга является ген, который кодирует либо кальцитонин, либо один из нейрогормонов. v. Если процессинг незрелой м-РНК осуществляется в нейронах, то первичный транскрипт преобразуется в м-РНК, кодирующую нейрогормон. v. В клетках щитовидной железы альтернативный сплайсинг того же предшественника приводит к образованию молекулы м-РНК, кодирующей кальцитонин.

Ø Участки с повторами (некодирующая ДНК) составляют не менее 50 % генома. Хотя, считается, что эта ДНК не имеет прямых функций, она принимает участие в структурообразовании хромосом и ее изменениях. В том числе она участвует в преобразовании генома, создании новых генов, перетасовке существующих. Ø Число «семейств генов» у человека мало отличается от других видов (даже эволюционно отдаленных – черви, членистоногие, растения), но количество «членов семьи» у человека больше (в основном за счет генов индивид. развития (developmental genes) и генов иммунной системы: Ø «Урбанистические центры» ДНК (эухроматин) содержат преимущественно Г- и Ц- нуклеотиды, а некодирующие «пустынные» участки (гетерохроматин) – А- и Т- нуклеотиды. . .

Отрезки с содержанием повторов пар Ц-Г протяженностью 30 000 п. н. как правило разделяют кодирующие участки от некодирующих. Считается, что эти островки принимают важное участие в регуляции работы генов. Ø Больше всего генов в 1 -ой хромосоме (2968), меньше всего в Y-хромосоме (231). В 21 -ой хромосоме генов меньше, чем в 22 -ой. Ø Генетический полиморфизм отдельных азотистых оснований (SNP – single nucleotide polymorphism) – обнаружено 1. 4 млн. таких нуклеотидных локусов. Ø Внедрение методики в практику поможет снизить риск рождения ребенка с наследственными заболеваниями (сегрегационный груз). Ø

Геном человека – первый из детально расшифрованных геномов среди Позвоночных Ø У человека (как, вероятно, и у других Млекопитающих) присутствуют гены, которых у непозвоночных не обнаружено: Что это за гены? Ø Ø Ø Антитела и антиген - рецепторы Т-лимфоцитов Комплекс антигенов основного комплекса гистосовестимости (HLA) Сигнальные клеточные молекулы, включая цитокины Протеины системы свертывания крови Медиаторы запрограммированной клеточной самоликвидации (апоптоза) (хотя некоторые из белков апоптоза обнаружены у Drosophila and C. elegans, мы имеем их в гораздо большем ассортименте).

Ø У каждого человека в среднем имеется 8 аномальных рецессивных генов, 4 – летальных Ø Любое заболевание в той или иной степени имеет генетическую основу Ø Полигенные болезни: как правило обусловлена лишь наследственная предрасположенность Ø Моногенные болезни: существует конкретный ген – причина аномалии. Ø Знание генома может помочь прежде всего в лечении последней группы нозологий

Промежуточные итоги: Завершен лишь Первый этап расшифровки Генома ГЕНОМ ЧЕЛОВЕКА ПРОЧИТАН, НО ДО КОНЦА НЕ ПОНЯТ: Смысловыми участками ДНК принято считать области, которые копируются молекулами м-РНК. Часть ДНК, которая не копируется молекулами РНК, считается информационно бессмысленной. Визуальное представление этих данных поражает воображение. Получается, что 98, 5% протяженности хромосом - это безжизненная территория вещества без информационной "начинки", информационная пустота Более трети всех наших генов имеют очевидные признаки сходства с генами бактерий Этот "золотой запас генов", обеспечивающих клетку энергией, пищей, балансом притока/оттока простых и сложных молекул, очень медленно эволюционирует, поскольку обеспечивает "непотопляемость" живых клеток в разных ситуациях. 1 ген не всегда = 1 белок (есть «сложные гены» , кодирующие не один белок, а больше)

Основные цели проекта «Геном человека» (реализованные и предстоящие) ü ü Выяснение структуры ДНК в хромосомах: последовательности нуклеотидов (+) Разграничение структурных и регуляторных генов (почти +) Выявление генетического полиморфизма (аллельных форм генов человеческой популяции) (50%) Выяснение механизмов генетических программ: дифференцировка, апоптоз, поэтапная активация и инактивация Понимание условий работы генов (регуляции) и их тканевой специфичности (концепция Жакоба – Моно и ее практическое применение) Разграничение моно- и полигенных патологий. Выяснение возможности коррекции последних Изучение постранскрипционных процессов преобразования НК (альтернативного сплайсинга) и функций кодируемых РНК и белков (изучение протеома). Теоретическое обоснование возможностей коррекции генных аномалий. Создание теоретической базы для генной терапии.

КЛОНИРОВАНИЕ: проблема XXI века

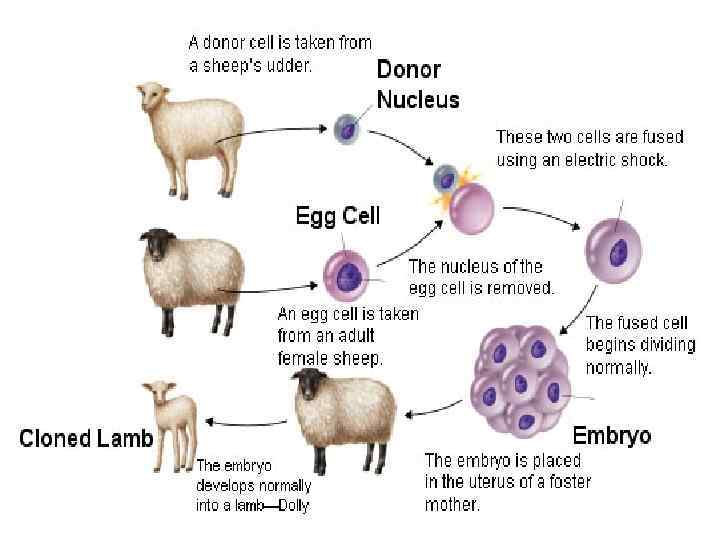
Ян Вильмут – создатель овечки Dolly - первого клонированного млекопитающего, 1997

1998: клонирование мыши • Риюцо Янагимачи (Гавайи) создал клонированную мышь Кумулину (Cumulina), использовав несколько иной методический подход: • Донорское ядро было получено из клетки фолликулярного эпителия, питающего яйцеклетку • Мышь прожила 2 года 7 месяцев, что для мыши достаточно много (~ 95 человеческих лет)

• Copy Cat (Cc) – первая из клонированных домашних животных, создан в лабораториях Техаса (февраль 2002). Внешне похожа на «мать» , но не является даже визуальной копией • Клонирование кошки может иметь интерес с позиций изучения кошачьего СПИДа – хорошей модели для исследования и поисков лечения иммунодефицитов • Тетра – первая клонированная обезьянка, полученная с помощью методики расщепления эмбриона (Gerald Shatten, Региональный центр исследования приматов, Орегон США)

Основные проблемы клонирования: n n n Ядро соматической клетки генетически не тождественно ядру яйцеклетки: как результат 4% всех генов клонированной особи не имеют нормальной регуляции. Репрограммирование остается мало эффективным Во всякой клетке со временем возникают спонтанные мутации, которые сказываются при попытке создать из нее целый организм Процедура переноса ядра далека от идеала и не учитывает роль цитоплазматических факторов, прежде всего – митохондрий Как результат, процент жизнеспособных клонов остается очень низким Для человека проблема усугубляется невозможностью воссоздания уникальных психоличностных качеств, отражающих уникальный жизненный опыт индивида
Естественный способ размножения до сих пор остается единственным, обеспечивающим полную дееспособность генома

Тканевая инженерия – технологии будущего § Омоложение тканей и замена поврежденных органов: реабилитация больных с ИМ путем вживления клонированных клеток здоровой ткани (Richard Seed). § Использование эмбриональных стволовых клеток для тканевой инженерии § Пластическая, реконструктивная и косметическая хирургия – технологии тканевой инженерии помогут отказаться от силиконовых имплантатов § Новые технологии лечения онкопатологий станут возможными после лучшего понимания процессов включения и выключения ключевых генов, механизмов клеточной дифференцировки,

Генная инженерия Ø Сущность ГИ: перенос гена, ответственного за ценное свойство от организма – донора гена организму – реципиенту гена u Генная инженерия микроорганизмов: v u Увеличение синтеза белков бактериями в биотехнологии v Создание лекарственных препаратов Генная инженерия растений Получение растений, устойчивых к вредителям v Получение растений, устойчивых к климату Повышение органолептических свойств культурных сортов v v u Генная инженерия животных Создание трансгенных животных – моделей изучения заболеваний, свойственных и человеку (TGR-мышь с крысиным геном ренина – модель вторичной АГ) v Коровы, дающие молоко, обогащенное геном человеческого глобулина, обладающее иммуностимулирующим действием v

Основные этапы генной инженерии 2 2 2 2 Обнаружение ценного свойства и ответственного за него гена Выделение ДНК из клетки – донора Выделение нужного гена (ДНК) Клонирование ДНК in vitro Создание рекомбинантной ДНК Использование вектора (средства доставки гена клетке-реципиенту): плазмиды, вирусы Верификация дееспособности гена в ряду клеточных поколений и правильности его инсерции Способность клетки регулировать работу гена и отсутствие побочных эффектов его внедрения
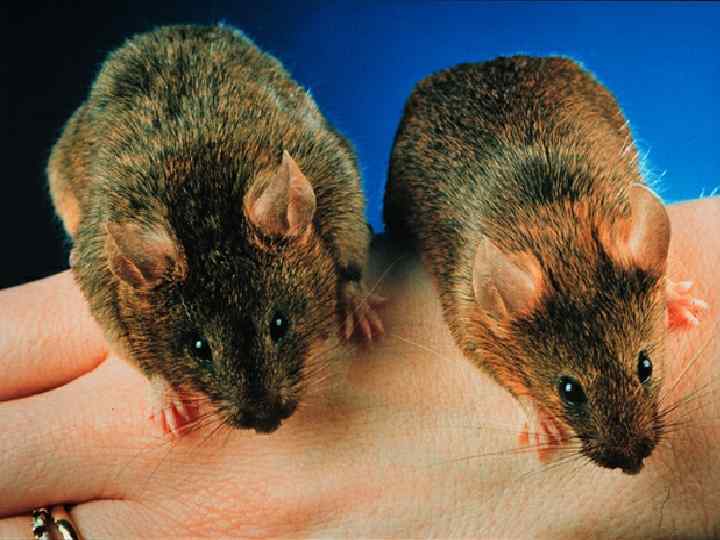

Генная терапия: • Направлена на устранение генетической первопричины наследственного заболевания (в отличие от любой другой формы терапии, которая воздействует только на фенотип) • Сущность: замена дефективного гена, обусловливающего развитие моногенной патологии • 2 принципиальных пути: • Замена гена в клеточной субпопуляции (ткани) – не наследуются • Замена гена на уровне половых клеток – передаются потомкам • Лечение онкопатологий • Введение аллогенов (клетка приобретает атипичные свойства и уничтожается иммунной системой)

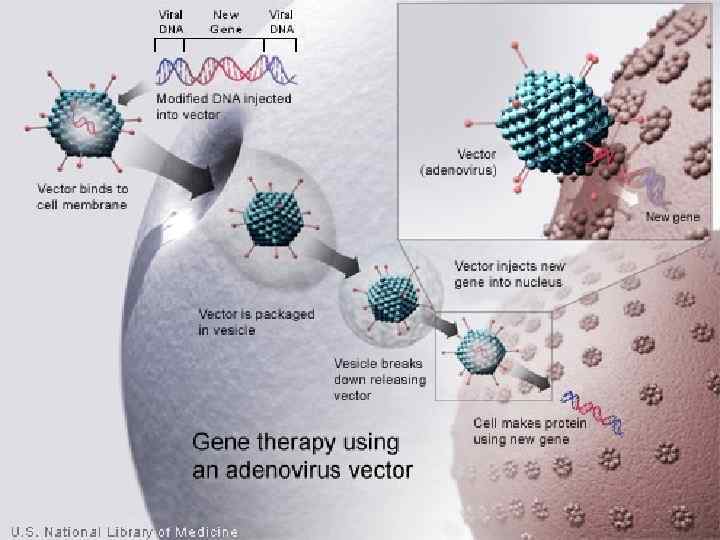
Векторы - средства доставки генов клетке - реципиенту Пути введения гена в организм: ► In Vivo (введение средства доставки гена в организм) ► Ex Vivo (инкубация части клеток с вектором возвращение в организм) Используемые средства и способы доставки генов: ► Вирусные: • Ретровирусы: + стабильно интегрируются в геном, тропны к митотически активным клеткам, но: трудно указать им верный путь • Аденовирусы: + могут нести крупные гены, но трудно лишить их вирулентных свойств полностью, иммунологически устойчивы • Липосомы, ДНК-конъюгаты • Плазмиды (главный недостаток – могут нести только гены до 10 000 нуклеотидов)
Вирусы – самые древние «специалисты» в области генной инженерии и типовые векторы для переноса генов
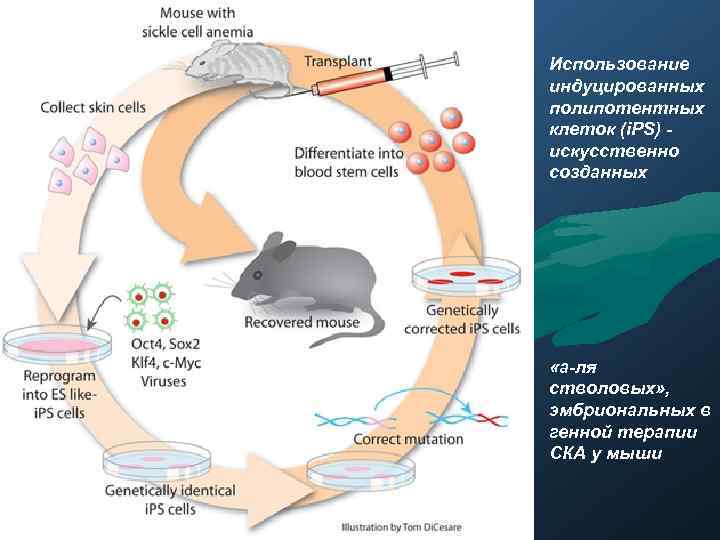
Использование индуцированных полипотентных клеток (i. PS) искусственно созданных «а-ля стволовых» , эмбриональных в генной терапии СКА у мыши

Заболевания, при которых генная терапия может помочь уже завтра: u АДА – дефицит (1990 – первая генотерапия) u ВИЧ- инфекция u Наследственная гиперхолестеринемия u Гемофилия u Талассемии u Муковисцидоз u Болезни накопления (Гоше и др. ) u Злокачественные новообразования

Основные проблемы генной терапии: G Получение устойчивой экспрессии гена G G Стабильность пересаженного гена Регуляция активности внедренного гена Безопасность средств доставки Целенаправленность действия гена

XX век стал веком физики: космонавтики, расщепления ядра и компьютерных технологий XXI век имеет все основания стать веком молекулярной биологии и генетики

СПАСИБО ЗА ВНИМАНИЕ

СПАСИБО ЗА ВНИМАНИЕ
ЛЕКЦИЯ Геном 2008.ppt